Werkinstructies adverse events rapportage STOP-BPD studie
|
|
|
- Christiana van der Velde
- 7 jaren geleden
- Aantal bezoeken:
Transcriptie
1 Werkinstructies adverse events rapportage STOP-BPD studie De STOP-BPD studie wordt uitgevoerd bij extreem prematuur geboren kinderen die los van deelname aan de studie een continu verhoogd risico hebben op ongewenste gebeurtenissen en complicaties (AE/AR) gerelateerd aan de prematuriteit en de routine behandeling. Volgens GCP richtlijnen dienen al deze AEs bij een geneesmiddelenstudie vermeld te worden in het ecrf. Het spreekt voor zich dat dit niet uitvoerbaar is binnen de populatie prematuur geboren kinderen en dat het melden van de gebruikelijke complicaties van prematuriteit de veiligheid van de patiënten niet zal verhogen. Om de clinicus te ondersteunen in het classificeren van AEs is een flowdiagram ontwikkeld (zie bijlage 1). Deze werkinstructies geven een extra toelichting op dit flowdiagram waarbij met name beargumenteerd wordt waarom in sommige situaties afgeweken wordt van de GCP richtlijn. AE/AR Dit is iedere niet-serieuze ongewenste gebeurtenis/complicatie die optreedt tijdens de studie. Zoals al eerder aangegeven is het natuurlijke ziektebeloop van een prematuur geboren kind één aaneenschakeling van AE/ARs. Het zal duidelijk zijn dat het noteren van al deze AE/ARs in de praktijk niet haalbaar is en de veiligheid van de patiënt niet zal verhogen. Alleen indien er sprake is van een klinisch significante AE/AR en deze niet voorkomt op de morbiditeit pagina van het ecrf, zal deze genoteerd worden op de AE pagina in het ecrf. Een klinische AE/AR is gedefinieerd als een ongewenste gebeurtenis met klinische symptomen en/of die leidt tot een klinische interventie, waarbij deze ongewenste bijwerking redelijkerwijs niet te verwachten was bij het normale klinische beloop na een premature geboorte. Voorbeelden van een NIET klinische relevante AE/AR zijn hyponatriemie, hypertryglyceridemie, hyper- of hypofosfatemie of andere electrolytstoornissen, metabole acidose, hypercapnie, voedingsretenties of onrust aan de beademing waarvoor sedatie noodzakelijk is etc.. Pulmonale fluctuaties of zelfs achteruitgang wordt, alhoewel niet wenselijk, beschouwd als een normale complicatie in deze hoog risico populatie en wordt derhalve niet beschouwd als een AE/AR. Voorbeeld van een klinische relevante AE/AR is koorts. SAE/SSAR/SUSAR Indien de ongewenste gebeurtenis/complicatie serieus is volgens de daarvoor geldende criteria (zie flowdiagram) wordt het een SAE genoemd. Indien er sprake is van een SAE die redelijkerwijs te verwachten is bij prematuur geboren kinderen en geen verband lijkt te houden met de studiemedicatie, dan spreekt men van een context-specific SAE. Deze worden vermeld op de morbiditeit pagina in het ecrf en vormen de secundaire uitkomstmaten van deze studie. Indien er geen sprake is van een verband met de premature geboorte en er geen verband bestaat met de studiemedicatie, wordt de SAE unrelated genoemd en genoteerd op de AE pagina van het ecrf. Bestaat er mogelijk wel een verband met de studiemedicatie en is het een bekende ernstige bijwerking volgens het SPC dan is er sprake van een SSAR. Deze worden genoteerd op de AE pagina van de ecrf, tenzij deze bekende bijwerkingen vermeld staan in de context-specific SAEs (maag/darm perforaties). Indien dit mogelijke verband niet eerder is beschreven, dan spreekt men van een SUSAR.
2 Web-alert procedures Om de veiligheid van de studie te verhogen zijn een 4-tal condities aangewezen die binnen 72 uren na optreden, gemeld moeten worden. Deze procedure is opgezet om continu geïnformeerd te zijn over een aantal mogelijk veiligheidsaspecten van de studie. Het gaat om de volgende condities: het optreden van hypertensie, het optreden van gastro-intestinale perforatie, het gelijktijdig toedienen van studiemedicatie en ibuprofen/indomethacine het gebruik van open label rescue therapie. Deze condities dienen binnen 72 uren na optreden ingevuld te worden in het ecrf. Bij het invullen zal een automatische verstuurd worden naar het onderzoeksteam in het AMC. Meldingsplicht AE/SAE/SSAR/SUSAR De AE/ARs en de context-specific SAEs worden genoteerd in het ecrf en 3-maandelijks gerapporteerd aan de Data Monitoring Committee (DMC) en jaarlijks aan de METC. Er bestaat dus geen directe meldingsplicht richting de principle investigator (PI). De uitzondering hierop is de context-specific SAE mortaliteit. Deze wordt binnen 72 uur gemeld aan de PI door het invullen van mortaliteit in het ecrf op de morbiditeit pagina. Dit verzendt een automatische naar het onderzoeksteam in het AMC. Indien er sprake is van een unrelated SAE of een (niet context specific) SSAR, dan dient deze ook binnen 72 uur genoteerd te worden in het ecrf op de AE pagina zodat er een automatisch gestuurd wordt naar het onderzoeksteam in het AMC. Er is hierbij gekozen voor een tijdsperiode van 72 uur om het proces praktisch uitvoerbaar te houden in een grote en complexe organisatie als een neonatale intensive care unit waar veel wisselingen van verantwoordelijk personeel plaatsvinden. Daarnaast gaat het in deze studie niet om een nieuw geneesmiddel maar om een geneesmiddel dat al jaren binnen de neonatologie gebruikt wordt voor zowel deze als andere indicaties. In tegenstelling tot de context-specific SAE, unrelated SAE en de SSAR, dient de SUSAR wel binnen 24 uur gemeld te worden aan de PI.
3
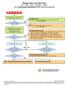
4 Bijlage 1 Stroomdiagram melding van ongewenste voorvallen SToP-BPD Studie Melding ongewenst voorval Is het voorval ernstig? Dit wordt gedefinieerd als: Is dodelijk Levert levensgevaar op (Verlenging van) opname in ziekenhuis noodzakelijk Veroorzaakt blijvende of significante invaliditeit Ander ernstig medisch voorval Vermoedelijke relatie met studiemedicatie?** (Mogelijk, Waarschijnlijk, Zeer waarschijnlijk), (Niet gerelateerd, Onwaarschijnlijk AE/AR Vermeld alle klinisch significante voorvallen* in het CRF op de AE pagina, tenzij deze voorvallen gemeld worden in de Morbidity sectie van het CRF. Behoort het voorval tot een mogelijke complicatie ten gevolge van prematuriteit (een normale complicatie van prematuriteit ) Context specific SAE Vermeld in het CRF in de relevante Morbidity sectie. NB. Overlijden moet gemeld worden in het CRF binnen 72 uur nadat het voorval bekend wordt. Dit zorgt voor een automatische naar het coördinerende centrum. Ongerelateerde SAE Meld binnen 72 uur nadat het voorval bekend wordt op de AE pagina van het CRF. Dit zorgt voor een automatische naar het coördinerende centrum. Is het voorval een bekende bijwerking van studiemedicatie, zie SPC/IMPD? *** (Bekend) SSAR Tenzij het voorval al gemeld wordt in de Morbidity sectie van het CRF, meld het binnen 72 uur nadat het voorval bekend wordt op de AE pagina van het CRF. Dit zorgt voor een automatische naar het coördinerende centrum. (Onbekend) SUSAR Meld het voorval binnen 24 uur aan de hoofdonderzoeker per telefoon en meld het voorval binnen 24 uur op de AE pagina van het CRF. Dit zorgt voor een automatische naar het coördinerende centrum.
5 *: een klinisch significante AE is gedefinieerd als een voorval met klinische manifestaties of benodigde interventies welke niet verwacht wordt ten gevolge van het normale klinische beloop bij prematuriteit; **: Zie de definities van causaliteit in de volgende textbox. AE/AR : Adverse Event/Adverse Reaction SPC: Summary of Product Characteristics SAE : Serious Adverse Event IMPD: Investigational Medicinal Product Dossier SSAR : Suspected Serious Adverse Reaction CRF: Case Report Form SUSAR : Suspected Unexpected Serious Adverse Reaction Definities van causaliteit Niet gerelateerd: There is no evidence of any causal relationship Onwaarschijnlijk: There is little evidence to suggest there is a causal relationship (e.g. the event did not occur within a reasonable time after administration of the trial medication). There is another reasonable explanation for the event (e.g. the patient s clinical condition, other concomitant treatment). Mogelijk: There is some evidence to suggest a causal relationship (e.g. because the event occurs within a reasonable time after administration of the trial medication). However, the influence of other factors may have contributed to the event (e.g. the patient s clinical condition, other concomitant treatments). Waarschijnlijk: There is evidence to suggest a causal relationship and the influence of other factors is unlikely. Zeer waarschijnlijk: There is clear evidence to suggest a causal relationship and other possible contributing factors can be ruled out.
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek
 Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
INCLUSIE SET PLAATS HIER DE PATIENTSTICKER VAN DE GEINCLUDEERDE PATIENT. ULTRA STUDIE INCLUSIE SET VERSIE 9 Pagina 1 van 9
 INCLUSIE SET Als de patiënt geïncludeerd kan worden in de studie, voert de arts in het behandelcentrum de randomisatieprocedure uit na telefonische aanmelding van de patiënt(e) PLAATS HIER DE PATIENTSTICKER
INCLUSIE SET Als de patiënt geïncludeerd kan worden in de studie, voert de arts in het behandelcentrum de randomisatieprocedure uit na telefonische aanmelding van de patiënt(e) PLAATS HIER DE PATIENTSTICKER
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U8 Melding van (Serious) Adverse Events en SUSARs Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies
Standard Operating Procedure STZ SOP: U8 Melding van (Serious) Adverse Events en SUSARs Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies
Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek
 Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek Melding voorval proefpersoon aan onderzoeker/arts 1 Rapportage voorval door onderzoeker/arts in patiëntenstatus
Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek Melding voorval proefpersoon aan onderzoeker/arts 1 Rapportage voorval door onderzoeker/arts in patiëntenstatus
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A1 Afsluiting studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A1 Afsluiting studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
De rol van de verpleegkundige binnen Medischwetenschappelijk
 De rol van de verpleegkundige binnen Medischwetenschappelijk onderzoek Moderator Mevr. R.C.A. Veldhoen-Tijben 1st author / speaker Miriam Gelderloos Co-author Erna Helmantel Belangenverklaring In overeenstemming
De rol van de verpleegkundige binnen Medischwetenschappelijk onderzoek Moderator Mevr. R.C.A. Veldhoen-Tijben 1st author / speaker Miriam Gelderloos Co-author Erna Helmantel Belangenverklaring In overeenstemming
CRF. Ladies trial. Randomisatienummer
 CRF de Ladies trial Laparoscopische peritoneale lavage of resectie voor gegeneraliseerde peritonitis voor geperforeerde diverticulitis: een landelijke multicentrum gerandomiseerde trial Sandra Vennix (AMC/Erasmus
CRF de Ladies trial Laparoscopische peritoneale lavage of resectie voor gegeneraliseerde peritonitis voor geperforeerde diverticulitis: een landelijke multicentrum gerandomiseerde trial Sandra Vennix (AMC/Erasmus
Titel: Good Clinical Practice & Monitoring. Initiation Investigator Driven Studies. Versie: 14-jan-2013
 Titel: Good Clinical Practice & Monitoring Initiation Investigator Driven Studies Inhoud Wet- en regelgeving/declaration of Helsinki Good Clinical Practice Patiënteninformatie/ informed consent Basisvereisten
Titel: Good Clinical Practice & Monitoring Initiation Investigator Driven Studies Inhoud Wet- en regelgeving/declaration of Helsinki Good Clinical Practice Patiënteninformatie/ informed consent Basisvereisten
STATEC trial praktische uitvoering Hilde Dijcker
 STATEC trial praktische uitvoering 17-04-2018 Hilde Dijcker Inhoud IKNL trialbureau Site activation Datamanagement Monitoring IKNL Trialbureau Site activation: - Ine Leenen en Hilde Dijcker Kwaliteit van
STATEC trial praktische uitvoering 17-04-2018 Hilde Dijcker Inhoud IKNL trialbureau Site activation Datamanagement Monitoring IKNL Trialbureau Site activation: - Ine Leenen en Hilde Dijcker Kwaliteit van
Patient information. Report information. Serious Adverse Event information
 HOVON Data Center Safety Desk NIEUWSBRIEF 4 06 mei 2014 Beste lezer, Met gepaste trots presenteren we u de nieuwe manier van rapporteren van SAE's. Hiermee hopen wij de werklast voor iedereen zoveel mogelijk
HOVON Data Center Safety Desk NIEUWSBRIEF 4 06 mei 2014 Beste lezer, Met gepaste trots presenteren we u de nieuwe manier van rapporteren van SAE's. Hiermee hopen wij de werklast voor iedereen zoveel mogelijk
IC ICF ICH ISF. Lijst met afkortingen, definities en termen STZ-Kwaliteitshandboek SOP s
 Lijst met afkortingen, definities en termen STZ-Kwaliteitshandboek SOP s ABR ADR AE AR BROK CCMO CRF CTA CV DSMB EMEA EU EudraCT FU brief GCP GMP IB IC ICF ICH IMPD ISF MEB METC EU RCT SAE SOP SPC SUSAR
Lijst met afkortingen, definities en termen STZ-Kwaliteitshandboek SOP s ABR ADR AE AR BROK CCMO CRF CTA CV DSMB EMEA EU EudraCT FU brief GCP GMP IB IC ICF ICH IMPD ISF MEB METC EU RCT SAE SOP SPC SUSAR
Monitorplan voorbeeld
 Monitorplan voorbeeld Protocol Er moet in het protocol beschreven worden dat er monitoring plaatsvindt (zie ook CCMO voorbeeld template). Het monitoringplan mag als bijlage worden toegevoegd (in dat geval
Monitorplan voorbeeld Protocol Er moet in het protocol beschreven worden dat er monitoring plaatsvindt (zie ook CCMO voorbeeld template). Het monitoringplan mag als bijlage worden toegevoegd (in dat geval
29 juni Initiatie bijeenkomst PORTEC 4. Kwaliteitsborging WMO GCP richtsnoer. Frank van Leeuwen IKNL
 29 juni 2012 Initiatie bijeenkomst PORTEC 4 Kwaliteitsborging WMO GCP richtsnoer Frank van Leeuwen IKNL Wet en regelgeving Verklaring van Helsinki Richtsnoer voor Good Clinical Practice (CPMP/ICH/135/95)
29 juni 2012 Initiatie bijeenkomst PORTEC 4 Kwaliteitsborging WMO GCP richtsnoer Frank van Leeuwen IKNL Wet en regelgeving Verklaring van Helsinki Richtsnoer voor Good Clinical Practice (CPMP/ICH/135/95)
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen. Farmaceutische Bedrijven Deelteam Klinisch Onderzoek
 Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL4 Investigator Site File Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: VL4 Investigator Site File Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Veiligheid en methodologie of Waarom voortijdig stoppen? Job van der Palen METC Twente
 Veiligheid en methodologie of Waarom voortijdig stoppen? Job van der Palen METC Twente Waarom voortijdig stoppen? Veiligheid Effectiviteit Futiliteit Andere redenen Veiligheid (1) Data and Safety Monitoring
Veiligheid en methodologie of Waarom voortijdig stoppen? Job van der Palen METC Twente Waarom voortijdig stoppen? Veiligheid Effectiviteit Futiliteit Andere redenen Veiligheid (1) Data and Safety Monitoring
Jouw GCP up-to-date in 45 minuten. Marieke Meulemans, oprichter GCP Central
 Jouw GCP up-to-date in 45 minuten Marieke Meulemans, oprichter GCP Central Waarom een GCP update tijdens de CRA dag? Gedreven Meesterschap. Meesterschap is vakmanschap. Vakmanschap is beheersing van het
Jouw GCP up-to-date in 45 minuten Marieke Meulemans, oprichter GCP Central Waarom een GCP update tijdens de CRA dag? Gedreven Meesterschap. Meesterschap is vakmanschap. Vakmanschap is beheersing van het
Inhoud onderzoeksdossier
 Inhoud onderzoeksdossier (documenten in de witte box zijn nodig voor de primaire beoordeling) A. Brieven B. Formulieren C. Onderzoeksprotocol en protocolamendementen D. Productinformatie E. Informatie
Inhoud onderzoeksdossier (documenten in de witte box zijn nodig voor de primaire beoordeling) A. Brieven B. Formulieren C. Onderzoeksprotocol en protocolamendementen D. Productinformatie E. Informatie
Standard Operating Procedure
 Standard Operating Procedure SOP: V1 Ontwikkelen Onderzoeksprotocol Auteur Naam: Functie instelling/afdeling Judie van den Elshout Staffunctionaris Wetenschapsbureau Wetenschapsbureau / Cluster Leerhuis
Standard Operating Procedure SOP: V1 Ontwikkelen Onderzoeksprotocol Auteur Naam: Functie instelling/afdeling Judie van den Elshout Staffunctionaris Wetenschapsbureau Wetenschapsbureau / Cluster Leerhuis
Veel gestelde vragen Medisch-wetenschappelijk onderzoek met medische hulpmiddelen 1
 Veel gestelde vragen Medisch-wetenschappelijk onderzoek met medische hulpmiddelen 1 1. Wat is een medisch hulpmiddel? De wettelijke definitie 2 van een medisch hulpmiddel luidt: Een medisch hulpmiddel
Veel gestelde vragen Medisch-wetenschappelijk onderzoek met medische hulpmiddelen 1 1. Wat is een medisch hulpmiddel? De wettelijke definitie 2 van een medisch hulpmiddel luidt: Een medisch hulpmiddel
Formulier Voortgangsrapportage
 Formulier Voortgangsrapportage De METC azm/um wil van al het door haar beoordeelde WMO-onderzoek jaarlijks een voortgangsrapportage zien. Zij heeft deze eis daartoe opgenomen in de tekst van haar eigen
Formulier Voortgangsrapportage De METC azm/um wil van al het door haar beoordeelde WMO-onderzoek jaarlijks een voortgangsrapportage zien. Zij heeft deze eis daartoe opgenomen in de tekst van haar eigen
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U4 Registratie /randomisatie procedure Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum
Standard Operating Procedure STZ SOP: U4 Registratie /randomisatie procedure Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum
Standard Operating Procedure
 Standard Operating Procedure SOP: V9 Initiatievisite Auteur Naam: Functie instelling/afdeling Judie van den Elshout Staffunctionaris Wetenschapsbureau Wetenschapsbureau / Cluster Leerhuis Handtekening:...
Standard Operating Procedure SOP: V9 Initiatievisite Auteur Naam: Functie instelling/afdeling Judie van den Elshout Staffunctionaris Wetenschapsbureau Wetenschapsbureau / Cluster Leerhuis Handtekening:...
Monitoring van Investigator Initiated onderzoek
 Monitoring van Investigator Initiated onderzoek V1.0 Angela Vlug Clinical Research Bureau VUmc Wat is een IIS (volgens de NFU) Onderzoek waarvoor de raad van bestuur van een (universitair) medisch centrum
Monitoring van Investigator Initiated onderzoek V1.0 Angela Vlug Clinical Research Bureau VUmc Wat is een IIS (volgens de NFU) Onderzoek waarvoor de raad van bestuur van een (universitair) medisch centrum
Informatie SToP-BPD studie
 Informatie SToP-BPD studie Systemic Hydrocortisone To Prevent Bronchopulmonary Dysplasia in preterm infants. A multicenter randomised placebo controlled trial. t.b.v kinderarts verwijzend ziekenhuis Plaats:
Informatie SToP-BPD studie Systemic Hydrocortisone To Prevent Bronchopulmonary Dysplasia in preterm infants. A multicenter randomised placebo controlled trial. t.b.v kinderarts verwijzend ziekenhuis Plaats:
Safety First: Vangnet of Maatwerk?
 Gedreven Meesterschap Safety First: Vangnet of Maatwerk? Het belang van Farmacovigilantie in Clinical Research 21 April 2016 Marielle Keulen Sandra van der Poel Tel: 071 524 4000 www.xendo.com Safety First:
Gedreven Meesterschap Safety First: Vangnet of Maatwerk? Het belang van Farmacovigilantie in Clinical Research 21 April 2016 Marielle Keulen Sandra van der Poel Tel: 071 524 4000 www.xendo.com Safety First:
APEC-trial. Case Record Form. Acute biliary Pancreatitis: early ERC plus sphincterotomy versus Conservative treatment
 APEC-trial Case Record Form Acute biliary Pancreatitis: early ERC plus sphincterotomy versus Conservative treatment Groep A: ERC (met sphincterotomie) Patiëntensticker Bel s.v.p. op volgorde 1-4 1. Noortje
APEC-trial Case Record Form Acute biliary Pancreatitis: early ERC plus sphincterotomy versus Conservative treatment Groep A: ERC (met sphincterotomie) Patiëntensticker Bel s.v.p. op volgorde 1-4 1. Noortje
Melding van ernstige ongewenste voorvallen en bijwerkingen. Biovigilantie Symposium TRIP November 2, 2016 Susan Marks, Medische Staf Eurotransplant
 Melding van ernstige ongewenste voorvallen en bijwerkingen Biovigilantie Symposium TRIP November 2, 2016 Susan Marks, Medische Staf Eurotransplant Introductie Uitvoeringrichtlijn 2012/25/EU van de commissie,
Melding van ernstige ongewenste voorvallen en bijwerkingen Biovigilantie Symposium TRIP November 2, 2016 Susan Marks, Medische Staf Eurotransplant Introductie Uitvoeringrichtlijn 2012/25/EU van de commissie,
Onderstaande vragen zijn van toepassing op de periode 6-12 maanden postoperatief
 9. Follow-up Aantal maanden? Datum: Setting: O klinisch O poliklinisch Beoordelaar: (naam) Algemeen Onderstaande vragen zijn van toepassing op de periode 6- postoperatief Is de patient opgenomen geweest
9. Follow-up Aantal maanden? Datum: Setting: O klinisch O poliklinisch Beoordelaar: (naam) Algemeen Onderstaande vragen zijn van toepassing op de periode 6- postoperatief Is de patient opgenomen geweest
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U9 Monitoren Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies Versiedatum Hoofdstuk Versiedatum Hoofdstuk
Standard Operating Procedure STZ SOP: U9 Monitoren Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies Versiedatum Hoofdstuk Versiedatum Hoofdstuk
Geneesmiddelenonderzoek en de ziekenhuisapotheek
 Geneesmiddelenonderzoek en de ziekenhuisapotheek Pierre Bet ziekenhuisapotheker Klinische Farmacologie & Apotheek VU medisch centrum feb 2011 Inhoud Verantwoordelijkheden Bereiding van IMP Voortraject
Geneesmiddelenonderzoek en de ziekenhuisapotheek Pierre Bet ziekenhuisapotheker Klinische Farmacologie & Apotheek VU medisch centrum feb 2011 Inhoud Verantwoordelijkheden Bereiding van IMP Voortraject
Beknopt protocol Gericht aan deelnemend neurologen (principal investigators)
 Beknopt protocol Gericht aan deelnemend neurologen (principal investigators) Second IVIg Dose in Guillain-Barré Syndrome patients with poor prognosis (SID-GBS trial) Erasmus MC Johns Hopkins Hospital,
Beknopt protocol Gericht aan deelnemend neurologen (principal investigators) Second IVIg Dose in Guillain-Barré Syndrome patients with poor prognosis (SID-GBS trial) Erasmus MC Johns Hopkins Hospital,
FOD Volksgezondheid, Veiligheid van de Voedselketen en Leefmilieu. Directoraat-generaal Geneesmiddelen
 Afdeling Wig ilantie' Amazone Afdeling `138(D'(Onderzoek&Ontwikkeling) Bischoffsheimlaan 33 B-1000 BRUSSEL Belgisch Centrum voor Geneesmiddelenbewaking voor geneeesmiddelen voor humaan gebruik Uw brief
Afdeling Wig ilantie' Amazone Afdeling `138(D'(Onderzoek&Ontwikkeling) Bischoffsheimlaan 33 B-1000 BRUSSEL Belgisch Centrum voor Geneesmiddelenbewaking voor geneeesmiddelen voor humaan gebruik Uw brief
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A2 Archiveren studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A2 Archiveren studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Elektronische melding van SAE s & SUSARs via ToetsingOnline
 Elektronische melding van SAE s & s via ToetsingOnline BROK-cursus VUmc Voorjaar 2014 Trinette van Vliet Wetenschappelijk stafmedewerker Casus: Propatria studie (2008) Probioticamengsel (maag/darm sonde)
Elektronische melding van SAE s & s via ToetsingOnline BROK-cursus VUmc Voorjaar 2014 Trinette van Vliet Wetenschappelijk stafmedewerker Casus: Propatria studie (2008) Probioticamengsel (maag/darm sonde)
Waarom studies voortijdig stoppen. Job van der Palen METC Twente
 Waarom studies voortijdig stoppen Job van der Palen METC Twente Waarom studies voortijdig stoppen? Veiligheid Effectiviteit Futiliteit Andere redenen Veiligheid (1) Data and Safety Monitoring Board (DSMB)
Waarom studies voortijdig stoppen Job van der Palen METC Twente Waarom studies voortijdig stoppen? Veiligheid Effectiviteit Futiliteit Andere redenen Veiligheid (1) Data and Safety Monitoring Board (DSMB)
Voor$jdig stoppen van studies Job van der Palen METC Twente
 Voor$jdig stoppen van studies Job van der Palen METC Twente Waarom voor$jdig stoppen? Veiligheid Effec9viteit Fu9liteit Andere redenen Veiligheid (1) Data and Safety Monitoring Board (DSMB) OnaEankelijk!
Voor$jdig stoppen van studies Job van der Palen METC Twente Waarom voor$jdig stoppen? Veiligheid Effec9viteit Fu9liteit Andere redenen Veiligheid (1) Data and Safety Monitoring Board (DSMB) OnaEankelijk!
Case Record Form (CRF)
 Case Record Form (CRF) POINTER trial: postponed or immediate catheter drainage of infected necrotizing pancreatitis Studiearm UITGESTELDE katheterdrainage / Studienummer POINT Datacenter Pancreatitis Werkgroep
Case Record Form (CRF) POINTER trial: postponed or immediate catheter drainage of infected necrotizing pancreatitis Studiearm UITGESTELDE katheterdrainage / Studienummer POINT Datacenter Pancreatitis Werkgroep
Richtlijn Melden van ernstige bijwerkingen van Vitamine K-antagonisten door de Nederlandse trombosediensten bij Lareb
 Richtlijn Melden van ernstige bijwerkingen van Vitamine K-antagonisten door de Nederlandse trombosediensten bij Lareb Deze richtlijn is een initiatief van de Federatie van Nederlandse Trombosediensten
Richtlijn Melden van ernstige bijwerkingen van Vitamine K-antagonisten door de Nederlandse trombosediensten bij Lareb Deze richtlijn is een initiatief van de Federatie van Nederlandse Trombosediensten
Informatie SToP-BPD studie
 Informatie SToP-BPD studie Systemic Hydrocortisone To Prevent Bronchopulmonary Dysplasia in preterm infants. A multicenter randomised placebo controlled trial. t.b.v kinderarts verwijzend ziekenhuis Plaats:
Informatie SToP-BPD studie Systemic Hydrocortisone To Prevent Bronchopulmonary Dysplasia in preterm infants. A multicenter randomised placebo controlled trial. t.b.v kinderarts verwijzend ziekenhuis Plaats:
Toetsingskader niet-wmo plichtig onderzoek
 Toetsingskader niet-wmo plichtig onderzoek Mieke D Trip, internist Voorzitter METC, AMC te Amsterdam Voorzitter BROK commissie, NFU 22 september 2011 Toetsingskader niet-wmo plichtig onderzoek Huidige
Toetsingskader niet-wmo plichtig onderzoek Mieke D Trip, internist Voorzitter METC, AMC te Amsterdam Voorzitter BROK commissie, NFU 22 september 2011 Toetsingskader niet-wmo plichtig onderzoek Huidige
SOP: Lokale werkwijze MR ASAP
 SOP: Lokale werkwijze MR ASAP SOP: L01 Versie Nr.: 1.1 Geldig m.i.v.: 17-09-2018 Auteur/coördinerend onderzoeker: S.A. van den Berg, arts-onderzoeker AMC (020 566 4591) Hoofdonderzoekers: Dr. H.B. van
SOP: Lokale werkwijze MR ASAP SOP: L01 Versie Nr.: 1.1 Geldig m.i.v.: 17-09-2018 Auteur/coördinerend onderzoeker: S.A. van den Berg, arts-onderzoeker AMC (020 566 4591) Hoofdonderzoekers: Dr. H.B. van
Vigilantie bij Omniplasma. Jo Wiersum-Osselton namens TRIP
 Vigilantie bij Omniplasma Jo Wiersum-Osselton namens TRIP TRIP Board (Medical Societies) Advisory board (Hospital associations, Sanquin BB) Hospitals blood Tf comm. Hospital laboratory clinicians national
Vigilantie bij Omniplasma Jo Wiersum-Osselton namens TRIP TRIP Board (Medical Societies) Advisory board (Hospital associations, Sanquin BB) Hospitals blood Tf comm. Hospital laboratory clinicians national
Aanmelden medischwetenschappelijk
 Aanmelden medischwetenschappelijk onderzoek SOP Aanmelden WMO-plichtig onderzoek_versie juli 2016.doc Pagina 1 van 10 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd
Aanmelden medischwetenschappelijk onderzoek SOP Aanmelden WMO-plichtig onderzoek_versie juli 2016.doc Pagina 1 van 10 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd
Onderstaande vragen zijn van toepassing op de periode 4-6 maanden postoperatief
 Aantal maanden? Datum: Setting: O klinisch O poliklinisch Beoordelaar: (naam) Algemeen Onderstaande vragen zijn van toepassing op de periode 4- postoperatief Is de patient opgenomen geweest in een van
Aantal maanden? Datum: Setting: O klinisch O poliklinisch Beoordelaar: (naam) Algemeen Onderstaande vragen zijn van toepassing op de periode 4- postoperatief Is de patient opgenomen geweest in een van
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U10 Audit Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: U10 Audit Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum Opmerkingen
Monitoren vs auditen. CRA dag 21 april 2016
 Monitoren vs auditen CRA dag 21 april 2016 Introductie Freelance consultant, mede oprichter TAPAS Group B.V. Mede oprichter/directeur van CRA B.V. Medical Adviser Yamanouchi Pharma Clinical trial monitor
Monitoren vs auditen CRA dag 21 april 2016 Introductie Freelance consultant, mede oprichter TAPAS Group B.V. Mede oprichter/directeur van CRA B.V. Medical Adviser Yamanouchi Pharma Clinical trial monitor
Disclosure belangen spreker
 Disclosure belangen spreker (potentiële) belangenverstrengeling Voor bijeenkomst mogelijk relevante relaties met bedrijven Sponsoring of onderzoeksgeld Honorarium of andere (financiële) vergoeding Aandeelhouder
Disclosure belangen spreker (potentiële) belangenverstrengeling Voor bijeenkomst mogelijk relevante relaties met bedrijven Sponsoring of onderzoeksgeld Honorarium of andere (financiële) vergoeding Aandeelhouder
Obesitas bij ortopedische ingrepen: challenge of contra-indicatie? Co-assistent: Philippe Leire Promotor: Dr. A. Kumar
 Obesitas bij ortopedische ingrepen: challenge of contra-indicatie? Co-assistent: Philippe Leire Promotor: Dr. A. Kumar Kaart toenemende demografie obesitas The influence of obesity on total joint arthroplasty.
Obesitas bij ortopedische ingrepen: challenge of contra-indicatie? Co-assistent: Philippe Leire Promotor: Dr. A. Kumar Kaart toenemende demografie obesitas The influence of obesity on total joint arthroplasty.
1. Voorafgaand aan de klinische fase van het onderzoek
 Essentiële documenten Bron: Richtsnoer voor good clinical practice (CPMP/ICH/135/95) De verwijzingen in dit document verwijzen naar de artikelen in bovenstaand document. 1. Voorafgaand aan de klinische
Essentiële documenten Bron: Richtsnoer voor good clinical practice (CPMP/ICH/135/95) De verwijzingen in dit document verwijzen naar de artikelen in bovenstaand document. 1. Voorafgaand aan de klinische
Het voorkomen van geneesmiddel gerelateerde problemen bij oudere patiënten met polyfarmacie ontslagen uit het ziekenhuis
 Samenvatting Het voorkomen van geneesmiddel gerelateerde problemen bij oudere patiënten met polyfarmacie ontslagen uit het ziekenhuis Hoofdstuk 1 bevat de algemene inleiding van dit proefschrift. Dit hoofdstuk
Samenvatting Het voorkomen van geneesmiddel gerelateerde problemen bij oudere patiënten met polyfarmacie ontslagen uit het ziekenhuis Hoofdstuk 1 bevat de algemene inleiding van dit proefschrift. Dit hoofdstuk
HYDROCORTISON TER VOORKOMING VAN BRONCHOPULMONALE DYSPLASIE; DE STOP-BPD STUDIE INFORMATIE TEN BEHOEVE VAN DE OUDERS
 HYDROCORTISON TER VOORKOMING VAN BRONCHOPULMONALE DYSPLASIE; DE STOP-BPD STUDIE INFORMATIE TEN BEHOEVE VAN DE OUDERS Geachte mevrouw/mijnheer, Uw kind is opgenomen op de afdeling Neonatologie van het omdat
HYDROCORTISON TER VOORKOMING VAN BRONCHOPULMONALE DYSPLASIE; DE STOP-BPD STUDIE INFORMATIE TEN BEHOEVE VAN DE OUDERS Geachte mevrouw/mijnheer, Uw kind is opgenomen op de afdeling Neonatologie van het omdat
Ongewenste uitkomsten van zorg
 Ongewenste uitkomsten van zorg De belangrijkste vragen op een rij Juni 2016 Drie vormen van ongewenste uitkomsten van zorg 1. Calamiteit 2. Incident 3. Complicatie Wat zijn de verschillen en hoe kunnen
Ongewenste uitkomsten van zorg De belangrijkste vragen op een rij Juni 2016 Drie vormen van ongewenste uitkomsten van zorg 1. Calamiteit 2. Incident 3. Complicatie Wat zijn de verschillen en hoe kunnen
COLOPEC trial. 9. Follow-up 2/3/4/5 jaar na primaire resectie. Anamnese. Lichamelijk onderzoek. Labwaarden. Patiënt Identificatie Nummer: Initialen:
 Aantal maanden? maanden Datum: Setting: O klinisch O poliklinisch Beoordelaar: (naam) Algemeen Onderstaande vragen zijn van toepassing op de periode 18- postoperatief Is de patient opgenomen geweest in
Aantal maanden? maanden Datum: Setting: O klinisch O poliklinisch Beoordelaar: (naam) Algemeen Onderstaande vragen zijn van toepassing op de periode 18- postoperatief Is de patient opgenomen geweest in
Psychofarmaca bij d e de ouderen Waarom slikken zij? A D. D Hooghe Hooghe
 Psychofarmaca bij de ouderen Waarom slikken zij? A. D Hooghe Psychofarmaca Benzodiazepines en aanverwanten Antidepressiva Antipsychotica Antipsychotica Assessment of antipsychotic prescribing in Belgian
Psychofarmaca bij de ouderen Waarom slikken zij? A. D Hooghe Psychofarmaca Benzodiazepines en aanverwanten Antidepressiva Antipsychotica Antipsychotica Assessment of antipsychotic prescribing in Belgian
Aanvraagformulier REGISTRATIE oncologie monitor
 Aanvraagformulier REGISTRATIE oncologie monitor 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:... Geboorteplaats:... Werkzaam bij: Organisatie + Afdeling:...
Aanvraagformulier REGISTRATIE oncologie monitor 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:... Geboorteplaats:... Werkzaam bij: Organisatie + Afdeling:...
Kwaliteitsborging onderzoek in het. NVMETC bijeenkomst 23 november UMC Utrecht. Oktober 2016
 1 Kwaliteitsborging onderzoek in het UMC Utrecht NVMETC bijeenkomst 23 november 2016 Eugenie Ram, kwaliteitsmanager Onderzoek - Office Concernstaf Raad van Bestuur Oktober 2016 UMC Utrecht breed kwaliteitssysteem
1 Kwaliteitsborging onderzoek in het UMC Utrecht NVMETC bijeenkomst 23 november 2016 Eugenie Ram, kwaliteitsmanager Onderzoek - Office Concernstaf Raad van Bestuur Oktober 2016 UMC Utrecht breed kwaliteitssysteem
Redon drainage bij post-sternotomie mediastinitis. Ivan Theunissen ANIOS Intensive Care
 Redon drainage bij post-sternotomie mediastinitis Ivan Theunissen ANIOS Intensive Care 20-05-2019 Post-sternotomie mediastinitis (PSM) Ernstige complicatie hartchirurgie Incidentie: 1-3% Verhoogde mortaliteit
Redon drainage bij post-sternotomie mediastinitis Ivan Theunissen ANIOS Intensive Care 20-05-2019 Post-sternotomie mediastinitis (PSM) Ernstige complicatie hartchirurgie Incidentie: 1-3% Verhoogde mortaliteit
Danazol voor idiopathische pulmonale fibrose
 Danazol voor idiopathische pulmonale fibrose Thijs W. Hoffman 18-04-2018 Idiopathische pulmonale fibrose (IPF) Normaal Ernstige interstitiële longziekte Ca. 3000 patiënten in NL Verlittekening van de longen
Danazol voor idiopathische pulmonale fibrose Thijs W. Hoffman 18-04-2018 Idiopathische pulmonale fibrose (IPF) Normaal Ernstige interstitiële longziekte Ca. 3000 patiënten in NL Verlittekening van de longen
Ervaringen met document X
 Martini Ziekenhuis Groningen Ervaringen met document X Ellen Rusch, wetenschappelijk medewerker Wetenschappelijk Instituut Wat gaan we doen? Structuur lokale haalbaarheid Martini Ziekenhuis Het werken
Martini Ziekenhuis Groningen Ervaringen met document X Ellen Rusch, wetenschappelijk medewerker Wetenschappelijk Instituut Wat gaan we doen? Structuur lokale haalbaarheid Martini Ziekenhuis Het werken
Handleiding. Investigational Medicinal Product Dossier (IMPD)
 Handleiding Investigational Medicinal Product Dossier (IMPD) Inhoudsopgave Afkortingen... - 3 - Wat is het IMPD?... - 4 - Beslisschema inhoud IMPD... - 5 - Beschrijving inhoud IMPD... - 6 - Overzicht hoofdstukken
Handleiding Investigational Medicinal Product Dossier (IMPD) Inhoudsopgave Afkortingen... - 3 - Wat is het IMPD?... - 4 - Beslisschema inhoud IMPD... - 5 - Beschrijving inhoud IMPD... - 6 - Overzicht hoofdstukken
Klinische implicaties van de EVOLVE studie
 ASN Review 2012 Klinische implicaties van de EVOLVE studie Marc Vervloet, internist-nefroloog VU medisch centrum Associatie PTH met mortaliteit Kalantar-Zadeh, Kidney Int 2007 Welke evidence? Associatie
ASN Review 2012 Klinische implicaties van de EVOLVE studie Marc Vervloet, internist-nefroloog VU medisch centrum Associatie PTH met mortaliteit Kalantar-Zadeh, Kidney Int 2007 Welke evidence? Associatie
1. Inloggen. 1.1 Eerste keer inloggen
 . Inloggen LET OP: Deze handleiding beschrijft data invoer voor de RACOST studie in de studie-database. Deze database is niet geschikt voor testdoeleinden. Als u de handelingen uit deze handleiding wilt
. Inloggen LET OP: Deze handleiding beschrijft data invoer voor de RACOST studie in de studie-database. Deze database is niet geschikt voor testdoeleinden. Als u de handelingen uit deze handleiding wilt
Positieve, Negatieve en Depressieve Subklinische Psychotische Symptomen en het Effect van Stress en Sekse op deze Subklinische Psychotische Symptomen
 Positieve, Negatieve en Depressieve Subklinische Psychotische Symptomen en het Effect van Stress en Sekse op deze Subklinische Psychotische Symptomen Positive, Negative and Depressive Subclinical Psychotic
Positieve, Negatieve en Depressieve Subklinische Psychotische Symptomen en het Effect van Stress en Sekse op deze Subklinische Psychotische Symptomen Positive, Negative and Depressive Subclinical Psychotic
Praktische implementatie Europese verordening Geneesmiddelen onderzoek
 Praktische implementatie Europese verordening Geneesmiddelen onderzoek Dr. Joost Keers Hoofd Wetenschappelijk Instituut j.keers@mzh.nl 050 524 5826 http://www.ccmo.nl/nl/europese-verordening Belangrijke
Praktische implementatie Europese verordening Geneesmiddelen onderzoek Dr. Joost Keers Hoofd Wetenschappelijk Instituut j.keers@mzh.nl 050 524 5826 http://www.ccmo.nl/nl/europese-verordening Belangrijke
Standaard onderzoeksdossier voor indiening van een onderzoeksvoorstel bij een WMO-toetsingscommissie en/of de bevoegde instantie
 Standaard onderzoeksdossier voor indiening van een onderzoeksvoorstel bij een WMO-toetsingscommissie en/of de bevoegde instantie A. Brieven A1: Aanbiedingsbrief aan toetsingscommissie en bevoegde instantie
Standaard onderzoeksdossier voor indiening van een onderzoeksvoorstel bij een WMO-toetsingscommissie en/of de bevoegde instantie A. Brieven A1: Aanbiedingsbrief aan toetsingscommissie en bevoegde instantie
Gids voor het interpreteren van spontane meldingen van vermoedelijke bijwerkingen van geneesmiddelen
 30 januari 2017 Inspecties, bewaking voor menselijk gebruik en comités EMA/749446/2016 Herziening 1* Gids voor het interpreteren van spontane meldingen van vermoedelijke bijwerkingen Overeenstemming door
30 januari 2017 Inspecties, bewaking voor menselijk gebruik en comités EMA/749446/2016 Herziening 1* Gids voor het interpreteren van spontane meldingen van vermoedelijke bijwerkingen Overeenstemming door
Onderstaande vragen zijn van toepassing op de periode maanden postoperatief
 9. Follow-up Aantal maanden? Datum: Setting: O klinisch O poliklinisch Beoordelaar: (naam) Algemeen Onderstaande vragen zijn van toepassing op de periode 12- postoperatief Is de patient opgenomen geweest
9. Follow-up Aantal maanden? Datum: Setting: O klinisch O poliklinisch Beoordelaar: (naam) Algemeen Onderstaande vragen zijn van toepassing op de periode 12- postoperatief Is de patient opgenomen geweest
TB zonder positieve kweek: hoe hard is de diagnose? Cecile Magis-Escurra, longarts Consulent klinische tuberulose KNCV/NVALT NTDD 20 juni 2013
 TB zonder positieve kweek: hoe hard is de diagnose? Cecile Magis-Escurra, longarts Consulent klinische tuberulose KNCV/NVALT NTDD 20 juni 2013 Gouden standaard TB diagnose: positieve kweek Mycobacterium
TB zonder positieve kweek: hoe hard is de diagnose? Cecile Magis-Escurra, longarts Consulent klinische tuberulose KNCV/NVALT NTDD 20 juni 2013 Gouden standaard TB diagnose: positieve kweek Mycobacterium
Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) Team Klinisch Onderzoek
 Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) 2014-2016 Team Klinisch Onderzoek Toezicht op IIT 2014-2016 Aanleiding en werkwijze Bevindingen vanuit de praktijk Conclusies en aandachtspunten
Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) 2014-2016 Team Klinisch Onderzoek Toezicht op IIT 2014-2016 Aanleiding en werkwijze Bevindingen vanuit de praktijk Conclusies en aandachtspunten
Aanmelden WMO-plichtig onderzoek
 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd wordt bij het aanmelden van onderzoek dat onder de WMO valt en waarbij ZGV optreedt als deelnemend centrum. Voordat
Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd wordt bij het aanmelden van onderzoek dat onder de WMO valt en waarbij ZGV optreedt als deelnemend centrum. Voordat
Clinical Trials in Nederland: op weg naar topkwaliteit DCTF Congres 3 oktober 2012 Lunteren. M.P.W. Lamberti, BA Algemeen Directeur
 Clinical Trials in Nederland: op weg naar topkwaliteit DCTF Congres 3 oktober 2012 Lunteren M.P.W. Lamberti, BA Algemeen Directeur Maastricht UMC-Holding MUMC-Holding CTCM BPCM MI Groningen Utrecht Nijmegen
Clinical Trials in Nederland: op weg naar topkwaliteit DCTF Congres 3 oktober 2012 Lunteren M.P.W. Lamberti, BA Algemeen Directeur Maastricht UMC-Holding MUMC-Holding CTCM BPCM MI Groningen Utrecht Nijmegen
Melden. aan de IGZ. Jeroen van Baare Senior inspecteur IGZ
 Melden aan de IGZ Jeroen van Baare Senior inspecteur IGZ Wanneer moet je melden? Wie moet melden? Wat moet melden? Wat gebeurt er na de melding? 2 Alle ernstige ongewenste voorvallen en ernstige ongewenste
Melden aan de IGZ Jeroen van Baare Senior inspecteur IGZ Wanneer moet je melden? Wie moet melden? Wat moet melden? Wat gebeurt er na de melding? 2 Alle ernstige ongewenste voorvallen en ernstige ongewenste
Zorgpaden: Evidence Based or Wishful thinking?
 Zorgpaden: Evidence Based or Wishful thinking? Jeroen van Oostrum Hoofd Business Intelligence Center 24 november 2009 Stellingen Stelling 1: Patiëntuitkomstmaten, zoals heropnames, complicaties en patiënttevredenheid,
Zorgpaden: Evidence Based or Wishful thinking? Jeroen van Oostrum Hoofd Business Intelligence Center 24 november 2009 Stellingen Stelling 1: Patiëntuitkomstmaten, zoals heropnames, complicaties en patiënttevredenheid,
nee nee nee Wordt proefpersoon aan handelingen onderworpen of gedragswijze opgelegd?
 Medischwetenschappelijk onderzoek en deelname proefpersonen? Wordt proefpersoon aan handelingen onderworpen of gedragswijze opgelegd? Worden behandelingen met elkaar via randomisatie vergeleken? Vallen
Medischwetenschappelijk onderzoek en deelname proefpersonen? Wordt proefpersoon aan handelingen onderworpen of gedragswijze opgelegd? Worden behandelingen met elkaar via randomisatie vergeleken? Vallen
Tweede Kamer der Staten-Generaal
 Tweede Kamer der Staten-Generaal 2 Vergaderjaar 2012 2013 33 646 Wijziging van de Wet medisch-wetenschappelijk onderzoek met mensen in verband met een uitbreiding van de meldingsplicht van ernstige ongewenste
Tweede Kamer der Staten-Generaal 2 Vergaderjaar 2012 2013 33 646 Wijziging van de Wet medisch-wetenschappelijk onderzoek met mensen in verband met een uitbreiding van de meldingsplicht van ernstige ongewenste
De praktijk van deferred consent bij spoedeisend onderzoek
 De praktijk van deferred consent bij spoedeisend onderzoek dr Erwin J.O. Kompanje Universitair docent klinische ethiek Klinisch ethicus Intensive care geneeskunde Het effect van wel/niet gebruik van Deferred
De praktijk van deferred consent bij spoedeisend onderzoek dr Erwin J.O. Kompanje Universitair docent klinische ethiek Klinisch ethicus Intensive care geneeskunde Het effect van wel/niet gebruik van Deferred
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik
 EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
Weefselvigilantie in een academisch ziekenhuis. Michaela van Bohemen, hemovigilantieconsulent en weefselvigilantiecoördinator Erasmus MC Rotterdam
 Weefselvigilantie in een academisch ziekenhuis Michaela van Bohemen, hemovigilantieconsulent en weefselvigilantiecoördinator Erasmus MC Rotterdam Wat is weefselvigilantie? Definitie volgens TRIP: Systematisch
Weefselvigilantie in een academisch ziekenhuis Michaela van Bohemen, hemovigilantieconsulent en weefselvigilantiecoördinator Erasmus MC Rotterdam Wat is weefselvigilantie? Definitie volgens TRIP: Systematisch
Includeer hem maar in de studie. De familie is onderweg!
 Includeer hem maar in de studie. De familie is onderweg! Ethiek van toestemming voor onderzoek in spoedeisende situaties dr Erwin J.O. Kompanje Department of Intensive Care Spoedeisend onderzoek op intensive
Includeer hem maar in de studie. De familie is onderweg! Ethiek van toestemming voor onderzoek in spoedeisende situaties dr Erwin J.O. Kompanje Department of Intensive Care Spoedeisend onderzoek op intensive
DATAVERZAMELING IN KLINISCHE TRIALS HET BELANG VAN GOEDE DATA LIDWINA WEVER, COÖRDINATOR TRIALBUREAU AVL
 DATAVERZAMELING IN KLINISCHE TRIALS HET BELANG VAN GOEDE DATA LIDWINA WEVER, COÖRDINATOR TRIALBUREAU AVL MIJN VERHAAL UIT HET BOEKJE Klinische trials vormen de basis voor de nieuwe ontwikkelingen binnen
DATAVERZAMELING IN KLINISCHE TRIALS HET BELANG VAN GOEDE DATA LIDWINA WEVER, COÖRDINATOR TRIALBUREAU AVL MIJN VERHAAL UIT HET BOEKJE Klinische trials vormen de basis voor de nieuwe ontwikkelingen binnen
Ongewenste uitkomsten van zorg
 Ongewenste uitkomsten van zorg De belangrijkste vragen op een rij Juni 2016 Drie vormen van ongewenste uitkomsten van zorg 1. Calamiteit 2. Incident 3. Complicatie Wat zijn de verschillen en hoe kunnen
Ongewenste uitkomsten van zorg De belangrijkste vragen op een rij Juni 2016 Drie vormen van ongewenste uitkomsten van zorg 1. Calamiteit 2. Incident 3. Complicatie Wat zijn de verschillen en hoe kunnen
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U11 Voortgangsrapportage Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: U11 Voortgangsrapportage Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U5 Datamanagement Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: U5 Datamanagement Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
CCMO Structuur documenten Technische Toetsing (ass.secr.) Inhoudelijke Toetsing (secretaris)
 CHECKLIST WMO Primaire indieningsproces WMO in METC Management, screening door Assistent Secretaris. Hieronder staan de generieke uitgangspunten en is toegelicht hoe de primaire toetsing indiening WMO
CHECKLIST WMO Primaire indieningsproces WMO in METC Management, screening door Assistent Secretaris. Hieronder staan de generieke uitgangspunten en is toegelicht hoe de primaire toetsing indiening WMO
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: O3 Ontwikkelen, implementeren en beheren van SOP s Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies
Standard Operating Procedure STZ SOP: O3 Ontwikkelen, implementeren en beheren van SOP s Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies
Nederlandse samenvatting
 Dit proefschrift richt zich op statinetherapie in type 2 diabetespatiënten; hiervan zijn verschillende aspecten onderzocht. In Deel I worden de effecten van statines op LDLcholesterol en cardiovasculaire
Dit proefschrift richt zich op statinetherapie in type 2 diabetespatiënten; hiervan zijn verschillende aspecten onderzocht. In Deel I worden de effecten van statines op LDLcholesterol en cardiovasculaire
Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen
 Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen Afdeling Farmaceutische Bedrijven, Klinisch Onderzoek Good Clinical Practice Inhoud Wat doet de IGJ aan toezicht op klinisch
Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen Afdeling Farmaceutische Bedrijven, Klinisch Onderzoek Good Clinical Practice Inhoud Wat doet de IGJ aan toezicht op klinisch
Follow-up na: maanden Datum: - - d d m m m j j j j. Voor de wondscore: (naam)
 Follow-up na: maanden Datum: Setting: O klinisch O poliklinisch Beoordelaar: (naam) Voor de wondscore: (naam) Functie beoordelaar: O Geblindeerde (stoma-)verpleegkundige,o Geblindeerde arts-assistent,
Follow-up na: maanden Datum: Setting: O klinisch O poliklinisch Beoordelaar: (naam) Voor de wondscore: (naam) Functie beoordelaar: O Geblindeerde (stoma-)verpleegkundige,o Geblindeerde arts-assistent,
BeNeDuctus Studie Onderzoek naar een optimale behandeling van een open ductus arteriosus (Botalli) bij te vroeg geboren kinderen.
 OUDERINFORMATIE BeNeDuctus Studie Onderzoek naar een optimale behandeling van een open ductus arteriosus (Botalli) bij te vroeg geboren kinderen. Geachte mevrouw/mijnheer, Uw kind is opgenomen op de Intensive
OUDERINFORMATIE BeNeDuctus Studie Onderzoek naar een optimale behandeling van een open ductus arteriosus (Botalli) bij te vroeg geboren kinderen. Geachte mevrouw/mijnheer, Uw kind is opgenomen op de Intensive
Onderstaande vragen zijn van toepassing op de periode 0-3 maanden postoperatief
 Aantal maanden? Setting: O klinisch O poliklinisch Beoordelaar: (naam) Algemeen Onderstaande vragen zijn van toepassing op de periode 0- postoperatief Is de patient opgenomen geweest in een van de volgende
Aantal maanden? Setting: O klinisch O poliklinisch Beoordelaar: (naam) Algemeen Onderstaande vragen zijn van toepassing op de periode 0- postoperatief Is de patient opgenomen geweest in een van de volgende
Doc.Ref.: CMDh/PhVWP/042/2012 January 2012 SUMMARY OF PRODUCT CHARACTERISTICS. New Class Warnings
 HMG-CoA Reductase Inhibitors and safety the risk of new onset diabetes/impaired glucose metabolism Final SmPC and PL wording agreed by PhVWP December 2011 Doc.Ref.: CMDh/PhVWP/042/2012 January 2012 SUMMARY
HMG-CoA Reductase Inhibitors and safety the risk of new onset diabetes/impaired glucose metabolism Final SmPC and PL wording agreed by PhVWP December 2011 Doc.Ref.: CMDh/PhVWP/042/2012 January 2012 SUMMARY
Propylhexedrine. Eventin. Postfach Ludwigshafen DE Germany. Lid-Staten Registratiehouder Naam van het geneesmiddel
 Bijlage I 3 Stoff: Propylhexedrine Lid-Staten Registratiehouder Naam van het geneesmiddel Duitsland Knoll AG Postfach 210805 Ludwigshafen DE 67008 Germany Eventin 4 Stoff: Fenbutrazaat Lid-Staten Registratiehouder
Bijlage I 3 Stoff: Propylhexedrine Lid-Staten Registratiehouder Naam van het geneesmiddel Duitsland Knoll AG Postfach 210805 Ludwigshafen DE 67008 Germany Eventin 4 Stoff: Fenbutrazaat Lid-Staten Registratiehouder
Kennislacunes NHG-Standaard Artritis
 Kennislacunes Kennislacunes* (Etiologie jichtartritis, reactieve artritis, reumatoïde artritis (hoofdtekst)) (Betrouwbare cijfers over het voorkomen van artritiden in de huisartspraktijk (met uitzondering
Kennislacunes Kennislacunes* (Etiologie jichtartritis, reactieve artritis, reumatoïde artritis (hoofdtekst)) (Betrouwbare cijfers over het voorkomen van artritiden in de huisartspraktijk (met uitzondering
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U7 Ondersteunende diensten Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: U7 Ondersteunende diensten Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Waarom koelen na out of hospital reanimatie? Klinische les IC-verpleegkundigen 1 december 2006 Intensive Care Laurentius ziekenhuis, Roermond
 Waarom koelen na out of hospital reanimatie? Marlous Steeghs,, keuze co-assistent Klinische les IC-verpleegkundigen 1 december 2006 Intensive Care Laurentius ziekenhuis, Roermond Inleiding Cardiac arrest
Waarom koelen na out of hospital reanimatie? Marlous Steeghs,, keuze co-assistent Klinische les IC-verpleegkundigen 1 december 2006 Intensive Care Laurentius ziekenhuis, Roermond Inleiding Cardiac arrest
Registratie van bijwerkingen door huisartsen
 Registratie van bijwerkingen door huisartsen 3 april 2014 GGG Congres Jako Burgers Monique Verduijn www.lareb.nl Inhoud Inleiding Bijwerkingen in de praktijk Herkennen van bijwerkingen door de huisarts
Registratie van bijwerkingen door huisartsen 3 april 2014 GGG Congres Jako Burgers Monique Verduijn www.lareb.nl Inhoud Inleiding Bijwerkingen in de praktijk Herkennen van bijwerkingen door de huisarts
Data invoer instructies OpenClinica
 Data invoer instructies OpenClinica TRUTH studie Inhoudsopgave Contactgegevens... 1 Introductie... 1 Legenda pictogrammen... 1 Inloggen... 2 Proefpersoon toevoegen... 2 Data invoeren... 2 Failed Validation
Data invoer instructies OpenClinica TRUTH studie Inhoudsopgave Contactgegevens... 1 Introductie... 1 Legenda pictogrammen... 1 Inloggen... 2 Proefpersoon toevoegen... 2 Data invoeren... 2 Failed Validation
Geachte MR CLEAN-Registry onderzoeker,
 Geachte MR CLEAN-Registry onderzoeker, Dank u zeer voor het aanmelden van een patiënt voor de MRCLEAN-Registry. Mocht u vragen hebben of onduidelijkheden kunt u onder kantooruren bellen met de MRCLEAN-Registry
Geachte MR CLEAN-Registry onderzoeker, Dank u zeer voor het aanmelden van een patiënt voor de MRCLEAN-Registry. Mocht u vragen hebben of onduidelijkheden kunt u onder kantooruren bellen met de MRCLEAN-Registry
Consent voor spoedeisend onderzoek bij acuut ernstig zieke patienten
 Consent voor spoedeisend onderzoek bij acuut ernstig zieke patienten dr Erwin J.O. Kompanje Erasmus MC Universitair medisch centrum Rotterdam Intensive Care volwassenen Spoedeisend onderzoek, definitie/
Consent voor spoedeisend onderzoek bij acuut ernstig zieke patienten dr Erwin J.O. Kompanje Erasmus MC Universitair medisch centrum Rotterdam Intensive Care volwassenen Spoedeisend onderzoek, definitie/
