FOD Volksgezondheid, Veiligheid van de Voedselketen en Leefmilieu. Directoraat-generaal Geneesmiddelen
|
|
|
- Hans Jonker
- 8 jaren geleden
- Aantal bezoeken:
Transcriptie
1 Afdeling Wig ilantie' Amazone Afdeling `138(D'(Onderzoek&Ontwikkeling) Bischoffsheimlaan 33 B-1000 BRUSSEL Belgisch Centrum voor Geneesmiddelenbewaking voor geneeesmiddelen voor humaan gebruik Uw brief van: Uw kenmerk: Omzendbrief nr 460 Ter attentie van Ons kenmerk: DGM/MG de verantwoordelijke voor Datum: OL geneesmiddelenbewaking inzake geneesmiddelen voor humaan gebruik en de opdrachtgevers van klinische proeven Bijlage(n): Telefoon Onthaal: Fax : Betreft: Toelichting betreffende : 1. Versnelde notificatie (binnen 7/15 dagen) van individuele rapporten van en van niet-geregistreerde en geregistreerde geneesmiddelen aan het directoraat-generaal Geneesmiddelen 2. Versnelde notificatie (binnen 7/15 dagen) van individuele rapporten van en van niet-geregistreerde en geregistreerde geneesmiddelen aan de Leidende Ethische Comites 3. Het in voege treden van elektronische rapportering van individuele rapporten van en in de 'Europese Economische Ruimte' ter aanvulling van de omzendbrief nr. 436 dd. 12 november 2003 Mevrouw, Mijnheer, Deze omzendbrief heeft tot doel u toelichting te verschaffen bij de actuele wetgeving die u verplicht individuele rapporten van en met geneesmiddelen, al dan niet geregistreerd, optredend uit klinische proeven of buiten klinische studies (spontane rapportering), over te maken aan het directoraat-generaal Geneesmiddelen (DGG) en de Leidende Ethische Comites. Dit kan momenteel hetzij niet-elektronisch (papier, PDF) hetzij elektronisch (ich-e2b-formaat) gebeuren. Rapporten, die via (PDF,...) ontvangen worden, worden niet beschouwd als een elektronische rapportering. Beide systemen zullen toegelicht worden. Ter verduidelijking herhalen wij ook enkele definities uit de Wet van 7 mei 2004 inzake experimenten op de menselijke persoon en uit de omzendbrief nr. 455 dd. 28 november Daarnaast willen wij extra aandacht besteden aan wat dient gerapporteerd te worden en u de' criteria verduidelijken voor zowel niet-elektronisch als elektronisch rapporteren. I. Definities (Wet dd. 7 mei 2004; omzendbrief nr. 455 dd. 28 november 2004) Een "klinische proef', hierna te noemen "proef', is elk onderzoek bij de menselijke persoon dat bedoeld is om de klinische, farmacologische en/of andere farmacodynamische bijwerkingen van één of meerdere geneesmiddelen voor onderzoek vast te stellen of te bevestigen, en/of eventuele bijwerkingen van aan of Contactpersoon: Mevr. Margriet Gabriels Margiet.nbrielsabhealth.fgov Tel.: Fax: Bezoekadres: Amazone Bischoffsheimlaan Bruxelles bttp://
2 meer geneesmiddelen voor onderzoek te signaleren en/of de resorptie, de distributie, het metabolisme en de uitscheiding van één of meer geneesmiddelen voor onderzoek te bestuderen, teneinde de veiligheid en/of de werkzaamheid van deze geneesmiddelen vast te stellen. Een "proef zonder interventie" is een onderzoek waarbij de geneesmiddelen worden voorgeschreven op de gebruikelijke wijze, overeenkomstig de in de vergunning voor het in de handel brengen vastgestelde voorwaarden. De indeling van de patient bij een bepaalde therapeutische strategie wordt niet van tevoren door een onderzoeksprotocol bepaald, maar maakt deel uit van de gangbare medische praktijk, en het besluit om het geneesmiddel voor te schrijven staat geheel los van het besluit om een patient te laten deelnemen aan het onderzoek. De patient in kwestie hoeft geen extra diagnostische of controleprocedure te doorlopen, en voor de analyse van de verkregen resultaten worden epidemiologische methodes gebruikt. Een "geneesmiddel voor onderzoek" is een farmaceutische vorm van een werkzame stof of een placebo die bij een klinische proef wordt onderzocht of als referentie wordt gebruikt, met inbegrip van een geneesmiddel waarvoor een vergunning voor het in de handel brengen is afgegeven maar dat op een andere manier wordt gebruikt of samengesteld (geformuleerd of verpakt) dan de toegelaten vorm, voor een niettoegelaten indicatie wordt gebruikt of wordt gebruikt om nadere informatie te krijgen over de toegelaten toepassing. Een "ongewenst voorval" is een schadelijk verschijnsel bij een patient of een deelnemer aan de behandelde groep tijdens een experiment, dat niet noodzakelijk met die behandeling verband houdt. Een "bijwerking" is elke schadelijke en niet gewenste reactie op een geneesmiddel voor onderzoek of op een experiment en, wanneer het om een geneesmiddel voor onderzoek gaat, ongeacht de toegediende dosis. Een " bijwerking" is een bijwerking waarvan de aard of de ernst niet overeenkomt met de informatie over het experiment en, wanneer het om een proef gaat, met de informatie over het product (zoals het onderzoekersdossier voor een geneesmiddel voor onderzoek waarvoor geen vergunning is afgegeven of in het geval van een geneesmiddel waarvoor een vergunning is afgegeven, de in de bijsluiter vervatte samenvatting van de kenmerken van het product). Een "ernstig ongewenst voorval" of een "" is een ongewenst voorval of een bijwerking die dodelijk is, levensgevaar oplevert voor de proefpersoon, opname in een ziekenhuis of verlenging van de opname noodzakelijk maakt, blijvende of significante invaliditeit of arbeidsongeschiktheid veroorzaakt, dan wel zich uit in een aangeboren afwijking of misvorming, en dit, wanneer het om een proef gaat, ongeacht de dosis. Een "opdrachtgever" is een persoon, bedrijf, instelling of organisatie die de verantwoordelijkheid op zich neemt voor het starten, het beheer en/of de financiering van een experiment. In het Kader van deze omzendbrief is het verschil tussen "pre"-registratie en "post"- registratie enkel gebaseerd op de registratie-status van een geneesmiddel in BELGIE. Een geneesmiddel wordt als een geregistreerd geneesmiddel beschouwd van zodra een vergunning voor het in de handel brengen van dat geneesmiddel toegekend werd. 2
3 Dit houdt in dat: 1. Alle rapporten afkomstig van een klinische proef met een in Belgie nietgeregistreerd geneesmiddel worden beschouwd als "pre-registratie" rapporten; 2. Alle rapporten, afkomstig uit een klinische proef met een in Belgie geregistreerd geneesmiddel worden beschouwd als "post-registratie" rapporten, ook indien de klinische proef wordt uitgevoerd in een nietgeregistreerde indicatie. Alle rapporten afkomstig uit een klinische proef met een geneesmiddel waarvan de registratieprocedure lopende is, worden beschouwd als 'pre-registratie' rapporten. Wat dient gerapporteerd te worden?.1./ Alle en en (SUSARs) die vermoedelijk gerelateerd zijn aan het geneesmiddel in onderzoek (experimenteel product zowel als comparator) in een klinische proef, die een onderzoeksplaats in Belgie heeft, dienen versneld gerapporteerd te worden. 2./ Bijkomend voor geneesmiddelen, die niet geregistreerd zijn in Belgie, dienen naast SUSARs die optreden tijdens een klinische proef, lopende in Belgie, ook SUSARs, afkomstig van andere niet-belgische klinische proeven met hetzelfde geneesmiddel, gerapporteerd te worden. Dit zijn : de SUSARs die optreden in een andere klinische proef, maar onder de verantwoordelijkheid van dezelfde opdrachtgever en afkomstige uit landen van de Europese Economische Ruimte (EER) of uit landen daarbuiten; de SUSARs die spontaan gemeld werden en deze afkomstig uit publicaties; de SUSARs die overgemaakt worden aan de opdrachtgever door een andere Iidstaat. Ook andere relevante informatie dient gerapporteerd te worden, indien deze de huidige risico/baten-beoordeling van het geneesmiddel in onderzoek wijzigen of een aanpassing in de toediening van het geneesmiddel of de uitvoering van de klinische proef vereisen, o.a. : individuele rapporten van verwachte bijwerkingen met een afloop vb. dodelijke afloop; een stijging in frequentie van optreden van verwachte bijwerkingen, die als klinisch' belangrijk beschouwd wordt; SUSARs die optreden nadat de patient de studie beêindigd heeft, en die de onderzoeker aan de opdrachtgever heeft overgemaakt; elke SUSAR gerelateerd aan de uitvoering van de klinische proef als dusdanig of elke informatie voortkomend uit de niet-klinische ontwikkeling van het geneesmiddel in onderzoek, die de veiligheid van proefpersonen eventueel in vraag stelt, zoals 3
4 n n n een gerelateerd aan de studieprocedure en die het verloop van de klinische proef kan wijzigen. Deze bijwerkingen dienen niet individueel gerapporteerd te worden maar dienen vermeld te worden in de zesmaandelijkse of jaarlijkse rapporten, voor zover het geneesmiddel in onderzoek niet (mede) van de bijwerking verdacht wordt; elk significant risico voor de proefpersonen en latere gebruikers, zoals by. een gebrek aan werkzaamheid van een geneesmiddel in onderzoek ter behandeling van een levensbedreigende ziekte; elke belangrijke bevinding betreffende de veiligheid van het geneesmiddel afkomstig van dierstudies (vb. carcinogeniciteit). 3./ Voor geneesmiddelen in onderzoek, die in Belgie geregisteerd zijn, blijft de huidige wetgeving ook van kracht. Wanneer het geneesmiddel in onderzoek in Belgi6 geregistreerd is en de opdrachtgever tevens de houder is van een vergunning voor het in de handel brengen van geneesmiddelen voor menselijk gebruik (= vergunninghouder), dient de Belgische reglementering betreffende farmacovigilantie (K.B. dd. 3 juli 1969) gevolgd te _yvorden. III. Het niet-elektronisch verzenden van individuele rapporten van ernstige bijwerkingen Volgens de actuele wetgeving dienen volgende meldingen naar het DGG gerapporteerd te worden : Rapporten uit klinische proeven Tabel 1 geeft aan op welke wijze individuele rapporten van ernstige, bijwerkingen, voorgekomen met een geneesmiddel in onderzoek, al dan niet geregistreerd, en waarmee een klinische proef lopende in Belgiè, dienen genotifieerd te worden. Het betreft bijwerkingen afkomstig uit Belgié, de EER of een land daarbuiten. Op basis van het K.B. dd. 3 juli 1969 dienen ook de ernstige verwachte bijwerkingen, die in Belgid optreden, gerapporteerd te worden door de vergunninghouder. 4
5 Tabel 1 : Notificatie van individuele rapporten van ernstige bijwerkngen uit klinische proeven Registratiestatus Pre Oorsprong/type van rapporten Tijdslijn Rapporteur Aan wie? Volgens Wet dd. 07/05/2004 en K.B. dd. 30/06/2004*** Belgié/ RD(1)/EC (3) Ander land in de EER/ RD 7/15 dagen Opdrachtgever RD Belgie/ VIG(2)/EC Ander land in de EER/ 7/15 dagen Opdrachtgever VIG VIG Volgens K.B. dd. 3/07/1969* en Verordening 2309/93/EC* (vanaf 20/11/2005 : Verordening 7 6/2004/EC*) verwachte 15 dagen Vergunninghouder VIG * Alle referenties zijn terug te vinden op de website van het DGG ( en van het Europees Geneesmiddelenbureau (eudravigilance.emea.eu.int) Bijhorende guidance documenten zijn : "Detailed guidance on the collection, verification and presentation of adverse reaction reports arising from clinical trials on medicinal products for human use" en "Detailed guidance on the European database of Suspected Unexpected Serious Adverse Reactions (EudraVigilance Clinical Trial Module)" In geval dat de SUSAR een overlijden betreft of ertoe geleid heeft of levensbedreigend is, dient het rapport binnen de 7 dagen toegestuurd te worden; alle relevante informatie over de gevolgen daarvan dient vervolgens binnen een nieuwe termijn van 8 dagen meegedeeld te worden. 11) RD = afdeling 'RD' (Onderzoek&Ontwikkeling) (2)VIG = afdeling (3)EC = Leidend Ethisch Comite Gezien comparators (meestal) geregistreerde geneesmiddelen zijn, hebben zij de registratiestatus van "" in Tabel 1. Zij dienen dus naar de afdeling "Vigilantie" gestuurd te worden. Indien de opdrachtgever van de klinische proef verschillend is van de vergunnninghouder van de comparator, zal het DGG de rapporten anoniem aan die vergunninghouder overmaken Spontane meldingen en meldingen uit niet-interventionele klinische proeven Tabel 2 beschrijft hoe spontane meldingen van verwachte en ernstige bijwerkingen van geregistreerde geneesmiddelen, optredend in Belgiè, dienen gerapporteerd te worden. Spontane meldingen uit landen buiten de EER voor zowel niet-geregistreerde als geregistreerde geneesmiddelen dienen gerapporteerd te worden, indien het een betreft. 5
6 Tabel 2 : Notificatie van individuele rapporten van spontane meidingen van ernstige bijwerkingen en van en uit klinische proeven zonder interventie Registratiestatus Oorsprong/type van rapporten Tijdslijn* Rapporteur Aan wie? Referentie" Spontane melding Pre Wet dd. 07/05/2004 7/15 dagen Opdrachtgever RD(1) K.B. dd. 30/06/2004, als de EEA opdrachtgever op de hoogte is van het rapport verwachte ernstige bijwerking VIG(2) Belgiè/ 15 dagen Vergunninghouder K.B. dd. 3/7/1969 VIG/EC(3) Verord. 2309/93/EC// vanaf 20/11/2005 : Verord. 726/2004/EC VIG Eudralex Vol. 9 Pre Rapporten uit klinische proeven zonder interventie verwachte ernstige bijwerking 7/15 dagen Opdrachtgever RD 15 dagen Vergunninghouder Opdrachtgever Opdrachtgever VIG VIG/EC VIG ICH E2D Eudralex Vol. 9 K.B. dd. 3/7/1969 Verord. 2309/93/EC// vanaf 20/11/2005 : Verord. 726/2004/EC ICH E2D Eudralex Vol. 9 * Alle referenties zijn terug te vinden op de website van het DGG ( en van het Europees Geneesmiddelenbureau (eudravigilance.emea.eu.int) Bijhorende guidance documenten zijn : "Detailed guidance on the collection, verification and presentation of adverse reaction reports arising from clinical trials on medicinal products for human use" en "Detailed guidance on the European database of Suspected Unexpected Serious Adverse Reactions feudravigilance Clinical Trial Module)" In geval dat de SUSAR een overlijden betreft of ertoe geleid heeft of levensbedreigend is, dient het rapport binnen de 7 dagen toegestuurd te worden; alle relevante informatie over de gevolgen dient vervolgens binnen een nieuwe termijn van 8 dagen meegedeeld te worden. (1)RD = afdeling RD (onderzoek en ontwikkeling) (2)VIG = Afdeling (3)EC = Leidend Ethisch Comite Opmerkinq : Een melding, die in het land van herkomst als spontaan wordt beschouwd, wordt ook binnen de EER als een spontane melding beschouwd, ook al betreft het een een niet-geregistreerd geneesmiddel in een klinische proef in Belgiè. 6
7 Rapporten van en uit niet-interventionele klinische proeven volgen de regels voor spontane rapportering, zoals aangegeven is in Tabel 2. De verantwoordelijkheid voor o.a. het rapporteren van bijwerkingen blijft bij de opdrachtgever van de klinische proef, ook als hij deze taak in praktijk door derden laat uitvoeren Naar welke afdeling van het DGG dienen de rapporten doorgestuurd te worden? In bovenstaande tabellen (Tabel 1 en 2) wordt aangegeven aan wie de rapporten dienen gezonden te worden. De individuele rapporten betreffende bijwerkingen met niet-geregistreerde geneesmiddelen dienen naar het departement 'R&D' (Onderzoek&Ontwikkeling) ter attentie van Mevr. Greet Musch gezonden te worden. De individuele rapporten betreffende ongewenste bijwerkingen met geregistreerde geneesmiddelen dienen naar het departement `Vigilantie' ter attentie van Mr. Thierry Roisin gezonden te worden Welke informatie dient naar het Leidend Ethisch Comite gezonden te worden? Volgens de wet van 7 mei 24 dienen alle individuele rapporten van bijwerkingen, vermeld onder titel II, aan het betrokken Leidend Ethisch Comite gezonden te worden. In praktijk worden enkel de individuele rapporten van en, die in Belgiè voorkomen, naar het betrokken Leidend Ethisch Comite gezonden. Alle niet-belgische individuele rapporten van ernstige, bijwerkingen, die normaal volgens de actuele wetgeving versneld (binnen 7/15 dagen) moeten genotifieerd worden, dienen opgenomen te worden in een zesmaandelijks rapport ("line listing"). Indien er vereist wordt in het kader van een internationale klinische proef (vb. IND- "Investigational New Drug proeven) om meer uitgebreid te rapporteren, kan dit uiteraard uitgevoerd worden. IV. Het elektronisch verzenden van individuele rapporten van bijwerkingen aan het DGG en het niet-electronisch verzenden ervan aan de Leidende Ethische Comites De rapporteringscriteria die hierboven voorgesteld werden, zijn enkel van toepassing op het niet-elektronisch rapporteren. Ter voorbereiding van de algemene verplichting tot elektronisch rapporteren van bijwerkingen die zal ingaan op 30 oktober 2005, kan het directoraat generaal Geneesmiddelen sinds januari 2005 ICH-E2B rapporten van en in XML ontvangen. Alvorens te kunnen starten met elektronische rapportering dient u, als opdrachtgever of als, vergunninghouder, een profiel aan te vragen om toegang te krijgen tot de EMEA 'Eudravigilance' gateway. Voor meer informatie, gelieve contact op te nemen met het EMEA. U kan ook terecht op de website van het EMEA (eudravigilance.ernea.euint). 1V.1. Elektronische rapportering van en Van zodra u elektronisch (in een ICH-E2B-formaat) rapporteert, zijn de volgende voorwaarden van kracht (Tabel 3) : 7
8 Tabel 3 : Het elektronisch verzenden van individuele rapporten van verwachte en en aan het directoraat-generaal Geneesmiddelen (DGG) en het niet-electronisch verzenden van individuele rapporten van en aan het Leidend Ethisch Comite (EC) Registratiestatus Pre Oorsprong/type van Rapporten BeIgiè/ Belgie/ verwachte Ander land in de EER/ Tijdslijn Rapporteur Rapportering? Klinische proef 7/15 dagen Opdrachtgever Ja, DGG*/EC - - Geen wetgeving 7/15 dagen Opdrachtgever Vrijstelling BeIgid/ Opdrachtgever of Vergunninghouder Pre Pre verwachte Ander land in de EER/ 7/15 dagen Vergunninghouder Ja, DGG/EC Ja, DGG Opdrachtgever Vrijstelling Belgiè/ Belgi&/ Spontaan rapport 7/15 dagen Opdrachtgever vrijstelling verwachte 15 dagen Vergunninghouder Be!gib*/ verwachte Klinische proef zonder interventie Ja, DGG/EC Ja, DGG Vrijstelling 7/15 dagen Opdrachtgever Vrijstelling Vergunninghouder Ja, DGG Ja, DGG/EC 15 dagen Opdrachtgever Vrijstelling * Individuele rapporten van en worden voor beide afdelingen, "R&D" en "Vigilantie", naar eenzelfde systeem gezonden. be 8,
9 Alle ernstige bijwerkingen, die optreden in Belgié, ongeacht of ze spontaan zijn of in klinische proeven optreden, dienen gerapporteerd te worden. Dit is geldig voor zowel geregistreerde als niet-geregistreerde geneesmiddelen. Verwachte bijwerkingen, die optreden in Belgie met geregistreerde geneesmiddelen, dienen gerapporteerd te worden. Voor de niet-geregistreerde geneesmiddelen heeft u deze verplichting niet. IV.2. Vrijsteling van de verplichting tot het verzenden van individuele rapporten van en, die niet voorgekomen zijn in BeIgib Indien U elektronisch (E2B) rapporteert aan het EMEA, kan U vrijgesteld worden van uw verplichting om de niet-belgische gevallen te rapporteren naar het DGG. U kan hiervoor een officièle schriftelijke vrijstelling van het DGG bekomen. Er worden 2 soorten vrijstellingen verleend : 1. een vrijstelling van onbepaalde duur, indien alle Belgische meldingen van bijwerkingen, elektronisch gerapporteerd worden aan het DGG en alle overige bijwerkingen elektronisch aan het Europees Geneesmiddelenbureau overmaakt. 2. een vrijstelling tot 30 oktober 2005 indien er elektronisch wordt gerapporteerd aan het Europees Geneesmiddelenbureau maar nog niet aan het DGG; in dit geval blijft de verplichting om de `Belgische' rapporten op papier of in PDF-formaat ( adres voor verzending : adversedrugreactions@health.fgov) over te maken aan het DGG. Voor beide vrijstellingen dient u contact op te nemen met het DGG. Het Europees Geneesmiddelenbureau maakt een onderscheid tussen rapporten van ongewenste bijwerkingen uit interventionele en klinische proeven zonder interventie voor wat de rapporteringsmodule betreft (EVCT-module voor rapporteren van uit klinische proeven of EVPM-module voor spontane meldingen). Een melding uit een klinische proef zonder interventie wordt beschouwd als een spontane melding en dient gerapporteerd te worden naar de desbetreffende EVPM-module. Voor meer uitleg kan u steeds terecht op de website van het Europees Geneesmiddelenbureau (eudravigilance.emea.eu.int). Het DGG voorziet slechts één enkele elektronische rapporteringsmodule, ongeacht de herkomst van de bijwerking (spontaan of klinische proef) en ongeacht de registratiestatus van het geneesmiddel. Deze omzendbrief beschrijft enkel het aspect "individuele rapporten van ongewenste bijwerkingen voor niet-geregistreerde en geregistreerde geneesmiddelen". De andere verplichtingen, die u opgelegd worden als gevolg van de actuele wetgeving o.a. notificatie van klinische proeven, de zesmaandelijkse line listings en de jaarlijkse veiligheidsrapporten omtrent klinische proeven, zullen in een latere fase meegedeeld worden. Aangezien u, als vergunninghouder of als opdrachtgever van een klinische proef, de verplichting hebt om vanaf 30 oktober 2005 elektronisch te rapporteren, kunnen wij u enkel aanmoedigen om de nodige voorbereidingen te treffen. Indien u vragen heeft omtrent deze omzendbrief of andere aspecten van het elektronisch rapporteren, kan u steeds contact opnemen met Mevr. M. Gabriêls (tel ; marqriet. qabriels@health. Wm. be). 9
10 Voor technische vragen betreffende elektronisch rapporteren kan u contact opnemen met Mr. K. Ngbabo Wa Mbuna (tel ; wambuna.kotophealth.fgov.tde). Voor meer algemene informatie betreffende klinische proeven en rapportering van bijwerkingen van niet-geregistreerde geneesmiddelen kan u steeds contact opnemen met Mevr. G. Musch (tel ; weetmusch@healthigov) (afdeling R&D). Voor algemene vragen betreffende farmacovigilantie en rapportering van bijwerkingen met geregistreerde geneesmiddelen mag u steeds contact opnemen met Mr. T. Roisin (tel ; thierry.roisin@health.fgov) (afdeling Vigilantie), of met Mevr. M. Gabriêls (tel ; margriet.gabriels(.?health.fgov) (afdeling Vigilantie). Met de meeste hoogachting, De Directeur-generaal, Afdelingshoofd Afdelingshoofd `R&D'(Onderzoek&Ontwikkeling), T. Roisin Referenties : Wet van 7 mei 2004 inzake experimenten op de menselijke persoon Koninklijk Besluit van 3/07/1969 betreffende de registratie van geneesmiddelen Koninklijk Besluit van 30 juni 2004 tot bepaling van uitvoeringsmaatregelen van de wet van 7 mei 2004 inzake experimenten op de menselijke persoon voor wat betreft klinische proeven met geneesmiddelen voor menselijk gebruik Verordening Nr. 2309/93 van de Raad van 22 full 1993 tot vaststelling van communautaire procedures voor het verlenen van vergunningen voor en het toezicht op geneesmiddelen voor menselijk en diergeneeskundig gebruik en tot oprichting van een Europees Bureau voor de geneesmiddelenbeoordeling Verordening Nr. 726/2004 van het Europees parlement en de Raad van 31 maxi tot vaststelling van communautaire procedures voor het verlenen van vergunningen en het toezicht op geneesmiddelen voor menselijk en diergeneeskundig gebruik en tot oprichting van een Europees Geneesmiddelenbureau (voor de EER relevante tekst) Omzendbrief nr. 455 dd. 28/11/2004 omtrent "Verdere toelichting bij de wet van 7 mei 2004 inzake experimenten op de menselijke persoon 'Detailed guidance on the collection, verification and presentation of adverse reaction reports arising from clinical trials on medicinal products for human use" "Detailed guidance on the European database of Suspected Unexpected Serious Adverse Reactions (EudraVigilance Clinical Trial Module)" Rules Governing Medicinal products in the European Union, published by the European Commission, Directorate Enterprise, Regulatory Framework and Market Authorisations : Volume 9 Pharmacovigilance ICH-E2D -Approval Safety Data Management: Definitions and Standards for Expedited Reporting 10
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek
 Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
Gids voor het interpreteren van spontane meldingen van vermoedelijke bijwerkingen van geneesmiddelen
 30 januari 2017 Inspecties, bewaking voor menselijk gebruik en comités EMA/749446/2016 Herziening 1* Gids voor het interpreteren van spontane meldingen van vermoedelijke bijwerkingen Overeenstemming door
30 januari 2017 Inspecties, bewaking voor menselijk gebruik en comités EMA/749446/2016 Herziening 1* Gids voor het interpreteren van spontane meldingen van vermoedelijke bijwerkingen Overeenstemming door
Handleiding. Investigational Medicinal Product Dossier (IMPD)
 Handleiding Investigational Medicinal Product Dossier (IMPD) Inhoudsopgave Afkortingen... - 3 - Wat is het IMPD?... - 4 - Beslisschema inhoud IMPD... - 5 - Beschrijving inhoud IMPD... - 6 - Overzicht hoofdstukken
Handleiding Investigational Medicinal Product Dossier (IMPD) Inhoudsopgave Afkortingen... - 3 - Wat is het IMPD?... - 4 - Beslisschema inhoud IMPD... - 5 - Beschrijving inhoud IMPD... - 6 - Overzicht hoofdstukken
FOD VOLKSGEZONDHEID, Brussel, 11/06/2009 VEILIGHEID VAN DE VOEDSELKETEN EN LEEFMILIEU
 FOD VOLKSGEZONDHEID, Brussel, 11/06/2009 VEILIGHEID VAN DE VOEDSELKETEN EN LEEFMILIEU DIRECTORAAT-GENERAAL ORGANISATIE VAN DE GEZONDHEIDSZORGVOORZIENINGEN NATIONALE RAAD VOOR ZIEKENHUISVOORZIENINGEN --------
FOD VOLKSGEZONDHEID, Brussel, 11/06/2009 VEILIGHEID VAN DE VOEDSELKETEN EN LEEFMILIEU DIRECTORAAT-GENERAAL ORGANISATIE VAN DE GEZONDHEIDSZORGVOORZIENINGEN NATIONALE RAAD VOOR ZIEKENHUISVOORZIENINGEN --------
De rol van de verpleegkundige binnen Medischwetenschappelijk
 De rol van de verpleegkundige binnen Medischwetenschappelijk onderzoek Moderator Mevr. R.C.A. Veldhoen-Tijben 1st author / speaker Miriam Gelderloos Co-author Erna Helmantel Belangenverklaring In overeenstemming
De rol van de verpleegkundige binnen Medischwetenschappelijk onderzoek Moderator Mevr. R.C.A. Veldhoen-Tijben 1st author / speaker Miriam Gelderloos Co-author Erna Helmantel Belangenverklaring In overeenstemming
Hoe garanderen België en Europa veilige vaccins? Pieter Neels, FAGG
 Hoe garanderen België en Europa veilige vaccins? Pieter Neels, FAGG Disclaimer Niettegenstaande mijn betrokkenheid bij het Comité voor geneesmiddelen voor menselijk gebruik (CHMP), kan deze presentatie
Hoe garanderen België en Europa veilige vaccins? Pieter Neels, FAGG Disclaimer Niettegenstaande mijn betrokkenheid bij het Comité voor geneesmiddelen voor menselijk gebruik (CHMP), kan deze presentatie
Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek
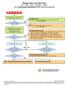 Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek Melding voorval proefpersoon aan onderzoeker/arts 1 Rapportage voorval door onderzoeker/arts in patiëntenstatus
Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek Melding voorval proefpersoon aan onderzoeker/arts 1 Rapportage voorval door onderzoeker/arts in patiëntenstatus
Vigilantie bij Omniplasma. Jo Wiersum-Osselton namens TRIP
 Vigilantie bij Omniplasma Jo Wiersum-Osselton namens TRIP TRIP Board (Medical Societies) Advisory board (Hospital associations, Sanquin BB) Hospitals blood Tf comm. Hospital laboratory clinicians national
Vigilantie bij Omniplasma Jo Wiersum-Osselton namens TRIP TRIP Board (Medical Societies) Advisory board (Hospital associations, Sanquin BB) Hospitals blood Tf comm. Hospital laboratory clinicians national
VRAGENLIJST BETREFFENDE EEN EXPERIMENT
 Commissie voor Ethiek Voorzitter L. Vanopdenbosch Leden D. Borrey G. Bru E. De Cuypere B. Deblauwe B. Dupon K. Hemeryck N. Sys A. Turf P. Van Lancker P. Van Trappen S. Vandecasteele W. Verhaeghe A. Verhaert
Commissie voor Ethiek Voorzitter L. Vanopdenbosch Leden D. Borrey G. Bru E. De Cuypere B. Deblauwe B. Dupon K. Hemeryck N. Sys A. Turf P. Van Lancker P. Van Trappen S. Vandecasteele W. Verhaeghe A. Verhaert
INCLUSIE SET PLAATS HIER DE PATIENTSTICKER VAN DE GEINCLUDEERDE PATIENT. ULTRA STUDIE INCLUSIE SET VERSIE 9 Pagina 1 van 9
 INCLUSIE SET Als de patiënt geïncludeerd kan worden in de studie, voert de arts in het behandelcentrum de randomisatieprocedure uit na telefonische aanmelding van de patiënt(e) PLAATS HIER DE PATIENTSTICKER
INCLUSIE SET Als de patiënt geïncludeerd kan worden in de studie, voert de arts in het behandelcentrum de randomisatieprocedure uit na telefonische aanmelding van de patiënt(e) PLAATS HIER DE PATIENTSTICKER
Inhoudstafel per onderwerp volume 2 experimenten op de mens en menselijk lichaamsmateriaal
 Inhoudstafel per onderwerp volume 2 experimenten op de mens en menselijk lichaamsmateriaal Pharma Codex Deel I vol. 2 vii Voor de bijlagen bij de omzendbrieven en de nota s, raadpleeg de website van het
Inhoudstafel per onderwerp volume 2 experimenten op de mens en menselijk lichaamsmateriaal Pharma Codex Deel I vol. 2 vii Voor de bijlagen bij de omzendbrieven en de nota s, raadpleeg de website van het
Basistekst. Niet-interventionele studies. Opzet van deze voordracht
 Niet-interventionele studies prof. dr. P. Cras Ethisch Comité UZA Opzet van deze voordracht FAQs bloemlezing uit de wetteksten aangeven waar er ruimte voor interpretatie is nadruk op nuttige termen en
Niet-interventionele studies prof. dr. P. Cras Ethisch Comité UZA Opzet van deze voordracht FAQs bloemlezing uit de wetteksten aangeven waar er ruimte voor interpretatie is nadruk op nuttige termen en
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U8 Melding van (Serious) Adverse Events en SUSARs Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies
Standard Operating Procedure STZ SOP: U8 Melding van (Serious) Adverse Events en SUSARs Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies
ETHISCH COMITÉ PZ HF KORTRIJK - PC MENEN
 ETHISCH COMITÉ PZ HF KORTRIJK - PC MENEN Aanvraagformulier Ethisch advies voor experimenten op de menselijke persoon Richtlijnen Ethische comités hebben een beperkte tijd om dossiers te evalueren en hun
ETHISCH COMITÉ PZ HF KORTRIJK - PC MENEN Aanvraagformulier Ethisch advies voor experimenten op de menselijke persoon Richtlijnen Ethische comités hebben een beperkte tijd om dossiers te evalueren en hun
Het melden van bijwerkingen van geneesmiddelen: vaak gestelde vragen
 Afdeling Vigilantie Het melden van bijwerkingen van geneesmiddelen: vaak gestelde vragen Wat is een bijwerking van een geneesmiddel? Een bijwerking van een geneesmiddel is een schadelijke en ongewilde
Afdeling Vigilantie Het melden van bijwerkingen van geneesmiddelen: vaak gestelde vragen Wat is een bijwerking van een geneesmiddel? Een bijwerking van een geneesmiddel is een schadelijke en ongewilde
UITVOERINGSBESLUIT VAN DE COMMISSIE. van (Voor de EER relevante tekst) (SLECHTS DE TEKST IN DE DEENSE TAAL IS AUTHENTIEK)
 EUROPESE COMMISSIE Brussel, 29.6.2011 C(2011)4837 def. UITVOERINGSBESLUIT VAN DE COMMISSIE van 29.6.2011 tot wijziging, met het oog op uitbreiding, van de vergunning voor het in de handel brengen van het
EUROPESE COMMISSIE Brussel, 29.6.2011 C(2011)4837 def. UITVOERINGSBESLUIT VAN DE COMMISSIE van 29.6.2011 tot wijziging, met het oog op uitbreiding, van de vergunning voor het in de handel brengen van het
Codex Pharma Commenté / Becommentarieerde Codex Pharma Artikel 6, 1
 Lid 1 Een geneesmiddel mag slechts in de handel worden gebracht, nadat een vergunning voor het in de handel brengen, hierna VHB genoemd, is verleend hetzij door de minister of zijn afgevaardigde overeenkomstig
Lid 1 Een geneesmiddel mag slechts in de handel worden gebracht, nadat een vergunning voor het in de handel brengen, hierna VHB genoemd, is verleend hetzij door de minister of zijn afgevaardigde overeenkomstig
Werkinstructies adverse events rapportage STOP-BPD studie
 Werkinstructies adverse events rapportage STOP-BPD studie De STOP-BPD studie wordt uitgevoerd bij extreem prematuur geboren kinderen die los van deelname aan de studie een continu verhoogd risico hebben
Werkinstructies adverse events rapportage STOP-BPD studie De STOP-BPD studie wordt uitgevoerd bij extreem prematuur geboren kinderen die los van deelname aan de studie een continu verhoogd risico hebben
Directoraat-generaal Geneesmiddelen. Omzendbrief n 440. Betreft: Levering en aflevering van geneesmiddelen voor diergeneeskundig gebruik
 Amazone Bischoffsheimlaan 33 B-1000 BRUSSEL Uw brief van: Uw kenmerk: Ons kenmerk: Datum: DGG/ 10 februari 2004 Omzendbrief n 440 Ter attentie van de apothekers die een voor het publiek toegankelijke officina
Amazone Bischoffsheimlaan 33 B-1000 BRUSSEL Uw brief van: Uw kenmerk: Ons kenmerk: Datum: DGG/ 10 februari 2004 Omzendbrief n 440 Ter attentie van de apothekers die een voor het publiek toegankelijke officina
Tweede Kamer der Staten-Generaal
 Tweede Kamer der Staten-Generaal 2 Vergaderjaar 2012 2013 33 646 Wijziging van de Wet medisch-wetenschappelijk onderzoek met mensen in verband met een uitbreiding van de meldingsplicht van ernstige ongewenste
Tweede Kamer der Staten-Generaal 2 Vergaderjaar 2012 2013 33 646 Wijziging van de Wet medisch-wetenschappelijk onderzoek met mensen in verband met een uitbreiding van de meldingsplicht van ernstige ongewenste
Verzoek tot advies van de Commissie Medische Ethiek betreffende een klinische studie
 Titel van het onderzoek: EudraCT nummer, indien van toepassing: Arts-onderzoeker HHZH Lier + medische discipline: PI (Naam, adres, tel en e-mail): Sponsor (Naam, contactpersoon, adres, tel en e-mail):
Titel van het onderzoek: EudraCT nummer, indien van toepassing: Arts-onderzoeker HHZH Lier + medische discipline: PI (Naam, adres, tel en e-mail): Sponsor (Naam, contactpersoon, adres, tel en e-mail):
FOD VOLKSGEZONDHEID, VEILIGHEID VAN DE VOEDSELKETEN EN LEEFMILIEU. Federale wetgeving over hemovigilantie
 1 Federale wetgeving over hemovigilantie 2 Wettelijk kader Achtereenvolgens komen aan bod : a) - de Europese wetgeving; b) - het onderscheid ziekenhuisbloedbank - bloedinstelling; c) - de Belgische wetgeving.
1 Federale wetgeving over hemovigilantie 2 Wettelijk kader Achtereenvolgens komen aan bod : a) - de Europese wetgeving; b) - het onderscheid ziekenhuisbloedbank - bloedinstelling; c) - de Belgische wetgeving.
Impact op de Belgische gezondheidszorg
 EUROPESE UNIE EN GEZONDHEIDSZORG OSE-IZRI studiedag EU geneesmiddelenbeleid: toegankelijkheid of concurrentiepositie versterken? Impact op de Belgische gezondheidszorg Minne Casteels Katholieke Universiteit
EUROPESE UNIE EN GEZONDHEIDSZORG OSE-IZRI studiedag EU geneesmiddelenbeleid: toegankelijkheid of concurrentiepositie versterken? Impact op de Belgische gezondheidszorg Minne Casteels Katholieke Universiteit
Sildenafil mag niet gebruikt worden voor de behandeling van intrauteriene
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Publicatieblad van de Europese Unie
 25.3.2017 L 80/7 UITVOERINGSVERORDENING (EU) 2017/556 VAN DE COMMISSIE van 24 maart 2017 houdende de nadere regeling voor de inspectieprocedures inzake goede klinische praktijken overeenkomstig Verordening
25.3.2017 L 80/7 UITVOERINGSVERORDENING (EU) 2017/556 VAN DE COMMISSIE van 24 maart 2017 houdende de nadere regeling voor de inspectieprocedures inzake goede klinische praktijken overeenkomstig Verordening
Rol van European Organisa4on for Research and Treatment of Cancer (EORTC)
 Overzicht Verschillende partners Klinische studies binnen de farmaceu4sche industrie Protocol bij klinische studies Goedkeuring klinische studies Regels bij klinische studies Rol van European Medicines
Overzicht Verschillende partners Klinische studies binnen de farmaceu4sche industrie Protocol bij klinische studies Goedkeuring klinische studies Regels bij klinische studies Rol van European Medicines
Capecitabine Accord moet permanent worden stopgezet bij patiënten die een ernstige huidreactie hebben gehad tijdens de behandeling.
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Onderzoek en Ontwikkeling
 Onderzoek en Ontwikkeling Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten UW BRIEF VAN UW REF. ONZE REF. DATUM FAGG/O&O/KVK OMZENDBRIEF nr. 566 Aan de voorzitters van de ethische comités
Onderzoek en Ontwikkeling Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten UW BRIEF VAN UW REF. ONZE REF. DATUM FAGG/O&O/KVK OMZENDBRIEF nr. 566 Aan de voorzitters van de ethische comités
Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814.
 STAATSCOURANT Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814. Nr. 20221 17 juli 2015 Regeling van de Minister van Volksgezondheid, Welzijn en Sport van 9 juli 2015, houdende regels voor
STAATSCOURANT Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814. Nr. 20221 17 juli 2015 Regeling van de Minister van Volksgezondheid, Welzijn en Sport van 9 juli 2015, houdende regels voor
REGISTRATIEFORMULIER KLINISCHE STUDIES UZ /KULEUVEN BIJ HET CLINICAL TRIAL CENTER (CTC)
 Elke klinische studie die wordt opgestart in UZ/, wordt eenmalig geregistreerd via loketfunctie CTC. Na registratie ontvangt de hoofdonderzoeker een S nummer (via e mail aangeduide e mailadressen). De
Elke klinische studie die wordt opgestart in UZ/, wordt eenmalig geregistreerd via loketfunctie CTC. Na registratie ontvangt de hoofdonderzoeker een S nummer (via e mail aangeduide e mailadressen). De
Farmacovigilantie. Veilige en doeltreffende geneesmiddelen met de inzet van alle gezondheidspartners. Wat is farmacovigilantie? december 07 nr 145
 Newsletter van pharma.be vzw Verschijnt niet in juli en augustus Afgiftekantoor Brussel X december 07 nr 145 Veilige en doeltreffende geneesmiddelen met de inzet van alle gezondheidspartners Wat is farmacovigilantie?
Newsletter van pharma.be vzw Verschijnt niet in juli en augustus Afgiftekantoor Brussel X december 07 nr 145 Veilige en doeltreffende geneesmiddelen met de inzet van alle gezondheidspartners Wat is farmacovigilantie?
Het melden van bijwerkingen van geneesmiddelen: vaak gestelde vragen
 Afdeling Vigilantie Het melden van bijwerkingen van geneesmiddelen: vaak gestelde vragen Wat is een bijwerking van een geneesmiddel? Een bijwerking van een geneesmiddel is een schadelijke en ongewilde
Afdeling Vigilantie Het melden van bijwerkingen van geneesmiddelen: vaak gestelde vragen Wat is een bijwerking van een geneesmiddel? Een bijwerking van een geneesmiddel is een schadelijke en ongewilde
Actieplan 2009 / 2010 Vraag- en antwoorddocument
 Actieplan 2009 / 2010 Vraag- en antwoorddocument 28/01/2009 Page 1 sur 7 Inactivatie 1. Welk e-mailadres gebruikt het FAGG om ontbrekende documenten op te vragen die noodzakelijk zijn voor de administratieve
Actieplan 2009 / 2010 Vraag- en antwoorddocument 28/01/2009 Page 1 sur 7 Inactivatie 1. Welk e-mailadres gebruikt het FAGG om ontbrekende documenten op te vragen die noodzakelijk zijn voor de administratieve
Aanvraagformulier Ethisch advies voor experimenten op de menselijke persoon
 groep emmaüs christelijke vereniging voor gezondheids- en welzijnszorg ETHISCH COMITÉ Edgard Tinellaan 1c 2800 MECHELEN Tel. : 015 44 67 21 Fax : 015 44 67 10 Erkenningsnummer: 0G 066 Aanvraagformulier
groep emmaüs christelijke vereniging voor gezondheids- en welzijnszorg ETHISCH COMITÉ Edgard Tinellaan 1c 2800 MECHELEN Tel. : 015 44 67 21 Fax : 015 44 67 10 Erkenningsnummer: 0G 066 Aanvraagformulier
Titel: Good Clinical Practice & Monitoring. Initiation Investigator Driven Studies. Versie: 14-jan-2013
 Titel: Good Clinical Practice & Monitoring Initiation Investigator Driven Studies Inhoud Wet- en regelgeving/declaration of Helsinki Good Clinical Practice Patiënteninformatie/ informed consent Basisvereisten
Titel: Good Clinical Practice & Monitoring Initiation Investigator Driven Studies Inhoud Wet- en regelgeving/declaration of Helsinki Good Clinical Practice Patiënteninformatie/ informed consent Basisvereisten
Procedure voor de verwerking van een aanvraag tot onderzoek
 Procedure voor de verwerking van een aanvraag tot onderzoek A Doel De doelstelling van deze procedure is het waarborgen van een standaardverloop bij aanvragen tot het uitvoeren van wetenschappelijk onderzoek
Procedure voor de verwerking van een aanvraag tot onderzoek A Doel De doelstelling van deze procedure is het waarborgen van een standaardverloop bij aanvragen tot het uitvoeren van wetenschappelijk onderzoek
Inleiding farmacovigilantie geneesmiddelen voor diergeneeskundig gebruik
 Inleiding farmacovigilantie geneesmiddelen voor diergeneeskundig gebruik 5de Vigilantiedag BRUSSEL Els Dewaele Inhoud Inleiding Bijwerkingen in EU en BE Verdeling van bijwerkingen Melden promoten? Toekomst
Inleiding farmacovigilantie geneesmiddelen voor diergeneeskundig gebruik 5de Vigilantiedag BRUSSEL Els Dewaele Inhoud Inleiding Bijwerkingen in EU en BE Verdeling van bijwerkingen Melden promoten? Toekomst
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik
 EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
Adviesaanvraag betreffende een protocol van een klinische proef of experiment
 Ethische Commissie UVC Brugmann Adviesaanvraag betreffende een protocol van een klinische proef of experiment Aanvraag te richten aan Dr J. VALSAMIS Ethische Commissie UVC Brugmann c/o Medische Directie
Ethische Commissie UVC Brugmann Adviesaanvraag betreffende een protocol van een klinische proef of experiment Aanvraag te richten aan Dr J. VALSAMIS Ethische Commissie UVC Brugmann c/o Medische Directie
PROCEDURE BETREFFENDE DE VERZENDING VAN BRIEVEN TER ATTENTIE VAN DE GEZONDHEIDSZORGBEOEFENAARS (DHPC's)
 PROCEDURE BETREFFENDE DE VERZENDING VAN BRIEVEN TER ATTENTIE VAN DE GEZONDHEIDSZORGBEOEFENAARS (DHPC's) 8/10/2015 (v2) Deze procedure werd opgesteld op initiatief van de vertegenwoordigers van de industrie
PROCEDURE BETREFFENDE DE VERZENDING VAN BRIEVEN TER ATTENTIE VAN DE GEZONDHEIDSZORGBEOEFENAARS (DHPC's) 8/10/2015 (v2) Deze procedure werd opgesteld op initiatief van de vertegenwoordigers van de industrie
Klinische studies: wetgeving in de EU en België en de implicaties ervan op de praktijk
 Klinische studies: wetgeving in de EU en België en de implicaties ervan op de praktijk Katelijne De Nys Inleiding - Richtlijnen en wetgeving in historisch perspectief De Europese Directive De Belgische
Klinische studies: wetgeving in de EU en België en de implicaties ervan op de praktijk Katelijne De Nys Inleiding - Richtlijnen en wetgeving in historisch perspectief De Europese Directive De Belgische
Safety First: Vangnet of Maatwerk?
 Gedreven Meesterschap Safety First: Vangnet of Maatwerk? Het belang van Farmacovigilantie in Clinical Research 21 April 2016 Marielle Keulen Sandra van der Poel Tel: 071 524 4000 www.xendo.com Safety First:
Gedreven Meesterschap Safety First: Vangnet of Maatwerk? Het belang van Farmacovigilantie in Clinical Research 21 April 2016 Marielle Keulen Sandra van der Poel Tel: 071 524 4000 www.xendo.com Safety First:
Online melden van bijwerkingen via de website www.gelefiche.be
 Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten Uw geneesmiddelen en gezondheidsproducten, onze zorg Online melden van bijwerkingen via de website www.gelefiche.be Het Federaal Agentschap
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten Uw geneesmiddelen en gezondheidsproducten, onze zorg Online melden van bijwerkingen via de website www.gelefiche.be Het Federaal Agentschap
Rechtstreekse mededeling aan de Gezondheidszorgbeoefenaars
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
President BeCRO organisatie van bedrijven die aktief zijn in het organiseren van klinische studies. Wat is? Medicament geneesmiddel device therapie?
 Melanoomstudiedag Els Vanpee President BeCRO organisatie van bedrijven die aktief zijn in het organiseren van klinische studies Hoofd klinische studies bij PAREXEL België Wat is? Medicament geneesmiddel
Melanoomstudiedag Els Vanpee President BeCRO organisatie van bedrijven die aktief zijn in het organiseren van klinische studies Hoofd klinische studies bij PAREXEL België Wat is? Medicament geneesmiddel
EUROPEES PARLEMENT Commissie landbouw en plattelandsontwikkeling. van de Commissie landbouw en plattelandsontwikkeling
 EUROPEES PARLEMENT 2014-2019 Commissie landbouw en plattelandsontwikkeling 27.3.2015 2014/0256(COD) ONTWERPADVIES van de Commissie landbouw en plattelandsontwikkeling aan de Commissie milieubeheer, volksgezondheid
EUROPEES PARLEMENT 2014-2019 Commissie landbouw en plattelandsontwikkeling 27.3.2015 2014/0256(COD) ONTWERPADVIES van de Commissie landbouw en plattelandsontwikkeling aan de Commissie milieubeheer, volksgezondheid
RICHTLIJN 2001/20/EG VAN HET EUROPEES PARLEMENT EN DE RAAD
 2001L0020 NL 07.08.2009 002.001 1 Dit document vormt slechts een documentatiehulpmiddel en verschijnt buiten de verantwoordelijkheid van de instellingen B RICHTLIJN 2001/20/EG VAN HET EUROPEES PARLEMENT
2001L0020 NL 07.08.2009 002.001 1 Dit document vormt slechts een documentatiehulpmiddel en verschijnt buiten de verantwoordelijkheid van de instellingen B RICHTLIJN 2001/20/EG VAN HET EUROPEES PARLEMENT
Zeldzame ziekten, weesgeneesmiddelen
 niet geautoriseerde Nederlandse vertaling Zeldzame ziekten, weesgeneesmiddelen De feiten op een rijtje De EMA wil graag dat Europese burgers met zeldzame ziekten toegang hebben tot specifieke en werkzame
niet geautoriseerde Nederlandse vertaling Zeldzame ziekten, weesgeneesmiddelen De feiten op een rijtje De EMA wil graag dat Europese burgers met zeldzame ziekten toegang hebben tot specifieke en werkzame
9.4.2005 Publicatieblad van de Europese Unie L 91/13
 9.4.2005 Publicatieblad van de Europese Unie L 91/13 RICHTLIJN 2005/28/EG VAN DE COMMISSIE van 8 april 2005 tot vaststelling van beginselen en gedetailleerde richtsnoeren inzake goede klinische praktijken
9.4.2005 Publicatieblad van de Europese Unie L 91/13 RICHTLIJN 2005/28/EG VAN DE COMMISSIE van 8 april 2005 tot vaststelling van beginselen en gedetailleerde richtsnoeren inzake goede klinische praktijken
KB 21 januari 2009: Onderrichtingen der apothekers Checklist Internet
 KB 21 januari 2009: Onderrichtingen der apothekers Checklist Internet In 2006 maakte de Belgische wetgever bij de hervorming van de Geneesmiddelenwet een opening voor verkoop op afstand, volgens het vrij
KB 21 januari 2009: Onderrichtingen der apothekers Checklist Internet In 2006 maakte de Belgische wetgever bij de hervorming van de Geneesmiddelenwet een opening voor verkoop op afstand, volgens het vrij
KB 21 januari 2009: onderrichtingen der apothekers Checklist Internet
 KB 21 januari 2009: onderrichtingen der apothekers Checklist Internet In 2006 maakte de Belgische wetgever bij de hervorming van de Geneesmiddelenwet een opening voor verkoop op afstand, volgens het vrij
KB 21 januari 2009: onderrichtingen der apothekers Checklist Internet In 2006 maakte de Belgische wetgever bij de hervorming van de Geneesmiddelenwet een opening voor verkoop op afstand, volgens het vrij
Omzendbrief betreffende het bezit van gewasbeschermingsmiddelen en toevoegingsstoffen waarvan de verkoop of het gebruik verboden is
 Federaal Agentschap voor de Veiligheid van de Voedselketen Omzendbrief betreffende het bezit van gewasbeschermingsmiddelen en toevoegingsstoffen waarvan de verkoop of het gebruik verboden is Huidige versie
Federaal Agentschap voor de Veiligheid van de Voedselketen Omzendbrief betreffende het bezit van gewasbeschermingsmiddelen en toevoegingsstoffen waarvan de verkoop of het gebruik verboden is Huidige versie
Studie namiddag Evidence Based Zorg
 Studie namiddag Evidence Based Zorg Ann Van den Bruel, MD PhD Clinical Lecturer, University of Oxford Huisarts Programma Ethische commissie Serious Gaming Recrutering Care4Safety Uitkomsten 1Heart2Care4
Studie namiddag Evidence Based Zorg Ann Van den Bruel, MD PhD Clinical Lecturer, University of Oxford Huisarts Programma Ethische commissie Serious Gaming Recrutering Care4Safety Uitkomsten 1Heart2Care4
Wat is een klinische studie?
 Wat is een klinische studie? Klinische studies Klinische studies Klinische studies worden verricht om de werkzaamheid van geneesmiddelen alsook combinaties van verschillende behandelingen te testen. Klinische
Wat is een klinische studie? Klinische studies Klinische studies Klinische studies worden verricht om de werkzaamheid van geneesmiddelen alsook combinaties van verschillende behandelingen te testen. Klinische
BIJLAGE. Wetenschappelijke aspecten
 BIJLAGE Wetenschappelijke aspecten 3 BIJLAGE Wetenschappelijke aspecten A) INLEIDING Sparfloxacine is een antibioticum van de chinolonengroep dat is geïndiceerd voor de behandeling van: - in gemeenschapsverband
BIJLAGE Wetenschappelijke aspecten 3 BIJLAGE Wetenschappelijke aspecten A) INLEIDING Sparfloxacine is een antibioticum van de chinolonengroep dat is geïndiceerd voor de behandeling van: - in gemeenschapsverband
Rechtstreekse mededeling aan de Gezondheidszorgbeoefenaars
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
61e jaargang 9 augustus 2018
 Publicatieblad van de Europese Unie L 202 Uitgave in de Nederlandse taal Wetgeving 61e jaargang 9 augustus 2018 Inhoud II Niet-wetgevingshandelingen VERORDENINGEN Uitvoeringsverordening (EU) 2018/1105
Publicatieblad van de Europese Unie L 202 Uitgave in de Nederlandse taal Wetgeving 61e jaargang 9 augustus 2018 Inhoud II Niet-wetgevingshandelingen VERORDENINGEN Uitvoeringsverordening (EU) 2018/1105
Geachte Mevrouw, Heer,
 Directoraat-generaal Organisatie Gezondheidszorvoorzieningen Dienst Datamanagement UW BRIEF VAN UW REF. ONZE REF. STA/CH/2007-181 DATUM 10 AUGUSTUS 2007 BIJLAGE(N) Ter attentie van de algemeen directeur
Directoraat-generaal Organisatie Gezondheidszorvoorzieningen Dienst Datamanagement UW BRIEF VAN UW REF. ONZE REF. STA/CH/2007-181 DATUM 10 AUGUSTUS 2007 BIJLAGE(N) Ter attentie van de algemeen directeur
Veel gestelde vragen Medisch-wetenschappelijk onderzoek met medische hulpmiddelen 1
 Veel gestelde vragen Medisch-wetenschappelijk onderzoek met medische hulpmiddelen 1 1. Wat is een medisch hulpmiddel? De wettelijke definitie 2 van een medisch hulpmiddel luidt: Een medisch hulpmiddel
Veel gestelde vragen Medisch-wetenschappelijk onderzoek met medische hulpmiddelen 1 1. Wat is een medisch hulpmiddel? De wettelijke definitie 2 van een medisch hulpmiddel luidt: Een medisch hulpmiddel
Dit document geeft antwoorden op veelgestelde vragen die bij het Europees Geneesmiddelenbureau (EMA) binnenkomen.
 13 februari 2017 EMA/527628/2011 rev. 1 Afdeling: Dit document geeft antwoorden op veelgestelde vragen die bij het Europees Geneesmiddelenbureau (EMA) binnenkomen. Indien u het antwoord op uw vraag hier
13 februari 2017 EMA/527628/2011 rev. 1 Afdeling: Dit document geeft antwoorden op veelgestelde vragen die bij het Europees Geneesmiddelenbureau (EMA) binnenkomen. Indien u het antwoord op uw vraag hier
Meewerken aan medische vooruitgang. Klinische proeven
 Meewerken aan medische vooruitgang Klinische proeven De medische wereld heeft de voorbije vijftig jaar een enorme vooruitgang gekend. En met de technologische ontwikkelingen van vandaag zal de medische
Meewerken aan medische vooruitgang Klinische proeven De medische wereld heeft de voorbije vijftig jaar een enorme vooruitgang gekend. En met de technologische ontwikkelingen van vandaag zal de medische
Inhoud van de Investigator s Brochure (IB)
 Inhoud van de Investigator s Brochure (IB) Bron: Richtsnoer voor good clinical practice (CPMP/ICH/135/95) 1. Algemene overwegingen De IB moet bevatten: 1.2 Titelpagina Deze moet de naam van de sponsor,
Inhoud van de Investigator s Brochure (IB) Bron: Richtsnoer voor good clinical practice (CPMP/ICH/135/95) 1. Algemene overwegingen De IB moet bevatten: 1.2 Titelpagina Deze moet de naam van de sponsor,
Vroege fase ontwikkeling en klinische proeven: evolutie over de voorbije jaren en een blik op de toekomst
 Vroege fase ontwikkeling en klinische proeven: evolutie over de voorbije jaren en een blik op de toekomst FAGG BRUSSEL 25.09.2018 Walter Janssens DG PRE vergunning Inleiding Klinische proeven worden traditioneel
Vroege fase ontwikkeling en klinische proeven: evolutie over de voorbije jaren en een blik op de toekomst FAGG BRUSSEL 25.09.2018 Walter Janssens DG PRE vergunning Inleiding Klinische proeven worden traditioneel
WERKNEMER. Verklaring van belangen. Algemeen. Melding van belangen op farmaceutisch gebied. Tussenvoegsels
 Verklaring van belangen Algemeen Titel(s) Voornaam Prof. dr. Bert Tussenvoegsels Achternaam Afdeling (Voor externe experts, wilt u aangeven voor welke afdeling van het CBG u werkt) Functienaam Omschrijving
Verklaring van belangen Algemeen Titel(s) Voornaam Prof. dr. Bert Tussenvoegsels Achternaam Afdeling (Voor externe experts, wilt u aangeven voor welke afdeling van het CBG u werkt) Functienaam Omschrijving
EUROPESE UNIE HET EUROPEES PARLEMENT
 EUROPESE UNIE HET EUROPEES PARLEMENT DE RAAD Luxemburg, 4 april 2001 (OR. fr) 97/0197 (COD) LEX 257 PE-CONS 3605/1/01 REV 1 ECO 8 SAN 3 CODEC 39 RICHTLIJN 2001/20/EG VAN HET EUROPEES PARLEMENT EN DE RAAD
EUROPESE UNIE HET EUROPEES PARLEMENT DE RAAD Luxemburg, 4 april 2001 (OR. fr) 97/0197 (COD) LEX 257 PE-CONS 3605/1/01 REV 1 ECO 8 SAN 3 CODEC 39 RICHTLIJN 2001/20/EG VAN HET EUROPEES PARLEMENT EN DE RAAD
Wetenschappelijk onderzoek en ontwikkeling (O&O) en onderzoek en ontwikkeling gericht op producten en procedés (PPORD)
 BEKNOPT RICHTSNOER Wetenschappelijk onderzoek en ontwikkeling (O&O) en onderzoek en ontwikkeling gericht op producten en procedés (PPORD) In dit document wordt in eenvoudige bewoordingen toegelicht welke
BEKNOPT RICHTSNOER Wetenschappelijk onderzoek en ontwikkeling (O&O) en onderzoek en ontwikkeling gericht op producten en procedés (PPORD) In dit document wordt in eenvoudige bewoordingen toegelicht welke
Richtlijnen voor onderzoek. met vrijwilligers in het AMC. met geneesmiddelen, hulpmiddelen of ingrepen die niet eerder bij de mens zijn toegepast
 Richtlijnen voor onderzoek met vrijwilligers in het AMC en met geneesmiddelen, hulpmiddelen of ingrepen die niet eerder bij de mens zijn toegepast bij patiënten in het AMC augustus 2008 Inhoud Inleiding
Richtlijnen voor onderzoek met vrijwilligers in het AMC en met geneesmiddelen, hulpmiddelen of ingrepen die niet eerder bij de mens zijn toegepast bij patiënten in het AMC augustus 2008 Inhoud Inleiding
COMMISSIE VAN DE EUROPESE GEMEENSCHAPPEN VERSLAG VAN DE COMMISSIE AAN DE RAAD
 COMMISSIE VAN DE EUROPESE GEMEENSCHAPPEN Brussel, 16.11.2000 COM(2000) 737 definitief (97/396/JBZ), over ketamine (97/396/JBZ), over GHB (97/396/JBZ), over ketamine (97/396/JBZ), over GHB Verslag van de
COMMISSIE VAN DE EUROPESE GEMEENSCHAPPEN Brussel, 16.11.2000 COM(2000) 737 definitief (97/396/JBZ), over ketamine (97/396/JBZ), over GHB (97/396/JBZ), over ketamine (97/396/JBZ), over GHB Verslag van de
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Neurexan; Tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 tablet (301,5 mg) bevat: Avena sativa D2 0,6 mg Coffea cruda
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Neurexan; Tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 tablet (301,5 mg) bevat: Avena sativa D2 0,6 mg Coffea cruda
KLINISCH GENEESMIDDELEN- ONDERZOEK
 KLINISCH GENEESMIDDELEN- ONDERZOEK HET PROCES VAN HET OPSTARTEN VAN KLINISCH ONDERZOEK MET GENEESMIDDELEN GAAT VERANDEREN De ECTR verandert het klinisch onderzoek met geneesmiddelen in Europa. Dit heeft
KLINISCH GENEESMIDDELEN- ONDERZOEK HET PROCES VAN HET OPSTARTEN VAN KLINISCH ONDERZOEK MET GENEESMIDDELEN GAAT VERANDEREN De ECTR verandert het klinisch onderzoek met geneesmiddelen in Europa. Dit heeft
Formulier Voortgangsrapportage
 Formulier Voortgangsrapportage De METC azm/um wil van al het door haar beoordeelde WMO-onderzoek jaarlijks een voortgangsrapportage zien. Zij heeft deze eis daartoe opgenomen in de tekst van haar eigen
Formulier Voortgangsrapportage De METC azm/um wil van al het door haar beoordeelde WMO-onderzoek jaarlijks een voortgangsrapportage zien. Zij heeft deze eis daartoe opgenomen in de tekst van haar eigen
VERORDENINGEN. 16.6.2009 Publicatieblad van de Europese Unie L 152/1
 16.6.2009 Publicatieblad van de Europese Unie L 152/1 I (Besluiten op grond van het EG- en het Euratom-Verdrag waarvan publicatie verplicht is) VERORDENINGEN VERORDENING (EG) Nr. 469/2009 VAN HET EUROPEES
16.6.2009 Publicatieblad van de Europese Unie L 152/1 I (Besluiten op grond van het EG- en het Euratom-Verdrag waarvan publicatie verplicht is) VERORDENINGEN VERORDENING (EG) Nr. 469/2009 VAN HET EUROPEES
(Niet-wetgevingshandelingen) VERORDENINGEN
 17.6.2017 L 155/1 II (Niet-wetgevingshandelingen) VERORDENINGEN GEDELEGEERDE VERORDENING (EU) 2017/1018 VAN DE COMMISSIE van 29 juni 2016 tot aanvulling van Richtlijn 2014/65/EU van het Europees Parlement
17.6.2017 L 155/1 II (Niet-wetgevingshandelingen) VERORDENINGEN GEDELEGEERDE VERORDENING (EU) 2017/1018 VAN DE COMMISSIE van 29 juni 2016 tot aanvulling van Richtlijn 2014/65/EU van het Europees Parlement
Q&A - KB 28 MEI 2013 EN OMZENDBRIEF NR 600
 Q&A - KB 28 MEI 2013 EN OMZENDBRIEF NR 600 1. Welke procedure moet gevolgd worden om zich als lokale contactpersoon aan te melden bij het fagg en aan welke vereisten moet de contactpersoon voldoen? In
Q&A - KB 28 MEI 2013 EN OMZENDBRIEF NR 600 1. Welke procedure moet gevolgd worden om zich als lokale contactpersoon aan te melden bij het fagg en aan welke vereisten moet de contactpersoon voldoen? In
Datum 1 juli 2014 Onderwerp Beantwoording Kamervragen over het onderzoek naar het verband tussen medicijngebruik en agressie
 1 > Retouradres Postbus 20301 2500 EH Den Haag De Voorzitter van de Tweede Kamer der Staten-Generaal Postbus 20018 2500 EA DEN HAAG Turfmarkt 147 2511 DP Den Haag Postbus 20301 2500 EH Den Haag www.rijksoverheid.nl/venj
1 > Retouradres Postbus 20301 2500 EH Den Haag De Voorzitter van de Tweede Kamer der Staten-Generaal Postbus 20018 2500 EA DEN HAAG Turfmarkt 147 2511 DP Den Haag Postbus 20301 2500 EH Den Haag www.rijksoverheid.nl/venj
Wet van 13 maart 2016 op het statuut van en het toezicht op de verzekerings- of herverzekeringsondernemingen, de artikelen 107 tot 122.
 de Berlaimontlaan 14 BE-1000 Brussel tel. +32 2 221 35 88 fax + 32 2 221 31 04 ondernemingsnummer: 0203.201.340 RPR Brussel www.nbb.be Mededeling Brussel, 2 juni 2017 Kenmerk: NBB_2017_18 uw correspondent:
de Berlaimontlaan 14 BE-1000 Brussel tel. +32 2 221 35 88 fax + 32 2 221 31 04 ondernemingsnummer: 0203.201.340 RPR Brussel www.nbb.be Mededeling Brussel, 2 juni 2017 Kenmerk: NBB_2017_18 uw correspondent:
T.a.v. Datum 11 november 2015 Onderwerp Meldingen lichaamsmateriaal. Geachte heer, mevrouw,
 > Retouradres Postbus 2680, 3500 GR Utrecht T.a.v. Inspectie voor de gezondheidszorg Stadsplateau 1 3521 AZ Utrecht Postbus 2680 3500 GR Utrecht T 088 120 50 00 F 088 120 50 01 www.igz.nl Inlichtingen
> Retouradres Postbus 2680, 3500 GR Utrecht T.a.v. Inspectie voor de gezondheidszorg Stadsplateau 1 3521 AZ Utrecht Postbus 2680 3500 GR Utrecht T 088 120 50 00 F 088 120 50 01 www.igz.nl Inlichtingen
Nieuwe wetgeving ten aanzien van orgaanvigilantie
 Nieuwe wetgeving ten aanzien van orgaanvigilantie 4e Symposium Weefselvigilantie, woensdag 30 november 2011 Hilga Katerberg Stafarts Orgaancentrum Inhoud Inleiding Wetgeving Definities Verantwoordelijkheden
Nieuwe wetgeving ten aanzien van orgaanvigilantie 4e Symposium Weefselvigilantie, woensdag 30 november 2011 Hilga Katerberg Stafarts Orgaancentrum Inhoud Inleiding Wetgeving Definities Verantwoordelijkheden
Beleidsdocument: Herregistratie van geneesmiddelen voor humaan gebruik ingeschreven via de nationale procedure
 OLLEGE TER BEOORDELING VAN GENEESIDDELEN Beleidsdocument: Herregistratie van geneesmiddelen voor humaan gebruik ingeschreven via de nationale procedure EB 42 14 maart 2013 EB-42 Inhoudsopgave 1. Inleiding
OLLEGE TER BEOORDELING VAN GENEESIDDELEN Beleidsdocument: Herregistratie van geneesmiddelen voor humaan gebruik ingeschreven via de nationale procedure EB 42 14 maart 2013 EB-42 Inhoudsopgave 1. Inleiding
Na consultatie herziene vertaling van de QRD-template
 Na consultatie herziene vertaling van de QRD-template Deelrapport voortkomend uit het adviestraject Het verbeteren van de begrijpelijkheid van patiëntenbijsluiters 10 juli 2009 Dr. Leo Lentz UiL-OTS Universiteit
Na consultatie herziene vertaling van de QRD-template Deelrapport voortkomend uit het adviestraject Het verbeteren van de begrijpelijkheid van patiëntenbijsluiters 10 juli 2009 Dr. Leo Lentz UiL-OTS Universiteit
Gebruikershandleiding voor webrapporten
 Bescherming van de gezondheid van patiënten Deze gebruikershandleiding voor webrapporten bevat informatie over de gegevenselementen, indeling, interpretatie en functionaliteiten van het webrapport. 1.
Bescherming van de gezondheid van patiënten Deze gebruikershandleiding voor webrapporten bevat informatie over de gegevenselementen, indeling, interpretatie en functionaliteiten van het webrapport. 1.
Materiovigilantie tijdens inspecties van aangemelde instanties en fabrikanten van medische hulpmiddelen
 Materiovigilantie tijdens inspecties van aangemelde instanties en fabrikanten van medische hulpmiddelen 5de Vigilantiedag BRUSSEL Katrien MARTENS Inhoud Inleiding DG INSPECTIE Afdeling Industrie - Medische
Materiovigilantie tijdens inspecties van aangemelde instanties en fabrikanten van medische hulpmiddelen 5de Vigilantiedag BRUSSEL Katrien MARTENS Inhoud Inleiding DG INSPECTIE Afdeling Industrie - Medische
Voorstel voor een VERORDENING VAN HET EUROPEES PARLEMENT EN DE RAAD
 EUROPESE COMMISSIE Brussel, 29.11.2017 COM(2017) 735 final 2017/0328 (COD) Voorstel voor een VERORDENING VAN HET EUROPEES PARLEMENT EN DE RAAD tot wijziging van Verordening (EG) nr. 726/2004 wat betreft
EUROPESE COMMISSIE Brussel, 29.11.2017 COM(2017) 735 final 2017/0328 (COD) Voorstel voor een VERORDENING VAN HET EUROPEES PARLEMENT EN DE RAAD tot wijziging van Verordening (EG) nr. 726/2004 wat betreft
Vermeld hier tevens de uitgevende instant. Titel voor het algemene publiek ('leken') in makkelijk te begrijpen taal.
 Welke gegevens moet u aanleveren (Trial Registration Data Set)? Graag ontvangen wij de informatie in het Engels gezien het internationale karakter van prospectieve registratie. Uw studie zal tevens terug
Welke gegevens moet u aanleveren (Trial Registration Data Set)? Graag ontvangen wij de informatie in het Engels gezien het internationale karakter van prospectieve registratie. Uw studie zal tevens terug
Aanvraagformulier REGISTRATIE oncologie monitor
 Aanvraagformulier REGISTRATIE oncologie monitor 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:... Geboorteplaats:... Werkzaam bij: Organisatie + Afdeling:...
Aanvraagformulier REGISTRATIE oncologie monitor 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:... Geboorteplaats:... Werkzaam bij: Organisatie + Afdeling:...
Omzendbrief met betrekking tot de wederzijdse erkenning van de Gekwalificeerde Persoon binnen de Benelux
 Federaal Agentschap voor de Veiligheid van de Voedselketen Omzendbrief met betrekking tot de wederzijdse erkenning van de Gekwalificeerde Persoon binnen de Benelux Referentie PCCB/S3/KVT/878741 Datum 16/08/2018
Federaal Agentschap voor de Veiligheid van de Voedselketen Omzendbrief met betrekking tot de wederzijdse erkenning van de Gekwalificeerde Persoon binnen de Benelux Referentie PCCB/S3/KVT/878741 Datum 16/08/2018
Directe communicatie aan gezondheidszorgbeoefenaars over de associatie van Sprycel (dasatinib) met Pulmonaire Arteriële Hypertensie (PAH)
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Gelet op het Verdrag tot oprichting van de Europese Economische Gemeenschap, inzonderheid op artikel 235,
 Avis juridique important 31993R2309 Verordening (EEG) nr. 2309/93 van de Raad van 22 juli 1993 tot vaststelling van communautaire procedures voor het verlenen van vergunningen voor en het toezicht op geneesmiddelen
Avis juridique important 31993R2309 Verordening (EEG) nr. 2309/93 van de Raad van 22 juli 1993 tot vaststelling van communautaire procedures voor het verlenen van vergunningen voor en het toezicht op geneesmiddelen
Bouwen aan vertrouwen: perspectief van de industrie
 Symposium ter gelegenheid afscheid Ad van Dooren Zelfredzaamheid van patiënten bij gebruik van veilige medicatie. Bouwen aan vertrouwen: perspectief van de industrie Rudolf van Olden, arts Medisch Directeur
Symposium ter gelegenheid afscheid Ad van Dooren Zelfredzaamheid van patiënten bij gebruik van veilige medicatie. Bouwen aan vertrouwen: perspectief van de industrie Rudolf van Olden, arts Medisch Directeur
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A2 Archiveren studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A2 Archiveren studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
LIJST MET NAMEN, FARMACEUTISCHE VORMEN, STERKTEN, DIERSOORTEN, TOEDIENINGSWEGEN, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN / AANVRAGERS
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORMEN, STERKTEN, DIERSOORTEN, TOEDIENINGSWEGEN, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN / AANVRAGERS 1/9 Lidstaat/nummer van de vergunning voor
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORMEN, STERKTEN, DIERSOORTEN, TOEDIENINGSWEGEN, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN / AANVRAGERS 1/9 Lidstaat/nummer van de vergunning voor
Hoofdstuk 1: Inleiding 1.1 Achtergrond
 Hoofdstuk 1: Inleiding 1.1 Achtergrond Het wordt algemeen erkend dat de werkzaamheid van geneesmiddelen bij kinderen kan afwijken van die bij volwassenen. Om te komen tot passende farmacotherapeutische
Hoofdstuk 1: Inleiding 1.1 Achtergrond Het wordt algemeen erkend dat de werkzaamheid van geneesmiddelen bij kinderen kan afwijken van die bij volwassenen. Om te komen tot passende farmacotherapeutische
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik
 EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor CCMO, METC s en onderzoekers- Paula Vossebeld DCTF jaarcongres 7 oktober 2015 Verordening
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor CCMO, METC s en onderzoekers- Paula Vossebeld DCTF jaarcongres 7 oktober 2015 Verordening
naamloze vennootschap Paepsem Business Park, Boulevard Paepsem 20 B-1070 Brussel, België BTW BE 0876.488.436 (Brussel)
 naamloze vennootschap Paepsem Business Park, Boulevard Paepsem 20 B-1070 Brussel, België BTW BE 0876.488.436 (Brussel) VOLMACHT gewone en buitengewone algemene vergadering van aandeelhouders die zal worden
naamloze vennootschap Paepsem Business Park, Boulevard Paepsem 20 B-1070 Brussel, België BTW BE 0876.488.436 (Brussel) VOLMACHT gewone en buitengewone algemene vergadering van aandeelhouders die zal worden
Informatie verkrijgen & onderhoud van vergunning voor parallelle invoer immunologisch diergeneesmiddel.
 Verkrijgen en onderhouden van een vergunning voor parallelle invoer van een immunologisch diergeneesmiddel In dit document staat informatie over de voorwaarden voor het verkrijgen en behouden van een vergunning
Verkrijgen en onderhouden van een vergunning voor parallelle invoer van een immunologisch diergeneesmiddel In dit document staat informatie over de voorwaarden voor het verkrijgen en behouden van een vergunning
KANKERONDERZOEK : DE ROL VAN DE COMMISSIES VOOR ETHIEK
 KANKERONDERZOEK : DE ROL VAN DE COMMISSIES VOOR ETHIEK Marc Bogaert (marc.bogaert@ugent.be) Brasschaat, 29 september 2005 Experimenten bij de mens : de situatie vanaf 1 mei 2004 De richtlijn (Directive)
KANKERONDERZOEK : DE ROL VAN DE COMMISSIES VOOR ETHIEK Marc Bogaert (marc.bogaert@ugent.be) Brasschaat, 29 september 2005 Experimenten bij de mens : de situatie vanaf 1 mei 2004 De richtlijn (Directive)
Hierbij zend ik u de antwoorden op de vragen van het Kamerlid Kuzu (PvdA) over de bijwerkingen van antidepressiva (SSRI s) (2014Z07811).
 > Retouradres Postbus 20350 2500 EJ Den Haag De Voorzitter van de Tweede Kamer der Staten-Generaal Postbus 2008 2500 EA DEN HAAG Bezoekadres: Rijnstraat 50 255 XP DEN HAAG T 070 340 79 F 070 340 78 34
> Retouradres Postbus 20350 2500 EJ Den Haag De Voorzitter van de Tweede Kamer der Staten-Generaal Postbus 2008 2500 EA DEN HAAG Bezoekadres: Rijnstraat 50 255 XP DEN HAAG T 070 340 79 F 070 340 78 34
