Titel: Good Clinical Practice & Monitoring. Initiation Investigator Driven Studies. Versie: 14-jan-2013
|
|
|
- Mark Aerts
- 8 jaren geleden
- Aantal bezoeken:
Transcriptie
1 Titel: Good Clinical Practice & Monitoring Initiation Investigator Driven Studies
2 Inhoud Wet- en regelgeving/declaration of Helsinki Good Clinical Practice Patiënteninformatie/ informed consent Basisvereisten dataverzameling Non-compliance Drug Safety Basisvereisten onderzoeker Essentiële Documenten Amendementen Monitoring 2
3 Wet- en regelgeving (Inter)nationale wet- en regelgeving Declaration of Helsinki Code of Federal Regulations 21CFR ICH/GCP Guidelines ISO Standards (Medical Devices) Europese wet- en regelgeving European Union Clinical Trial Directive EU CTD Law on Data Protection European medicines law Nationale wet- en regelgeving WMO, Wbp, WGBO, KWZ, Geneesmiddelenwet, BIG, Archiefwet Intern UMCU DIGD Standard Operating Procedures (SOP s) 3
4 Declaration of Helsinki Ontwikkeld door de World Medical Association (WMA) in 1964 en regelmatig geupdate. Enkele belangrijke principes zijn: Het is de plicht van de arts om de gezondheid van patiënten te bevorderen en te waarborgen, inclusief degene die betrokken is in medisch onderzoek Het welbevinden van de individuele proefpersoon dient boven alle andere belangen te gaan Goede afweging van de risico s en belasting t.o.v. de verwachte voordelen Patiënten moeten geïnformeerd worden over alle aspecten van het onderzoek en weigering tot deelname mag de arts- patiënt relatie niet beïnvloeden 4
5 Good Clinical Practice Good Clinical Practice (GCP) is een internationale ethische en wetenschappelijke kwaliteitsstandaard die is opgenomen in de Nederlandse wetgeving. Het is een kwaliteitsstandaard voor het opzetten, uitvoeren en het vastleggen van klinisch wetenschappelijk onderzoek waarbij sprake is van deelname door proefpersonen. Alle principes zijn gebaseerd op de 2 pijlers van GCP: Bescherming van de proefpersoon: vrijwillig, zonder druk, mondelinge en schriftelijke instemming, bescherming van de privacy Kwaliteit van data 5
6 Patiënteninformatie/ informed consent Informed Consent procedure: Mondeling informeren Tijd geven om zich te beraden en alle vragen te kunnen stellen Tekenen van het Informed Consent formulier bij voorkeur samen met de patiënt en controleren of alle gegevens ingevuld zijn Patiënt een kopie geven óf 2 ICF s tekenen Documenteren van Informed Consent proces in de status of EPD 6
7 Aandachtspunten IC procedure Let op! Degene die de IC procedure afneemt, moet hiervoor geautoriseerd zijn door de PI De patiënt tekent altijd eerst De juiste, door de METC goedgekeurde versie moet getekend worden Patiënt dient zelf zijn/haar naam en datum in te vullen Studiehandelingen mogen niet verricht worden vóór tekenen van ICF Als de procedure anders verloopt dan dient dit te worden vastgelegd in een beschrijving van de procedure of Note to File 7
8 Patiënteninformatie/ informed consent #1 audit findings! Geen handtekening onderzoeker of stempel Datum ondertekening mist, is incompleet of verschillend Ontbrekende Informed Consent Forms Informed Consent Proces niet gedocumenteerd Getekend na de eerste studiehandelingen Getekend door een niet geautoriseerd persoon Incorrecte versie gebruikt Patiënten informatie en informed consent zijn onlosmakelijk met elkaar verbonden en dienen ook zo gefiled te worden 8
9 Basis vereisten dataverzameling (1) Niet te identificeren verzameling van patiënten data: geen naam en patiëntnummer en geboortedatum op CRF en eventuele correspondentie Alleen verzamelen van die data die nodig zijn voor het specifieke doel zoals vermeld in het protocol Alle CRF gegevens moeten in brondocumenten vermeld staan (papier of elektronisch) tenzij anders in protocol of studiehandleiding omschreven 9
10 Basis vereisten dataverzameling (2) Indien data gecorrigeerd dienen te worden, dan de oorspronkelijke tekst doorhalen (zodat deze nog wel zichtbaar blijft) en juiste antwoord vermelden met paraaf en datum (reden) Gelimiteerde toegang tot brongegevens van de geïncludeerde patiënten voor de CRA regelen 10
11 Brondocumentatie : eisen Herleidbaar Traceerbaar naar de persoon die de data geobserveerd en gerapporteerd heeft, door handtekening (of paraaf) en datum Leesbaar Tijdig Leesbaar en gerapporteerd op een permanent medium Gerapporteerd op het tijdstip van de observatie. Indien later source toegevoegd wordt deze dateren en paraferen Origineel De 1e observaties Accuraat Accuraat en compleet weergeven van de observatie 11
12 Non-compliance (1) = Niet voldoen aan de vereisten van ICH GCP, landelijke wetgeving en richtlijnen en/of studieprotocol De ernst van de non-compliance kan onderverdeeld worden in deviation of violation 12
13 Non-compliance (2) Protocol deviation: De risico s of voordelen voor de patiënt zijn niet beïnvloed De waarde van de verzamelde data is niet beïnvloed Betrof een onbewuste fout van de onderzoeksstaf Protocol violation: De bevinding heeft geleid tot een risico voor de patiënt of De bevinding heeft de wetenschappelijke waarde van de data beïnvloed of Er is bewijs dat er een bewuste fout is gemaakt waarvan de consequenties niet werden overzien 13
14 Documenteren van een deviation (1) Schrijf een Note to File tenzij de afwijking op een ander document toegelicht kan worden 14
15 Documenteren van een deviation (2) Geef op de Note to File aan: Description of the issue: Een beschrijving van wat is gebeurd, en wat de impact is op de studie. Ook als er geen impact is op de studie, dan moet dat ook vermeld zijn. Action taken: Wat gedaan is om het probleem op te lossen en wat gedaan wordt, om soortgelijke problemen in de toekomst te voorkomen 15
16 Documenteren van een violation Noteer de violation in de brondocumenten en/of ecrf Overleg met de sponsor welke stappen ondernomen moeten worden Vul een Protocol Violaton formulier in en geef aan welke stappen ondernomen worden om het probleem op te lossen en in de toekomst te voorkomen Stuur een kopie naar de sponsor en file het origineel in ISF 16
17 Drug safety (1) Adverse Event (AE) Elk ongewenst medisch voorval bij een patiënt of proefpersoon aan wie een product is toegediend binnen studieverband, ongeacht het oorzakelijke verband met de behandeling. 17
18 Drug safety (2) Serious Adverse Event (SAE) Elk ongewenst medisch voorval ongeacht het oorzakelijke verband met de (dosis van de)behandeling dat: De dood tot gevolg heeft Levensbedreigend is (ten tijde van het voorval) Ziekenhuisopname of verlenging van opname Een aangeboren afwijking van het nageslacht tot gevolg heeft Resulteert in aanhoudende of significante invaliditeit / ongeschiktheid Uitzonderingen moeten protocollair zijn vastgelegd! 18
19 Drug safety (3) Procedure SAE reporting Raadpleeg de procedure in protocol of studiehandleiding Vul het SAE formulier in en fax of mail (ingescand) dit formulier binnen 24 uur na kennisname naar de Sponsor (als sponsor niet coördinerend onderzoeker is) Sponsor meldt de SAE in ToetsingOnline Stuur additionele documenten of informatie via een follow up formulier 19
20 Drug safety (4) (SUSAR) Suspected Unexpected Serious Adverse Reaction Suspected - mogelijk gerelateerd aan de studie behandeling Unexpected - de aard of ernst van de aandoening is niet in overeenstemming met de beschikbare productinformatie 20
21 Drug safety (5) Expedited reporting SUSAR (WMO) aan CBG Wanneer het voorval in jouw protocol plaatsvindt Binnen 15 dagen nadat de sponsor de initiële informatie ontving over het voorval Voor fatale of levensbedreigende voorvallen rapportage binnen 7 dagen Wanneer het voorval in een ander protocol plaatsvindt 6 maandelijkse line listing Wanneer het voorval vergaande gevolgen heeft voor de veiligheid dienen de expedited timelines in acht te worden genomen. SUSAR s dienen ook aan de IRB/IEC,CA en onderzoekers gemeld te worden binnen deze tijdslijnen 21
22 Drug safety (6) Annual safety report (WMO) door sponsor Gedurende het gehele onderzoek 1x per jaar, samen met de voortgangsrapportage Overzicht van alle SAE s en SUSAR s in het onderzoek 22
23 Basis vereisten onderzoeker Volgens de NFU richtlijn dient de onderzoeker in Academische centra BROK gecertificeerd te zijn en in overige centra over aantoonbare GCP kennis te beschikken (Certificaten van GCP training toevoegen aan CV) Overig research personeel dient door de PI geautoriseerd te worden vóór start van de studie De PI dient ervoor te zorgen dat alle personen die meewerken aan het onderzoek voldoende getraind zijn in het protocol, het onderzoeksproduct en de verplichtingen/taken De PI dient garant te staan voor het feit dat de betrokkenen gekwalificeerd zijn voor de aan hen gedelegeerde taken 23
24 Essentiële documenten Investigator Site File (ISF) Een file van de onderzoeker welke alle documenten voor die specifieke onderzoekslocatie bevat én alle algemene documenten die van toepassing zijn. De onderzoeker of gedelegeerde is verantwoordelijk voor het bijhouden van de ISF (o.a. Screening en enrolment log, Subject ID log en Document Referral Note). Archiveren van de files, CRF s en medische dossiers Standaard: 20 jaar in Academische ziekenhuizen (volgens archiefwet) en 15 jaar in de periferie na afloop studie (volgens GCP) 24
25 Amendementen Alle wijzigingen die doorgevoerd worden in bijvoorbeeld het studieprotocol moeten vooraf aan implementatie zijn goedgekeurd door de METC Wijzigingen worden als substantiële of niet-substantiële (slechts administratieve wijzigingen) amendementen ingediend bij de METC 25
26 Monitoring (1) Het bewaken van de voortgang, de uitvoering en het vastleggen van een klinisch onderzoek conform het protocol, de Standaard Werkvoorschriften (SOP s), Good Clinical Practice (GCP), en de relevante wettelijke vereisten 26
27 Monitoring (2) Doel van monitoring Verifiëren of de rechten en het welzijn van de proefpersonen worden gewaarborgd Verifiëren of de gerapporteerde data accuraat, compleet en verifieerbaar zijn met de brondocumenten (source data verification) Verifiëren of de uitvoering van de studie in overeenstemming is met het huidige goedgekeurde protocol/amendment(s), GCP, en alle relevante wet- en regelgeving. 27
28 Monitoring (3) NFU richtlijnen Julius Clinical wordt ingeschakeld voor UMCU studies met een matig en hoog risico. Alle ICF s worden 100% gecontroleerd De data van studies (in/exclusiecriteria, SAE s, visite gegevens) met een hoog risico worden 100% gemonitord 28
29 Monitoring (4) De CRA stuurt de sponsor na ieder bezoek binnen 3 weken een rapport, brief en actielijst. In het rapport worden de bevindingen, afwijkingen, conclusies en de genomen of te nemen maatregelen en/of aanbevelingen beschreven. Overige deelnemende centra ontvangen een brief en een actielijst. We vragen de sites om de actiepunten binnen 1 à 1,5 maand na het bezoek op te volgen. 29
30 Monitoring (5) Aan het einde van de studie vindt de close-out visite plaats Doel: Officiële beëindiging van alle studie gerelateerde activiteiten op een onderzoekslocatie Bespreken van de verantwoordelijkheden van de onderzoeker na de studie Bespreken archivering Over het algemeen wordt een close-out visite gedaan wanneer alle data clean zijn ( database lock ). 30
31 Veel succes! Contact: Karin Groot E. Senior Clinical Research Associate M T Broederplein CD Zeist Nederland 31
Monitorplan voorbeeld
 Monitorplan voorbeeld Protocol Er moet in het protocol beschreven worden dat er monitoring plaatsvindt (zie ook CCMO voorbeeld template). Het monitoringplan mag als bijlage worden toegevoegd (in dat geval
Monitorplan voorbeeld Protocol Er moet in het protocol beschreven worden dat er monitoring plaatsvindt (zie ook CCMO voorbeeld template). Het monitoringplan mag als bijlage worden toegevoegd (in dat geval
Standard Operating Procedure
 Standard Operating Procedure SOP: V9 Initiatievisite Auteur Naam: Functie instelling/afdeling Judie van den Elshout Staffunctionaris Wetenschapsbureau Wetenschapsbureau / Cluster Leerhuis Handtekening:...
Standard Operating Procedure SOP: V9 Initiatievisite Auteur Naam: Functie instelling/afdeling Judie van den Elshout Staffunctionaris Wetenschapsbureau Wetenschapsbureau / Cluster Leerhuis Handtekening:...
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U9 Monitoren Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies Versiedatum Hoofdstuk Versiedatum Hoofdstuk
Standard Operating Procedure STZ SOP: U9 Monitoren Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies Versiedatum Hoofdstuk Versiedatum Hoofdstuk
29 juni Initiatie bijeenkomst PORTEC 4. Kwaliteitsborging WMO GCP richtsnoer. Frank van Leeuwen IKNL
 29 juni 2012 Initiatie bijeenkomst PORTEC 4 Kwaliteitsborging WMO GCP richtsnoer Frank van Leeuwen IKNL Wet en regelgeving Verklaring van Helsinki Richtsnoer voor Good Clinical Practice (CPMP/ICH/135/95)
29 juni 2012 Initiatie bijeenkomst PORTEC 4 Kwaliteitsborging WMO GCP richtsnoer Frank van Leeuwen IKNL Wet en regelgeving Verklaring van Helsinki Richtsnoer voor Good Clinical Practice (CPMP/ICH/135/95)
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A1 Afsluiting studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A1 Afsluiting studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U10 Audit Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: U10 Audit Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum Opmerkingen
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U4 Registratie /randomisatie procedure Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum
Standard Operating Procedure STZ SOP: U4 Registratie /randomisatie procedure Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum
Aanvraagformulier REGISTRATIE oncologie monitor
 Aanvraagformulier REGISTRATIE oncologie monitor 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:... Geboorteplaats:... Werkzaam bij: Organisatie + Afdeling:...
Aanvraagformulier REGISTRATIE oncologie monitor 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:... Geboorteplaats:... Werkzaam bij: Organisatie + Afdeling:...
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen. Farmaceutische Bedrijven Deelteam Klinisch Onderzoek
 Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U5 Datamanagement Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: U5 Datamanagement Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U1 Identificatie, werving en pre-screening proefpersonen Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure STZ SOP: U1 Identificatie, werving en pre-screening proefpersonen Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere
Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen
 Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen Afdeling Farmaceutische Bedrijven, Klinisch Onderzoek Good Clinical Practice Inhoud Wat doet de IGJ aan toezicht op klinisch
Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen Afdeling Farmaceutische Bedrijven, Klinisch Onderzoek Good Clinical Practice Inhoud Wat doet de IGJ aan toezicht op klinisch
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U8 Melding van (Serious) Adverse Events en SUSARs Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies
Standard Operating Procedure STZ SOP: U8 Melding van (Serious) Adverse Events en SUSARs Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL4 Investigator Site File Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: VL4 Investigator Site File Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL5 Protocolamendement (lokaal) Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: VL5 Protocolamendement (lokaal) Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
De rol van de verpleegkundige binnen Medischwetenschappelijk
 De rol van de verpleegkundige binnen Medischwetenschappelijk onderzoek Moderator Mevr. R.C.A. Veldhoen-Tijben 1st author / speaker Miriam Gelderloos Co-author Erna Helmantel Belangenverklaring In overeenstemming
De rol van de verpleegkundige binnen Medischwetenschappelijk onderzoek Moderator Mevr. R.C.A. Veldhoen-Tijben 1st author / speaker Miriam Gelderloos Co-author Erna Helmantel Belangenverklaring In overeenstemming
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek
 Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
INFORMATIEBLAD. Maart 2011
 INFORMATIEBLAD AANMELDING TRIALBUREAU/DATACENTRUM Maart 2011 Kanker zo snel mogelijk terugdringen en onder controle brengen. We zijn er voor mensen die leven met kanker en de mensen die met hen samenleven.
INFORMATIEBLAD AANMELDING TRIALBUREAU/DATACENTRUM Maart 2011 Kanker zo snel mogelijk terugdringen en onder controle brengen. We zijn er voor mensen die leven met kanker en de mensen die met hen samenleven.
INCLUSIE SET PLAATS HIER DE PATIENTSTICKER VAN DE GEINCLUDEERDE PATIENT. ULTRA STUDIE INCLUSIE SET VERSIE 9 Pagina 1 van 9
 INCLUSIE SET Als de patiënt geïncludeerd kan worden in de studie, voert de arts in het behandelcentrum de randomisatieprocedure uit na telefonische aanmelding van de patiënt(e) PLAATS HIER DE PATIENTSTICKER
INCLUSIE SET Als de patiënt geïncludeerd kan worden in de studie, voert de arts in het behandelcentrum de randomisatieprocedure uit na telefonische aanmelding van de patiënt(e) PLAATS HIER DE PATIENTSTICKER
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U11 Voortgangsrapportage Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: U11 Voortgangsrapportage Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Monitoren vs auditen. CRA dag 21 april 2016
 Monitoren vs auditen CRA dag 21 april 2016 Introductie Freelance consultant, mede oprichter TAPAS Group B.V. Mede oprichter/directeur van CRA B.V. Medical Adviser Yamanouchi Pharma Clinical trial monitor
Monitoren vs auditen CRA dag 21 april 2016 Introductie Freelance consultant, mede oprichter TAPAS Group B.V. Mede oprichter/directeur van CRA B.V. Medical Adviser Yamanouchi Pharma Clinical trial monitor
Monitoring van Investigator Initiated onderzoek
 Monitoring van Investigator Initiated onderzoek V1.0 Angela Vlug Clinical Research Bureau VUmc Wat is een IIS (volgens de NFU) Onderzoek waarvoor de raad van bestuur van een (universitair) medisch centrum
Monitoring van Investigator Initiated onderzoek V1.0 Angela Vlug Clinical Research Bureau VUmc Wat is een IIS (volgens de NFU) Onderzoek waarvoor de raad van bestuur van een (universitair) medisch centrum
Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) Team Klinisch Onderzoek
 Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) 2014-2016 Team Klinisch Onderzoek Toezicht op IIT 2014-2016 Aanleiding en werkwijze Bevindingen vanuit de praktijk Conclusies en aandachtspunten
Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) 2014-2016 Team Klinisch Onderzoek Toezicht op IIT 2014-2016 Aanleiding en werkwijze Bevindingen vanuit de praktijk Conclusies en aandachtspunten
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A2 Archiveren studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A2 Archiveren studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Site selectie visite checklist
 Site selectie visite checklist Informatie sponsor: Naam sponsor: Contactpersoon: Functie: Afdeling: Telefoonnummer : Email : Informatie onderzoekslocatie: Naam onderzoekslocatie : Naam onderzoeker: Functie:
Site selectie visite checklist Informatie sponsor: Naam sponsor: Contactpersoon: Functie: Afdeling: Telefoonnummer : Email : Informatie onderzoekslocatie: Naam onderzoekslocatie : Naam onderzoeker: Functie:
IC ICF ICH ISF. Lijst met afkortingen, definities en termen STZ-Kwaliteitshandboek SOP s
 Lijst met afkortingen, definities en termen STZ-Kwaliteitshandboek SOP s ABR ADR AE AR BROK CCMO CRF CTA CV DSMB EMEA EU EudraCT FU brief GCP GMP IB IC ICF ICH IMPD ISF MEB METC EU RCT SAE SOP SPC SUSAR
Lijst met afkortingen, definities en termen STZ-Kwaliteitshandboek SOP s ABR ADR AE AR BROK CCMO CRF CTA CV DSMB EMEA EU EudraCT FU brief GCP GMP IB IC ICF ICH IMPD ISF MEB METC EU RCT SAE SOP SPC SUSAR
Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek
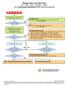 Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek Melding voorval proefpersoon aan onderzoeker/arts 1 Rapportage voorval door onderzoeker/arts in patiëntenstatus
Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek Melding voorval proefpersoon aan onderzoeker/arts 1 Rapportage voorval door onderzoeker/arts in patiëntenstatus
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VC8 Beoordeling amendement toetsende commissie (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure STZ SOP: VC8 Beoordeling amendement toetsende commissie (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL2 Aanpassen proefpersoneninformatie / toestemmingsformulier aan lokale situatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen
Standard Operating Procedure STZ SOP: VL2 Aanpassen proefpersoneninformatie / toestemmingsformulier aan lokale situatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen
Formulier Voortgangsrapportage
 Formulier Voortgangsrapportage De METC azm/um wil van al het door haar beoordeelde WMO-onderzoek jaarlijks een voortgangsrapportage zien. Zij heeft deze eis daartoe opgenomen in de tekst van haar eigen
Formulier Voortgangsrapportage De METC azm/um wil van al het door haar beoordeelde WMO-onderzoek jaarlijks een voortgangsrapportage zien. Zij heeft deze eis daartoe opgenomen in de tekst van haar eigen
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VC9 Proefpersonen- en aansprakelijkheidsverzekering (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure STZ SOP: VC9 Proefpersonen- en aansprakelijkheidsverzekering (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
1. Voorafgaand aan de klinische fase van het onderzoek
 Essentiële documenten Bron: Richtsnoer voor good clinical practice (CPMP/ICH/135/95) De verwijzingen in dit document verwijzen naar de artikelen in bovenstaand document. 1. Voorafgaand aan de klinische
Essentiële documenten Bron: Richtsnoer voor good clinical practice (CPMP/ICH/135/95) De verwijzingen in dit document verwijzen naar de artikelen in bovenstaand document. 1. Voorafgaand aan de klinische
Toezicht op IIT: bevindingen vanuit de praktijk
 Toezicht op IIT: bevindingen vanuit de praktijk Elysée Hille, senior inspecteur namens deelteam KO-GCP Teamcoördinator KO-GCP/PhV/GZH Afdeling Farmaceutische Bedrijven Wat doet de IGZ? Toezicht op klinisch
Toezicht op IIT: bevindingen vanuit de praktijk Elysée Hille, senior inspecteur namens deelteam KO-GCP Teamcoördinator KO-GCP/PhV/GZH Afdeling Farmaceutische Bedrijven Wat doet de IGZ? Toezicht op klinisch
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: O3 Ontwikkelen, implementeren en beheren van SOP s Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies
Standard Operating Procedure STZ SOP: O3 Ontwikkelen, implementeren en beheren van SOP s Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies
De rol van de Contract Research Organisatie (CRO) Klinisch onderzoek
 De rol van de Contract Research Organisatie (CRO) in klinisch geneesmiddelenonderzoek Klinisch onderzoek Inhoud Aanleiding CRO project Methode en resultaten» Werkwijze en resultaten foto van het veld vragenlijst»
De rol van de Contract Research Organisatie (CRO) in klinisch geneesmiddelenonderzoek Klinisch onderzoek Inhoud Aanleiding CRO project Methode en resultaten» Werkwijze en resultaten foto van het veld vragenlijst»
1. Beschrijving werkgebieden / thema s
 1. Beschrijving werkgebieden / thema s Nr 1 Thema Wetenschappelijke Achtergrond en Opzet van Onderzoek 2 Ethische en veiligheid overwegingen 3 Ontwikkeling en Regelgeving 4 Clinical Trial Operations (Projectorganisatie)
1. Beschrijving werkgebieden / thema s Nr 1 Thema Wetenschappelijke Achtergrond en Opzet van Onderzoek 2 Ethische en veiligheid overwegingen 3 Ontwikkeling en Regelgeving 4 Clinical Trial Operations (Projectorganisatie)
Aanvraagformulier REGISTRATIE oncologie datamanager
 Aanvraagformulier REGISTRATIE oncologie datamanager 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:.... Geboorteplaats:.... Werkzaam bij: Organisatie +
Aanvraagformulier REGISTRATIE oncologie datamanager 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:.... Geboorteplaats:.... Werkzaam bij: Organisatie +
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U2 Informed consent Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: U2 Informed consent Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Jouw GCP up-to-date in 45 minuten. Marieke Meulemans, oprichter GCP Central
 Jouw GCP up-to-date in 45 minuten Marieke Meulemans, oprichter GCP Central Waarom een GCP update tijdens de CRA dag? Gedreven Meesterschap. Meesterschap is vakmanschap. Vakmanschap is beheersing van het
Jouw GCP up-to-date in 45 minuten Marieke Meulemans, oprichter GCP Central Waarom een GCP update tijdens de CRA dag? Gedreven Meesterschap. Meesterschap is vakmanschap. Vakmanschap is beheersing van het
Toezicht op klinisch onderzoek - bevindingen vanuit de praktijk
 Toezicht op klinisch onderzoek - bevindingen vanuit de praktijk Namens Deelprogramma Klinisch Onderzoek, IGZ Spreker Dr. ir. J. Eland-Gerritsen Coördinerend/Specialistisch Senior inspecteur Inhoud Toezicht
Toezicht op klinisch onderzoek - bevindingen vanuit de praktijk Namens Deelprogramma Klinisch Onderzoek, IGZ Spreker Dr. ir. J. Eland-Gerritsen Coördinerend/Specialistisch Senior inspecteur Inhoud Toezicht
Gedigitaliseerd onderzoek..
 Gedigitaliseerd onderzoek.. ITC Validation Consultants an extra measure of Quality Frans Leijse Managing Director GSK Global QA-eCompliance Manager Adviseurs voor.. GxP compliance van ICT Systemen Computer
Gedigitaliseerd onderzoek.. ITC Validation Consultants an extra measure of Quality Frans Leijse Managing Director GSK Global QA-eCompliance Manager Adviseurs voor.. GxP compliance van ICT Systemen Computer
Het Clinical Research Bureau (CRB) van VUmc
 1 Het Clinical Research Bureau (CRB) van VUmc Angela Vlug Kwaliteitsborging van mensgebonden onderzoek 1 Het Clinical Research Bureau heeft als doel om optimale kwaliteit van de uitvoering van mensgebonden
1 Het Clinical Research Bureau (CRB) van VUmc Angela Vlug Kwaliteitsborging van mensgebonden onderzoek 1 Het Clinical Research Bureau heeft als doel om optimale kwaliteit van de uitvoering van mensgebonden
HOVON 141 CLL. Instructies voor de deelnemende site: ICF studie template aanpassen naar een lokaal biobank ICF
 Instructies voor de deelnemende site: ICF studie template aanpassen naar een lokaal biobank ICF Doel van deze studie template Deze studie template is bestemd voor de deelnemende sites in Nederland van
Instructies voor de deelnemende site: ICF studie template aanpassen naar een lokaal biobank ICF Doel van deze studie template Deze studie template is bestemd voor de deelnemende sites in Nederland van
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A4 Publicatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A4 Publicatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
SOP: Voorlichtingsgesprek en uitgesteld informed consent CONTRAST trials
 SOP: Voorlichtingsgesprek en uitgesteld informed consent CONTRAST trials SOP: IC1 Versie Nr.: 1.1 Geldig m.i.v.: 03-04-2018 Auteur: S.A. van den Berg, arts-onderzoeker AMC Autorisator: Dr. H.B. van der
SOP: Voorlichtingsgesprek en uitgesteld informed consent CONTRAST trials SOP: IC1 Versie Nr.: 1.1 Geldig m.i.v.: 03-04-2018 Auteur: S.A. van den Berg, arts-onderzoeker AMC Autorisator: Dr. H.B. van der
WMO-GCP opfriscursus Nederlandse Vereniging voor Oncologie Datamanagers 27 februari 2019
 WMO-GCP opfriscursus Nederlandse Vereniging voor Oncologie Datamanagers 27 februari 2019 Agenda Introductie ICH-GCP R2 AVG Kwaliteitssyteem Informed Consent ISF e-tmf Monitoren SAE rapportage Waarom wetgeving?
WMO-GCP opfriscursus Nederlandse Vereniging voor Oncologie Datamanagers 27 februari 2019 Agenda Introductie ICH-GCP R2 AVG Kwaliteitssyteem Informed Consent ISF e-tmf Monitoren SAE rapportage Waarom wetgeving?
Antwoorden CRO-vragenlijst - foto van het veld
 Antwoorden CRO-vragenlijst - foto van het veld In samenwerking met het RIVM heeft de Inspectie voor de Gezondheidszorg (IGZ) een digitale vragenlijst ontwikkeld die bestond uit drie delen (zie Vragenlijst
Antwoorden CRO-vragenlijst - foto van het veld In samenwerking met het RIVM heeft de Inspectie voor de Gezondheidszorg (IGZ) een digitale vragenlijst ontwikkeld die bestond uit drie delen (zie Vragenlijst
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U7 Ondersteunende diensten Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: U7 Ondersteunende diensten Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Toezicht op kwaliteitsborging: ken uw verantwoordelijkheden
 Toezicht op kwaliteitsborging: ken uw verantwoordelijkheden Elysée Hille Karina van Wonderen namens deelteam Klinisch Onderzoek-GCP Afdeling Farmaceutische Bedrijven Workshop Kwaliteitsbewaking door samenwerking
Toezicht op kwaliteitsborging: ken uw verantwoordelijkheden Elysée Hille Karina van Wonderen namens deelteam Klinisch Onderzoek-GCP Afdeling Farmaceutische Bedrijven Workshop Kwaliteitsbewaking door samenwerking
Patiënteninformatieformulier imprint studie
 Patiënteninformatieformulier imprint studie (imaging of PSMA: Registratie en Inventarisatie voor Nederlandse Toepassing) Inleiding Uw arts heeft voorgesteld een aanvraag te doen voor een PSMA-PET-scan.
Patiënteninformatieformulier imprint studie (imaging of PSMA: Registratie en Inventarisatie voor Nederlandse Toepassing) Inleiding Uw arts heeft voorgesteld een aanvraag te doen voor een PSMA-PET-scan.
Aanmelden medischwetenschappelijk
 Aanmelden medischwetenschappelijk onderzoek SOP Aanmelden WMO-plichtig onderzoek_versie juli 2016.doc Pagina 1 van 10 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd
Aanmelden medischwetenschappelijk onderzoek SOP Aanmelden WMO-plichtig onderzoek_versie juli 2016.doc Pagina 1 van 10 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd
Werkinstructies adverse events rapportage STOP-BPD studie
 Werkinstructies adverse events rapportage STOP-BPD studie De STOP-BPD studie wordt uitgevoerd bij extreem prematuur geboren kinderen die los van deelname aan de studie een continu verhoogd risico hebben
Werkinstructies adverse events rapportage STOP-BPD studie De STOP-BPD studie wordt uitgevoerd bij extreem prematuur geboren kinderen die los van deelname aan de studie een continu verhoogd risico hebben
Kwaliteitsborging onderzoek in het. NVMETC bijeenkomst 23 november UMC Utrecht. Oktober 2016
 1 Kwaliteitsborging onderzoek in het UMC Utrecht NVMETC bijeenkomst 23 november 2016 Eugenie Ram, kwaliteitsmanager Onderzoek - Office Concernstaf Raad van Bestuur Oktober 2016 UMC Utrecht breed kwaliteitssysteem
1 Kwaliteitsborging onderzoek in het UMC Utrecht NVMETC bijeenkomst 23 november 2016 Eugenie Ram, kwaliteitsmanager Onderzoek - Office Concernstaf Raad van Bestuur Oktober 2016 UMC Utrecht breed kwaliteitssysteem
NVvOD Privacy Enquête - antwoorden
 NVvOD Privacy Enquête - antwoorden Gegevens opvragen: 1) a) Welke identificerende gegevens gebruik je in interne e-mail correspondentie met artsen en collega s? Ziekenhuis registratienummer Geboortedatum
NVvOD Privacy Enquête - antwoorden Gegevens opvragen: 1) a) Welke identificerende gegevens gebruik je in interne e-mail correspondentie met artsen en collega s? Ziekenhuis registratienummer Geboortedatum
Recente ontwikkelingen in de ethische normen voor medisch-wetenschappelijk onderzoek
 Recente ontwikkelingen in de ethische normen voor medisch-wetenschappelijk onderzoek Prof dr JJM van Delden Julius Centrum, UMC Utrecht j.j.m.vandelden@umcutrecht.nl Inleiding Medisch-wetenschappelijk
Recente ontwikkelingen in de ethische normen voor medisch-wetenschappelijk onderzoek Prof dr JJM van Delden Julius Centrum, UMC Utrecht j.j.m.vandelden@umcutrecht.nl Inleiding Medisch-wetenschappelijk
Klinische studies. Veel meer dan een extra tube
 Klinische studies Veel meer dan een extra tube Good Clinical Practice Het geheel van kwaliteitseisen op ethisch en wetenschappelijk gebied, die internationaal zijn erkend en moeten worden gerespecteerd
Klinische studies Veel meer dan een extra tube Good Clinical Practice Het geheel van kwaliteitseisen op ethisch en wetenschappelijk gebied, die internationaal zijn erkend en moeten worden gerespecteerd
Informatiebrief voor de deelnemers aan experimenten
 Informatiebrief voor de deelnemers aan experimenten 1 Titel van de studie: ETPOS : Een Studie over het Europese Transfusiebeleid en de mogelijke geassocieerde verwikkelingen Een evaluatie van het transfusiebeleid
Informatiebrief voor de deelnemers aan experimenten 1 Titel van de studie: ETPOS : Een Studie over het Europese Transfusiebeleid en de mogelijke geassocieerde verwikkelingen Een evaluatie van het transfusiebeleid
ALGEMENE INFORMATIE Versie 1.8
 ALGEMENE INFORMATIE Donders Centre for Cognition In deze folder komen zaken aan de orde die u beslist moet weten alvorens u kunt deelnemen aan een onderzoek in het Donders Centre for Cognition van het
ALGEMENE INFORMATIE Donders Centre for Cognition In deze folder komen zaken aan de orde die u beslist moet weten alvorens u kunt deelnemen aan een onderzoek in het Donders Centre for Cognition van het
RISK BASED MONITORING IIS FROM AN ACADEMIC PERSPECTIVE; SURGICAL SPECIALTIES
 RISK BASED MONITORING IIS FROM AN ACADEMIC PERSPECTIVE; SURGICAL SPECIALTIES 8 Oktober 2014, DCTF Onderzoeksbureau Divisie Heelkundige Specialismen UMC Utrecht Marianne van Es-Gulinck, arts, F.F.P.M. RISK
RISK BASED MONITORING IIS FROM AN ACADEMIC PERSPECTIVE; SURGICAL SPECIALTIES 8 Oktober 2014, DCTF Onderzoeksbureau Divisie Heelkundige Specialismen UMC Utrecht Marianne van Es-Gulinck, arts, F.F.P.M. RISK
1. Inloggen. 1.1 Eerste keer inloggen
 . Inloggen LET OP: Deze handleiding beschrijft data invoer voor de RACOST studie in de studie-database. Deze database is niet geschikt voor testdoeleinden. Als u de handelingen uit deze handleiding wilt
. Inloggen LET OP: Deze handleiding beschrijft data invoer voor de RACOST studie in de studie-database. Deze database is niet geschikt voor testdoeleinden. Als u de handelingen uit deze handleiding wilt
Aanmelden WMO-plichtig onderzoek
 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd wordt bij het aanmelden van onderzoek dat onder de WMO valt en waarbij ZGV optreedt als deelnemend centrum. Voordat
Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd wordt bij het aanmelden van onderzoek dat onder de WMO valt en waarbij ZGV optreedt als deelnemend centrum. Voordat
Veel gestelde vragen Medisch-wetenschappelijk onderzoek met medische hulpmiddelen 1
 Veel gestelde vragen Medisch-wetenschappelijk onderzoek met medische hulpmiddelen 1 1. Wat is een medisch hulpmiddel? De wettelijke definitie 2 van een medisch hulpmiddel luidt: Een medisch hulpmiddel
Veel gestelde vragen Medisch-wetenschappelijk onderzoek met medische hulpmiddelen 1 1. Wat is een medisch hulpmiddel? De wettelijke definitie 2 van een medisch hulpmiddel luidt: Een medisch hulpmiddel
Handleiding. Investigational Medicinal Product Dossier (IMPD)
 Handleiding Investigational Medicinal Product Dossier (IMPD) Inhoudsopgave Afkortingen... - 3 - Wat is het IMPD?... - 4 - Beslisschema inhoud IMPD... - 5 - Beschrijving inhoud IMPD... - 6 - Overzicht hoofdstukken
Handleiding Investigational Medicinal Product Dossier (IMPD) Inhoudsopgave Afkortingen... - 3 - Wat is het IMPD?... - 4 - Beslisschema inhoud IMPD... - 5 - Beschrijving inhoud IMPD... - 6 - Overzicht hoofdstukken
SOP aanleveren en afhandelen WMO onderzoek METC Onze Lieve Vrouwe Gasthuis, versie 1, juli
 Aanmelden en afhandelen medisch-wetenschappelijk onderzoek met mensen (WMO-onderzoek) Medisch-ethische toetsingscommissie (METC) Onze Lieve Vrouwe Gasthuis Hieronder treft u aan de procedure van aanmelding
Aanmelden en afhandelen medisch-wetenschappelijk onderzoek met mensen (WMO-onderzoek) Medisch-ethische toetsingscommissie (METC) Onze Lieve Vrouwe Gasthuis Hieronder treft u aan de procedure van aanmelding
Aanvraagformulier REGISTRATIE CENTRAAL ONCOLOGIE DATAMANAGER GEGEVENS AANVRAGER
 GEGEVENS AANVRAGER Naam + Voorletters Voorna(a)m(en) Adres Postcode + Woonplaats Geboortedatum Geboorteplaats E-mailadres/telefoon Lidmaatschapsnummer NVvOD geen lid Datum preregistratie CDM Werkervaring
GEGEVENS AANVRAGER Naam + Voorletters Voorna(a)m(en) Adres Postcode + Woonplaats Geboortedatum Geboorteplaats E-mailadres/telefoon Lidmaatschapsnummer NVvOD geen lid Datum preregistratie CDM Werkervaring
Gecertificeerde opleiding voor alle klinisch onderzoekers
 Gecertificeerde opleiding voor alle klinisch onderzoekers Joep Rijnierse, Medical Director Amgen namens Werkgroep Verbetering R&D klimaat DCTF workshop Oktober 2012 Uitdaging Uitdaging Oplossing - Patiëntgebonden
Gecertificeerde opleiding voor alle klinisch onderzoekers Joep Rijnierse, Medical Director Amgen namens Werkgroep Verbetering R&D klimaat DCTF workshop Oktober 2012 Uitdaging Uitdaging Oplossing - Patiëntgebonden
Clinical Trials in Nederland: op weg naar topkwaliteit DCTF Congres 3 oktober 2012 Lunteren. M.P.W. Lamberti, BA Algemeen Directeur
 Clinical Trials in Nederland: op weg naar topkwaliteit DCTF Congres 3 oktober 2012 Lunteren M.P.W. Lamberti, BA Algemeen Directeur Maastricht UMC-Holding MUMC-Holding CTCM BPCM MI Groningen Utrecht Nijmegen
Clinical Trials in Nederland: op weg naar topkwaliteit DCTF Congres 3 oktober 2012 Lunteren M.P.W. Lamberti, BA Algemeen Directeur Maastricht UMC-Holding MUMC-Holding CTCM BPCM MI Groningen Utrecht Nijmegen
Vragen en antwoorden over de gegevenssectie van de model-pif
 Vragen en antwoorden over de gegevenssectie van de model-pif Algemene informatie over de Algemene Verordening Gegevensbescherming Waar vind ik algemene informatie over de gevolgen van de Algemene Verordening
Vragen en antwoorden over de gegevenssectie van de model-pif Algemene informatie over de Algemene Verordening Gegevensbescherming Waar vind ik algemene informatie over de gevolgen van de Algemene Verordening
Checklist voor het indienen van onderzoek bij de CE Communicatiewetenschap Versie 10 januari 2012
 voor Afdeling Communicatiewetenschap Checklist voor het indienen van onderzoek bij de CE Communicatiewetenschap Versie 10 januari 2012 Lees voor het invullen van deze checklist het document Procedure voor
voor Afdeling Communicatiewetenschap Checklist voor het indienen van onderzoek bij de CE Communicatiewetenschap Versie 10 januari 2012 Lees voor het invullen van deze checklist het document Procedure voor
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U6 Studie medicatie Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: U6 Studie medicatie Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Data invoer instructies OpenClinica
 Data invoer instructies OpenClinica TRUTH studie Inhoudsopgave Contactgegevens... 1 Introductie... 1 Legenda pictogrammen... 1 Inloggen... 2 Proefpersoon toevoegen... 2 Data invoeren... 2 Failed Validation
Data invoer instructies OpenClinica TRUTH studie Inhoudsopgave Contactgegevens... 1 Introductie... 1 Legenda pictogrammen... 1 Inloggen... 2 Proefpersoon toevoegen... 2 Data invoeren... 2 Failed Validation
Kwaliteit borgen wij samen! Monitoren van studies in het ziekenhuis door onderzoekers zelf
 Kwaliteit borgen wij samen! Monitoren van studies in het ziekenhuis door onderzoekers zelf Noortje Koppelman, Adviseur Opleiding & Ontwikkeling Olivier Wegelin, AIOS PhD-student DCTF-congres 5 oktober
Kwaliteit borgen wij samen! Monitoren van studies in het ziekenhuis door onderzoekers zelf Noortje Koppelman, Adviseur Opleiding & Ontwikkeling Olivier Wegelin, AIOS PhD-student DCTF-congres 5 oktober
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik
 EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
Patiënten Informatie Folder
 Patiënten Informatie Folder imprint studie OZBS62.15245 Patiënten Informatie Folder imprint studie (imaging of PSMA: Registratie en Inventarisatie voor Nederlandse Toepassing) Inleiding Uw arts heeft voorgesteld
Patiënten Informatie Folder imprint studie OZBS62.15245 Patiënten Informatie Folder imprint studie (imaging of PSMA: Registratie en Inventarisatie voor Nederlandse Toepassing) Inleiding Uw arts heeft voorgesteld
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk. De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak Officiële titel: De rol van endoscopische echografie
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak Officiële titel: De rol van endoscopische echografie
CRO s kwaliteit en toegevoegde waarde
 CRO s kwaliteit en toegevoegde waarde dr. Annejet P. Meijler Programmadirecteur Geneesmiddelen IGZ 1 Medisch-wetenschappelijk onderzoek 4 april 2011 Deze workshop Inleiding I prof. Herman Pieterse Inleiding
CRO s kwaliteit en toegevoegde waarde dr. Annejet P. Meijler Programmadirecteur Geneesmiddelen IGZ 1 Medisch-wetenschappelijk onderzoek 4 april 2011 Deze workshop Inleiding I prof. Herman Pieterse Inleiding
nee nee nee Wordt proefpersoon aan handelingen onderworpen of gedragswijze opgelegd?
 Medischwetenschappelijk onderzoek en deelname proefpersonen? Wordt proefpersoon aan handelingen onderworpen of gedragswijze opgelegd? Worden behandelingen met elkaar via randomisatie vergeleken? Vallen
Medischwetenschappelijk onderzoek en deelname proefpersonen? Wordt proefpersoon aan handelingen onderworpen of gedragswijze opgelegd? Worden behandelingen met elkaar via randomisatie vergeleken? Vallen
Geachte MR CLEAN-Registry onderzoeker,
 Geachte MR CLEAN-Registry onderzoeker, Dank u zeer voor het aanmelden van een patiënt voor de MRCLEAN-Registry. Mocht u vragen hebben of onduidelijkheden kunt u onder kantooruren bellen met de MRCLEAN-Registry
Geachte MR CLEAN-Registry onderzoeker, Dank u zeer voor het aanmelden van een patiënt voor de MRCLEAN-Registry. Mocht u vragen hebben of onduidelijkheden kunt u onder kantooruren bellen met de MRCLEAN-Registry
Kwaliteitsborging Geneesmiddelenonderzoek UMC Utrecht Jaarverslag 2007 Bureau Kwaliteitsborging Onderzoek
 Kwaliteitsborging Geneesmiddelenonderzoek UMC Utrecht Jaarverslag 2007 Bureau Kwaliteitsborging Onderzoek UMC Utrecht Julius Centrum voor Gezondheidswetenschappen en Eerstelijns Geneeskunde Clinical Trial
Kwaliteitsborging Geneesmiddelenonderzoek UMC Utrecht Jaarverslag 2007 Bureau Kwaliteitsborging Onderzoek UMC Utrecht Julius Centrum voor Gezondheidswetenschappen en Eerstelijns Geneeskunde Clinical Trial
Waar draait het om bij de METC? Yvonne Donselaar
 Waar draait het om bij de METC? Yvonne Donselaar Yvonne Donselaar METC AMC Waarom dit verhaal? details naar de geest proefpersoon grote lijnen naar de letter naleven van regels Axel Munthe (1857 1949):
Waar draait het om bij de METC? Yvonne Donselaar Yvonne Donselaar METC AMC Waarom dit verhaal? details naar de geest proefpersoon grote lijnen naar de letter naleven van regels Axel Munthe (1857 1949):
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
SEMINAR 4 NOVEMBER 2014
 SEMINAR 4 NOVEMBER 2014 Professioneel opzetten en uitvoeren van klinisch onderzoek www.deresearchmanager.nl Striksteeg 7 7411 KR Deventer 0570 594 789 info@deresearchmanager.nl Ontwikkeling Afdeling Innovatie
SEMINAR 4 NOVEMBER 2014 Professioneel opzetten en uitvoeren van klinisch onderzoek www.deresearchmanager.nl Striksteeg 7 7411 KR Deventer 0570 594 789 info@deresearchmanager.nl Ontwikkeling Afdeling Innovatie
Case Report Form (CRF) behorende bij de SASIV-study
 Case Report Form (CRF) behorende bij de SASIV-study Inclusiecriteria 0 70 jaar of ouder 0 Acute opgenomen op de longgeneeskunde of chirurgie 0 Spreekt en verstaat Nederlands 0 Komt niet van andere afdeling
Case Report Form (CRF) behorende bij de SASIV-study Inclusiecriteria 0 70 jaar of ouder 0 Acute opgenomen op de longgeneeskunde of chirurgie 0 Spreekt en verstaat Nederlands 0 Komt niet van andere afdeling
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Prospectieve registratie studie voor de diagnose en behandeling van borstkanker tijdens zwangerschap (BOOG ) PATIENTENINFORMATIE
 Prospectieve registratie studie voor de diagnose en behandeling van borstkanker tijdens zwangerschap (BOOG 2003-04) PATIENTENINFORMATIE Geachte mevrouw, Uw behandelend arts heeft u geïnformeerd over bovengenoemd
Prospectieve registratie studie voor de diagnose en behandeling van borstkanker tijdens zwangerschap (BOOG 2003-04) PATIENTENINFORMATIE Geachte mevrouw, Uw behandelend arts heeft u geïnformeerd over bovengenoemd
ALGEMENE INFORMATIE Versie 2.1. Donders Centre for Cognition
 ALGEMENE INFORMATIE Versie 2.1 Donders Centre for Cognition In deze folder komen zaken aan de orde die u beslist moet weten alvorens u kunt deelnemen aan een onderzoek in het Donders Centre for Cognition
ALGEMENE INFORMATIE Versie 2.1 Donders Centre for Cognition In deze folder komen zaken aan de orde die u beslist moet weten alvorens u kunt deelnemen aan een onderzoek in het Donders Centre for Cognition
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk. De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak Officiële titel: De rol van endoscopische echografie
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak Officiële titel: De rol van endoscopische echografie
Toezicht op uitvoering kan beter. Aanbevelingen uit rapport Toezicht op Medisch Wetenschappelijk Onderzoek met mensen
 Toezicht op uitvoering kan beter Aanbevelingen uit rapport Toezicht op Medisch Wetenschappelijk Onderzoek met mensen Najaarsbijeenkomst NVMETC 25 november 2015 Kor Grit, Jacqueline van Oijen 2 Inhoud presentatie
Toezicht op uitvoering kan beter Aanbevelingen uit rapport Toezicht op Medisch Wetenschappelijk Onderzoek met mensen Najaarsbijeenkomst NVMETC 25 november 2015 Kor Grit, Jacqueline van Oijen 2 Inhoud presentatie
Klinische studies: wetgeving in de EU en België en de implicaties ervan op de praktijk
 Klinische studies: wetgeving in de EU en België en de implicaties ervan op de praktijk Katelijne De Nys Inleiding - Richtlijnen en wetgeving in historisch perspectief De Europese Directive De Belgische
Klinische studies: wetgeving in de EU en België en de implicaties ervan op de praktijk Katelijne De Nys Inleiding - Richtlijnen en wetgeving in historisch perspectief De Europese Directive De Belgische
AMC Uitvoeringsrichtlijnen: Goedkeuring medisch-wetenschappelijk onderzoek door de Raad van Bestuur
 AMC Uitvoeringsrichtlijnen: Goedkeuring medisch-wetenschappelijk onderzoek door de Raad van Bestuur en Deelname van personeelsleden en studenten aan medisch-wetenschappelijk onderzoek Versie 1.1 Dit document
AMC Uitvoeringsrichtlijnen: Goedkeuring medisch-wetenschappelijk onderzoek door de Raad van Bestuur en Deelname van personeelsleden en studenten aan medisch-wetenschappelijk onderzoek Versie 1.1 Dit document
 ------------------------------------------------------------------------------------------------------------------------------------------- Concept Procedure Lokale Haalbaarheid klinisch geneesmiddelenonderzoek
------------------------------------------------------------------------------------------------------------------------------------------- Concept Procedure Lokale Haalbaarheid klinisch geneesmiddelenonderzoek
Inhoud onderzoeksdossier
 Inhoud onderzoeksdossier (documenten in de witte box zijn nodig voor de primaire beoordeling) A. Brieven B. Formulieren C. Onderzoeksprotocol en protocolamendementen D. Productinformatie E. Informatie
Inhoud onderzoeksdossier (documenten in de witte box zijn nodig voor de primaire beoordeling) A. Brieven B. Formulieren C. Onderzoeksprotocol en protocolamendementen D. Productinformatie E. Informatie
PATIENTENINFORMATIE EN TOESTEMMINGFORMULIER. Register voor Neuro-endocriene Digestieve Tumoren D.N.E.T.
 PATIENTENINFORMATIE EN TOESTEMMINGFORMULIER Register voor Neuro-endocriene Digestieve Tumoren D.N.E.T. Inleiding De Belgian Group of Digestive Oncology (BGDO) wenst een register samen te stellen waarin
PATIENTENINFORMATIE EN TOESTEMMINGFORMULIER Register voor Neuro-endocriene Digestieve Tumoren D.N.E.T. Inleiding De Belgian Group of Digestive Oncology (BGDO) wenst een register samen te stellen waarin
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
KWALITEITSHANDBOEK WETENSCHAPSBELEID KENNEMER GASTHUIS EN SPAARNE ZIEKENHUIS. Organisatie en richtlijnen medisch-wetenschappelijk onderzoek
 KWALITEITSHANDBOEK WETENSCHAPSBELEID KENNEMER GASTHUIS EN SPAARNE ZIEKENHUIS Organisatie en richtlijnen medisch-wetenschappelijk onderzoek april 2014 Inhoudsopgave 1. INLEIDING 1.1. Organisatie wetenschap
KWALITEITSHANDBOEK WETENSCHAPSBELEID KENNEMER GASTHUIS EN SPAARNE ZIEKENHUIS Organisatie en richtlijnen medisch-wetenschappelijk onderzoek april 2014 Inhoudsopgave 1. INLEIDING 1.1. Organisatie wetenschap
WAAROM MAG IEDEREEN ZICH CRA NOEMEN?
 WAAROM MAG IEDEREEN ZICH CRA NOEMEN? Geen keurmerk voor een goede CRA, geen kaders voor kwaliteitsbewaking Op dit moment stelt niemand nascholing verplicht voor ervaren CRA s 1 PROFESSIONEEL KLINISCH ONDERZOEK
WAAROM MAG IEDEREEN ZICH CRA NOEMEN? Geen keurmerk voor een goede CRA, geen kaders voor kwaliteitsbewaking Op dit moment stelt niemand nascholing verplicht voor ervaren CRA s 1 PROFESSIONEEL KLINISCH ONDERZOEK
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Observationeel onderzoek van de BioMimics 3D-stent bij de behandeling van perifeer vaatlijden Officiële titel: Een prospectief,
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Observationeel onderzoek van de BioMimics 3D-stent bij de behandeling van perifeer vaatlijden Officiële titel: Een prospectief,
Titel van het onderzoek: Bepaling van Zink en het Ontstekingseiwit PTX3 bij Patiënten met Sikkelcelziekte (ZIP studie)
 INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR PATIËNTEN Titel van het onderzoek: Bepaling van Zink en het Ontstekingseiwit PTX3 bij Patiënten met Sikkelcelziekte () Geachte heer/mevrouw, Wij vragen u om
INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR PATIËNTEN Titel van het onderzoek: Bepaling van Zink en het Ontstekingseiwit PTX3 bij Patiënten met Sikkelcelziekte () Geachte heer/mevrouw, Wij vragen u om
Dit onderzoek wordt uitgevoerd en gefinancierd door Acerta (een farmaceutisch bedrijf).
 Titel: Een gerandomiseerd, multicenter, open-label, fase 3-onderzoek naar de nietinferioriteit van ACP-196 versus Ibrutinib bij eerder behandelde proefpersonen met hoog-risico chronische lymfatische leukemie
Titel: Een gerandomiseerd, multicenter, open-label, fase 3-onderzoek naar de nietinferioriteit van ACP-196 versus Ibrutinib bij eerder behandelde proefpersonen met hoog-risico chronische lymfatische leukemie
KLINISCH GENEESMIDDELEN- ONDERZOEK
 KLINISCH GENEESMIDDELEN- ONDERZOEK HET PROCES VAN HET OPSTARTEN VAN KLINISCH ONDERZOEK MET GENEESMIDDELEN GAAT VERANDEREN De ECTR verandert het klinisch onderzoek met geneesmiddelen in Europa. Dit heeft
KLINISCH GENEESMIDDELEN- ONDERZOEK HET PROCES VAN HET OPSTARTEN VAN KLINISCH ONDERZOEK MET GENEESMIDDELEN GAAT VERANDEREN De ECTR verandert het klinisch onderzoek met geneesmiddelen in Europa. Dit heeft
