Standard Operating Procedure
|
|
|
- Katrien van der Woude
- 8 jaren geleden
- Aantal bezoeken:
Transcriptie
1 Standard Operating Procedure STZ SOP: U5 Datamanagement Distributielijst : STZ Datum : Revisiedatum : Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum Opmerkingen Jaarlijkse revisie en administratieve wijzigingen Versiedatum Pagina 1 van 7
2 1. Doel Het bewerkstelligen van uniformiteit in het registreren van de gegevens op en het omgaan met een CRF. 2. Afkortingen, definities en termen CCMO CRF METC ICH-GCP SOP WMO Centrale Commissie Mensgeboden Onderzoek Case Report Form Medisch Ethische Toetsingscommissie International Conference on Harmonisation Standard Operating Procedure Wet Medisch-wetenschappelijk Onderzoek met mensen Audit trail: (digitale) documentatie die volledige reconstructie van het verloop van de gebeurtenissen vóór, tijdens en na uitvoer van het onderzoek mogelijk maakt. Brondocumentatie: Dit zijn documenten die individuele of collectieve evaluatie van de uitvoeringswijze van het onderzoeksprotocol mogelijk maken en mede de kwaliteit van de data verbeteren dan wel waarborgen. Dat zijn o.a. originele documenten, gegevens en registraties (bv. ziekenhuisdossiers, klinische en administratieve grafieken, laboratoriumaantekeningen, memoranda, dagboeken of evaluatielijsten van proefpersonen, uitgifteregistratie van de apotheek, vastgelegde gegevens van geautomatiseerde instrumenten, kopieën of afschriften die gewaarmerkt zijn nadat is vastgesteld dat het exacte kopieën zijn, microfiches, negatieven, microfilm of magnetische media, röntgenfoto s, dossiers van proefpersonen, en gegevens die bewaard worden in de apotheek, in laboratoria en op medisch-technische afdelingen die bij het klinisch onderzoek betrokken zijn) waarvan geen eerdere geschreven of elektronisch vastgelegde gegevens bestaan. Brondocumenten blijven te allen tijde op de onderzoekssite aanwezig. Case Report Form: een gedrukt, optisch of elektronisch document dat ontworpen is om alle volgens het protocol vereiste informatie die per proefpersoon aan de sponsor/verrichter moet worden gerapporteerd. Data-entry: Het invoeren en verwerken van gegevens vanuit (hand) geschreven formulieren en andere documenten zodat het digitaal opgeslagen en gebruikt kan worden. Data-validatie: proces waarbij gecontroleerd wordt of de informatie in de database volledig, consistent en plausibel is. Investigator / onderzoeker: De persoon die verantwoordelijk is voor de uitvoering van een klinisch onderzoek op één onderzoekslocatie. De onderzoeker die landelijk verantwoordelijk is voor de studie wordt de CCI (country co-ordinating investigator) genoemd. Als een klinisch onderzoek op één onderzoekslocatie door één team van personen wordt uitgevoerd dan is de onderzoeker de verantwoordelijke teamleider en kan deze als hoofdonderzoeker (principal investigator; PI) worden aangeduid. Investigator Site File: een hoofddossier voor alle Essentiële documenten (ICH-GCP Richtsnoer Hoofdstuk 8) dat aangelegd dient te worden aan het begin van elk onderzoek en dat aanwezig moet zijn zowel op de locatie van het onderzoek/instelling als ten kantore van de sponsor (dat kan dezelfde locatie zijn wanneer de sponsor tevens de hoofdonderzoeker is). METC: Een zelfstandig en onafhankelijk bestuursorgaan (instellings-, regionale, nationale of supranationale beoordelingsraad of commissie), bestaande uit medici, wetenschappers en niet-medici/wetenschappers, dat de verantwoordelijkheid heeft er voor te zorgen dat de rechten, veiligheid en het welzijn van de proefpersonen in een onderzoek worden zeker gesteld. Deze bescherming moet openbaar worden gewaarborgd door onder andere het beoordelen van en een positief oordeel geven over het onderzoeksprotocol, de geschiktheid van de onderzoekers, de faciliteiten en de methoden en het materiaal dat zal worden gebruikt om het informed consent van de proefpersonen te verkrijgen en te documenteren. Onderzoekslocatie: De locatie(s) waar onderzoeksactiviteiten plaatsvinden. Versiedatum Pagina 2 van 7
3 Protocol: Een document waarin doelstelling(en), opzet, methodologie, statistische overwegingen en organisatie van een onderzoek staan beschreven. Het protocol beschrijft doorgaans ook de achtergrond van en de verantwoording voor het onderzoeksproject, maar deze kunnen ook in de andere documenten, waarnaar in het protocol wordt verwezen, zijn opgenomen. In het ICH GCP richtsnoer verwijst de term protocol zowel naar protocol als naar protocolamendementen. Query: vraag die schriftelijk wordt gesteld naar aanleiding van onduidelijkheden in het CRF door de sponsor of datamanager van een studie. Deze Query pagina s hebben dezelfde status als een CRF pagina. Waar over CRF pagina s wordt geschreven kan ook query pagina s gelezen worden. Standard Operating Procedure (SOP): Dit zijn gedetailleerde schriftelijke instructies om uniformiteit te bereiken in de uitvoering van een bepaalde taak. Sponsor/verrichter: Een persoon, bedrijf, instelling of organisatie die de verantwoordelijkheid neemt voor het initiëren, organiseren en/of financieren van een klinisch onderzoek. In de WMO spreekt men van verrichter als zijnde diegene die opdracht heeft gegeven voor de organisatie en/of uitvoering van een klinisch onderzoek. 3. Verantwoordelijkheden Hieronder worden de verantwoordelijkheden van de verschillende partijen met betrekking tot deze STZ SOP U5 Datamanagement beschreven. Investigator is eindverantwoordelijk voor: het beschikbaar hebben van een CRF; het correct invullen en up to date houden van het CRF; d.w.z. nauwkeurig, leesbaar en tijdig gerapporteerd; het beschikbaar hebben van brondocumenten; het verklaren van afwijkingen van de brondocumenten; verandering/correctie in het CRF voorzien van datum en paraaf van degene die de verandering/correctie heeft gemaakt; overigens mag dit de oorspronkelijke tekst niet onleesbaar maken. Indien het een elektronisch CRF (e-crf) betreft zullen de wijzigingen moeten worden opgeslagen in de Audit trail incl. datum van wijziging, oorspronkelijke waarde van het veld en de persoon die de wijziging heeft doorgevoerd. Sponsor / verrichter is eindverantwoordelijk voor: het beschikbaar stellen van een CRF aan de onderzoeker bij aanvang van de studie; geven van instructies hoe het CRF gehanteerd moet worden; opstellen van invulinstructies voor het CRF. Versiedatum Pagina 3 van 7
4 4. Stroomdiagram 5.1 CRF aanwezig? nee 5.2 Ontwikkelen Case report form STZ SOP VC3 ja 5.3 Gedurende studie invoeren van patiëntgegevens volgens instructies (data-entry) 5.4 Zorg voor datavalidatie en compleet CRF ja nee 5.5 Data validatie compleet? ja 5.6 Database lock 5.7 Database heropenen nee Start dataverwerking STZ SOP A3 5.8 CRF pagina s archiveren volgens instructies Versiedatum Pagina 4 van 7
5 5. Werkwijze 5.1. Om het verzamelen van de (medische) gegevens voor de studie geordend te doen, wordt er vaak een CRF gemaakt. In dit CRF kan er per bezoek van de proefpersoon ingevuld worden welke gegevens verzameld zijn. De gegevens die in een CRF worden genoteerd zijn altijd overgenomen uit brondocumentatie. Een CRF geeft ook houvast aan wat er per bezoek nagegaan moet worden. Een CRF kan een papieren boek of losbladig systeem zijn maar ook elektronisch. Een elektronisch CRF geeft vaak meteen een query of bladert niet verder als gegevens missen of incorrect worden ingevoerd CRF zelf maken: zie STZ SOP VC3 Ontwikkelen Case Report Form (CRF) 5.3. Bij het invoeren en verwerken van gegevens in het CRF wordt gebruik gemaakt van algemene invulinstructies en onderzoek specifieke invulinstructies zoals opgesteld door de sponsor (zie ook STZ SOP VC3 Ontwikkelen Case Report Form (CRF) ). Het invoeren van de gegevens gebeurt door de investigator of door de investigator geautoriseerd personeel. Invulinstructies CRF Algemeen: Voor verschillende CRFs kunnen specifieke instructies gegeven worden voor het invullen en managen van het CRF. Algemene instructies die altijd gelden zijn: Vul alle gegevens in daarvoor bestemde vakjes in. Alleen opmerkingen buiten de vakken indien daarom gevraagd wordt; Schrijf leesbaar en in geval van NCR papier (zelfkopiërend papier) gebruik een blauwe of zwarte balpen; Gebruik een standaard datumaanduiding: bv. DD-MM-YYYY; Papieren CRF: Verbeter fouten als volgt: doorhalen van foute antwoord met een streep zodat het wel leesbaar blijft, vul het goede antwoord in evt. met verklaring, zet datum en paraaf erbij. Bv. Dr. H. Janssen meet een bloeddruk 168/95 en vult onderdruk in i.p.v. bovendruk, dus 95/95. In CRF bloeddruk: 95, 168, , HJ. Indien het een e-crf betreft zullen de wijzigingen moeten worden opgeslagen in de Audit trail incl. datum van wijziging, oorspronkelijke waarde van het veld en de persoon die de wijziging heeft doorgevoerd; Gebruik NOOIT correctievloeistof (zoals Tipp-ex); Indien een vraag niet van toepassing is invullen: N.V.T. of N.A. (= not applicable); Indien een onderzoek niet gedaan is invullen: N.D. (= not done); Indien een vraag niet te beantwoorden is invullen: UNK (= unknown); Indien een resultaat nul is dan invullen: 0. In het geval van papieren CRF s kan het origineel exemplaar van het CRF naar de sponsor gaan voor verdere verwerking (data-entry in een elektronisch systeem en data validatie). Een kopie/doordruk blijft achter of moet gemaakt worden voordat originelen verzonden worden Data validatie vindt plaats op de onderzoekslocatie of bij de sponsor. In het geval van ontbrekende of inconsistente/niet plausibele gegevens zal de investigator gevraagd worden om de gegevens te verifiëren met de brondocumenten. In het geval van ontbrekende of foutieve informatie kan worden volstaan met het wijzigen van de data in het CRF. In alle andere gevallen kan worden volstaan met een verklaring van de investigator. Deze verklaring moet worden bewaard bij de studie documentatie (in het geval van een elektronisch CRF zal dit veelal rechtstreeks worden opgeslagen in de database). Gedurende de looptijd van de studie zal er in veel gevallen gemonitord worden (zie ook STZ SOP U9 Monitoren ). Er zal dan gevraagd worden het CRF klaar te hebben. D.w.z. ingevuld, gevalideerd en (evt. elektronisch) ondertekend door de investigator. Versiedatum Pagina 5 van 7
6 Ga voor het einde van de studie na of alle (van toepassing zijnde) CRF pagina s zijn ingevuld gevalideerd en gemonitord (indien van toepassing). Indien dat het geval is kan het CRF worden gearchiveerd, zie paragraaf 5.6. Indien dit niet het geval is, zie paragraaf Indien nog niet alle data gevalideerd en gemonitord (indien van toepassing) zijn zorg dan dat dit eerst in orde komt daarna kan er gearchiveerd worden Als de gegevens voldoen aan de voor de studie vastgestelde kwaliteitsnorm, sluit de sponsor de studiedatabase, de database lock. Na database lock vindt indien van toepassing deblindering plaats De database kan weer geopend worden als aanvullende informatie vanuit de sponsor of investigator dat vereist, waarbij de argumentatie voor heropening wordt vastgelegd (op papier of in de database). Uiteindelijk moeten ook dan alle veranderingen worden gevalideerd en de database gesloten zoals boven beschreven In de instructies van de sponsor staat vaak aangegeven wat te doen met de volledig ingevulde CRF pagina s. Volg deze instructies. Zie ook de STZ SOP A2 Archiveren studie. 6. Archivering De volgende documenten dienen gearchiveerd te worden in de Investigator site file (zie STZ SOP VL4 Investigator Site File ): ingevulde, getekende en van een datum voorziene CRF (op de onderzoekslocatie alleen kopie); documentatie van correcties in het CRF (kan ook elektronisch aanwezig zijn: audit trail); verklaring investigator in geval van ontbrekende, inconsistente en niet plausibele data; argumentatie heropening na database lock (sponsor file). 7. Referenties Richtsnoer voor Good Clinical Practice (CPMP/ICH/135/95), officiële Nederlandse vertaling Wet Medisch-wetenschappelijk Onderzoek met mensen STZ SOP VC3: Ontwikkelen Case Report Form (CRF) STZ SOP VL4: Investigator Site File STZ SOP U9: Monitoren STZ SOP A2: Archiveren studie 8. Literatuur Richtsnoer voor Good Clinical Practice (CPMP/ICH/135/95), officiële Nederlandse vertaling Website van de CCMO ( 9. Bijlage(n) n.v.t. 10. MGG specifiek Wanneer een MGG onderzoeker zelf een onderzoek initieert, dient de onderzoeker zelf een CRF te maken. Zie STZ SOP VC3 Ontwikkelen Case Report Form (CRF). Wanneer een onderzoek elders is geïnitieerd zijn er vaak algemene invulinstructies opgesteld door de verrichter. Wanneer het onderzoek zelf is geïnitieerd dient de MGG onderzoeker deze op te stellen. Versiedatum Pagina 6 van 7
7 Een onderzoeker kan een deel van deze verantwoordelijkheden delegeren. Bij het delegeren van deeltaken dient rekening gehouden te worden met de aard van het onderzoek en de kwalificaties van diegenen aan wie verantwoordelijkheden worden gedelegeerd. Versiedatum Pagina 7 van 7
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U10 Audit Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: U10 Audit Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum Opmerkingen
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U4 Registratie /randomisatie procedure Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum
Standard Operating Procedure STZ SOP: U4 Registratie /randomisatie procedure Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U1 Identificatie, werving en pre-screening proefpersonen Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure STZ SOP: U1 Identificatie, werving en pre-screening proefpersonen Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U9 Monitoren Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies Versiedatum Hoofdstuk Versiedatum Hoofdstuk
Standard Operating Procedure STZ SOP: U9 Monitoren Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies Versiedatum Hoofdstuk Versiedatum Hoofdstuk
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL2 Aanpassen proefpersoneninformatie / toestemmingsformulier aan lokale situatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen
Standard Operating Procedure STZ SOP: VL2 Aanpassen proefpersoneninformatie / toestemmingsformulier aan lokale situatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U11 Voortgangsrapportage Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: U11 Voortgangsrapportage Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VC8 Beoordeling amendement toetsende commissie (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure STZ SOP: VC8 Beoordeling amendement toetsende commissie (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL5 Protocolamendement (lokaal) Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: VL5 Protocolamendement (lokaal) Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VC9 Proefpersonen- en aansprakelijkheidsverzekering (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure STZ SOP: VC9 Proefpersonen- en aansprakelijkheidsverzekering (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A2 Archiveren studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A2 Archiveren studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure
 Standard Operating Procedure SOP: V9 Initiatievisite Auteur Naam: Functie instelling/afdeling Judie van den Elshout Staffunctionaris Wetenschapsbureau Wetenschapsbureau / Cluster Leerhuis Handtekening:...
Standard Operating Procedure SOP: V9 Initiatievisite Auteur Naam: Functie instelling/afdeling Judie van den Elshout Staffunctionaris Wetenschapsbureau Wetenschapsbureau / Cluster Leerhuis Handtekening:...
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: O3 Ontwikkelen, implementeren en beheren van SOP s Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies
Standard Operating Procedure STZ SOP: O3 Ontwikkelen, implementeren en beheren van SOP s Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A4 Publicatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A4 Publicatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A1 Afsluiting studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A1 Afsluiting studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U2 Informed consent Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: U2 Informed consent Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U7 Ondersteunende diensten Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: U7 Ondersteunende diensten Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U6 Studie medicatie Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: U6 Studie medicatie Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U8 Melding van (Serious) Adverse Events en SUSARs Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies
Standard Operating Procedure STZ SOP: U8 Melding van (Serious) Adverse Events en SUSARs Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL4 Investigator Site File Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: VL4 Investigator Site File Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
IC ICF ICH ISF. Lijst met afkortingen, definities en termen STZ-Kwaliteitshandboek SOP s
 Lijst met afkortingen, definities en termen STZ-Kwaliteitshandboek SOP s ABR ADR AE AR BROK CCMO CRF CTA CV DSMB EMEA EU EudraCT FU brief GCP GMP IB IC ICF ICH IMPD ISF MEB METC EU RCT SAE SOP SPC SUSAR
Lijst met afkortingen, definities en termen STZ-Kwaliteitshandboek SOP s ABR ADR AE AR BROK CCMO CRF CTA CV DSMB EMEA EU EudraCT FU brief GCP GMP IB IC ICF ICH IMPD ISF MEB METC EU RCT SAE SOP SPC SUSAR
Aanmelden medischwetenschappelijk
 Aanmelden medischwetenschappelijk onderzoek SOP Aanmelden WMO-plichtig onderzoek_versie juli 2016.doc Pagina 1 van 10 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd
Aanmelden medischwetenschappelijk onderzoek SOP Aanmelden WMO-plichtig onderzoek_versie juli 2016.doc Pagina 1 van 10 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd
Aanmelden WMO-plichtig onderzoek
 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd wordt bij het aanmelden van onderzoek dat onder de WMO valt en waarbij ZGV optreedt als deelnemend centrum. Voordat
Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd wordt bij het aanmelden van onderzoek dat onder de WMO valt en waarbij ZGV optreedt als deelnemend centrum. Voordat
1. Voorafgaand aan de klinische fase van het onderzoek
 Essentiële documenten Bron: Richtsnoer voor good clinical practice (CPMP/ICH/135/95) De verwijzingen in dit document verwijzen naar de artikelen in bovenstaand document. 1. Voorafgaand aan de klinische
Essentiële documenten Bron: Richtsnoer voor good clinical practice (CPMP/ICH/135/95) De verwijzingen in dit document verwijzen naar de artikelen in bovenstaand document. 1. Voorafgaand aan de klinische
Monitorplan voorbeeld
 Monitorplan voorbeeld Protocol Er moet in het protocol beschreven worden dat er monitoring plaatsvindt (zie ook CCMO voorbeeld template). Het monitoringplan mag als bijlage worden toegevoegd (in dat geval
Monitorplan voorbeeld Protocol Er moet in het protocol beschreven worden dat er monitoring plaatsvindt (zie ook CCMO voorbeeld template). Het monitoringplan mag als bijlage worden toegevoegd (in dat geval
Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen
 Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen Afdeling Farmaceutische Bedrijven, Klinisch Onderzoek Good Clinical Practice Inhoud Wat doet de IGJ aan toezicht op klinisch
Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen Afdeling Farmaceutische Bedrijven, Klinisch Onderzoek Good Clinical Practice Inhoud Wat doet de IGJ aan toezicht op klinisch
Titel: Good Clinical Practice & Monitoring. Initiation Investigator Driven Studies. Versie: 14-jan-2013
 Titel: Good Clinical Practice & Monitoring Initiation Investigator Driven Studies Inhoud Wet- en regelgeving/declaration of Helsinki Good Clinical Practice Patiënteninformatie/ informed consent Basisvereisten
Titel: Good Clinical Practice & Monitoring Initiation Investigator Driven Studies Inhoud Wet- en regelgeving/declaration of Helsinki Good Clinical Practice Patiënteninformatie/ informed consent Basisvereisten
Aanvraagformulier REGISTRATIE oncologie monitor
 Aanvraagformulier REGISTRATIE oncologie monitor 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:... Geboorteplaats:... Werkzaam bij: Organisatie + Afdeling:...
Aanvraagformulier REGISTRATIE oncologie monitor 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:... Geboorteplaats:... Werkzaam bij: Organisatie + Afdeling:...
29 juni Initiatie bijeenkomst PORTEC 4. Kwaliteitsborging WMO GCP richtsnoer. Frank van Leeuwen IKNL
 29 juni 2012 Initiatie bijeenkomst PORTEC 4 Kwaliteitsborging WMO GCP richtsnoer Frank van Leeuwen IKNL Wet en regelgeving Verklaring van Helsinki Richtsnoer voor Good Clinical Practice (CPMP/ICH/135/95)
29 juni 2012 Initiatie bijeenkomst PORTEC 4 Kwaliteitsborging WMO GCP richtsnoer Frank van Leeuwen IKNL Wet en regelgeving Verklaring van Helsinki Richtsnoer voor Good Clinical Practice (CPMP/ICH/135/95)
Site selectie visite checklist
 Site selectie visite checklist Informatie sponsor: Naam sponsor: Contactpersoon: Functie: Afdeling: Telefoonnummer : Email : Informatie onderzoekslocatie: Naam onderzoekslocatie : Naam onderzoeker: Functie:
Site selectie visite checklist Informatie sponsor: Naam sponsor: Contactpersoon: Functie: Afdeling: Telefoonnummer : Email : Informatie onderzoekslocatie: Naam onderzoekslocatie : Naam onderzoeker: Functie:
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VC2 Ontwikkelen proefpersoneninformatie / toestemmingsformulier (centraal) Distributielijst : STZ Datum : 18-02-2014 Revisiedatum : 18-02-2015 Veranderingen ten opzichte
Standard Operating Procedure STZ SOP: VC2 Ontwikkelen proefpersoneninformatie / toestemmingsformulier (centraal) Distributielijst : STZ Datum : 18-02-2014 Revisiedatum : 18-02-2015 Veranderingen ten opzichte
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen. Farmaceutische Bedrijven Deelteam Klinisch Onderzoek
 Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
Toezicht op kwaliteitsborging: ken uw verantwoordelijkheden
 Toezicht op kwaliteitsborging: ken uw verantwoordelijkheden Elysée Hille Karina van Wonderen namens deelteam Klinisch Onderzoek-GCP Afdeling Farmaceutische Bedrijven Workshop Kwaliteitsbewaking door samenwerking
Toezicht op kwaliteitsborging: ken uw verantwoordelijkheden Elysée Hille Karina van Wonderen namens deelteam Klinisch Onderzoek-GCP Afdeling Farmaceutische Bedrijven Workshop Kwaliteitsbewaking door samenwerking
De rol van de Contract Research Organisatie (CRO) Klinisch onderzoek
 De rol van de Contract Research Organisatie (CRO) in klinisch geneesmiddelenonderzoek Klinisch onderzoek Inhoud Aanleiding CRO project Methode en resultaten» Werkwijze en resultaten foto van het veld vragenlijst»
De rol van de Contract Research Organisatie (CRO) in klinisch geneesmiddelenonderzoek Klinisch onderzoek Inhoud Aanleiding CRO project Methode en resultaten» Werkwijze en resultaten foto van het veld vragenlijst»
Gedigitaliseerd onderzoek..
 Gedigitaliseerd onderzoek.. ITC Validation Consultants an extra measure of Quality Frans Leijse Managing Director GSK Global QA-eCompliance Manager Adviseurs voor.. GxP compliance van ICT Systemen Computer
Gedigitaliseerd onderzoek.. ITC Validation Consultants an extra measure of Quality Frans Leijse Managing Director GSK Global QA-eCompliance Manager Adviseurs voor.. GxP compliance van ICT Systemen Computer
INFORMATIEBLAD. Maart 2011
 INFORMATIEBLAD AANMELDING TRIALBUREAU/DATACENTRUM Maart 2011 Kanker zo snel mogelijk terugdringen en onder controle brengen. We zijn er voor mensen die leven met kanker en de mensen die met hen samenleven.
INFORMATIEBLAD AANMELDING TRIALBUREAU/DATACENTRUM Maart 2011 Kanker zo snel mogelijk terugdringen en onder controle brengen. We zijn er voor mensen die leven met kanker en de mensen die met hen samenleven.
Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) Team Klinisch Onderzoek
 Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) 2014-2016 Team Klinisch Onderzoek Toezicht op IIT 2014-2016 Aanleiding en werkwijze Bevindingen vanuit de praktijk Conclusies en aandachtspunten
Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) 2014-2016 Team Klinisch Onderzoek Toezicht op IIT 2014-2016 Aanleiding en werkwijze Bevindingen vanuit de praktijk Conclusies en aandachtspunten
Antwoorden CRO-vragenlijst - foto van het veld
 Antwoorden CRO-vragenlijst - foto van het veld In samenwerking met het RIVM heeft de Inspectie voor de Gezondheidszorg (IGZ) een digitale vragenlijst ontwikkeld die bestond uit drie delen (zie Vragenlijst
Antwoorden CRO-vragenlijst - foto van het veld In samenwerking met het RIVM heeft de Inspectie voor de Gezondheidszorg (IGZ) een digitale vragenlijst ontwikkeld die bestond uit drie delen (zie Vragenlijst
Aanvraagformulier REGISTRATIE CENTRAAL ONCOLOGIE DATAMANAGER GEGEVENS AANVRAGER
 GEGEVENS AANVRAGER Naam + Voorletters Voorna(a)m(en) Adres Postcode + Woonplaats Geboortedatum Geboorteplaats E-mailadres/telefoon Lidmaatschapsnummer NVvOD geen lid Datum preregistratie CDM Werkervaring
GEGEVENS AANVRAGER Naam + Voorletters Voorna(a)m(en) Adres Postcode + Woonplaats Geboortedatum Geboorteplaats E-mailadres/telefoon Lidmaatschapsnummer NVvOD geen lid Datum preregistratie CDM Werkervaring
Het Clinical Research Bureau (CRB) van VUmc
 1 Het Clinical Research Bureau (CRB) van VUmc Angela Vlug Kwaliteitsborging van mensgebonden onderzoek 1 Het Clinical Research Bureau heeft als doel om optimale kwaliteit van de uitvoering van mensgebonden
1 Het Clinical Research Bureau (CRB) van VUmc Angela Vlug Kwaliteitsborging van mensgebonden onderzoek 1 Het Clinical Research Bureau heeft als doel om optimale kwaliteit van de uitvoering van mensgebonden
Data invoer instructies OpenClinica
 Data invoer instructies OpenClinica TRUTH studie Inhoudsopgave Contactgegevens... 1 Introductie... 1 Legenda pictogrammen... 1 Inloggen... 2 Proefpersoon toevoegen... 2 Data invoeren... 2 Failed Validation
Data invoer instructies OpenClinica TRUTH studie Inhoudsopgave Contactgegevens... 1 Introductie... 1 Legenda pictogrammen... 1 Inloggen... 2 Proefpersoon toevoegen... 2 Data invoeren... 2 Failed Validation
1. Inloggen. 1.1 Eerste keer inloggen
 . Inloggen LET OP: Deze handleiding beschrijft data invoer voor de RACOST studie in de studie-database. Deze database is niet geschikt voor testdoeleinden. Als u de handelingen uit deze handleiding wilt
. Inloggen LET OP: Deze handleiding beschrijft data invoer voor de RACOST studie in de studie-database. Deze database is niet geschikt voor testdoeleinden. Als u de handelingen uit deze handleiding wilt
Monitoren vs auditen. CRA dag 21 april 2016
 Monitoren vs auditen CRA dag 21 april 2016 Introductie Freelance consultant, mede oprichter TAPAS Group B.V. Mede oprichter/directeur van CRA B.V. Medical Adviser Yamanouchi Pharma Clinical trial monitor
Monitoren vs auditen CRA dag 21 april 2016 Introductie Freelance consultant, mede oprichter TAPAS Group B.V. Mede oprichter/directeur van CRA B.V. Medical Adviser Yamanouchi Pharma Clinical trial monitor
SOP aanleveren en afhandelen WMO onderzoek METC Onze Lieve Vrouwe Gasthuis, versie 1, juli
 Aanmelden en afhandelen medisch-wetenschappelijk onderzoek met mensen (WMO-onderzoek) Medisch-ethische toetsingscommissie (METC) Onze Lieve Vrouwe Gasthuis Hieronder treft u aan de procedure van aanmelding
Aanmelden en afhandelen medisch-wetenschappelijk onderzoek met mensen (WMO-onderzoek) Medisch-ethische toetsingscommissie (METC) Onze Lieve Vrouwe Gasthuis Hieronder treft u aan de procedure van aanmelding
Aanvraagformulier REGISTRATIE oncologie datamanager
 Aanvraagformulier REGISTRATIE oncologie datamanager 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:.... Geboorteplaats:.... Werkzaam bij: Organisatie +
Aanvraagformulier REGISTRATIE oncologie datamanager 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:.... Geboorteplaats:.... Werkzaam bij: Organisatie +
1. Beschrijving werkgebieden / thema s
 1. Beschrijving werkgebieden / thema s Nr 1 Thema Wetenschappelijke Achtergrond en Opzet van Onderzoek 2 Ethische en veiligheid overwegingen 3 Ontwikkeling en Regelgeving 4 Clinical Trial Operations (Projectorganisatie)
1. Beschrijving werkgebieden / thema s Nr 1 Thema Wetenschappelijke Achtergrond en Opzet van Onderzoek 2 Ethische en veiligheid overwegingen 3 Ontwikkeling en Regelgeving 4 Clinical Trial Operations (Projectorganisatie)
Kwaliteitsborging onderzoek in het. NVMETC bijeenkomst 23 november UMC Utrecht. Oktober 2016
 1 Kwaliteitsborging onderzoek in het UMC Utrecht NVMETC bijeenkomst 23 november 2016 Eugenie Ram, kwaliteitsmanager Onderzoek - Office Concernstaf Raad van Bestuur Oktober 2016 UMC Utrecht breed kwaliteitssysteem
1 Kwaliteitsborging onderzoek in het UMC Utrecht NVMETC bijeenkomst 23 november 2016 Eugenie Ram, kwaliteitsmanager Onderzoek - Office Concernstaf Raad van Bestuur Oktober 2016 UMC Utrecht breed kwaliteitssysteem
Toezicht op IIT: bevindingen vanuit de praktijk
 Toezicht op IIT: bevindingen vanuit de praktijk Elysée Hille, senior inspecteur namens deelteam KO-GCP Teamcoördinator KO-GCP/PhV/GZH Afdeling Farmaceutische Bedrijven Wat doet de IGZ? Toezicht op klinisch
Toezicht op IIT: bevindingen vanuit de praktijk Elysée Hille, senior inspecteur namens deelteam KO-GCP Teamcoördinator KO-GCP/PhV/GZH Afdeling Farmaceutische Bedrijven Wat doet de IGZ? Toezicht op klinisch
Hoofdlijnen van beleid management onderzoeksdata Universiteit voor Humanistiek
 1 november 2016 Hoofdlijnen van beleid management onderzoeksdata Universiteit voor Humanistiek Preambule In deze notitie wordt op hoofdlijnen vastgelegd hoe onderzoeksdata moet worden beheerd. Het is van
1 november 2016 Hoofdlijnen van beleid management onderzoeksdata Universiteit voor Humanistiek Preambule In deze notitie wordt op hoofdlijnen vastgelegd hoe onderzoeksdata moet worden beheerd. Het is van
SOP: Voorlichtingsgesprek en uitgesteld informed consent CONTRAST trials
 SOP: Voorlichtingsgesprek en uitgesteld informed consent CONTRAST trials SOP: IC1 Versie Nr.: 1.1 Geldig m.i.v.: 03-04-2018 Auteur: S.A. van den Berg, arts-onderzoeker AMC Autorisator: Dr. H.B. van der
SOP: Voorlichtingsgesprek en uitgesteld informed consent CONTRAST trials SOP: IC1 Versie Nr.: 1.1 Geldig m.i.v.: 03-04-2018 Auteur: S.A. van den Berg, arts-onderzoeker AMC Autorisator: Dr. H.B. van der
Vragen en antwoorden over de gegevenssectie van de model-pif
 Vragen en antwoorden over de gegevenssectie van de model-pif Algemene informatie over de Algemene Verordening Gegevensbescherming Waar vind ik algemene informatie over de gevolgen van de Algemene Verordening
Vragen en antwoorden over de gegevenssectie van de model-pif Algemene informatie over de Algemene Verordening Gegevensbescherming Waar vind ik algemene informatie over de gevolgen van de Algemene Verordening
GOOD CLINICAL PRACTICE
 INTERNATIONAAL RICHTSNOER VOOR GOOD CLINICAL PRACTICE VOOR HET ONDERZOEK MET GENEESMIDDELEN VERTALING NAAR DE NEDERLANDSE PRAKTIJK eerste versie: september 1993 herziene versie: maart 1995 compleet herziene
INTERNATIONAAL RICHTSNOER VOOR GOOD CLINICAL PRACTICE VOOR HET ONDERZOEK MET GENEESMIDDELEN VERTALING NAAR DE NEDERLANDSE PRAKTIJK eerste versie: september 1993 herziene versie: maart 1995 compleet herziene
AMC Uitvoeringsrichtlijnen: Goedkeuring medisch-wetenschappelijk onderzoek door de Raad van Bestuur
 AMC Uitvoeringsrichtlijnen: Goedkeuring medisch-wetenschappelijk onderzoek door de Raad van Bestuur en Deelname van personeelsleden en studenten aan medisch-wetenschappelijk onderzoek Versie 1.1 Dit document
AMC Uitvoeringsrichtlijnen: Goedkeuring medisch-wetenschappelijk onderzoek door de Raad van Bestuur en Deelname van personeelsleden en studenten aan medisch-wetenschappelijk onderzoek Versie 1.1 Dit document
Kwaliteitssysteem datamanagement. Meetbaar Beter
 Kwaliteitssysteem datamanagement Meetbaar Beter Datum: 20 juli 2017 Versie : 0.10 Kwaliteitssysteem Meetbaar Beter versie 0.10.docx Pagina 1 van 8 Voorwoord Het aantal centra dat is aangesloten bij Meetbaar
Kwaliteitssysteem datamanagement Meetbaar Beter Datum: 20 juli 2017 Versie : 0.10 Kwaliteitssysteem Meetbaar Beter versie 0.10.docx Pagina 1 van 8 Voorwoord Het aantal centra dat is aangesloten bij Meetbaar
Kwaliteitssysteem datamanagement. Meetbaar Beter
 Kwaliteitssysteem datamanagement Meetbaar Beter Datum: 22 maart 2016 Versie : 0.8 Kwaliteitssysteem Meetbaar Beter versie 0.8 Pagina 1 van 8 Voorwoord Het aantal centra dat is aangesloten bij Meetbaar
Kwaliteitssysteem datamanagement Meetbaar Beter Datum: 22 maart 2016 Versie : 0.8 Kwaliteitssysteem Meetbaar Beter versie 0.8 Pagina 1 van 8 Voorwoord Het aantal centra dat is aangesloten bij Meetbaar
Handleiding. Investigational Medicinal Product Dossier (IMPD)
 Handleiding Investigational Medicinal Product Dossier (IMPD) Inhoudsopgave Afkortingen... - 3 - Wat is het IMPD?... - 4 - Beslisschema inhoud IMPD... - 5 - Beschrijving inhoud IMPD... - 6 - Overzicht hoofdstukken
Handleiding Investigational Medicinal Product Dossier (IMPD) Inhoudsopgave Afkortingen... - 3 - Wat is het IMPD?... - 4 - Beslisschema inhoud IMPD... - 5 - Beschrijving inhoud IMPD... - 6 - Overzicht hoofdstukken
Toezicht op klinisch onderzoek - bevindingen vanuit de praktijk
 Toezicht op klinisch onderzoek - bevindingen vanuit de praktijk Namens Deelprogramma Klinisch Onderzoek, IGZ Spreker Dr. ir. J. Eland-Gerritsen Coördinerend/Specialistisch Senior inspecteur Inhoud Toezicht
Toezicht op klinisch onderzoek - bevindingen vanuit de praktijk Namens Deelprogramma Klinisch Onderzoek, IGZ Spreker Dr. ir. J. Eland-Gerritsen Coördinerend/Specialistisch Senior inspecteur Inhoud Toezicht
Checklist en toelichting indienen WMO amendement uitbreiding centrum
 Checklist en toelichting indienen WMO amendement uitbreiding centrum In onderstaande tabel staan de documenten die u moet indienen als u een amendement uitbreiding centrum wilt laten beoordelen door de
Checklist en toelichting indienen WMO amendement uitbreiding centrum In onderstaande tabel staan de documenten die u moet indienen als u een amendement uitbreiding centrum wilt laten beoordelen door de
Monitoring van Investigator Initiated onderzoek
 Monitoring van Investigator Initiated onderzoek V1.0 Angela Vlug Clinical Research Bureau VUmc Wat is een IIS (volgens de NFU) Onderzoek waarvoor de raad van bestuur van een (universitair) medisch centrum
Monitoring van Investigator Initiated onderzoek V1.0 Angela Vlug Clinical Research Bureau VUmc Wat is een IIS (volgens de NFU) Onderzoek waarvoor de raad van bestuur van een (universitair) medisch centrum
Bijlage I bij het Kaderreglement van het Parelsnoer Initiatief. Handleiding Parelspecifiek reglement
 Bijlage I bij het Kaderreglement van het Parelsnoer Initiatief Handleiding Parelspecifiek reglement Op grond van artikel 4 lid 17 van het Kaderreglement Parelsnoer Initiatief dient per Parel een reglement
Bijlage I bij het Kaderreglement van het Parelsnoer Initiatief Handleiding Parelspecifiek reglement Op grond van artikel 4 lid 17 van het Kaderreglement Parelsnoer Initiatief dient per Parel een reglement
Checklist Lokale Uitvoerbaarheid
 Primaire indieningsproces Lokale Uitvoerbaarheid in METC Management, screening door Assistent Secretaris. Hieronder staan de generieke uitgangspunten en is toegelicht hoe de toetsing indiening Lokale Uitvoerbaarheid
Primaire indieningsproces Lokale Uitvoerbaarheid in METC Management, screening door Assistent Secretaris. Hieronder staan de generieke uitgangspunten en is toegelicht hoe de toetsing indiening Lokale Uitvoerbaarheid
Kwaliteit: Minder is meer
 Kwaliteit: Minder is meer Kwaliteit in klinisch onderzoek met medische hulpmiddelen Jako Pranger QA Manager Cardialysis 9 Nov 2012 Kwaliteit en integriteit Mensgebonden onderzoek Trends in kwaliteitsbeleving
Kwaliteit: Minder is meer Kwaliteit in klinisch onderzoek met medische hulpmiddelen Jako Pranger QA Manager Cardialysis 9 Nov 2012 Kwaliteit en integriteit Mensgebonden onderzoek Trends in kwaliteitsbeleving
BROK staat voor Basiscursus Regelgeving en Organisatie voor Klinisch onderzoekers.
 VEELGESTELDE VRAGEN OVER DE BROK CURSUS Wat is de BROK cursus? BROK staat voor Basiscursus Regelgeving en Organisatie voor Klinisch onderzoekers. Aan de uitvoering van mensgebonden onderzoek worden door
VEELGESTELDE VRAGEN OVER DE BROK CURSUS Wat is de BROK cursus? BROK staat voor Basiscursus Regelgeving en Organisatie voor Klinisch onderzoekers. Aan de uitvoering van mensgebonden onderzoek worden door
WMO-GCP opfriscursus Nederlandse Vereniging voor Oncologie Datamanagers 27 februari 2019
 WMO-GCP opfriscursus Nederlandse Vereniging voor Oncologie Datamanagers 27 februari 2019 Agenda Introductie ICH-GCP R2 AVG Kwaliteitssyteem Informed Consent ISF e-tmf Monitoren SAE rapportage Waarom wetgeving?
WMO-GCP opfriscursus Nederlandse Vereniging voor Oncologie Datamanagers 27 februari 2019 Agenda Introductie ICH-GCP R2 AVG Kwaliteitssyteem Informed Consent ISF e-tmf Monitoren SAE rapportage Waarom wetgeving?
Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek
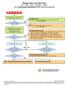 Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek Melding voorval proefpersoon aan onderzoeker/arts 1 Rapportage voorval door onderzoeker/arts in patiëntenstatus
Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek Melding voorval proefpersoon aan onderzoeker/arts 1 Rapportage voorval door onderzoeker/arts in patiëntenstatus
Geachte MR CLEAN-Registry onderzoeker,
 Geachte MR CLEAN-Registry onderzoeker, Dank u zeer voor het aanmelden van een patiënt voor de MRCLEAN-Registry. Mocht u vragen hebben of onduidelijkheden kunt u onder kantooruren bellen met de MRCLEAN-Registry
Geachte MR CLEAN-Registry onderzoeker, Dank u zeer voor het aanmelden van een patiënt voor de MRCLEAN-Registry. Mocht u vragen hebben of onduidelijkheden kunt u onder kantooruren bellen met de MRCLEAN-Registry
5. Goedkeuring deelname door de toetsende METC 6. Start- en einddatum onderzoek 7. Rekening
 Aanleveren documenten voor het uitbrengen van advies over lokale uitvoerbaarheid bij de Medisch-ethische toetsingscommissie (METC) in het Onze Lieve Vrouwe Gasthuis Mocht u nog vragen hebben naar aanleiding
Aanleveren documenten voor het uitbrengen van advies over lokale uitvoerbaarheid bij de Medisch-ethische toetsingscommissie (METC) in het Onze Lieve Vrouwe Gasthuis Mocht u nog vragen hebben naar aanleiding
Voorzitter, vice-voorzitter en secretaris(sen) van de METC Erasmus MC.
 REGLEMENT MEDISCH ETHISCHE TOETSINGS COMMISSIE ERASMUS MC Inleiding Dit reglement geeft, in aanmerking nemende het bepaalde in artikel 16, lid 2, onder b tot en met d van de WMO, voorschriften betreffende
REGLEMENT MEDISCH ETHISCHE TOETSINGS COMMISSIE ERASMUS MC Inleiding Dit reglement geeft, in aanmerking nemende het bepaalde in artikel 16, lid 2, onder b tot en met d van de WMO, voorschriften betreffende
SEMINAR 4 NOVEMBER 2014
 SEMINAR 4 NOVEMBER 2014 Professioneel opzetten en uitvoeren van klinisch onderzoek www.deresearchmanager.nl Striksteeg 7 7411 KR Deventer 0570 594 789 info@deresearchmanager.nl Ontwikkeling Afdeling Innovatie
SEMINAR 4 NOVEMBER 2014 Professioneel opzetten en uitvoeren van klinisch onderzoek www.deresearchmanager.nl Striksteeg 7 7411 KR Deventer 0570 594 789 info@deresearchmanager.nl Ontwikkeling Afdeling Innovatie
Handleiding Goedkeuringsprocedure Raad van Bestuur Zuyderland wetenschappelijk onderzoek
 Handleiding Goedkeuringsprocedure Raad van Bestuur Zuyderland wetenschappelijk onderzoek INLEIDING oor al het onderzoek dat binnen Zuyderland wordt uitgevoerd moet goedkeuring worden verkregen van de Raad
Handleiding Goedkeuringsprocedure Raad van Bestuur Zuyderland wetenschappelijk onderzoek INLEIDING oor al het onderzoek dat binnen Zuyderland wordt uitgevoerd moet goedkeuring worden verkregen van de Raad
Checklist en toelichting indienen Lokale Uitvoerbaarheid
 Checklist en toelichting indienen Lokale Uitvoerbaarheid In onderstaande tabel staan de documenten die u moet indienen als u toestemming wilt van de Raad van Bestuur VUmc voor uitvoering van uw onderzoek
Checklist en toelichting indienen Lokale Uitvoerbaarheid In onderstaande tabel staan de documenten die u moet indienen als u toestemming wilt van de Raad van Bestuur VUmc voor uitvoering van uw onderzoek
Standard Operating Procedure
 Standard Operating Procedure SOP: V1 Ontwikkelen Onderzoeksprotocol Auteur Naam: Functie instelling/afdeling Judie van den Elshout Staffunctionaris Wetenschapsbureau Wetenschapsbureau / Cluster Leerhuis
Standard Operating Procedure SOP: V1 Ontwikkelen Onderzoeksprotocol Auteur Naam: Functie instelling/afdeling Judie van den Elshout Staffunctionaris Wetenschapsbureau Wetenschapsbureau / Cluster Leerhuis
RICHTSNOER VOOR GOOD CLINICAL PRACTICE (CPMP/ICH/135/95)
 RICHTSNOER VOOR GOOD CLINICAL PRACTICE (CPMP/ICH/135/95) Stap 5, vastgesteld richtsnoer 1.5.96 (inclusief errata na Stap 4) ICH Harmonised Tripartite Guideline INHOUDSOPGAVE INHOUDSOPGAVE...i INLEIDING...1
RICHTSNOER VOOR GOOD CLINICAL PRACTICE (CPMP/ICH/135/95) Stap 5, vastgesteld richtsnoer 1.5.96 (inclusief errata na Stap 4) ICH Harmonised Tripartite Guideline INHOUDSOPGAVE INHOUDSOPGAVE...i INLEIDING...1
Checklist en toelichting indienen Lokale Uitvoerbaarheid
 Checklist en toelichting indienen Lokale Uitvoerbaarheid In onderstaande tabel staan de documenten die u moet indienen als u toestemming wilt van de Raad van Bestuur VUmc voor uitvoering van uw onderzoek
Checklist en toelichting indienen Lokale Uitvoerbaarheid In onderstaande tabel staan de documenten die u moet indienen als u toestemming wilt van de Raad van Bestuur VUmc voor uitvoering van uw onderzoek
Kwaliteit borgen wij samen! Monitoren van studies in het ziekenhuis door onderzoekers zelf
 Kwaliteit borgen wij samen! Monitoren van studies in het ziekenhuis door onderzoekers zelf Noortje Koppelman, Adviseur Opleiding & Ontwikkeling Olivier Wegelin, AIOS PhD-student DCTF-congres 5 oktober
Kwaliteit borgen wij samen! Monitoren van studies in het ziekenhuis door onderzoekers zelf Noortje Koppelman, Adviseur Opleiding & Ontwikkeling Olivier Wegelin, AIOS PhD-student DCTF-congres 5 oktober
Inhoud onderzoeksdossier
 Inhoud onderzoeksdossier (documenten in de witte box zijn nodig voor de primaire beoordeling) A. Brieven B. Formulieren C. Onderzoeksprotocol en protocolamendementen D. Productinformatie E. Informatie
Inhoud onderzoeksdossier (documenten in de witte box zijn nodig voor de primaire beoordeling) A. Brieven B. Formulieren C. Onderzoeksprotocol en protocolamendementen D. Productinformatie E. Informatie
Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814.
 STAATSCOURANT Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814. Nr. 20221 17 juli 2015 Regeling van de Minister van Volksgezondheid, Welzijn en Sport van 9 juli 2015, houdende regels voor
STAATSCOURANT Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814. Nr. 20221 17 juli 2015 Regeling van de Minister van Volksgezondheid, Welzijn en Sport van 9 juli 2015, houdende regels voor
Op naar het snel opstarten van klinisch onderzoek in Nederland!
 Op naar het snel opstarten van klinisch onderzoek in Nederland! Marika Trieling Voorzitter DCRF werkgroep Lokale uitvoerbaarheid 12 februari 2019 Wat is er in Nederland nodig? Verkorten tijdslijnen van
Op naar het snel opstarten van klinisch onderzoek in Nederland! Marika Trieling Voorzitter DCRF werkgroep Lokale uitvoerbaarheid 12 februari 2019 Wat is er in Nederland nodig? Verkorten tijdslijnen van
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek
 Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
CCMO Structuur documenten Technische Toetsing (ass.secr.) Inhoudelijke Toetsing (secretaris)
 CHECKLIST WMO Primaire indieningsproces WMO in METC Management, screening door Assistent Secretaris. Hieronder staan de generieke uitgangspunten en is toegelicht hoe de primaire toetsing indiening WMO
CHECKLIST WMO Primaire indieningsproces WMO in METC Management, screening door Assistent Secretaris. Hieronder staan de generieke uitgangspunten en is toegelicht hoe de primaire toetsing indiening WMO
Procedure aanvraag voor het verrichten van wetenschappelijk onderzoek in Meander Medisch Centrum
 Procedure aanvraag voor het verrichten van wetenschappelijk onderzoek in Meander Medisch Centrum Commissie Toetsing Wetenschappelijk Onderzoek (TWO) I II Algemeen 1. Alvorens onderzoek in Meander MC van
Procedure aanvraag voor het verrichten van wetenschappelijk onderzoek in Meander Medisch Centrum Commissie Toetsing Wetenschappelijk Onderzoek (TWO) I II Algemeen 1. Alvorens onderzoek in Meander MC van
Clinical Trials in Nederland: op weg naar topkwaliteit DCTF Congres 3 oktober 2012 Lunteren. M.P.W. Lamberti, BA Algemeen Directeur
 Clinical Trials in Nederland: op weg naar topkwaliteit DCTF Congres 3 oktober 2012 Lunteren M.P.W. Lamberti, BA Algemeen Directeur Maastricht UMC-Holding MUMC-Holding CTCM BPCM MI Groningen Utrecht Nijmegen
Clinical Trials in Nederland: op weg naar topkwaliteit DCTF Congres 3 oktober 2012 Lunteren M.P.W. Lamberti, BA Algemeen Directeur Maastricht UMC-Holding MUMC-Holding CTCM BPCM MI Groningen Utrecht Nijmegen
HOVON 141 CLL. Instructies voor de deelnemende site: ICF studie template aanpassen naar een lokaal biobank ICF
 Instructies voor de deelnemende site: ICF studie template aanpassen naar een lokaal biobank ICF Doel van deze studie template Deze studie template is bestemd voor de deelnemende sites in Nederland van
Instructies voor de deelnemende site: ICF studie template aanpassen naar een lokaal biobank ICF Doel van deze studie template Deze studie template is bestemd voor de deelnemende sites in Nederland van
RISK BASED MONITORING IIS FROM AN ACADEMIC PERSPECTIVE; SURGICAL SPECIALTIES
 RISK BASED MONITORING IIS FROM AN ACADEMIC PERSPECTIVE; SURGICAL SPECIALTIES 8 Oktober 2014, DCTF Onderzoeksbureau Divisie Heelkundige Specialismen UMC Utrecht Marianne van Es-Gulinck, arts, F.F.P.M. RISK
RISK BASED MONITORING IIS FROM AN ACADEMIC PERSPECTIVE; SURGICAL SPECIALTIES 8 Oktober 2014, DCTF Onderzoeksbureau Divisie Heelkundige Specialismen UMC Utrecht Marianne van Es-Gulinck, arts, F.F.P.M. RISK
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik
 EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
VOORBEEL. De expert is verbonden aan mijn vakgroep/instituut. Ik heb samen met een datamanagement expert intern het DMP opgesteld.
 DMP title Project Name Voorbeeld ingevuld DMP 'Analgosedation after cardiac surgery in infants: A "model-based" nation-wide randomized controlled trial' - DMP title Principal Investigator / Researcher
DMP title Project Name Voorbeeld ingevuld DMP 'Analgosedation after cardiac surgery in infants: A "model-based" nation-wide randomized controlled trial' - DMP title Principal Investigator / Researcher
Kwaliteitsborging vanuit academisch perspectief DCTF jaarcongres 2016
 Kwaliteitsborging vanuit academisch perspectief DCTF jaarcongres 2016 Gemma Voss 5 oktober 2016 Mensgebonden onderzoek (WMO) in Nederland 2015 CCMO-jaarverslag 2015 CCMO-jaarverslag 2015 Mensgebonden onderzoek
Kwaliteitsborging vanuit academisch perspectief DCTF jaarcongres 2016 Gemma Voss 5 oktober 2016 Mensgebonden onderzoek (WMO) in Nederland 2015 CCMO-jaarverslag 2015 CCMO-jaarverslag 2015 Mensgebonden onderzoek
DISTRICTS. Case Record Form Baseline meting arts VERTROUWELIJK. Versie 1.7. Contactinformatie: Wijnand Palmbergen, uitvoerend onderzoeker
 Studienummer: Pagina 1 van 10 DISTRICTS Case Record Form Baseline meting arts Versie 1.7 VERTROUWELIJK DISTRICTS studienummer: (wordt gegenereerd) Contactinformatie: Wijnand Palmbergen, uitvoerend onderzoeker
Studienummer: Pagina 1 van 10 DISTRICTS Case Record Form Baseline meting arts Versie 1.7 VERTROUWELIJK DISTRICTS studienummer: (wordt gegenereerd) Contactinformatie: Wijnand Palmbergen, uitvoerend onderzoeker
NAN 2006 Richtlijn 9 Documenten
 NAN 2006 Richtlijn 9 Documenten Versie: 26 februari 2007 Auteur: KNMP/WINAp Leeswijzer richtlijn 9 Deze richtlijn is een uitwerking van hoofdstuk 9 van de NAN 2006 en gaat over het bewaren en vernietigen
NAN 2006 Richtlijn 9 Documenten Versie: 26 februari 2007 Auteur: KNMP/WINAp Leeswijzer richtlijn 9 Deze richtlijn is een uitwerking van hoofdstuk 9 van de NAN 2006 en gaat over het bewaren en vernietigen
CRO s kwaliteit en toegevoegde waarde
 CRO s kwaliteit en toegevoegde waarde dr. Annejet P. Meijler Programmadirecteur Geneesmiddelen IGZ 1 Medisch-wetenschappelijk onderzoek 4 april 2011 Deze workshop Inleiding I prof. Herman Pieterse Inleiding
CRO s kwaliteit en toegevoegde waarde dr. Annejet P. Meijler Programmadirecteur Geneesmiddelen IGZ 1 Medisch-wetenschappelijk onderzoek 4 april 2011 Deze workshop Inleiding I prof. Herman Pieterse Inleiding
HANDLEIDING AANGIFTE BIJ DE PRIVACYCOMMISSIE - Biomedisch onderzoek aan de UGent
 HANDLEIDING AANGIFTE BIJ DE PRIVACYCOMMISSIE - Biomedisch onderzoek aan de UGent Beste UGent onderzoeker, De Privacywet is de Wet van 8 december 1992 voor de bescherming van de persoonlijke levenssfeer
HANDLEIDING AANGIFTE BIJ DE PRIVACYCOMMISSIE - Biomedisch onderzoek aan de UGent Beste UGent onderzoeker, De Privacywet is de Wet van 8 december 1992 voor de bescherming van de persoonlijke levenssfeer
Ervaringen met document X
 Martini Ziekenhuis Groningen Ervaringen met document X Ellen Rusch, wetenschappelijk medewerker Wetenschappelijk Instituut Wat gaan we doen? Structuur lokale haalbaarheid Martini Ziekenhuis Het werken
Martini Ziekenhuis Groningen Ervaringen met document X Ellen Rusch, wetenschappelijk medewerker Wetenschappelijk Instituut Wat gaan we doen? Structuur lokale haalbaarheid Martini Ziekenhuis Het werken
Beheer van niet-conformiteiten, preventieve acties en externe klachten. Inhoudstafel
 P. : 1/5 Opsteller: AM Vanherle Verificateur :P. Cliquet, C.Graide Vertaler : AM Vanherle Goedkeuring Naam Functie Handtekening Datum Goedgekeurd door : H. Van Oyen Operationele directeur 29/08/2012 Inhoudstafel
P. : 1/5 Opsteller: AM Vanherle Verificateur :P. Cliquet, C.Graide Vertaler : AM Vanherle Goedkeuring Naam Functie Handtekening Datum Goedgekeurd door : H. Van Oyen Operationele directeur 29/08/2012 Inhoudstafel
Formulier Datamanagementplan
 Formulier Datamanagementplan NWO is in 2015 gestart met een pilot Datamanagement. Tijdens deze pilot vraagt NWO onderzoekers met toegekende onderzoeksprojecten onderstaand datamanagementplan in te dienen.
Formulier Datamanagementplan NWO is in 2015 gestart met een pilot Datamanagement. Tijdens deze pilot vraagt NWO onderzoekers met toegekende onderzoeksprojecten onderstaand datamanagementplan in te dienen.
9 Documenten. 9.1 t/m 9.3 beheer van documenten. Statusoverzicht. Voorgenomen besluit Bestuursgroep OR. Vastgesteld door Bestuursgroep
 Statusoverzicht. Consultatie 1 Consultatie 2 Voorgenomen besluit Bestuursgroep OR q Instemming q Advies q N.v.t. Vastgesteld door Bestuursgroep N.v.t. N.v.t. Borging. Implementatie m.i.v. Opgenomen in
Statusoverzicht. Consultatie 1 Consultatie 2 Voorgenomen besluit Bestuursgroep OR q Instemming q Advies q N.v.t. Vastgesteld door Bestuursgroep N.v.t. N.v.t. Borging. Implementatie m.i.v. Opgenomen in
NVvOD Privacy Enquête - antwoorden
 NVvOD Privacy Enquête - antwoorden Gegevens opvragen: 1) a) Welke identificerende gegevens gebruik je in interne e-mail correspondentie met artsen en collega s? Ziekenhuis registratienummer Geboortedatum
NVvOD Privacy Enquête - antwoorden Gegevens opvragen: 1) a) Welke identificerende gegevens gebruik je in interne e-mail correspondentie met artsen en collega s? Ziekenhuis registratienummer Geboortedatum
Controle-instructies VeleHanden project Holland Amerika Lijn Passagierslijsten
 Controle-instructies VeleHanden project Holland Amerika Lijn Passagierslijsten Versie 2 11 januari 2019 (aanpassingen t.o.v. vorige versie in rood) De controleur De controleur bepaalt welke invoer de juiste
Controle-instructies VeleHanden project Holland Amerika Lijn Passagierslijsten Versie 2 11 januari 2019 (aanpassingen t.o.v. vorige versie in rood) De controleur De controleur bepaalt welke invoer de juiste
Praktisch: Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis. Procedure niet-wmo-plichtig klinisch wetenschappelijk onderzoek
 Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure niet-wmo-plichtig klinisch wetenschappelijk onderzoek Deze procedure geldt voor niet-wmo-plichtig onderzoek dat of: a) enkel
Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure niet-wmo-plichtig klinisch wetenschappelijk onderzoek Deze procedure geldt voor niet-wmo-plichtig onderzoek dat of: a) enkel
Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis. Procedure niet-wmo-plichtig klinisch wetenschappelijk onderzoek
 Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure niet-wmo-plichtig klinisch wetenschappelijk onderzoek Deze procedure geldt voor niet-wmo-plichtig onderzoek dat of: a) enkel
Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure niet-wmo-plichtig klinisch wetenschappelijk onderzoek Deze procedure geldt voor niet-wmo-plichtig onderzoek dat of: a) enkel
Klinische studies. Veel meer dan een extra tube
 Klinische studies Veel meer dan een extra tube Good Clinical Practice Het geheel van kwaliteitseisen op ethisch en wetenschappelijk gebied, die internationaal zijn erkend en moeten worden gerespecteerd
Klinische studies Veel meer dan een extra tube Good Clinical Practice Het geheel van kwaliteitseisen op ethisch en wetenschappelijk gebied, die internationaal zijn erkend en moeten worden gerespecteerd
