Klinisch onderzoek beter mogelijk met een EPD. Prof. Dr. H. Pieterse Profess Medical Consultancy Voorzitter NVMA 3 juni 2010
|
|
|
- Thijmen ten Wolde
- 8 jaren geleden
- Aantal bezoeken:
Transcriptie
1 1 Klinisch onderzoek beter mogelijk met een EPD Prof. Dr. H. Pieterse Profess Medical Consultancy Voorzitter NVMA 3 juni 2010
2 Agenda 2 Aan welke wettelijke eisen moet mensgebonden onderzoek in Nederland voldoen? Hoe test je de betrouwbaarheid van de resultaten? Hoe kan ik daarbij het EPD als brondocument gebruiken? Aan welke eisen moet het EPD dan voldoen?
3 Soorten onderzoek 3 Interventie onderzoek Observationeel onderzoek (niet-wmo plichtig) Bevolkingsonderzoek Onderzoek met embryo s, foetussen, geslachtscellen
4 Soorten interventie onderzoek 4 Geneesmiddelen Medische hulpmiddelen Voedingssupplementen Chirurgische technieken Gedrags- en psychologisch onderzoek Waarbij handeling wordt verricht of gedragswijze beinvloed Interviews en enquetes Waarbij handeling wordt verricht of gedragswijze beinvloed
5 Regelgeving relaties bij Onderzoek 5 Laboratorium Proefpersoon WBP Apotheker Medische Administratie WGBO KWZ Directie Ziekenhuis WBP WGBO ICH GCP WMO WMO WBP WMO ICH GCP Onderzoeker ICH GCP KWZ KWZ WBIG WMO METC WMO ICH GCP AWB WMO WBP WBP ICH GCP WOG BBA Sponsor Centrale Commissie
6 Wettelijke eisen voor onderzoek 6 Wet Medisch Wetenschappelijk Onderzoek met Mensen Geneesmiddelenwet ICH Good Clinical Practice Guideline WGBO WBP
7 Rode draad 7 Zorgvuldig handelen Geloofwaardig handelen Verantwoording afleggen Transparantie Consistentie
8 Sponsor initiates study Study starts Investigator records all observations in CRF and in source documents Study completed experimentally Study protocol draft Appoint monitor Select investigator(s) Perform feasibility study Manufacture study medication Design and implement SOP s Appoint coordinating clinical investigator Quality and train sponsor personnel Make/update Investigator s Drug Brochure (IB) Design study protocol Discuss and include statistics in protocol Documents Submitted to aec and CA Regulatory and technical green lights obtained All essential documents obtained Perform Monitoring Visits Monitor: Check completeness Check accuracy Check consistency Check procedures Verify filing Check reliability by conducting SDV Verify drug accountability Report Adverse Events Start data entry and validation Investigator: Report Serious Adverse Event immediately Sponsor: Submit reportable events (SUSARs) to the MEB Report SUSARs to aec and other investigators Study data analyzed Data management starts when completed CRF becomes available: Perform data validation (queries) Arrange Data Review Meeting Close database Study documents final Instruct, train and qualify investigators Label and pack materials Make overall project plan (time, resources) Arrange for submission to aec Make cost budget Notify study to CCMO/Minister Design Case Report Form Finalize investigator contracts Prepare study monitoring forms Finalize third party contracts Prepare instruction manuals Randomize study treatment Design patient information and consent Arrange start up meetings Arrange for insurance coverage Design database Design data validation plan Design Statistical Analysis plan Quality Assurance: Independent auditing prior to, during and after study for investigational site and monitoring activities Study report finalized Write statistical report Write integrated study report Send summary of report to investigators, CCMO and aec Study documents: IB, study protocol CV s investigators List centres aec approval CCMO notification Investigator agreement Insurance certificate Patient info, consent CRF Forms AE, ADE Monitor contact info Version nr. 1.0 NL version date 04-Jun-2004 Copyright Profess Sponsor responsibilities: Sign approved study protocol Ensure that all deviations from protocol are reported and accounted for Ensure that all AE s are reported as required Inform all investigators about all SAE s Inform investigator when study is terminated prematurely or suspended Inform investigators on development status drug Review and approve deviations from study protocol Collect, store, keep secured and ensure completion of essential documents Monitor responsibilities: Verify if compliance with protocol is maintained Verify if drug is used according to plan Verify qualification of investigational staff Verify if investigator has access to adequate number of subjects Verify if informed consents are properly signed and dated Verify if AE have been recorded and reported adequately Verify drug accountability and traceability Verify maintenance and calibration equipment Verify recording subject withdrawal, non-compliance Report monitoring visits Investigator responsibilities: Have resources to conduct study Has no conflict of interest Knows the drug and its properties Knows the study protocol Supports the monitor and auditor Communicates deviations from the protocol Ensures compliance with protocol for all staff Protects health and welfare of subjects Communicates with the aec on SAE s, submission amendments Endeavors to ensure adequate recruitment Ensures that informed consent is obtained and documented Reports any deviation due to emergency Ensures drug accountability
9 Initiatiefase-1 9 Sponsor initiates study Appoint monitor Select investigator(s) Perform feasibility study Manufacture study medication Design and implement SOP s Appoint coordinating clinical investigator Qualify and train sponsor personnel Make/update Investigator s Drug Brochure (IB) Make/update Investigational Medicinal Product Dossier (IMPD) Design study protocol Discuss and include statistics in protocol
10 Interne voorbereidingsfase-1 10 Study protocol draft Instruct, train and qualify investigators Make overall project plan (time, resources) Make cost budget Design Case Report Form Prepare study monitoring forms Prepare instruction manuals Design patient information and consent Arrange for insurance coverage Study documents final
11 In te dienen documenten-1 11 Study documents final Essential documents to be submitted For details see 2.3 Prepare other relevant documents like: Study forms Monitoring guidelines SAE form Monitor contact reports Documents Submitted to aec and CA
12 Externe voorbereidingsfase-1 12 Study documents final Documents Submitted to aec+ccmo Label and pack materials Arrange for submission to aec Notify study to CCMO/Minister or arrange for approval in case of gene therapy Finalize investigator contracts Finalize third party contracts Randomize study treatment Arrange start up meetings Design database Design data validation plan Design Statistical Analysis plan
13 Groen licht-1 13 Documents Submitted to aec+ccmo Regulatory and technical green lights obtained All essential documents obtained Study starts
14 Uitvoeringsfase-2 14 Study starts Investigator records all observations in CRF and in source documents Study completed experimentally Perform Monitoring Visits Monitor: Check completeness Check accuracy Check consistency Check procedures Check reliability by conducting SDV Verify filing Verify drug accountability
15 Uitvoeringsfase 15 Study starts Investigator records all observations in CRF and in source documents Study completed experimentally Start data entry and validation
16 Analyse fase 16 Study completed experimentally Data management starts when completed CRF becomes available: Perform data validation (queries) Arrange Data Review Meeting Close database Study data analyzed
17 Rapportage fase 17 Study data analyzed Write statistical report Write integrated study report Send summary of report to investigators, CCMO and aec Study report finalized
18 Sponsor initiates study Study starts Investigator records all observations in CRF and in source documents Study completed experimentally Study protocol draft Appoint monitor Select investigator(s) Perform feasibility study Manufacture study medication Design and implement SOP s Appoint coordinating clinical investigator Quality and train sponsor personnel Make/update Investigator s Drug Brochure (IB) Design study protocol Discuss and include statistics in protocol Documents Submitted to aec and CA Regulatory and technical green lights obtained All essential documents obtained Perform Monitoring Visits Monitor: Check completeness Check accuracy Check consistency Check procedures Verify filing Check reliability by conducting SDV Verify drug accountability Report Adverse Events Start data entry and validation Investigator: Report Serious Adverse Event immediately Sponsor: Submit reportable events (SUSARs) to the MEB Report SUSARs to aec and other investigators Study data analyzed Data management starts when completed CRF becomes available: Perform data validation (queries) Arrange Data Review Meeting Close database Study documents final Instruct, train and qualify investigators Label and pack materials Make overall project plan (time, resources) Arrange for submission to aec Make cost budget Notify study to CCMO/Minister Design Case Report Form Finalize investigator contracts Prepare study monitoring forms Finalize third party contracts Prepare instruction manuals Randomize study treatment Design patient information and consent Arrange start up meetings Arrange for insurance coverage Design database Design data validation plan Design Statistical Analysis plan Quality Assurance: Independent auditing prior to, during and after study for investigational site and monitoring activities Study report finalized Write statistical report Write integrated study report Send summary of report to investigators, CCMO and aec Study documents: IB, study protocol CV s investigators List centres aec approval CCMO notification Investigator agreement Insurance certificate Patient info, consent CRF Forms AE, ADE Monitor contact info Version nr. 1.0 NL version date 04-Jun-2004 Copyright Profess Sponsor responsibilities: Sign approved study protocol Ensure that all deviations from protocol are reported and accounted for Ensure that all AE s are reported as required Inform all investigators about all SAE s Inform investigator when study is terminated prematurely or suspended Inform investigators on development status drug Review and approve deviations from study protocol Collect, store, keep secured and ensure completion of essential documents Monitor responsibilities: Verify if compliance with protocol is maintained Verify if drug is used according to plan Verify qualification of investigational staff Verify if investigator has access to adequate number of subjects Verify if informed consents are properly signed and dated Verify if AE have been recorded and reported adequately Verify drug accountability and traceability Verify maintenance and calibration equipment Verify recording subject withdrawal, non-compliance Report monitoring visits Investigator responsibilities: Have resources to conduct study Has no conflict of interest Knows the drug and its properties Knows the study protocol Supports the monitor and auditor Communicates deviations from the protocol Ensures compliance with protocol for all staff Protects health and welfare of subjects Communicates with the aec on SAE s, submission amendments Endeavors to ensure adequate recruitment Ensures that informed consent is obtained and documented Reports any deviation due to emergency Ensures drug accountability
19 Betrouwbaarheid toetsen 19 Verificatie tegen de brongegevens (ICH GCP 5.18) Representatieve steekproef door monitor Check validatie van computersystemen (ICH GCP 5.5.3) Systeem voldoet aan eisen gebruiker (acceptance testing) Ontwikkeling van systeem conform state of the art model (V-model) Procedures zijn beschreven voor alle taken en verantwoordelijkheden
20 Resultaten registeren 20 De onderzoeksgegevens worden op een verzamelformulier vastgelegd Case Report Form
21 Gegevens verwerking 21 Data verifiëren met medisch dossier/epd Data invoeren in gevalideerde software systeem (data management plan) Data schonen (data validatie plan) Data analyseren (statistisch analyse plan) Data rapporteren (studie rapport en publicatie)
22 lab results ECGs CRF s Het data handling proces kluis 1. Data invoer DB1 controle & 2. in-house medical review Kluis 3. SAS checks query query query 4. data validatie Onderzoeker inconsistenties? query query query NEE JA 5. schone database 8. statistische analyse 6. data acceptatie bijeenkomst 9. statistisch rapport 7. database bevriezen
23 23
24 Betrouwbaarheid toetsen 24 Check validatie van computersystemen (ICH GCP 5.5.3) Logging procedure (audit trail) Beveiligingssysteem Lijst met bevoegden Backup en restoring faciliteiten
25 EPD als betrouwbare bron 25 EPD wordt robuust gebouwd (V-model) In EPD is een logging procedure vereist Geen ongeoorloofde wijzigingen Geen misbruik van gegevens Geen wijziging door onbevoegden Voor WMO plichtig onderzoek (interventie onderzoek) Toegang tot EPD (inzage) voor derden geregeld met toestemming van patiënt
26 EPD als betrouwbare bron 26 Voor niet-wmo plichtig onderzoek (observationeel onderzoek) toestemming voor inzage door derden als gegevens herleidbaar zijn tot de natuurlijke persoon Inzage voor derden procedure vastleggen conform procedures beveiliging
27 Validatie van het EPD 27 Acceptatiecriteria voor opdrachtgevers van onderzoek Zijn de procedures beschreven? Is het systeem volgens V-model ontwikkeld? Is de beveiliging van het systeem geregeld? Is er een logging procedure die werkt? Is de backup en restoring geregeld? Is de elektronische handtekening gevalideerd?
28 28
29 Toekomst 29 Een zorgvuldig en betrouwbaar EPD is essentieel voor mensgebonden onderzoek om te zorgen dat
30 Toekomst 30 Kosten kunnen worden bespaard op data management (voorkomen van dubbele invoer en de vele controles die plaatsvinden) Human factors worden gunstig beïnvloed (velen hebben een pesthekel aan alle bureaucratie!) Kwaliteit zal met sprongen stijgen, want alle gegevens worden goed vastgelegd aan de basis en kunnen voor vele doeleinden worden ingezet
31 31 V r a g en?
nee nee nee Wordt proefpersoon aan handelingen onderworpen of gedragswijze opgelegd?
 Medischwetenschappelijk onderzoek en deelname proefpersonen? Wordt proefpersoon aan handelingen onderworpen of gedragswijze opgelegd? Worden behandelingen met elkaar via randomisatie vergeleken? Vallen
Medischwetenschappelijk onderzoek en deelname proefpersonen? Wordt proefpersoon aan handelingen onderworpen of gedragswijze opgelegd? Worden behandelingen met elkaar via randomisatie vergeleken? Vallen
Wet- en Regelgeving klinisch Onderzoek in Nederland anno 2015
 Wet- en Regelgeving klinisch Onderzoek in Nederland anno 2015 Prof. Dr. H. Pieterse Profess Medical Consultancy Januari 2015 1 Introduction Herman Pieterse 37 yr experience in clinical research with drugs
Wet- en Regelgeving klinisch Onderzoek in Nederland anno 2015 Prof. Dr. H. Pieterse Profess Medical Consultancy Januari 2015 1 Introduction Herman Pieterse 37 yr experience in clinical research with drugs
Wet- en Regelgeving klinisch Onderzoek in Nederland anno 2013
 Wet- en Regelgeving klinisch Onderzoek in Nederland anno 2013 Prof. Dr. H. Pieterse Profess Medical Consultancy November 2013 1 Introductie Herman Pieterse 35 jaar ervaring klinisch onderzoek geneesmiddelen
Wet- en Regelgeving klinisch Onderzoek in Nederland anno 2013 Prof. Dr. H. Pieterse Profess Medical Consultancy November 2013 1 Introductie Herman Pieterse 35 jaar ervaring klinisch onderzoek geneesmiddelen
Monitorplan voorbeeld
 Monitorplan voorbeeld Protocol Er moet in het protocol beschreven worden dat er monitoring plaatsvindt (zie ook CCMO voorbeeld template). Het monitoringplan mag als bijlage worden toegevoegd (in dat geval
Monitorplan voorbeeld Protocol Er moet in het protocol beschreven worden dat er monitoring plaatsvindt (zie ook CCMO voorbeeld template). Het monitoringplan mag als bijlage worden toegevoegd (in dat geval
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U9 Monitoren Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies Versiedatum Hoofdstuk Versiedatum Hoofdstuk
Standard Operating Procedure STZ SOP: U9 Monitoren Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies Versiedatum Hoofdstuk Versiedatum Hoofdstuk
Kwaliteitsborging onderzoek in het. NVMETC bijeenkomst 23 november UMC Utrecht. Oktober 2016
 1 Kwaliteitsborging onderzoek in het UMC Utrecht NVMETC bijeenkomst 23 november 2016 Eugenie Ram, kwaliteitsmanager Onderzoek - Office Concernstaf Raad van Bestuur Oktober 2016 UMC Utrecht breed kwaliteitssysteem
1 Kwaliteitsborging onderzoek in het UMC Utrecht NVMETC bijeenkomst 23 november 2016 Eugenie Ram, kwaliteitsmanager Onderzoek - Office Concernstaf Raad van Bestuur Oktober 2016 UMC Utrecht breed kwaliteitssysteem
Monitoren vs auditen. CRA dag 21 april 2016
 Monitoren vs auditen CRA dag 21 april 2016 Introductie Freelance consultant, mede oprichter TAPAS Group B.V. Mede oprichter/directeur van CRA B.V. Medical Adviser Yamanouchi Pharma Clinical trial monitor
Monitoren vs auditen CRA dag 21 april 2016 Introductie Freelance consultant, mede oprichter TAPAS Group B.V. Mede oprichter/directeur van CRA B.V. Medical Adviser Yamanouchi Pharma Clinical trial monitor
Risk Based Monitoring:
 Risk Based Monitoring: Sharing best practices Tine Horsten, MSc Manager Quality Control Unit / Risk Counselor Clinical Trial Center Maastricht (CTCM) Dianne Neppelenbroek, MSc Sr CRA AstraZeneca, Zoetermeer
Risk Based Monitoring: Sharing best practices Tine Horsten, MSc Manager Quality Control Unit / Risk Counselor Clinical Trial Center Maastricht (CTCM) Dianne Neppelenbroek, MSc Sr CRA AstraZeneca, Zoetermeer
Titel: Good Clinical Practice & Monitoring. Initiation Investigator Driven Studies. Versie: 14-jan-2013
 Titel: Good Clinical Practice & Monitoring Initiation Investigator Driven Studies Inhoud Wet- en regelgeving/declaration of Helsinki Good Clinical Practice Patiënteninformatie/ informed consent Basisvereisten
Titel: Good Clinical Practice & Monitoring Initiation Investigator Driven Studies Inhoud Wet- en regelgeving/declaration of Helsinki Good Clinical Practice Patiënteninformatie/ informed consent Basisvereisten
Gezondheidszorg en Clinical Trials: Samen Sterk!
 Gezondheidszorg en Clinical Trials: Samen Sterk! De basis voor succes Bert Hartog, PhD Director Clinical R&D, Benelux and Nordic countries 15 mei 2012 De basis voor succes Agenda 1. Registratieonderzoek
Gezondheidszorg en Clinical Trials: Samen Sterk! De basis voor succes Bert Hartog, PhD Director Clinical R&D, Benelux and Nordic countries 15 mei 2012 De basis voor succes Agenda 1. Registratieonderzoek
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U10 Audit Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: U10 Audit Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum Opmerkingen
Clinical Trials in Nederland: op weg naar topkwaliteit DCTF Congres 3 oktober 2012 Lunteren. M.P.W. Lamberti, BA Algemeen Directeur
 Clinical Trials in Nederland: op weg naar topkwaliteit DCTF Congres 3 oktober 2012 Lunteren M.P.W. Lamberti, BA Algemeen Directeur Maastricht UMC-Holding MUMC-Holding CTCM BPCM MI Groningen Utrecht Nijmegen
Clinical Trials in Nederland: op weg naar topkwaliteit DCTF Congres 3 oktober 2012 Lunteren M.P.W. Lamberti, BA Algemeen Directeur Maastricht UMC-Holding MUMC-Holding CTCM BPCM MI Groningen Utrecht Nijmegen
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL4 Investigator Site File Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: VL4 Investigator Site File Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Site selectie visite checklist
 Site selectie visite checklist Informatie sponsor: Naam sponsor: Contactpersoon: Functie: Afdeling: Telefoonnummer : Email : Informatie onderzoekslocatie: Naam onderzoekslocatie : Naam onderzoeker: Functie:
Site selectie visite checklist Informatie sponsor: Naam sponsor: Contactpersoon: Functie: Afdeling: Telefoonnummer : Email : Informatie onderzoekslocatie: Naam onderzoekslocatie : Naam onderzoeker: Functie:
Gedigitaliseerd onderzoek..
 Gedigitaliseerd onderzoek.. ITC Validation Consultants an extra measure of Quality Frans Leijse Managing Director GSK Global QA-eCompliance Manager Adviseurs voor.. GxP compliance van ICT Systemen Computer
Gedigitaliseerd onderzoek.. ITC Validation Consultants an extra measure of Quality Frans Leijse Managing Director GSK Global QA-eCompliance Manager Adviseurs voor.. GxP compliance van ICT Systemen Computer
Clinical Research with medicinal products in the Netherlands
 VWS015 WTK Binnenwerk 29-09-2005 11:04 Page 1 Clinical Research with medicinal products in the Netherlands Instruction Manual The Hague, October 2005 Ministry of Health, Welfare and Sport VWS015 WTK Binnenwerk
VWS015 WTK Binnenwerk 29-09-2005 11:04 Page 1 Clinical Research with medicinal products in the Netherlands Instruction Manual The Hague, October 2005 Ministry of Health, Welfare and Sport VWS015 WTK Binnenwerk
Standard Operating Procedure
 Standard Operating Procedure SOP: V9 Initiatievisite Auteur Naam: Functie instelling/afdeling Judie van den Elshout Staffunctionaris Wetenschapsbureau Wetenschapsbureau / Cluster Leerhuis Handtekening:...
Standard Operating Procedure SOP: V9 Initiatievisite Auteur Naam: Functie instelling/afdeling Judie van den Elshout Staffunctionaris Wetenschapsbureau Wetenschapsbureau / Cluster Leerhuis Handtekening:...
Wat verwacht de Inspectie van Klinisch onderzoek?
 Wat verwacht de Inspectie van Klinisch onderzoek? Jos Kraus, senior inspecteur Inspectie voor de gezondheidszorg Baarn, 7 oktober 009. Wat is klinisch onderzoek Introductie Definities De weg door de wet
Wat verwacht de Inspectie van Klinisch onderzoek? Jos Kraus, senior inspecteur Inspectie voor de gezondheidszorg Baarn, 7 oktober 009. Wat is klinisch onderzoek Introductie Definities De weg door de wet
29 juni Initiatie bijeenkomst PORTEC 4. Kwaliteitsborging WMO GCP richtsnoer. Frank van Leeuwen IKNL
 29 juni 2012 Initiatie bijeenkomst PORTEC 4 Kwaliteitsborging WMO GCP richtsnoer Frank van Leeuwen IKNL Wet en regelgeving Verklaring van Helsinki Richtsnoer voor Good Clinical Practice (CPMP/ICH/135/95)
29 juni 2012 Initiatie bijeenkomst PORTEC 4 Kwaliteitsborging WMO GCP richtsnoer Frank van Leeuwen IKNL Wet en regelgeving Verklaring van Helsinki Richtsnoer voor Good Clinical Practice (CPMP/ICH/135/95)
Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) Team Klinisch Onderzoek
 Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) 2014-2016 Team Klinisch Onderzoek Toezicht op IIT 2014-2016 Aanleiding en werkwijze Bevindingen vanuit de praktijk Conclusies en aandachtspunten
Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) 2014-2016 Team Klinisch Onderzoek Toezicht op IIT 2014-2016 Aanleiding en werkwijze Bevindingen vanuit de praktijk Conclusies en aandachtspunten
Handleiding. Investigational Medicinal Product Dossier (IMPD)
 Handleiding Investigational Medicinal Product Dossier (IMPD) Inhoudsopgave Afkortingen... - 3 - Wat is het IMPD?... - 4 - Beslisschema inhoud IMPD... - 5 - Beschrijving inhoud IMPD... - 6 - Overzicht hoofdstukken
Handleiding Investigational Medicinal Product Dossier (IMPD) Inhoudsopgave Afkortingen... - 3 - Wat is het IMPD?... - 4 - Beslisschema inhoud IMPD... - 5 - Beschrijving inhoud IMPD... - 6 - Overzicht hoofdstukken
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U4 Registratie /randomisatie procedure Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum
Standard Operating Procedure STZ SOP: U4 Registratie /randomisatie procedure Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum
Antwoorden CRO-vragenlijst - foto van het veld
 Antwoorden CRO-vragenlijst - foto van het veld In samenwerking met het RIVM heeft de Inspectie voor de Gezondheidszorg (IGZ) een digitale vragenlijst ontwikkeld die bestond uit drie delen (zie Vragenlijst
Antwoorden CRO-vragenlijst - foto van het veld In samenwerking met het RIVM heeft de Inspectie voor de Gezondheidszorg (IGZ) een digitale vragenlijst ontwikkeld die bestond uit drie delen (zie Vragenlijst
Verificatie van Onderzoeksgegevens. Een internationaal perspectief. Jean-Paul Eycken. FormaliS. EPD-Dag Amsterdam, NL 12 juni 2008
 Verificatie van Onderzoeksgegevens Een internationaal perspectief Jean-Paul Eycken -Dag Amsterdam, NL 12 juni 2008 Slide 1 Mag ik mij even voorstellen? Jean-Paul Eycken Bioingenieur, MBA 20 jaren ervaring
Verificatie van Onderzoeksgegevens Een internationaal perspectief Jean-Paul Eycken -Dag Amsterdam, NL 12 juni 2008 Slide 1 Mag ik mij even voorstellen? Jean-Paul Eycken Bioingenieur, MBA 20 jaren ervaring
Europese verordening klinische proeven. Harrie Storms (VWS)
 Europese verordening klinische proeven Harrie Storms (VWS) 1 Veranderingen EU verordening Indiening via EU-portal (nationale studies en multinationale studies) Centrale beoordeling van multinationaal onderzoek
Europese verordening klinische proeven Harrie Storms (VWS) 1 Veranderingen EU verordening Indiening via EU-portal (nationale studies en multinationale studies) Centrale beoordeling van multinationaal onderzoek
Praktische implementatie Europese verordening Geneesmiddelen onderzoek
 Praktische implementatie Europese verordening Geneesmiddelen onderzoek Dr. Joost Keers Hoofd Wetenschappelijk Instituut j.keers@mzh.nl 050 524 5826 http://www.ccmo.nl/nl/europese-verordening Belangrijke
Praktische implementatie Europese verordening Geneesmiddelen onderzoek Dr. Joost Keers Hoofd Wetenschappelijk Instituut j.keers@mzh.nl 050 524 5826 http://www.ccmo.nl/nl/europese-verordening Belangrijke
Bouwen aan vertrouwen: perspectief van de industrie
 Symposium ter gelegenheid afscheid Ad van Dooren Zelfredzaamheid van patiënten bij gebruik van veilige medicatie. Bouwen aan vertrouwen: perspectief van de industrie Rudolf van Olden, arts Medisch Directeur
Symposium ter gelegenheid afscheid Ad van Dooren Zelfredzaamheid van patiënten bij gebruik van veilige medicatie. Bouwen aan vertrouwen: perspectief van de industrie Rudolf van Olden, arts Medisch Directeur
1. Voorafgaand aan de klinische fase van het onderzoek
 Essentiële documenten Bron: Richtsnoer voor good clinical practice (CPMP/ICH/135/95) De verwijzingen in dit document verwijzen naar de artikelen in bovenstaand document. 1. Voorafgaand aan de klinische
Essentiële documenten Bron: Richtsnoer voor good clinical practice (CPMP/ICH/135/95) De verwijzingen in dit document verwijzen naar de artikelen in bovenstaand document. 1. Voorafgaand aan de klinische
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A1 Afsluiting studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A1 Afsluiting studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A2 Archiveren studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A2 Archiveren studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Opleiding PECB ISO 9001 Quality Manager.
 Opleiding PECB ISO 9001 Quality Manager www.bpmo-academy.nl Wat is kwaliteitsmanagement? Kwaliteitsmanagement beoogt aan te sturen op het verbeteren van kwaliteit. Tevens houdt het zich bezig met het verbinden
Opleiding PECB ISO 9001 Quality Manager www.bpmo-academy.nl Wat is kwaliteitsmanagement? Kwaliteitsmanagement beoogt aan te sturen op het verbeteren van kwaliteit. Tevens houdt het zich bezig met het verbinden
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen. Farmaceutische Bedrijven Deelteam Klinisch Onderzoek
 Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
Patient information. Report information. Serious Adverse Event information
 HOVON Data Center Safety Desk NIEUWSBRIEF 4 06 mei 2014 Beste lezer, Met gepaste trots presenteren we u de nieuwe manier van rapporteren van SAE's. Hiermee hopen wij de werklast voor iedereen zoveel mogelijk
HOVON Data Center Safety Desk NIEUWSBRIEF 4 06 mei 2014 Beste lezer, Met gepaste trots presenteren we u de nieuwe manier van rapporteren van SAE's. Hiermee hopen wij de werklast voor iedereen zoveel mogelijk
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U5 Datamanagement Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: U5 Datamanagement Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Process Mining and audit support within financial services. KPMG IT Advisory 18 June 2014
 Process Mining and audit support within financial services KPMG IT Advisory 18 June 2014 Agenda INTRODUCTION APPROACH 3 CASE STUDIES LEASONS LEARNED 1 APPROACH Process Mining Approach Five step program
Process Mining and audit support within financial services KPMG IT Advisory 18 June 2014 Agenda INTRODUCTION APPROACH 3 CASE STUDIES LEASONS LEARNED 1 APPROACH Process Mining Approach Five step program
Toezicht op IIT: bevindingen vanuit de praktijk
 Toezicht op IIT: bevindingen vanuit de praktijk Elysée Hille, senior inspecteur namens deelteam KO-GCP Teamcoördinator KO-GCP/PhV/GZH Afdeling Farmaceutische Bedrijven Wat doet de IGZ? Toezicht op klinisch
Toezicht op IIT: bevindingen vanuit de praktijk Elysée Hille, senior inspecteur namens deelteam KO-GCP Teamcoördinator KO-GCP/PhV/GZH Afdeling Farmaceutische Bedrijven Wat doet de IGZ? Toezicht op klinisch
MDR (2017/745) en klinisch onderzoek - Implementatie in Nederland -
 MDR (2017/745) en klinisch onderzoek - Implementatie in Nederland - DCRF 26 september 2018 Monique Al Teamcoördinator Landelijk Bureau CCMO MDR: Drie hoofdcategoriën klinisch onderzoek I II III Klinisch
MDR (2017/745) en klinisch onderzoek - Implementatie in Nederland - DCRF 26 september 2018 Monique Al Teamcoördinator Landelijk Bureau CCMO MDR: Drie hoofdcategoriën klinisch onderzoek I II III Klinisch
Brigitte de Vries Staedion. Kwaliteitsbeheersing De uitdagingen voor een éénpitter
 Brigitte de Vries Staedion Kwaliteitsbeheersing De uitdagingen voor een éénpitter Kwaliteitsbeheersing voor de éénpitter Wat kunt u verwachten Wie ben ik en waar werk ik Mijn uitdagingen Ervaring met kwaliteitstoetsing
Brigitte de Vries Staedion Kwaliteitsbeheersing De uitdagingen voor een éénpitter Kwaliteitsbeheersing voor de éénpitter Wat kunt u verwachten Wie ben ik en waar werk ik Mijn uitdagingen Ervaring met kwaliteitstoetsing
CRO s kwaliteit en toegevoegde waarde
 CRO s kwaliteit en toegevoegde waarde dr. Annejet P. Meijler Programmadirecteur Geneesmiddelen IGZ 1 Medisch-wetenschappelijk onderzoek 4 april 2011 Deze workshop Inleiding I prof. Herman Pieterse Inleiding
CRO s kwaliteit en toegevoegde waarde dr. Annejet P. Meijler Programmadirecteur Geneesmiddelen IGZ 1 Medisch-wetenschappelijk onderzoek 4 april 2011 Deze workshop Inleiding I prof. Herman Pieterse Inleiding
Issues in PET Drug Manufacturing Steve Zigler PETNET Solutions April 14, 2010
 Issues in PET Drug Manufacturing Steve Zigler PETNET Solutions April 14, 2010 Topics ANDA process for FDG User fees Contract manufacturing PETNET's perspective Colleagues Michael Nazerias Ken Breslow Ed
Issues in PET Drug Manufacturing Steve Zigler PETNET Solutions April 14, 2010 Topics ANDA process for FDG User fees Contract manufacturing PETNET's perspective Colleagues Michael Nazerias Ken Breslow Ed
Onderzoeksresultaten transparantie en openbaarheid
 Onderzoeksresultaten transparantie en openbaarheid Peter W de Leeuw Afd. Interne Geneeskunde, azm, Maastricht en Nederlands Tijdschrift voor Geneeskunde Uitgangspunten Rapportage van resultaten van (biomedisch)
Onderzoeksresultaten transparantie en openbaarheid Peter W de Leeuw Afd. Interne Geneeskunde, azm, Maastricht en Nederlands Tijdschrift voor Geneeskunde Uitgangspunten Rapportage van resultaten van (biomedisch)
Inspectie beleid GDP Guideline. Ageeth Dekker Senior Inspecteur
 Inspectie beleid GDP Guideline Ageeth Dekker Senior Inspecteur Agenda 1. Inleiding 2. Groothandelsvergunning 3. GDP inspecties, rapportage en certificaat 4. Samenvatting 5. Vragen 2 Inleiding Nieuwe GDP
Inspectie beleid GDP Guideline Ageeth Dekker Senior Inspecteur Agenda 1. Inleiding 2. Groothandelsvergunning 3. GDP inspecties, rapportage en certificaat 4. Samenvatting 5. Vragen 2 Inleiding Nieuwe GDP
Recente ontwikkelingen in de ethische normen voor medisch-wetenschappelijk onderzoek
 Recente ontwikkelingen in de ethische normen voor medisch-wetenschappelijk onderzoek Prof dr JJM van Delden Julius Centrum, UMC Utrecht j.j.m.vandelden@umcutrecht.nl Inleiding Medisch-wetenschappelijk
Recente ontwikkelingen in de ethische normen voor medisch-wetenschappelijk onderzoek Prof dr JJM van Delden Julius Centrum, UMC Utrecht j.j.m.vandelden@umcutrecht.nl Inleiding Medisch-wetenschappelijk
De rol van de Contract Research Organisatie (CRO) Klinisch onderzoek
 De rol van de Contract Research Organisatie (CRO) in klinisch geneesmiddelenonderzoek Klinisch onderzoek Inhoud Aanleiding CRO project Methode en resultaten» Werkwijze en resultaten foto van het veld vragenlijst»
De rol van de Contract Research Organisatie (CRO) in klinisch geneesmiddelenonderzoek Klinisch onderzoek Inhoud Aanleiding CRO project Methode en resultaten» Werkwijze en resultaten foto van het veld vragenlijst»
Geleerde lessen Compliance. Utrecht, 19 januari 2017 Mr. Stijn Sarneel MBA CIPP/E. Agenda
 Geleerde lessen Compliance Toegepast op WP 29: Guideline DPO Utrecht, 19 januari 2017 Mr. Stijn Sarneel MBA CIPP/E Agenda Kennismaken met VCO Ontwikkeling van Compliance in NL WP 29 Triggers Lessons learned
Geleerde lessen Compliance Toegepast op WP 29: Guideline DPO Utrecht, 19 januari 2017 Mr. Stijn Sarneel MBA CIPP/E Agenda Kennismaken met VCO Ontwikkeling van Compliance in NL WP 29 Triggers Lessons learned
Aanvraagformulier REGISTRATIE oncologie monitor
 Aanvraagformulier REGISTRATIE oncologie monitor 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:... Geboorteplaats:... Werkzaam bij: Organisatie + Afdeling:...
Aanvraagformulier REGISTRATIE oncologie monitor 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:... Geboorteplaats:... Werkzaam bij: Organisatie + Afdeling:...
Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen
 Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen Afdeling Farmaceutische Bedrijven, Klinisch Onderzoek Good Clinical Practice Inhoud Wat doet de IGJ aan toezicht op klinisch
Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen Afdeling Farmaceutische Bedrijven, Klinisch Onderzoek Good Clinical Practice Inhoud Wat doet de IGJ aan toezicht op klinisch
Ervaringen met document X
 Martini Ziekenhuis Groningen Ervaringen met document X Ellen Rusch, wetenschappelijk medewerker Wetenschappelijk Instituut Wat gaan we doen? Structuur lokale haalbaarheid Martini Ziekenhuis Het werken
Martini Ziekenhuis Groningen Ervaringen met document X Ellen Rusch, wetenschappelijk medewerker Wetenschappelijk Instituut Wat gaan we doen? Structuur lokale haalbaarheid Martini Ziekenhuis Het werken
IC ICF ICH ISF. Lijst met afkortingen, definities en termen STZ-Kwaliteitshandboek SOP s
 Lijst met afkortingen, definities en termen STZ-Kwaliteitshandboek SOP s ABR ADR AE AR BROK CCMO CRF CTA CV DSMB EMEA EU EudraCT FU brief GCP GMP IB IC ICF ICH IMPD ISF MEB METC EU RCT SAE SOP SPC SUSAR
Lijst met afkortingen, definities en termen STZ-Kwaliteitshandboek SOP s ABR ADR AE AR BROK CCMO CRF CTA CV DSMB EMEA EU EudraCT FU brief GCP GMP IB IC ICF ICH IMPD ISF MEB METC EU RCT SAE SOP SPC SUSAR
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U8 Melding van (Serious) Adverse Events en SUSARs Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies
Standard Operating Procedure STZ SOP: U8 Melding van (Serious) Adverse Events en SUSARs Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies
Kwaliteit: Minder is meer
 Kwaliteit: Minder is meer Kwaliteit in klinisch onderzoek met medische hulpmiddelen Jako Pranger QA Manager Cardialysis 9 Nov 2012 Kwaliteit en integriteit Mensgebonden onderzoek Trends in kwaliteitsbeleving
Kwaliteit: Minder is meer Kwaliteit in klinisch onderzoek met medische hulpmiddelen Jako Pranger QA Manager Cardialysis 9 Nov 2012 Kwaliteit en integriteit Mensgebonden onderzoek Trends in kwaliteitsbeleving
Activant Prophet 21. Prophet 21 Version 12.0 Upgrade Information
 Activant Prophet 21 Prophet 21 Version 12.0 Upgrade Information This class is designed for Customers interested in upgrading to version 12.0 IT staff responsible for the managing of the Prophet 21 system
Activant Prophet 21 Prophet 21 Version 12.0 Upgrade Information This class is designed for Customers interested in upgrading to version 12.0 IT staff responsible for the managing of the Prophet 21 system
Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek
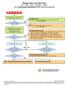 Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek Melding voorval proefpersoon aan onderzoeker/arts 1 Rapportage voorval door onderzoeker/arts in patiëntenstatus
Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek Melding voorval proefpersoon aan onderzoeker/arts 1 Rapportage voorval door onderzoeker/arts in patiëntenstatus
Werkinstructies adverse events rapportage STOP-BPD studie
 Werkinstructies adverse events rapportage STOP-BPD studie De STOP-BPD studie wordt uitgevoerd bij extreem prematuur geboren kinderen die los van deelname aan de studie een continu verhoogd risico hebben
Werkinstructies adverse events rapportage STOP-BPD studie De STOP-BPD studie wordt uitgevoerd bij extreem prematuur geboren kinderen die los van deelname aan de studie een continu verhoogd risico hebben
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: O3 Ontwikkelen, implementeren en beheren van SOP s Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies
Standard Operating Procedure STZ SOP: O3 Ontwikkelen, implementeren en beheren van SOP s Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies
3.C.1 Communicatieplan CO2-reductiesysteem
 3.C.1 Communicatieplan systeem General Document approval by: John Waltman (Europe) Classification: Approved for External / 3rd Party Use Document version: 5.0 Approval status: Approved NON-DISCLOSURE OF
3.C.1 Communicatieplan systeem General Document approval by: John Waltman (Europe) Classification: Approved for External / 3rd Party Use Document version: 5.0 Approval status: Approved NON-DISCLOSURE OF
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik
 EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
AANVULLENDE AJS SAFETY RULES
 Pagina: 1 van 5 Inleiding Naast de regels en procedures die Harsco Infrastructure B.V. heeft opgesteld hebben een aantal van onze klanten aanvullende veiligheidseisen en procedures. Als je voor onze opdrachtgever
Pagina: 1 van 5 Inleiding Naast de regels en procedures die Harsco Infrastructure B.V. heeft opgesteld hebben een aantal van onze klanten aanvullende veiligheidseisen en procedures. Als je voor onze opdrachtgever
Rechten en plichten op gebied van privacy bij wetenschappelijk onderzoek met mensen Prof. Dr. H. Pieterse
 Rechten en plichten op gebied van privacy bij wetenschappelijk onderzoek met mensen Prof. Dr. H. Pieterse Heymans Instituut Universiteit Gent Voorzitter NVMA 21 november 2013 1 Introductie Herman Pieterse
Rechten en plichten op gebied van privacy bij wetenschappelijk onderzoek met mensen Prof. Dr. H. Pieterse Heymans Instituut Universiteit Gent Voorzitter NVMA 21 november 2013 1 Introductie Herman Pieterse
Actuele ontwikkelingen ten aanzien van toetsen van medisch-wetenschappelijk
 Actuele ontwikkelingen ten aanzien van toetsen van medisch-wetenschappelijk onderzoek met mensen NVMETC scholingsdagen 2016 Monique Al Sr wetenschappelijk stafmedewerker CCMO Ontwikkelingen wetgeving 1.
Actuele ontwikkelingen ten aanzien van toetsen van medisch-wetenschappelijk onderzoek met mensen NVMETC scholingsdagen 2016 Monique Al Sr wetenschappelijk stafmedewerker CCMO Ontwikkelingen wetgeving 1.
Lessen te leren uit de Farma wereld. Arjan Roovers Managing Consultant
 Lessen te leren uit de Farma wereld Arjan Roovers Managing Consultant Vragen centraal in dit symposium 1. Waarom validatie? 2. Opzet en frequentie periodieke validatie 3. Rol van validatie protocol en
Lessen te leren uit de Farma wereld Arjan Roovers Managing Consultant Vragen centraal in dit symposium 1. Waarom validatie? 2. Opzet en frequentie periodieke validatie 3. Rol van validatie protocol en
Blik van de IGJ op implementatie veiligheidskenmerken
 Blik van de IGJ op implementatie veiligheidskenmerken Mieke van der Meulen BOGIN symposium - veiligheidskenmerken 2 Inhoud Fabrikanten Groothandels - risk based verificatie Aggregatie van codes Inrichting
Blik van de IGJ op implementatie veiligheidskenmerken Mieke van der Meulen BOGIN symposium - veiligheidskenmerken 2 Inhoud Fabrikanten Groothandels - risk based verificatie Aggregatie van codes Inrichting
1. Beschrijving werkgebieden / thema s
 1. Beschrijving werkgebieden / thema s Nr 1 Thema Wetenschappelijke Achtergrond en Opzet van Onderzoek 2 Ethische en veiligheid overwegingen 3 Ontwikkeling en Regelgeving 4 Clinical Trial Operations (Projectorganisatie)
1. Beschrijving werkgebieden / thema s Nr 1 Thema Wetenschappelijke Achtergrond en Opzet van Onderzoek 2 Ethische en veiligheid overwegingen 3 Ontwikkeling en Regelgeving 4 Clinical Trial Operations (Projectorganisatie)
Introduction Henk Schwietert
 Introduction Henk Schwietert Evalan develops, markets and sells services that use remote monitoring and telemetry solutions. Our Company Evalan develops hard- and software to support these services: mobile
Introduction Henk Schwietert Evalan develops, markets and sells services that use remote monitoring and telemetry solutions. Our Company Evalan develops hard- and software to support these services: mobile
ISO 20000 @ CTG Europe
 ISO 20000 @ CTG Europe 31/10/2007 mieke.roelens@ctg.com +32 496266725 1 Agenda 31 oktober 2007 Voorstelling Project Business Case: Doel & Scope Projectorganisatie Resultaten assessments en conclusies De
ISO 20000 @ CTG Europe 31/10/2007 mieke.roelens@ctg.com +32 496266725 1 Agenda 31 oktober 2007 Voorstelling Project Business Case: Doel & Scope Projectorganisatie Resultaten assessments en conclusies De
Toetsingskader nwmo. Peggy Manders 4 november 2016 Symposium V&VN Research Professionals
 Toetsingskader nwmo Peggy Manders 4 november 2016 Symposium V&VN Research Professionals Biobank: definitie en rationale Wat is een biobank? + + Waarom een biobank starten? Verbeteren gezondheidszorg voor
Toetsingskader nwmo Peggy Manders 4 november 2016 Symposium V&VN Research Professionals Biobank: definitie en rationale Wat is een biobank? + + Waarom een biobank starten? Verbeteren gezondheidszorg voor
 1.1 ORGANIZATION INFORMATION 1.2 CONTACT INFORMATION 2.1 SCOPE OF CERTIFICATION 2.2 AUDITOR INFORMATION 3.1 AUDIT CONCLUSIONS 3.2 MANAGEMENT SYSTEM EFFECTIVENESS 3.3 OBSERVATIONS Organization Address Name
1.1 ORGANIZATION INFORMATION 1.2 CONTACT INFORMATION 2.1 SCOPE OF CERTIFICATION 2.2 AUDITOR INFORMATION 3.1 AUDIT CONCLUSIONS 3.2 MANAGEMENT SYSTEM EFFECTIVENESS 3.3 OBSERVATIONS Organization Address Name
Naar een nieuw Privacy Control Framework (PCF)
 Naar een nieuw Privacy Control Framework (PCF) Ed Ridderbeekx 22 november 2017 Een stukje geschiedenis 2001: Raamwerk Privacy Audit (door Samenwerkingsverband Audit Aanpak onder verantwoordelijkheid CPB)
Naar een nieuw Privacy Control Framework (PCF) Ed Ridderbeekx 22 november 2017 Een stukje geschiedenis 2001: Raamwerk Privacy Audit (door Samenwerkingsverband Audit Aanpak onder verantwoordelijkheid CPB)
AdVISHE: Assessment of the Validation Status of Health- Economic Decision Models
 AdVISHE: Assessment of the Validation Status of Health- Economic Decision Models Pepijn Vemer, George van Voorn, Isaac Corro Ramos, Maiwenn Al, Talitha Feenstra Rationale In theorie: Doe alles! Een model
AdVISHE: Assessment of the Validation Status of Health- Economic Decision Models Pepijn Vemer, George van Voorn, Isaac Corro Ramos, Maiwenn Al, Talitha Feenstra Rationale In theorie: Doe alles! Een model
Welke factoren beïnvloeden het gezamenlijk leren door leraren? Een systematische literatuurreview Thurlings, M.C.G.; den Brok, P.J.
 Welke factoren beïnvloeden het gezamenlijk leren door leraren? Een systematische literatuurreview Thurlings, M.C.G.; den Brok, P.J. Published in: Onderwijs Research Dagen(ORD), 11-12 Juni 2014, Groningen,
Welke factoren beïnvloeden het gezamenlijk leren door leraren? Een systematische literatuurreview Thurlings, M.C.G.; den Brok, P.J. Published in: Onderwijs Research Dagen(ORD), 11-12 Juni 2014, Groningen,
Toezicht op klinisch onderzoek - bevindingen vanuit de praktijk
 Toezicht op klinisch onderzoek - bevindingen vanuit de praktijk Namens Deelprogramma Klinisch Onderzoek, IGZ Spreker Dr. ir. J. Eland-Gerritsen Coördinerend/Specialistisch Senior inspecteur Inhoud Toezicht
Toezicht op klinisch onderzoek - bevindingen vanuit de praktijk Namens Deelprogramma Klinisch Onderzoek, IGZ Spreker Dr. ir. J. Eland-Gerritsen Coördinerend/Specialistisch Senior inspecteur Inhoud Toezicht
3.D.1. Sector- en keteninitiatieven
 3.D.1. Sector- en keteninitiatieven General Document approval by: John Waltman (Europe) Classification: Approved for External / 3rd Party Use Document version: 4.0 Approval status: Approved NON-DISCLOSURE
3.D.1. Sector- en keteninitiatieven General Document approval by: John Waltman (Europe) Classification: Approved for External / 3rd Party Use Document version: 4.0 Approval status: Approved NON-DISCLOSURE
Voorlichting Erasmus+ KA2 15 november 2018
 Voorlichting Erasmus+ 15 november 2018 Check in 2 Wat is Wie bent u en wie zijn wij? Wanneer in Help Doel van de workshop 3 Wat is Wanneer in Help U weet wat inhoudt U weet welke instrumenten u kunt gebruiken
Voorlichting Erasmus+ 15 november 2018 Check in 2 Wat is Wie bent u en wie zijn wij? Wanneer in Help Doel van de workshop 3 Wat is Wanneer in Help U weet wat inhoudt U weet welke instrumenten u kunt gebruiken
Patiëntenparticipatie in
 Patiëntenparticipatie in Europees perspectief Marleen Kaatee Oprichter & voorzitter Patiëntenparticipatie in Europa: 1. PSC Patients Europe 2. EMA 3. ERNs, European Reference Networks Noodzaak: internationaal
Patiëntenparticipatie in Europees perspectief Marleen Kaatee Oprichter & voorzitter Patiëntenparticipatie in Europa: 1. PSC Patients Europe 2. EMA 3. ERNs, European Reference Networks Noodzaak: internationaal
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A4 Publicatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A4 Publicatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Understanding the role of health literacy in self-management and health behaviors among older adults Geboers, Bas
 University of Groningen Understanding the role of health literacy in self-management and health behaviors among older adults Geboers, Bas IMPORTANT NOTE: You are advised to consult the publisher's version
University of Groningen Understanding the role of health literacy in self-management and health behaviors among older adults Geboers, Bas IMPORTANT NOTE: You are advised to consult the publisher's version
CCMO Structuur documenten Technische Toetsing (ass.secr.) Inhoudelijke Toetsing (secretaris)
 CHECKLIST WMO Primaire indieningsproces WMO in METC Management, screening door Assistent Secretaris. Hieronder staan de generieke uitgangspunten en is toegelicht hoe de primaire toetsing indiening WMO
CHECKLIST WMO Primaire indieningsproces WMO in METC Management, screening door Assistent Secretaris. Hieronder staan de generieke uitgangspunten en is toegelicht hoe de primaire toetsing indiening WMO
Online Resource 1. Title: Implementing the flipped classroom: An exploration of study behaviour and student performance
 Online Resource 1 Title: Implementing the flipped classroom: An exploration of study behaviour and student performance Journal: Higher Education Authors: Anja J. Boevé, Rob R. Meijer, Roel J. Bosker, Jorien
Online Resource 1 Title: Implementing the flipped classroom: An exploration of study behaviour and student performance Journal: Higher Education Authors: Anja J. Boevé, Rob R. Meijer, Roel J. Bosker, Jorien
Certificate of Conformity Part I
 1. Supplier Serial No. Certificate of Conformity Part I 2. Supplier (Include Name, Address, Email etc.): 3. Contract Number: 4. Contract Modification Number: 5. Approved Deviations and/or Concessions:
1. Supplier Serial No. Certificate of Conformity Part I 2. Supplier (Include Name, Address, Email etc.): 3. Contract Number: 4. Contract Modification Number: 5. Approved Deviations and/or Concessions:
Certificering NDT personeel Aerospace industrie
 Certificering NDT personeel Aerospace industrie en de rol die de NANDT Board hierbij vervult Pieter Troost (Review Board) 13/11/2018 1 Onderwerpen Introductie kwalificatie en certificatie van NDT personeel
Certificering NDT personeel Aerospace industrie en de rol die de NANDT Board hierbij vervult Pieter Troost (Review Board) 13/11/2018 1 Onderwerpen Introductie kwalificatie en certificatie van NDT personeel
VLC. De betekenis van de Verantwoordelijk LasCoördinator in de EN 1090 en ISO 3834 series. Ing Raoul Heremans, ewe
 1 VLC De betekenis van de Verantwoordelijk LasCoördinator in de EN 1090 en ISO 3834 series Ing Raoul Heremans, ewe De VLC, een nieuw begrip? Met welke verordeningen, standaarden en normen is het begrip
1 VLC De betekenis van de Verantwoordelijk LasCoördinator in de EN 1090 en ISO 3834 series Ing Raoul Heremans, ewe De VLC, een nieuw begrip? Met welke verordeningen, standaarden en normen is het begrip
INFORMATIEBLAD. Maart 2011
 INFORMATIEBLAD AANMELDING TRIALBUREAU/DATACENTRUM Maart 2011 Kanker zo snel mogelijk terugdringen en onder controle brengen. We zijn er voor mensen die leven met kanker en de mensen die met hen samenleven.
INFORMATIEBLAD AANMELDING TRIALBUREAU/DATACENTRUM Maart 2011 Kanker zo snel mogelijk terugdringen en onder controle brengen. We zijn er voor mensen die leven met kanker en de mensen die met hen samenleven.
2 e webinar herziening ISO 14001
 2 e webinar herziening ISO 14001 Webinar SCCM 25 september 2014 Frans Stuyt Doel 2 e webinar herziening ISO 14001 Planning vervolg herziening Overgangsperiode certificaten Korte samenvatting 1 e webinar
2 e webinar herziening ISO 14001 Webinar SCCM 25 september 2014 Frans Stuyt Doel 2 e webinar herziening ISO 14001 Planning vervolg herziening Overgangsperiode certificaten Korte samenvatting 1 e webinar
Fidelity of a Strengths-based method for Homeless Youth
 Fidelity of a Strengths-based method for Homeless Youth Manon krabbenborg, Sandra Boersma, Marielle Beijersbergen & Judith Wolf s.boersma@elg.umcn.nl Homeless youth in the Netherlands Latest estimate:
Fidelity of a Strengths-based method for Homeless Youth Manon krabbenborg, Sandra Boersma, Marielle Beijersbergen & Judith Wolf s.boersma@elg.umcn.nl Homeless youth in the Netherlands Latest estimate:
Vragen en antwoorden over de gegevenssectie van de model-pif
 Vragen en antwoorden over de gegevenssectie van de model-pif Algemene informatie over de Algemene Verordening Gegevensbescherming Waar vind ik algemene informatie over de gevolgen van de Algemene Verordening
Vragen en antwoorden over de gegevenssectie van de model-pif Algemene informatie over de Algemene Verordening Gegevensbescherming Waar vind ik algemene informatie over de gevolgen van de Algemene Verordening
Informatie Researchcursus
 Informatie Researchcursus Cursus research professional Data Management De Data Management training is opgebouwd uit twee delen (gecombineerd in één trainingssessie). In deel 1 wordt een algemene inleiding
Informatie Researchcursus Cursus research professional Data Management De Data Management training is opgebouwd uit twee delen (gecombineerd in één trainingssessie). In deel 1 wordt een algemene inleiding
Informatie voor niet verzekerde patiënten en/of in het buitenland
 Informatie voor niet verzekerde patiënten en/of in het buitenland verzekerde patiënten Ook als u geen ziektekostenverzekering heeft of in het buitenland verzekerd bent, kunt u voor behandeling terecht
Informatie voor niet verzekerde patiënten en/of in het buitenland verzekerde patiënten Ook als u geen ziektekostenverzekering heeft of in het buitenland verzekerd bent, kunt u voor behandeling terecht
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U1 Identificatie, werving en pre-screening proefpersonen Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure STZ SOP: U1 Identificatie, werving en pre-screening proefpersonen Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere
WMO-GCP opfriscursus Nederlandse Vereniging voor Oncologie Datamanagers 27 februari 2019
 WMO-GCP opfriscursus Nederlandse Vereniging voor Oncologie Datamanagers 27 februari 2019 Agenda Introductie ICH-GCP R2 AVG Kwaliteitssyteem Informed Consent ISF e-tmf Monitoren SAE rapportage Waarom wetgeving?
WMO-GCP opfriscursus Nederlandse Vereniging voor Oncologie Datamanagers 27 februari 2019 Agenda Introductie ICH-GCP R2 AVG Kwaliteitssyteem Informed Consent ISF e-tmf Monitoren SAE rapportage Waarom wetgeving?
Inhoud onderzoeksdossier
 Inhoud onderzoeksdossier (documenten in de witte box zijn nodig voor de primaire beoordeling) A. Brieven B. Formulieren C. Onderzoeksprotocol en protocolamendementen D. Productinformatie E. Informatie
Inhoud onderzoeksdossier (documenten in de witte box zijn nodig voor de primaire beoordeling) A. Brieven B. Formulieren C. Onderzoeksprotocol en protocolamendementen D. Productinformatie E. Informatie
Testplan Module 12: Bachelor assignment ( )
 Testplan Module 12: Bachelor assignment (201500466) BSc Chemical Engineering, academic year: 2017-2018 Module information Module examiners Module parts EC Gardeniers, Bouwmeester, Betlem, Huskens, Brilman,
Testplan Module 12: Bachelor assignment (201500466) BSc Chemical Engineering, academic year: 2017-2018 Module information Module examiners Module parts EC Gardeniers, Bouwmeester, Betlem, Huskens, Brilman,
Lamotrigine in bipolar depression Loos, Marcus Lambertus Maria van der
 Lamotrigine in bipolar depression Loos, Marcus Lambertus Maria van der IMPORTANT NOTE: You are advised to consult the publisher's version (publisher's PDF) if you wish to cite from it. Please check the
Lamotrigine in bipolar depression Loos, Marcus Lambertus Maria van der IMPORTANT NOTE: You are advised to consult the publisher's version (publisher's PDF) if you wish to cite from it. Please check the
Linda Collins Director Lynelle Gehrke Associate Director
 Linda Collins Director Lynelle Gehrke Associate Director Agenda Growth of Sponsored Research Customer Service Improvement Proposal Tracking Process Improvements Timely Submission of Proposals Award Notification
Linda Collins Director Lynelle Gehrke Associate Director Agenda Growth of Sponsored Research Customer Service Improvement Proposal Tracking Process Improvements Timely Submission of Proposals Award Notification
"Baselines: eigenwijsheid of wijsheid?"
 "Baselines: eigenwijsheid of wijsheid?" Een afrondende 'beschouwende' presentatie Ing. Ernst J. Oud CISA CISSP Philips Toshiba Crypsys Data Security Getronics Business Continuity (a.k.a. CUC) Urenco Deloitte
"Baselines: eigenwijsheid of wijsheid?" Een afrondende 'beschouwende' presentatie Ing. Ernst J. Oud CISA CISSP Philips Toshiba Crypsys Data Security Getronics Business Continuity (a.k.a. CUC) Urenco Deloitte
Insurance Coverage in Clinical Trials : What about insurance amount harmonization? Isabelle de Hemptinne BAREC Meeting 22 Nov.
 Insurance Coverage in Clinical Trials : What about insurance amount harmonization? Isabelle de Hemptinne BAREC Meeting 22 Nov. 2017 What about Insurance Amount Harmonization? What does the law say? No
Insurance Coverage in Clinical Trials : What about insurance amount harmonization? Isabelle de Hemptinne BAREC Meeting 22 Nov. 2017 What about Insurance Amount Harmonization? What does the law say? No
Published in: Onderwijs Research Dagen 2013 (ORD2013), mei 2013, Brussel, Belgie
 Samenwerkend leren van leerkrachten : leeropbrengsten gerelateerd aan activiteiten en foci van samenwerking Doppenberg, J.J.; den Brok, P.J.; Bakx, A.W.E.A. Published in: Onderwijs Research Dagen 2013
Samenwerkend leren van leerkrachten : leeropbrengsten gerelateerd aan activiteiten en foci van samenwerking Doppenberg, J.J.; den Brok, P.J.; Bakx, A.W.E.A. Published in: Onderwijs Research Dagen 2013
University of Groningen. Structured diabetes care in general practice Fokkens, Sudara Andrea
 University of Groningen Structured diabetes care in general practice Fokkens, Sudara Andrea IMPORTANT NOTE: You are advised to consult the publisher's version (publisher's PDF) if you wish to cite from
University of Groningen Structured diabetes care in general practice Fokkens, Sudara Andrea IMPORTANT NOTE: You are advised to consult the publisher's version (publisher's PDF) if you wish to cite from
2019 SUNEXCHANGE USER GUIDE LAST UPDATED
 2019 SUNEXCHANGE USER GUIDE LAST UPDATED 0 - -19 1 WELCOME TO SUNEX DISTRIBUTOR PORTAL This user manual will cover all the screens and functions of our site. MAIN SCREEN: Welcome message. 2 LOGIN SCREEN:
2019 SUNEXCHANGE USER GUIDE LAST UPDATED 0 - -19 1 WELCOME TO SUNEX DISTRIBUTOR PORTAL This user manual will cover all the screens and functions of our site. MAIN SCREEN: Welcome message. 2 LOGIN SCREEN:
NEN EN ISO 13485:2016
 NEN EN ISO 13485:2016 Relatie met de huidige MDD en aankomende MDR Arjan van Drongelen Inhoud 1. Inleiding 2. Kwaliteitssystemen in MDD 3. Kwaliteitssystemen in MDR 4. Common specifications & standaarden
NEN EN ISO 13485:2016 Relatie met de huidige MDD en aankomende MDR Arjan van Drongelen Inhoud 1. Inleiding 2. Kwaliteitssystemen in MDD 3. Kwaliteitssystemen in MDR 4. Common specifications & standaarden
