1. Beschrijving werkgebieden / thema s
|
|
|
- Alfred Sanders
- 7 jaren geleden
- Aantal bezoeken:
Transcriptie
1 1. Beschrijving werkgebieden / thema s Nr 1 Thema Wetenschappelijke Achtergrond en Opzet van Onderzoek 2 Ethische en veiligheid overwegingen 3 Ontwikkeling en Regelgeving 4 Clinical Trial Operations (Projectorganisatie) 5 Site Management 6 Professioneel Leiderschap 7 Communicatie en teamwork 8 Data Management en Informatica Bevat medische kennis en kennis van wetenschappelijke methoden en technieken m.b.t. de opzet en analyse van medisch wetenschappelijk Bevat kennis en vaardigheden m.b.t. patiëntenzorg, aspecten van waarborging van de veiligheid van proefpersonen en veiligheid in de uitvoer van medisch wetenschappelijk Bevat kennis over ontwikkeling van geneesmiddelen / interventies en de regulering hiervan. Bevat kennis en vaardigheden rond studiemanagement, zorgdragen voor GCP compliance, veiligheidsmanagement (AE identificatie en rapportage) en omgaan met een onderzoeksproduct/medisch hulpmiddel/voedingssupplement. Bevat kennis en vaardigheden die nodig zijn op de onderzoekslocatie om een onderzoek uit te voeren, zoals aspecten m.b.t. uitvoer van studie werkzaamheden door de site, welke al dan niet gerelateerd zijn aan wetgeving of GCP (dus ook bv financiën en personeel). Bevat alle principes en praktijken van leiderschap en professioneel handelen in medisch wetenschappelijk Bevat kennis en vaardigheden van teamwork en communicatie nodig om medisch wetenschappelijk onderzoek te begeleiden en uit te voeren, zoals elementen van communicatie met het onderzoeksteam, tussen de onderzoeklocatie en sponsor/ CRO en met overheidsinstanties. Bevat kennis en vaardigheden over de manier van dataverzameling en -management gedurende medisch wetenschappelijk onderzoek, waaronder brongegevens, data entry, queries, QC en correcties en het concept van database lock. NVFG Toetsmatri Competentiegebieden_Basis CRA
2 2. Competenties en indicatoren specifiek voor dit thema Monitoren (Mon) o kiest voor de meest effectieve manier van monitoren van medisch wetenschappelijk onderzoek o monitort, registreert en rapporteert de (kwaliteit van de) uitvoer van een onderzoek o analyseert de risico s voor, en beoordeelt mogelijke impact van, de kwaliteit van de uitvoer van onderzoek o geeft duiding vanuit medische wetenschappelijke epertise aan de resultaten van de monitoring en signalering Communicatie (Com) o communiceert over doel en nut van monitoring en over keuzes van methoden en de financieel economische consequenties daarvan o rapporteert de bevindingen aan onderzoeksgroep en andere belanghebbenden (bv. verrichter, sponsor, uitvoerder, autoriteiten etc.) op een wijze die op de doelgroep is afgestemd o toont zich in staat tot een bij de situatie en inhoud van de communicatie passende professionele wijze van communiceren Samenwerken (SW) o neemt een faciliterende rol aan in de (multidisciplinaire) samenwerking met onderzoekslocaties en sponsor o onderhoudt een relevant netwerk in het kader van monitoren o is in staat samenwerking te organiseren en vereiste deelnemers aan samenwerkingsverbanden te motiveren tot participatie o toont zich fleibel in (de organisatie van) de samenwerking Kennis en wetenschap (KW) o heeft kennis van relevante wetten en regelgeving, internationale richtlijnen en operationele procedure beschrijvingen o verdiept zich in de medisch wetenschappelijke achtergrond van de onderzoeken, om voldoende inzicht te hebben en te kunnen toepassen in de uitvoering van de eigen taken o heeft voldoende kennis van onderzoeksmethodologie Ethisch handelen (Eth) o stelt het belang van deelnemende proefpersonen/patiënten centraal/voorop bij de (controle op de) opzet en uitvoering van onderzoek o spreekt de uitvoerenden aan op ethische aspecten van de (uitvoering van de) studie Organisatie (Org) o neemt initiatief tot opzetten en het in stand houden van de voor de uitvoer van een studie noodzakelijke structuur, processen en procedures, bijeenkomsten en trainingen o weet anderen in de organisatie en op site te activeren bij te dragen o houdt vanuit eigen inhoudelijke epertise toezicht op werkprocessen o werkt aantoonbaar effectief en kostenefficiënt en houdt daarbij rekening met schaarste of beperkingen inzake financiële middelen o documenteert adequaat en accuraat Professionaliteit (Prof) o onderhoudt kennis en verwerft waar nodig proactief aanvullende of nieuwe kennis o kent eigen grenzen op het gebied van de methodologie en uitvoering van wetenschappelijk onderzoek, organisatie en vaardigheden, en toont dit in de praktijk o maakt ethische afwegingen en is zich daarbij bewust van de eigen persoonlijke en professionele normen en waarden o is zich bewust van zijn maatschappelijke en professionele verantwoordelijkheid en handelt daarna o hanteert relevante juridische en ethische kaders NVFG Toetsmatri Competentiegebieden_Basis CRA
3 3. Toetskaart Toetsvormen: Kennistoets (): Een toets met vragen over beroepsgerichte, theoretische en vakgerichte kennis. Hiervoor kan de EMWO BROK, WMO-GCP toets gebruikt worden. Casustoets (): Een toets gebaseerd op een authentieke casus: een gevalsbeschrijving in een beroepscontet. Hierin staan gebeurtenissen, vraagstukken of problemen beschreven, zoals die voorkomen in de beroepspraktijk. De student lost dit op of beoordeelt de ontstane situatie. Vaardigheidheidstoets (VT): een toets waarbij de deelnemer demonstreert dat bepaalde beroepsvaardigheden correct en adequaat worden uitgevoerd. Bijvoorbeeld: Simulatietoetsen Je krijgt korter of langer van tevoren een opdracht die uitgevoerd moet worden onder het oog van beoordelaars. De toetsopdracht geeft aan wat de situatie is waarin de deelnemers handelt en (vaak) ook met wie hij te maken krijgt. Bijvoorbeeld: monitorvisite wrap up met investigator aan het eind van de monitor visite: De monitor krijgt een aantal lastige issues die ze met de investigator moet bespreken. Bijvoorbeeld: een groepsopdracht waarbij meerdere studenten centraal samenwerken met als doel het realiseren van een bepaald product: discussie over een onderwerp, een video analyseren, elkaar feedback geven, mogelijke oplossingen inventariseren. Evaluatie (E): evaluatie van de competenties en of vaardigheid door beoordelaar. Bijvoorbeeld tijdens co-visite. NVFG Toetsmatri Competentiegebieden_Basis CRA
4 Nr Thema Kenmerkende beroepssituaties Competentiegebieden Toetsvorm Mon Com SW KW Eth Org Prof 1.1 Beschrijf het proces van medisch wetenschappelijk onderzoek en de activiteiten die nodig zijn om de interventie beschikbaar te maken. 1.2 Beschrijf de specifieke processen en fasen die moeten worden doorlopen in het onderzoek om de regelgevende instantie in staat te stellen de handelsvergunning voor een product te kunnen goedkeuren Wetenschappelijke Toon kennis, begrip en inzicht van pathofysiologie en toicologie in het kader van medisch wetenschappelijk Achtergrond en Opzet van Onderzoek 1.4 Uitleggen van de onderdelen (statistiek, epidemiologie en klinische uitvoering) van medisch wetenschappelijk 1.5 Uitleggen van de studie opzet, rationale, eindpunten en verrichtingen van een onderzoeksprotocol. 2.1 Beschrijf de vereisten van de regelgevende instanties voor veiligheidsrapportage. 2.2 Vat de principes en methoden samen die gelden en worden toegepast waarmee proefpersonen een goede afweging kunnen maken tussen het risico en de meerwaarde van deelname aan een studie (ze tekenen mn ook voor het gebruik van hun samples in ICF procedure). 2.3 Beschrijf de vereisten voor de bescherming van rechten en privacy van proefpersonen volgens de lokale, nationale en internationale regelgeving en zorg voor de implementatie hiervan in alle fasen van een medisch Ethische en veiligheid wetenschappelijke studie. 2 overwegingen 2.4 Beschrijf de rapportage vereisten van de regelgevende instanties met betrekking tot de uitvoering van een medisch wetenschappelijk 2.5 Beschrijf de ethische kwesties die te maken hebben met het omgaan met kwetsbare bevolkingsgroepen en de behoefte aan additionele handelingen om hun bescherming te waarborgen. 2.6 Onderscheid de typen bijwerkingen die optreden tijdens medisch wetenschappelijk onderzoek, begrijp het identificatieproces voor AE's en pas de rapportage-vereisten richting de ethische commissie(s), sponsor en regelgevende instanties toe. 3.1 Vergelijk de voorschriften en richtlijnen van de regelgevende instanties met betrekking tot de goedkeuring en uitvoering van medisch wetenschappelijk Leg het doel, inhoud en proces rondom de schriftelijke toestemming (Informed Consent) van proefpersonen om 3 Ontwikkeling en deel te nemen aan medisch wetenschappelijk onderzoek uit en de inhoud van de belangrijkste documenten die de 3.2 Regelgeving bescherming van proefpersonen moet garanderen in medisch wetenschappelijk onderzoek en verifieer in de praktijk. 3.3 Beschrijf hoe de wereldwijde regelgeving en richtlijnen de bescherming en privacy van proefpersonen in medisch wetenschappelijk onderzoek waarborgen. 3.4 Vergelijk de standaard klinische zorg met de klinische behandeling van proefpersonen in een studie. Identificeer en leg uit welke specifieke procedurele taken, documentatie vereisten en toezicht 4.1 verantwoordelijkheden de belangrijkste partijen binnen medisch wetenschappelijk onderzoek hebben, waaronder onderzoekers, sponsors, CROs en de regelgevende instanties. Het controleren van gegevens en processen op geleide van een risicoclassificatie en indien van toepassing het risk 4 Clinical Trial Operations (Projectorganisatie) 4.2 management plan naleven. 4.3 Heeft kennis van de opzet, uitvoering en documentatie van medisch wetenschappelijke studies zoals vereist voor de naleving van Good Clinical Practice Guidelines. 4.4 Het beschrijven en uitvoeren van de rol en het proces van het monitoren van een studie. 4.5 Het uitvoeren van het monitorplan (op basis van SOPs en guidelines, SDV, rapport en soorten bezoeken). VT 4.6 Beschrijf de verschillende methodes waarmee veiligheids-issues geïdentificeerd en gemanaged worden. 4.7 Heeft kennis van de vereisten documentatie en procedures betreffende MEC, BI en RvB NVFG Toetsmatri Competentiegebieden_Basis CRA
5 5 Site Management Professioneel Leiderschap Communicatie en teamwork Data Management en Informatica 5.1 Verklaar waarom in- en eclusie criteria in het protocol zijn opgenomen zodat de juiste proefpersonen voor het onderzoek te worden geselecteerd en worden beschermd en dit ook verifiëren 5.2 Beschrijf hoe het onderzoeksproduct opgeslagen, verstrekt en gemonitord moet worden. 5.3 Leg uit wat essentiële GCP documenten zijn en hoe ze gearchiveerd en eventueel gebruikt dienen te worden. 5.4 Beschrijf de rollen en verantwoordelijkheden van het onderzoeksteam zoals gedefinieerd door Good Clinical Practice richtlijnen. 5.5 Beschrijf de randvoorwaarden en het proces van site selectie. In staat zijn om ethische en professionele conflicten die gelieerd zijn aan het doen van medisch wetenschappelijk 6.1 onderzoek te identificeren en escaleren en procedures ter voorkomen van fraude en misconduct in samenwerking met het team te implementeren. 6.2 Beschrijf het doel van audits en inspecties van medisch wetenschappelijke studies. 6.3 Pas vaardigheden en effectieve training methoden toe om risico's te beheren en is in staat de kwaliteit in de E uitvoering van een medisch wetenschappelijke studie te verbeteren. 6.4 Identificeer en pas de richtlijnen en ethische codes van medisch wetenschappelijk onderzoek toe. VT 7.1 Omschrijf de principes en praktijk van het samenwerken op het gebied van medisch wetenschappelijk onderzoek en de rol van de monitor daar in. 7.2 Identificeer en implementeer processen om ethische en professionele conflicten te voorkomen en / of managen. 8.1 Controleert het proces en voorwaarden van elektronische data verzameling (EDC) en het belang van IT in data verzameling en management. 8.2 Controleert de volgorde van onderzoeksmetingen en de daarmee gegenereerde gegevens binnen een medisch wetenschappelijk 8.3 Controleert de ICH-GCP vereisten op het gebied van data correctie en queries. NVFG Toetsmatri Competentiegebieden_Basis CRA
WAAROM MAG IEDEREEN ZICH CRA NOEMEN?
 WAAROM MAG IEDEREEN ZICH CRA NOEMEN? Geen keurmerk voor een goede CRA, geen kaders voor kwaliteitsbewaking Op dit moment stelt niemand nascholing verplicht voor ervaren CRA s 1 PROFESSIONEEL KLINISCH ONDERZOEK
WAAROM MAG IEDEREEN ZICH CRA NOEMEN? Geen keurmerk voor een goede CRA, geen kaders voor kwaliteitsbewaking Op dit moment stelt niemand nascholing verplicht voor ervaren CRA s 1 PROFESSIONEEL KLINISCH ONDERZOEK
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U9 Monitoren Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies Versiedatum Hoofdstuk Versiedatum Hoofdstuk
Standard Operating Procedure STZ SOP: U9 Monitoren Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies Versiedatum Hoofdstuk Versiedatum Hoofdstuk
Monitorplan voorbeeld
 Monitorplan voorbeeld Protocol Er moet in het protocol beschreven worden dat er monitoring plaatsvindt (zie ook CCMO voorbeeld template). Het monitoringplan mag als bijlage worden toegevoegd (in dat geval
Monitorplan voorbeeld Protocol Er moet in het protocol beschreven worden dat er monitoring plaatsvindt (zie ook CCMO voorbeeld template). Het monitoringplan mag als bijlage worden toegevoegd (in dat geval
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U10 Audit Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: U10 Audit Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum Opmerkingen
Monitoren vs auditen. CRA dag 21 april 2016
 Monitoren vs auditen CRA dag 21 april 2016 Introductie Freelance consultant, mede oprichter TAPAS Group B.V. Mede oprichter/directeur van CRA B.V. Medical Adviser Yamanouchi Pharma Clinical trial monitor
Monitoren vs auditen CRA dag 21 april 2016 Introductie Freelance consultant, mede oprichter TAPAS Group B.V. Mede oprichter/directeur van CRA B.V. Medical Adviser Yamanouchi Pharma Clinical trial monitor
De rol van de Contract Research Organisatie (CRO) Klinisch onderzoek
 De rol van de Contract Research Organisatie (CRO) in klinisch geneesmiddelenonderzoek Klinisch onderzoek Inhoud Aanleiding CRO project Methode en resultaten» Werkwijze en resultaten foto van het veld vragenlijst»
De rol van de Contract Research Organisatie (CRO) in klinisch geneesmiddelenonderzoek Klinisch onderzoek Inhoud Aanleiding CRO project Methode en resultaten» Werkwijze en resultaten foto van het veld vragenlijst»
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL5 Protocolamendement (lokaal) Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: VL5 Protocolamendement (lokaal) Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL2 Aanpassen proefpersoneninformatie / toestemmingsformulier aan lokale situatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen
Standard Operating Procedure STZ SOP: VL2 Aanpassen proefpersoneninformatie / toestemmingsformulier aan lokale situatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen
Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen
 Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen Afdeling Farmaceutische Bedrijven, Klinisch Onderzoek Good Clinical Practice Inhoud Wat doet de IGJ aan toezicht op klinisch
Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen Afdeling Farmaceutische Bedrijven, Klinisch Onderzoek Good Clinical Practice Inhoud Wat doet de IGJ aan toezicht op klinisch
Toezicht op kwaliteitsborging: ken uw verantwoordelijkheden
 Toezicht op kwaliteitsborging: ken uw verantwoordelijkheden Elysée Hille Karina van Wonderen namens deelteam Klinisch Onderzoek-GCP Afdeling Farmaceutische Bedrijven Workshop Kwaliteitsbewaking door samenwerking
Toezicht op kwaliteitsborging: ken uw verantwoordelijkheden Elysée Hille Karina van Wonderen namens deelteam Klinisch Onderzoek-GCP Afdeling Farmaceutische Bedrijven Workshop Kwaliteitsbewaking door samenwerking
Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) Team Klinisch Onderzoek
 Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) 2014-2016 Team Klinisch Onderzoek Toezicht op IIT 2014-2016 Aanleiding en werkwijze Bevindingen vanuit de praktijk Conclusies en aandachtspunten
Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) 2014-2016 Team Klinisch Onderzoek Toezicht op IIT 2014-2016 Aanleiding en werkwijze Bevindingen vanuit de praktijk Conclusies en aandachtspunten
Site selectie visite checklist
 Site selectie visite checklist Informatie sponsor: Naam sponsor: Contactpersoon: Functie: Afdeling: Telefoonnummer : Email : Informatie onderzoekslocatie: Naam onderzoekslocatie : Naam onderzoeker: Functie:
Site selectie visite checklist Informatie sponsor: Naam sponsor: Contactpersoon: Functie: Afdeling: Telefoonnummer : Email : Informatie onderzoekslocatie: Naam onderzoekslocatie : Naam onderzoeker: Functie:
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen. Farmaceutische Bedrijven Deelteam Klinisch Onderzoek
 Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
Antwoorden CRO-vragenlijst - foto van het veld
 Antwoorden CRO-vragenlijst - foto van het veld In samenwerking met het RIVM heeft de Inspectie voor de Gezondheidszorg (IGZ) een digitale vragenlijst ontwikkeld die bestond uit drie delen (zie Vragenlijst
Antwoorden CRO-vragenlijst - foto van het veld In samenwerking met het RIVM heeft de Inspectie voor de Gezondheidszorg (IGZ) een digitale vragenlijst ontwikkeld die bestond uit drie delen (zie Vragenlijst
Aanvraagformulier REGISTRATIE oncologie monitor
 Aanvraagformulier REGISTRATIE oncologie monitor 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:... Geboorteplaats:... Werkzaam bij: Organisatie + Afdeling:...
Aanvraagformulier REGISTRATIE oncologie monitor 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:... Geboorteplaats:... Werkzaam bij: Organisatie + Afdeling:...
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VC8 Beoordeling amendement toetsende commissie (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure STZ SOP: VC8 Beoordeling amendement toetsende commissie (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
RISK BASED MONITORING IIS FROM AN ACADEMIC PERSPECTIVE; SURGICAL SPECIALTIES
 RISK BASED MONITORING IIS FROM AN ACADEMIC PERSPECTIVE; SURGICAL SPECIALTIES 8 Oktober 2014, DCTF Onderzoeksbureau Divisie Heelkundige Specialismen UMC Utrecht Marianne van Es-Gulinck, arts, F.F.P.M. RISK
RISK BASED MONITORING IIS FROM AN ACADEMIC PERSPECTIVE; SURGICAL SPECIALTIES 8 Oktober 2014, DCTF Onderzoeksbureau Divisie Heelkundige Specialismen UMC Utrecht Marianne van Es-Gulinck, arts, F.F.P.M. RISK
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A2 Archiveren studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A2 Archiveren studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
1. Voorafgaand aan de klinische fase van het onderzoek
 Essentiële documenten Bron: Richtsnoer voor good clinical practice (CPMP/ICH/135/95) De verwijzingen in dit document verwijzen naar de artikelen in bovenstaand document. 1. Voorafgaand aan de klinische
Essentiële documenten Bron: Richtsnoer voor good clinical practice (CPMP/ICH/135/95) De verwijzingen in dit document verwijzen naar de artikelen in bovenstaand document. 1. Voorafgaand aan de klinische
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U1 Identificatie, werving en pre-screening proefpersonen Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure STZ SOP: U1 Identificatie, werving en pre-screening proefpersonen Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VC9 Proefpersonen- en aansprakelijkheidsverzekering (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure STZ SOP: VC9 Proefpersonen- en aansprakelijkheidsverzekering (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Toezicht op IIT: bevindingen vanuit de praktijk
 Toezicht op IIT: bevindingen vanuit de praktijk Elysée Hille, senior inspecteur namens deelteam KO-GCP Teamcoördinator KO-GCP/PhV/GZH Afdeling Farmaceutische Bedrijven Wat doet de IGZ? Toezicht op klinisch
Toezicht op IIT: bevindingen vanuit de praktijk Elysée Hille, senior inspecteur namens deelteam KO-GCP Teamcoördinator KO-GCP/PhV/GZH Afdeling Farmaceutische Bedrijven Wat doet de IGZ? Toezicht op klinisch
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U11 Voortgangsrapportage Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: U11 Voortgangsrapportage Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Titel: Good Clinical Practice & Monitoring. Initiation Investigator Driven Studies. Versie: 14-jan-2013
 Titel: Good Clinical Practice & Monitoring Initiation Investigator Driven Studies Inhoud Wet- en regelgeving/declaration of Helsinki Good Clinical Practice Patiënteninformatie/ informed consent Basisvereisten
Titel: Good Clinical Practice & Monitoring Initiation Investigator Driven Studies Inhoud Wet- en regelgeving/declaration of Helsinki Good Clinical Practice Patiënteninformatie/ informed consent Basisvereisten
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A1 Afsluiting studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A1 Afsluiting studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U4 Registratie /randomisatie procedure Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum
Standard Operating Procedure STZ SOP: U4 Registratie /randomisatie procedure Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum
Klinische studies. Veel meer dan een extra tube
 Klinische studies Veel meer dan een extra tube Good Clinical Practice Het geheel van kwaliteitseisen op ethisch en wetenschappelijk gebied, die internationaal zijn erkend en moeten worden gerespecteerd
Klinische studies Veel meer dan een extra tube Good Clinical Practice Het geheel van kwaliteitseisen op ethisch en wetenschappelijk gebied, die internationaal zijn erkend en moeten worden gerespecteerd
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U5 Datamanagement Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: U5 Datamanagement Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Vragenlijst zelfevaluatie RvC
 Vragenlijst zelfevaluatie RvC Naam: Datum: 1. Verantwoordelijkheden en samenstelling van de RvC 1.1 Ik heb een duidelijk beeld van het mandaat en de verantwoordelijk heden van de RvC. 1.2 De RvC heeft
Vragenlijst zelfevaluatie RvC Naam: Datum: 1. Verantwoordelijkheden en samenstelling van de RvC 1.1 Ik heb een duidelijk beeld van het mandaat en de verantwoordelijk heden van de RvC. 1.2 De RvC heeft
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: O3 Ontwikkelen, implementeren en beheren van SOP s Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies
Standard Operating Procedure STZ SOP: O3 Ontwikkelen, implementeren en beheren van SOP s Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies
Aanvraagformulier REGISTRATIE oncologie datamanager
 Aanvraagformulier REGISTRATIE oncologie datamanager 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:.... Geboorteplaats:.... Werkzaam bij: Organisatie +
Aanvraagformulier REGISTRATIE oncologie datamanager 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:.... Geboorteplaats:.... Werkzaam bij: Organisatie +
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A4 Publicatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A4 Publicatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Henk Jan Out, Paul van Meurs en Rudolf van Olden. Van eerste humane toediening tot algemeen gebruik
 VII 1 Introductie tot de farmaceutische geneeskunde................................ 1 Henk Jan Out, Paul van Meurs en Rudolf van Olden I Van eerste humane toediening tot algemeen gebruik 2 Exploratory
VII 1 Introductie tot de farmaceutische geneeskunde................................ 1 Henk Jan Out, Paul van Meurs en Rudolf van Olden I Van eerste humane toediening tot algemeen gebruik 2 Exploratory
Model informatiebrief medisch onderwijsonderzoek Met voorbeeldpassages versie juli 2017
 Model informatiebrief medisch onderwijsonderzoek Met voorbeeldpassages versie juli 2017 De brief kan voor studenten op HBO/WO niveau geschreven worden omdat de doelgroep in onderwijsonderzoek meestal studenten
Model informatiebrief medisch onderwijsonderzoek Met voorbeeldpassages versie juli 2017 De brief kan voor studenten op HBO/WO niveau geschreven worden omdat de doelgroep in onderwijsonderzoek meestal studenten
CRO s kwaliteit en toegevoegde waarde
 CRO s kwaliteit en toegevoegde waarde dr. Annejet P. Meijler Programmadirecteur Geneesmiddelen IGZ 1 Medisch-wetenschappelijk onderzoek 4 april 2011 Deze workshop Inleiding I prof. Herman Pieterse Inleiding
CRO s kwaliteit en toegevoegde waarde dr. Annejet P. Meijler Programmadirecteur Geneesmiddelen IGZ 1 Medisch-wetenschappelijk onderzoek 4 april 2011 Deze workshop Inleiding I prof. Herman Pieterse Inleiding
Toezicht op uitvoering kan beter. Aanbevelingen uit rapport Toezicht op Medisch Wetenschappelijk Onderzoek met mensen
 Toezicht op uitvoering kan beter Aanbevelingen uit rapport Toezicht op Medisch Wetenschappelijk Onderzoek met mensen Najaarsbijeenkomst NVMETC 25 november 2015 Kor Grit, Jacqueline van Oijen 2 Inhoud presentatie
Toezicht op uitvoering kan beter Aanbevelingen uit rapport Toezicht op Medisch Wetenschappelijk Onderzoek met mensen Najaarsbijeenkomst NVMETC 25 november 2015 Kor Grit, Jacqueline van Oijen 2 Inhoud presentatie
FUNCTIEBESCHRIJVING BELEIDSMEDEWERKER ONDERZOEKSINFRASTRUCTUUR
 FUNCTIEBESCHRIJVING BELEIDSMEDEWERKER ONDERZOEKSINFRASTRUCTUUR A. DOEL VAN DE FUNCTIE: Het beleidsthema vanuit theoretische en praktische deskundigheid implementeren en uitbouwen teneinde toepassingen
FUNCTIEBESCHRIJVING BELEIDSMEDEWERKER ONDERZOEKSINFRASTRUCTUUR A. DOEL VAN DE FUNCTIE: Het beleidsthema vanuit theoretische en praktische deskundigheid implementeren en uitbouwen teneinde toepassingen
Workshop 4: Scholing: heden en toekomst Welkom! Works
 Workshop 4: Scholing: heden en toekomst Welkom! Works Welke kennis en kunde is nodig voor het doen van klinisch onderzoek? Klinisch onderzoek in Nederland: Beter, veilig en snel. Inbreng van de patiënt
Workshop 4: Scholing: heden en toekomst Welkom! Works Welke kennis en kunde is nodig voor het doen van klinisch onderzoek? Klinisch onderzoek in Nederland: Beter, veilig en snel. Inbreng van de patiënt
Taxanomie van Bloom en de kunst van het vragen stellen. Anouk Mulder verschil in talent
 Onthouden Kunnen ophalen van specifieke informatie, variërend van feiten tot complete theorieën Opslaan en ophalen van informatie (herkennen) Kennis van data, gebeurtenissen, plaatsen Kennis van belangrijkste
Onthouden Kunnen ophalen van specifieke informatie, variërend van feiten tot complete theorieën Opslaan en ophalen van informatie (herkennen) Kennis van data, gebeurtenissen, plaatsen Kennis van belangrijkste
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U2 Informed consent Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: U2 Informed consent Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Toezicht op klinisch onderzoek - bevindingen vanuit de praktijk
 Toezicht op klinisch onderzoek - bevindingen vanuit de praktijk Namens Deelprogramma Klinisch Onderzoek, IGZ Spreker Dr. ir. J. Eland-Gerritsen Coördinerend/Specialistisch Senior inspecteur Inhoud Toezicht
Toezicht op klinisch onderzoek - bevindingen vanuit de praktijk Namens Deelprogramma Klinisch Onderzoek, IGZ Spreker Dr. ir. J. Eland-Gerritsen Coördinerend/Specialistisch Senior inspecteur Inhoud Toezicht
Standard Operating Procedure
 Standard Operating Procedure SOP: V9 Initiatievisite Auteur Naam: Functie instelling/afdeling Judie van den Elshout Staffunctionaris Wetenschapsbureau Wetenschapsbureau / Cluster Leerhuis Handtekening:...
Standard Operating Procedure SOP: V9 Initiatievisite Auteur Naam: Functie instelling/afdeling Judie van den Elshout Staffunctionaris Wetenschapsbureau Wetenschapsbureau / Cluster Leerhuis Handtekening:...
Rijke Lessen. zetten je aan het denken. Handleiding(etje) Minka Dumont 26 november 2009 SLO - Landelijke Plusklasnetwerkdag
 Rijke Lessen zetten je aan het denken Minka Dumont 2009 www.lesmateriaalvoorhoogbegaafden.com Handleiding(etje) Minka Dumont 26 november 2009 SLO - Landelijke Plusklasnetwerkdag Onthouden Kunnen ophalen
Rijke Lessen zetten je aan het denken Minka Dumont 2009 www.lesmateriaalvoorhoogbegaafden.com Handleiding(etje) Minka Dumont 26 november 2009 SLO - Landelijke Plusklasnetwerkdag Onthouden Kunnen ophalen
De 6 Friesland College-competenties.
 De 6 Friesland College-competenties. Het vermogen om met een open enthousiaste houding nieuwe dingen aan te pakken. Het vermogen jezelf steeds beter te leren kennen. Het vermogen om in te schatten in welke
De 6 Friesland College-competenties. Het vermogen om met een open enthousiaste houding nieuwe dingen aan te pakken. Het vermogen jezelf steeds beter te leren kennen. Het vermogen om in te schatten in welke
Patiëntenparticipatiecultuur in ziekenhuizen Implementatietrajecten 2015
 Patiëntenparticipatiecultuur in ziekenhuizen Implementatietrajecten 2015 Ondersteuningsplan Meerjarenplan 2013 2017 Prof. dr. Ann Van Hecke Prof. dr. Kristof Eeckloo Simon Malfait Doel van de begeleidingssessies
Patiëntenparticipatiecultuur in ziekenhuizen Implementatietrajecten 2015 Ondersteuningsplan Meerjarenplan 2013 2017 Prof. dr. Ann Van Hecke Prof. dr. Kristof Eeckloo Simon Malfait Doel van de begeleidingssessies
Aanvraagformulier REGISTRATIE centraal oncologie datamanager
 Aanvraagformulier REGISTRATIE centraal oncologie datamanager 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:... Geboorteplaats:... Werkzaam bij: Organisatie
Aanvraagformulier REGISTRATIE centraal oncologie datamanager 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:... Geboorteplaats:... Werkzaam bij: Organisatie
3 april 2014 Partnership in Clinical Trials Martijn Griep, PhD Associate Director Kwaliteit en Naleving Janssen GCO Benelux, Tilburg
 Ideale site ideale samenwerking in clinical trials 3 april 2014 Partnership in Clinical Trials Martijn Griep, PhD Associate Director Kwaliteit en Naleving Janssen GCO Benelux, Tilburg MICROSOFT CORPORATION
Ideale site ideale samenwerking in clinical trials 3 april 2014 Partnership in Clinical Trials Martijn Griep, PhD Associate Director Kwaliteit en Naleving Janssen GCO Benelux, Tilburg MICROSOFT CORPORATION
Jouw GCP up-to-date in 45 minuten. Marieke Meulemans, oprichter GCP Central
 Jouw GCP up-to-date in 45 minuten Marieke Meulemans, oprichter GCP Central Waarom een GCP update tijdens de CRA dag? Gedreven Meesterschap. Meesterschap is vakmanschap. Vakmanschap is beheersing van het
Jouw GCP up-to-date in 45 minuten Marieke Meulemans, oprichter GCP Central Waarom een GCP update tijdens de CRA dag? Gedreven Meesterschap. Meesterschap is vakmanschap. Vakmanschap is beheersing van het
Richtlijnen voor onderzoek. met vrijwilligers in het AMC. met geneesmiddelen, hulpmiddelen of ingrepen die niet eerder bij de mens zijn toegepast
 Richtlijnen voor onderzoek met vrijwilligers in het AMC en met geneesmiddelen, hulpmiddelen of ingrepen die niet eerder bij de mens zijn toegepast bij patiënten in het AMC augustus 2008 Inhoud Inleiding
Richtlijnen voor onderzoek met vrijwilligers in het AMC en met geneesmiddelen, hulpmiddelen of ingrepen die niet eerder bij de mens zijn toegepast bij patiënten in het AMC augustus 2008 Inhoud Inleiding
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U8 Melding van (Serious) Adverse Events en SUSARs Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies
Standard Operating Procedure STZ SOP: U8 Melding van (Serious) Adverse Events en SUSARs Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies
Kwaliteit: Minder is meer
 Kwaliteit: Minder is meer Kwaliteit in klinisch onderzoek met medische hulpmiddelen Jako Pranger QA Manager Cardialysis 9 Nov 2012 Kwaliteit en integriteit Mensgebonden onderzoek Trends in kwaliteitsbeleving
Kwaliteit: Minder is meer Kwaliteit in klinisch onderzoek met medische hulpmiddelen Jako Pranger QA Manager Cardialysis 9 Nov 2012 Kwaliteit en integriteit Mensgebonden onderzoek Trends in kwaliteitsbeleving
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U6 Studie medicatie Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: U6 Studie medicatie Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Toelichting bij de Voortgangsrapportage Maatschappelijke Zorg
 Naam: Klas: praktijkbegeleider: Werkplek: Toelichting bij de Voortgangsrapportage Maatschappelijke Zorg Gedurende de opleiding werken de studenten in de praktijk aan praktijkopdrachten. Een schooljaar
Naam: Klas: praktijkbegeleider: Werkplek: Toelichting bij de Voortgangsrapportage Maatschappelijke Zorg Gedurende de opleiding werken de studenten in de praktijk aan praktijkopdrachten. Een schooljaar
De Taxonomie van Bloom Toelichting
 De Taxonomie van Bloom Toelichting Een van de meest gebruikte manier om verschillende kennisniveaus in te delen, is op basis van de taxonomie van Bloom. Deze is tussen 1948 en 1956 ontwikkeld door de onderwijspsycholoog
De Taxonomie van Bloom Toelichting Een van de meest gebruikte manier om verschillende kennisniveaus in te delen, is op basis van de taxonomie van Bloom. Deze is tussen 1948 en 1956 ontwikkeld door de onderwijspsycholoog
Workshop voorbereiden Authentieke instructiemodel
 Workshop voorbereiden Authentieke instructiemodel Workshop voorbereiden Uitleg Start De workshop start met een echte, herkenbare en uitdagende situatie. (v.b. het is een probleem, een prestatie, het heeft
Workshop voorbereiden Authentieke instructiemodel Workshop voorbereiden Uitleg Start De workshop start met een echte, herkenbare en uitdagende situatie. (v.b. het is een probleem, een prestatie, het heeft
STATEC trial praktische uitvoering Hilde Dijcker
 STATEC trial praktische uitvoering 17-04-2018 Hilde Dijcker Inhoud IKNL trialbureau Site activation Datamanagement Monitoring IKNL Trialbureau Site activation: - Ine Leenen en Hilde Dijcker Kwaliteit van
STATEC trial praktische uitvoering 17-04-2018 Hilde Dijcker Inhoud IKNL trialbureau Site activation Datamanagement Monitoring IKNL Trialbureau Site activation: - Ine Leenen en Hilde Dijcker Kwaliteit van
Monitoring van Investigator Initiated onderzoek
 Monitoring van Investigator Initiated onderzoek V1.0 Angela Vlug Clinical Research Bureau VUmc Wat is een IIS (volgens de NFU) Onderzoek waarvoor de raad van bestuur van een (universitair) medisch centrum
Monitoring van Investigator Initiated onderzoek V1.0 Angela Vlug Clinical Research Bureau VUmc Wat is een IIS (volgens de NFU) Onderzoek waarvoor de raad van bestuur van een (universitair) medisch centrum
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik
 EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
Het EPD, hoe deal ik ermee? NVFG - Nederlandse Vereniging voor Farmaceutische Geneeskunde. CRA dag 25 april 2013
 0 Het EPD, hoe deal ik ermee? NVFG - Nederlandse Vereniging voor Farmaceutische Geneeskunde CRA dag 25 april 2013 Het EPD, hoe deal ik ermee? Moderators: Sharon Anderson Hans Martens Presentators: Robbert
0 Het EPD, hoe deal ik ermee? NVFG - Nederlandse Vereniging voor Farmaceutische Geneeskunde CRA dag 25 april 2013 Het EPD, hoe deal ik ermee? Moderators: Sharon Anderson Hans Martens Presentators: Robbert
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL4 Investigator Site File Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: VL4 Investigator Site File Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
PR V1. Beroepscompetentie- profiel RBCZ therapeuten
 PR 180724 V1 Beroepscompetentie- profiel Afgeleid van de niveaubepaling NLQF, niveau 6 heeft RBCZ kerncompetenties benoemd voor de complementair/alternatief therapeut. Als uitgangspunt zijn de algemene
PR 180724 V1 Beroepscompetentie- profiel Afgeleid van de niveaubepaling NLQF, niveau 6 heeft RBCZ kerncompetenties benoemd voor de complementair/alternatief therapeut. Als uitgangspunt zijn de algemene
ALGEMENE INSTRUCTIE EXAMINERING BEROEPSOPDRACHT A (BOL)
 ALGEMENE INSTRUCTIE EXAMINERING BEROEPSOPDRACHT A (BOL) VOOR STUDENTEN EN BEOORDELAARS Datum: AUG 2015 Crebo 95 ALGEMENE INLEIDING Elke beroepstaak bestaat uit een aantal beroepsopdrachten dat de student
ALGEMENE INSTRUCTIE EXAMINERING BEROEPSOPDRACHT A (BOL) VOOR STUDENTEN EN BEOORDELAARS Datum: AUG 2015 Crebo 95 ALGEMENE INLEIDING Elke beroepstaak bestaat uit een aantal beroepsopdrachten dat de student
Laag Vaardigheden Leerdoelen Formulering van vragen /opdrachten
 Blooms taxonomie Laag Vaardigheden Leerdoelen Formulering van vragen /opdrachten Evalueren Evalueren = de vaardigheid om de waarde van iets (literatuur, onderzoeksrapport, presentatie etc) te kunnen beoordelen
Blooms taxonomie Laag Vaardigheden Leerdoelen Formulering van vragen /opdrachten Evalueren Evalueren = de vaardigheid om de waarde van iets (literatuur, onderzoeksrapport, presentatie etc) te kunnen beoordelen
Resultaten CRO-vragenlijst - foto van het veld
 Resultaten CRO-vragenlijst - foto van het veld Dee1: Algemene kenmerken van de organisatie Dit hoofdstuk beschrijft de kenmerken, werkzaamheden en de kwaliteit van 9 CRO s waaraan verrrichters taken en
Resultaten CRO-vragenlijst - foto van het veld Dee1: Algemene kenmerken van de organisatie Dit hoofdstuk beschrijft de kenmerken, werkzaamheden en de kwaliteit van 9 CRO s waaraan verrrichters taken en
Aanmelden WMO-plichtig onderzoek
 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd wordt bij het aanmelden van onderzoek dat onder de WMO valt en waarbij ZGV optreedt als deelnemend centrum. Voordat
Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd wordt bij het aanmelden van onderzoek dat onder de WMO valt en waarbij ZGV optreedt als deelnemend centrum. Voordat
Kwaliteitsborging vanuit academisch perspectief DCTF jaarcongres 2016
 Kwaliteitsborging vanuit academisch perspectief DCTF jaarcongres 2016 Gemma Voss 5 oktober 2016 Mensgebonden onderzoek (WMO) in Nederland 2015 CCMO-jaarverslag 2015 CCMO-jaarverslag 2015 Mensgebonden onderzoek
Kwaliteitsborging vanuit academisch perspectief DCTF jaarcongres 2016 Gemma Voss 5 oktober 2016 Mensgebonden onderzoek (WMO) in Nederland 2015 CCMO-jaarverslag 2015 CCMO-jaarverslag 2015 Mensgebonden onderzoek
Aanmelden medischwetenschappelijk
 Aanmelden medischwetenschappelijk onderzoek SOP Aanmelden WMO-plichtig onderzoek_versie juli 2016.doc Pagina 1 van 10 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd
Aanmelden medischwetenschappelijk onderzoek SOP Aanmelden WMO-plichtig onderzoek_versie juli 2016.doc Pagina 1 van 10 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd
Het Clinical Research Bureau (CRB) van VUmc
 1 Het Clinical Research Bureau (CRB) van VUmc Angela Vlug Kwaliteitsborging van mensgebonden onderzoek 1 Het Clinical Research Bureau heeft als doel om optimale kwaliteit van de uitvoering van mensgebonden
1 Het Clinical Research Bureau (CRB) van VUmc Angela Vlug Kwaliteitsborging van mensgebonden onderzoek 1 Het Clinical Research Bureau heeft als doel om optimale kwaliteit van de uitvoering van mensgebonden
Ervaringen met document X
 Martini Ziekenhuis Groningen Ervaringen met document X Ellen Rusch, wetenschappelijk medewerker Wetenschappelijk Instituut Wat gaan we doen? Structuur lokale haalbaarheid Martini Ziekenhuis Het werken
Martini Ziekenhuis Groningen Ervaringen met document X Ellen Rusch, wetenschappelijk medewerker Wetenschappelijk Instituut Wat gaan we doen? Structuur lokale haalbaarheid Martini Ziekenhuis Het werken
Arbo- en Milieudeskundige
 Arbo- en Milieudeskundige Doel Ontwikkelen van beleid, adviseren, ondersteunen en begeleiden van management, medewerkers en studenten, alsmede bijdragen aan de handhaving van wet- en regelgeving, binnen
Arbo- en Milieudeskundige Doel Ontwikkelen van beleid, adviseren, ondersteunen en begeleiden van management, medewerkers en studenten, alsmede bijdragen aan de handhaving van wet- en regelgeving, binnen
Bijlage V. Bij het advies van de Commissie NLQF EQF. Tabel vergelijking NLQF-niveaus 5 t/m 8 en Dublin descriptoren.
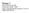 Bijlage V Bij het advies van de Commissie NLQF EQF Tabel vergelijking NLQF-niveaus 5 t/m 8 en. Tabel ter vergelijking NLQF niveaus 5 t/m 8 en Dublindescriptoren NLQF Niveau 5 Context Een onbekende, wisselende
Bijlage V Bij het advies van de Commissie NLQF EQF Tabel vergelijking NLQF-niveaus 5 t/m 8 en. Tabel ter vergelijking NLQF niveaus 5 t/m 8 en Dublindescriptoren NLQF Niveau 5 Context Een onbekende, wisselende
ISO 14001:2015 Readiness Review
 ISO 14001:2015 Readiness Review Organisatie Adres Certificaat Nr. Contactpersoon Functie Telefoon Email BSI is vastbesloten ervoor te zorgen dat klanten die willen certificeren op ISO 14001:2015 een soepele
ISO 14001:2015 Readiness Review Organisatie Adres Certificaat Nr. Contactpersoon Functie Telefoon Email BSI is vastbesloten ervoor te zorgen dat klanten die willen certificeren op ISO 14001:2015 een soepele
Toetsingskader nwmo. Peggy Manders 4 november 2016 Symposium V&VN Research Professionals
 Toetsingskader nwmo Peggy Manders 4 november 2016 Symposium V&VN Research Professionals Biobank: definitie en rationale Wat is een biobank? + + Waarom een biobank starten? Verbeteren gezondheidszorg voor
Toetsingskader nwmo Peggy Manders 4 november 2016 Symposium V&VN Research Professionals Biobank: definitie en rationale Wat is een biobank? + + Waarom een biobank starten? Verbeteren gezondheidszorg voor
(Industrie geïnitieerd) Onderzoek in de STZ Omgeving' Joep Dille (j.dille@isala.nl) Manager wetenschapsbureau Isala klinieken, Zwolle
 (Industrie geïnitieerd) Onderzoek in de STZ Omgeving' Joep Dille (j.dille@isala.nl) Manager wetenschapsbureau Isala klinieken, Zwolle Take home message Ga op zoek naar wat mensen drijft en sluit daarbij
(Industrie geïnitieerd) Onderzoek in de STZ Omgeving' Joep Dille (j.dille@isala.nl) Manager wetenschapsbureau Isala klinieken, Zwolle Take home message Ga op zoek naar wat mensen drijft en sluit daarbij
Stappenplan naar GDPR compliance
 Stappenplan naar GDPR compliance Stappenplan voor compliance met de Algemene Verordening Gegevensbescherming Het Europees Parlement heeft op 14 april 2016 de Algemene Verordening Gegevensbescherming (AVG)
Stappenplan naar GDPR compliance Stappenplan voor compliance met de Algemene Verordening Gegevensbescherming Het Europees Parlement heeft op 14 april 2016 de Algemene Verordening Gegevensbescherming (AVG)
Stappenplan naar GDPR compliance
 Stappenplan naar GDPR compliance In samenwerking met ESET heeft Mazars een whitepaper geschreven met als doel om meer inzicht te geven in het ontstaan en de gevolgen van de General Data Protection Regulation
Stappenplan naar GDPR compliance In samenwerking met ESET heeft Mazars een whitepaper geschreven met als doel om meer inzicht te geven in het ontstaan en de gevolgen van de General Data Protection Regulation
INFORMATIEBLAD. Maart 2011
 INFORMATIEBLAD AANMELDING TRIALBUREAU/DATACENTRUM Maart 2011 Kanker zo snel mogelijk terugdringen en onder controle brengen. We zijn er voor mensen die leven met kanker en de mensen die met hen samenleven.
INFORMATIEBLAD AANMELDING TRIALBUREAU/DATACENTRUM Maart 2011 Kanker zo snel mogelijk terugdringen en onder controle brengen. We zijn er voor mensen die leven met kanker en de mensen die met hen samenleven.
Competenties van de klinisch psycholoog. Ger Keijsers
 Competenties van de klinisch psycholoog Ger Keijsers Onderwerpen 1. achtergrond 2. CanMEDS 3. competenties KP 4. themakaarten 5. waterscheiding 6. implementatie Achtergrond competentiegericht opleiden
Competenties van de klinisch psycholoog Ger Keijsers Onderwerpen 1. achtergrond 2. CanMEDS 3. competenties KP 4. themakaarten 5. waterscheiding 6. implementatie Achtergrond competentiegericht opleiden
De Nederlandse Vereniging voor Farmaceutische Geneeskunde (NVFG) is een wetenschappelijke beroepsvereniging die professionals werkzaam op het gebied
 De Nederlandse Vereniging voor Farmaceutische Geneeskunde (NVFG) is een wetenschappelijke beroepsvereniging die professionals werkzaam op het gebied van klinisch onderzoek, registratie, bijwerkingenrapportage
De Nederlandse Vereniging voor Farmaceutische Geneeskunde (NVFG) is een wetenschappelijke beroepsvereniging die professionals werkzaam op het gebied van klinisch onderzoek, registratie, bijwerkingenrapportage
Bijlage V. Bij het advies van de Commissie NLQF EQF. Tabel vergelijking NLQF-niveaus 5 t/m 8 en Dublin descriptoren.
 Bijlage V Bij het advies van de Commissie NLQF EQF Tabel vergelijking NLQF-niveaus 5 t/m 8 en. Tabel ter vergelijking NLQF niveaus 5 t/m 8 en Dublindescriptoren NLQF Niveau 5 Context Een onbekende, wisselende
Bijlage V Bij het advies van de Commissie NLQF EQF Tabel vergelijking NLQF-niveaus 5 t/m 8 en. Tabel ter vergelijking NLQF niveaus 5 t/m 8 en Dublindescriptoren NLQF Niveau 5 Context Een onbekende, wisselende
Toelichting bij de Voortgangsrapportage Maatschappelijke Zorg
 Naam: Klas: praktijkbegeleider: Werkplek: Toelichting bij de Voortgangsrapportage Maatschappelijke Zorg Het werken aan en en de relatie daarvan met de voortgangsrapportage Gedurende de verdiepingsfase
Naam: Klas: praktijkbegeleider: Werkplek: Toelichting bij de Voortgangsrapportage Maatschappelijke Zorg Het werken aan en en de relatie daarvan met de voortgangsrapportage Gedurende de verdiepingsfase
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek
 Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
Generieke systeemeisen
 Bijlage Generieke Systeem in kader van LAT-RB, versie 27 maart 2012 Generieke systeem NTA 8620 BRZO (VBS elementen) Arbowet Bevb / NTA 8000 OHSAS 18001 ISO 14001 Compliance competence checklist 1. Algemene
Bijlage Generieke Systeem in kader van LAT-RB, versie 27 maart 2012 Generieke systeem NTA 8620 BRZO (VBS elementen) Arbowet Bevb / NTA 8000 OHSAS 18001 ISO 14001 Compliance competence checklist 1. Algemene
Materiovigilantie tijdens inspecties van aangemelde instanties en fabrikanten van medische hulpmiddelen
 Materiovigilantie tijdens inspecties van aangemelde instanties en fabrikanten van medische hulpmiddelen 5de Vigilantiedag BRUSSEL Katrien MARTENS Inhoud Inleiding DG INSPECTIE Afdeling Industrie - Medische
Materiovigilantie tijdens inspecties van aangemelde instanties en fabrikanten van medische hulpmiddelen 5de Vigilantiedag BRUSSEL Katrien MARTENS Inhoud Inleiding DG INSPECTIE Afdeling Industrie - Medische
AMC Uitvoeringsrichtlijnen: Goedkeuring medisch-wetenschappelijk onderzoek door de Raad van Bestuur
 AMC Uitvoeringsrichtlijnen: Goedkeuring medisch-wetenschappelijk onderzoek door de Raad van Bestuur en Deelname van personeelsleden en studenten aan medisch-wetenschappelijk onderzoek Versie 1.1 Dit document
AMC Uitvoeringsrichtlijnen: Goedkeuring medisch-wetenschappelijk onderzoek door de Raad van Bestuur en Deelname van personeelsleden en studenten aan medisch-wetenschappelijk onderzoek Versie 1.1 Dit document
1. Algemene functie-informatie Resultaatgebieden
 Profielschets Coördinerend Voorzitter Regionale Toetsingscommissies Euthanasie, tevens (plaatsvervangend) Voorzitter van een van de vijf Regionale Toetsingscommissies Euthanasie 1. Algemene functie-informatie
Profielschets Coördinerend Voorzitter Regionale Toetsingscommissies Euthanasie, tevens (plaatsvervangend) Voorzitter van een van de vijf Regionale Toetsingscommissies Euthanasie 1. Algemene functie-informatie
President BeCRO organisatie van bedrijven die aktief zijn in het organiseren van klinische studies. Wat is? Medicament geneesmiddel device therapie?
 Melanoomstudiedag Els Vanpee President BeCRO organisatie van bedrijven die aktief zijn in het organiseren van klinische studies Hoofd klinische studies bij PAREXEL België Wat is? Medicament geneesmiddel
Melanoomstudiedag Els Vanpee President BeCRO organisatie van bedrijven die aktief zijn in het organiseren van klinische studies Hoofd klinische studies bij PAREXEL België Wat is? Medicament geneesmiddel
MDR (2017/745) en klinisch onderzoek - Implementatie in Nederland -
 MDR (2017/745) en klinisch onderzoek - Implementatie in Nederland - DCRF 26 september 2018 Monique Al Teamcoördinator Landelijk Bureau CCMO MDR: Drie hoofdcategoriën klinisch onderzoek I II III Klinisch
MDR (2017/745) en klinisch onderzoek - Implementatie in Nederland - DCRF 26 september 2018 Monique Al Teamcoördinator Landelijk Bureau CCMO MDR: Drie hoofdcategoriën klinisch onderzoek I II III Klinisch
Rol van European Organisa4on for Research and Treatment of Cancer (EORTC)
 Overzicht Verschillende partners Klinische studies binnen de farmaceu4sche industrie Protocol bij klinische studies Goedkeuring klinische studies Regels bij klinische studies Rol van European Medicines
Overzicht Verschillende partners Klinische studies binnen de farmaceu4sche industrie Protocol bij klinische studies Goedkeuring klinische studies Regels bij klinische studies Rol van European Medicines
Energie Management Programma. InTraffic
 Energie Management Programma InTraffic Wijzigingsblad Versie Datum Auteur Wijzigingen 0.1 17/2/2012 Marije de Vreeze Opzet structuur 0.2 13/3/2012 Marije de Vreeze Gegevens 0.3 5/4/2012 Dirk Bijkerk Input
Energie Management Programma InTraffic Wijzigingsblad Versie Datum Auteur Wijzigingen 0.1 17/2/2012 Marije de Vreeze Opzet structuur 0.2 13/3/2012 Marije de Vreeze Gegevens 0.3 5/4/2012 Dirk Bijkerk Input
DIFFERENT STEPS IN DRUG DEVELOPMENT: FROM THEORETICAL CONCEPT TO ACCESS FOR PATIENTS ROLE OF THE ETHICAL COMMITTEES
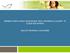 DIFFERENT STEPS IN DRUG DEVELOPMENT: FROM THEORETICAL CONCEPT TO ACCESS FOR PATIENTS ROLE OF THE ETHICAL COMMITTEES Klinische trials Verplicht vooraleer een geneesmiddel een marketing autorisatie kan krijgen
DIFFERENT STEPS IN DRUG DEVELOPMENT: FROM THEORETICAL CONCEPT TO ACCESS FOR PATIENTS ROLE OF THE ETHICAL COMMITTEES Klinische trials Verplicht vooraleer een geneesmiddel een marketing autorisatie kan krijgen
WORKSHOP: Competentiegericht opleiden
 Praktijkopleidersmiddag 15 november 2012 RINO Groep WORKSHOP: Competentiegericht opleiden Prof. dr. Theo K. Bouman & Drs. Valerie A. Hoogendoorn Hoofdopleider GZ & Praktijkcoördinator Opleidingsinstituut
Praktijkopleidersmiddag 15 november 2012 RINO Groep WORKSHOP: Competentiegericht opleiden Prof. dr. Theo K. Bouman & Drs. Valerie A. Hoogendoorn Hoofdopleider GZ & Praktijkcoördinator Opleidingsinstituut
De rol van de verpleegkundige binnen Medischwetenschappelijk
 De rol van de verpleegkundige binnen Medischwetenschappelijk onderzoek Moderator Mevr. R.C.A. Veldhoen-Tijben 1st author / speaker Miriam Gelderloos Co-author Erna Helmantel Belangenverklaring In overeenstemming
De rol van de verpleegkundige binnen Medischwetenschappelijk onderzoek Moderator Mevr. R.C.A. Veldhoen-Tijben 1st author / speaker Miriam Gelderloos Co-author Erna Helmantel Belangenverklaring In overeenstemming
4.2 Inzichten in de behoeften en verwachtingen van de belanghebbenden. 4.3 Het toepassingsgebied van het milieumanagementsystee m vaststellen
 4 Context van de organisatie 4 Milieumanagementsysteemeisen 4.1 Inzicht in de organisatie en haar context 4.2 Inzichten in de behoeften en verwachtingen van de belanghebbenden 4.3 Het toepassingsgebied
4 Context van de organisatie 4 Milieumanagementsysteemeisen 4.1 Inzicht in de organisatie en haar context 4.2 Inzichten in de behoeften en verwachtingen van de belanghebbenden 4.3 Het toepassingsgebied
Functieprofiel Functionaris Gegevensbescherming
 Functionaris Gegevensbescherming Inhoudsopgave 1. Doel van de functie 2. Plaats in de organisatie 3. Resultaatgebieden 4. Taken, verantwoordelijkheden & bevoegdheden 5. Contacten 6. Opleiding, kennis,
Functionaris Gegevensbescherming Inhoudsopgave 1. Doel van de functie 2. Plaats in de organisatie 3. Resultaatgebieden 4. Taken, verantwoordelijkheden & bevoegdheden 5. Contacten 6. Opleiding, kennis,
Uitbestedingsbeleid Stichting Pensioenfonds van de ABN AMRO Bank N.V.
 Uitbestedingsbeleid Stichting Pensioenfonds van de ABN AMRO Bank N.V. [geldend vanaf 1 juni 2015, PB15-220] Artikel 1 Definities De definities welke in dit uitbestedingsbeleid worden gebruikt zijn nader
Uitbestedingsbeleid Stichting Pensioenfonds van de ABN AMRO Bank N.V. [geldend vanaf 1 juni 2015, PB15-220] Artikel 1 Definities De definities welke in dit uitbestedingsbeleid worden gebruikt zijn nader
TOETSTERMEN INHAAL-/PE-EXAMEN. Volmacht Overig. Bijlage E10 ----------------------
 TOETSTERMEN INHAAL-/PE-EXAMEN Volmacht Overig Bijlage E10 ---------------------- College Deskundigheid Financiële Dienstverlening Juni 2013, Den Haag 1 ALGEMENE KENNIS EN VAARDIGHEDEN KENNIS Eindterm 1a
TOETSTERMEN INHAAL-/PE-EXAMEN Volmacht Overig Bijlage E10 ---------------------- College Deskundigheid Financiële Dienstverlening Juni 2013, Den Haag 1 ALGEMENE KENNIS EN VAARDIGHEDEN KENNIS Eindterm 1a
VMS veiligheidseisen voor het ZKN-Keurmerk Een vertaling van de NTA8009:2011 naar de situatie van de zelfstandige klinieken
 VMS veiligheidseisen voor het ZKN-Keurmerk Een vertaling van de NTA8009:2011 naar de situatie van de zelfstandige klinieken Leiderschap 1. De directie heeft vastgelegd en is eindverantwoordelijk voor het
VMS veiligheidseisen voor het ZKN-Keurmerk Een vertaling van de NTA8009:2011 naar de situatie van de zelfstandige klinieken Leiderschap 1. De directie heeft vastgelegd en is eindverantwoordelijk voor het
Samenwerking in academisch netwerkenrken
 Home no. 3 Juni 2015 Juridische aspecten Eerdere edities Verenso.nl Samenwerking in academisch netwerkenrken Goed gedrag in wetenschappelijk onderzoek Dr. Anke Persoon, coördinator UKON, afdeling ELG,
Home no. 3 Juni 2015 Juridische aspecten Eerdere edities Verenso.nl Samenwerking in academisch netwerkenrken Goed gedrag in wetenschappelijk onderzoek Dr. Anke Persoon, coördinator UKON, afdeling ELG,
Recente ontwikkelingen in de ethische normen voor medisch-wetenschappelijk onderzoek
 Recente ontwikkelingen in de ethische normen voor medisch-wetenschappelijk onderzoek Prof dr JJM van Delden Julius Centrum, UMC Utrecht j.j.m.vandelden@umcutrecht.nl Inleiding Medisch-wetenschappelijk
Recente ontwikkelingen in de ethische normen voor medisch-wetenschappelijk onderzoek Prof dr JJM van Delden Julius Centrum, UMC Utrecht j.j.m.vandelden@umcutrecht.nl Inleiding Medisch-wetenschappelijk
