JAARVERSLAG METC & BESTUUR van de STICHTING BEOORDELING ETHIEK BIOMEDISCH ONDERZOEK
|
|
|
- Robert Roeland Brouwer
- 4 jaren geleden
- Aantal bezoeken:
Transcriptie
1 JAARVERSLAG 2018 METC & BESTUUR van de STICHTING BEOORDELING ETHIEK BIOMEDISCH ONDERZOEK Telefoon: / info@stbebo.nl / Website: Jaarverslag 2018 Stichting Beoordeling Ethiek Biomedisch Onderzoek
2 INHOUDSOPGAVE pagina 2 SAMENSTELLING STICHTING BEBO - Bestuur van de Stichting, Medisch Ethische Toetsingscommissie en Ambtelijk Secretariaat pagina 3 BESTUUR STICHTING BEBO - Activiteiten pagina 5 - Verantwoording pagina 6 METC - Status pagina 7 - Vergadering en Activiteiten pagina 8 - Algemene vergadering & Bijscholing leden en contacten opdrachtgevers pagina 10 - Ambtelijk secretariaat pagina 11 PROEFPERSONEN - Voorlichting aan proefpersonen pagina 12 - Klachten proefpersonen pagina 12 ONDERZOEKSDOSSIERS - Aantallen en multicenteronderzoek pagina 13 - Beoordeling onderzoeksdossiers pagina 14 - Ernstige voorvallen/bijwerkingen (SUSAR s/sae s) pagina 14 - Interimrapportages pagina 14 - Slotwoord pagina 15 Jaarverslag 2018 Stichting Beoordeling Ethiek Biomedisch Onderzoek 2
3 SAMENSTELLING STICHTING BEBO Bestuur van de Stichting prof. dr. G.H. Koëter, voorzitter drs. J.N. Jedema, secretaris drs. G.J. Udding, penningmeester dr. J.T. Prins, lid Medisch Ethische Toetsingscommissie overzicht leden prof. dr. J.R.B.J. Brouwers, lid ziekenhuisapotheker en klinisch farmacoloog: algemeen voorzitter METC / tevens voorzitter kamer B prof. dr B. Wilffert, lid-klinisch farmacoloog en apotheker: 1 ste vicevoorzitter METC / tevens voorzitter kamer A dr. A. Wolthuis, lid (klinisch chemicus): 2 de vicevoorzitter METC / tevens voorzitter kamer C prof. dr. J.G. Aarnoudse, arts-lid (gynaecoloog) dr. G.L. Bartels (vicevoorzitter kamer B), arts-lid (cardioloog) dr. E.C. Boerma, arts-lid (internist-intensivist) (tot ) prof. dr. P.W. Boonstra, arts-lid (cardiothoracaal chirurg) mw. dr. A.A. Broekema, plv. lid (anesthesioloog n.p.) mr. W.B. Bruins, lid-jurist dr. S.M.J.G. Daenen, arts-lid (internist-hematoloog) dr. mr. J.P. van Dijk (secretaris), lid-jurist (arts n.p.) mw. mr. Y.E. van Dijk (secretaris), lid- jurist prof. dr. P.A. de Graeff, arts-lid-klinisch farmacoloog (internist) prof. dr. A.C. van Grootheest, plv.lid-arts (em.hoogleraar farmacovigilantie) prof. dr. E. Hak, lid-methodoloog prof. dr. H.J. Hoekstra, arts-lid (em.hoogleraar oncologisch chirurg) mw. A.C.M. ter Horst-Haitink, lid-proefpersonenvertegenwoordiger dr. F.G.A. Jansman, lid-ziekenhuisapotheker en klinisch farmacoloog dr. J.P. de Jong, lid-ethicus prof. dr. C.G.M. Kallenberg, lid (expert immunologie/reumatologie) dr. A.W.A. Kamps, lid-kinderarts mw. drs. M. Kesting-Koopmans, lid (research verpleegkundige) dr. A. S. Keverling Buisman, expert-lid (fysicus, stralingsdeskundige) dr. M.A. Kuiper, arts-lid (intensivist-neuroloog) prof. dr. L.F.M.H. de Leij, expert-lid (medische biologie, em.hoogleraar) mw. mr. Lijffijt, lid (in opleiding tot lid-jurist) E.A. Luijten, lid (verpleegkundig specialist) H. Lyklema, lid-proefpersonenvertegenwoordiger Jaarverslag 2018 Stichting Beoordeling Ethiek Biomedisch Onderzoek 3
4 Overzicht leden METC vervolg M. Mange, lid (verpleegkundig specialist) dr. J.G. Maring, lid-ziekenhuisapotheker en klinisch farmacoloog mw. drs. A.E. van Melle, plv. lid proefpersonenvertegenwoordiger (docent ethiek) mw. drs. Y.T. Nawijn, lid (revalidatie verpleegkundige) dr. P. Nieboer, lid (internist-oncoloog) mw. dr. A.N. Raat, lid-ethicus mw. dr. E. van t Riet, lid-methodoloog (vanaf ) dr. A.J. Risselada, plv. lid ziekenhuisapotheker en klinisch farmacoloog drs. J.M. van Rooijen, plv. lid (internist-oncoloog) prof. dr. E.N. van Roon, lid-ziekenhuisapotheker en klinisch farmacoloog drs. H. Sikkema, lid (deskundige steriele medische hulpmiddelen) prof. dr. D.R.A. Uges, lid-klinisch farmacoloog (ziekenhuisapotheker n.p. en klinisch toxicoloog) dr. N.J.G.M. Veeger, lid-methodoloog (tot ) dr. L.J.G. Veehof, lid (huisarts) Mw. C. Verlind, plv. lid proefpersonenvertegenwoordiger (fysiotherapeut n.p.) dr. R. de Vries, lid arts (internist) mw. dr. E.M. ten Vergert, lid-methodoloog mw. dr. J. van der Wal, arts-lid (patholoog-anatoom) dr. J.P. Yska, lid-ziekenhuisapotheker mw. H.J. Zand, lid-proefpersonenvertegenwoordiger Per 31 december 2018 telde de METC van de Stichting BEBO in totaal 48 leden. Ambtelijk Secretariaat mw. A. Boer, ambtelijk secretaris mw. M.L.G. Hiemink, ambtelijk secretaris (tot ) mw. M.E. de Jong-Vroom, ambtelijk secretaris mw. mr. C.M.C.J. Kortstee, ambtelijk secretaris de heer drs. A.V. van Schoonhoven, wetenschappelijk-ambtelijk secretaris (vanaf ) de heer drs. O. Doornbos, administratief medewerker (vanaf ) mw. V. Schuiling-Moes, administratief medewerker (vanaf ) mw. M.E. Zwart-Brockman, administratief medewerker Jaarverslag 2018 Stichting Beoordeling Ethiek Biomedisch Onderzoek 4
5 BESTUUR STICHTING BEBO Ieder lid van het bestuur vermijdt elke vorm en schijn van persoonlijke bevoordeling dan wel belangenverstrengeling tussen hem/haar en de Stichting. Activiteiten HET BESTUUR ONDERNAM IN 2018 DE VOLGENDE ACTIVITEITEN: - 6 maal vergaderde het Bestuur; - 3 maal werd met de voorzitter en/of vicevoorzitter (s)van de METC vergaderd; - enkele malen werd door een bestuurslid ten kantore met de ambtelijk secretarissen overlegd om lopende zaken af te handelen. Het Bestuur heeft de balans en de staat van baten en lasten 2018 laten controleren door UNP Accountants Adviseurs te Assen en vervolgens in haar vergadering d.d. 13 februari 2019 vastgesteld. Tijdens de bestuursvergaderingen en de vergaderingen met de voorzitters van de METC kwamen de volgende onderwerpen aan de orde: In het verslagjaar had de Stichting te kampen met een fors bezettingsprobleem op het ambtelijk secretariaat. Enerzijds door vertrek van één van de secretarissen, anderzijds door ziekte ontstonden acute capaciteitsproblemen. Door tijdelijk extra inzet vanuit het bestuur en de inzet van een voormalig secretaris kon aan de vraag van onze vaste opdrachtgevers worden voldaan. Indieningen van protocollen door andere opdrachtgevers konden helaas tijdelijk niet worden aangenomen. De bezetting van het secretariaat was aan het eind van 2018 weer op orde, mede door het uitbreiden van de bezetting. Tevens werd een wetenschappelijk-ambtelijk secretaris aangetrokken, waarmee wordt geanticipeerd op veranderingen in de werkwijze van de METC vanwege de aangekondigde invoering van de EU-verordening 536/2014 (zie voor nadere toelichting pag.7 bij Activiteiten METC). Naast bovengenoemde zaken kwamen tijdens de bestuursvergaderingen en de vergaderingen met de voorzitters van de METC de volgende onderwerpen aan de orde: - onderzoek nieuwe huisvesting / verhuizing - evaluatie werkwijze Kamers, samenstelling Kamers en uitbreiding leden METC; - faciliteren bijscholing METC-leden en vaststellen budget; - evaluatie werkzaamheden en werkwijze bestuur; - communicatie met opdrachtgevers en algemene zaken. In het verslagjaar verstreek voor enkele leden de eerste termijn van het lidmaatschap en de meesten zijn voor herbenoeming voorgedragen. Daarnaast zijn er 2 nieuwe leden voorgedragen en door de CCMO goedgekeurd. In december 2018 bedankte het Bestuur van de Stichting alle METC-leden voor hun inzet met een eindejaarsattentie. Jaarverslag 2018 Stichting Beoordeling Ethiek Biomedisch Onderzoek 5
6 Verantwoording De (voormalige) functies en nevenfuncties van de leden van het bestuur zijn als volgt: Prof. dr. G.H. Koeter: Medio november 2008-november 2014: voorzitter van de Centrale Commissie Mensgebonden Onderzoek (CCMO). Voormalig hoofdfunctie: Hoogleraar Longziekten bij de RUG. Drs. J.N. Jedema: Voormalige hoofdfunctie: Ziekenhuisapotheker Wilhelmina Ziekenhuis te Assen. Drs. G.J. Udding: Voormalige hoofdfunctie: voorzitter Directie ING-Bank, district Noord-Nederland. Huidige functie is zelfstandig bedrijfsadviseur. Huidige nevenfunctie: Bestuurslid Regionaal Ondernemers Instituut (ROI). Dr. J.T. Prins: Hoofdfunctie bij Medisch Centrum Leeuwarden: decaan MCL Academie/directielid MCL. Huidige nevenfuncties: - Bestuurslid Artsen Stichting Nederland. - Bestuurslid Profportaal Zorg. Jaarverslag 2018 Stichting Beoordeling Ethiek Biomedisch Onderzoek 6
7 METC Status De METC van de Stichting Beoordeling Ethiek Biomedisch Onderzoek is als toetsingscommissie erkend door de CCMO. Tevens is de METC geaccrediteerd door de NVMETC. Activiteiten DE METC KENDE IN 2018 DE VOLGENDE ACTIVITEITEN: Implementatie EU-verordening 536/2014 klinisch geneesmiddelenonderzoek Een belangrijk onderdeel van de METC werkzaamheden is het voorbereiden op de nieuwe wetgeving voor toetsing van klinisch geneesmiddelenonderzoek. Deze wetgeving is vastgelegd in een verordening met als doel het goedkeuringsproces voor geneesmiddelenonderzoek in de EU te harmoniseren en te versnellen, zodat nieuwe geneesmiddelen sneller op de markt kunnen komen waardoor patiënten er eerder van kunnen profiteren. Om dit te realiseren wordt de beoordeling van geneesmiddelenonderzoek een gezamenlijke verantwoordelijkheid van alle EU-lidstaten. Het Europees Geneesmiddelen Agentschap (EMA) heeft te maken met forse vertragingen als het gaat om de ontwikkeling van de software voor het nieuwe webportaal. De invoering van de nieuwe werkwijze is al een paar keer uitgesteld; de verwachting is nu dat in de loop van 2020 de invoering daadwerkelijk zal gaan plaatsvinden. Pilot voor EU-verordening - VHP Sinds januari 2017 doet onze METC, samen met 11 andere erkende METC s in Nederland mee in de Vrijwillige Harmonisatie Procedure (VHP). De VHP vertoont grote procedurele overeenkomsten met die van de verordening, maar de VHP heeft geen formele status. Door ervaring op te doen met de procedures van de VHP zijn wij straks voorbereid op het uitvoeren van de nieuwe regels onder de verordening geneesmiddelenonderzoek. De voorzitter van de METC heeft namens de Stichting zitting in de werkgroep van het Ministerie van VWS die samen met de CCMO het kader bespreekt waarbinnen samenwerking tussen de METC s en het landelijk bureau (van de CCMO) moet plaatsvinden in samenhang met de invoering van EU verordening 536/2014. Gevolgen AVG voor medisch-wetenschappelijk onderzoek Op 25 mei 2018 werd de Algemene Verordening Gegevensbescherming (AVG) van toepassing, waarmee in de hele Europese Unie de vereisten voor de verwerking van persoonsgegevens gelijk zijn getrokken. Dit had ook gevolgen voor het verzamelen en verwerken van persoonsgegevens in medisch-wetenschappelijk onderzoek en de manier waarop dit in o.a. de proefpersoneninformatie werd verwoord. Inmiddels heeft de CCMO hiervoor een tekstvoorstel geformuleerd dat voor onze METC als toetskader van toepassing is. Jaarverslag 2018 Stichting Beoordeling Ethiek Biomedisch Onderzoek 7
8 Vergaderingen Er vonden in dit verslagjaar 35 vergaderingen plaats, verdeeld over de kamers A, B en C. Er werden 2 extra vergaderingen gehouden. In de vergadering werd steeds geborgd dat alle door de wet- en overige relevante regelgeving vereiste disciplines aanwezig waren. In deze vergaderingen werden in totaal 143 onderzoeksdossiers beoordeeld. Tevens werden er bijna 400 (bijna 300 in 2017) amendementen op lopende studies beoordeeld. De beoordeling van onderzoeksdossiers werd uitgevoerd op verzoek van de vaste de opdrachtgevers PRA Health Sciences te Groningen, QPS Netherlands te Groningen, CHDR te Leiden, en IQVIA te Hoofddorp. Het merendeel van deze dossiers bestond uit fase I en II geneesmiddelenonderzoek. Naast de studies van de genoemde CRO s werden meerdere fase III onderzoeksdossiers aangeboden door o.a. Janssen, MSD en Roche. In totaal bediende de METC 20 verschillende opdrachtgevers. Het totaal aantal initiële beoordelingen is ten opzichte van 2017 gedaald (vanwege de eerder genoemde omstandigheden, zie pag.5 bij Activiteiten Bestuur). Gezien het forse aantal fase III studies dat in portefeuille is, is er wel weer een forse toename van het aantal substantiële amendementen geweest. Dat komt door het langlopende karakter van veelal multicenter onderzoeken waaraan meerdere sites in Nederland én in het buitenland deelnemen. Tevens heeft de invoering van de AVG (zie pag.9 bij Activiteiten METC) extra amendementen met zich meegebracht. In de vergaderingen vond nabespreking plaats van 80 eindverslagen van (geneesmiddelen)onderzoeken die initieel door de commissie werden beoordeeld, ter afsluiting van het studiedossier. Voor studies die langer dan een jaar lopen dient jaarlijks een voortgangsrapportage aangeleverd te worden. In het verslagjaar werd voor 91 langlopende studies een dergelijke rapportage besproken in de kamer. Tijdens de vergaderingen werd aandacht besteed aan het op peil houden van de specifieke kennis en beoordelingsvaardigheden van de commissieleden, onder meer door middel van bespreking van relevante publicaties op medisch-farmaceutisch en ethisch gebied (zie ook bijscholing, pag. 10). Activiteiten voorzitters en leden De voorzitter en vicevoorzitters van de METC vergaderden 3x keer met het Bestuur van de Stichting. De besproken punten staan vermeld onder de activiteiten van het Bestuur. De METC-voorzitter is door het bestuur met de uitvoerende werkzaamheden van het ambtelijk secretariaat belast. Ook werd hij tijdelijk belast met de planning van de studies (vanwege de eerder genoemde onderbezetting). Naast de frequente digitale en telefonische contacten vond er zevenmaal een werkoverleg plaats. Personele zaken werden ad interim vanuit het bestuur waargenomen. Vicevoorzitter Wilffert van de METC is bestuurslid van de NVMETC en hij woont in die hoedanigheid gedurende het jaar diverse besprekingen en vergaderingen bij. Jaarverslag 2018 Stichting Beoordeling Ethiek Biomedisch Onderzoek 8
9 In het verslagjaar woonden de voorzitter en/of de vicevoorzitter van de METC tweemaal het CCMOvoorzittersoverleg in Den Haag bij en waren zij bij de voorjaarsvergadering van de NVMETC te Utrecht. De voorzitter was tevens bij de najaarsvergadering van de NVMETC te Utrecht aanwezig. De METC voorzitter woonde in München het AGAH congres voor fase 1 studies bij. De METC voorzitter en de vicevoorzitter waren beide begin oktober aanwezig tijdens de Geneesmiddelendagen van de FIGON te Ede. In december woonde de vicevoorzitter de EUPATI conferentie te Brussel bij. Van al deze bijeenkomsten werd mondeling verslag gedaan in de kamers van de METC. Ook werden relevante presentaties gepubliceerd op het (interne) ledenportaal. Vier leden van de METC, uit verschillende disciplines, zijn momenteel actief voor het Intervisie Team van de NVMETC. Het team is in 2012 ingesteld om de kwaliteitsverbetering van METC s door middel van collegiale ondersteuning en advisering te bevorderen. Overige activiteiten In het verslagjaar werd geen gebruik gemaakt van de METC-klachtencommissie. De METC is al enige jaren betrokken bij het opleiden van klinisch farmacologen en ook in 2018 werd op verzoek hier medewerking aan verleend. Voor de beoordeling van ingrijpende wijzigingen en substantiële amendementen, die door de voorzitter van een kamer en preadviseur(s) en/of andere leden van de METC worden beoordeeld, wordt een termijn van vier werkdagen aangehouden. De afspraken omtrent de METC-termijnen voor tussentijdse beoordelingen zijn in het verslagjaar kenbaar gemaakt aan nieuwe opdrachtgevers. Indien amendementen door de gehele kamer beoordeeld moeten worden dient er door de opdrachtgever gewacht te worden totdat er door de desbetreffende kamer vergaderd wordt. De informatie is ook te vinden op de website van de METC. De METC heeft er in het verslagjaar steeds op toegezien dat in onderzoeksdossiers geen voorwaarden gesteld worden die publicatie van de onderzoeksresultaten in de weg staan en onterechte voortijdige beëindiging van een studie mogelijk maken. Vaste opdrachtgevers geven zich goed rekenschap van de Nederlandse regelgeving. Jaarverslag 2018 Stichting Beoordeling Ethiek Biomedisch Onderzoek 9
10 Algemene Vergadering & Bijscholing METC-leden Dit jaar kon er helaas, vanwege de capaciteitsproblemen, geen Algemene Vergadering worden georganiseerd. In het kader van de bijscholing werden de leden gedurende het gehele verslagjaar gestimuleerd om deel te nemen aan relevante symposia, congressen en themabijeenkomsten. Het Bestuur heeft hiervoor net zoals in voorgaande jaren een bijscholingsbudget beschikbaar gesteld. Hiermee wordt de professionaliteit en kwaliteit van de METC op peil gehouden. De leden kunnen studiepunten behalen door het bijwonen van geselecteerde bijeenkomsten. Leden van de METC namen in 2018 deel aan de verschillende bijeenkomsten, waaronder de NVMETC bijscholingsbijeenkomsten. Contacten met opdrachtgevers In het verslagjaar werden geen site-visits uitgevoerd. Wel werd éénmaal een afstemmingsoverleg met PRA en CHDR (afzonderlijk van elkaar) gevoerd. Voorts werd door de voorzitter van de METC en de voorzitter van het bestuur de opening van de nieuwe PRA-kliniek in Groningen bijgewoond. Jaarverslag 2018 Stichting Beoordeling Ethiek Biomedisch Onderzoek 10
11 Ambtelijk secretariaat Het secretariaat ondersteunt en faciliteert de werkzaamheden van het Bestuur, de METC (vice)voorzitters en de METC-leden. Het kantoor is het gehele jaar op werkdagen geopend en bereikbaar. De ambtelijk secretarissen, of een afvaardiging, bezochten de volgende bijeenkomsten: - NVMETC Scholingsdagen; - de secretarissenwerkgroep van erkende METC s; - andere relevante bijeenkomsten, o.a. in verband met de VHP. Het ambtelijk secretariaat heeft 33 reguliere vergaderingen georganiseerd. Er waren 2 extra vergaderingen nodig. Naast het inplannen en begeleiden van het proces van de 143 aangeboden studies heeft het secretariaat zich bezig gehouden met allerlei vragen en amendementen die lopende studies met zich meebrengen. Aan het einde van het kalenderjaar waren er 250 studies nog actief in portefeuille. Daarnaast is er aan 4 VHP beoordelingen meegedaan. De vele vragen en amendementen in verband met de AVG (privacywetgeving) werden behandeld. In december werd het nieuwe pand aan de Nassaulaan 10 te Assen betrokken. De werknemers hebben veel werk verricht om deze verhuizing goed te laten verlopen. De heren drs. O. Doornbos en mw. V. Schuiling-Moes werden als administratief medewerkers aangesteld. De heer drs. A.V. van Schoonhoven trad als wetenschappelijk-ambtelijk secretaris in dienst. Zij werden door het zittende personeel ingewerkt. Jaarverslag 2018 Stichting Beoordeling Ethiek Biomedisch Onderzoek 11
12 PROEFPERSONEN Voorlichting aan proefpersonen De werving van proefpersonen voor deelname aan de diverse onderzoeken vindt plaats door de opdrachtgever via diverse media en wervingsacties. In de praktijk worden gezonde proefpersonen steeds vaker via de websites van de opdrachtgevers en de sociale media geworven, en via advertenties in regionale- en landelijke bladen. De teksten voor de werving behoeven voor gebruik een goedkeuring van de METC. Het Informed Consent Form (ICF) of patiënteninformatiebrief en andere daarbij behorende documenten bevatten volledige en heldere geschreven informatie voor de proefpersoon. Dit formulier wordt door de onderzoeker per pagina doorgenomen met de proefpersoon; waar nodig wordt nadere toelichting gegeven. Deze informatie is dan al door de METC goedgekeurd. De METC benadrukt steeds de noodzaak van duidelijke en voor de leek begrijpelijke teksten en dringt regelmatig aan bij opdrachtgevers om teksten bondiger te formuleren. De belasting van gezonde deelnemers, of extra belasting voor patiënten, is een vast onderdeel van de beraadslagingen en was regelmatig onderwerp van discussie tijdens de METC-vergaderingen. Het maximale aantal deelnames aan onderzoeken is voor zowel mannen als vrouwen vier per jaar. In principe is de minimale exclusieperiode tussen opeenvolgende klinische onderzoeken 30 dagen. Controle vindt plaats via het zogenaamde Verified Clinical Trials (VCT) systeem. Dit systeem heeft in 2018 het VIP-checksysteem vervangen. De vaste opdrachtgevers PRA, QPS en CHDR hebben allen voor dit Amerikaanse systeem gekozen, dat veilig is en zich houdt aan de Europese (privacy) wetgeving. Klachten proefpersonen In het verslagjaar deden zich geen voorvallen voor die tot een interventie door de METC hebben geleid. Wel is een klacht ontvangen van een deelnemer van fase 1 onderzoek die vond dat hij een te lage vergoeding had ontvangen. Jaarverslag 2018 Stichting Beoordeling Ethiek Biomedisch Onderzoek 12
13 ONDERZOEKSDOSSIERS Aantallen In het verslagjaar werden 143 onderzoeksdossiers beoordeeld (in 2017:165). Bij het merendeel van de protocollen ging het om onderzoek met potentiële geneesmiddelen of nieuwe toedieningsvormen. De METC constateert dat Fase I onderzoek met biologicals/biosimilars complex is en blijft; hiervoor wordt dan ook altijd een extra beoordelaar (expert) ingezet. In Nederland bedraagt het marktaandeel van de BEBO bij Fase 1 onderzoek ca. 70% en op het totaal geneesmiddelenonderzoek ca. 25% van alle aangeboden onderzoek. Onderverdeling per fase: Fase I Fase II Fase III Overig beoordeelde onderzoeksdossiers Multicenter-onderzoek De METC heeft in het verslagjaar voor ongeveer 30 multicenter protocollen als oordelende commissie opgetreden. In een aantal gevallen betrof het Fase II of III onderzoeken die in meerdere Europese landen van start zouden gaan, met slechts één deelnemend centrum in Nederland. Jaarverslag 2018 Stichting Beoordeling Ethiek Biomedisch Onderzoek 13
14 Beoordeling onderzoeksdossiers De METC kan alleen een positief dan wel een negatief oordeel geven, of een onderzoeksdossier aanhouden, ter verkrijging van meer of aangepaste informatie. Het merendeel van de aangeboden studies werd, na gewenste aanpassing van het dossier, goedgekeurd. Eenmaal heeft de METC een onderzoeksdossier van een negatief oordeel voorzien. Er werd een beroepsprocedure door de opdrachtgever gestart en deze werd door de CCMO gegrond verklaard. Het onderzoek is inmiddels gestart. Tevens werd een groot amendement afgewezen. Er werd door de opdrachtgever een beroepsprocedure bij de CCMO gestart. Bij nadere bestudering werd het amendement alsnog door de METC goedgekeurd. De beroepsprocedure kon daarmee vervallen. In het verslagjaar werd meerdere malen een onderzoek door de opdrachtgever teruggetrokken. Tevens werden 5 studies voortijdig beëindigd, bijvoorbeeld vanwege onverwachte/ongewenste preklinische data of een negatief benefit-risk ratio. De termijn van 60 dagen, waarbinnen een initiële indiening door de METC beoordeeld moet worden, is in alle gevallen gehaald. Naast de non-substantiële wijzigingen die ter notificatie werden aangeboden, zijn er gedurende 2018 bijna 400 substantiële amendementen door de METC beoordeeld. Ernstige voorvallen / bijwerkingen (SUSAR s/sae s) De meldingen bij Fase I studies worden te allen tijde direct aan de voorzitters ter beoordeling voorgelegd. Alle meldingen voor alle lopende studies worden volgens regelgeving aan de METC gemeld en vervolgens door ons gearchiveerd. Dat geldt ook voor de Line Listings en DSUR s (verzameloverzichten per halfjaar en per jaar). Interimrapportages Bij alle First in Human studies met opklimmende doseringen zal de METC, vanwege het hogere risico, de onderzoeker vragen via Interim Rapporten te rapporteren aan de METC en zal daarmee toestemming voor de volgende dosering worden gevraagd. De voorzitter heeft hiervoor mandaat van de vergadering en mag hierover in principe alleen beslissen. Waar nodig en gewenst zal hij andere leden bij de besluitvorming betrekken. Voor andere onderzoeken wordt de tussentijdse rapportage ter informatie aangeleverd. Door de opdrachtgever wordt soms een Safety Evaluating Committee (SEC) ingesteld om advies uit te brengen over deze dosisverhogingen. De METC kan het onderzoek op basis van de interim-resultaten laten stoppen. Jaarverslag 2018 Stichting Beoordeling Ethiek Biomedisch Onderzoek 14
15 Slotwoord De Stichting heeft zich ingespannen om met de uitbreiding van de capaciteit op het ambtelijk secretariaat de kwaliteit en snelheid van de beoordelingen op het gebruikelijke niveau te brengen en ook voor de toekomst te waarborgen. Door actieve deelname aan de VHP kan beter ingespeeld worden op de veranderingen die na de inwerkingtreding van de EU verordening 536/2014 worden verwacht. De METC van de Stichting BEBO wil graag een substantiële bijdrage blijven leveren aan de beoordeling van geneesmiddelenonderzoek in Nederland. Assen, december 2018 Jaarverslag 2018 Stichting Beoordeling Ethiek Biomedisch Onderzoek 15
JAARVERSLAG 2017 METC & BESTUUR. van de STICHTING BEOORDELING ETHIEK BIOMEDISCH ONDERZOEK. te ASSEN. Postbus 1004, 9400 BA Assen
 JAARVERSLAG 2017 METC & BESTUUR van de STICHTING BEOORDELING ETHIEK BIOMEDISCH ONDERZOEK te ASSEN Postbus 1004, 9400 BA Assen Telefoon: 0592-405871 / E-mail: info@stbebo.nl / Website: www.stbebo.nl Jaarverslag
JAARVERSLAG 2017 METC & BESTUUR van de STICHTING BEOORDELING ETHIEK BIOMEDISCH ONDERZOEK te ASSEN Postbus 1004, 9400 BA Assen Telefoon: 0592-405871 / E-mail: info@stbebo.nl / Website: www.stbebo.nl Jaarverslag
KLINISCH GENEESMIDDELEN- ONDERZOEK
 KLINISCH GENEESMIDDELEN- ONDERZOEK HET PROCES VAN HET OPSTARTEN VAN KLINISCH ONDERZOEK MET GENEESMIDDELEN GAAT VERANDEREN De ECTR verandert het klinisch onderzoek met geneesmiddelen in Europa. Dit heeft
KLINISCH GENEESMIDDELEN- ONDERZOEK HET PROCES VAN HET OPSTARTEN VAN KLINISCH ONDERZOEK MET GENEESMIDDELEN GAAT VERANDEREN De ECTR verandert het klinisch onderzoek met geneesmiddelen in Europa. Dit heeft
Formulier Voortgangsrapportage
 Formulier Voortgangsrapportage De METC azm/um wil van al het door haar beoordeelde WMO-onderzoek jaarlijks een voortgangsrapportage zien. Zij heeft deze eis daartoe opgenomen in de tekst van haar eigen
Formulier Voortgangsrapportage De METC azm/um wil van al het door haar beoordeelde WMO-onderzoek jaarlijks een voortgangsrapportage zien. Zij heeft deze eis daartoe opgenomen in de tekst van haar eigen
Bijgaand ontvangt u het primaire besluit van de commissie over het hierna vermelde onderzoek.
 Medisch :' i < r. c Toetsingscommissie Noord-Holland t AMC Orthopedie A.J. Kievit Staalmeesterslaan 271 1057 NZ Amsterdam datum kenmerk METC- registratie CCMO-registratie EudraCTnummer 30 oktober 2012
Medisch :' i < r. c Toetsingscommissie Noord-Holland t AMC Orthopedie A.J. Kievit Staalmeesterslaan 271 1057 NZ Amsterdam datum kenmerk METC- registratie CCMO-registratie EudraCTnummer 30 oktober 2012
website www.nvmetc.nl
 Verslag NVMETC secretarissenoverleg 19 juni 2014 1. Opening en vaststelling agenda Dhr. Davids geeft aan, dat een belangrijke reden van dit secretarissenoverleg is, dat we van elkaar horen wat er speelt
Verslag NVMETC secretarissenoverleg 19 juni 2014 1. Opening en vaststelling agenda Dhr. Davids geeft aan, dat een belangrijke reden van dit secretarissenoverleg is, dat we van elkaar horen wat er speelt
Jaarverslag 2014. METC Máxima Medisch Centrum
 Jaarverslag 2014 METC Máxima Medisch Centrum Inhoud Voorwoord p. 3 Inleiding p. 3 Bevoegd gezag METC p. 4 Samenstelling commissie p. 4 Samenstelling secretariaat p. 4 Werkwijze commissie p. 5 Samenvatting
Jaarverslag 2014 METC Máxima Medisch Centrum Inhoud Voorwoord p. 3 Inleiding p. 3 Bevoegd gezag METC p. 4 Samenstelling commissie p. 4 Samenstelling secretariaat p. 4 Werkwijze commissie p. 5 Samenvatting
Actuele ontwikkelingen ten aanzien van toetsen van medisch-wetenschappelijk onderzoek met mensen
 Actuele ontwikkelingen ten aanzien van toetsen van medisch-wetenschappelijk onderzoek met mensen NVMETC scholingsdagen 2017 Monique Al Sr wetenschappelijk stafmedewerker CCMO Ontwikkelingen wetgeving 1.
Actuele ontwikkelingen ten aanzien van toetsen van medisch-wetenschappelijk onderzoek met mensen NVMETC scholingsdagen 2017 Monique Al Sr wetenschappelijk stafmedewerker CCMO Ontwikkelingen wetgeving 1.
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek
 Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
adresgegevens postadres CMO Regio Arnhem-Nijmegen P/a UMC St Radboud Huispostnummer 578 Postbus HB Nijmegen
 Commissie Mensgebonden Onderzoek jaarverslag 2013 adresgegevens postadres CMO Regio Arnhem-Nijmegen P/a UMC St Radboud Huispostnummer 578 Postbus 9101 6500 HB Nijmegen bezoekadres CMO Regio Arnhem-Nijmegen
Commissie Mensgebonden Onderzoek jaarverslag 2013 adresgegevens postadres CMO Regio Arnhem-Nijmegen P/a UMC St Radboud Huispostnummer 578 Postbus 9101 6500 HB Nijmegen bezoekadres CMO Regio Arnhem-Nijmegen
AMC Uitvoeringsrichtlijnen: Goedkeuring medisch-wetenschappelijk onderzoek door de Raad van Bestuur
 AMC Uitvoeringsrichtlijnen: Goedkeuring medisch-wetenschappelijk onderzoek door de Raad van Bestuur en Deelname van personeelsleden en studenten aan medisch-wetenschappelijk onderzoek Versie 1.1 Dit document
AMC Uitvoeringsrichtlijnen: Goedkeuring medisch-wetenschappelijk onderzoek door de Raad van Bestuur en Deelname van personeelsleden en studenten aan medisch-wetenschappelijk onderzoek Versie 1.1 Dit document
JAARVERSLAG MEDISCH ETHISCHE TOETSINGSCOMMISSIE
 JAARVERSLAG 2015 MEDISCH ETHISCHE TOETSINGSCOMMISSIE Inhoudsopgave Pag. Voorwoord 2 1. Positionering 3 1.1 Plaats in de organisatie 1.2 Regionale samenwerking 3 3 2. Samenstelling van de Commissie 4 3.
JAARVERSLAG 2015 MEDISCH ETHISCHE TOETSINGSCOMMISSIE Inhoudsopgave Pag. Voorwoord 2 1. Positionering 3 1.1 Plaats in de organisatie 1.2 Regionale samenwerking 3 3 2. Samenstelling van de Commissie 4 3.
INHOUDSOPGAVE. Vooruitblik 2016 p. 11. Bijlagen: 1. Gebruikte afkortingen p Colofon p. 13. Jaarverslag 2015 METC MMC
 INHOUDSOPGAVE Voorwoord p. 3 Inleiding p. 3 Onderwerpen 2015 p. 4 Bevoegd gezag METC p. 4 Samenstelling commissie p. 5 Mutaties 2015 p. 5 Samenstelling en wijziging secretariaat p. 6 Werkwijze METC p.
INHOUDSOPGAVE Voorwoord p. 3 Inleiding p. 3 Onderwerpen 2015 p. 4 Bevoegd gezag METC p. 4 Samenstelling commissie p. 5 Mutaties 2015 p. 5 Samenstelling en wijziging secretariaat p. 6 Werkwijze METC p.
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik
 EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
Algemeen Plaats in de organisatie Regionale samenwerking Samenstelling van de Commissie Werkwijze 6
 Inhoudsopgave Algemeen 2 Pag. 1. Positionering 1.1 Plaats in de organisatie 3 1.2 Regionale samenwerking 3 2. Samenstelling van de Commissie 4 3. Werkwijze 6 4. Beoordeling medisch wetenschappelijk onderzoek
Inhoudsopgave Algemeen 2 Pag. 1. Positionering 1.1 Plaats in de organisatie 3 1.2 Regionale samenwerking 3 2. Samenstelling van de Commissie 4 3. Werkwijze 6 4. Beoordeling medisch wetenschappelijk onderzoek
IRB Nijmegen. I R B N ij m egen. Independent Review Board Nijmegen JAARVERSLAG Independent Review Board Nijmegen
 Independent Review Board Nijmegen JAARVERSLAG 6 IRB Nijmegen Independent Review Board Nijmegen Medisch-Ethische ToetsingsCommissie voor Medisch Wetenschappelijk Onderzoek Mei 7 Jaarverslag metc IRB Nijmegen
Independent Review Board Nijmegen JAARVERSLAG 6 IRB Nijmegen Independent Review Board Nijmegen Medisch-Ethische ToetsingsCommissie voor Medisch Wetenschappelijk Onderzoek Mei 7 Jaarverslag metc IRB Nijmegen
Europese verordening klinische proeven. Harrie Storms (VWS)
 Europese verordening klinische proeven Harrie Storms (VWS) 1 Veranderingen EU verordening Indiening via EU-portal (nationale studies en multinationale studies) Centrale beoordeling van multinationaal onderzoek
Europese verordening klinische proeven Harrie Storms (VWS) 1 Veranderingen EU verordening Indiening via EU-portal (nationale studies en multinationale studies) Centrale beoordeling van multinationaal onderzoek
Op naar het snel opstarten van klinisch onderzoek in Nederland!
 Op naar het snel opstarten van klinisch onderzoek in Nederland! Marika Trieling Voorzitter DCRF werkgroep Lokale uitvoerbaarheid 12 februari 2019 Wat is er in Nederland nodig? Verkorten tijdslijnen van
Op naar het snel opstarten van klinisch onderzoek in Nederland! Marika Trieling Voorzitter DCRF werkgroep Lokale uitvoerbaarheid 12 februari 2019 Wat is er in Nederland nodig? Verkorten tijdslijnen van
METC MMC Jaarverslag 2018
 METC MMC Jaarverslag 2018 Inhoudsopgave Voorwoord p. 3 Inleiding p. 3 Onderwerpen 2018 p. 3 Activiteiten 2018 p. 3 Bevoegd gezag METC p. 4 Samenstelling commissie p. 4 Mutaties 2018 p. 4 Samenstelling
METC MMC Jaarverslag 2018 Inhoudsopgave Voorwoord p. 3 Inleiding p. 3 Onderwerpen 2018 p. 3 Activiteiten 2018 p. 3 Bevoegd gezag METC p. 4 Samenstelling commissie p. 4 Mutaties 2018 p. 4 Samenstelling
Nieuwsbrief MasterPlan professionalisering voorbereiding mensgebonden genees- en hulpmiddelen onderzoek]
![Nieuwsbrief MasterPlan professionalisering voorbereiding mensgebonden genees- en hulpmiddelen onderzoek] Nieuwsbrief MasterPlan professionalisering voorbereiding mensgebonden genees- en hulpmiddelen onderzoek]](/thumbs/68/59829458.jpg) In deze eerste nieuwsbrief: - MasterPlan gelanceerd - Stuurgroep en werkgroepen aan de slag - Opbrengst startbijeenkomsten - Organogram en bezetting werkgroepen Het startpunt van samenwerken is: Het eens
In deze eerste nieuwsbrief: - MasterPlan gelanceerd - Stuurgroep en werkgroepen aan de slag - Opbrengst startbijeenkomsten - Organogram en bezetting werkgroepen Het startpunt van samenwerken is: Het eens
De ECTR: een kans voor Nederland! Annelies van Woudenberg, DCRF congres, 5 oktober 2016
 De ECTR: een kans voor Nederland! Annelies van Woudenberg, DCRF congres, 5 oktober 2016 European Clinical Trial Regulation 536/ 2014 European Clinical Trial Regulation (ECTR): EU Verordening betreffende
De ECTR: een kans voor Nederland! Annelies van Woudenberg, DCRF congres, 5 oktober 2016 European Clinical Trial Regulation 536/ 2014 European Clinical Trial Regulation (ECTR): EU Verordening betreffende
Inhoud onderzoeksdossier
 Inhoud onderzoeksdossier (documenten in de witte box zijn nodig voor de primaire beoordeling) A. Brieven B. Formulieren C. Onderzoeksprotocol en protocolamendementen D. Productinformatie E. Informatie
Inhoud onderzoeksdossier (documenten in de witte box zijn nodig voor de primaire beoordeling) A. Brieven B. Formulieren C. Onderzoeksprotocol en protocolamendementen D. Productinformatie E. Informatie
REGLEMENT. van de TE ASSEN
 9 Stichting Beoordeling Fthiek Bionwdisch Onderzoek REGLEMENT van de MEDISCH ETHISCHE TOETSINGSCOMMISSIE TE ASSEN van de Postbus 1004 9400 BA ASSEN opgericht 1984 Pagina 1 van 17 Stichting Beoordeling
9 Stichting Beoordeling Fthiek Bionwdisch Onderzoek REGLEMENT van de MEDISCH ETHISCHE TOETSINGSCOMMISSIE TE ASSEN van de Postbus 1004 9400 BA ASSEN opgericht 1984 Pagina 1 van 17 Stichting Beoordeling
JAARVERSLAG MEDISCH ETHISCHE TOETSINGSCOMMISSIE
 JAARVERSLAG 2016 MEDISCH ETHISCHE TOETSINGSCOMMISSIE Inhoudsopgave Pag. Voorwoord 2 1. Positionering 3 1.1 Plaats in de organisatie 1.2 Regionale samenwerking 3 3 2. Samenstelling van de Commissie 4 3.
JAARVERSLAG 2016 MEDISCH ETHISCHE TOETSINGSCOMMISSIE Inhoudsopgave Pag. Voorwoord 2 1. Positionering 3 1.1 Plaats in de organisatie 1.2 Regionale samenwerking 3 3 2. Samenstelling van de Commissie 4 3.
nwmo toetsingskader Eveline Loriaux projectleider 4 oktober 2017 Jaarcongres DCRF
 nwmo toetsingskader Eveline Loriaux projectleider 4 oktober 2017 Jaarcongres DCRF Zien we door de bomen nog het bos? nwmo Toetsingskader Overzicht Start: juli 2015 In 2017 zijn 39 aanvragen ingediend
nwmo toetsingskader Eveline Loriaux projectleider 4 oktober 2017 Jaarcongres DCRF Zien we door de bomen nog het bos? nwmo Toetsingskader Overzicht Start: juli 2015 In 2017 zijn 39 aanvragen ingediend
CCMO op 22 oktober 2015;
 Versie 7, goedgekeurd door METC AVL op 25 november CCMO op 22 oktober 2015; door RvB op 15 maart 2016 en door REGLEMENT VAN DE MEDISCHE-ETHISCHE TOETSINGSCOMMISSIE (METC) VAN STICHTING NEDERLANDS KANKERINSTITUUT
Versie 7, goedgekeurd door METC AVL op 25 november CCMO op 22 oktober 2015; door RvB op 15 maart 2016 en door REGLEMENT VAN DE MEDISCHE-ETHISCHE TOETSINGSCOMMISSIE (METC) VAN STICHTING NEDERLANDS KANKERINSTITUUT
Bijlage 2 bij het Convenant PSI Samenstelling en werkwijze toetsingscommissie
 Bijlage 2 bij het Convenant PSI Samenstelling en werkwijze toetsingscommissie 1. Samenstelling toetsingscommissie De kerncommissie betstaat uit leden met ten minste de volgende specialismes 1 : Arts of
Bijlage 2 bij het Convenant PSI Samenstelling en werkwijze toetsingscommissie 1. Samenstelling toetsingscommissie De kerncommissie betstaat uit leden met ten minste de volgende specialismes 1 : Arts of
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL5 Protocolamendement (lokaal) Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: VL5 Protocolamendement (lokaal) Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
MDR (2017/745) en klinisch onderzoek - Implementatie in Nederland -
 MDR (2017/745) en klinisch onderzoek - Implementatie in Nederland - DCRF 26 september 2018 Monique Al Teamcoördinator Landelijk Bureau CCMO MDR: Drie hoofdcategoriën klinisch onderzoek I II III Klinisch
MDR (2017/745) en klinisch onderzoek - Implementatie in Nederland - DCRF 26 september 2018 Monique Al Teamcoördinator Landelijk Bureau CCMO MDR: Drie hoofdcategoriën klinisch onderzoek I II III Klinisch
Impact van de ECTR en hoe zorgen we dat NL als beste uit de bus komt. Annelies van Woudenberg, ACRON Najaarsvergadering, 2 november 2016
 Impact van de ECTR en hoe zorgen we dat NL als beste uit de bus komt Annelies van Woudenberg, ACRON Najaarsvergadering, 2 november 2016 2 Dutch Clinical Research Foundation (DCRF) European Clinical Trial
Impact van de ECTR en hoe zorgen we dat NL als beste uit de bus komt Annelies van Woudenberg, ACRON Najaarsvergadering, 2 november 2016 2 Dutch Clinical Research Foundation (DCRF) European Clinical Trial
Onderzoek naar de gebruiksvriendelijkheid van de OLVG PIJN app
 Onderzoek naar de gebruiksvriendelijkheid van de OLVG PIJN app Engels: Proof of concept OLVG PAIN app. Betreft: Patiënten informatiebrief, onderzoek naar de gebruiksvriendelijkheid van de OLVG PIJN app
Onderzoek naar de gebruiksvriendelijkheid van de OLVG PIJN app Engels: Proof of concept OLVG PAIN app. Betreft: Patiënten informatiebrief, onderzoek naar de gebruiksvriendelijkheid van de OLVG PIJN app
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VC9 Proefpersonen- en aansprakelijkheidsverzekering (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure STZ SOP: VC9 Proefpersonen- en aansprakelijkheidsverzekering (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Henk Jan Out, Paul van Meurs en Rudolf van Olden. Van eerste humane toediening tot algemeen gebruik
 VII 1 Introductie tot de farmaceutische geneeskunde................................ 1 Henk Jan Out, Paul van Meurs en Rudolf van Olden I Van eerste humane toediening tot algemeen gebruik 2 Exploratory
VII 1 Introductie tot de farmaceutische geneeskunde................................ 1 Henk Jan Out, Paul van Meurs en Rudolf van Olden I Van eerste humane toediening tot algemeen gebruik 2 Exploratory
JAARVERSLAG 2016 METC
 JAARVERSLAG 2016 METC INHOUDSOPGAVE Voorwoord p. 3 Inleiding p. 3 Toetsing van geneesmiddelenonderzoek p. 3 Onderwerpen 2016 p. 3 Bevoegd gezag METC p. 4 Samenstelling commissie p. 4 Mutaties 2016 p. 4
JAARVERSLAG 2016 METC INHOUDSOPGAVE Voorwoord p. 3 Inleiding p. 3 Toetsing van geneesmiddelenonderzoek p. 3 Onderwerpen 2016 p. 3 Bevoegd gezag METC p. 4 Samenstelling commissie p. 4 Mutaties 2016 p. 4
 ------------------------------------------------------------------------------------------------------------------------------------------- Concept Procedure Lokale Haalbaarheid klinisch geneesmiddelenonderzoek
------------------------------------------------------------------------------------------------------------------------------------------- Concept Procedure Lokale Haalbaarheid klinisch geneesmiddelenonderzoek
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VC8 Beoordeling amendement toetsende commissie (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure STZ SOP: VC8 Beoordeling amendement toetsende commissie (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Bijgaand ontvangt u het primair besluit van de commissie over het hierna vermelde onderzoek.
 Medisch To e ts ingsco mmiss ie Noord-Holland Noordwest Ziekenhuisgroep Dhr. F. Hagemans Afdeling Orthopedie Wilhelminalaan 12 1815 JD Alkmaar datum 7 juni 2016 kenmerk NH017.140 METC- registratie M016-030
Medisch To e ts ingsco mmiss ie Noord-Holland Noordwest Ziekenhuisgroep Dhr. F. Hagemans Afdeling Orthopedie Wilhelminalaan 12 1815 JD Alkmaar datum 7 juni 2016 kenmerk NH017.140 METC- registratie M016-030
Toetsingskader nwmo. Peggy Manders 4 november 2016 Symposium V&VN Research Professionals
 Toetsingskader nwmo Peggy Manders 4 november 2016 Symposium V&VN Research Professionals Biobank: definitie en rationale Wat is een biobank? + + Waarom een biobank starten? Verbeteren gezondheidszorg voor
Toetsingskader nwmo Peggy Manders 4 november 2016 Symposium V&VN Research Professionals Biobank: definitie en rationale Wat is een biobank? + + Waarom een biobank starten? Verbeteren gezondheidszorg voor
Modelreglement METC s
 Modelreglement METC s CONSIDERANS De medisch-ethische toetsingscommissie als bedoeld in artikel 16, eerste lid, van de Wet medischwetenschappelijk onderzoek met mensen van 26 februari 1998, Stb 1998 161,
Modelreglement METC s CONSIDERANS De medisch-ethische toetsingscommissie als bedoeld in artikel 16, eerste lid, van de Wet medischwetenschappelijk onderzoek met mensen van 26 februari 1998, Stb 1998 161,
drs. J.N. Jedema, voorzitter METC Stichting BEBO Ontstaan en ontwikkeling van de Stichting
 drs. J.N. Jedema, voorzitter METC Stichting BEBO Ontstaan en ontwikkeling van de Stichting 25 jaar Stichting Beoordeling Ethiek Biomedisch Onderzoek De Medisch Ethische Commissie van de Stichting BEBO
drs. J.N. Jedema, voorzitter METC Stichting BEBO Ontstaan en ontwikkeling van de Stichting 25 jaar Stichting Beoordeling Ethiek Biomedisch Onderzoek De Medisch Ethische Commissie van de Stichting BEBO
Officiële uitgave van het Koninkrijk der Nederlanden sinds Organisatie en Werkwijze Medisch Ethische Toetsingscommissies
 STAATSCOURANT Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814. Nr. 3243 7 februari 2014 Organisatie en Werkwijze Medisch Ethische Toetsingscommissies Richtlijn van de Centrale Commissie
STAATSCOURANT Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814. Nr. 3243 7 februari 2014 Organisatie en Werkwijze Medisch Ethische Toetsingscommissies Richtlijn van de Centrale Commissie
nwmo toetsingskader Eveline Loriaux - projectleider Kennisatelier 10 mei 2017 Vereniging Innovatieve Geneesmiddelen
 nwmo toetsingskader Eveline Loriaux - projectleider Kennisatelier 10 mei 2017 Vereniging Innovatieve Geneesmiddelen Zien we door de bomen nog het bos? 1 Overzicht nwmo Toetsingskader Start: juli 2015 Sinds
nwmo toetsingskader Eveline Loriaux - projectleider Kennisatelier 10 mei 2017 Vereniging Innovatieve Geneesmiddelen Zien we door de bomen nog het bos? 1 Overzicht nwmo Toetsingskader Start: juli 2015 Sinds
Dexamethasone for Cardiac Surgery (DECS) trial (Studie naar dexamethason bij hartchirurgie)
 PATIËNTEN INFORMATIE Dexamethasone for Cardiac Surgery (DECS) trial (Studie naar dexamethason bij hartchirurgie) Geachte heer/mevrouw, 1. Inleiding U bent onlangs op de wachtlijst geplaatst voor een open
PATIËNTEN INFORMATIE Dexamethasone for Cardiac Surgery (DECS) trial (Studie naar dexamethason bij hartchirurgie) Geachte heer/mevrouw, 1. Inleiding U bent onlangs op de wachtlijst geplaatst voor een open
Algemene informatie. Medisch wetenschappelijk onderzoek
 Algemene informatie Medisch wetenschappelijk onderzoek 1 Inleiding Artsen verrichten naast hun normale behandelingen soms medisch wetenschappelijk onderzoek. Dit doen artsen in het Scheper Ziekenhuis Emmen
Algemene informatie Medisch wetenschappelijk onderzoek 1 Inleiding Artsen verrichten naast hun normale behandelingen soms medisch wetenschappelijk onderzoek. Dit doen artsen in het Scheper Ziekenhuis Emmen
Patiëntinformatie TES
 Patiëntinformatie TES Datum: 6 november 2013 Onderwerp: Proefpersoneninformatie Geachte heer / mevrouw, U bent gevraagd om mee te doen aan een onderzoek naar de behoefte aan ondersteuning bij zorgen over
Patiëntinformatie TES Datum: 6 november 2013 Onderwerp: Proefpersoneninformatie Geachte heer / mevrouw, U bent gevraagd om mee te doen aan een onderzoek naar de behoefte aan ondersteuning bij zorgen over
Toezicht op uitvoering kan beter. Aanbevelingen uit rapport Toezicht op Medisch Wetenschappelijk Onderzoek met mensen
 Toezicht op uitvoering kan beter Aanbevelingen uit rapport Toezicht op Medisch Wetenschappelijk Onderzoek met mensen Najaarsbijeenkomst NVMETC 25 november 2015 Kor Grit, Jacqueline van Oijen 2 Inhoud presentatie
Toezicht op uitvoering kan beter Aanbevelingen uit rapport Toezicht op Medisch Wetenschappelijk Onderzoek met mensen Najaarsbijeenkomst NVMETC 25 november 2015 Kor Grit, Jacqueline van Oijen 2 Inhoud presentatie
JAARVERSLAG MEDISCH ETHISCHE TOETSINGSCOMMISSIE
 JAARVERSLAG 2018 MEDISCH ETHISCHE TOETSINGSCOMMISSIE Inhoudsopgave Pag. Voorwoord 2 1. Positionering 1.1 Plaats in de organisatie 1.2 Interne organisatie: administratie en gegevensbescherming / doorlooptijden
JAARVERSLAG 2018 MEDISCH ETHISCHE TOETSINGSCOMMISSIE Inhoudsopgave Pag. Voorwoord 2 1. Positionering 1.1 Plaats in de organisatie 1.2 Interne organisatie: administratie en gegevensbescherming / doorlooptijden
Ervaringen Adviescommissie nwmo
 Martini Ziekenhuis Groningen Ervaringen Adviescommissie nwmo Ellen Rusch, ambtelijk secretaris Wat gaan we doen? Adviescommissie nwmo Martini Ziekenhuis Wat hebben we de afgelopen periode gedaan? Documenten:
Martini Ziekenhuis Groningen Ervaringen Adviescommissie nwmo Ellen Rusch, ambtelijk secretaris Wat gaan we doen? Adviescommissie nwmo Martini Ziekenhuis Wat hebben we de afgelopen periode gedaan? Documenten:
Rapport Institutioneel Onderzoek
 Rapport Institutioneel Onderzoek Beleidsterrein patiëntenbeleid / Wet medisch-wetenschappelijk onderzoek met mensen Behorend bij het Basisselectiedocument voor de neerslag van de handelingen van de Medisch
Rapport Institutioneel Onderzoek Beleidsterrein patiëntenbeleid / Wet medisch-wetenschappelijk onderzoek met mensen Behorend bij het Basisselectiedocument voor de neerslag van de handelingen van de Medisch
Onderzoek naar de beste behandeling van patiënten met galstenen
 Onderzoek naar de beste behandeling van patiënten met galstenen Geachte heer/mevrouw, Wij doen onderzoek naar de beste behandeling van galstenen. Een onderzoeker zal contact met u opnemen om te vragen
Onderzoek naar de beste behandeling van patiënten met galstenen Geachte heer/mevrouw, Wij doen onderzoek naar de beste behandeling van galstenen. Een onderzoeker zal contact met u opnemen om te vragen
Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814.
 STAATSCOURANT Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814. Nr. 3583 24 januari 2017 Richtlijn van de Centrale Commissie Mensgebonden Onderzoek, de CCMO, krachtens artikel 24 van de
STAATSCOURANT Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814. Nr. 3583 24 januari 2017 Richtlijn van de Centrale Commissie Mensgebonden Onderzoek, de CCMO, krachtens artikel 24 van de
INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN TROMBOSEBEEN
 INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN TROMBOSEBEEN Hokusai post VTE studie: Lange termijn uitkomst na edoxaban versus warfarine voor
INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN TROMBOSEBEEN Hokusai post VTE studie: Lange termijn uitkomst na edoxaban versus warfarine voor
Verklaring van belangen
 Verklaring van belangen Reden voor invulling van dit formulier Ik verklaar hierbij dat er geen wijzigingen zijn te melden ten opzichte van de meest recente door mij ingevulde Verklaring van Belangen, waarvan
Verklaring van belangen Reden voor invulling van dit formulier Ik verklaar hierbij dat er geen wijzigingen zijn te melden ten opzichte van de meest recente door mij ingevulde Verklaring van Belangen, waarvan
JAARVERSLAG 2010. Commissie integriteit overheid (CIO)
 JAARVERSLAG 2010 Commissie integriteit overheid (CIO) Inhoudsopgave 1. Instelling en taken CIO 3 2. Samenstelling CIO en secretariaat 4 3. Aantallen en doorlooptijd 4 4. Analyse aantallen 4 5. Opvolging
JAARVERSLAG 2010 Commissie integriteit overheid (CIO) Inhoudsopgave 1. Instelling en taken CIO 3 2. Samenstelling CIO en secretariaat 4 3. Aantallen en doorlooptijd 4 4. Analyse aantallen 4 5. Opvolging
Kenmerk: V /R17.001/dj/ld Datum:
 Meander Medisch Centrum T.a.v. dr. P.H.G. Hogeman, kinderarts Postbus 1502 3800 BM AMERSFOORT Kenmerk: V.112232/R17.001/dj/ld Datum: 7-8-2017 Betreft: besluit NL59723.100.16 R17.001/PREP cariesrisk Geachte
Meander Medisch Centrum T.a.v. dr. P.H.G. Hogeman, kinderarts Postbus 1502 3800 BM AMERSFOORT Kenmerk: V.112232/R17.001/dj/ld Datum: 7-8-2017 Betreft: besluit NL59723.100.16 R17.001/PREP cariesrisk Geachte
EU verordening geneesmiddelenonderzoek
 EU verordening geneesmiddelenonderzoek Beoordelingen Europese s/jl mul/na/onaal vs. na/onale aanvraag Let op: de beoordeling wordt niet bij u ingediend maar in Europa via een Europese portal De beoordeling
EU verordening geneesmiddelenonderzoek Beoordelingen Europese s/jl mul/na/onaal vs. na/onale aanvraag Let op: de beoordeling wordt niet bij u ingediend maar in Europa via een Europese portal De beoordeling
Universitair Medisch Centrum. Dierexperimentencommissie Geneeskunde (DEC-GNK)
 Universitair Medisch Centrum utrecht JAARVERSLAG 2001 Dierexperimentencommissie Geneeskunde (DEC-GNK) Dierexperimentencommissie Geneeskunde UMC Utrecht, huispostnummer D 01,343, Postbus 85500, 3508 GA
Universitair Medisch Centrum utrecht JAARVERSLAG 2001 Dierexperimentencommissie Geneeskunde (DEC-GNK) Dierexperimentencommissie Geneeskunde UMC Utrecht, huispostnummer D 01,343, Postbus 85500, 3508 GA
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL2 Aanpassen proefpersoneninformatie / toestemmingsformulier aan lokale situatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen
Standard Operating Procedure STZ SOP: VL2 Aanpassen proefpersoneninformatie / toestemmingsformulier aan lokale situatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen
Onderzoek naar de optimale behandeling van patiënten met galstenen
 Onderzoek naar de optimale behandeling van patiënten met galstenen Geachte heer/mevrouw, Wij doen onderzoek naar de behandeling van galstenen. Uw arts heeft u gevraagd of u mee wilt werken aan dit onderzoek.
Onderzoek naar de optimale behandeling van patiënten met galstenen Geachte heer/mevrouw, Wij doen onderzoek naar de behandeling van galstenen. Uw arts heeft u gevraagd of u mee wilt werken aan dit onderzoek.
Titel van het onderzoek: Biobank voor chronische lymfatische leukemie, lymfeklierkanker en myeloom
 INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR PATIENTEN Titel van het onderzoek: Biobank voor chronische lymfatische leukemie, lymfeklierkanker en myeloom Geachte heer, mevrouw, Uw arts heeft u geïnformeerd
INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR PATIENTEN Titel van het onderzoek: Biobank voor chronische lymfatische leukemie, lymfeklierkanker en myeloom Geachte heer, mevrouw, Uw arts heeft u geïnformeerd
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
European Clinical Trial Regulation: Kans voor Nederland
 European Clinical Trial Regulation: Kans voor Nederland Annelies van Woudenberg, 13 november 2017 European Clinical Trial Regulation 536/ 2014 EU Verordening betreffende klinische proeven met geneesmiddelen
European Clinical Trial Regulation: Kans voor Nederland Annelies van Woudenberg, 13 november 2017 European Clinical Trial Regulation 536/ 2014 EU Verordening betreffende klinische proeven met geneesmiddelen
European Clinical Trial Regulation: Kans voor Nederland
 European Clinical Trial Regulation: Kans voor Nederland Annelies van Woudenberg, 14 november 2018 ECTR-project NL CCMO, DCRF en VWS: samenwerking bij implementatie ECTR Doel: als verordening van kracht
European Clinical Trial Regulation: Kans voor Nederland Annelies van Woudenberg, 14 november 2018 ECTR-project NL CCMO, DCRF en VWS: samenwerking bij implementatie ECTR Doel: als verordening van kracht
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen. Farmaceutische Bedrijven Deelteam Klinisch Onderzoek
 Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
DIFFERENT STEPS IN DRUG DEVELOPMENT: FROM THEORETICAL CONCEPT TO ACCESS FOR PATIENTS ROLE OF THE ETHICAL COMMITTEES
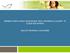 DIFFERENT STEPS IN DRUG DEVELOPMENT: FROM THEORETICAL CONCEPT TO ACCESS FOR PATIENTS ROLE OF THE ETHICAL COMMITTEES Klinische trials Verplicht vooraleer een geneesmiddel een marketing autorisatie kan krijgen
DIFFERENT STEPS IN DRUG DEVELOPMENT: FROM THEORETICAL CONCEPT TO ACCESS FOR PATIENTS ROLE OF THE ETHICAL COMMITTEES Klinische trials Verplicht vooraleer een geneesmiddel een marketing autorisatie kan krijgen
European Clinical Trial Regulation: Kans voor Nederland. Annelies van Woudenberg, ClinOps-dag NVFG, 20 april 2017
 European Clinical Trial Regulation: Kans voor Nederland Annelies van Woudenberg, ClinOps-dag NVFG, 20 april 2017 2 Dutch Clinical Research Foundation (DCRF) Doel ECTR project In oktober 2018 is Nederland
European Clinical Trial Regulation: Kans voor Nederland Annelies van Woudenberg, ClinOps-dag NVFG, 20 april 2017 2 Dutch Clinical Research Foundation (DCRF) Doel ECTR project In oktober 2018 is Nederland
Informatie voor donoren over UMC Utrecht Biobank TiN
 Informatie voor donoren over UMC Utrecht Biobank TiN Geachte mevrouw/mijnheer, In het kader van de Trombocytopathie in Nederland studie wordt een gedeelte van het extra afgenomen bloed opgeslagen in een
Informatie voor donoren over UMC Utrecht Biobank TiN Geachte mevrouw/mijnheer, In het kader van de Trombocytopathie in Nederland studie wordt een gedeelte van het extra afgenomen bloed opgeslagen in een
INFORMATIEBLAD VOOR PROEFPERSONEN ONDERZOEK VAN TRANSTHYRETINE-GEASSOCICIEERDE AMYLOÏDOSEN (THAOS)
 INFORMATIEBLAD VOOR PROEFPERSONEN ONDERZOEK VAN TRANSTHYRETINE-GEASSOCICIEERDE AMYLOÏDOSEN (THAOS) Protocoltitel: Protocolnummer: Naam opdrachtgever: Naam van THAOS-arts, contactgegevens en telefoonnummer:
INFORMATIEBLAD VOOR PROEFPERSONEN ONDERZOEK VAN TRANSTHYRETINE-GEASSOCICIEERDE AMYLOÏDOSEN (THAOS) Protocoltitel: Protocolnummer: Naam opdrachtgever: Naam van THAOS-arts, contactgegevens en telefoonnummer:
Antwoorden CRO-vragenlijst - foto van het veld
 Antwoorden CRO-vragenlijst - foto van het veld In samenwerking met het RIVM heeft de Inspectie voor de Gezondheidszorg (IGZ) een digitale vragenlijst ontwikkeld die bestond uit drie delen (zie Vragenlijst
Antwoorden CRO-vragenlijst - foto van het veld In samenwerking met het RIVM heeft de Inspectie voor de Gezondheidszorg (IGZ) een digitale vragenlijst ontwikkeld die bestond uit drie delen (zie Vragenlijst
REGLEMENT BEOORDELING AANVRAGEN TOT EEN BIJDRAGE UIT HET NATIONAAL RAMPENFONDS
 REGLEMENT BEOORDELING AANVRAGEN TOT EEN BIJDRAGE UIT HET NATIONAAL RAMPENFONDS van de stichting NATIONAAL RAMPENFONDS gevestigd te 's-gravenhage zoals vastgesteld in de vergadering van het Bestuur d.d.
REGLEMENT BEOORDELING AANVRAGEN TOT EEN BIJDRAGE UIT HET NATIONAAL RAMPENFONDS van de stichting NATIONAAL RAMPENFONDS gevestigd te 's-gravenhage zoals vastgesteld in de vergadering van het Bestuur d.d.
Handleiding. Investigational Medicinal Product Dossier (IMPD)
 Handleiding Investigational Medicinal Product Dossier (IMPD) Inhoudsopgave Afkortingen... - 3 - Wat is het IMPD?... - 4 - Beslisschema inhoud IMPD... - 5 - Beschrijving inhoud IMPD... - 6 - Overzicht hoofdstukken
Handleiding Investigational Medicinal Product Dossier (IMPD) Inhoudsopgave Afkortingen... - 3 - Wat is het IMPD?... - 4 - Beslisschema inhoud IMPD... - 5 - Beschrijving inhoud IMPD... - 6 - Overzicht hoofdstukken
NCTD Monitor. augustus 2008. vereniging innovatieve geneesmiddelen Nederland. Nefarma Clinical Trial Database
 NCTD Monitor augustus 2008 vereniging innovatieve geneesmiddelen Nederland Nefarma Clinical Trial Database Inhoudsopgave NCTD Monitor 2008 Samenvatting en conclusies 5 Inleiding 7 Monitor 2008 9 Overall
NCTD Monitor augustus 2008 vereniging innovatieve geneesmiddelen Nederland Nefarma Clinical Trial Database Inhoudsopgave NCTD Monitor 2008 Samenvatting en conclusies 5 Inleiding 7 Monitor 2008 9 Overall
Informatiebrief GRAFITI-studie
 Informatiebrief GRAFITI-studie Titel van het onderzoek GRAFITI-studie: onderzoek naar de groei van agressieve fibromatose. Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Informatiebrief GRAFITI-studie Titel van het onderzoek GRAFITI-studie: onderzoek naar de groei van agressieve fibromatose. Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A4 Publicatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A4 Publicatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Leids Universitair Medisch Centrum
 Leids Universitair Medisch Centrum afcte1in 9 postzone Commissie Medische Ethiek Hl-Q Mw. mr. S.Y.M. van der Heijden telefoon (071) 526 3241 e-mail cme@lumc.nl P16.054/SH/sh onze referentie uw referentie
Leids Universitair Medisch Centrum afcte1in 9 postzone Commissie Medische Ethiek Hl-Q Mw. mr. S.Y.M. van der Heijden telefoon (071) 526 3241 e-mail cme@lumc.nl P16.054/SH/sh onze referentie uw referentie
Verdiepende sessie Klinisch onderzoek MHM
 Verdiepende sessie Klinisch onderzoek MHM Opbrengsten en actiepunten Woensdag 14 februari 2018 Sufficient clinical evidence Wat is voldoende klinisch bewijs (voor medische hulpmiddelen zonder directe relatie
Verdiepende sessie Klinisch onderzoek MHM Opbrengsten en actiepunten Woensdag 14 februari 2018 Sufficient clinical evidence Wat is voldoende klinisch bewijs (voor medische hulpmiddelen zonder directe relatie
European Clinical Trial Regulation: Kans voor Nederland
 European Clinical Trial Regulation: Kans voor Nederland Annelies van Woudenberg, 9 juni 2017 ECTR biedt kans ambitie NL waar te maken Eenduidige toestemmingsprocedures Europa interessant voor internationale
European Clinical Trial Regulation: Kans voor Nederland Annelies van Woudenberg, 9 juni 2017 ECTR biedt kans ambitie NL waar te maken Eenduidige toestemmingsprocedures Europa interessant voor internationale
Patiënteninformatieformulier imprint studie
 Patiënteninformatieformulier imprint studie (imaging of PSMA: Registratie en Inventarisatie voor Nederlandse Toepassing) Inleiding Uw arts heeft voorgesteld een aanvraag te doen voor een PSMA-PET-scan.
Patiënteninformatieformulier imprint studie (imaging of PSMA: Registratie en Inventarisatie voor Nederlandse Toepassing) Inleiding Uw arts heeft voorgesteld een aanvraag te doen voor een PSMA-PET-scan.
Officiële uitgave van het Koninkrijk der Nederlanden sinds CCMO Deskundigheidseisen (WMO-)Leden METC s
 STAATSCOURANT Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814. Nr. 13083 29 juni 2012 CCMO Deskundigheidseisen (WMO-)Leden METC s Richtlijn van de centrale commissie voor medisch-wetenschappelijk
STAATSCOURANT Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814. Nr. 13083 29 juni 2012 CCMO Deskundigheidseisen (WMO-)Leden METC s Richtlijn van de centrale commissie voor medisch-wetenschappelijk
Jaarverslag Regionale Toetsingscommissie Patiëntgebonden Onderzoek
 Jaarverslag 2018 Regionale Toetsingscommissie Patiëntgebonden Onderzoek Secretariaat: Mw. A. Jonker MCL 3 e etage Dunantflat Postbus 888 8901 BR Leeuwarden Tel. : 058-2861151 Mail : RTPO@znb.nl Inhoud
Jaarverslag 2018 Regionale Toetsingscommissie Patiëntgebonden Onderzoek Secretariaat: Mw. A. Jonker MCL 3 e etage Dunantflat Postbus 888 8901 BR Leeuwarden Tel. : 058-2861151 Mail : RTPO@znb.nl Inhoud
Wetenschappelijke Commissie
 Taken en Werkwijze DPCG Wetenschappelijke Commissie Versie 09.04.2018 Inhoud 1. Begripsbepalingen 2. Taken Wetenschappelijke Commissie 3. Samenstelling Wetenschappelijke Commissie 4. Vergaderingen van
Taken en Werkwijze DPCG Wetenschappelijke Commissie Versie 09.04.2018 Inhoud 1. Begripsbepalingen 2. Taken Wetenschappelijke Commissie 3. Samenstelling Wetenschappelijke Commissie 4. Vergaderingen van
INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN LONGEMBOLIE
 INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN LONGEMBOLIE Hokusai post VTE studie: Lange termijn uitkomst na edoxaban versus warfarine voor
INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN LONGEMBOLIE Hokusai post VTE studie: Lange termijn uitkomst na edoxaban versus warfarine voor
METC MMC Jaarverslag 2017
 METC MMC Jaarverslag 2017 Inhoudsopgave Voorwoord p. 3 Inleiding p. 3 Onderwerpen 2017 p. 3 Activiteiten 2017 p. 4 Bevoegd gezag METC p. 4 Samenstelling commissie p. 4 Mutaties 2017 p. 5 Samenstelling
METC MMC Jaarverslag 2017 Inhoudsopgave Voorwoord p. 3 Inleiding p. 3 Onderwerpen 2017 p. 3 Activiteiten 2017 p. 4 Bevoegd gezag METC p. 4 Samenstelling commissie p. 4 Mutaties 2017 p. 5 Samenstelling
Cijfers jaarverslag CCMO 2015
 Cijfers jaarverslag CCMO 2015 Bron ToetsingOnline Peildatum 19 januari 2016 Sortering 2015 De commissies zijn gerangschikt naar het aantal besluiten dat zij over 2015 namen De cijfers Aan de in het Excel
Cijfers jaarverslag CCMO 2015 Bron ToetsingOnline Peildatum 19 januari 2016 Sortering 2015 De commissies zijn gerangschikt naar het aantal besluiten dat zij over 2015 namen De cijfers Aan de in het Excel
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik
 EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor CCMO, METC s en onderzoekers- Paula Vossebeld DCTF jaarcongres 7 oktober 2015 Verordening
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor CCMO, METC s en onderzoekers- Paula Vossebeld DCTF jaarcongres 7 oktober 2015 Verordening
Hierbij bieden wij u het jaarverslag aan van de commissie bezwaarschriften over het jaar 2017.
 Gemeente Coevorden Ing. 1 9 FEB. 2018 Aan Class nr. /lenftl ^uf Bezwaarschriftencommissie Gemeente Coevorden Postbus 2, 7740 AA Coevorden Telefoon: 0524-598631 Aan het college van burgemeester en wethouders
Gemeente Coevorden Ing. 1 9 FEB. 2018 Aan Class nr. /lenftl ^uf Bezwaarschriftencommissie Gemeente Coevorden Postbus 2, 7740 AA Coevorden Telefoon: 0524-598631 Aan het college van burgemeester en wethouders
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek PACER-onderzoek: Onderzoek naar de noodzaak van correctie van bloedplaatjestekort voor het plaatsen van een centraal veneuze
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek PACER-onderzoek: Onderzoek naar de noodzaak van correctie van bloedplaatjestekort voor het plaatsen van een centraal veneuze
Jouw GCP up-to-date in 45 minuten. Marieke Meulemans, oprichter GCP Central
 Jouw GCP up-to-date in 45 minuten Marieke Meulemans, oprichter GCP Central Waarom een GCP update tijdens de CRA dag? Gedreven Meesterschap. Meesterschap is vakmanschap. Vakmanschap is beheersing van het
Jouw GCP up-to-date in 45 minuten Marieke Meulemans, oprichter GCP Central Waarom een GCP update tijdens de CRA dag? Gedreven Meesterschap. Meesterschap is vakmanschap. Vakmanschap is beheersing van het
Proefpersoneninformatie Prevent trial
 Proefpersoneninformatie Prevent trial Voorkómen van een littekenbreuk naast het stoma door plaatsing van een kunststof matje. Originele titel: Preventie van parastomale hernia door versterking van de buikwand
Proefpersoneninformatie Prevent trial Voorkómen van een littekenbreuk naast het stoma door plaatsing van een kunststof matje. Originele titel: Preventie van parastomale hernia door versterking van de buikwand
Titel van het onderzoek: Bepaling van Zink en het Ontstekingseiwit PTX3 bij Patiënten met Sikkelcelziekte (ZIP studie)
 INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR PATIËNTEN Titel van het onderzoek: Bepaling van Zink en het Ontstekingseiwit PTX3 bij Patiënten met Sikkelcelziekte () Geachte heer/mevrouw, Wij vragen u om
INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR PATIËNTEN Titel van het onderzoek: Bepaling van Zink en het Ontstekingseiwit PTX3 bij Patiënten met Sikkelcelziekte () Geachte heer/mevrouw, Wij vragen u om
Proefpersoneninformatie
 Proefpersoneninformatie Titel van het onderzoek: Implementatie van de keuzehulp bestraling bij borstkanker en DCIS: een pre- en post-interventie studie. Geachte mevrouw, Uw behandelend arts heeft met u
Proefpersoneninformatie Titel van het onderzoek: Implementatie van de keuzehulp bestraling bij borstkanker en DCIS: een pre- en post-interventie studie. Geachte mevrouw, Uw behandelend arts heeft met u
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Routine versus op indicatie verwijderen van de stelschroef Routinematig versus op indicatie verwijderen van de stelschroef:
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Routine versus op indicatie verwijderen van de stelschroef Routinematig versus op indicatie verwijderen van de stelschroef:
Toenemende vraag naar nwmo studies Kwaliteit en transparantie voorop
 Beterdan Toenemende vraag naar nwmo studies Kwaliteit en transparantie voorop Joke Eggermont, Medisch Directeur Bristol-Myers Squibb Voorzitter Nefarma projectgroep niet-wmo plichtig onderzoek 1 Waarom?
Beterdan Toenemende vraag naar nwmo studies Kwaliteit en transparantie voorop Joke Eggermont, Medisch Directeur Bristol-Myers Squibb Voorzitter Nefarma projectgroep niet-wmo plichtig onderzoek 1 Waarom?
Informatie voor patiënten en toestemmingsformulier behorende bij het onderzoek:
 Informatie voor patiënten en toestemmingsformulier behorende bij het onderzoek: Titel: Karakterisering van buffycoat afgeleide granulocyten (witte bloedcellen) om klinische parameters te identificeren
Informatie voor patiënten en toestemmingsformulier behorende bij het onderzoek: Titel: Karakterisering van buffycoat afgeleide granulocyten (witte bloedcellen) om klinische parameters te identificeren
Standard Operating Procedure
 Standard Operating Procedure SOP: V9 Initiatievisite Auteur Naam: Functie instelling/afdeling Judie van den Elshout Staffunctionaris Wetenschapsbureau Wetenschapsbureau / Cluster Leerhuis Handtekening:...
Standard Operating Procedure SOP: V9 Initiatievisite Auteur Naam: Functie instelling/afdeling Judie van den Elshout Staffunctionaris Wetenschapsbureau Wetenschapsbureau / Cluster Leerhuis Handtekening:...
Patiënten Informatie formulier. SPLINT-trial
 Patiënten Informatie formulier SPLINT-trial Preventie van urologische complicaties bij niertransplantaties van levende donoren: splint of geen splint? Versie 2 09-10-2013 pagina 1 van 8 Titel van het onderzoek
Patiënten Informatie formulier SPLINT-trial Preventie van urologische complicaties bij niertransplantaties van levende donoren: splint of geen splint? Versie 2 09-10-2013 pagina 1 van 8 Titel van het onderzoek
JAARVERSLAG Inhoud. 1. Stichting Part-Ner. 2. Belangrijkste werkzaamheden Samenwerking met andere organisaties. 4.
 JAARVERSLAG 2015 Inhoud 1. Stichting Part-Ner 2. Belangrijkste werkzaamheden 2015 3. Samenwerking met andere organisaties 4. Vooruitblik 1 1. Stichting Part-Ner Na afronding van het project certificering
JAARVERSLAG 2015 Inhoud 1. Stichting Part-Ner 2. Belangrijkste werkzaamheden 2015 3. Samenwerking met andere organisaties 4. Vooruitblik 1 1. Stichting Part-Ner Na afronding van het project certificering
REGLEMENT RAAD VAN TOEZICHT HOGESCHOOL LEIDEN
 REGLEMENT RAAD VAN TOEZICHT HOGESCHOOL LEIDEN ALGEMEEN Artikel 1. Algemene bepalingen 1. Dit reglement is het huishoudelijk reglement van de Raad van Toezicht, bedoeld in artikel 15 van de statuten van
REGLEMENT RAAD VAN TOEZICHT HOGESCHOOL LEIDEN ALGEMEEN Artikel 1. Algemene bepalingen 1. Dit reglement is het huishoudelijk reglement van de Raad van Toezicht, bedoeld in artikel 15 van de statuten van
Therapeutisch versus niet-therapeutisch onderzoek bij minderjarige en wilsonbekwame proefpersonen
 Therapeutisch versus niet-therapeutisch onderzoek bij minderjarige en wilsonbekwame proefpersonen In de Wet medisch-wetenschappelijk onderzoek met mensen (WMO) staat: Het is verboden wetenschappelijk onderzoek
Therapeutisch versus niet-therapeutisch onderzoek bij minderjarige en wilsonbekwame proefpersonen In de Wet medisch-wetenschappelijk onderzoek met mensen (WMO) staat: Het is verboden wetenschappelijk onderzoek
