Antwoorden CRO-vragenlijst - foto van het veld
|
|
|
- Adriaan Baert
- 4 jaren geleden
- Aantal bezoeken:
Transcriptie
1 Antwoorden CRO-vragenlijst - foto van het veld In samenwerking met het RIVM heeft de Inspectie voor de Gezondheidszorg (IGZ) een digitale vragenlijst ontwikkeld die bestond uit drie delen (zie Vragenlijst CRO). Deze waren: Deel 1 - Algemene kenmerken van de organisatie Deel 2 - Werkzaamheden voor opdrachtgevers Deel 3 - Kwaliteit en procedures Eind augustus 2012 stuurde de IGZ 180 bedrijven, die mogelijk onder de definitie van CRO vielen en werkzaamheden gedelegeerd kregen van verrichters in klinisch geneesmiddelenonderzoek in Nederland, een vooraankondiging met informatie over het project en het vragenlijstonderzoek. Vervolgens ontvingen 157 bedrijven in binnen- en buitenland een uitnodiging om de digitale vragenlijst in te vullen. Op de sluitingsdatum van de digitale vragenlijst hadden 119 bedrijven de vragenlijst ingevuld. In totaal voldeden 69 bedrijven aan de definitie van CRO, zoals deze in het richtsnoer ICH-GCP staat genoemd (zie ICH-GCP 1.20) en waren zij betrokken bij klinisch geneesmiddelenonderzoek in Nederland. Hieronder staan de resulaten van de vragenlijst (n=69). Deel 1 - Algemene kenmerken N % Totaal % Vraag 2 Nederlandse vestiging Ja 54 78,3% Nee 15 21,7% Vraag 3 Organisatievorm (gehercodeerd *) Vennootschap 57 82,6% Vraag 4 Is uw organisatie onderdeel van een grotere/internationale organisatie/moederbedrijf? Vraag 9A Aantal werknemers in dienst op (gehercodeerd ^) Vraag 9B % werknemers betrokken bij klinisch geneesmiddelenonderzoek (gehercodeerd ^) Non-profit 7 10,1% ZZP 5 7,2% Ja 33 47,8% Nee 36 52,2% ,7% ,9% > ,4% 0-25% 28 40,6% 26-75% 17 24,6% % 24 34,8% Vraag 10 Gem. aantal dienstjaren in 2011 (gehercodeerd ^) <1 9 13,0% 1 tot ,4% 5 tot ,0% ,6% Vraag 11 Aantal werknemers uit dienst in 2011 (gehercodeerd ^) 0 t/m ,5% Vraag 12 Type opdrachtgever 6 t/m ,8% 11 t/m ,3% > ,3% Academische ziekenhuizen Ja 24 34,8% Nee 45 65,2% Overige ziekenhuizen Ja 12 17,4% Nee 57 82,6% Pagina 1 van 6
2 Vraag 12A Farmaceutische bedrijven Ja 61 88,4% Nee 8 11,6% Andere CRO s Ja 30 43,5% Nee 39 56,5% Onderzoeksgroepen Ja 13 18,8% Nee 56 81,2% Niet farmaceutische organisaties Ja 10 14,5% Aantal verschillende type opdrachtgevers (gehercodeerd obv vraag 12 ^) Nee 59 85,5% 0 1 1,4% ,0% ,7% ,4% 4 6 8,7% 5 5 7,2% 6 1 1,4% Vraag 13 Opdrachtgevers in NL in 2011 (gehercodeerd ^) ,1% 1 t/m ,4% 6 t/m ,8% >10 6 8,7% Vraag 14 Opdrachtgevers in buitenland in 2011 (gehercodeerd ^) ,1% 1 t/m ,0% 6 t/m ,0% > ,8% Vraag 15 Studies in NL in 2011 (gehercodeerd ^) ,0% 1 t/m ,8% 6 t/m ,0% 11 t/m ,5% > ,6% Vraag 17 Vast aanspreekpunt bij opdrachtgever (gehercodeerd *) Ja 55 79,7% Nee 5 7,2% Wisselend 5 7,2% N.v.t. 3 4,3% Vraag 19 Deel 2 Werkzaamheden N % Type onderzoek Klinisch geneesmiddelenonderzoek (WMO: wetenschappelijk onderzoek met geneesmiddelen) Totaal % Ja 68 98,6% Nee 1 1,4% Interventieonderzoek met medische hulpmiddelen Ja 45 65,2% Interventieonderzoek met voedingsmiddelen en voedingssupplementen Nee 24 34,8% Ja 21 30,4% Nee 48 69,6% Ander interventieonderzoek Ja 16 23,2% Nee 53 76,8% Observationeel onderzoek Ja 42 60,9% Nee 27 39,1% Anders, namelijk: Ja 6 8,7% Vraag 19A Aantal verschillende type onderzoek ,6% Vraag 20 Sponsortaken Opstellen studiedocumentatie (SOPs; studieprotocol; Investigator s Brochure) ,8% ,6% ,4% ,5% Ja 48 69,6% Nee 21 30,4% Selectie en rekrutering onderzoekers/instellingen Ja 51 73,9% Nee 18 26,1% Monitoring Ja 53 76,8% Auditing van kwaliteitsborging Ja 39 56,5% Pagina 2 van 6
3 Nee 30 43,5% Training (gericht op de studie) Ja 49 71,0% Nee 20 29,0% Interactive voice response (IVRS), randomisatie Ja 24 34,8% Nee 45 65,2% Verplichtingen rond geneesmiddel voor onderzoek Ja 14 20,3% (bereiden, verpakken, etiketteren, coderen, beheer voor afleveren) Nee 55 79,7% Data management Ja 41 59,4% Farmacovigilantie-werkzaamheden (inclusief rapportage bijwerkingen) Nee 28 40,6% Ja 36 52,2% Nee 33 47,8% Statistische analyse Ja 37 53,6% Nee 32 46,4% Opstellen Clinical study reports (CSR) Ja 36 52,2% Regulatoire taken, zoals het opstellen en indienen van aanvragen Nee 33 47,8% Ja 51 73,9% Nee 18 26,1% ICT Ja 5 7,2% Nee 64 92,8% Anders, namelijk Ja 2 2,9% Nee 67 97,1% Vraag 20A Aantal sponsortaken (gehercodeerd obv vraag 20 ^) 1 t/m ,1% Vraag 21 Overige taken 6 t/m ,8% > ,1% Rekrutering proefpersonen (taak onderzoeker/uitvoerder) Ja 13 18,8% Uitvoeren van onderzoek op eigen onderzoekslocatie (taak onderzoeker/uitvoerder) Beheer geneesmiddel voor onderzoek op onderzoekslocatie (taak onderzoeker/uitvoerder) Nee 56 81,2% Ja 13 18,8% Nee 56 81,2% Ja 10 14,5% Nee 59 85,5% Marketing en communicatie Ja 12 17,4% Nee 57 82,6% Schrijven van artikelen Ja 27 39,1% Nee 42 60,9% Sales Ja 5 7,2% Nee 64 92,8% Laboratorium en/of diagnostisch onderzoek Ja 17 24,6% Anders, namelijk Ja 6 8,7% Geen Ja 25 36,2% Nee 44 63,8% Vraag 21A Aantal overige taken (gehercodeerd obv vraag 21 ^) ,5% Vraag 22 Taken uitbesteed Opstellen studiedocumentatie (SOPs; studieprotocol; Investigator s Brochure) 1 t/m ,7% >6 4 5,8% Ja 1 1,4% Nee 68 98,6% Selectie en rekrutering onderzoekers/instellingen Ja 3 4,3% Monitoring Ja 8 11,6% Nee 61 88,4% Auditing van kwaliteitsborging Ja 2 2,9% Nee 67 97,1% Training (gericht op de studie) Ja 3 4,3% Interactive voice response (IVRS), randomisatie Ja 17 24,6% Verplichtingen rond geneesmiddel voor onderzoek (bereiden, verpakken, etiketteren, coderen, beheer voor Ja 17 24,6% Pagina 3 van 6
4 afleveren) Data management Ja 7 10,1% Farmacovigilantie-werkzaamheden (inclusief rapportage bijwerkingen) Nee 62 89,9% Ja 7 10,1% Nee 62 89,9% Statistische analyse Ja 6 8,7% Opstellen Clinical study reports (CSR) Ja 3 4,3% Regulatoire taken, zoals het opstellen en indienen van aanvragen Ja 6 8,7% Anders, namelijk Ja 9 13,0% Nee 60 87,0% Geen Ja 39 56,5% Nee 30 43,5% Vraag 22A Aantal taken gedelegeerd (gehercodeerd obv vraag 22 ^) ,5% Vraag 23 Vraag 24 Wordt een opdrachtgever altijd geïnformeerd indien uw organisatie taken aan subcontractors delegeert? Heeft uw organisatie invloed op de totstandkoming van het studieprotocol en amendementen? 1 t/m ,1% >6 3 4,3% Ja 50 72,5% n.v.t ,6% Anders, reden 2 2,9% Ja 34 49,3% Nee 20 29,0% Wisselend 15 21,7% Deel 3 - Kwaliteit en procedures N % Totaal % Vraag 27 Werken met SOPs Ja, eigen 14 20,3% Ja, sponsor 6 8,7% Ja, beide 46 66,7% Nee 3 4,3% Vraag 29 Worden SOPs up-to-date gehouden (gehercodeerd *)? Periodiek en ad 23 33,3% hoc Periodiek 35 50,7% Ad hoc 4 5,8% N.v.t. 7 10,1% Vraag 30 Werken met Kwaliteitssysteem Ja, eigen 19 27,5% Vraag 33 Wordt het Kwaliteitssysteem up-to-date gehouden (gehercodeerd *)? Ja, sponsor 6 8,7% Ja, beide 42 60,9% Nee 2 2,9% Periodiek en ad 19 27,5% hoc Periodiek 30 43,5% Ad hoc 12 17,4% N.v.t. 8 11,6% Vraag 32 Heeft uw organisatie een kwaliteitsfunctionaris? Ja, namelijk 53 76,8% Vraag 35 Aantal audits sinds 2011 (gehercodeerd ^) ,3% 1 5 7,2% ,3% 3 3 4,3% 4 t/m ,6% 10 of vaker 16 23,2% Vraag 36 Is uw organisatie bezocht door een (nationale of Ja, aantal keer 17 24,6% internationale) overheidsinspectiedienst t.b.v. klinisch geneesmiddelenonderzoek in de periode van 1 januari 2011 t/m heden? Vraag 37 Worden subcontractors geauditeerd (gehercodeerd *)? Ja 44 63,8% Nee 1 1,4% Pagina 4 van 6
5 Vraag 38 Vraag 39 Heeft uw organisatie kwalificatie-eisen vastgesteld voor de verschillende functies binnen uw organisatie? Is er voor iedere werknemer die betrokken is bij klinisch geneesmiddelenonderzoek een opleidingsplan? Anders 8 11,6% N.v.t ,2% Ja 60 87,0% Nee 9 13,0% Ja, 50 72,5% opleidingsplan is schriftelijk Ja, maar 10 14,5% opleidingsplan is niet schriftelijk Nee 9 13,0% Vraag 40 Update opleidingsplan (gehercodeerd *) Ja, periodiek 37 53,6% Ja, ad hoc 19 27,5% Geen plan of in 4 5,8% ontwikkeling N.v.t. 9 13,0% Vraag 41 Vindt er studiespecifieke training plaats? Ja, namelijk 63 91,3% Vraag 42 Vraag 43 Vraag 44 Vraag 45 Opleiding geneesmiddelenonderzoek algemeen Nee 6 8,7% Kwaliteitssysteem en SOPs Ja 62 89,9% Nee 7 10,1% Wet- en regelgeving over klinisch onderzoek Ja 59 85,5% Nee 10 14,5% GMP Ja 14 20,3% Nee 55 79,7% Farmacovigilantie Ja 35 50,7% Nee 34 49,3% Klinisch-wetenschappelijke kennis Ja 50 72,5% Nee 19 27,5% Anders, namelijk Ja 25 36,2% Nee 44 63,8% Geen training/opleiding Ja 2 2,9% Vindt er training/opleiding plaats van tijdelijk ingehuurde medewerkers die direct betrokken zijn bij klinisch geneesmiddelenonderzoek? Heeft uw organisatie een gedragscode t.b.v. klinisch geneesmiddelenonderzoek voor directie en medewerkers? Heeft uw organisatie regels omtrent nevenfuncties van personeel? Nee 67 97,1% Ja 47 68,1% Nee 1 1,4% N.v.t ,4% Ja, schriftelijk 37 53,6% Ja, maar niet 11 15,9% schriftelijk Nee 21 30,4% Ja, schriftelijk 50 72,5% Ja, maar niet 3 4,3% schriftelijk Vraag 46 Is uw organisatie aangesloten bij een branchevereniging? Ja 47 68,1% Nee 22 31,9% Vraag 47 Bij wie maakt CRO betrokkenheid studie bekend? 0,0% Toetsende instanties (METC s en bevoegde instantie) Ja 53 76,8% Proefpersonen Ja 19 27,5% Nee 50 72,5% Onderzoekers Ja 51 73,9% Nee 18 26,1% Betrokkenheid wordt niet bekend gemaakt Ja 5 7,2% Nee 64 92,8% Anders: namelijk Ja 15 21,7% Nee 54 78,3% Dit is niet bekend Ja 3 4,3% Pagina 5 van 6
6 * Op basis van de antwoorden zijn de antwoordcategorieën aangepast ^ Op basis van de antwoorden zijn er antwoordcategorieën gemaakt Pagina 6 van 6
Resultaten CRO-vragenlijst - foto van het veld
 Resultaten CRO-vragenlijst - foto van het veld Dee1: Algemene kenmerken van de organisatie Dit hoofdstuk beschrijft de kenmerken, werkzaamheden en de kwaliteit van 9 CRO s waaraan verrrichters taken en
Resultaten CRO-vragenlijst - foto van het veld Dee1: Algemene kenmerken van de organisatie Dit hoofdstuk beschrijft de kenmerken, werkzaamheden en de kwaliteit van 9 CRO s waaraan verrrichters taken en
De rol van de Contract Research Organisatie (CRO) Klinisch onderzoek
 De rol van de Contract Research Organisatie (CRO) in klinisch geneesmiddelenonderzoek Klinisch onderzoek Inhoud Aanleiding CRO project Methode en resultaten» Werkwijze en resultaten foto van het veld vragenlijst»
De rol van de Contract Research Organisatie (CRO) in klinisch geneesmiddelenonderzoek Klinisch onderzoek Inhoud Aanleiding CRO project Methode en resultaten» Werkwijze en resultaten foto van het veld vragenlijst»
Toezicht op IIT: bevindingen vanuit de praktijk
 Toezicht op IIT: bevindingen vanuit de praktijk Elysée Hille, senior inspecteur namens deelteam KO-GCP Teamcoördinator KO-GCP/PhV/GZH Afdeling Farmaceutische Bedrijven Wat doet de IGZ? Toezicht op klinisch
Toezicht op IIT: bevindingen vanuit de praktijk Elysée Hille, senior inspecteur namens deelteam KO-GCP Teamcoördinator KO-GCP/PhV/GZH Afdeling Farmaceutische Bedrijven Wat doet de IGZ? Toezicht op klinisch
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen. Farmaceutische Bedrijven Deelteam Klinisch Onderzoek
 Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) Team Klinisch Onderzoek
 Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) 2014-2016 Team Klinisch Onderzoek Toezicht op IIT 2014-2016 Aanleiding en werkwijze Bevindingen vanuit de praktijk Conclusies en aandachtspunten
Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) 2014-2016 Team Klinisch Onderzoek Toezicht op IIT 2014-2016 Aanleiding en werkwijze Bevindingen vanuit de praktijk Conclusies en aandachtspunten
Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen
 Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen Afdeling Farmaceutische Bedrijven, Klinisch Onderzoek Good Clinical Practice Inhoud Wat doet de IGJ aan toezicht op klinisch
Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen Afdeling Farmaceutische Bedrijven, Klinisch Onderzoek Good Clinical Practice Inhoud Wat doet de IGJ aan toezicht op klinisch
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U9 Monitoren Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies Versiedatum Hoofdstuk Versiedatum Hoofdstuk
Standard Operating Procedure STZ SOP: U9 Monitoren Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies Versiedatum Hoofdstuk Versiedatum Hoofdstuk
CRO s kwaliteit en toegevoegde waarde
 CRO s kwaliteit en toegevoegde waarde dr. Annejet P. Meijler Programmadirecteur Geneesmiddelen IGZ 1 Medisch-wetenschappelijk onderzoek 4 april 2011 Deze workshop Inleiding I prof. Herman Pieterse Inleiding
CRO s kwaliteit en toegevoegde waarde dr. Annejet P. Meijler Programmadirecteur Geneesmiddelen IGZ 1 Medisch-wetenschappelijk onderzoek 4 april 2011 Deze workshop Inleiding I prof. Herman Pieterse Inleiding
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U11 Voortgangsrapportage Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: U11 Voortgangsrapportage Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Formulier Voortgangsrapportage
 Formulier Voortgangsrapportage De METC azm/um wil van al het door haar beoordeelde WMO-onderzoek jaarlijks een voortgangsrapportage zien. Zij heeft deze eis daartoe opgenomen in de tekst van haar eigen
Formulier Voortgangsrapportage De METC azm/um wil van al het door haar beoordeelde WMO-onderzoek jaarlijks een voortgangsrapportage zien. Zij heeft deze eis daartoe opgenomen in de tekst van haar eigen
Monitoren vs auditen. CRA dag 21 april 2016
 Monitoren vs auditen CRA dag 21 april 2016 Introductie Freelance consultant, mede oprichter TAPAS Group B.V. Mede oprichter/directeur van CRA B.V. Medical Adviser Yamanouchi Pharma Clinical trial monitor
Monitoren vs auditen CRA dag 21 april 2016 Introductie Freelance consultant, mede oprichter TAPAS Group B.V. Mede oprichter/directeur van CRA B.V. Medical Adviser Yamanouchi Pharma Clinical trial monitor
Inhoud onderzoeksdossier
 Inhoud onderzoeksdossier (documenten in de witte box zijn nodig voor de primaire beoordeling) A. Brieven B. Formulieren C. Onderzoeksprotocol en protocolamendementen D. Productinformatie E. Informatie
Inhoud onderzoeksdossier (documenten in de witte box zijn nodig voor de primaire beoordeling) A. Brieven B. Formulieren C. Onderzoeksprotocol en protocolamendementen D. Productinformatie E. Informatie
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U10 Audit Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: U10 Audit Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum Opmerkingen
Toezicht op klinisch onderzoek - bevindingen vanuit de praktijk
 Toezicht op klinisch onderzoek - bevindingen vanuit de praktijk Namens Deelprogramma Klinisch Onderzoek, IGZ Spreker Dr. ir. J. Eland-Gerritsen Coördinerend/Specialistisch Senior inspecteur Inhoud Toezicht
Toezicht op klinisch onderzoek - bevindingen vanuit de praktijk Namens Deelprogramma Klinisch Onderzoek, IGZ Spreker Dr. ir. J. Eland-Gerritsen Coördinerend/Specialistisch Senior inspecteur Inhoud Toezicht
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A1 Afsluiting studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A1 Afsluiting studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL5 Protocolamendement (lokaal) Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: VL5 Protocolamendement (lokaal) Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A2 Archiveren studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A2 Archiveren studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Monitoring van Investigator Initiated onderzoek
 Monitoring van Investigator Initiated onderzoek V1.0 Angela Vlug Clinical Research Bureau VUmc Wat is een IIS (volgens de NFU) Onderzoek waarvoor de raad van bestuur van een (universitair) medisch centrum
Monitoring van Investigator Initiated onderzoek V1.0 Angela Vlug Clinical Research Bureau VUmc Wat is een IIS (volgens de NFU) Onderzoek waarvoor de raad van bestuur van een (universitair) medisch centrum
Toezicht op uitvoering kan beter. Aanbevelingen uit rapport Toezicht op Medisch Wetenschappelijk Onderzoek met mensen
 Toezicht op uitvoering kan beter Aanbevelingen uit rapport Toezicht op Medisch Wetenschappelijk Onderzoek met mensen Najaarsbijeenkomst NVMETC 25 november 2015 Kor Grit, Jacqueline van Oijen 2 Inhoud presentatie
Toezicht op uitvoering kan beter Aanbevelingen uit rapport Toezicht op Medisch Wetenschappelijk Onderzoek met mensen Najaarsbijeenkomst NVMETC 25 november 2015 Kor Grit, Jacqueline van Oijen 2 Inhoud presentatie
Toezicht op kwaliteitsborging: ken uw verantwoordelijkheden
 Toezicht op kwaliteitsborging: ken uw verantwoordelijkheden Elysée Hille Karina van Wonderen namens deelteam Klinisch Onderzoek-GCP Afdeling Farmaceutische Bedrijven Workshop Kwaliteitsbewaking door samenwerking
Toezicht op kwaliteitsborging: ken uw verantwoordelijkheden Elysée Hille Karina van Wonderen namens deelteam Klinisch Onderzoek-GCP Afdeling Farmaceutische Bedrijven Workshop Kwaliteitsbewaking door samenwerking
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VC9 Proefpersonen- en aansprakelijkheidsverzekering (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure STZ SOP: VC9 Proefpersonen- en aansprakelijkheidsverzekering (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL2 Aanpassen proefpersoneninformatie / toestemmingsformulier aan lokale situatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen
Standard Operating Procedure STZ SOP: VL2 Aanpassen proefpersoneninformatie / toestemmingsformulier aan lokale situatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VC8 Beoordeling amendement toetsende commissie (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure STZ SOP: VC8 Beoordeling amendement toetsende commissie (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Toenemende vraag naar nwmo studies Kwaliteit en transparantie voorop
 Beterdan Toenemende vraag naar nwmo studies Kwaliteit en transparantie voorop Joke Eggermont, Medisch Directeur Bristol-Myers Squibb Voorzitter Nefarma projectgroep niet-wmo plichtig onderzoek 1 Waarom?
Beterdan Toenemende vraag naar nwmo studies Kwaliteit en transparantie voorop Joke Eggermont, Medisch Directeur Bristol-Myers Squibb Voorzitter Nefarma projectgroep niet-wmo plichtig onderzoek 1 Waarom?
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: O3 Ontwikkelen, implementeren en beheren van SOP s Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies
Standard Operating Procedure STZ SOP: O3 Ontwikkelen, implementeren en beheren van SOP s Distributielijst : STZ Datum : 15-10-2012 Revisiedatum : 15-10-2013 Veranderingen ten opzichte van eerdere versies
1. Voorafgaand aan de klinische fase van het onderzoek
 Essentiële documenten Bron: Richtsnoer voor good clinical practice (CPMP/ICH/135/95) De verwijzingen in dit document verwijzen naar de artikelen in bovenstaand document. 1. Voorafgaand aan de klinische
Essentiële documenten Bron: Richtsnoer voor good clinical practice (CPMP/ICH/135/95) De verwijzingen in dit document verwijzen naar de artikelen in bovenstaand document. 1. Voorafgaand aan de klinische
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U4 Registratie /randomisatie procedure Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum
Standard Operating Procedure STZ SOP: U4 Registratie /randomisatie procedure Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum
Klinisch Onderzoek met Medische Hulpmiddelen
 Klinisch Onderzoek met Medische Hulpmiddelen Het perspectief van de toezichthouder Dhr. dr. P.W. (Paul) Riem Vis Doel en outline Doelen: 1) Veilig op de markt brengen medische hulpmiddelen; 2) Inzicht
Klinisch Onderzoek met Medische Hulpmiddelen Het perspectief van de toezichthouder Dhr. dr. P.W. (Paul) Riem Vis Doel en outline Doelen: 1) Veilig op de markt brengen medische hulpmiddelen; 2) Inzicht
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U6 Studie medicatie Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: U6 Studie medicatie Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Geneesmiddelenonderzoek en de ziekenhuisapotheek
 Geneesmiddelenonderzoek en de ziekenhuisapotheek Pierre Bet ziekenhuisapotheker Klinische Farmacologie & Apotheek VU medisch centrum feb 2011 Inhoud Verantwoordelijkheden Bereiding van IMP Voortraject
Geneesmiddelenonderzoek en de ziekenhuisapotheek Pierre Bet ziekenhuisapotheker Klinische Farmacologie & Apotheek VU medisch centrum feb 2011 Inhoud Verantwoordelijkheden Bereiding van IMP Voortraject
Site selectie visite checklist
 Site selectie visite checklist Informatie sponsor: Naam sponsor: Contactpersoon: Functie: Afdeling: Telefoonnummer : Email : Informatie onderzoekslocatie: Naam onderzoekslocatie : Naam onderzoeker: Functie:
Site selectie visite checklist Informatie sponsor: Naam sponsor: Contactpersoon: Functie: Afdeling: Telefoonnummer : Email : Informatie onderzoekslocatie: Naam onderzoekslocatie : Naam onderzoeker: Functie:
1. Beschrijving werkgebieden / thema s
 1. Beschrijving werkgebieden / thema s Nr 1 Thema Wetenschappelijke Achtergrond en Opzet van Onderzoek 2 Ethische en veiligheid overwegingen 3 Ontwikkeling en Regelgeving 4 Clinical Trial Operations (Projectorganisatie)
1. Beschrijving werkgebieden / thema s Nr 1 Thema Wetenschappelijke Achtergrond en Opzet van Onderzoek 2 Ethische en veiligheid overwegingen 3 Ontwikkeling en Regelgeving 4 Clinical Trial Operations (Projectorganisatie)
Contract Research Organisaties in Nederland Inventarisatie en kwaliteitsniveau
 Contract Research Organisaties in Nederland Inventarisatie en kwaliteitsniveau RIVM rapport 370005001/2011 K. Notenboom A.R. Molema-Buursma I. Hegger Contract Research Organisaties in Nederland: inventarisatie
Contract Research Organisaties in Nederland Inventarisatie en kwaliteitsniveau RIVM rapport 370005001/2011 K. Notenboom A.R. Molema-Buursma I. Hegger Contract Research Organisaties in Nederland: inventarisatie
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U1 Identificatie, werving en pre-screening proefpersonen Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure STZ SOP: U1 Identificatie, werving en pre-screening proefpersonen Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere
Contract Research Organisaties in Nederland Inventarisatie en kwaliteitsniveau
 Contract Research Organisaties in Nederland Inventarisatie en kwaliteitsniveau RIVM rapport 370005001/2011 K. Notenboom A.R. Molema-Buursma I. Hegger Contract Research Organisaties in Nederland: inventarisatie
Contract Research Organisaties in Nederland Inventarisatie en kwaliteitsniveau RIVM rapport 370005001/2011 K. Notenboom A.R. Molema-Buursma I. Hegger Contract Research Organisaties in Nederland: inventarisatie
Klinische studies. Veel meer dan een extra tube
 Klinische studies Veel meer dan een extra tube Good Clinical Practice Het geheel van kwaliteitseisen op ethisch en wetenschappelijk gebied, die internationaal zijn erkend en moeten worden gerespecteerd
Klinische studies Veel meer dan een extra tube Good Clinical Practice Het geheel van kwaliteitseisen op ethisch en wetenschappelijk gebied, die internationaal zijn erkend en moeten worden gerespecteerd
Gez Hulpmiddelen met Klinis KO me t amenlijk MH: Medisc ge ch zam enlij Onderzoek toezicht k toe zich he t
 Klinisch Onderzoek met Medische Hulpmiddelen Gezamenlijk toezicht Doel en outline Doelen: 1) Verbeteren veiligheid medische hulpmiddelen voor patiënten; 2) Inzicht geven in insteek inspectie bij KO met
Klinisch Onderzoek met Medische Hulpmiddelen Gezamenlijk toezicht Doel en outline Doelen: 1) Verbeteren veiligheid medische hulpmiddelen voor patiënten; 2) Inzicht geven in insteek inspectie bij KO met
Monitorplan voorbeeld
 Monitorplan voorbeeld Protocol Er moet in het protocol beschreven worden dat er monitoring plaatsvindt (zie ook CCMO voorbeeld template). Het monitoringplan mag als bijlage worden toegevoegd (in dat geval
Monitorplan voorbeeld Protocol Er moet in het protocol beschreven worden dat er monitoring plaatsvindt (zie ook CCMO voorbeeld template). Het monitoringplan mag als bijlage worden toegevoegd (in dat geval
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A4 Publicatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A4 Publicatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek
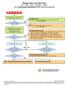 Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek Melding voorval proefpersoon aan onderzoeker/arts 1 Rapportage voorval door onderzoeker/arts in patiëntenstatus
Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek Melding voorval proefpersoon aan onderzoeker/arts 1 Rapportage voorval door onderzoeker/arts in patiëntenstatus
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U5 Datamanagement Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: U5 Datamanagement Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Praktische implementatie Europese verordening Geneesmiddelen onderzoek
 Praktische implementatie Europese verordening Geneesmiddelen onderzoek Dr. Joost Keers Hoofd Wetenschappelijk Instituut j.keers@mzh.nl 050 524 5826 http://www.ccmo.nl/nl/europese-verordening Belangrijke
Praktische implementatie Europese verordening Geneesmiddelen onderzoek Dr. Joost Keers Hoofd Wetenschappelijk Instituut j.keers@mzh.nl 050 524 5826 http://www.ccmo.nl/nl/europese-verordening Belangrijke
Standard Operating Procedure
 Standard Operating Procedure SOP: V9 Initiatievisite Auteur Naam: Functie instelling/afdeling Judie van den Elshout Staffunctionaris Wetenschapsbureau Wetenschapsbureau / Cluster Leerhuis Handtekening:...
Standard Operating Procedure SOP: V9 Initiatievisite Auteur Naam: Functie instelling/afdeling Judie van den Elshout Staffunctionaris Wetenschapsbureau Wetenschapsbureau / Cluster Leerhuis Handtekening:...
Aanmelden medischwetenschappelijk
 Aanmelden medischwetenschappelijk onderzoek SOP Aanmelden WMO-plichtig onderzoek_versie juli 2016.doc Pagina 1 van 10 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd
Aanmelden medischwetenschappelijk onderzoek SOP Aanmelden WMO-plichtig onderzoek_versie juli 2016.doc Pagina 1 van 10 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL4 Investigator Site File Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: VL4 Investigator Site File Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Overzicht interne scholing oncologie monitor
 Overzicht interne scholing oncologie monitor Gegevens monitor: Naam + Voorletters:... Lidmaatschapsnummer NVvOD:... Werkzaam bij: Naam organisatie I:... Adres:... Postcode:... Plaats:... Bereikbaar via
Overzicht interne scholing oncologie monitor Gegevens monitor: Naam + Voorletters:... Lidmaatschapsnummer NVvOD:... Werkzaam bij: Naam organisatie I:... Adres:... Postcode:... Plaats:... Bereikbaar via
Handleiding Goedkeuringsprocedure Raad van Bestuur Zuyderland wetenschappelijk onderzoek
 Handleiding Goedkeuringsprocedure Raad van Bestuur Zuyderland wetenschappelijk onderzoek INLEIDING oor al het onderzoek dat binnen Zuyderland wordt uitgevoerd moet goedkeuring worden verkregen van de Raad
Handleiding Goedkeuringsprocedure Raad van Bestuur Zuyderland wetenschappelijk onderzoek INLEIDING oor al het onderzoek dat binnen Zuyderland wordt uitgevoerd moet goedkeuring worden verkregen van de Raad
Clinical Trials in Nederland: op weg naar topkwaliteit DCTF Congres 3 oktober 2012 Lunteren. M.P.W. Lamberti, BA Algemeen Directeur
 Clinical Trials in Nederland: op weg naar topkwaliteit DCTF Congres 3 oktober 2012 Lunteren M.P.W. Lamberti, BA Algemeen Directeur Maastricht UMC-Holding MUMC-Holding CTCM BPCM MI Groningen Utrecht Nijmegen
Clinical Trials in Nederland: op weg naar topkwaliteit DCTF Congres 3 oktober 2012 Lunteren M.P.W. Lamberti, BA Algemeen Directeur Maastricht UMC-Holding MUMC-Holding CTCM BPCM MI Groningen Utrecht Nijmegen
KLINISCH GENEESMIDDELEN- ONDERZOEK
 KLINISCH GENEESMIDDELEN- ONDERZOEK HET PROCES VAN HET OPSTARTEN VAN KLINISCH ONDERZOEK MET GENEESMIDDELEN GAAT VERANDEREN De ECTR verandert het klinisch onderzoek met geneesmiddelen in Europa. Dit heeft
KLINISCH GENEESMIDDELEN- ONDERZOEK HET PROCES VAN HET OPSTARTEN VAN KLINISCH ONDERZOEK MET GENEESMIDDELEN GAAT VERANDEREN De ECTR verandert het klinisch onderzoek met geneesmiddelen in Europa. Dit heeft
Digitale vragenlijst De vragenlijst is opgezet als een 'webbased survey', een vragenlijst die via het internet ingevuld kan worden.
 Vragenlijst CRO 2012 Infrmatie ver de digitale vragenlijst De Inspectie vr de Gezndheidszrg (hierna: de inspectie) hudt tezicht p klinisch nderzek p basis van de Wet medisch-wetenschappelijk nderzek met
Vragenlijst CRO 2012 Infrmatie ver de digitale vragenlijst De Inspectie vr de Gezndheidszrg (hierna: de inspectie) hudt tezicht p klinisch nderzek p basis van de Wet medisch-wetenschappelijk nderzek met
Aanvraagformulier REGISTRATIE oncologie monitor
 Aanvraagformulier REGISTRATIE oncologie monitor 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:... Geboorteplaats:... Werkzaam bij: Organisatie + Afdeling:...
Aanvraagformulier REGISTRATIE oncologie monitor 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:... Geboorteplaats:... Werkzaam bij: Organisatie + Afdeling:...
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek
 Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
Vragen en antwoorden over de gegevenssectie van de model-pif
 Vragen en antwoorden over de gegevenssectie van de model-pif Algemene informatie over de Algemene Verordening Gegevensbescherming Waar vind ik algemene informatie over de gevolgen van de Algemene Verordening
Vragen en antwoorden over de gegevenssectie van de model-pif Algemene informatie over de Algemene Verordening Gegevensbescherming Waar vind ik algemene informatie over de gevolgen van de Algemene Verordening
Kwaliteitsborging vanuit academisch perspectief DCTF jaarcongres 2016
 Kwaliteitsborging vanuit academisch perspectief DCTF jaarcongres 2016 Gemma Voss 5 oktober 2016 Mensgebonden onderzoek (WMO) in Nederland 2015 CCMO-jaarverslag 2015 CCMO-jaarverslag 2015 Mensgebonden onderzoek
Kwaliteitsborging vanuit academisch perspectief DCTF jaarcongres 2016 Gemma Voss 5 oktober 2016 Mensgebonden onderzoek (WMO) in Nederland 2015 CCMO-jaarverslag 2015 CCMO-jaarverslag 2015 Mensgebonden onderzoek
Jouw GCP up-to-date in 45 minuten. Marieke Meulemans, oprichter GCP Central
 Jouw GCP up-to-date in 45 minuten Marieke Meulemans, oprichter GCP Central Waarom een GCP update tijdens de CRA dag? Gedreven Meesterschap. Meesterschap is vakmanschap. Vakmanschap is beheersing van het
Jouw GCP up-to-date in 45 minuten Marieke Meulemans, oprichter GCP Central Waarom een GCP update tijdens de CRA dag? Gedreven Meesterschap. Meesterschap is vakmanschap. Vakmanschap is beheersing van het
Ervaringen Adviescommissie nwmo
 Martini Ziekenhuis Groningen Ervaringen Adviescommissie nwmo Ellen Rusch, ambtelijk secretaris Wat gaan we doen? Adviescommissie nwmo Martini Ziekenhuis Wat hebben we de afgelopen periode gedaan? Documenten:
Martini Ziekenhuis Groningen Ervaringen Adviescommissie nwmo Ellen Rusch, ambtelijk secretaris Wat gaan we doen? Adviescommissie nwmo Martini Ziekenhuis Wat hebben we de afgelopen periode gedaan? Documenten:
Henk Jan Out, Paul van Meurs en Rudolf van Olden. Van eerste humane toediening tot algemeen gebruik
 VII 1 Introductie tot de farmaceutische geneeskunde................................ 1 Henk Jan Out, Paul van Meurs en Rudolf van Olden I Van eerste humane toediening tot algemeen gebruik 2 Exploratory
VII 1 Introductie tot de farmaceutische geneeskunde................................ 1 Henk Jan Out, Paul van Meurs en Rudolf van Olden I Van eerste humane toediening tot algemeen gebruik 2 Exploratory
De ECTR: een kans voor Nederland! Annelies van Woudenberg, DCRF congres, 5 oktober 2016
 De ECTR: een kans voor Nederland! Annelies van Woudenberg, DCRF congres, 5 oktober 2016 European Clinical Trial Regulation 536/ 2014 European Clinical Trial Regulation (ECTR): EU Verordening betreffende
De ECTR: een kans voor Nederland! Annelies van Woudenberg, DCRF congres, 5 oktober 2016 European Clinical Trial Regulation 536/ 2014 European Clinical Trial Regulation (ECTR): EU Verordening betreffende
RISK BASED MONITORING IIS FROM AN ACADEMIC PERSPECTIVE; SURGICAL SPECIALTIES
 RISK BASED MONITORING IIS FROM AN ACADEMIC PERSPECTIVE; SURGICAL SPECIALTIES 8 Oktober 2014, DCTF Onderzoeksbureau Divisie Heelkundige Specialismen UMC Utrecht Marianne van Es-Gulinck, arts, F.F.P.M. RISK
RISK BASED MONITORING IIS FROM AN ACADEMIC PERSPECTIVE; SURGICAL SPECIALTIES 8 Oktober 2014, DCTF Onderzoeksbureau Divisie Heelkundige Specialismen UMC Utrecht Marianne van Es-Gulinck, arts, F.F.P.M. RISK
Aanvraagformulier REGISTRATIE LOKAAL ONCOLOGIE DATAMANAGER GEGEVENS AANVRAGER
 GEGEVENS AANVRAGER Naam + Voorletters Voorna(a)m(en) Adres Postcode + Woonplaats Geboortedatum Geboorteplaats E-mailadres/telefoon Lidmaatschapsnummer NVvOD geen lid Datum preregistratie LDM Werkervaring
GEGEVENS AANVRAGER Naam + Voorletters Voorna(a)m(en) Adres Postcode + Woonplaats Geboortedatum Geboorteplaats E-mailadres/telefoon Lidmaatschapsnummer NVvOD geen lid Datum preregistratie LDM Werkervaring
Verklaring van belangen
 Verklaring van belangen Reden voor invulling van dit formulier Maak uw keuze Ik werk reeds voor het CBG en vul de Verklaring van belangen opnieuw in Algemeen Titel(s) Voornaam Dr. Gabe Tussenvoegsels Achternaam
Verklaring van belangen Reden voor invulling van dit formulier Maak uw keuze Ik werk reeds voor het CBG en vul de Verklaring van belangen opnieuw in Algemeen Titel(s) Voornaam Dr. Gabe Tussenvoegsels Achternaam
SOP aanleveren en afhandelen WMO onderzoek METC Onze Lieve Vrouwe Gasthuis, versie 1, juli
 Aanmelden en afhandelen medisch-wetenschappelijk onderzoek met mensen (WMO-onderzoek) Medisch-ethische toetsingscommissie (METC) Onze Lieve Vrouwe Gasthuis Hieronder treft u aan de procedure van aanmelding
Aanmelden en afhandelen medisch-wetenschappelijk onderzoek met mensen (WMO-onderzoek) Medisch-ethische toetsingscommissie (METC) Onze Lieve Vrouwe Gasthuis Hieronder treft u aan de procedure van aanmelding
INFORMATIEBLAD. Maart 2011
 INFORMATIEBLAD AANMELDING TRIALBUREAU/DATACENTRUM Maart 2011 Kanker zo snel mogelijk terugdringen en onder controle brengen. We zijn er voor mensen die leven met kanker en de mensen die met hen samenleven.
INFORMATIEBLAD AANMELDING TRIALBUREAU/DATACENTRUM Maart 2011 Kanker zo snel mogelijk terugdringen en onder controle brengen. We zijn er voor mensen die leven met kanker en de mensen die met hen samenleven.
Verklaring van belangen
 Verklaring van belangen Reden voor invulling van dit formulier Maak uw keuze Algemeen Gewenste aanhef Titel(s) Voornaam Ik werk reeds voor het CBG en vul de Verklaring van belangen opnieuw in Dhr. Dr.
Verklaring van belangen Reden voor invulling van dit formulier Maak uw keuze Algemeen Gewenste aanhef Titel(s) Voornaam Ik werk reeds voor het CBG en vul de Verklaring van belangen opnieuw in Dhr. Dr.
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U2 Informed consent Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: U2 Informed consent Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
 ------------------------------------------------------------------------------------------------------------------------------------------- Concept Procedure Lokale Haalbaarheid klinisch geneesmiddelenonderzoek
------------------------------------------------------------------------------------------------------------------------------------------- Concept Procedure Lokale Haalbaarheid klinisch geneesmiddelenonderzoek
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik
 EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
Link naar het filmpje: https://www.youtube.com/watch?v =PLIVVDmDjDI. Eerst even dit:
 Link naar het filmpje: https://www.youtube.com/watch?v =PLIVVDmDjDI Eerst even dit: 1 ECTR: Keep calm and get organised! Marieke Meulemans, GCP Central Annelies van Woudenberg, DCRF Workshop ECTR DCRF
Link naar het filmpje: https://www.youtube.com/watch?v =PLIVVDmDjDI Eerst even dit: 1 ECTR: Keep calm and get organised! Marieke Meulemans, GCP Central Annelies van Woudenberg, DCRF Workshop ECTR DCRF
CCMO Structuur documenten Technische Toetsing (ass.secr.) Inhoudelijke Toetsing (secretaris)
 CHECKLIST WMO Primaire indieningsproces WMO in METC Management, screening door Assistent Secretaris. Hieronder staan de generieke uitgangspunten en is toegelicht hoe de primaire toetsing indiening WMO
CHECKLIST WMO Primaire indieningsproces WMO in METC Management, screening door Assistent Secretaris. Hieronder staan de generieke uitgangspunten en is toegelicht hoe de primaire toetsing indiening WMO
Checklist Lokale Uitvoerbaarheid
 Primaire indieningsproces Lokale Uitvoerbaarheid in METC Management, screening door Assistent Secretaris. Hieronder staan de generieke uitgangspunten en is toegelicht hoe de toetsing indiening Lokale Uitvoerbaarheid
Primaire indieningsproces Lokale Uitvoerbaarheid in METC Management, screening door Assistent Secretaris. Hieronder staan de generieke uitgangspunten en is toegelicht hoe de toetsing indiening Lokale Uitvoerbaarheid
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U8 Melding van (Serious) Adverse Events en SUSARs Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies
Standard Operating Procedure STZ SOP: U8 Melding van (Serious) Adverse Events en SUSARs Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies
IC ICF ICH ISF. Lijst met afkortingen, definities en termen STZ-Kwaliteitshandboek SOP s
 Lijst met afkortingen, definities en termen STZ-Kwaliteitshandboek SOP s ABR ADR AE AR BROK CCMO CRF CTA CV DSMB EMEA EU EudraCT FU brief GCP GMP IB IC ICF ICH IMPD ISF MEB METC EU RCT SAE SOP SPC SUSAR
Lijst met afkortingen, definities en termen STZ-Kwaliteitshandboek SOP s ABR ADR AE AR BROK CCMO CRF CTA CV DSMB EMEA EU EudraCT FU brief GCP GMP IB IC ICF ICH IMPD ISF MEB METC EU RCT SAE SOP SPC SUSAR
Informatiebrief PGx Lung cancer studie
 Informatiebrief PGx Lung cancer studie Genetische variaties als risicofactor voor toxiciteit bij longkankerpatiënten die chemoradiotherapie of chemotherapie ondergaan Geachte meneer, mevrouw, U bent door
Informatiebrief PGx Lung cancer studie Genetische variaties als risicofactor voor toxiciteit bij longkankerpatiënten die chemoradiotherapie of chemotherapie ondergaan Geachte meneer, mevrouw, U bent door
Utrecht, september 2016
 Eindrapport van het inspectiebezoek in het kader van Geneesmiddelen zonder Handelsvergunning aan ziekenhuisapotheek Nij Smellinghe te Drachten, op 25 mei 2016 Utrecht, september 2016 Documentnummer: 1008874
Eindrapport van het inspectiebezoek in het kader van Geneesmiddelen zonder Handelsvergunning aan ziekenhuisapotheek Nij Smellinghe te Drachten, op 25 mei 2016 Utrecht, september 2016 Documentnummer: 1008874
De laatste versie van dit document is te downloaden op: www.umcutrecht.nl/metc. Indienen documenten bij de METC UMC Utrecht
 Indienen documenten bij de METC UMC Utrecht Begin hier Bekijk in onderstaande tabel wat u wilt indienen. Kijk daarna welke methode van indiening en welke documenten bij uw indiening horen. Volg bij het
Indienen documenten bij de METC UMC Utrecht Begin hier Bekijk in onderstaande tabel wat u wilt indienen. Kijk daarna welke methode van indiening en welke documenten bij uw indiening horen. Volg bij het
Aanmelden WMO-plichtig onderzoek
 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd wordt bij het aanmelden van onderzoek dat onder de WMO valt en waarbij ZGV optreedt als deelnemend centrum. Voordat
Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd wordt bij het aanmelden van onderzoek dat onder de WMO valt en waarbij ZGV optreedt als deelnemend centrum. Voordat
Verklaring van belangen
 Verklaring van belangen Reden voor invulling van dit formulier Ik verklaar hierbij dat er geen wijzigingen zijn te melden ten opzichte van de meest recente door mij ingevulde Verklaring van Belangen, waarvan
Verklaring van belangen Reden voor invulling van dit formulier Ik verklaar hierbij dat er geen wijzigingen zijn te melden ten opzichte van de meest recente door mij ingevulde Verklaring van Belangen, waarvan
Op naar het snel opstarten van klinisch onderzoek in Nederland!
 Op naar het snel opstarten van klinisch onderzoek in Nederland! Marika Trieling Voorzitter DCRF werkgroep Lokale uitvoerbaarheid 12 februari 2019 Wat is er in Nederland nodig? Verkorten tijdslijnen van
Op naar het snel opstarten van klinisch onderzoek in Nederland! Marika Trieling Voorzitter DCRF werkgroep Lokale uitvoerbaarheid 12 februari 2019 Wat is er in Nederland nodig? Verkorten tijdslijnen van
Verklaring van belangen
 Verklaring van belangen Reden voor invulling van dit formulier Maak uw keuze Ik werk reeds voor het CBG en vul de Verklaring van belangen opnieuw in Algemeen Titel(s) Voornaam Tussenvoegsels Achternaam
Verklaring van belangen Reden voor invulling van dit formulier Maak uw keuze Ik werk reeds voor het CBG en vul de Verklaring van belangen opnieuw in Algemeen Titel(s) Voornaam Tussenvoegsels Achternaam
Aanvraagformulier REGISTRATIE oncologie datamanager
 Aanvraagformulier REGISTRATIE oncologie datamanager 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:.... Geboorteplaats:.... Werkzaam bij: Organisatie +
Aanvraagformulier REGISTRATIE oncologie datamanager 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:.... Geboorteplaats:.... Werkzaam bij: Organisatie +
Centrum klinische farmacologie: deelnemen aan een klinische studie
 Centrum klinische farmacologie: deelnemen aan een klinische studie informatie voor gezonde proefpersonen en patïenten INLEIDING 3 KLINISCHE STUDIES: EEN INLEIDING 4 De ontwikkeling van een nieuw geneesmiddel
Centrum klinische farmacologie: deelnemen aan een klinische studie informatie voor gezonde proefpersonen en patïenten INLEIDING 3 KLINISCHE STUDIES: EEN INLEIDING 4 De ontwikkeling van een nieuw geneesmiddel
Eindrapport van het GDP inspectiebezoek aan Ursapharm Benelux B.V. te Helmond, op 8 maart Utrecht, 2016
 Eindrapport van het GDP inspectiebezoek aan Ursapharm Benelux B.V. te Helmond, op 8 maart 2016 Utrecht, 2016 1. Geïnspecteerde locatie(s): Ursapharm Benelux B.V. Steenovenweg 5 5708 HN HELMOND 2. Activiteiten:
Eindrapport van het GDP inspectiebezoek aan Ursapharm Benelux B.V. te Helmond, op 8 maart 2016 Utrecht, 2016 1. Geïnspecteerde locatie(s): Ursapharm Benelux B.V. Steenovenweg 5 5708 HN HELMOND 2. Activiteiten:
European Clinical Trial Regulation: Kans voor Nederland
 European Clinical Trial Regulation: Kans voor Nederland Annelies van Woudenberg, 9 juni 2017 ECTR biedt kans ambitie NL waar te maken Eenduidige toestemmingsprocedures Europa interessant voor internationale
European Clinical Trial Regulation: Kans voor Nederland Annelies van Woudenberg, 9 juni 2017 ECTR biedt kans ambitie NL waar te maken Eenduidige toestemmingsprocedures Europa interessant voor internationale
Verklaring van belangen
 Reden voor invulling van dit formulier Maak uw keuze Algemeen Verklaring van belangen Gewenste aanhef Titel(s) Voornaam Tussenvoegsels Achternaam Afdeling Functienaam Omschrijving van uw werkzaamheden
Reden voor invulling van dit formulier Maak uw keuze Algemeen Verklaring van belangen Gewenste aanhef Titel(s) Voornaam Tussenvoegsels Achternaam Afdeling Functienaam Omschrijving van uw werkzaamheden
MDR (2017/745) en klinisch onderzoek - Implementatie in Nederland -
 MDR (2017/745) en klinisch onderzoek - Implementatie in Nederland - DCRF 26 september 2018 Monique Al Teamcoördinator Landelijk Bureau CCMO MDR: Drie hoofdcategoriën klinisch onderzoek I II III Klinisch
MDR (2017/745) en klinisch onderzoek - Implementatie in Nederland - DCRF 26 september 2018 Monique Al Teamcoördinator Landelijk Bureau CCMO MDR: Drie hoofdcategoriën klinisch onderzoek I II III Klinisch
Handleiding Goedkeuringsprocedure Raad van Bestuur Zuyderland voor wetenschappelijk onderzoek
 Handleiding Goedkeuringsprocedure Raad van Bestuur Zuyderland voor wetenschappelijk onderzoek Deze handleiding wordt voortdurend geupdate naar aanleiding van de meest recente wet- en regelgeving en wijzigingen
Handleiding Goedkeuringsprocedure Raad van Bestuur Zuyderland voor wetenschappelijk onderzoek Deze handleiding wordt voortdurend geupdate naar aanleiding van de meest recente wet- en regelgeving en wijzigingen
Verklaring van belangen
 Verklaring van belangen Algemeen Titel(s) Voornaam Dr. A.A.M. Tussenvoegsels Achternaam Afdeling (Voor externe experts, wilt u aangeven voor welke afdeling van het CBG u werkt) Functienaam Omschrijving
Verklaring van belangen Algemeen Titel(s) Voornaam Dr. A.A.M. Tussenvoegsels Achternaam Afdeling (Voor externe experts, wilt u aangeven voor welke afdeling van het CBG u werkt) Functienaam Omschrijving
Introductie en uitleg nieuwe GDP Richtsnoer door insiders
 Introductie en uitleg nieuwe GDP Richtsnoer door insiders Riekert Bruinink IGZ Ethel Mertens FAGG Brussel IGZ bijeenkomst de nieuwe GDP Guideline, een stap voorwaarts 2 september 2013 Plaatje gezondheidszorg
Introductie en uitleg nieuwe GDP Richtsnoer door insiders Riekert Bruinink IGZ Ethel Mertens FAGG Brussel IGZ bijeenkomst de nieuwe GDP Guideline, een stap voorwaarts 2 september 2013 Plaatje gezondheidszorg
Kwaliteit: Minder is meer
 Kwaliteit: Minder is meer Kwaliteit in klinisch onderzoek met medische hulpmiddelen Jako Pranger QA Manager Cardialysis 9 Nov 2012 Kwaliteit en integriteit Mensgebonden onderzoek Trends in kwaliteitsbeleving
Kwaliteit: Minder is meer Kwaliteit in klinisch onderzoek met medische hulpmiddelen Jako Pranger QA Manager Cardialysis 9 Nov 2012 Kwaliteit en integriteit Mensgebonden onderzoek Trends in kwaliteitsbeleving
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U7 Ondersteunende diensten Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: U7 Ondersteunende diensten Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Research data management in een academisch ziekenhuis
 Research data management in een academisch ziekenhuis 9 november 2016 Rudy Scholte, Hoofd data management Clinical Research Unit Academisch Medisch Centrum r.a.scholte@amc.nl Research data management Onderzoek
Research data management in een academisch ziekenhuis 9 november 2016 Rudy Scholte, Hoofd data management Clinical Research Unit Academisch Medisch Centrum r.a.scholte@amc.nl Research data management Onderzoek
Bouwen aan vertrouwen: perspectief van de industrie
 Symposium ter gelegenheid afscheid Ad van Dooren Zelfredzaamheid van patiënten bij gebruik van veilige medicatie. Bouwen aan vertrouwen: perspectief van de industrie Rudolf van Olden, arts Medisch Directeur
Symposium ter gelegenheid afscheid Ad van Dooren Zelfredzaamheid van patiënten bij gebruik van veilige medicatie. Bouwen aan vertrouwen: perspectief van de industrie Rudolf van Olden, arts Medisch Directeur
1. Er is sprake van medisch wetenschappelijk onderzoek én
 Normen voor toetsing nwmo onderzoek Introductie De gezondheidszorg is gebaat bij het plaatsvinden van verantwoord medisch- wetenschappelijk onderzoek. Voor onderzoek dat onder de Wet Medisch Wetenschappelijk
Normen voor toetsing nwmo onderzoek Introductie De gezondheidszorg is gebaat bij het plaatsvinden van verantwoord medisch- wetenschappelijk onderzoek. Voor onderzoek dat onder de Wet Medisch Wetenschappelijk
Verklaring van belangen
 Verklaring van belangen Reden voor invulling van dit formulier Maak uw keuze Ik werk reeds voor het CBG en vul de Verklaring van belangen opnieuw in Algemeen Mw. Titel(s) Voornaam Tussenvoegsels Achternaam
Verklaring van belangen Reden voor invulling van dit formulier Maak uw keuze Ik werk reeds voor het CBG en vul de Verklaring van belangen opnieuw in Algemeen Mw. Titel(s) Voornaam Tussenvoegsels Achternaam
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik
 EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor CCMO, METC s en onderzoekers- Paula Vossebeld DCTF jaarcongres 7 oktober 2015 Verordening
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor CCMO, METC s en onderzoekers- Paula Vossebeld DCTF jaarcongres 7 oktober 2015 Verordening
WERKNEMER. Verklaring van belangen. Algemeen. Melding van belangen op farmaceutisch gebied. Tussenvoegsels
 Verklaring van belangen Algemeen Titel(s) Voornaam Prof. dr. Bert Tussenvoegsels Achternaam Afdeling (Voor externe experts, wilt u aangeven voor welke afdeling van het CBG u werkt) Functienaam Omschrijving
Verklaring van belangen Algemeen Titel(s) Voornaam Prof. dr. Bert Tussenvoegsels Achternaam Afdeling (Voor externe experts, wilt u aangeven voor welke afdeling van het CBG u werkt) Functienaam Omschrijving
5. Goedkeuring deelname door de toetsende METC 6. Start- en einddatum onderzoek 7. Rekening
 Aanleveren documenten voor het uitbrengen van advies over lokale uitvoerbaarheid bij de Medisch-ethische toetsingscommissie (METC) in het Onze Lieve Vrouwe Gasthuis Mocht u nog vragen hebben naar aanleiding
Aanleveren documenten voor het uitbrengen van advies over lokale uitvoerbaarheid bij de Medisch-ethische toetsingscommissie (METC) in het Onze Lieve Vrouwe Gasthuis Mocht u nog vragen hebben naar aanleiding
Verdiepende sessie Klinisch onderzoek MHM
 Verdiepende sessie Klinisch onderzoek MHM Opbrengsten en actiepunten Woensdag 14 februari 2018 Sufficient clinical evidence Wat is voldoende klinisch bewijs (voor medische hulpmiddelen zonder directe relatie
Verdiepende sessie Klinisch onderzoek MHM Opbrengsten en actiepunten Woensdag 14 februari 2018 Sufficient clinical evidence Wat is voldoende klinisch bewijs (voor medische hulpmiddelen zonder directe relatie
Titel: Good Clinical Practice & Monitoring. Initiation Investigator Driven Studies. Versie: 14-jan-2013
 Titel: Good Clinical Practice & Monitoring Initiation Investigator Driven Studies Inhoud Wet- en regelgeving/declaration of Helsinki Good Clinical Practice Patiënteninformatie/ informed consent Basisvereisten
Titel: Good Clinical Practice & Monitoring Initiation Investigator Driven Studies Inhoud Wet- en regelgeving/declaration of Helsinki Good Clinical Practice Patiënteninformatie/ informed consent Basisvereisten
De BOOG: Kan het nog beter en waar gaan we naar toe? S. Sleijfer, Erasmus MC-DDHK
 De BOOG: Kan het nog beter en waar gaan we naar toe? S. Sleijfer, Erasmus MC-DDHK Visie en focus Visie: BOOG coördineert en faciliteert het klinisch borstkankeronderzoek in Nederland om de behandeling
De BOOG: Kan het nog beter en waar gaan we naar toe? S. Sleijfer, Erasmus MC-DDHK Visie en focus Visie: BOOG coördineert en faciliteert het klinisch borstkankeronderzoek in Nederland om de behandeling
