Uitwerkingen Basischemie hoofdstuk 8
|
|
|
- Ine Peters
- 4 jaren geleden
- Aantal bezoeken:
Transcriptie
1 Uitwerkinen Basischemie hoofdstuk 8 Opave 8. Opave 8. Zuur of basisch? Van vier oplossinen, enummerd A, B, C en D, wordt de ph met een ph-meter bepaald. Hieronder staan de resultaten. Opl. A: ph = 8,5 Opl. B: ph = 0,80 Opl. C: ph = 6,0 Opl. D: ph =,7 a. De [HO + ] is het rootst bij de kleinste ph Als ph = - dan [HO + ]=0 /, als ph = 0 dan [HO + ] = / en als ph = 0, dan [HO + ] = 0,8 / Dus oplossin B heeft de rootste [HO + ] b. De [OH - ] is het rootst als de [HO + ] het kleinst is. De [HO + ] is het kleinst als de ph het rootst is. Dus oplossin D heeft de rootste waarde van [OH - ] Zoutzuur in het lab In het chemisch lab hant een bord met de concentratie van een aantal standaardoplossinen. a. HCl (l) + HO (l) HO + (aq) + Cl - (aq) b. ph = -lo(ho + )= -lo(0,066) = 0,97 [HO + ] = 0,066 / d. ph = 0,97 De concentratie [HO + ] hant niet af van het volume! Opave 8. Opave 8.4 ph uitrekenen Bereken de ph van: a. ph = -lo([ho + ]) = -lo(0,05) =,46 b. ph= -lo([ho + ]) = -lo(0,045) =,46 ( protolyse stap) [HO + ] = 0,0 0-4 =,0 0 - ph = -lo([ho + ]) = -lo(,0 0 - ) =,00 Zure reen [HO + ] = 6,5 0-4 / ph = -lo([ho + ]) = -lo(6,5 0-4 ) =,9 Opave 8.5 [HO + ] uitrekenen a. ph = 4, [HO + ] = 0-4, = 6, 0-5 / aferond [HO + ]= / (opm: aantal decimalen ph = aantal sinificante cijfers [HO + ]) b. ph =, [HO + ] = 0 -, = 0,050 / aferond: [HO + ]= 0,05 / ph =,0 [HO + ] = 0 -,0 = 0,0 / uitwerkinen hoofdstuk 8 Basischemie 07 Vervoort Boeken
2 d. ph = 0,855 [HO + ] = 0-0,855 = 0,40 / e. ph =,85 [HO + ] = 0 -,85 = 0,04 / Opave 8.6 ph van bloed ph = 7,5 [HO + ] = 0-7,5 = 4,5 0-8 / ph = 7,45 [HO + ] = 0-7,45 =,5 0-8 / Opave 8.7 Zwavelzuur [HO + ] = 7, 0 4 / a. ph lit tussen en 4 7, 0-4 lit tussen 0-4 en ofwel tussen,0 0-4 en,0 0 - b. ph lo( 7, 0 ), Klopt met antwoord vraa a. Afronden op decimalen ( cijfers achter de komma) omdat de concentratie is eeven in sinificante cijfers Opave 8.8 ph berekeninen TUSSENSTAPPEN a. ph=,80 [HO + ] = 0 -,8 =,6 0-4 / n c V n, 6 0 0, 00, 0 m n M m, 0 6, 46, 6 0 HCl Opave 8.9 Neatieve ph ph = -0,7 [HO + ] = 0 -ph = 0 +0,7 = 5 / Opave 8.0 Handelsoplossin zoutzuur a. (HCl-opl), m(hcl-opl) V, 00 m 0 m m m( HCl) 6% van 0 0, 6 0 4, m 4, n,8 M 6,46 b. n,8 c H O,8 V 0,00 ph lo([h O ]) lo(, 8), 07 uitwerkinen hoofdstuk 8 Basischemie 07 Vervoort Boeken
3 Opave 8. ph berekeninen 4 Het maximale massapercentae van een zwavelzuuroplossin bedraat 96 %. a. HSO4(aq) + HO(l) HO + (aq) + HSO4 - (aq) b. k m 800, 8 m( ) 800 n 8,5 M 98,079 n 8,5 [H O ] 8,5 V,000 b. ph = -lo([ho + ]) = -lo(8,5) = -,6 Opave 8. Manesium oplossen in zoutzuur M (s) + HO + (aq) M + (aq) + HO (l) + H () Je voet 00 m manesium bij 00 m,00 M zoutzuur. a. M : M 4,05 4,05 m m 00 m n(m) 8, m 4,05 m m + n(h O ) V c 0,00,00 0,00 00 m Er is een overmaat aan HO + -ionen b. Er kan maximaal 8, m H () ontstaan + + n H O : n M : n H O 8, 6, 5 m Er reaeert 8, = 6,5 m HO + Er blijft over 00 6,5 = 8,5 m HO + n 8,5 m [ HO ] 0,85 m 0,85 V 00 m m ph (einde reactie) = -lo([ho + ]) = -lo(0,85) = 0,078 Opave 8. Standaardoplossinen,0 zoutzuur met ph=,50,0 salpeterzuur met ph =,50 [HO + ] = 0 -,50 = 0,006 / aferond: [HO + ] = 0,00 / m(hcl) n M 0, 006 6, 46 0, 5 m(hno ) n M 0, 006 6, 0 0, 99 uitwerkinen hoofdstuk 8 Basischemie 07 Vervoort Boeken
4 Opave 8.4 ph bij verdunnin a. ph = 5,8 [HO + ] = 0 -ph = 0-5,8 =,6 0-6 / Volens afrondinsreel eienlijk ph = 0-6 / b. De [HO + ] wordt kleiner en dus de ph roter. Het volume wordt,0. De [HO + ] wordt dus 0, / ph 6 6 (H O ),6 0 7 d. n cv 0,50 8,00 e. V wordt,0 7 n 8, f. [ HO ], V 0,. ph = -lo(8,0 0-7 ) = 6, h. ph = 6,8 [HO + ] = 0-6,8 =,6 0-7 /, 8 6, 8 0 0, 5 0 c V c V V 8, 0 0, 5 V 50, 68, 0 Er moet 4,5 water toeevoed worden. Opave 8.5 Salpeterzuur verdunnen UITDAGING 50 m Salpeterzuuroplossin met een ph van,40 wordt met water verdund tot,0. Bereken de ph van de verdunde oplossin. a. HNO (l) + HO (l) HO + (aq) + NO - (aq) b. [HO + ]oud = 0 -ph = 0 -,40 = 0,098 / Aferond op sin. cijfers: [HO + ]oud = 0,040 / 0,040 c V 0,050 c V c V c 0,000 V,0 of c, 0 0 of [H O ], 0 0 nieuw d. ph(nieuw) = -lo([ho + ]) = -lo(,0 0 - ) = -,70 e. [HO + ] =,0 0-7 / = 0, / Dit is te verwaarlozen t.o.v [HO + ] = 0,000 / Opave 8.6 ph van mensel Maak altijd een schets van de situatie. + ph =,0 ph = 5,0 ph =? 00 m 00 m m 4 uitwerkinen hoofdstuk 8 Basischemie 07 Vervoort Boeken
5 a. De ph van dit mensel niet elijk aan 4,0 omdat de [HO + ] omdat 0-4 niet in het midden lit van 0 - en 0-5 b. Het emiddelde van 0,00 en 0,0000 lit dicht bij 0,00 Dus de ph lit tussen,0 en 5,0 en dicht bij,0 [HO + ] = 0 -ph =,0 0 - /. d. n c V, 0 0 0,00, 0 0 e [HO + ] =,0 0-5 /. f.. 6 n c V, 0 0 0,00, 0 0 n n n, 0 0 0, 0 0, 0 0 V V V 0,00 h n,00 [H O ] 5, 050 V 0,00 j ph = -lo ([HO + ]) = -lo(5, ) =,97 Opave 8.7 ph van mensel Volume zuur 75 m ph =, [HO + ] = 0 -, /, n c V 0 0,75,040 Volume zuur 50 m ph =,7 [HO + ] = 0 -,7 /,7 n c V 0 0,50 4,9880 Mensel V V V n n n 6,09 0 [H O ],4 0 0,45 ph lo(, m,04 0 4, ,09 0 ),84 aferond : ph,8 ph = -lo(5,6 0-4 ) =, 5 uitwerkinen hoofdstuk 8 Basischemie 07 Vervoort Boeken
6 Opave 8.8 Zwembadwater Volume water 400 m ph = 8, [HO + ] = 0-8, / 8, n c V , 50 Mensel V V V 400 m ( volume HCl 0) Volume HCl x 0, M [HO + ] = 0, / n c V 0, x n n n (, 50 0, x ) ph 75, [H O ] 0 0 7,5 n c V ,650, 5 0 0, x,650 0, x 0, 0 x 0, Er moet dus 0, liter HCl toeevoed worden. De verwaarlozin van het volume van de HCl was dus terecht! Opave 8.9 Bromide in zeewater 6 uitwerkinen hoofdstuk 8 Basischemie 07 Vervoort Boeken
7 Volume water,0 m =,0 0 ph = 7,0 [HO + ] = 0-7,0 / 7,0 n c V 0,0 0,0 0 Mensel V V Volume HSO4 x, 0 M HSO4 4,0 M HO + bij volledie protolyse [HO + ] = 4,0 / n c V 4,0 x n n V n m (,0 0 ( volume H SO 4,0 x ) 0) ph [H O ] 0,0 0,0 0 n c V,0 0,0,0 0 4,0 x,0 4,0x,0 x 0,5 4 Opave 8.0 poh berekenin a. [OH - ] = 0,007 / poh = -lo [OH - ] = 0,9970 b. poh + ph = 4,00 ph = 4,00 0,9970 =,00 (5 x verdund), [ OH ], / 5 d. nieuwe poh = -lo([oh - ]) = -lo(4, ) =,95 e. nieuwe ph = 4,00,95 =,60 Opave 8. ph berekenin van basische oplossinen Bereken de ph van de volende oplossinen: a. KOH (s) K + (aq) + OH - (aq) poh = -lo([oh - ] = -lo(0,05) =,8 poh + ph =4,00 ph = 4,00,8 =,8 b. NaOH (s) Na + + OH - poh = -lo([oh - ] = -lo(0,8) = 0,89 poh + ph =4,0 ph = 4,00 0,89 =, poh = -lo([oh - ] = -lo(, 0 - ) =,9 poh + ph =4,0 ph = 4,00,9 =,08 d. Ba(OH) (s) Ba + (aq) + OH - (aq) poh = -lo([oh - ] = -lo( 0,0045) =,05 poh + ph =4,00 ph = 4,00,05=,95 7 uitwerkinen hoofdstuk 8 Basischemie 07 Vervoort Boeken
8 Opave 8. [OH ] berekeninen a. ph = 9,80 poh = 4,00 9,80 = 4,0 [OH - ] = 0 -poh = 0-4,0 = 6, 0-5 / b. ph = 9,5 poh = 4,00 9,5 = 4,85 [OH - ] = 0 -poh = 0-4,85 =,4 0-5 / ph = 0,5 poh = 4,00 0,5 =,5 [OH - ] = 0 -poh = 0 -,5 =, 0-4 / Opave 8. Natronloo maken a. m,65 n( NaOH) 0,0665 M 9,997 b. NaOH (s) Na + (aq) + OH - (aq) d. e. n [OH ],0, V 50,0 m m 0,0665 poh lo(, 5) 0, ph 4, 00 ( 0, ) 4, Opave 8.4 Basische oplossin maken a. ph =, poh = 4,00, =,89 [OH - ] = 0 -poh =0 -,89 =,9 0 - / b. NaO (s) + HO Na + + OH - verhoudin aantal NaO : OH - = : Er moet 0,5,9 0 - = 0, opelost worden d. m n M 0,645 0 aferond : m 0,0400 6,9789 0,0998 Opave 8.5 Natronloo maken Je moet 5 liter standaardoplossin maken van 0, M natronloo. Bereken hoeveel natronloo je moet afween en oplossen. n(naoh) c V 0, 5 =0,5 m(naoh) n M 0,5 9,997 =0 Opm: eevens zijn eeven met sinificant cijfer, dus je kunt de massa ook nemen als 40 8 uitwerkinen hoofdstuk 8 Basischemie 07 Vervoort Boeken
9 Opave 8.6 Kalkwater maken a. CaO (s) + HO (l) Ca + + OH - Ca(OH) (s) Ca + (aq) + OH - (aq) b. 0,50 CaO in,0 d. e. m 0,500 n(cao) 8,96 0 M 56,077 n(oh ) 8, ,8 0 m 0,50 0 n(ca(oh) ) 6,748 0 M 74, 09 n(oh ) 6, 748 0,5 0 poh lo([oh ]) - 7,8 0 - n [OH ] 7,8 0 V,0 poh(heleen) lo( 7, 8 0 ), 75 poh lo([ OH [OH ] n V ]),5 0,5 0,0 poh(rick) lo(, ),87 f. Heleen: poh =,75 ph = 4,00,75 =,5 Rick : poh =,87 ph = 4,00,87 =, Opave 8.7 Zuur en base menen a. HO + + OH - HO b. n(h O ) c V 0 n(oh ) c V 0,5 ph 9,5 poh 4,5 0,85,70 0,50 0,790 9 uitwerkinen hoofdstuk 8 Basischemie 07 Vervoort Boeken,5 d. Er is een overmaat HO + e. Er blijft een zure oplossin over. f. Er blijft,70 0,790 0,460 HO n -6 0,46 0 [H O ] =6,7 0 V 0, ph lo([h O ]) lo(6,7 0 ) 5, 7 over
10 Opave 8.8 Zuur en base menen Volume zuur HCl 50 m ph = 4,5 [HO + ] = 0-4,5 / + 5, n(ho ) cv 0 0, 50, 07 0 Volume base NaOH 85 m ph =9,5 poh = 4,5 [OH - ] = 0-4,5 / - 5, n(oh ) cv 0 0,85,7 0 Mensel V V V 75 m overmaat base : n(oh ), 70, 070 0, ,0 [OH ] 0, ,75 poh lo([oh ]) lo( 0, ), 8 ph 4, 0, 8 0, Opave 8.9 Grondonderzoek UITDAGING a. [HO + ] = 0 -ph = 0-4,50 =, 0-5 / b. ph, 50 [H O ] oud 0 0, 6 0 n(ho ) oud 000,6 0,6 0 ph, 00 [H O ] nieuw 0 0, 0 0 n(ho ) nieuw 000, 00,0 0 n n,6 0, 0 0, 6 0 oud nieuw aferond: n(verwijderd) n n, 0 oud nieuw 0 uitwerkinen hoofdstuk 8 Basischemie 07 Vervoort Boeken
11 CaCO (s) + HO + (aq) Ca + (aq) + CO () + HO verhoudin n(caco) : n( HO + ) = : n(caco) = ½, 0 - =, 0 - d. m(caco) = n M =, 0-00, / =, Per m rond moet, CaCO estrooid worden. uitwerkinen hoofdstuk 8 Basischemie 07 Vervoort Boeken
Uitwerkingen Basischemie hoofdstuk 8
 Uitwerkie Basischemie hoofdstuk 8 Opave 8. Opave 8. Zuur of basisch? Va vier oplossie, eummerd A, B, C e D, wordt de ph met ee ph-meter bepaald. Hieroder staa de resultate. Opl. A: ph = 8,5 Opl. B: ph
Uitwerkie Basischemie hoofdstuk 8 Opave 8. Opave 8. Zuur of basisch? Va vier oplossie, eummerd A, B, C e D, wordt de ph met ee ph-meter bepaald. Hieroder staa de resultate. Opl. A: ph = 8,5 Opl. B: ph
Uitwerkingen Basischemie hoofdstuk 9
 Uitwerkinen Basischeie hoofdstuk 9 Opave 9.1 Berekenin directe titratie eevens HCl zuur 20,00 NaOH bein 12,85 eind 6,0 c 0,105 / NaOH (s) Na + (aq) + OH - (aq) b. c(oh ) = 0,105 / =0,105 / c. ( NaOH) eind
Uitwerkinen Basischeie hoofdstuk 9 Opave 9.1 Berekenin directe titratie eevens HCl zuur 20,00 NaOH bein 12,85 eind 6,0 c 0,105 / NaOH (s) Na + (aq) + OH - (aq) b. c(oh ) = 0,105 / =0,105 / c. ( NaOH) eind
Opgaven zuurgraad (ph) berekenen. ph = -log [H + ] poh = -log [OH - ] [H + ] = 10 -ph [OH - ] = 10 -poh. ph = 14 poh poh = 14 ph ph + poh = 14
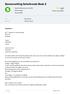
![Opgaven zuurgraad (ph) berekenen. ph = -log [H + ] poh = -log [OH - ] [H + ] = 10 -ph [OH - ] = 10 -poh. ph = 14 poh poh = 14 ph ph + poh = 14 Opgaven zuurgraad (ph) berekenen. ph = -log [H + ] poh = -log [OH - ] [H + ] = 10 -ph [OH - ] = 10 -poh. ph = 14 poh poh = 14 ph ph + poh = 14](/thumbs/82/85039734.jpg) Opgaven zuurgraad (ph) berekenen Met behulp van deze formules dien je berekeningen te kunnen uitvoeren. Deze hoef je niet uit je hoofd te leren, maar je moet ze wel kunnen toepassen. Bij een toets zullen
Opgaven zuurgraad (ph) berekenen Met behulp van deze formules dien je berekeningen te kunnen uitvoeren. Deze hoef je niet uit je hoofd te leren, maar je moet ze wel kunnen toepassen. Bij een toets zullen
Uitwerkingen Basischemie hoofdstuk 6 paragraaf 6.4
 Uitwerkinen Basischeie hoofdstuk 6 pararaaf 6. Opave 6.6 Oplossen Geeven:,00 keukenzout lost op in liter water. b. c,00,00 L,00 L ( NaCl ),99 5,5 58, n,00 58, 0,0 0,0 c 0,0,00 L L d. NaCl (s) Na (aq) Cl
Uitwerkinen Basischeie hoofdstuk 6 pararaaf 6. Opave 6.6 Oplossen Geeven:,00 keukenzout lost op in liter water. b. c,00,00 L,00 L ( NaCl ),99 5,5 58, n,00 58, 0,0 0,0 c 0,0,00 L L d. NaCl (s) Na (aq) Cl
De waterconstante en de ph
 EVENWICHTEN BIJ PROTOLYSEREACTIES De waterconstante en de ph Water is een amfotere stof, dat wil zeggen dat het zowel zure als basische eigenschappen heeft. In zuiver water treedt daarom een reactie van
EVENWICHTEN BIJ PROTOLYSEREACTIES De waterconstante en de ph Water is een amfotere stof, dat wil zeggen dat het zowel zure als basische eigenschappen heeft. In zuiver water treedt daarom een reactie van
Uitwerkingen Basischemie hoofdstuk 6
 Uitwerkinen Basischemie hoofdstuk 6 pave 6. Tellen met verschillende eenheden a. trio s = 33 een half ros = 7 c. Met twee klassen van totaal 66 leerlinen kun je elftallen vormen. d. 5,66667 six pack =
Uitwerkinen Basischemie hoofdstuk 6 pave 6. Tellen met verschillende eenheden a. trio s = 33 een half ros = 7 c. Met twee klassen van totaal 66 leerlinen kun je elftallen vormen. d. 5,66667 six pack =
a) Bereken de molariteit van deze basisoplossing zwavelzuur.
 1.1 Vraen 1.1.1 Zwavelzuur verdunnen Antwoord op p. 4 Een TOA (Technische Onderwijs Assistent) heeft verdund zwavelzuur (H 2 SO 4 ) nodi. Hij/zij heeft de beschikkin over zwavelzuur met een dichtheid van
1.1 Vraen 1.1.1 Zwavelzuur verdunnen Antwoord op p. 4 Een TOA (Technische Onderwijs Assistent) heeft verdund zwavelzuur (H 2 SO 4 ) nodi. Hij/zij heeft de beschikkin over zwavelzuur met een dichtheid van
Hoofdstuk 12 Zuren en basen
 Hoofdstuk 12 Zuren en basen bladzijde 1 Opgave 1 Reactie van de volgende zuren met water: HNO 3 HNO 3 H 2O H 3O NO 3 C 2H 5NH 3 C 2H 5NH 3 H 2O H 3O C 2H 5NH 2 HCN HCN H 2O H 3O CN HClO 4 HClO 4 H 2O H
Hoofdstuk 12 Zuren en basen bladzijde 1 Opgave 1 Reactie van de volgende zuren met water: HNO 3 HNO 3 H 2O H 3O NO 3 C 2H 5NH 3 C 2H 5NH 3 H 2O H 3O C 2H 5NH 2 HCN HCN H 2O H 3O CN HClO 4 HClO 4 H 2O H
Je kunt de ph van een oplossing meten met een ph-meter, met universeelindicatorpapier of met behulp van zuur-base-indicatoren.
 Boekverslag door Merel 797 woorden 22 januari 2017 6.9 14 keer beoordeeld Vak Methode Scheikunde Chemie overal Zie de bijlage voor de grafiek en alle tabellen. H8 Zuren en en Basen Chemie Overal 8.2 De
Boekverslag door Merel 797 woorden 22 januari 2017 6.9 14 keer beoordeeld Vak Methode Scheikunde Chemie overal Zie de bijlage voor de grafiek en alle tabellen. H8 Zuren en en Basen Chemie Overal 8.2 De
vrijdag 15 juni 2012 15:26:05 Midden-Europese zomertijd H6 Zuren en basen 4havo voorjaar 2012
 H6 Zuren en basen 4havo voorjaar 2012 Toetsing in periode 4! 6 juni! DTM-T zuur/base t/m 6.6! Tabel 6.10,6.13,6.17 en ph-berekeningen (zoals in vragen 14,15,26 en 27)! Toetsweek einde periode! TW441 H1
H6 Zuren en basen 4havo voorjaar 2012 Toetsing in periode 4! 6 juni! DTM-T zuur/base t/m 6.6! Tabel 6.10,6.13,6.17 en ph-berekeningen (zoals in vragen 14,15,26 en 27)! Toetsweek einde periode! TW441 H1
6 VWO SK Extra (reken)opgaven Buffers.
 6 VWO SK Extra (reken)opgaven Buffers. Opgave I. 1 Je wilt een buffermengsel maken met ph = 4,20. Welke stoffen kun je het beste als uitgangsstoffen nemen? Opgave II. 2 In 1,00 liter water is opgelost
6 VWO SK Extra (reken)opgaven Buffers. Opgave I. 1 Je wilt een buffermengsel maken met ph = 4,20. Welke stoffen kun je het beste als uitgangsstoffen nemen? Opgave II. 2 In 1,00 liter water is opgelost
5.4 ph van oplossingen van zwakke zuren of zwakke basen
 Opmerking: We gaan ervan uit, dat bij het mengen van oplossingen geen volumecontractie optreedt. Bij verdunde oplossingen is die veronderstelling gerechtvaardigd. 5.4 ph van oplossingen van zwakke zuren
Opmerking: We gaan ervan uit, dat bij het mengen van oplossingen geen volumecontractie optreedt. Bij verdunde oplossingen is die veronderstelling gerechtvaardigd. 5.4 ph van oplossingen van zwakke zuren
Samenvatting Scheikunde Hoofdstuk 9, 10, 11 Zuren/Basen, Evenwichtsconstanten
 Samenvatting Scheikunde Hoofdstuk 9, 10, 11 Zuren/Basen, Evenwichtsconstanten Samenvatting door een scholier 1087 woorden 22 januari 2009 6 42 keer beoordeeld Vak Methode Scheikunde Pulsar chemie Scheikunde
Samenvatting Scheikunde Hoofdstuk 9, 10, 11 Zuren/Basen, Evenwichtsconstanten Samenvatting door een scholier 1087 woorden 22 januari 2009 6 42 keer beoordeeld Vak Methode Scheikunde Pulsar chemie Scheikunde
5 VWO. H8 zuren en basen
 5 VWO H8 zuren en basen Inleiding Opdracht 1, 20 min in tweetallen Nakijken; eventueel vragen stellen 8.2 Zure, neutrale en basische oplossingen 8.2 Zure, neutrale en Indicator (tabel 52A) Zuurgraad 0-14?
5 VWO H8 zuren en basen Inleiding Opdracht 1, 20 min in tweetallen Nakijken; eventueel vragen stellen 8.2 Zure, neutrale en basische oplossingen 8.2 Zure, neutrale en Indicator (tabel 52A) Zuurgraad 0-14?
Hoofdstuk 3: Zuren en basen
 Hoofdstuk 3: Zuren en basen Scheikunde VWO 2011/2012 www.lyceo.nl Onderwerpen Scheikunde 2011 2012 Stoffen, structuur en binding Kenmerken van Reacties Zuren en base Redox Chemische technieken Koolstofchemie
Hoofdstuk 3: Zuren en basen Scheikunde VWO 2011/2012 www.lyceo.nl Onderwerpen Scheikunde 2011 2012 Stoffen, structuur en binding Kenmerken van Reacties Zuren en base Redox Chemische technieken Koolstofchemie
PbSO 4(s) d NH 4Cl + KOH KCl + H 2O + NH 3(g) NH 4. + OH - NH 3(g) + H 2O e 2 NaOH + CuCl 2 Cu(OH) 2(s) + 2 NaCl
 Hoofdstuk 11 Chemische reacties bladzijde 1 Opgave 1 De ionen die in water ontstaan: a NaCl Na Cl - b AgNO 3 Ag - NO 3 c (NH 4) 2SO 4 2 NH 4 SO 4 d KOH K OH - e NiSO 4 Ni 2 SO 4 Opgave 2 Schrijf de volgende
Hoofdstuk 11 Chemische reacties bladzijde 1 Opgave 1 De ionen die in water ontstaan: a NaCl Na Cl - b AgNO 3 Ag - NO 3 c (NH 4) 2SO 4 2 NH 4 SO 4 d KOH K OH - e NiSO 4 Ni 2 SO 4 Opgave 2 Schrijf de volgende
5 Water, het begrip ph
 5 Water, het begrip ph 5.1 Water Waterstofchloride is een sterk zuur, het reageert als volgt met water: HCI(g) + H 2 0(I) Cl (aq) + H 3 O + (aq) z b Hierbij reageert water als base. Ammoniak is een zwakke
5 Water, het begrip ph 5.1 Water Waterstofchloride is een sterk zuur, het reageert als volgt met water: HCI(g) + H 2 0(I) Cl (aq) + H 3 O + (aq) z b Hierbij reageert water als base. Ammoniak is een zwakke
ßCalciumChloride oplossing
 Samenvatting door R. 1673 woorden 17 februari 2013 8 1 keer beoordeeld Vak Methode Scheikunde Pulsar chemie Additiereactie Bij een reactie tussen hexeen en broom springt de C=C binding open. Aan het molecuul
Samenvatting door R. 1673 woorden 17 februari 2013 8 1 keer beoordeeld Vak Methode Scheikunde Pulsar chemie Additiereactie Bij een reactie tussen hexeen en broom springt de C=C binding open. Aan het molecuul
Oefenopgaven ZUREN en BASEN havo
 Oefenopgaven ZUREN en BASEN havo OPGAVE 1 Men lost de volgende zouten op in water: (i) ammoniumnitraat (ii) kaliumsulfide (iii) natriumwaterstofsulfaat 01 Geef voor elk van deze zouten de oplosvergelijking.
Oefenopgaven ZUREN en BASEN havo OPGAVE 1 Men lost de volgende zouten op in water: (i) ammoniumnitraat (ii) kaliumsulfide (iii) natriumwaterstofsulfaat 01 Geef voor elk van deze zouten de oplosvergelijking.
Uitwerkingen Basischemie hoofdstuk 6
 Uitwerkinen Basischeie hoofdstuk 6 pave 6. Tellen et verschillende eenheden trio s = b. een half ros = 7 c. Met twee klassen van totaal 66 leerlinen kun je 66/ = 6 elftallen voren. d. 5,66667 six pack
Uitwerkinen Basischeie hoofdstuk 6 pave 6. Tellen et verschillende eenheden trio s = b. een half ros = 7 c. Met twee klassen van totaal 66 leerlinen kun je 66/ = 6 elftallen voren. d. 5,66667 six pack
OEFENTOETS Zuren en basen 5 VWO
 OEFENTOETS Zuren en basen 5 VWO Gesloten vragen 1. Carolien wil de zuurgraad van een oplossing onderzoeken met twee verschillende zuur-baseindicatoren en neemt hierbij het volgende waar: I de oplossing
OEFENTOETS Zuren en basen 5 VWO Gesloten vragen 1. Carolien wil de zuurgraad van een oplossing onderzoeken met twee verschillende zuur-baseindicatoren en neemt hierbij het volgende waar: I de oplossing
ANTWOORDEN Herhaling zuren, basen en buffers
 ANTWOORDEN Herhaling zuren, basen en buffers 1) Wat geeft de onderstaande afbeelding weer? Je ziet deze deeltjes afgebeeld: het zwakke zuur HA (want veel deeltjes zijn niet geïoniseerd), de zwakke base
ANTWOORDEN Herhaling zuren, basen en buffers 1) Wat geeft de onderstaande afbeelding weer? Je ziet deze deeltjes afgebeeld: het zwakke zuur HA (want veel deeltjes zijn niet geïoniseerd), de zwakke base
Oefenopgaven ZUREN en BASEN vwo
 Oefenopgaven ZUREN en BASEN vwo OPGAVE 1 Men lost de volgende zouten op in water: (i) ammoniumnitraat (ii) kaliumsulfide (iii) natriumwaterstofsulfaat 01 Geef voor elk van deze zouten de oplosvergelijking.
Oefenopgaven ZUREN en BASEN vwo OPGAVE 1 Men lost de volgende zouten op in water: (i) ammoniumnitraat (ii) kaliumsulfide (iii) natriumwaterstofsulfaat 01 Geef voor elk van deze zouten de oplosvergelijking.
Hoofdstuk 6: Zure en base oplossingen / ph
 Hoofdstuk 6: Zure en base oplossingen / ph 6.1 Herhaling: zure en basische oplossingen Arrhenius definieerde zuren als volgt: zuren zijn polaire covalente verbindingen die bij het oplossen in water H +
Hoofdstuk 6: Zure en base oplossingen / ph 6.1 Herhaling: zure en basische oplossingen Arrhenius definieerde zuren als volgt: zuren zijn polaire covalente verbindingen die bij het oplossen in water H +
Oefenvraagstukken 5 VWO Hoofdstuk 11. Opgave 1 [HCO ] [H O ] x x. = 4,5 10 [CO ] 1,00 x 10
![Oefenvraagstukken 5 VWO Hoofdstuk 11. Opgave 1 [HCO ] [H O ] x x. = 4,5 10 [CO ] 1,00 x 10 Oefenvraagstukken 5 VWO Hoofdstuk 11. Opgave 1 [HCO ] [H O ] x x. = 4,5 10 [CO ] 1,00 x 10](/thumbs/19/200750.jpg) Oefenvraagstukken 5 VWO Hoofdstuk 11 Zuren en basen Opgave 1 1 Ga na of de volgende zuren en basen met elkaar kunnen reageren. Zo ja, geef de reactievergelijking. Zo nee, leg duidelijk uit waarom niet.
Oefenvraagstukken 5 VWO Hoofdstuk 11 Zuren en basen Opgave 1 1 Ga na of de volgende zuren en basen met elkaar kunnen reageren. Zo ja, geef de reactievergelijking. Zo nee, leg duidelijk uit waarom niet.
ZUREN EN BASEN. Samenvatting voor het HAVO. versie mei 2013
 ZUREN EN BASEN Samenvatting voor het HAVO versie mei 2013 INHOUDSOPGAVE 1. Vooraf 2. Algemeen 3. Zuren 4. Basen 5. Het waterevenwicht 6. Definities ph en poh 7. ph BEREKENINGEN 7.1. Algemeen 7.2. Water
ZUREN EN BASEN Samenvatting voor het HAVO versie mei 2013 INHOUDSOPGAVE 1. Vooraf 2. Algemeen 3. Zuren 4. Basen 5. Het waterevenwicht 6. Definities ph en poh 7. ph BEREKENINGEN 7.1. Algemeen 7.2. Water
H4SK-H7. Willem de Zwijgerteam. CC Naamsvermelding-GelijkDelen 3.0 Nederland licentie. https://maken.wikiwijs.nl/67689
 Auteur Laatst gewijzigd Licentie Webadres Willem de Zwijgerteam 28 juli 2016 CC Naamsvermelding-GelijkDelen 3.0 Nederland licentie https://maken.wikiwijs.nl/67689 Dit lesmateriaal is gemaakt met Wikiwijs
Auteur Laatst gewijzigd Licentie Webadres Willem de Zwijgerteam 28 juli 2016 CC Naamsvermelding-GelijkDelen 3.0 Nederland licentie https://maken.wikiwijs.nl/67689 Dit lesmateriaal is gemaakt met Wikiwijs
Uitwerkingen Basischemie hoofdstuk 2
 Uitwerkingen Basischemie hoofdstuk 2 Opgave 2.1 Opgave 2.2 Elementen leren Maak met de afbeeldingen 2.1A en 2.1B kaartjes met aan de ene kant de naam van het element en aan de andere kant het symbool en
Uitwerkingen Basischemie hoofdstuk 2 Opgave 2.1 Opgave 2.2 Elementen leren Maak met de afbeeldingen 2.1A en 2.1B kaartjes met aan de ene kant de naam van het element en aan de andere kant het symbool en
OEFENOPGAVEN VWO6sk1 TENTAMEN H1-11
 OEFENOPGAVEN VWO6sk1 TENTAMEN H1-11 06-07, HU, oktober 2006 1. POLARITEIT, WATERSTOFBRUGGEN Zie het apart uitgedeelde stencil voor extra theorie (is tentamenstof!) en een oefenopgave. 2. CHEMISCH REKENEN
OEFENOPGAVEN VWO6sk1 TENTAMEN H1-11 06-07, HU, oktober 2006 1. POLARITEIT, WATERSTOFBRUGGEN Zie het apart uitgedeelde stencil voor extra theorie (is tentamenstof!) en een oefenopgave. 2. CHEMISCH REKENEN
Uitwerkingen van de opgaven uit: BASISCHEMIE voor het MLO ISBN 9789077423875, 3 e druk, Uitgeverij Syntax Media Hoofdstuk 10 Concentratie bladzijde 1
 Hoofdstuk 10 Concentratie bladzijde 1 Opgave 1 rekenformule: c(b) = ------- toepassen: n B V opl. Bereken de analytische concentratie (mol/l) in elk van de volgende oplossingen: a 5,00 mol NaCl in 5,00
Hoofdstuk 10 Concentratie bladzijde 1 Opgave 1 rekenformule: c(b) = ------- toepassen: n B V opl. Bereken de analytische concentratie (mol/l) in elk van de volgende oplossingen: a 5,00 mol NaCl in 5,00
Zuren en basen. Inhoud
 Zuren en n Je kunt bij een onderwerp komen door op de gewenste rubriek in de inhoud te klikken. Wil je vanuit een rubriek terug naar de inhoud, klik dan op de tekst van de rubriek waar je bent. Gewoon
Zuren en n Je kunt bij een onderwerp komen door op de gewenste rubriek in de inhoud te klikken. Wil je vanuit een rubriek terug naar de inhoud, klik dan op de tekst van de rubriek waar je bent. Gewoon
Chemisch rekenen, zo doe je dat!
 1 Chemisch rekenen, zo doe je dat! GOE Opmerkingen vooraf: 1. Belangrijke schrijfwijzen: 100 = 10 2 ; 1000 = 10 3, enz. 0,1 = 1/10 = 10-1 ; 0,001 = 1/1000 = 10-3 ; 0,000.000.1 = 10-7, enz. gram/kg = gram
1 Chemisch rekenen, zo doe je dat! GOE Opmerkingen vooraf: 1. Belangrijke schrijfwijzen: 100 = 10 2 ; 1000 = 10 3, enz. 0,1 = 1/10 = 10-1 ; 0,001 = 1/1000 = 10-3 ; 0,000.000.1 = 10-7, enz. gram/kg = gram
Hoofdstuk 6. Zuren en basen. Chemie 5 (2u)
 Hoofdstuk 6 Zuren en basen Chemie 5 (2u) Deze slides voor de lesbegeleiding worden ter beschikking gesteld, maar ze zijn te beperkt om als samenvatting van de cursus te kunnen dienen. Dissociatie van ionverbindingen
Hoofdstuk 6 Zuren en basen Chemie 5 (2u) Deze slides voor de lesbegeleiding worden ter beschikking gesteld, maar ze zijn te beperkt om als samenvatting van de cursus te kunnen dienen. Dissociatie van ionverbindingen
OEFENOPGAVEN VWO ZUREN EN BASEN + ph-berekeningen
 OEFENOPGAVEN VWO ZUREN EN BASEN + ph-berekeningen OPGAVE 1 01 Bereken hoeveel mmol HCOOH is opgelost in 40 ml HCOOH oplossing met ph = 3,60. 02 Bereken ph van 0,300 M NaF oplossing. 03 Bereken hoeveel
OEFENOPGAVEN VWO ZUREN EN BASEN + ph-berekeningen OPGAVE 1 01 Bereken hoeveel mmol HCOOH is opgelost in 40 ml HCOOH oplossing met ph = 3,60. 02 Bereken ph van 0,300 M NaF oplossing. 03 Bereken hoeveel
Hoofdstuk 6. De ph/zuurgraad is een getal waarin de hoeveelheid zuur of base wordt uitgedrukt. Dit getal ligt meestal tussen de 0 en 14.
 Samenvatting door W. 879 woorden 15 oktober 2012 5,8 52 keer beoordeeld Vak Methode Scheikunde Chemie overal Hoofdstuk 6 2 De PH van een oplossing De ph/zuurgraad is een getal waarin de hoeveelheid zuur
Samenvatting door W. 879 woorden 15 oktober 2012 5,8 52 keer beoordeeld Vak Methode Scheikunde Chemie overal Hoofdstuk 6 2 De PH van een oplossing De ph/zuurgraad is een getal waarin de hoeveelheid zuur
Weet je het nog? Welke bewerking moet in afbeelding 21.1 langs elke pijl staan?
 Hoofdstuk 21 Chemisch rekenen (4) bladzijde 1 Opgave 1 Weet je het nog? Welke bewerking moet in afbeelding 21.1 langs elke pijl staan? Opgave 2 We lossen op: 25,0 g NaCl in een maatkolf tot 100 ml. De
Hoofdstuk 21 Chemisch rekenen (4) bladzijde 1 Opgave 1 Weet je het nog? Welke bewerking moet in afbeelding 21.1 langs elke pijl staan? Opgave 2 We lossen op: 25,0 g NaCl in een maatkolf tot 100 ml. De
Zelfs zuiver water geleidt in zeer kleine mate elektrische stroom en dus wijst dit op de aanwezigheid van geladen deeltjes.
 Cursus Chemie 4-1 Hoofdstuk 4: CHEMISCH EVENWICHT 1. DE STERKTE VAN ZUREN EN BASEN Als HCl in water opgelost wordt dan bekomen we een oplossing die bijna geen enkele covalente HCl meer bevat. In de reactievergelijking
Cursus Chemie 4-1 Hoofdstuk 4: CHEMISCH EVENWICHT 1. DE STERKTE VAN ZUREN EN BASEN Als HCl in water opgelost wordt dan bekomen we een oplossing die bijna geen enkele covalente HCl meer bevat. In de reactievergelijking
Hoofdstuk 3: Water, zuren en basen
 Hoofdstuk 3: Water, zuren en basen NaSk II Vmbo 2011/2012 www.lyceo.nl Hoofdstuk 3: Water, zuren en basen NaSk II 1. Bouw van materie 2. Verbranding 3. Water, zuren en basen 4. Basis chemie voor beroep
Hoofdstuk 3: Water, zuren en basen NaSk II Vmbo 2011/2012 www.lyceo.nl Hoofdstuk 3: Water, zuren en basen NaSk II 1. Bouw van materie 2. Verbranding 3. Water, zuren en basen 4. Basis chemie voor beroep
Uitwerkingen van de opgaven uit: CHEMISCHE ANALYSE ISBN , 1 e druk, Uitgeverij Syntax Media Hoofdstuk 3 Acidimetrie bladzijde 1
 Hoofdstuk 3 Acidimetrie bladzijde 1 Opgave 1 a We titreren HCl met NaOH. Welke van de boven gegeven indicatoren kunnen we gebruiken? Elke genoemde indicator, de phverandering gaat ongeveer van ph = 3 tot
Hoofdstuk 3 Acidimetrie bladzijde 1 Opgave 1 a We titreren HCl met NaOH. Welke van de boven gegeven indicatoren kunnen we gebruiken? Elke genoemde indicator, de phverandering gaat ongeveer van ph = 3 tot
Basisscheikunde voor het hbo ISBN e druk Uitgeverij Syntax media
 Hoofstuk 8 Zuren en basen blazije 1 Opgave 1 Reactie van e volgene zuren met water: a HNO 3 HNO 3 + H 2O H 3O + + NO 3 b C 2H 5NH + 3 C 2H 5NH + 3 + H 2O H 3O + + C 2H 5NH 2 c HCN HCN + H 2O H 3O + + CN
Hoofstuk 8 Zuren en basen blazije 1 Opgave 1 Reactie van e volgene zuren met water: a HNO 3 HNO 3 + H 2O H 3O + + NO 3 b C 2H 5NH + 3 C 2H 5NH + 3 + H 2O H 3O + + C 2H 5NH 2 c HCN HCN + H 2O H 3O + + CN
10.2. Kwantitatieve aspecten van zuurbase-reacties
 10.2. Kwantitatieve aspecten van zuurbase-reacties 1. ph-berekeningen van oplossingen van zuren en basen De zuurgraad ph = weergave van de zuurgraad van een oplossing ( zuurconcentratie) ph = - log a(h
10.2. Kwantitatieve aspecten van zuurbase-reacties 1. ph-berekeningen van oplossingen van zuren en basen De zuurgraad ph = weergave van de zuurgraad van een oplossing ( zuurconcentratie) ph = - log a(h
Chemie (ph) bij het inkuilen Scheikunde klas V41a en V41b door Erik Held
 Chemie (ph) bij het inkuilen Scheikunde klas V41a en V41b door Erik Held Inkuilproces Proces bij het inkuilen: In de kuil ondergaat het gewas een biochemisch proces onder invloed van micro-organismen Een
Chemie (ph) bij het inkuilen Scheikunde klas V41a en V41b door Erik Held Inkuilproces Proces bij het inkuilen: In de kuil ondergaat het gewas een biochemisch proces onder invloed van micro-organismen Een
Wennen aan het idee dat je de eenheden eerst aanpast aan de nieuwe grootheid. Hier: eerst omrekenen naar gram en liter.
 Hoofdstuk 4 Massaconcentratie bladzijde 1 Opgave 1 Wennen aan het idee dat je de eenheden eerst aanpast aan de nieuwe grootheid. Hier: eerst omrekenen naar gram en liter. a 25,0 mg ethanol in 100 ml 0,025
Hoofdstuk 4 Massaconcentratie bladzijde 1 Opgave 1 Wennen aan het idee dat je de eenheden eerst aanpast aan de nieuwe grootheid. Hier: eerst omrekenen naar gram en liter. a 25,0 mg ethanol in 100 ml 0,025
Basisscheikunde voor het hbo ISBN e druk Uitgeverij Syntax media
 Hoofdstuk 5 Chemische reacties bladzijde 1 Opgave 1 Maak de volgende reactievergelijkingen kloppend: a C 3H 8O 2 4 O 2 3 CO 2 4 H 2O b P 4 5 O 2 6 H 2O 4 H 3PO 4 c 4 Al 3 O 2 2 Al 2O 3 d 2 Fe 3 Cl 2 2
Hoofdstuk 5 Chemische reacties bladzijde 1 Opgave 1 Maak de volgende reactievergelijkingen kloppend: a C 3H 8O 2 4 O 2 3 CO 2 4 H 2O b P 4 5 O 2 6 H 2O 4 H 3PO 4 c 4 Al 3 O 2 2 Al 2O 3 d 2 Fe 3 Cl 2 2
Scheikunde hoofdstuk 8 en 9 VWO 5 SE 2 Hoofdstuk 8
 Scheikunde hoofdstuk 8 en 9 VWO 5 SE 2 Hoofdstuk 8 2 Een oplossing kan zuur, basisch of neutraal zijn. Om het verschil in zuurgraad in een getal te kunnen uitdrukken gebruik je de ph. Is de ph < 7 is de
Scheikunde hoofdstuk 8 en 9 VWO 5 SE 2 Hoofdstuk 8 2 Een oplossing kan zuur, basisch of neutraal zijn. Om het verschil in zuurgraad in een getal te kunnen uitdrukken gebruik je de ph. Is de ph < 7 is de
EVENWICHTEN VOOR ZUREN EN BASEN
 EVENWICHTEN VOOR ZUREN EN BASEN Een zuur is een chemisch bestanddeel dat waterstofionen afsplitst bij oplossen in water H zuurrest water H zuurrest Een base is een chemisch bestanddeel dat hydroxide-ionen
EVENWICHTEN VOOR ZUREN EN BASEN Een zuur is een chemisch bestanddeel dat waterstofionen afsplitst bij oplossen in water H zuurrest water H zuurrest Een base is een chemisch bestanddeel dat hydroxide-ionen
Opgave 1. Opgave 2. b En bij een verbruik van 10 ml? Dan wordt de procentuele onnauwkeurigheid 2 x zo groot: 0,03 / 20 x 100% = 0,3% Opgave 3
 Hoofdstuk 13 Titratieberekeningen bladzijde 1 Opgave 1 Wat is het theoretisch eindpunt? Het theoretisch eindpunt is het titratievolume waarbij de bedoelde reactie precies is afgelopen. En wat is dan het
Hoofdstuk 13 Titratieberekeningen bladzijde 1 Opgave 1 Wat is het theoretisch eindpunt? Het theoretisch eindpunt is het titratievolume waarbij de bedoelde reactie precies is afgelopen. En wat is dan het
ZUREN EN BASEN. Samenvatting voor het VWO. versie mei 2013
 ZUREN EN BASEN Samenvatting voor het VWO versie mei 2013 INHOUDSOPGAVE 1. Vooraf 2. Algemeen 3. Zuren 4. Basen 5. Het waterevenwicht 6. Definities ph en poh 7. ph BEREKENINGEN 7.1. Algemeen 7.2. Water
ZUREN EN BASEN Samenvatting voor het VWO versie mei 2013 INHOUDSOPGAVE 1. Vooraf 2. Algemeen 3. Zuren 4. Basen 5. Het waterevenwicht 6. Definities ph en poh 7. ph BEREKENINGEN 7.1. Algemeen 7.2. Water
Oplossingen oefeningenreeks 1
 Oplossingen oefeningenreeks 1 4. Door diffractie van X-stralen in natriumchloride-kristallen stelt men vast dat de eenheidscel van dit zout een kubus is waarvan de ribbe een lengte heeft van 5.64 10-10
Oplossingen oefeningenreeks 1 4. Door diffractie van X-stralen in natriumchloride-kristallen stelt men vast dat de eenheidscel van dit zout een kubus is waarvan de ribbe een lengte heeft van 5.64 10-10
Wat is de verhouding tussen de aantallen atomen van de elementen Mg, P en O in magnesiumfosfaat?
 Chemie Vraag 1 Wat is de verhouding tussen de aantallen atomen van de elementen Mg, P en O in magnesiumfosfaat? 1 : 1 : 4 2 : 1 : 4 2 : 3 : 12 3 : 2 : 8 Chemie: vraag 1 Chemie Vraag 2 Welke
Chemie Vraag 1 Wat is de verhouding tussen de aantallen atomen van de elementen Mg, P en O in magnesiumfosfaat? 1 : 1 : 4 2 : 1 : 4 2 : 3 : 12 3 : 2 : 8 Chemie: vraag 1 Chemie Vraag 2 Welke
Wat is de verhouding tussen de aantallen atomen van de elementen Mg, P en O in magnesiumfosfaat?
 Chemie Vraag 1 Wat is de verhouding tussen de aantallen atomen van de elementen Mg, P en O in magnesiumfosfaat? 3 : 2 : 8 2 : 3 : 12 2 : 1 : 4 1 : 1 : 4 Chemie: vraag 1 Chemie Vraag 2 Welke
Chemie Vraag 1 Wat is de verhouding tussen de aantallen atomen van de elementen Mg, P en O in magnesiumfosfaat? 3 : 2 : 8 2 : 3 : 12 2 : 1 : 4 1 : 1 : 4 Chemie: vraag 1 Chemie Vraag 2 Welke
V5SK-H9. Willem de Zwijgerteam. CC Naamsvermelding-GelijkDelen 3.0 Nederland licentie.
 Auteur Laatst gewijzigd Licentie Webadres Willem de Zwijgerteam 27 October 2016 CC Naamsvermelding-GelijkDelen 3.0 Nederland licentie http://maken.wikiwijs.nl/81457 Dit lesmateriaal is gemaakt met Wikiwijs
Auteur Laatst gewijzigd Licentie Webadres Willem de Zwijgerteam 27 October 2016 CC Naamsvermelding-GelijkDelen 3.0 Nederland licentie http://maken.wikiwijs.nl/81457 Dit lesmateriaal is gemaakt met Wikiwijs
4 Mathematiseren. Uitwerkingen hoofdstuk 4 versie Verdunnen van een zoutoplossing. Tip: Maak eerst een schets van de gegevens.
 Uitwerkinen hoofdstuk versie 0 Mthetiseren. Opve. Verdunnen vn een zoutoplossin. ip: Mk eerst een shets vn de eevens. V b V 0, 0, 0,667 0,5 hoeveelheid zout blijft hetzelfde 0,50, 0,5 Opdrht. V 0 V 0,
Uitwerkinen hoofdstuk versie 0 Mthetiseren. Opve. Verdunnen vn een zoutoplossin. ip: Mk eerst een shets vn de eevens. V b V 0, 0, 0,667 0,5 hoeveelheid zout blijft hetzelfde 0,50, 0,5 Opdrht. V 0 V 0,
Module 4 Zuren en Basen Antwoorden
 1 ph en indicatoren Opmerking: informatie over zuurbase indicatoren vind je in tabel 52A. 1 Een H + ion is eigenlijk gewoon een proton (zonder elektronenwolk). 2 Er moet een elektron worden verwijderd.
1 ph en indicatoren Opmerking: informatie over zuurbase indicatoren vind je in tabel 52A. 1 Een H + ion is eigenlijk gewoon een proton (zonder elektronenwolk). 2 Er moet een elektron worden verwijderd.
Scheikundige berekeningen rond bereidingen
 Scheikundige berekeningen rond bereidingen 1 Introductie Bereidingsvoorschriften zijn zo opgesteld dat er in het product precies de juiste hoeveelheden stoffen aanwezig zijn. Maar wat te doen als je niet
Scheikundige berekeningen rond bereidingen 1 Introductie Bereidingsvoorschriften zijn zo opgesteld dat er in het product precies de juiste hoeveelheden stoffen aanwezig zijn. Maar wat te doen als je niet
2 H 2 O(vl) H 3 O + (aq) + OH - (aq) Deze evenwichtsreactie wordt meestal eenvoudiger als volgt geschreven:
 Zuren en basen 1. Autoionisatie van water Op het eerste gezicht geleidt water de elektrische stroom niet. Bij gebruik van meer gevoelige meetapparatuur blijkt water toch de elektrische stroom te geleiden,
Zuren en basen 1. Autoionisatie van water Op het eerste gezicht geleidt water de elektrische stroom niet. Bij gebruik van meer gevoelige meetapparatuur blijkt water toch de elektrische stroom te geleiden,
Uitwerkingen Uitwerkingen 4.3.4
 Uitwerkingen 4.3.1 1 1,5 12 = 18 eieren 2 3,25 144 = 468 figuurzaagjes 3 25 24 = 600 bierflesjes 4 3,75 20.000 = 75.000 korrels hagelslag 5 2,25 10.000.000 = 22.500.000 zoutkorrels 6 1,5 6 10 23 = 9 10
Uitwerkingen 4.3.1 1 1,5 12 = 18 eieren 2 3,25 144 = 468 figuurzaagjes 3 25 24 = 600 bierflesjes 4 3,75 20.000 = 75.000 korrels hagelslag 5 2,25 10.000.000 = 22.500.000 zoutkorrels 6 1,5 6 10 23 = 9 10
Scheikunde SE2. Hoofdstuk 8
 Scheikunde SE2 Hoofdstuk 8 Paragraaf 2 Indicatoren: stoffen waarmee je kunt bepalen of een oplossing zuur of basisch is. Zuur: als een oplossing een ph heeft van minder dan 7. Basisch: als een oplossing
Scheikunde SE2 Hoofdstuk 8 Paragraaf 2 Indicatoren: stoffen waarmee je kunt bepalen of een oplossing zuur of basisch is. Zuur: als een oplossing een ph heeft van minder dan 7. Basisch: als een oplossing
BUFFEROPLOSSINGEN. Inleiding
 BUFFEROPLOSSINGEN Inleiding Zowel in de analytische chemie als in de biochemie is het van belang de ph van een oplossing te regelen. Denk bijvoorbeeld aan een complexometrische titratie met behulp van
BUFFEROPLOSSINGEN Inleiding Zowel in de analytische chemie als in de biochemie is het van belang de ph van een oplossing te regelen. Denk bijvoorbeeld aan een complexometrische titratie met behulp van
Opgave 1. n = m / M. e 500 mg soda (Na 2CO 3) = 0,00472 mol. Opgave 2. m = n x M
 Hoofdstuk 8 Rekenen met de mol bladzijde 1 Opgave 1 n = m / M a 64,0 g zuurstofgas (O 2) = 2,00 mol (want n = 64,0 / 32,0) enz b 10,0 g butaan (C 4H 10) = 0,172 mol c 1,00 g suiker (C 12H 22O 11) = 0,00292
Hoofdstuk 8 Rekenen met de mol bladzijde 1 Opgave 1 n = m / M a 64,0 g zuurstofgas (O 2) = 2,00 mol (want n = 64,0 / 32,0) enz b 10,0 g butaan (C 4H 10) = 0,172 mol c 1,00 g suiker (C 12H 22O 11) = 0,00292
UITWERKING CCVS-TENTAMEN 26 mei 2015
 UITWERKING CCVS-TENTAMEN 26 mei 2015 Frank Povel NB. Deze uitwerking is door mij gemaakt en is niet de uitwerking die de CCVS hanteert. Er kunnen dan ook op geen enkele wijze rechten aan deze uitwerking
UITWERKING CCVS-TENTAMEN 26 mei 2015 Frank Povel NB. Deze uitwerking is door mij gemaakt en is niet de uitwerking die de CCVS hanteert. Er kunnen dan ook op geen enkele wijze rechten aan deze uitwerking
UITWERKING CCVS-TENTAMEN 18 april 2017
 UITWERKING CCVSTENTAMEN 18 april 2017 Frank Povel NB. Deze uitwerking is door mij gemaakt en is niet de uitwerking die de CCVS hanteert. Er kunnen dan ook op geen enkele wijze rechten aan deze uitwerking
UITWERKING CCVSTENTAMEN 18 april 2017 Frank Povel NB. Deze uitwerking is door mij gemaakt en is niet de uitwerking die de CCVS hanteert. Er kunnen dan ook op geen enkele wijze rechten aan deze uitwerking
Wat is de formule van het metaalchloride waarin M het symbool van het metaal voorstelt?
 Chemie Vraag 1 5,0.10-4 mol van een metaalchloride wordt opgelost in water. Er is 60 ml van een 2,5.10-2 mol.l -1 zilvernitraatoplossing nodig om alle chlorideionen neer te slaan onder de vorm van zilverchloride.
Chemie Vraag 1 5,0.10-4 mol van een metaalchloride wordt opgelost in water. Er is 60 ml van een 2,5.10-2 mol.l -1 zilvernitraatoplossing nodig om alle chlorideionen neer te slaan onder de vorm van zilverchloride.
Wat is de formule van het metaalchloride waarin M het symbool van het metaal voorstelt?
 Chemie Vraag 1 5,0.10-4 mol van een metaalchloride wordt opgelost in water. Er is 60 ml van een 2,5.10-2 mol.l -1 zilvernitraatoplossing nodig om alle chlorideionen neer te slaan onder de vorm van zilverchloride.
Chemie Vraag 1 5,0.10-4 mol van een metaalchloride wordt opgelost in water. Er is 60 ml van een 2,5.10-2 mol.l -1 zilvernitraatoplossing nodig om alle chlorideionen neer te slaan onder de vorm van zilverchloride.
Uitwerkingen van de opgaven uit: BASISCHEMIE voor het MLO ISBN , 3 e druk, Uitgeverij Syntax Media Hoofdstuk 14 Zouten bladzijde 1
 BASISCHEMIE het MLO ISBN 9789077423875, 3 e druk, Uitgeverij Syntax Media Hoofdstuk 14 Zouten bladzijde 1 Opgave 1 Van onderstaande zouten worden steeds waterige oplossingen samengevoegd. Welk slecht oplosbare
BASISCHEMIE het MLO ISBN 9789077423875, 3 e druk, Uitgeverij Syntax Media Hoofdstuk 14 Zouten bladzijde 1 Opgave 1 Van onderstaande zouten worden steeds waterige oplossingen samengevoegd. Welk slecht oplosbare
Module 2 Chemische berekeningen Antwoorden
 2 Meten is weten 1 Nee, want bijvoorbeeld 0,0010 kg is net zo nauwkeurig als 1,0 gram. 2 De minst betrouwbare meting is de volumemeting. Deze variabele bepaald het aantal significante cijfers. 3 IJs: 1,5
2 Meten is weten 1 Nee, want bijvoorbeeld 0,0010 kg is net zo nauwkeurig als 1,0 gram. 2 De minst betrouwbare meting is de volumemeting. Deze variabele bepaald het aantal significante cijfers. 3 IJs: 1,5
25/02/2017. [H 2 S] = K b,2 [OH ] = 1,
![25/02/2017. [H 2 S] = K b,2 [OH ] = 1, 25/02/2017. [H 2 S] = K b,2 [OH ] = 1,](/thumbs/67/57105853.jpg) 25/02/207 Meerstapshydrolyse van anionen Sommige anionen, afkomstig van meerbasische zuren hydrolyseren in meerdere stappen. De mate waarin elk van die hydrolysestappen doorgaat is afhankelijk van de desbetreffende
25/02/207 Meerstapshydrolyse van anionen Sommige anionen, afkomstig van meerbasische zuren hydrolyseren in meerdere stappen. De mate waarin elk van die hydrolysestappen doorgaat is afhankelijk van de desbetreffende
Wat zijn anorganische of minerale stoffen? In hoeveel stofklassen zijn de anorganische stoffen in te delen?
 Wat zijn anorganische of minerale stoffen? A. Deze stoffen komen hoofdzakelijk voor in de niet-levende natuur. In hoeveel stofklassen zijn de anorganische stoffen in te delen? B. 4 Welk van deze stofklassen
Wat zijn anorganische of minerale stoffen? A. Deze stoffen komen hoofdzakelijk voor in de niet-levende natuur. In hoeveel stofklassen zijn de anorganische stoffen in te delen? B. 4 Welk van deze stofklassen
13 Evenwichten. Hoofdstuk 13 Evenwichten. 13.1 Omkeerbare reacties. 13.2 Dynamisch evenwicht
 13 Evenwichten 13.1 Omkeerbare reacties Hoofdstuk 13 Evenwichten Het is in de praktijk vrijwel onmogelijk om beide reacties tegelijk te laten verlopen. 7 a Roze + n H 2 O Blauw.n H 2 O 3 1 a Schrijf beide
13 Evenwichten 13.1 Omkeerbare reacties Hoofdstuk 13 Evenwichten Het is in de praktijk vrijwel onmogelijk om beide reacties tegelijk te laten verlopen. 7 a Roze + n H 2 O Blauw.n H 2 O 3 1 a Schrijf beide
TF5 Scheikunde 4 VWO H 8 en H 9 16 juni 2011
 TF5 Scheikunde 4 VWO H 8 en H 9 16 juni 2011 Deze toets bestaat uit 28 onderdelen. Hiervoor zijn in totaal X punten te behalen. Kalkwater Calciumhydroxide, Ca(OH) 2 (s) is matig oplosbaar in water. Als
TF5 Scheikunde 4 VWO H 8 en H 9 16 juni 2011 Deze toets bestaat uit 28 onderdelen. Hiervoor zijn in totaal X punten te behalen. Kalkwater Calciumhydroxide, Ca(OH) 2 (s) is matig oplosbaar in water. Als
Oefenopgaven TITRATIES
 Oefenopgaven TITRATIES vwo ZUURBASE-TITRATIES OPGAVE 1 Tijdens een titratie wordt 10,00 ml 3,00 10-4 M zwavelzuur getitreerd met natronloog van onbekende molariteit. Er is 21,83 ml natronloog nodig om
Oefenopgaven TITRATIES vwo ZUURBASE-TITRATIES OPGAVE 1 Tijdens een titratie wordt 10,00 ml 3,00 10-4 M zwavelzuur getitreerd met natronloog van onbekende molariteit. Er is 21,83 ml natronloog nodig om
Cursus Chemie 5-1. Hoofdstuk 5: KWANTITATIEVE ASPECTEN VAN CHEMISCHE REACTIES 1. BELANGRIJKE BEGRIPPEN. 1.1. Relatieve Atoommassa (A r)
 Cursus Chemie 5-1 Hoofdstuk 5: KWANTITATIEVE ASPECTEN VAN CHEMISCHE REACTIES 1. BELANGRIJKE BEGRIPPEN 1.1. Relatieve Atoommassa (A r) A r = een onbenoemd getal dat de verhouding weergeeft van de atoommassa
Cursus Chemie 5-1 Hoofdstuk 5: KWANTITATIEVE ASPECTEN VAN CHEMISCHE REACTIES 1. BELANGRIJKE BEGRIPPEN 1.1. Relatieve Atoommassa (A r) A r = een onbenoemd getal dat de verhouding weergeeft van de atoommassa
Uitwerkingen 3.7.1. Uitwerkingen 3.7.4
 Uitwerkingen 3.7.1 1 1,5 12 = 18 eieren 2 3,25 144 = 468 figuurzaagjes 3 25 24 = 600 bierflesjes 4 3,75 20.000 = 75.000 korrels hagelslag 5 2,25 10.000.000 = 22.500.000 zoutkorrels 6 1,5 6 10 23 = 9 10
Uitwerkingen 3.7.1 1 1,5 12 = 18 eieren 2 3,25 144 = 468 figuurzaagjes 3 25 24 = 600 bierflesjes 4 3,75 20.000 = 75.000 korrels hagelslag 5 2,25 10.000.000 = 22.500.000 zoutkorrels 6 1,5 6 10 23 = 9 10
Uitwerkingen huiswerk week 4
 Calculus/analyse najaar 007 Uitwerkinen huiswerk week 4 Opave 1. Bepaal de hoote en het volume van de rootste cilinder qua volume) die in een koel van straal r past. Oplossin. We noemen de hoote van de
Calculus/analyse najaar 007 Uitwerkinen huiswerk week 4 Opave 1. Bepaal de hoote en het volume van de rootste cilinder qua volume) die in een koel van straal r past. Oplossin. We noemen de hoote van de
EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN Dit examen bestaat voor iedere kandidaat uit 5 OPGAVEN
 MAVO-4 I EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN 1974 MAVO-4 Woensdag 8 mei, 9.00 11.00 NATUUR-EN SCHEIKUNDE II (Scheikunde) OPEN VRAGEN Dit examen bestaat voor iedere kandidaat uit 5 OPGAVEN
MAVO-4 I EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN 1974 MAVO-4 Woensdag 8 mei, 9.00 11.00 NATUUR-EN SCHEIKUNDE II (Scheikunde) OPEN VRAGEN Dit examen bestaat voor iedere kandidaat uit 5 OPGAVEN
1 XIII. Oplosbaarheid
 XIII. Oplobaarheid 1 3 4 Oploen van ionaire verbindingen in water: het oplobaarheidprodut 5 oploen: Ca (v) Ca (aq) - (aq) neerlaan: Ca (aq) - (aq) Ca (v) evenwihtintelling: Ca (v) Ca (aq) - (aq) verzadigde
XIII. Oplobaarheid 1 3 4 Oploen van ionaire verbindingen in water: het oplobaarheidprodut 5 oploen: Ca (v) Ca (aq) - (aq) neerlaan: Ca (aq) - (aq) Ca (v) evenwihtintelling: Ca (v) Ca (aq) - (aq) verzadigde
T8: Zoutoplossingen en Zuren en Basen
 T8: Zoutoplossingen en Zuren en Basen 2009 Voorbeeldtoets maandag 25 januari 60 minuten NASK 2, 4 VMBO-TGK, DEEL A. H3: ZOUTOPLOSSINGEN 4 VMBO-TGK, DEEL B. H4: ZUREN EN BASEN Toets voor het vak Nask2.
T8: Zoutoplossingen en Zuren en Basen 2009 Voorbeeldtoets maandag 25 januari 60 minuten NASK 2, 4 VMBO-TGK, DEEL A. H3: ZOUTOPLOSSINGEN 4 VMBO-TGK, DEEL B. H4: ZUREN EN BASEN Toets voor het vak Nask2.
Samenvatting Scheikunde Hoofdstukken 8&9: zuren en basen
 Samenvatting Scheikunde Hoofdstukken 8&9: zuren en basen Samenvatting door een scholier 1810 woorden 4 december 2017 4,8 9 keer beoordeeld Vak Methode Scheikunde Chemie overal Scheikunde hoofdstuk 8 Zuren
Samenvatting Scheikunde Hoofdstukken 8&9: zuren en basen Samenvatting door een scholier 1810 woorden 4 december 2017 4,8 9 keer beoordeeld Vak Methode Scheikunde Chemie overal Scheikunde hoofdstuk 8 Zuren
Augustus geel Chemie Vraag 1
 Chemie Vraag 1 Men beschikt over een oplossing van ijzer(ii)nitraat met c = 3,00 mol/l en heeft voor een experiment 0,600 mol nitraationen nodig. Hoeveel ml van de oplossing dient men te gebruiken?
Chemie Vraag 1 Men beschikt over een oplossing van ijzer(ii)nitraat met c = 3,00 mol/l en heeft voor een experiment 0,600 mol nitraationen nodig. Hoeveel ml van de oplossing dient men te gebruiken?
Cursus Chemie 3-1. Hoofdstuk 3: Zuren, basen en zouten 1. INLEIDING
 Cursus Chemie 3-1 Hoofdstuk 3: Zuren, basen en zouten 1. INLEIDING Gedurende de geschiedenis van de scheikunde is er gepoogd om op allerlei manieren een classificatie van de verbindingen op te stellen.
Cursus Chemie 3-1 Hoofdstuk 3: Zuren, basen en zouten 1. INLEIDING Gedurende de geschiedenis van de scheikunde is er gepoogd om op allerlei manieren een classificatie van de verbindingen op te stellen.
Samenvatting Scheikunde Boek 2
 Samenvatting Scheikunde Boek 2 Samenvatting door een scholier 2661 woorden 26 april 2005 6,2 89 keer beoordeeld Vak Methode Scheikunde Chemie overal Hoofdstuk 1 1.1 -> Reactie en molverhouding M Vm NA
Samenvatting Scheikunde Boek 2 Samenvatting door een scholier 2661 woorden 26 april 2005 6,2 89 keer beoordeeld Vak Methode Scheikunde Chemie overal Hoofdstuk 1 1.1 -> Reactie en molverhouding M Vm NA
Aluminium reageert met zuurstof tot aluminiumoxide. Geeft het reactieschema van deze reactie.
 RECTIESCHEM S EINDS LEVEL 2 RECTIESCHEM S EINDS C LEVEL 2 luminium reageert met zuurstof tot aluminiumoxide. Geeft het reactieschema van deze reactie. IJzer reageert met zuurstof tot IJzer(III)oxide. Geef
RECTIESCHEM S EINDS LEVEL 2 RECTIESCHEM S EINDS C LEVEL 2 luminium reageert met zuurstof tot aluminiumoxide. Geeft het reactieschema van deze reactie. IJzer reageert met zuurstof tot IJzer(III)oxide. Geef
Wiskundig Modelleren 1 Chemische Mengsels en Reacties. Anne Buijsrogge en Corine Laan
 Wiskundig Modelleren 1 Chemische Mengsels en Reacties Anne Buijsrogge en Corine Laan 23 oktober 2009 1 Vragen uit het lab Als je chemische mengsels wilt maken, kunnen daar een hoop vragen bij opkomen Hoe
Wiskundig Modelleren 1 Chemische Mengsels en Reacties Anne Buijsrogge en Corine Laan 23 oktober 2009 1 Vragen uit het lab Als je chemische mengsels wilt maken, kunnen daar een hoop vragen bij opkomen Hoe
Hoofdstuk 14: Zuur-Base
 Hoofdstuk : uur-ase Wat is een zuur? -het bevat H-atomen -het splitst H af bij oplossen in water HO H zelfde energie als covalente binding H-rest H rest H-rest HO HO rest HO permanent Hl H l Sp² hybridisatie
Hoofdstuk : uur-ase Wat is een zuur? -het bevat H-atomen -het splitst H af bij oplossen in water HO H zelfde energie als covalente binding H-rest H rest H-rest HO HO rest HO permanent Hl H l Sp² hybridisatie
29ste VLAAMSE CHEMIE OLYMPIADE EERSTE RONDE
 Actieve steun Vlaamse Chemie Olympiade UAntwerpen K.U.Leuven K.U.Leuven Kulak UGent UHasselt VUB BNV KVCV VOB KBIN VeLeWe 29ste VLAAMSE CHEMIE OLYMPIADE EERSTE RONDE Sponsors 16 november 2011 Gewest Brussel
Actieve steun Vlaamse Chemie Olympiade UAntwerpen K.U.Leuven K.U.Leuven Kulak UGent UHasselt VUB BNV KVCV VOB KBIN VeLeWe 29ste VLAAMSE CHEMIE OLYMPIADE EERSTE RONDE Sponsors 16 november 2011 Gewest Brussel
OEFENOPGAVEN MOLBEREKENINGEN
 OEFENOPGAVEN MOLBEREKENINGEN * = voor VWO Salmiak, NH 4 Cl(s), kan gemaakt worden door waterstofchloride, HCl(g), te laten reageren met ammoniak, NH 3 (g) 01 Wat is de chemische naam voor salmiak? 02 Geef
OEFENOPGAVEN MOLBEREKENINGEN * = voor VWO Salmiak, NH 4 Cl(s), kan gemaakt worden door waterstofchloride, HCl(g), te laten reageren met ammoniak, NH 3 (g) 01 Wat is de chemische naam voor salmiak? 02 Geef
Uitwerkingen van de opgaven uit: CHEMISCHE ANALYSE ISBN , 1 e druk, Uitgeverij Syntax Media Hoofdstuk 5 Argentometrie bladzijde 1
 Hoofdstuk 5 Argentometrie bladzijde 1 Opgave 1 Bereken met behulp van het oplosbaarheidsproduct de oplosbaarheid (g/l) in zuiver water bij kamertemperatuur, van: a CuBr K s = 5,2 x 10-9 CuBr Cu + + Br
Hoofdstuk 5 Argentometrie bladzijde 1 Opgave 1 Bereken met behulp van het oplosbaarheidsproduct de oplosbaarheid (g/l) in zuiver water bij kamertemperatuur, van: a CuBr K s = 5,2 x 10-9 CuBr Cu + + Br
OEFENOPGAVEN VWO EVENWICHTEN
 OPGAVE 1 OEFENOPGAVEN VWO EVENWICHTEN In een ruimte van 5,00 liter brengt men 9,50 mol HCl(g) en 2,60 mol O 2 (g). Na evenwichtsinstelling is 40,0% van de beginstoffen omgezet en is er Cl 2 (g) en H 2
OPGAVE 1 OEFENOPGAVEN VWO EVENWICHTEN In een ruimte van 5,00 liter brengt men 9,50 mol HCl(g) en 2,60 mol O 2 (g). Na evenwichtsinstelling is 40,0% van de beginstoffen omgezet en is er Cl 2 (g) en H 2
Hoofdstuk 3-5. Reacties. Klas
 Hoofdstuk 3-5 Reacties Klas 3 MOLECUULFORMULES OPDRACHT 1: MOLECUULFORMULES LEVEL 1 A H 2O C 2H 6 C C 2H 6O D CO 2 E F C 4H 8O CHN OPDRACHT 2: MOLECUULFORMULES LEVEL 1 A HNO C 3H 6O C C 2H 2 D C 6H 5NO
Hoofdstuk 3-5 Reacties Klas 3 MOLECUULFORMULES OPDRACHT 1: MOLECUULFORMULES LEVEL 1 A H 2O C 2H 6 C C 2H 6O D CO 2 E F C 4H 8O CHN OPDRACHT 2: MOLECUULFORMULES LEVEL 1 A HNO C 3H 6O C C 2H 2 D C 6H 5NO
Uitwerkingen van de opgaven uit: BASISCHEMIE voor het MLO ISBN , 3 e druk, Uitgeverij Syntax Media Hoofdstuk 18 Oxidimetrie bladzijde 1
 Hoofdstuk 18 Oxidimetrie bladzijde 1 Opgave 1 Bepaal met behulp van tabel II de reactie tussen kaliumpermanganaat in zuur milieu met: a Sn 2+ ionen MnO 4 + 8 H 3O + + 5 e Mn 2+ + 12 H 2O x 2 Sn 2+ Sn 4+
Hoofdstuk 18 Oxidimetrie bladzijde 1 Opgave 1 Bepaal met behulp van tabel II de reactie tussen kaliumpermanganaat in zuur milieu met: a Sn 2+ ionen MnO 4 + 8 H 3O + + 5 e Mn 2+ + 12 H 2O x 2 Sn 2+ Sn 4+
Verband tussen aantal mol en de massa symbool naam eenheid voorbeeld
 Naam : Klas: Datum: Rekenen in de chemie Informatie over de massa van 1 deeltje A a A r M a M r u (1 atoom) Relatieve (1 atoom) molecuulmassa (1 molecule) Relatieve (1 molecule) referentiemassa (1 proton)
Naam : Klas: Datum: Rekenen in de chemie Informatie over de massa van 1 deeltje A a A r M a M r u (1 atoom) Relatieve (1 atoom) molecuulmassa (1 molecule) Relatieve (1 molecule) referentiemassa (1 proton)
SCHEIKUNDE KLAS 3 REACTIES SKILL TREE
 SKILL TREE MOLECUULFORMULES OPDRACHT 1: MOLECUULFORMULES LEVEL 1 A H 2 O C 2 H 6 C C 2 H 6 O D CO 2 E F C 4 H 8 O CHN OPDRACHT 2: MOLECUULFORMULES LEVEL 1 A HNO C 3 H 6 O C C 2 H 2 D C 6 H 5 NO E C 5 H
SKILL TREE MOLECUULFORMULES OPDRACHT 1: MOLECUULFORMULES LEVEL 1 A H 2 O C 2 H 6 C C 2 H 6 O D CO 2 E F C 4 H 8 O CHN OPDRACHT 2: MOLECUULFORMULES LEVEL 1 A HNO C 3 H 6 O C C 2 H 2 D C 6 H 5 NO E C 5 H
Curie Hoofdstuk 6 HAVO 4
 Rekenen aan reacties Curie Hoofdstuk 6 HAVO 4 6.1 Rekenen met de mol 6.2 Rekenen met massa s 6.3 Concentratie 6.4 SPA en Stappenplan 6.1 Rekenen met de mol Eenheden en grootheden 1d dozijn potloden 12
Rekenen aan reacties Curie Hoofdstuk 6 HAVO 4 6.1 Rekenen met de mol 6.2 Rekenen met massa s 6.3 Concentratie 6.4 SPA en Stappenplan 6.1 Rekenen met de mol Eenheden en grootheden 1d dozijn potloden 12
Gegeven is volgende niet-uitgebalanceerde reactievergelijking waarin X de formule van een verbinding voorstelt:
 Chemie Vraag 1 Gegeven is volgende niet-uitgebalanceerde reactievergelijking waarin X de formule van een verbinding voorstelt: CS2 + X + KOH K2SO4 + K2CO3 + KCl + H2O De hoeveelheden (in mol) van de betrokken
Chemie Vraag 1 Gegeven is volgende niet-uitgebalanceerde reactievergelijking waarin X de formule van een verbinding voorstelt: CS2 + X + KOH K2SO4 + K2CO3 + KCl + H2O De hoeveelheden (in mol) van de betrokken
7.0 Enkele belangrijke groepen van verbindingen
 7.0 Enkele belangrijke groepen van verbindingen 7.1 Oxiden Vrijwel alle elementen kunnen, min of meer heftig reageren met zuurstof. De gevormde verbindingen worden oxiden genoemd. In een van de voorafgaande
7.0 Enkele belangrijke groepen van verbindingen 7.1 Oxiden Vrijwel alle elementen kunnen, min of meer heftig reageren met zuurstof. De gevormde verbindingen worden oxiden genoemd. In een van de voorafgaande
Wet van Behoud van Massa
 Les 3 E42 Wet van Behoud van Massa In 1789 door Antoine Lavoiser ontdekt dat : De totale massa tijdens een reactie altijd gelijk blijft. Bij chemische reacties worden moleculen dus veranderd in andere
Les 3 E42 Wet van Behoud van Massa In 1789 door Antoine Lavoiser ontdekt dat : De totale massa tijdens een reactie altijd gelijk blijft. Bij chemische reacties worden moleculen dus veranderd in andere
Kaliumaluminiumsulfaat is een dubbelzout met drie ionsoorten, twee positieve monoatomische en één negatief polyatomisch.
 Chemie Vraag 1 Kaliumaluminiumsulfaat is een dubbelzout met drie ionsoorten, twee positieve monoatomische en één negatief polyatomisch. Wat is de juiste formule van dit dubbelzout? KAlSO4 KAl(SO4)2 K3Al(SO4)2
Chemie Vraag 1 Kaliumaluminiumsulfaat is een dubbelzout met drie ionsoorten, twee positieve monoatomische en één negatief polyatomisch. Wat is de juiste formule van dit dubbelzout? KAlSO4 KAl(SO4)2 K3Al(SO4)2
Kaliumaluminiumsulfaat is een dubbelzout met drie ionsoorten, twee positieve monoatomische en één negatief polyatomisch.
 Chemie Vraag 1 Kaliumaluminiumsulfaat is een dubbelzout met drie ionsoorten, twee positieve monoatomische en één negatief polyatomisch. Wat is de juiste formule van dit dubbelzout? K3AlSO4 K3Al(SO4)2 KAl(SO4)2
Chemie Vraag 1 Kaliumaluminiumsulfaat is een dubbelzout met drie ionsoorten, twee positieve monoatomische en één negatief polyatomisch. Wat is de juiste formule van dit dubbelzout? K3AlSO4 K3Al(SO4)2 KAl(SO4)2
UITWERKING CCVS-TENTAMEN 21 juli 2017
 UITWERKING CCVS-TENTAMEN 21 juli 2017 Frank Povel NB. Deze uitwerking is door mij gemaakt en is niet de uitwerking die de CCVS hanteert. Er kunnen dan ook op geen enkele wijze rechten aan deze uitwerking
UITWERKING CCVS-TENTAMEN 21 juli 2017 Frank Povel NB. Deze uitwerking is door mij gemaakt en is niet de uitwerking die de CCVS hanteert. Er kunnen dan ook op geen enkele wijze rechten aan deze uitwerking
34 ste Vlaamse Chemie Olympiade
 34 ste Vlaamse hemie Olympiade 2016-2017 2 de ronde 22 februari 2017 Je naam en voornaam: Je adres: De naam van je school: Het adres van je school: Je leerjaar: antal lesuren chemie per week die je dit
34 ste Vlaamse hemie Olympiade 2016-2017 2 de ronde 22 februari 2017 Je naam en voornaam: Je adres: De naam van je school: Het adres van je school: Je leerjaar: antal lesuren chemie per week die je dit
