Jaarverslag METC UMC Utrecht
|
|
|
- Thomas Dijkstra
- 4 jaren geleden
- Aantal bezoeken:
Transcriptie
1 Jaarverslag 2018 METC UMC Utrecht Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht Huispostnummer D Postbus GA Utrecht Telefoon: info@metcutrecht.nl
2 INHOUD Inhoud Voorwoord 3 Samenvatting 4 Summary 5 1. Bevoegd gezag METC 6 2. Samenstelling commissie 7 3. Secretariaat 8 4. Werkwijze commissie 9 5. De toetsing van WMO-plichtig onderzoek Administratief beroep Embryowet Overige werkzaamheden Klachten, Wob-verzoeken en dwangsommen Kwaliteitsbeleid en scholing Intervisie CCMO toezicht Financiën 23 Tot Slot 24 Bijlagen: 1. Ingediende protocollen per verrichter en per divisie Gebruikte afkortingen Leden en secretariaat Colofon 33 2
3 Voorwoord van de voorzitter Geachte lezer, Voor u ligt het recentste jaarverslag van de Medisch Ethische Toetsingscommissie van het UMC Utrecht. Hierin vindt u de belangrijkste getallen die ons werk reflecteren, zoals het aantal beoordelingen van WMO dossiers (114 dossiers), het aantal wel/niet-wmo afwegingen (600) en de gemiddelde toetsingstermijn (44,4 dagen). In grote lijnen komen deze overeen met voorgaande jaren. Het afgelopen jaar was bijzonder. Ten eerste is in 2018 gewerkt aan de voorbereiding op een samenwerking tussen het UMC Utrecht en het Prinses Máxima Centrum voor kinderoncologie, waarbij beide organisaties hun krachten hebben gebundeld in een gezamenlijke METC per 1 januari Per die datum is de METC UMC Utrecht verder gegaan onder de naam METC Utrecht. Onderdeel van deze samenwerking is de toetreding van professor Michel Zwaan tot het Dagelijks Bestuur van de METC. In 2019 verwachten we dat leden met specifieke kinderoncologische expertise beide METC-kamers komen versterken. Ten tweede heeft de METC ook gekozen om de kwaliteit van de toetsing van medische hulpmiddelen verder te verbeteren. We hebben niet alleen de jaarlijkse plenaire scholing van commissieleden hierop gericht, maar ook de adviserende rol van de afdeling Klinische Fysica omgezet in METC-lidmaatschap van Ir. Rens Wientjes, klinisch fysicus. Ten derde wordt vol ingezet op voorbereiding van de nieuwe EU-Verordening door deelname aan de Vrijwillige Harmonisatie Procedure (VHP). Ten slotte hebben eerdere acties geleid tot volwaardige bezetting van beide Kamers van de METC met een uitstekend gedifferentieerde groep experts, die hebben laten zien continu op zoek te zijn naar verbetering. de METC haar werk kan doen, zich kan inzetten voor bescherming van proefpersonen en een bijdrage kan leveren aan de kwaliteit van het onderzoeksklimaat. We kijken er naar uit om de ingeslagen weg met de gemeenschappelijke METC van het Prinses Máxima Centrum en het UMC Utrecht in 2019 verder vorm te geven. Wij wensen u veel leesplezier! Prof.dr. L. J. Bont, algemeen voorzitter en voorzitter Kamer M, mede namens Dr. G.J.M. van Thiel, voorzitter Kamer D Prof. dr. C. M. Zwaan, Lid Dagelijks Bestuur Mr. S. de Weerd-Hamer, Hoofd Toetsing Onderzoek Het is dankzij de deskundige inzet van de leden en het niet aflatend enthousiasme en de professionaliteit van het secretariaat dat 3
4 Samenvatting In dit jaarverslag doet de Medisch Ethische Toetsingscommissie (METC) van het UMC Utrecht verslag van haar activiteiten in De primaire taak van de METC is het medisch, wetenschappelijk en ethisch toetsen van onderzoeksvoorstellen voor medisch-wetenschappelijk onderzoek met mensen in het kader van de Wet Medisch-wetenschappelijk Onderzoek met Mensen (WMO). Het wettelijk kader van de METC wordt ook bepaald door de Embryowet, het Besluit Medische Hulpmiddelen en het Besluit Actieve Implantaten en de Algemene Verordening Gegevensbescherming (AVG). Bij de toetsing staat de bescherming van de proefpersoon voorop, waarbij tegelijkertijd oog wordt gehouden voor de vooruitgang van de medische wetenschap. De METC streeft ernaar haar toetsingsprocedures zo in te richten dat aan de afweging van de verschillende belangen recht wordt gedaan en de procedures binnen de wettelijk vastgestelde termijnen worden afgerond. De toename van het aantal beoordeelde geneesmiddelendossiers zette zich ook in 2018 voort. Daarentegen nam het beoogd aantal proefpersonen af, wat een goede ontwikkeling lijkt te zijn: minder mensen hoeven belast te worden om de resultaten te bereiken. Ook in 2018 kwamen de meeste onderzoekers hun onderzoek mondeling toelichten in de vergadering, wat de verdere afhandeling vereenvoudigde. De commissie slaagde er dan ook weer in haar gemiddeld korte toetsingstijd te handhaven: met 44,4 dagen ruim binnen de wettelijk verplichte termijn. Voor het eerst sinds jaren nam het aantal verzoeken tot afweging of een voorstel wel of niet WMO-plichtig is, niet toe. Gegevens van 2017 en 2018: Aantal WMO besluiten Waarvan multicenter Aantal negatieve besluiten 7 2 Beoogd aantal betrokken proefpersonen Aantal beoordeelde Geneesmiddelen dossiers (met name fase II/III) Aantal beoordeelde WMO dossiers met Medisch Hulpmiddel Toetsingstijd METC WMO-dossiers, gemiddeld 42,34 44,4 (kalenderdagen) Aantal ingediende verzoeken afweging wel/niet WMO-plichtig
5 Summary This annual report describes the activities of the UMC Utrecht METC (Medical Research Ethics Committee, MREC) in The main task of the METC is to review research proposals on their medical, scientific and ethical aspects under the Medical Research involving Human Subjects Act (WMO). The legal framework of the MREC also includes the Embryo Act, the Medical Device Decree and the Active Implants Decree. The primary aim of the MREC review is protection of the research subjects who will be participating in medical scientific studies, while at the same time supporting progress in medical scientific research. The increase in the number of research proposals involving a medicinal product submitted for WMO-review continued in In contrast, the total required number of participating subjects proposed by researchers decreased. This seems to be a positive development: fewer subjects need to be involved in research, to obtain results. In 2018, again at most MREC procedures, researchers joined the committee meeting to explain their study proposal, which contributed to a shorter review procedure. With an average of 44.4 days, the MREC review procedure stayed well within the formal time-limit. For the first time, the number of research proposals submitted to the MREC for consideration of whether or not the proposal falls within the scope of the WMO did not increase. Summary numbers of 2017 and 2018: Reviewed WMO-research proposals Multicentre Negative Judgement 7 2 Proposed number of participating research subjects Reviewed research proposals with medicinal products Studies with a medical device Timelines MREC WMO-research (calendar days) Assessments of whether the proposal falls within the scope of the WMO
6 Hoofdstuk 1 Bevoegd gezag METC De METC van het UMC Utrecht is ingesteld door de Raad van Bestuur (RvB) van het UMC Utrecht en is op 19 november 1999 door de Centrale Commissie Mensgebonden Onderzoek (CCMO) erkend als toetsingscommissie in het kader van de Wet Medisch-wetenschappelijk Onderzoek met Mensen (WMO). De METC is een instellingsgebonden commissie die wordt gefaciliteerd door de RvB van het UMC Utrecht. De METC van het UMC Utrecht is als Zelfstandig Bestuursorgaan (ZBO) bevoegd om voor de burger bindende besluiten te nemen. De METC is dan ook in haar besluitvorming volstrekt onafhankelijk van de instelling. De kring waarvoor de METC van het UMC Utrecht beoordelingen uitvoert, strekt zich uit over heel Nederland. Met ingang van 1 januari 2019 is het UMC Utrecht en het Prinses Maxima Centrum voor kinderoncologie (inclusief SKION) gaan samenwerken op het gebied van toetsing van medisch-wetenschappelijk onderzoek. De samenwerking ziet op de toetsing van medisch-wetenschappelijk onderzoek en het Prinses Máxima Centrum zal daartoe als participerend centrum deel gaan uitmaken van de gezamenlijke METC Utrecht. 6
7 Hoofdstuk 2 Samenstelling commissie In iedere METC-vergadering moeten ten tenminste de door de WMO vereiste deskundigen aanwezig zijn om tot een rechtsgeldig besluit te kunnen komen. De METC is samengesteld uit meerdere personen per discipline. De verplichte disciplines zijn: arts, jurist, ethicus, methodoloog en een lid namens de proefpersonen. Bij beoordeling van geneesmiddelenonderzoek is tevens de aanwezigheid van een klinisch-farmacoloog en een ziekenhuisapotheker vereist. Vooruitlopend op de ontwikkelingen rond het toetsen van onderzoek met Medische Hulpmiddelen heeft de METC een klinisch fysicus als METC lid laten benoemen door de CCMO. Voor een volledige ledenlijst zie bijlage 3, waar ook vermeld staat welke leden afscheid namen en welke nieuwe leden bij de commissie kwamen in de loop van Nieuwe leden zijn door de CCMO goedgekeurd en door de RvB benoemd. Bij hun aantreden ontvingen zij een digitaal informatiepakket met documenten over de wet- en regelgeving en de werkwijze van de METC. Daarnaast werden zij ingewerkt door vergaderingen bij te wonen van de commissie en door individuele begeleiding van METC leden en het METC secretariaat. De scholing van METC-leden is verder beschreven in hoofdstuk 10. Algemeen voorzitter is de heer prof. dr. L.J. Bont, tevens voorzitter Kamer M. De voorzitter van Kamer D is mevrouw dr. G. J.M. van Thiel. 7
8 Hoofdstuk 3 Het secretariaat van de METC Het secretariaat van de METC wordt gevoerd door de afdeling Toetsing Onderzoek. Deze afdeling bestaat uit het secretariaat van twee toetsingscommissies, te weten de METC en de Toetsingscommissie Biobanken (TCBio). Zij staat onder leiding van mevrouw mr. S. de Weerd als hoofd Toetsing Onderzoek. De afdeling Toetsing Onderzoek bestond in 2018 uit een administratief medewerker, drie procedure coördinatoren en vier secretarissen. De afdeling valt organisatorisch onder de Directie Kwaliteit van zorg & Patiënt Veiligheid. Een lijst van de medewerkers van het secretariaat vindt u in bijlage 3. Het secretariaat is, naast via en telefoon, ook tweemaal per week bereikbaar tijdens een inloop spreekuur. Onderzoekers maken hiervan frequent gebruik. 8
9 Hoofdstuk 4 Werkwijze commissie De METC vergadert wekelijks (51 maal in 2018). De METC-leden zijn verdeeld over twee Kamers; Kamer M en Kamer D. Kamer M vergadert op de maandag in de oneven weken. Kamer D vergadert op de dinsdag in de even weken. De samenstelling van de expertise van de kamers is gelijkwaardig. De commissie beschikt over een grote diversiteit aan expertise, welke wordt ingezet al naar gelang het onderwerp van het onderzoek. Zo nodig worden vervangende leden gevraagd om in de vergadering te komen. De commissieleden ontvangen de vergaderstukken een week voor de vergadering op een digitaal platform (Viadesk), waarbij ieder dossier wordt voorzien van referenten rapporten (op het betreffende vakgebied en verder op het gebied van methodologie, vanuit het lid namens de proefpersoon, en waar het geneesmiddelenonderzoek betreft, van de klinisch farmacoloog en ziekenhuisapotheker). De referenten voegen hun rapporten bij de vergaderstukken op Viadesk. Aan het begin van iedere vergadering stelt de voorzitter vast of de verplichte disciplines aanwezig zijn en of geen van de aanwezigen betrokken zijn bij het te bespreken onderzoek. Indien een METC lid betrokken is bij het onderzoek verlaat hij/ zij de vergadering gedurende de bespreking van dat dossier. Dit wordt vastgelegd in de verslaglegging van de vergadering. In het verslag wordt tevens vastgelegd hoe de besluitvorming verloopt. De besluiten worden genomen met meerderheid van stemmen, maar vrijwel altijd leidt de discussie tot consensus. In veel gevallen wordt, na een genomen besluit, de afhandeling daarvan gemandateerd aan het Dagelijks Bestuur (bestaande uit de Algemeen voorzitter en de voorzitters van de kamers) of de secretaris. De commissie heeft haar werkwijze vastgelegd in haar reglement. De vigerende versie van het reglement is op 29 mei 2018 vastgesteld door de METC en door de Raad van Bestuur van het UMC Utrecht. Het reglement is te vinden op de websites van de METC en van de CCMO. 989
10 HOOfDStUk 5 De toetsing VaN wmo-plichtig ONDerzOek 5.1 Ingediende onderzoeksdossiers Bij rond de 80% van het ingediende onderzoek is het UMC Utrecht betrokken. De overige dossiers worden ingediend door andere aanvragers waaronder de Universiteit Utrecht (met name de Faculteit Sociale Wetenschappen), het RIVM, Revalidatiecentrum De Hoogstraat, het Prinses Máxima Centrum voor kinderoncologie, Tergooi Ziekenhuizen, Hogeschool Utrecht, IRAS, NIVEL, Trimbos Instituut, diverse andere ziekenhuizen en GGD instellingen. Voor een overzicht, zie bijlage 1. De METC nam enkele studies over van METC Noord Holland en eind 2018/ begin 2019 van Slotervaart Ziekenhuis en Reade. betrokken bij de administratieve afhandeling van deze verzoeken. Deze cijfers zijn daarom niet in dit jaarverslag opgenomen. 5.2 Primaire beoordeling De vorige paragraaf betrof het aantal ingediende dossiers. Deze paragraaf betreft het aantal in 2018 genomen besluiten. Deze besluiten kunnen betrekking hebben op dossiers die in 2017 zijn ingediend. Enkele dossiers die in 2018 zijn ingediend, zullen in 2019 beoordeeld worden. De laatste 3 jaar leek er sprake van een lichte daling van het aantal WMO-besluiten. Deze daling heeft zich in 2018 niet verder doorgezet. Figuur 1: In 2018 ingediende aanvragen, onderverdeeld naar WMO en (niet-) WMO afweging. N.B.: De METC beoordeelt geen onderzoek dat wordt uitgevoerd in het UMC Utrecht en primair door een andere METC in Nederland getoetst is. Hieronder valt ook onderzoek dat door de CCMO getoetst is, maar uitgevoerd wordt in het UMC Utrecht, zoals Gentherapie of onderzoek met genetisch gemodificeerde organismen (GGO). De METC beoordeelt ook geen verzoek om Toestemming van de RvB. Alleen het secretariaat van de METC, en niet de commissie, is Figuur 2: In het kader van de WMO afgegeven besluiten in 2012 t/m In 2018 heeft de METC twee keer een negatief besluit genomen over onderzoek. Bij beide studies had de commissie bezwaren tegen de gekozen patiëntenpopulatie en vond de commissie dat de belasting van de proefpersonen niet in verhouding stond met de therapeutische voordelen en wetenschappelijke opbrengst. 10
11 HOOfDStUk 5 De toetsing VaN wmo-plichtig ONDerzOek Het percentage beoogde aantal proefpersonen in geneesmiddelenonderzoek ten opzichte van het beoogde aantal proefpersonen in al het onderzoek waarover de METC een oordeel gaf, nam in 2018 af tot 9,3%. Een sterke daling na de stijging in de afgelopen jaren van 3,5% in 2015 naar 14,5% in 2016 en naar 26,2% in Gezien de lichte stijging in het aantal geneesmiddelendossiers, betekent dit dat minder proefpersonen per dossier beoogd worden. Ten aanzien van de 34 door de METC beoordeelde dossiers inzake WMO plichtig geneesmiddelenonderzoeken vond een stijging plaats van het aantal Fase I (ten koste van Fase II) en Fase III dossiers tot resp. 6, 7 en 16 dossiers (in 2016 resp. 2, 6 en 8 in , 11 en 11). Figuur 3: Beoogd aantal proefpersonen bij primair WMO-oordeel per type onderzoek in Figuur 4: De verdeling van het aantal door de METC beoordeelde dossiers inzake WMO plichtig geneesmiddelenonderzoeken over de verschillende fasen. Al enige jaren is ruim de helft van het aantal getoetste dossiers een monocenter studie. In 2018: 60 monocenter studies, tegenover 54 multicenter studies. Het aandeel geneesmiddelenstudies ten opzichte van het totaal aantal beoordeelde studies nam in 2018 verder toe van iets minder tot iets meer dan 25% van de besluiten. In 2018 nam de commissie in totaal 18 besluiten bij onderzoek met een medisch hulpmiddel. Een lichte stijging ten opzichte van 11 in 2016 en 15 in De commissie ontving dit jaar geen verzoek tot toetsing op basis van de Embryowet. 11
12 Hoofdstuk 5 De toetsing van WMO-plichtig onderzoek 5.3 Amendementen De forse stijging van het aantal nadere besluiten bij amendementen in 2016 (ruim 20% meer amendementen dan in 2015), heeft niet verder doorgezet: in 2018 beoordeelde de METC 372 amendementen ten opzichte van 390 in 2017, en 423 in In 2013 waren dat er nog slechts 127 bij een ongeveer vergelijkbaar aantal primaire beoordelingen. Het aantal positief beoordeelde dossiers ligt al jaren rond de 120. De noodzaak tot amenderen kan verschillende oorzaken hebben: een voorbeeld is trage inclusie van proefpersonen, waardoor verlenging van de studie of deelname van meerdere centra nodig blijkt komt regelmatig voor. Op dit moment is er geen maximum gesteld aan het aantal amendementen per studie, of aan de termijn waarbinnen amendementen (nog) kunnen worden ingediend. 5.4 SAE s en SUSAR s De commissie beoordeelde weer een groot aantal meldingen van Serious Adverse Events (SAE s) en Suspected Unexpected Serious Adverse Reactions (SUSAR s). Het merendeel wordt via de portal van de CCMO aangeleverd (Toetsing Online). In de meeste gevallen wordt de melding voor kennisgeving aangenomen. Bij opvallende zaken stelt de commissie vragen aan de onderzoeker. 5.5 Opschorting en voortijdig einde Iedere METC dient de CCMO op grond van artikel 22 lid 1 van de WMO op de hoogte te brengen van een opschorting van een onderzoek en de voortijdige beëindiging van een studie. In 2018 werden 7studies door de onderzoeker opgeschort of voortijdig beëindigd. In de meeste gevallen hield de stopzetting verband met gebrek aan inclusie, gebrek aan werkzaamheid en een enkele keer het vertrek van onderzoekers en/of bij het onderzoek betrokken personeel. Indien de commissie vragen heeft, bijvoorbeeld wanneer zij zich afvraagt of de veiligheid van de proefpersoon in het geding is of of het gebrek aan inclusies vooraf te voorzien zou zijn geweest, dan verzoekt zij de onderzoeker om nadere toelichting te verstrekken. Ook beoordeelt de METC het informeren van de proefpersonen. De METC heeft bepaald dat langlopende (cohort-)studies om de 10 jaar aan de dan geldende wet- en regelgeving getoetst dienen te worden (ook als er geen amendementen plaatsvinden). 12
13 Hoofdstuk 5 De toetsing van WMO-plichtig onderzoek 5.6 Voortgangs- en eindrapportages De gemiddelde looptijd van een onderzoek is 3 jaar. De commissie beoordeelt de voortgangsrapportages van het lopend onderzoek waarover zij een positief WMO oordeel uitsprak. Dit betreft ongeveer 350 rapportages per jaar (zowel lopend in het UMC Utrecht, als in perifere ziekenhuizen of instellingen). Daarnaast beoordeelt de METC gemiddeld ongeveer 120 eindrapportages per jaar van de studies die afgerond zijn. Meestal wordt de rapportage voor kennisgeving aangenomen. Bij opvallende zaken stelt de commissie vragen aan de onderzoeker. 5.7 Beoordelingstijd Beoordeling toetsingstijd WMO dossiers. De wettelijke verplichte termijnen voor de toetsingstijd is voor geneesmiddelenonderzoek 60 dagen, voor niet-geneesmiddelenonderzoek 56, met mogelijkheid van verlenging. In 2018 kwam de toetsingstijd uit op een gemiddelde van 44,4 dagen (in 2016 en 2017 was dat resp, 44,7 en 42,34 dagen), waarbij zowel het geneesmiddelenonderzoek als het overig onderzoek ruim onder de maximale termijn bleef (met resp. 50,3 van de 60 en 42 van de 56 dagen). Beoordelingstijd amendementen en SAE s en SUSARs: Als er geen bijzonderheden zijn, kan een amendement binnen ongeveer 2 weken beoordeeld worden. Voor beoordeling van onverwachte ernstige voorvallen of bijwerkingen (SAE s en SUSARs) geldt hetzelfde. Indien de commissie vragen heeft bij een amendement of een melding, dan is uiteraard meer tijd nodig voor beoordeling. 13
14 Hoofdstuk 6 Administratief beroep Er is in 2018 één administratief beroep ingediend tegen een negatief besluit van de METC. De CCMO organiseerde een hoorzitting, waarbij vanuit de METC de voorzitter, een arts en een secretaris aanwezig waren. Vanuit de indiener waren drie vertegenwoordigers van de verrichter aanwezig. Op grond van de hoorzitting heeft de voorzitter van de CCMO de indiener de keuze voorgelegd om het beroep bij de CCMO voort te zetten, of het beroep in te trekken en een nieuwe versie van het protocol bij de METC in te dienen. De indiener heeft het beroep ingetrokken en besloten ook geen nieuwe versie van het protocol bij de METC in te dienen. 14
15 Hoofdstuk 7 Embryowet De beoordeling van onderzoek bij de foetus valt onder de Embryowet. Niet-invasief observationeel onderzoek bij de foetus mag sinds de wijziging van de Embryowet in 2013 worden beoordeeld door een erkende METC. De commissie ontving in 2018 geen verzoek tot toetsing van onderzoek op basis van de Embryowet. 15
16 HOOfDStUk 8 OVerIge werkzaamheden 8.1 Wel of niet WMO-plichtig? De commissie ontving 600 verzoeken om af te wegen of een voorstel onder de reikwijdte van de WMO valt. Bij 19 voorstellen besloot het Dagelijks Bestuur dat de WMO wel van toepassing was. Vier dossiers die ter toetsing aan de WMO waren ingediend, werden bij behandeling in de vergadering alsnog niet-wmo plichtig bevonden. Bij voorstellen die niet onder de reikwijdte van de WMO vielen vond verder geen inhoudelijke toetsing plaats. De niet-wmo verklaring betreft geen goedkeuring door de METC voor de uitvoer van het betreffende voorstel. 8.3 Medisch hulpmiddel Wanneer een medisch hulpmiddel onderwerp van onderzoek is, maar de WMO niet van toepassing is, dan is het toetsingskader voor de METC het Besluit Medische Hulpmiddelen. De METC bracht in 2018 in dit kader geen advies uit. 8.4 Algemene Verordening Gegevensbescherming (AVG) Met ingang van 25 mei 2018 werd de AVG van toepassing. Het landelijk model proefpersoneninformatie is hierop aangepast om aan de informatieplicht voortvloeiend uit de AVG te voldoen (versie mei 2018).De belangrijkste wijziging betrof paragraaf 10 over het gebruik en bewaren van gegevens en lichaamsmateriaal. Paragraaf 10 van het model proefpersoneninformatie is sindsdien een verplicht onderdeel van de informatiebrief. Een indirect gevolg van de aandacht voor de AVG was dat er meer vragen opkwamen vanuit zowel de onderzoekers als de commissie over privacy, met name bij onderzoek met apps en beeldmateriaal. Figuur 5 : Aantal voorgelegde verzoeken tot afweging wel/niet-wmo plichtig. 8.2 WMO met Biobank Indien in een WMO-dossier sprake is van extra afname van lichaamsmateriaal voor nog niet gespecificeerde onderzoeksvragen, dan wordt dit onderdeel van dat dossier door de METC op verzoek van de Toetsingscommissie Biobanken getoetst aan het Kaderreglement Biobanken van het UMC Utrecht. Hiervan was in 2018 sprake bij 5 dossiers. 16
17 Hoofdstuk 8 Overige werkzaamheden 8.5 Vragen Het METC secretariaat behandelt dagelijks uiteenlopende vragen via e- mail, telefoon of inloopspreekuur. Wanneer een vraag uitgebreider overleg binnen de commissie behoeft en niet binnen het Dagelijks Bestuur wordt afgehandeld, dan wordt deze vraag opgenomen in de METC database. De METC ontving in dat kader 9 vragen. Deze betroffen met name onderzoek met Medische Hulpmiddelen en enkele betreffende onderzoek met Lichaamsmateriaal. Ook kwamen vragen op ethisch of methodologisch vlak aan bod. 17
18 Hoofdstuk 9 Klachten, Wob-verzoeken en dwangsommen 9.1 Klachten De METC heeft een klachtenregeling ten behoeve van de waarborging van een behoorlijke behandeling van klachten geformuleerd in haar reglement. Dit is in overeenstemming met de Algemene wet bestuursrecht (Awb). Klachten worden tevens gemeld aan de CCMO. De METC ontving in 2018 twee klachten. In 2017 heeft de METC een bericht ontvangen, dat een patiënt het niet eens was met het goedgekeurde protocol. Het bezwaar werd eind 2017 ingediend als administratief beroep bij de CCMO, die het niet ontvankelijk verklaarde en vervolgens kwam dit in 2018 bij de METC, waar het als klacht werd behandeld. Zij kwam tot de conclusie dat de METC de vraag van de patiënt niet kon beantwoorden, en dat de patiënt de vraag aan de onderzoeker kon voorleggen. 9.2 Wob-verzoeken De Wet openbaarheid van bestuur (Wob) regelt het recht op informatie en zorgt ervoor dat iedereen inzage heeft in het handelen van de overheid of een bepaald bestuursorgaan, zoals een METC. In 2018 heeft de METC een Wob verzoek ontvangen: de aanvrager vroeg om openbaarmaking van namen van METC leden in een specifiek verband van een dossier uit In de loop van 2018 is de werkwijze van de METC aangepast en worden bij ieder besluit de namen van de aanwezige leden vermeld. 9.3 Dwangsommen In 2018 is door de onderzoekers geen beroep gedaan op art. 4:17 Algemene wet bestuursrecht. Daarnaast ontving de METC een bericht van een potentieel deelnemend centrum bij een studie, waarin vragen werden gesteld over de goedkeuring van de METC voor bepaalde aspecten in de opzet van de studie. Na een gesprek tussen een lid van het onderzoeksteam en het deelnemend centrum is geen officiële klacht bij de METC ingediend. 18
19 Hoofdstuk 10 Kwaliteitsbeleid en scholing 10.1 Kwaliteitsbeleid Zowel de kwaliteit van toetsing door de commissie als de kwaliteit van het METC secretariaat vormen een continu aandachtspunt van de METC en haar secretariaat. Via intervisie en evaluatie momenten wordt de werkwijze van de commissie en van het secretariaat steeds weer doorgelicht op verbeterpunten. De werkwijze ligt vast in de Standard Operating Procedures (SOPs), die regelmatig bijgewerkt worden. Ook onderhouden de voorzitters en de secretarissen van de verschillende METC s onderling contact. Gepoogd wordt de werkwijzen van de verschillende METC s op landelijk niveau zoveel mogelijk op elkaar af te stemmen. Een standaard werkwijze en SOPs werken betere kwaliteit in de hand. Maar het blijven hulpmiddelen en de werkelijke toetsing ligt binnen de commissie, in ethiek en haalbaarheid. Praktische zaken waar de METC soms tegen aan loopt, betreffen bijvoorbeeld onderzoek waarbij een financiële sponsor veel ondersteuning verleent en ook data beschikbaar krijgt, maar geen verrichter is. Waar liggen de grenzen van verantwoordelijkheid? Een ander punt betreft onderzoek met weinig risico en belasting, maar met veel centra (bijvoorbeeld bij huisartsen). In hoeverre moet de commissie de uitvoerbaarheid controleren (via samenwerkingsovereenkomsten, contracten e.d.?) Scholing: Plenaire vergadering Donderdag 22 november 2018 vond de jaarlijkse plenaire vergadering plaats in het Academiegebouw te Utrecht. Deze bijeenkomst betrof een gezamenlijke vergadering van de leden METC en de leden van de Toetsingscommissie Biobanken (TCBio). De plenaire vergadering betreft een belangrijk scholingsmoment voor de commissies. Naar aanleiding van de twee Europese verordeningen die op dit gebied de komende jaren van kracht worden, werd gesproken over Ontwikkelingen m.b.t. Medische hulpmiddelen en In-Vitro- Diagnostica; wat verandert er en wat betekent dat voor (de beoordeling van) onderzoek? Drie sprekers waren uitgenodigd: Drs. S.L. Hoekstra-van den Bosch, apotheker, medisch secretaris medische hulmiddelen (CCMO) sprak over Verordening Medische Hulpmiddelen: wat is nieuw en wat betekent dit voor klinisch onderzoek in Nederland? Vervolgens was het woord aan Prof. dr. K.G.M. Moons (UMC Utrecht), die een toelichting gaf bij de stelling: Evaluation of medical devices - no one size fits all. De derde spreker was METC lid en klinisch Fysicus Ir. R. Wientjes (afdeling Medische Technologie en Klinische Fysica) en hij wisselde van gedachten over: Onderzoek met medische hulpmiddelen en de rol van de MTKF en de klinisch fysicus in de METC. De opkomst was groot en de bijeenkomst geanimeerd. De aanwezigen kwamen tot de conclusie dat nieuwe ontwikkelingen op het gebied van wet- en regelgeving (de nieuwe EU verordeningen) en nieuwe medische hulpmiddelen een METC voor grote uitdagingen zal plaatsen Scholing: Cursussen Scholing in de vorm van basis- en vervolgtraining WMO/GCP en BROK-cursussen werd ook in 2018 mede door enkele METC-leden en secretariaatsmedewerkers verzorgd en gevolgd Scholing: Studie-uur Scholing van de METC leden vindt tevens plaats via de studie-uren die het secretariaat jaarlijks organiseert voor alle METC leden. In 2018 was het studie-uur op 18 juni en betrof een voordracht van prof. dr. C.B. Roes (Julius Centrum van het UMC Utrecht) over methodologische innovaties. De commissie krijgt steeds meer te maken met adaptieve trial designs. In het studie-uur is nader ingaan 19
20 Hoofdstuk 10 Kwaliteitsbeleid en scholing op wat er momenteel speelt op het gebied van innovatieve trials. Daarnaast werd stil gestaan bij de basis: wat kan geleerd worden uit de ervaring met eenvoudige studie designs? 10.5 Scholing: Landelijk overleg en voordrachten De voorzitters en secretarissen trachten zoveel mogelijk aanwezig te zijn bij landelijk overleg van de CCMO en de NVMETC. Het in werking treden van de nieuwe Europese Clinical Trial Regulation is verder uitgesteld. Zolang deze niet van kracht is wordt de werkwijze van toetsing geoefend in de VHP pilot. In 2018 zijn er 2 CCMO bijeenkomsten geweest waarin de VHP pilot werd geëvalueerd, een aantal leden uit METC en secretarissen waren hierbij aanwezig. De METC heeft in 2018 drie VHP-dossiers als betrokken lidstaat mede beoordeeld. In 2019 zal de METC een aantal keer gaan oefenen met het zelf opstellen van beoordelingsrapporten van geneesmiddelenstudies Scholing: Klinisch farmacologen i.o. De METC draagt bij aan de opleiding van klinisch farmacologen. Met enige regelmaat is een klinisch farmacoloog in opleiding aanwezig als toehoorder in de vergadering, onder begeleiding van het METC lid klinisch farmacoloog. Uiteraard wordt vooraf een geheimhoudingsverklaring getekend. 20
21 Hoofdstuk 11 Intervisie In het jaar 2018 heeft geen intervisie bij de METC van het UMC Utrecht plaatsgevonden. Voor 2019 staat dit wel weer gepland
22 Hoofdstuk 12 CCMO-toezicht In 2018 werd geen gerichte toezichtactie op de METC uitgevoerd vanuit de CCMO
23 Hoofdstuk 13 Financiën De METC ontvangt een structurele financiële bijdrage van de RvB van het UMC Utrecht. Voor de beoordeling van onderzoeksvoorstellen van UMC Utrecht-onderzoekers bracht de METC tot en met 2017 geen kosten in rekening, tenzij het onderzoek gesponsord werd door een verrichter met winstoogmerk. Met ingang van 1 januari 2018 zijn tarieven gewijzigd en is een nieuwe interne vergoedingenstructuur geïntroduceerd. De tarieven die de METC in rekening brengt voor de toetsing van protocollen zijn niet kostendekkend. Leden van de METC ontvingen een vergoeding indien zij niet in dienst waren van het UMC Utrecht. Voor leden van de METC die in dienst zijn van het UMC Utrecht zijn aparte afspraken over de vergoeding gemaakt met de divisies
24 Tot slot De METC en haar secretariaat hechten aan goede communicatie van de commissie met de onderzoekers, om zo het toetsingsproces optimaal te laten verlopen. Daarom wordt veel belang gehecht aan het inloopspreekuur en de mondelinge toelichting door de onderzoeker bij vrijwel ieder nieuw dossier in de commissie vergadering voorafgaand aan de beoordeling. Verder wordt permanent gewerkt aan optimalisering van de processen. Daarbij streeft de commissie naar een transparante en consistente toetsing. Tevens werkt de METC en het secretariaat aan de voorbereiding op de EU Verordening Geneesmiddelenonderzoek (naar verwachting van kracht in 2020) teneinde deze soepel te laten verlopen, onder andere via de VHP-pilot. De METC en haar secretariaat anticipeert op de ontwikkelingen rond het onderzoek met medische hulpmiddelen en in-vitro diagnostica. Het betreft nieuwe Europese wetgeving, waaraan voldaan moet worden met ingang van respectievelijk 26 mei 2020 en 26 mei Tot slot zal 2019 voor de METC in het teken staan van het verder vorm geven aan de samenwerking in één METC tussen het UMC Utrecht en het Prinses Máxima Centrum voor kinderoncologie (inclusief SKION) te Utrecht. In het volgend jaarverslag kunt u daar meer over lezen
25 Bijlage 1: Overzicht ingediende protocollen In 2018 ingediend WMO-plichtig onderzoek, aantal dossiers per verrichter. Verrichter Aantal dossiers ingediend UMC Utrecht 61 Universiteit Utrecht, FSW 6 Vertex Pharmaceuticals 3 Agios Pharmaceuticals Inc. 2 Prinses Máxima Centrum voor kinderoncologie 2 RIVM 2 Universiteit Utrecht 2 AbbVie 1 AI Therapeutics 1 Alexion Pharmaceuticals 1 Alfred Hospital 1 Altrecht GGZ 1 CARMAT SA 1 Cytokinetics Inc 1 Delft University of Technology 1 Diakonessenhuis Utrecht 1 EORTC 1 Genentech, Inc. 1 GGD Zeeland 1 GGZ Oost Brabant 1 Helen Dowling Instituut 1 Hoffmann-La Roche
26 Bijlage 1: Overzicht ingediende protocollen Idera Pharmaceutical, Inc. 1 Keystone Heart 1 LivaNova USA 1 Medtronic B.V. 1 NovImmune S.A. 1 Orion Corporation Orion Pharma 1 Orphazyme A/S 1 Peloton Therapeutics, Inc 1 Philips 1 Polyganics BV 1 Tergooiziekenhuizen 1 Trimbos Instituut 1 Universiteit van Amsterdam 1 Wageningen Universiteit 1 You2Yourself B.V. 1 26
27 Bijlage 1: Overzicht ingediende protocollen Aantal dossiers ingediend ter uitvoering in het UMC Utrecht per Divisie. Divisie in het UMC Utrecht 2018 Beeld 9 Biomedische Genetica 1 Hart en Longen 3 Heelkundige Specialismen 7 Hersenen 6 Interne Geneeskunde en Dermatologie 9 Cancer Center 5 Julius Centrum 4 Kinderen 7 Laboratoria en Apotheek 1 Vitale Functies 4 Vrouw en Baby 4 27
28 Bijlage 2: Gebruikte afkortingen ABR AVG Awb BCB BI BROK CCMO DCRF EMA IGJ IMPD METC NVMETC RvB SAE SUSAR TC Bio VHP VWS WGBO WMO Wob ZBO Algemeen beoordelings- en registratie formulier van de CCMO Algemene Verordening Gegevensbescherming Algemene wet bestuursrecht Besluit Centrale Beoordeling medisch-wetenschappelijk onderzoek met mensen Bevoegde Instantie Basiscursus regelgeving en organisatie voor klinisch onderzoekers Centrale Commissie Mensgebonden Onderzoek Dutch Clinical Research Foundation European Medicines Agency Inspectie Gezondheidszorg en Jeugd Investigational Medicinal Product Dossier Medisch-Ethische ToetsingsCommissie Nederlandse Vereniging van Medisch-Ethische Toetsingscommissies Raad van Bestuur Serious Adverse Events Suspected Unexpected Serious Adverse Reaction Toetsingscommissie Biobanken van het UMC Utrecht Vrijwillige Harmonisatie Procedure Ministerie van Volksgezondheid, Welzijn en Sport Wet op de Geneeskundige Behandelingsovereenkomst Wet medisch-wetenschappelijk onderzoek met mensen Wet openbaarheid van bestuur Zelfstandig Bestuursorgaan 28
29 Bijlage 3: Ledenlijst en medewerkers secretariaat METC Leden METC UMC Utrecht 1 januari 31 december Naam Functiebeschrijving WMO-discipline, lid vanaf/tot Dr. J.M.P. Baas Experimenteel psycholoog en psychofarmacoloog Prof. dr. L. Bont Kinderarts (Kinder-)arts - voorzitter Kamer M, alg. voorzitter Prof. dr. M.L. Bots Arts-epidemioloog Methodoloog, Plv tot Prof. dr. A.L. Bredenoord Ethicus Ethicus Prof. dr. F.J.M. Broekmans Gynaecoloog Arts, Plv tot I.E. de Bruijne Studiekeuze-/loopbaancoach Proefpersonenlid, Plv tot Prof. dr. W. Cahn Psychiater Arts Mr. M.R.D. Crijns Jurist Jurist, Plv vanaf Mr. R.H. Edema-Spaans Jurist; proefpersoonlid Proefpersonenlid, Plv Dr. S.G. Elias Klinisch epidemioloog Methodoloog, Plv Dr. K.J. van Erpecum MDL-arts Arts, vanaf Dr. M.A. van Es Neuroloog Arts Mr. A.M. Franse Jurist Jurist, Plv Dr. M.I. Geerlings Epidemioloog Methodoloog, Plv -tot Dr. I.M. van Geijlswijk Ziekenhuisapotheker, hoofd Apotheek Ziekenhuisapotheker Diergeneeskunde Dr. S.G. Geuze Neuropsycholoog Geen Dr. C.H. van Gils Epidemioloog Methodoloog, Plv tot Dr R. van der Graaf Ethicus Ethicus Dr.ir. J.P. Greving Epidemioloog Methodoloog, Plv tot Dr. F. Groenendaal Kinderarts - vicevoorzitter Kamer M (Kinder)arts Dr. W.W. Hale GZ-psycholoog, universitair hoofddocent Geen Dr. H.E. Hart Huisarts Arts Dr. E.S. van Hattum Vaatchirurg Geen, vanaf dr. J.W.G. Jacobs Reumatoloog Arts, vanaf Geen 29
30 Bijlage 3: Ledenlijst en medewerkers secretariaat METC Naam Functiebeschrijving WMO-discipline, lid vanaf/tot Prof. dr. P.A. de Jong Radioloog Arts Prof. dr. M.V. de Jonge GZ-psycholoog Geen, Plv tot Dr. K.R. Jongsma Ethicus Ethicus Dr. S. Kalkman Ethicus Ethicus Dr. M.J.A. van Kempen Klinisch moleculair geneticus Geen, Plv- tot Dr. K. Klipstein-Grobusch Methodoloog Methodoloog Prof. dr. L. Koenderman Immunobioloog Geen, Plv- tot Prof. dr. M. Koopman Internist-oncoloog Arts, Plv Prof. dr. F.P.J.G. Lafeber Medisch bioloog Geen, Plv tot Dr. A. Lalmohamed Ziekenhuisapotheker en klinisch farmacoloog Ziekenhuisapotheker en klinisch farmacoloog, vanaf Mr. H.E. van Lier Jurist Proefpersoonlid Dr. P.D. van der Linden Ziekenhuisapotheker Ziekenhuisapotheker, vanaf Dr. A.M. May Universitair Hoofddocent Methodoloog Dr. M. Meine Cardioloog Arts Dr. E.M. Monninkhof Epidemioloog; Methodoloog, Plv Mr. M. Mostert Jurist Jurist, Plv Dr. T. Mudrikova Internist Arts Dr. E.J.H. Mulder bioloog Geen Prof. dr. F.C. Oner Orthopedisch chirurg Arts, Plv tot Dr. N.C. Onland-Moret Epidemioloog Methodoloog, Plv tot Prof.dr. E.M. van de Putte Kinderarts (Kinder-)arts, Plv Dr. P.F.W.M. Rosier Arts, Urodynamicus Arts Prof. dr. A.F.A.M. Schobben Ziekenhuisapotheker en klinisch farmacoloog Klinisch farmacoloog, Plv 30
31 Bijlage 3: Ledenlijst en medewerkers secretariaat METC Naam Functiebeschrijving WMO-discipline, lid vanaf/tot Dr. E. Schuit Epidemioloog Methodoloog Dr. G.Tj. Sieswerda Cardioloog Arts, Plv tot Dr. M.G. Slieker Kindercardioloog (Kinder-)arts, vanaf Dr. T. Takken Medisch fysioloog Geen, tot Prof. dr. C.H.J. Terhaard Radiotherapeut Arts Dr. G.J.M. van Thiel Ethicus, voorzitter Kamer D Ethicus Dr. E.V. Uijtendaal Ziekenhuisapotheker en klinisch farmacoloog Klinisch farmacoloog en Ziekenhuisapotheker Dr. C.S.P.M. Uiterwaal Klinisch Epidemioloog Methodoog, Plv -tot Dr. C.H. Vaartjes Universitair hoofddocent cardiovasculaire Methodoloog epidemiologie Dr. R.P. Venekamp Huisarts Arts Mr. A.J. Verbout Jurist Jurist Mr. A.M. Vermaas Jurist Jurist Ir. R. Wientjes Klinisch Fysicus Geen, vanaf Dr. I. Wilting Ziekenhuisapotheker en klinisch farmacoloog Klinisch farmacoloog en Ziekenhuisapotheker Mr. A.M. Zijlmans Jurist Proefpersonenlid Prof. dr. C.M. Zwaan Kinderarts (Kinder-)arts, vanaf
32 Bijlage 3: Ledenlijst en medewerkers secretariaat METC Medewerkers Secretariaat METC 2018 Mw. M. (Marion) Berk-van der Linden Administratief medewerker Mw. P. B. (Pauline) de Vries Secretaresse Mw. mr. N.M. (Nina) Beusmans Senior Procedurecoördinator Dhr. drs. V. (Vincent) Bontrop Senior Procedurecoördinator Dhr. drs. R.P. (Rutger) Chorus Senior Procedurecoördinator Mw. R.G. (Rashieda) Jahangier Procedurecoördinator Mw. D.G. (Dion) Vredeveldt Procedurecoördinator ( t/m ) Mw. E. (Eva) van Wilgen Procedurecoördinator ( t/m ) Mw. dr. W. A. (Antoinette) Groenewegen Secretaris METC (niet-wmo) en Toetsingscommissie Biobanken Mw. drs. S. (Solange) Levison Secretaris METC (Kamer D) Mw. drs. M.D. (Myriam) van de Loo-Waller Secretaris METC (Kamer M) Mw. mr. N.M.A. (Noor) Verkleij Secretaris METC (Kamer M) t/m Mw. mr. S. (Saskia) de Weerd Hoofd Toetsing Onderzoek 32
33 Bijlage 4: Colofon Tekst en data: Secretariaat METC Redactie: Myriam van de Loo Contact: Datum: maart
34 Jaarverslag 2018 METC UMC Utrecht
Jaarverslag Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht
 Jaarverslag 2017 Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht Huispostnummer D 01.343 Postbus 85500
Jaarverslag 2017 Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht Huispostnummer D 01.343 Postbus 85500
Jaarverslag METC UMC Utrecht
 Jaarverslag 2016 METC UMC Utrecht INHOUD Voorwoord van de voorzitter blz. 3 Voorwoord 3 Samenvatting 4 Summary 5 1. Bevoegd gezag METC 6 2. Samenstelling commissie 7 3. Secretariaat 8 Kader 1: Mondelinge
Jaarverslag 2016 METC UMC Utrecht INHOUD Voorwoord van de voorzitter blz. 3 Voorwoord 3 Samenvatting 4 Summary 5 1. Bevoegd gezag METC 6 2. Samenstelling commissie 7 3. Secretariaat 8 Kader 1: Mondelinge
KLINISCH GENEESMIDDELEN- ONDERZOEK
 KLINISCH GENEESMIDDELEN- ONDERZOEK HET PROCES VAN HET OPSTARTEN VAN KLINISCH ONDERZOEK MET GENEESMIDDELEN GAAT VERANDEREN De ECTR verandert het klinisch onderzoek met geneesmiddelen in Europa. Dit heeft
KLINISCH GENEESMIDDELEN- ONDERZOEK HET PROCES VAN HET OPSTARTEN VAN KLINISCH ONDERZOEK MET GENEESMIDDELEN GAAT VERANDEREN De ECTR verandert het klinisch onderzoek met geneesmiddelen in Europa. Dit heeft
Jaarverslag Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht
 Jaarverslag 2015 Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht INHOUD Voorwoord van de voorzitter blz. 3 Samenvatting blz. 4 Summary blz. 5 Inleiding blz. 6 Hoofdstuk 1. Samenstelling
Jaarverslag 2015 Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht INHOUD Voorwoord van de voorzitter blz. 3 Samenvatting blz. 4 Summary blz. 5 Inleiding blz. 6 Hoofdstuk 1. Samenstelling
Jaarverslag 2014. METC Máxima Medisch Centrum
 Jaarverslag 2014 METC Máxima Medisch Centrum Inhoud Voorwoord p. 3 Inleiding p. 3 Bevoegd gezag METC p. 4 Samenstelling commissie p. 4 Samenstelling secretariaat p. 4 Werkwijze commissie p. 5 Samenvatting
Jaarverslag 2014 METC Máxima Medisch Centrum Inhoud Voorwoord p. 3 Inleiding p. 3 Bevoegd gezag METC p. 4 Samenstelling commissie p. 4 Samenstelling secretariaat p. 4 Werkwijze commissie p. 5 Samenvatting
METC MMC Jaarverslag 2018
 METC MMC Jaarverslag 2018 Inhoudsopgave Voorwoord p. 3 Inleiding p. 3 Onderwerpen 2018 p. 3 Activiteiten 2018 p. 3 Bevoegd gezag METC p. 4 Samenstelling commissie p. 4 Mutaties 2018 p. 4 Samenstelling
METC MMC Jaarverslag 2018 Inhoudsopgave Voorwoord p. 3 Inleiding p. 3 Onderwerpen 2018 p. 3 Activiteiten 2018 p. 3 Bevoegd gezag METC p. 4 Samenstelling commissie p. 4 Mutaties 2018 p. 4 Samenstelling
Bijlage 2 bij het Convenant PSI Samenstelling en werkwijze toetsingscommissie
 Bijlage 2 bij het Convenant PSI Samenstelling en werkwijze toetsingscommissie 1. Samenstelling toetsingscommissie De kerncommissie betstaat uit leden met ten minste de volgende specialismes 1 : Arts of
Bijlage 2 bij het Convenant PSI Samenstelling en werkwijze toetsingscommissie 1. Samenstelling toetsingscommissie De kerncommissie betstaat uit leden met ten minste de volgende specialismes 1 : Arts of
Bijgaand ontvangt u het primaire besluit van de commissie over het hierna vermelde onderzoek.
 Medisch :' i < r. c Toetsingscommissie Noord-Holland t AMC Orthopedie A.J. Kievit Staalmeesterslaan 271 1057 NZ Amsterdam datum kenmerk METC- registratie CCMO-registratie EudraCTnummer 30 oktober 2012
Medisch :' i < r. c Toetsingscommissie Noord-Holland t AMC Orthopedie A.J. Kievit Staalmeesterslaan 271 1057 NZ Amsterdam datum kenmerk METC- registratie CCMO-registratie EudraCTnummer 30 oktober 2012
JAARVERSLAG MEDISCH ETHISCHE TOETSINGSCOMMISSIE
 JAARVERSLAG 2015 MEDISCH ETHISCHE TOETSINGSCOMMISSIE Inhoudsopgave Pag. Voorwoord 2 1. Positionering 3 1.1 Plaats in de organisatie 1.2 Regionale samenwerking 3 3 2. Samenstelling van de Commissie 4 3.
JAARVERSLAG 2015 MEDISCH ETHISCHE TOETSINGSCOMMISSIE Inhoudsopgave Pag. Voorwoord 2 1. Positionering 3 1.1 Plaats in de organisatie 1.2 Regionale samenwerking 3 3 2. Samenstelling van de Commissie 4 3.
INHOUDSOPGAVE. Vooruitblik 2016 p. 11. Bijlagen: 1. Gebruikte afkortingen p Colofon p. 13. Jaarverslag 2015 METC MMC
 INHOUDSOPGAVE Voorwoord p. 3 Inleiding p. 3 Onderwerpen 2015 p. 4 Bevoegd gezag METC p. 4 Samenstelling commissie p. 5 Mutaties 2015 p. 5 Samenstelling en wijziging secretariaat p. 6 Werkwijze METC p.
INHOUDSOPGAVE Voorwoord p. 3 Inleiding p. 3 Onderwerpen 2015 p. 4 Bevoegd gezag METC p. 4 Samenstelling commissie p. 5 Mutaties 2015 p. 5 Samenstelling en wijziging secretariaat p. 6 Werkwijze METC p.
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL5 Protocolamendement (lokaal) Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: VL5 Protocolamendement (lokaal) Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Algemeen Plaats in de organisatie Regionale samenwerking Samenstelling van de Commissie Werkwijze 6
 Inhoudsopgave Algemeen 2 Pag. 1. Positionering 1.1 Plaats in de organisatie 3 1.2 Regionale samenwerking 3 2. Samenstelling van de Commissie 4 3. Werkwijze 6 4. Beoordeling medisch wetenschappelijk onderzoek
Inhoudsopgave Algemeen 2 Pag. 1. Positionering 1.1 Plaats in de organisatie 3 1.2 Regionale samenwerking 3 2. Samenstelling van de Commissie 4 3. Werkwijze 6 4. Beoordeling medisch wetenschappelijk onderzoek
METC MMC Jaarverslag 2017
 METC MMC Jaarverslag 2017 Inhoudsopgave Voorwoord p. 3 Inleiding p. 3 Onderwerpen 2017 p. 3 Activiteiten 2017 p. 4 Bevoegd gezag METC p. 4 Samenstelling commissie p. 4 Mutaties 2017 p. 5 Samenstelling
METC MMC Jaarverslag 2017 Inhoudsopgave Voorwoord p. 3 Inleiding p. 3 Onderwerpen 2017 p. 3 Activiteiten 2017 p. 4 Bevoegd gezag METC p. 4 Samenstelling commissie p. 4 Mutaties 2017 p. 5 Samenstelling
JAARVERSLAG 2016 METC
 JAARVERSLAG 2016 METC INHOUDSOPGAVE Voorwoord p. 3 Inleiding p. 3 Toetsing van geneesmiddelenonderzoek p. 3 Onderwerpen 2016 p. 3 Bevoegd gezag METC p. 4 Samenstelling commissie p. 4 Mutaties 2016 p. 4
JAARVERSLAG 2016 METC INHOUDSOPGAVE Voorwoord p. 3 Inleiding p. 3 Toetsing van geneesmiddelenonderzoek p. 3 Onderwerpen 2016 p. 3 Bevoegd gezag METC p. 4 Samenstelling commissie p. 4 Mutaties 2016 p. 4
Toetsingskader nwmo. Denkmodel. Niet-interventioneel onderzoek. Toetsen?! Welk probleem lossen we precies op?
 Niet-interventioneel onderzoek ( niet WMO ) Toetsen?! Kit Roes Voorzitter stuurgroep Implementatie Toetsingkader nwmo Directeur Kwaliteit en Patiëntveiligheid UMC Utrecht NFU Platform Klinisch Onderzoek
Niet-interventioneel onderzoek ( niet WMO ) Toetsen?! Kit Roes Voorzitter stuurgroep Implementatie Toetsingkader nwmo Directeur Kwaliteit en Patiëntveiligheid UMC Utrecht NFU Platform Klinisch Onderzoek
Europese verordening klinische proeven. Harrie Storms (VWS)
 Europese verordening klinische proeven Harrie Storms (VWS) 1 Veranderingen EU verordening Indiening via EU-portal (nationale studies en multinationale studies) Centrale beoordeling van multinationaal onderzoek
Europese verordening klinische proeven Harrie Storms (VWS) 1 Veranderingen EU verordening Indiening via EU-portal (nationale studies en multinationale studies) Centrale beoordeling van multinationaal onderzoek
Jaarverslag Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht
 Jaarverslag 2014 Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht INHOUD Voorwoord van de voorzitter blz. 3 Samenvatting blz. 4 Summary blz. 5 Hoofdstuk 1. Samenstelling commissie
Jaarverslag 2014 Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht INHOUD Voorwoord van de voorzitter blz. 3 Samenvatting blz. 4 Summary blz. 5 Hoofdstuk 1. Samenstelling commissie
Wetenschappelijke Commissie
 Taken en Werkwijze DPCG Wetenschappelijke Commissie Versie 09.04.2018 Inhoud 1. Begripsbepalingen 2. Taken Wetenschappelijke Commissie 3. Samenstelling Wetenschappelijke Commissie 4. Vergaderingen van
Taken en Werkwijze DPCG Wetenschappelijke Commissie Versie 09.04.2018 Inhoud 1. Begripsbepalingen 2. Taken Wetenschappelijke Commissie 3. Samenstelling Wetenschappelijke Commissie 4. Vergaderingen van
MDR (2017/745) en klinisch onderzoek - Implementatie in Nederland -
 MDR (2017/745) en klinisch onderzoek - Implementatie in Nederland - DCRF 26 september 2018 Monique Al Teamcoördinator Landelijk Bureau CCMO MDR: Drie hoofdcategoriën klinisch onderzoek I II III Klinisch
MDR (2017/745) en klinisch onderzoek - Implementatie in Nederland - DCRF 26 september 2018 Monique Al Teamcoördinator Landelijk Bureau CCMO MDR: Drie hoofdcategoriën klinisch onderzoek I II III Klinisch
Actuele ontwikkelingen ten aanzien van toetsen van medisch-wetenschappelijk onderzoek met mensen
 Actuele ontwikkelingen ten aanzien van toetsen van medisch-wetenschappelijk onderzoek met mensen NVMETC scholingsdagen 2017 Monique Al Sr wetenschappelijk stafmedewerker CCMO Ontwikkelingen wetgeving 1.
Actuele ontwikkelingen ten aanzien van toetsen van medisch-wetenschappelijk onderzoek met mensen NVMETC scholingsdagen 2017 Monique Al Sr wetenschappelijk stafmedewerker CCMO Ontwikkelingen wetgeving 1.
MEDISCH ETHISCHE TOETSINGSCOMMISSIE
 MEDISCH ETHISCHE TOETSINGSCOMMISSIE UMC UTRECHT JAARVERSLAG 2008 Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht Huispostnummer D 01.343 Postbus 85500 3508 GA Utrecht Telefoon:
MEDISCH ETHISCHE TOETSINGSCOMMISSIE UMC UTRECHT JAARVERSLAG 2008 Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht Huispostnummer D 01.343 Postbus 85500 3508 GA Utrecht Telefoon:
Jaarverslag 2012 Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht
 Jaarverslag 2012 Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht ii Jaarverslag 2012 Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht iii Colofon Redactie
Jaarverslag 2012 Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht ii Jaarverslag 2012 Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht iii Colofon Redactie
adresgegevens postadres CMO Regio Arnhem-Nijmegen P/a UMC St Radboud Huispostnummer 578 Postbus HB Nijmegen
 Commissie Mensgebonden Onderzoek jaarverslag 2013 adresgegevens postadres CMO Regio Arnhem-Nijmegen P/a UMC St Radboud Huispostnummer 578 Postbus 9101 6500 HB Nijmegen bezoekadres CMO Regio Arnhem-Nijmegen
Commissie Mensgebonden Onderzoek jaarverslag 2013 adresgegevens postadres CMO Regio Arnhem-Nijmegen P/a UMC St Radboud Huispostnummer 578 Postbus 9101 6500 HB Nijmegen bezoekadres CMO Regio Arnhem-Nijmegen
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek
 Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
Aanmelden medischwetenschappelijk
 Aanmelden medischwetenschappelijk onderzoek SOP Aanmelden WMO-plichtig onderzoek_versie juli 2016.doc Pagina 1 van 10 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd
Aanmelden medischwetenschappelijk onderzoek SOP Aanmelden WMO-plichtig onderzoek_versie juli 2016.doc Pagina 1 van 10 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd
Jouw GCP up-to-date in 45 minuten. Marieke Meulemans, oprichter GCP Central
 Jouw GCP up-to-date in 45 minuten Marieke Meulemans, oprichter GCP Central Waarom een GCP update tijdens de CRA dag? Gedreven Meesterschap. Meesterschap is vakmanschap. Vakmanschap is beheersing van het
Jouw GCP up-to-date in 45 minuten Marieke Meulemans, oprichter GCP Central Waarom een GCP update tijdens de CRA dag? Gedreven Meesterschap. Meesterschap is vakmanschap. Vakmanschap is beheersing van het
Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis. Procedure niet-wmo-plichtig klinisch wetenschappelijk onderzoek
 Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure niet-wmo-plichtig klinisch wetenschappelijk onderzoek Deze procedure geldt voor niet-wmo-plichtig onderzoek dat of: a) enkel
Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure niet-wmo-plichtig klinisch wetenschappelijk onderzoek Deze procedure geldt voor niet-wmo-plichtig onderzoek dat of: a) enkel
website www.nvmetc.nl
 Verslag NVMETC secretarissenoverleg 19 juni 2014 1. Opening en vaststelling agenda Dhr. Davids geeft aan, dat een belangrijke reden van dit secretarissenoverleg is, dat we van elkaar horen wat er speelt
Verslag NVMETC secretarissenoverleg 19 juni 2014 1. Opening en vaststelling agenda Dhr. Davids geeft aan, dat een belangrijke reden van dit secretarissenoverleg is, dat we van elkaar horen wat er speelt
Inhoud onderzoeksdossier
 Inhoud onderzoeksdossier (documenten in de witte box zijn nodig voor de primaire beoordeling) A. Brieven B. Formulieren C. Onderzoeksprotocol en protocolamendementen D. Productinformatie E. Informatie
Inhoud onderzoeksdossier (documenten in de witte box zijn nodig voor de primaire beoordeling) A. Brieven B. Formulieren C. Onderzoeksprotocol en protocolamendementen D. Productinformatie E. Informatie
Formulier Voortgangsrapportage
 Formulier Voortgangsrapportage De METC azm/um wil van al het door haar beoordeelde WMO-onderzoek jaarlijks een voortgangsrapportage zien. Zij heeft deze eis daartoe opgenomen in de tekst van haar eigen
Formulier Voortgangsrapportage De METC azm/um wil van al het door haar beoordeelde WMO-onderzoek jaarlijks een voortgangsrapportage zien. Zij heeft deze eis daartoe opgenomen in de tekst van haar eigen
JAARVERSLAG MEDISCH ETHISCHE TOETSINGSCOMMISSIE
 JAARVERSLAG 2016 MEDISCH ETHISCHE TOETSINGSCOMMISSIE Inhoudsopgave Pag. Voorwoord 2 1. Positionering 3 1.1 Plaats in de organisatie 1.2 Regionale samenwerking 3 3 2. Samenstelling van de Commissie 4 3.
JAARVERSLAG 2016 MEDISCH ETHISCHE TOETSINGSCOMMISSIE Inhoudsopgave Pag. Voorwoord 2 1. Positionering 3 1.1 Plaats in de organisatie 1.2 Regionale samenwerking 3 3 2. Samenstelling van de Commissie 4 3.
Ik onderschrijf het advies van de Commissie Bevolkingsonderzoek.
 Gezondheidsraad Health Council of the Netherlands Aan de minister van Volksgezondheid, Welzijn en Sport Onderwerp : Briefadvies Amendement DENSE-studie Uw kenmerk : 701406-129805-PG Ons kenmerk : I-1611/JB/pm/894-O1
Gezondheidsraad Health Council of the Netherlands Aan de minister van Volksgezondheid, Welzijn en Sport Onderwerp : Briefadvies Amendement DENSE-studie Uw kenmerk : 701406-129805-PG Ons kenmerk : I-1611/JB/pm/894-O1
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen. Farmaceutische Bedrijven Deelteam Klinisch Onderzoek
 Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
 ------------------------------------------------------------------------------------------------------------------------------------------- Concept Procedure Lokale Haalbaarheid klinisch geneesmiddelenonderzoek
------------------------------------------------------------------------------------------------------------------------------------------- Concept Procedure Lokale Haalbaarheid klinisch geneesmiddelenonderzoek
IRB Nijmegen. I R B N ij m egen. Independent Review Board Nijmegen JAARVERSLAG Independent Review Board Nijmegen
 Independent Review Board Nijmegen JAARVERSLAG 6 IRB Nijmegen Independent Review Board Nijmegen Medisch-Ethische ToetsingsCommissie voor Medisch Wetenschappelijk Onderzoek Mei 7 Jaarverslag metc IRB Nijmegen
Independent Review Board Nijmegen JAARVERSLAG 6 IRB Nijmegen Independent Review Board Nijmegen Medisch-Ethische ToetsingsCommissie voor Medisch Wetenschappelijk Onderzoek Mei 7 Jaarverslag metc IRB Nijmegen
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VC8 Beoordeling amendement toetsende commissie (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure STZ SOP: VC8 Beoordeling amendement toetsende commissie (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik
 EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek
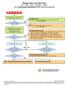 Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek Melding voorval proefpersoon aan onderzoeker/arts 1 Rapportage voorval door onderzoeker/arts in patiëntenstatus
Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek Melding voorval proefpersoon aan onderzoeker/arts 1 Rapportage voorval door onderzoeker/arts in patiëntenstatus
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VC9 Proefpersonen- en aansprakelijkheidsverzekering (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure STZ SOP: VC9 Proefpersonen- en aansprakelijkheidsverzekering (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Cijfers jaarverslag CCMO 2015
 Cijfers jaarverslag CCMO 2015 Bron ToetsingOnline Peildatum 19 januari 2016 Sortering 2015 De commissies zijn gerangschikt naar het aantal besluiten dat zij over 2015 namen De cijfers Aan de in het Excel
Cijfers jaarverslag CCMO 2015 Bron ToetsingOnline Peildatum 19 januari 2016 Sortering 2015 De commissies zijn gerangschikt naar het aantal besluiten dat zij over 2015 namen De cijfers Aan de in het Excel
Reglement Wetenschapscommissie Medisch Centrum Haaglanden
 Reglement Wetenschapscommissie Medisch Centrum Haaglanden 1 Inhoudsopgave 1. Begripsbepalingen 2. Taakopdracht 3. Samenstelling commissie, benoeming en zittingduur 4. Werkwijze en besluitvorming 5. Taken
Reglement Wetenschapscommissie Medisch Centrum Haaglanden 1 Inhoudsopgave 1. Begripsbepalingen 2. Taakopdracht 3. Samenstelling commissie, benoeming en zittingduur 4. Werkwijze en besluitvorming 5. Taken
Op naar het snel opstarten van klinisch onderzoek in Nederland!
 Op naar het snel opstarten van klinisch onderzoek in Nederland! Marika Trieling Voorzitter DCRF werkgroep Lokale uitvoerbaarheid 12 februari 2019 Wat is er in Nederland nodig? Verkorten tijdslijnen van
Op naar het snel opstarten van klinisch onderzoek in Nederland! Marika Trieling Voorzitter DCRF werkgroep Lokale uitvoerbaarheid 12 februari 2019 Wat is er in Nederland nodig? Verkorten tijdslijnen van
Kwaliteitsborging onderzoek in het. NVMETC bijeenkomst 23 november UMC Utrecht. Oktober 2016
 1 Kwaliteitsborging onderzoek in het UMC Utrecht NVMETC bijeenkomst 23 november 2016 Eugenie Ram, kwaliteitsmanager Onderzoek - Office Concernstaf Raad van Bestuur Oktober 2016 UMC Utrecht breed kwaliteitssysteem
1 Kwaliteitsborging onderzoek in het UMC Utrecht NVMETC bijeenkomst 23 november 2016 Eugenie Ram, kwaliteitsmanager Onderzoek - Office Concernstaf Raad van Bestuur Oktober 2016 UMC Utrecht breed kwaliteitssysteem
Toetsingskader nwmo. Peggy Manders 4 november 2016 Symposium V&VN Research Professionals
 Toetsingskader nwmo Peggy Manders 4 november 2016 Symposium V&VN Research Professionals Biobank: definitie en rationale Wat is een biobank? + + Waarom een biobank starten? Verbeteren gezondheidszorg voor
Toetsingskader nwmo Peggy Manders 4 november 2016 Symposium V&VN Research Professionals Biobank: definitie en rationale Wat is een biobank? + + Waarom een biobank starten? Verbeteren gezondheidszorg voor
JAARVERSLAG MEDISCH ETHISCHE TOETSINGSCOMMISSIE
 JAARVERSLAG 2018 MEDISCH ETHISCHE TOETSINGSCOMMISSIE Inhoudsopgave Pag. Voorwoord 2 1. Positionering 1.1 Plaats in de organisatie 1.2 Interne organisatie: administratie en gegevensbescherming / doorlooptijden
JAARVERSLAG 2018 MEDISCH ETHISCHE TOETSINGSCOMMISSIE Inhoudsopgave Pag. Voorwoord 2 1. Positionering 1.1 Plaats in de organisatie 1.2 Interne organisatie: administratie en gegevensbescherming / doorlooptijden
Praktisch: Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis. Procedure niet-wmo-plichtig klinisch wetenschappelijk onderzoek
 Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure niet-wmo-plichtig klinisch wetenschappelijk onderzoek Deze procedure geldt voor niet-wmo-plichtig onderzoek dat of: a) enkel
Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure niet-wmo-plichtig klinisch wetenschappelijk onderzoek Deze procedure geldt voor niet-wmo-plichtig onderzoek dat of: a) enkel
AMC Uitvoeringsrichtlijnen: Goedkeuring medisch-wetenschappelijk onderzoek door de Raad van Bestuur
 AMC Uitvoeringsrichtlijnen: Goedkeuring medisch-wetenschappelijk onderzoek door de Raad van Bestuur en Deelname van personeelsleden en studenten aan medisch-wetenschappelijk onderzoek Versie 1.1 Dit document
AMC Uitvoeringsrichtlijnen: Goedkeuring medisch-wetenschappelijk onderzoek door de Raad van Bestuur en Deelname van personeelsleden en studenten aan medisch-wetenschappelijk onderzoek Versie 1.1 Dit document
 ------------------------------------------------------------------------------------------------------------------------------------------- Tweede concept van de Procedure Lokale Haalbaarheid klinisch
------------------------------------------------------------------------------------------------------------------------------------------- Tweede concept van de Procedure Lokale Haalbaarheid klinisch
Rapport Institutioneel Onderzoek
 Rapport Institutioneel Onderzoek Beleidsterrein patiëntenbeleid / Wet medisch-wetenschappelijk onderzoek met mensen Behorend bij het Basisselectiedocument voor de neerslag van de handelingen van de Medisch
Rapport Institutioneel Onderzoek Beleidsterrein patiëntenbeleid / Wet medisch-wetenschappelijk onderzoek met mensen Behorend bij het Basisselectiedocument voor de neerslag van de handelingen van de Medisch
Concept procedure Lokale Haalbaarheid
 -------------------------------------------------------------------------------------------------------------------------------------------- Opzet pilot Stap 2 Lokale Haalbaarheid ter voorbereiding op
-------------------------------------------------------------------------------------------------------------------------------------------- Opzet pilot Stap 2 Lokale Haalbaarheid ter voorbereiding op
European Clinical Trial Regulation: Kans voor Nederland
 European Clinical Trial Regulation: Kans voor Nederland Annelies van Woudenberg, 13 november 2017 European Clinical Trial Regulation 536/ 2014 EU Verordening betreffende klinische proeven met geneesmiddelen
European Clinical Trial Regulation: Kans voor Nederland Annelies van Woudenberg, 13 november 2017 European Clinical Trial Regulation 536/ 2014 EU Verordening betreffende klinische proeven met geneesmiddelen
nwmo toetsingskader Eveline Loriaux projectleider 4 oktober 2017 Jaarcongres DCRF
 nwmo toetsingskader Eveline Loriaux projectleider 4 oktober 2017 Jaarcongres DCRF Zien we door de bomen nog het bos? nwmo Toetsingskader Overzicht Start: juli 2015 In 2017 zijn 39 aanvragen ingediend
nwmo toetsingskader Eveline Loriaux projectleider 4 oktober 2017 Jaarcongres DCRF Zien we door de bomen nog het bos? nwmo Toetsingskader Overzicht Start: juli 2015 In 2017 zijn 39 aanvragen ingediend
MEDISCH ETHISCHE TOETSINGSCOMMISSIE UMC UTRECHT JAARVERSLAG 2009
 MEDISCH ETHISCHE TOETSINGSCOMMISSIE UMC UTRECHT JAARVERSLAG 2009 Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht Huispostnummer D 01.343 Postbus 85500 3508 GA Utrecht Telefoon:
MEDISCH ETHISCHE TOETSINGSCOMMISSIE UMC UTRECHT JAARVERSLAG 2009 Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht Huispostnummer D 01.343 Postbus 85500 3508 GA Utrecht Telefoon:
De laatste versie van dit document is te downloaden op: www.umcutrecht.nl/metc. Indienen documenten bij de METC UMC Utrecht
 Indienen documenten bij de METC UMC Utrecht Begin hier Bekijk in onderstaande tabel wat u wilt indienen. Kijk daarna welke methode van indiening en welke documenten bij uw indiening horen. Volg bij het
Indienen documenten bij de METC UMC Utrecht Begin hier Bekijk in onderstaande tabel wat u wilt indienen. Kijk daarna welke methode van indiening en welke documenten bij uw indiening horen. Volg bij het
Handleiding. Investigational Medicinal Product Dossier (IMPD)
 Handleiding Investigational Medicinal Product Dossier (IMPD) Inhoudsopgave Afkortingen... - 3 - Wat is het IMPD?... - 4 - Beslisschema inhoud IMPD... - 5 - Beschrijving inhoud IMPD... - 6 - Overzicht hoofdstukken
Handleiding Investigational Medicinal Product Dossier (IMPD) Inhoudsopgave Afkortingen... - 3 - Wat is het IMPD?... - 4 - Beslisschema inhoud IMPD... - 5 - Beschrijving inhoud IMPD... - 6 - Overzicht hoofdstukken
Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen
 Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen Afdeling Farmaceutische Bedrijven, Klinisch Onderzoek Good Clinical Practice Inhoud Wat doet de IGJ aan toezicht op klinisch
Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen Afdeling Farmaceutische Bedrijven, Klinisch Onderzoek Good Clinical Practice Inhoud Wat doet de IGJ aan toezicht op klinisch
Modelreglement METC s
 Modelreglement METC s CONSIDERANS De medisch-ethische toetsingscommissie als bedoeld in artikel 16, eerste lid, van de Wet medischwetenschappelijk onderzoek met mensen van 26 februari 1998, Stb 1998 161,
Modelreglement METC s CONSIDERANS De medisch-ethische toetsingscommissie als bedoeld in artikel 16, eerste lid, van de Wet medischwetenschappelijk onderzoek met mensen van 26 februari 1998, Stb 1998 161,
Toenemende vraag naar nwmo studies Kwaliteit en transparantie voorop
 Beterdan Toenemende vraag naar nwmo studies Kwaliteit en transparantie voorop Joke Eggermont, Medisch Directeur Bristol-Myers Squibb Voorzitter Nefarma projectgroep niet-wmo plichtig onderzoek 1 Waarom?
Beterdan Toenemende vraag naar nwmo studies Kwaliteit en transparantie voorop Joke Eggermont, Medisch Directeur Bristol-Myers Squibb Voorzitter Nefarma projectgroep niet-wmo plichtig onderzoek 1 Waarom?
Veel gestelde vragen Medisch-wetenschappelijk onderzoek met medische hulpmiddelen 1
 Veel gestelde vragen Medisch-wetenschappelijk onderzoek met medische hulpmiddelen 1 1. Wat is een medisch hulpmiddel? De wettelijke definitie 2 van een medisch hulpmiddel luidt: Een medisch hulpmiddel
Veel gestelde vragen Medisch-wetenschappelijk onderzoek met medische hulpmiddelen 1 1. Wat is een medisch hulpmiddel? De wettelijke definitie 2 van een medisch hulpmiddel luidt: Een medisch hulpmiddel
Impact van de ECTR en hoe zorgen we dat NL als beste uit de bus komt. Annelies van Woudenberg, ACRON Najaarsvergadering, 2 november 2016
 Impact van de ECTR en hoe zorgen we dat NL als beste uit de bus komt Annelies van Woudenberg, ACRON Najaarsvergadering, 2 november 2016 2 Dutch Clinical Research Foundation (DCRF) European Clinical Trial
Impact van de ECTR en hoe zorgen we dat NL als beste uit de bus komt Annelies van Woudenberg, ACRON Najaarsvergadering, 2 november 2016 2 Dutch Clinical Research Foundation (DCRF) European Clinical Trial
Addendum Procedure Wetenschappelijke aanvragen DHBA
 Addendum Procedure Wetenschappelijke aanvragen DHBA De DHBA wetenschappelijke commissie beoordeelt studievoorstellen met gebruik van bestaande DHBA data, en coördineert verschillende wetenschappelijke
Addendum Procedure Wetenschappelijke aanvragen DHBA De DHBA wetenschappelijke commissie beoordeelt studievoorstellen met gebruik van bestaande DHBA data, en coördineert verschillende wetenschappelijke
Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814.
 STAATSCOURANT Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814. Nr. 20221 17 juli 2015 Regeling van de Minister van Volksgezondheid, Welzijn en Sport van 9 juli 2015, houdende regels voor
STAATSCOURANT Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814. Nr. 20221 17 juli 2015 Regeling van de Minister van Volksgezondheid, Welzijn en Sport van 9 juli 2015, houdende regels voor
Jaarverslag. medisch-ethische toetsingscommissie (METC) azm/um
 Jaarverslag medisch-ethische toetsingscommissie (METC) azm/um 2018 Inhoudsopgave Voorwoord 3 Samenvatting (Nederlands en Engels) 5 1. Algemene informatie 6 1.1 Bevoegd gezag METC 6 1.2 Samenstelling commissie
Jaarverslag medisch-ethische toetsingscommissie (METC) azm/um 2018 Inhoudsopgave Voorwoord 3 Samenvatting (Nederlands en Engels) 5 1. Algemene informatie 6 1.1 Bevoegd gezag METC 6 1.2 Samenstelling commissie
European Clinical Trial Regulation: Kans voor Nederland. Annelies van Woudenberg, ClinOps-dag NVFG, 20 april 2017
 European Clinical Trial Regulation: Kans voor Nederland Annelies van Woudenberg, ClinOps-dag NVFG, 20 april 2017 2 Dutch Clinical Research Foundation (DCRF) Doel ECTR project In oktober 2018 is Nederland
European Clinical Trial Regulation: Kans voor Nederland Annelies van Woudenberg, ClinOps-dag NVFG, 20 april 2017 2 Dutch Clinical Research Foundation (DCRF) Doel ECTR project In oktober 2018 is Nederland
CCMO op 22 oktober 2015;
 Versie 7, goedgekeurd door METC AVL op 25 november CCMO op 22 oktober 2015; door RvB op 15 maart 2016 en door REGLEMENT VAN DE MEDISCHE-ETHISCHE TOETSINGSCOMMISSIE (METC) VAN STICHTING NEDERLANDS KANKERINSTITUUT
Versie 7, goedgekeurd door METC AVL op 25 november CCMO op 22 oktober 2015; door RvB op 15 maart 2016 en door REGLEMENT VAN DE MEDISCHE-ETHISCHE TOETSINGSCOMMISSIE (METC) VAN STICHTING NEDERLANDS KANKERINSTITUUT
Klachtencommissie Jaarverslag Stichting Cardiologie Centra Nederland
 Klachtencommissie Jaarverslag 2013 Stichting Inhoud 1 Voorwoord... 2 2 Samenstelling van de commissie... 2 3 Registratie & rapportage... 2 4 Gegevens over de klachtenbehandeling... 3 5 Onderwerp van de
Klachtencommissie Jaarverslag 2013 Stichting Inhoud 1 Voorwoord... 2 2 Samenstelling van de commissie... 2 3 Registratie & rapportage... 2 4 Gegevens over de klachtenbehandeling... 3 5 Onderwerp van de
Kenmerk: V /R17.001/dj/ld Datum:
 Meander Medisch Centrum T.a.v. dr. P.H.G. Hogeman, kinderarts Postbus 1502 3800 BM AMERSFOORT Kenmerk: V.112232/R17.001/dj/ld Datum: 7-8-2017 Betreft: besluit NL59723.100.16 R17.001/PREP cariesrisk Geachte
Meander Medisch Centrum T.a.v. dr. P.H.G. Hogeman, kinderarts Postbus 1502 3800 BM AMERSFOORT Kenmerk: V.112232/R17.001/dj/ld Datum: 7-8-2017 Betreft: besluit NL59723.100.16 R17.001/PREP cariesrisk Geachte
Vragen en antwoorden over de gegevenssectie van de model-pif
 Vragen en antwoorden over de gegevenssectie van de model-pif Algemene informatie over de Algemene Verordening Gegevensbescherming Waar vind ik algemene informatie over de gevolgen van de Algemene Verordening
Vragen en antwoorden over de gegevenssectie van de model-pif Algemene informatie over de Algemene Verordening Gegevensbescherming Waar vind ik algemene informatie over de gevolgen van de Algemene Verordening
Aanmelden WMO-plichtig onderzoek
 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd wordt bij het aanmelden van onderzoek dat onder de WMO valt en waarbij ZGV optreedt als deelnemend centrum. Voordat
Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd wordt bij het aanmelden van onderzoek dat onder de WMO valt en waarbij ZGV optreedt als deelnemend centrum. Voordat
MEDISCH ETHISCHE TOETSINGSCOMMISSIE UMC UTRECHT JAARVERSLAG 2010
 MEDISCH ETHISCHE TOETSINGSCOMMISSIE UMC UTRECHT JAARVERSLAG 2010 Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht Huispostnummer D 01.343 Postbus 85500 3508 GA Utrecht Telefoon:
MEDISCH ETHISCHE TOETSINGSCOMMISSIE UMC UTRECHT JAARVERSLAG 2010 Medisch Ethische Toetsingscommissie Universitair Medisch Centrum Utrecht Huispostnummer D 01.343 Postbus 85500 3508 GA Utrecht Telefoon:
Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814.
 STAATSCOURANT Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814. Nr. 3583 24 januari 2017 Richtlijn van de Centrale Commissie Mensgebonden Onderzoek, de CCMO, krachtens artikel 24 van de
STAATSCOURANT Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814. Nr. 3583 24 januari 2017 Richtlijn van de Centrale Commissie Mensgebonden Onderzoek, de CCMO, krachtens artikel 24 van de
Derde evaluatie van de WMO
 Derde evaluatie van de WMO Belangrijkste conclusies en aanbevelingen Nicolette Woestenburg Corrette Ploem Sjef Gevers Voorjaarsbijeenkomst, NVMETC 6 juni 2018 Opdrachtgever: ministerie van VWS/ZonMw Onderzoekers
Derde evaluatie van de WMO Belangrijkste conclusies en aanbevelingen Nicolette Woestenburg Corrette Ploem Sjef Gevers Voorjaarsbijeenkomst, NVMETC 6 juni 2018 Opdrachtgever: ministerie van VWS/ZonMw Onderzoekers
European Clinical Trial Regulation: Kans voor Nederland
 European Clinical Trial Regulation: Kans voor Nederland Annelies van Woudenberg, 14 november 2018 ECTR-project NL CCMO, DCRF en VWS: samenwerking bij implementatie ECTR Doel: als verordening van kracht
European Clinical Trial Regulation: Kans voor Nederland Annelies van Woudenberg, 14 november 2018 ECTR-project NL CCMO, DCRF en VWS: samenwerking bij implementatie ECTR Doel: als verordening van kracht
Officiële uitgave van het Koninkrijk der Nederlanden sinds Organisatie en Werkwijze Medisch Ethische Toetsingscommissies
 STAATSCOURANT Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814. Nr. 3243 7 februari 2014 Organisatie en Werkwijze Medisch Ethische Toetsingscommissies Richtlijn van de Centrale Commissie
STAATSCOURANT Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814. Nr. 3243 7 februari 2014 Organisatie en Werkwijze Medisch Ethische Toetsingscommissies Richtlijn van de Centrale Commissie
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL2 Aanpassen proefpersoneninformatie / toestemmingsformulier aan lokale situatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen
Standard Operating Procedure STZ SOP: VL2 Aanpassen proefpersoneninformatie / toestemmingsformulier aan lokale situatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen
Jaarverslag Commissie Medische Ethiek 2013
 Jaarverslag Commissie Medische Ethiek 2013 Bijgevoegd treft u aan het jaarverslag over 2013 van de Commissie Medische Ethiek van het Leids Universitair Medisch Centrum. De Commissie legt hiermee verantwoording
Jaarverslag Commissie Medische Ethiek 2013 Bijgevoegd treft u aan het jaarverslag over 2013 van de Commissie Medische Ethiek van het Leids Universitair Medisch Centrum. De Commissie legt hiermee verantwoording
JAARVERSLAG MEDISCH ETHISCHE TOETSINGSCOMMISSIE
 JAARVERSLAG 2017 MEDISCH ETHISCHE TOETSINGSCOMMISSIE Inhoudsopgave Pag. Voorwoord 2 1. Positionering 1.1 Plaats in de organisatie 1.2 Interne organisatie 1.3 Regionale samenwerking 3 2. Samenstelling van
JAARVERSLAG 2017 MEDISCH ETHISCHE TOETSINGSCOMMISSIE Inhoudsopgave Pag. Voorwoord 2 1. Positionering 1.1 Plaats in de organisatie 1.2 Interne organisatie 1.3 Regionale samenwerking 3 2. Samenstelling van
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U11 Voortgangsrapportage Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: U11 Voortgangsrapportage Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
nwmo toetsingskader Eveline Loriaux - projectleider Kennisatelier 10 mei 2017 Vereniging Innovatieve Geneesmiddelen
 nwmo toetsingskader Eveline Loriaux - projectleider Kennisatelier 10 mei 2017 Vereniging Innovatieve Geneesmiddelen Zien we door de bomen nog het bos? 1 Overzicht nwmo Toetsingskader Start: juli 2015 Sinds
nwmo toetsingskader Eveline Loriaux - projectleider Kennisatelier 10 mei 2017 Vereniging Innovatieve Geneesmiddelen Zien we door de bomen nog het bos? 1 Overzicht nwmo Toetsingskader Start: juli 2015 Sinds
Patiënteninformatieformulier imprint studie
 Patiënteninformatieformulier imprint studie (imaging of PSMA: Registratie en Inventarisatie voor Nederlandse Toepassing) Inleiding Uw arts heeft voorgesteld een aanvraag te doen voor een PSMA-PET-scan.
Patiënteninformatieformulier imprint studie (imaging of PSMA: Registratie en Inventarisatie voor Nederlandse Toepassing) Inleiding Uw arts heeft voorgesteld een aanvraag te doen voor een PSMA-PET-scan.
Jaarverslag. medisch-ethische toetsingscommissie (METC) azm/um
 Jaarverslag medisch-ethische toetsingscommissie (METC) azm/um 2017 Inhoudsopgave Voorwoord 3 Samenvatting (Nederlands en Engels) 5 1. Algemene informatie 6 1.1 Bevoegd gezag METC 6 1.2 Samenstelling commissie
Jaarverslag medisch-ethische toetsingscommissie (METC) azm/um 2017 Inhoudsopgave Voorwoord 3 Samenvatting (Nederlands en Engels) 5 1. Algemene informatie 6 1.1 Bevoegd gezag METC 6 1.2 Samenstelling commissie
Praktische implementatie Europese verordening Geneesmiddelen onderzoek
 Praktische implementatie Europese verordening Geneesmiddelen onderzoek Dr. Joost Keers Hoofd Wetenschappelijk Instituut j.keers@mzh.nl 050 524 5826 http://www.ccmo.nl/nl/europese-verordening Belangrijke
Praktische implementatie Europese verordening Geneesmiddelen onderzoek Dr. Joost Keers Hoofd Wetenschappelijk Instituut j.keers@mzh.nl 050 524 5826 http://www.ccmo.nl/nl/europese-verordening Belangrijke
Stichting VHAN. Reglement Wetenschapscommissie
 Stichting VHAN Reglement Wetenschapscommissie Aangepaste versie januari 2015 Inhoudsopgave 1. Begripsbepalingen 2. Taakopdracht 3. Samenstelling commissie, benoeming en zittingsduur 4. Werkwijze en besluitvorming
Stichting VHAN Reglement Wetenschapscommissie Aangepaste versie januari 2015 Inhoudsopgave 1. Begripsbepalingen 2. Taakopdracht 3. Samenstelling commissie, benoeming en zittingsduur 4. Werkwijze en besluitvorming
Verklaring van belangen
 Verklaring van belangen Reden voor invulling van dit formulier Ik verklaar hierbij dat er geen wijzigingen zijn te melden ten opzichte van de meest recente door mij ingevulde Verklaring van Belangen, waarvan
Verklaring van belangen Reden voor invulling van dit formulier Ik verklaar hierbij dat er geen wijzigingen zijn te melden ten opzichte van de meest recente door mij ingevulde Verklaring van Belangen, waarvan
JAARVERSLAG Dierexperimentencommissie Diergeneeskunde en Farmaceutische Wetenschappen, Scheikunde en Biologie (DEC-DGK/FSB)
 zs Univ«sïtcU Utrecht JAARVERSLAG 2006 Dierexperimentencommissie Diergeneeskunde en Farmaceutische Wetenschappen, Scheikunde en Biologie (DEC-DGK/FSB) Dierexperimentencommissie Diergeneeskunde en Farmaceutische
zs Univ«sïtcU Utrecht JAARVERSLAG 2006 Dierexperimentencommissie Diergeneeskunde en Farmaceutische Wetenschappen, Scheikunde en Biologie (DEC-DGK/FSB) Dierexperimentencommissie Diergeneeskunde en Farmaceutische
Actuele ontwikkelingen ten aanzien van toetsen van medisch-wetenschappelijk
 Actuele ontwikkelingen ten aanzien van toetsen van medisch-wetenschappelijk onderzoek met mensen NVMETC scholingsdagen 2016 Monique Al Sr wetenschappelijk stafmedewerker CCMO Ontwikkelingen wetgeving 1.
Actuele ontwikkelingen ten aanzien van toetsen van medisch-wetenschappelijk onderzoek met mensen NVMETC scholingsdagen 2016 Monique Al Sr wetenschappelijk stafmedewerker CCMO Ontwikkelingen wetgeving 1.
Onderzoek naar de gebruiksvriendelijkheid van de OLVG PIJN app
 Onderzoek naar de gebruiksvriendelijkheid van de OLVG PIJN app Engels: Proof of concept OLVG PAIN app. Betreft: Patiënten informatiebrief, onderzoek naar de gebruiksvriendelijkheid van de OLVG PIJN app
Onderzoek naar de gebruiksvriendelijkheid van de OLVG PIJN app Engels: Proof of concept OLVG PAIN app. Betreft: Patiënten informatiebrief, onderzoek naar de gebruiksvriendelijkheid van de OLVG PIJN app
Jaarverslag METC UMC Utrecht
 Jaarverslag 2011 METC UMC Utrecht 2 Inhoud Voorwoord pag 5 Samenvatting pag 7 Summary pag 8 1. Bevoegd gezag METC pag 10 2. Samenstelling commissie pag 10 3. Secretariaat pag 11 4. Werkwijze commissie
Jaarverslag 2011 METC UMC Utrecht 2 Inhoud Voorwoord pag 5 Samenvatting pag 7 Summary pag 8 1. Bevoegd gezag METC pag 10 2. Samenstelling commissie pag 10 3. Secretariaat pag 11 4. Werkwijze commissie
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: A1 Afsluiting studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Standard Operating Procedure STZ SOP: A1 Afsluiting studie Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen Versiedatum
Universitair Medisch Centrum. Dierexperimentencommissie Geneeskunde (DEC-GNK)
 Universitair Medisch Centrum utrecht JAARVERSLAG 2001 Dierexperimentencommissie Geneeskunde (DEC-GNK) Dierexperimentencommissie Geneeskunde UMC Utrecht, huispostnummer D 01,343, Postbus 85500, 3508 GA
Universitair Medisch Centrum utrecht JAARVERSLAG 2001 Dierexperimentencommissie Geneeskunde (DEC-GNK) Dierexperimentencommissie Geneeskunde UMC Utrecht, huispostnummer D 01,343, Postbus 85500, 3508 GA
Procedure deelnemend aan multicenter WMO-plichtig klinisch wetenschappelijk onderzoek
 Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure deelnemend aan multicenter WMO-plichtig klinisch wetenschappelijk onderzoek Bij dit type onderzoek neemt de onderzoeker van het
Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure deelnemend aan multicenter WMO-plichtig klinisch wetenschappelijk onderzoek Bij dit type onderzoek neemt de onderzoeker van het
SOP aanleveren en afhandelen WMO onderzoek METC Onze Lieve Vrouwe Gasthuis, versie 1, juli
 Aanmelden en afhandelen medisch-wetenschappelijk onderzoek met mensen (WMO-onderzoek) Medisch-ethische toetsingscommissie (METC) Onze Lieve Vrouwe Gasthuis Hieronder treft u aan de procedure van aanmelding
Aanmelden en afhandelen medisch-wetenschappelijk onderzoek met mensen (WMO-onderzoek) Medisch-ethische toetsingscommissie (METC) Onze Lieve Vrouwe Gasthuis Hieronder treft u aan de procedure van aanmelding
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Gemeente Gennep. Jaarverslag Commissie Bezwaarschriften Gennep 2016
 Gemeente Gennep Jaarverslag Commissie Bezwaarschriften Gennep 206 8-5-207 Inhoud Inleiding... 2. De commissie... 3. Instelling commissie... 3.2 Samenstelling van de commissie... 3.3 Vergaderfrequentie...
Gemeente Gennep Jaarverslag Commissie Bezwaarschriften Gennep 206 8-5-207 Inhoud Inleiding... 2. De commissie... 3. Instelling commissie... 3.2 Samenstelling van de commissie... 3.3 Vergaderfrequentie...
Jaarverslag Commissie Medische Ethiek 2014
 Jaarverslag Commissie Medische Ethiek 2014 Bijgevoegd treft u aan het jaarverslag over 2014 van de Commissie Medische Ethiek van het Leids Universitair Medisch Centrum. De Commissie legt hiermee verantwoording
Jaarverslag Commissie Medische Ethiek 2014 Bijgevoegd treft u aan het jaarverslag over 2014 van de Commissie Medische Ethiek van het Leids Universitair Medisch Centrum. De Commissie legt hiermee verantwoording
Jaarverslag Medisch Ethische Toetsingscommissie AMC
 Jaarverslag 2017 Medisch Ethische Toetsingscommissie AMC Voorwoord Voor u ligt het jaarverslag 2017 van de Medisch Ethische Toetsingscommissie van het AMC. De Wet medisch-wetenschappelijk onderzoek (WMO)
Jaarverslag 2017 Medisch Ethische Toetsingscommissie AMC Voorwoord Voor u ligt het jaarverslag 2017 van de Medisch Ethische Toetsingscommissie van het AMC. De Wet medisch-wetenschappelijk onderzoek (WMO)
Aan de minister van Volksgezondheid, Welzijn en Sport
 Gezondheidsraad H e a l t h C o u n c i l o f t h e N e t h e r l a n d s Aan de minister van Volksgezondheid, Welzijn en Sport Onderwerp : Briefadvies Amendement bij het onderzoek naar NIPT voor prenatale
Gezondheidsraad H e a l t h C o u n c i l o f t h e N e t h e r l a n d s Aan de minister van Volksgezondheid, Welzijn en Sport Onderwerp : Briefadvies Amendement bij het onderzoek naar NIPT voor prenatale
De ECTR: een kans voor Nederland! Annelies van Woudenberg, DCRF congres, 5 oktober 2016
 De ECTR: een kans voor Nederland! Annelies van Woudenberg, DCRF congres, 5 oktober 2016 European Clinical Trial Regulation 536/ 2014 European Clinical Trial Regulation (ECTR): EU Verordening betreffende
De ECTR: een kans voor Nederland! Annelies van Woudenberg, DCRF congres, 5 oktober 2016 European Clinical Trial Regulation 536/ 2014 European Clinical Trial Regulation (ECTR): EU Verordening betreffende
Wetenschappelijk onderzoek met Karakter
 Wetenschappelijk onderzoek met Karakter 1 Inleiding Karakter is als academisch centrum partner in een groot aantal multicenter studies. Voor het uitvoeren van uw onderzoek in samenwerking met Karakter
Wetenschappelijk onderzoek met Karakter 1 Inleiding Karakter is als academisch centrum partner in een groot aantal multicenter studies. Voor het uitvoeren van uw onderzoek in samenwerking met Karakter
