De laatste versie van dit document is te downloaden op: Indienen documenten bij de METC UMC Utrecht
|
|
|
- Elke van der Woude
- 8 jaren geleden
- Aantal bezoeken:
Transcriptie
1 Indienen documenten bij de METC UMC Utrecht Begin hier Bekijk in onderstaande tabel wat u wilt indienen. Kijk daarna welke methode van indiening en welke documenten bij uw indiening horen. Volg bij het gereed maken van de PDF bestanden voor uw indiening nauwkeurig de regels op pagina 3 van dit document. Let op: als documenten niet juist zijn ingediend of niet compleet zijn, dan kunnen we uw documenten niet in behandeling nemen. Alleen door correcte indiening kan (het ondersteunende personeel van) de METC uw aanvragen goed en tijdig verwerken. Bewaar altijd eigen kopieën van ingediende bestanden! Soort indiening Methode indiening Welke documenten Niet WMO plichtig onderzoek / verzoek om advies over WMOplichtigheid Amendement op niet WMO-plichtig onderzoek Nieuw dossier voor WMO toetsing, niet-geneesmiddelenonderzoek Nieuw dossier voor WMO toetsing, wél geneesmiddelenonderzoek Nieuw amendement bij aan de WMO getoetst niet-geneesmiddelen onderzoek Nieuw amendement bij aan de WMO getoetst wél geneesmiddelen onderzoek Toevoegen van centra bij multicenter onderzoek Reactie op vragen bij WMO toetsing (nieuwe dossiers en amendementen) Melding datum eerste inclusie proefpersoon (=startdatum 1.2 Geen ( volstaat) onderzoek) Voortgangsrapportage Veiligheidsmeldingen en (periodieke) veiligheidsrapportages Melding datum laatste onderzoekshandeling bij laatste proefpersoon (=einddatum) Eindresultaten (publicaties, samenvattingen, eindrapportage) METC UMC Utrecht, versiedatum
2 Sectie 1. Methode indiening 1.1 (indieningen voor toetsing aan de WMO) CD-ROM met papieren aanbiedingsbrief 1. Kies de juiste Model aanbiedingsbrief op de website van de METC (zie het kopje. 2. Deze invullen, uitprinten en volledig (laten) ondertekenen. 3. De aanbiedingsbrief en alle andere documenten in PDF formaat opslaan/scannen en voorzien van de juiste bestandsnamen (volg de regels en voorbeelden op pagina s 3 t/m 5 van dit document en gebruik in de bestandsnamen de juiste letter, nummer en benaming zoals staat voorgeschreven) 4. Alle PDF documenten met juiste bestandsnaam branden op een CD- ROM (svp geen mappen aanmaken op de CD-ROM en geen bestanden in andere bestandsformaten op de CD-ROM plaatsen). 5. CD-ROM en de papieren versie van de aanbiedingsbrief met originele handtekeningen samen per post versturen aan de METC. Postadres: UMC Utrecht T.a.v. Medisch Ethische Toetsings Commissie Huispost D Postbus GA Utrecht 1.2 (overige documenten) Per (of bij >8 MB per CD-ROM) 1. Alle documenten bij uw indiening in PDF formaat opslaan en voorzien van de juiste bestandsnamen (volg de regels en voorbeelden op pagina s 3 t/m 5 van dit document en gebruik in de bestandsnamen de juiste letter, nummer en benaming zoals staat voorgeschreven) 2. Zijn de PDF bestanden van uw indiening bij elkaar minder dan 8 MB groot? Dan als bijlagen bij een versturen aan metc@umcutrecht.nl. In de graag kort aangeven welk onderwerp uw indiening betreft en indien bekend het METC protocolnummer van het betreffende onderzoek vermelden. 3. Zijn de PDF bestanden van uw indiening bij elkaar meer dan 8 MB groot? Dan graag alle PDF documenten met juiste bestandsnaam branden op een CD-ROM (svp geen mappen aanmaken op de CD-ROM en geen bestanden in andere bestandsformaten op de CD-ROM plaatsen). Graag op de verpakking of in een begeleidende brief vermelden welk onderwerp de indiening op de CD-ROM betreft en indien bekend het METC protocolnummer van het betreffende onderzoek vermelden. Dan graag per post insturen (zie postadres hier boven bij 1.1). adres: metc@umcutrecht.nl METC UMC Utrecht, versiedatum
3 Sectie 2. Verplichte codering en naamgeving PDF bestanden Verplichte naamgeving digitale PDF bestanden Bij het benoemen van de bestandsnamen wordt de format van het standaard onderzoeksdossier van de overheid gevolgd. Hieronder vindt u voorbeelden van de juiste codering en bestandsnamen voor het document (deze lijst geeft niet aan welke documenten je moet indienen, kijk in de tabel bovenaan dit document welke instructie je daarvoor moet raadplegen). Regels bij het aanmaken en indienen van PDF bestanden - Alle documenten dienen geconverteerd te zijn naar PDF formaat. De METC kan geen documenten in WORD, Excel of andere bestandsformaten accepteren. - SVP geen beveiliging gebruiken in de PDF bestanden die worden ingediend. Zodra PDF bestanden zijn beveiligd tegen bewerken, kan het secretariaat van de METC deze bestanden niet samenvoegen of verkleinen voor in de digitale vergaderset voor METC leden. Losse bestanden en bestandsgrootte verhinderen dan het maken, digitaal versturen en gebruik van een digitale vergaderset, waardoor de METC uw onderzoek niet kan behandelen. - De bestanden dienen unieke bestandsnamen te hebben. Gebruik dus géén identieke bestandsnamen en zorg dus dat er minstens een verschil is in bijvoorbeeld de datum of omschrijving van het document in de bestandsnaam. Alleen indien nodig, voegt u dus iets toe aan de standaardbenaming van het document. - Voeg geen documenten samen in één bestand als het aparte documenten horen te zijn zoals hieronder in de lijst is beschreven. - Maak geen mapjes aan op de CD-ROM. Sla alle bestanden op de CD-ROM op zonder een map te gebruiken. - Gebruik géén zip-bestanden op CD-ROM of in de - Volg de verplichte codering en naamgeving van bestanden die hieronder is beschreven: Letter en cijfer dus ook in de bestandsnaam opnemen! Codering en naamgeving documenten (deze lijst geeft niet aan welke documenten je moet indienen, kijk in de tabel bovenaan dit document welke instructie je daarvoor moet raadpelegen). Bij de geel gemarkeerde gedeelten moet u de gevraagde gegevens invullen in de bestandsnamen. De cursief weergegeven tekst tussen haakjes is een korte toelichting. A. Brieven A1. Aanbiedingsbrief indiener dd dd-mm-jj (voor Model aanbiedingsbrieven die op papier bij de CD-ROM moeten worden ingediend: deze zijn te downloaden van de METC website onder A1. Reactie op vragen METC dd dd-mm-jj (puntsgewijze beantwoording van vragen van de METC) A1. Formulier niet-wmo dd dd-mm-jj (te downloaden van de METC website) A2. Machtiging verrichter dd dd-mm-jj (vereist als de opdrachtgever niet de indiener is) A3. Ontvangstbewijs EudraCTnr dd dd-mm-jj (i.e., automatisch bericht) B. Formulieren B1. ABR-formulier versie (zie B3. EudraCT-aanvraagformulier dd dd-mm-jj B5. EudraCT-formulier kennisgeving wijziging dd dd-mm-jj B5. Melding toevoeging centrum [naam centrum] dd dd-mm-jj METC UMC Utrecht, versiedatum
4 B7. EudraCT-formulier einde onderzoek dd dd-mm-jj C. Onderzoeksprotocol en eventuele protocol amendementen C1. Onderzoeksprotocol NLxxxxx.xxx.xx, versie C2. Protocol amendement versie D. Productinformatie D1. IB [naam product] versie D1. Overzichtlijst SUSAR s dd dd-mm-jj (alleen voor SUSAR s na de IB datum) D2. IMPD [naam product] versie D2. SPC [naam product] D2. Lijst met relevante trials D3. Voorbeeldetiketten versie D4. TSE-statement dd dd-mm-jj D4. GMP-verklaring dd dd-mm-jj D4. CE certificaat [naam product] dd dd-mm-jj (Bij studie met Medisch Hulpmiddel) D4. CE Declaration of Conformity [naam product] dd dd-mm-jj (Bij studie met Medisch Hulpmiddel) D4. Andere statements/vergunningen (benoem type document) D5. Productgegevens zh. apotheker D6. Aanvullende productgegevens (benoem type document) D6. Rapport Cluster MT&KF [naam product] dd dd-mm-jj (indien geen CE markering bij Medisch Hulpmiddel) E. Informatie voor proefpersonen E1. Informatiebrief versie E2. Toestemmingsformulier versie E3. Overig wervingsmateriaal versie (benoem type document) E4. Overig voorlichtingsmateriaal versie (benoem type document) E5. Nieuwsbrief dd dd-mm-jj E5. Brief met resultaten dd dd-mm-jj F. Vragenlijsten, patiëntendagboekje, -kaart, etc. F1. Vragenlijst versie F1. Draaiboek interview versie F2. Patiëntendagboek versie F3. Patiëntenkaart versie F4. Andere documenten (benoem type document) G. Informatie over de verzekering G1. WMO-verzekeringscertificaat dd dd-mm-jj G2. Bewijs dekking aansprakelijkheid dd dd-mm-jj H. CV s H1. CV onafh. deskundige [naam deskundige] dd dd-mm-jj H2. CV coörd. onderzoeker [naam onderzoeker] dd dd-mm-jj I. Informatie per deelnemend centrum in Nederland I1. Lijst deelnemende centra met hoofdonderzoeker per centrum dd-mm-jj I2. Onderzoeksverklaring [naam centrum] dd dd-mm-jj I3. CV hoofdonderzoeker [naam onderzoeker] [naam centrum] dd dd-mm-jj I3. CV onafh. deskundige [naam deskundige] dd dd-mm-jj (indien een andere dan bij H1) I4. Overige centruminformatie (benoem type document) J. Aanvullende informatie financiële vergoedingen (indien niet vermeld in ABRformulier) J1. Aan proefpersonen dd dd-mm-jj J2. Aan onderzoekers en centra dd dd-mm-jj K: Overige relevante documenten: K1. Beoordeling/advies [naam instantie] dd dd-mm-jj (subsidiegever, advies EMEA, FDA etc.) K2. Overzichtslijst beoordeling buitenlandse METC s en/of BI s (inclusief VHP) dd ddmm-jj K3. Onderzoekscontract dd dd-mm-jj METC UMC Utrecht, versiedatum
5 K3. Toekenning subsidie dd dd-mm-jj K3. Verklaring dat onderzoekscontracten gelijk zijn aan door TC beoordeelde versie dd dd-mm-jj K4. Ingediende publicatie [naam tijdschrift] [publicatiedatum] K5. Charter Data Safety Monitoring Board versie K6. Overige documenten (benoem type document bijvoorbeeld: brief aan huisarts, brief aan behandelend specialist, advies stralingscommissie, etc.) K6. Monitoringplan versie (verplicht bij onderzoeker geïnitieerd onderzoek, uitgevoerd in het UMC Utrecht) L: Veiligheidsinformatie L1. SUSAR kenmerk. dd dd-mm-jj L1. SADR kenmerk. dd dd-mm-jj L2. Periodieke overzichtslijst SUSAR s [naam product] dd dd-mm-jj L3. Jaarlijkse veiligheidsrapportage [naam product] dd dd-mm-jj L4. SAE kenmerk. dd dd-mm-jj L5. Advies Data Safety Monitoring Board dd dd-mm-jj L6. Overige relevante veiligheidsinformatie (benoem type document) M: Voortgangsrapportages en studieresultaten M1. Voortgangsrapportage dd dd-mm-jj M1. Interimanalyse dd dd-mm-jj M2. Samenvatting studieresultaten dd dd-mm-jj M2. Wetenschappelijke publicatie dd dd-mm-jj M3. Studierapport dd dd-mm-jj METC UMC Utrecht, versiedatum
6 Sectie 3. Welke documenten dien ik in? 3.1 (primaire toetsing van een onderzoek aan de WMO) Documenten nodig bij WMO toetsing A1 (Model Aanbiedingsbrief, te downloaden van de METC website onder A2 (vereist als de opdrachtgever niet de indiener is) B1 C1 E1, E2, E3 (wanneer van toepassing, benoem type document) E4 (wanneer van toepassing, benoem type document) F1 t/m F4 (wanneer van toepassing) G1 (indien niet de UMC Utrecht proefpersonenverzekering) G2 (indien de verrichter niet het UMC Utrecht is) H1, H2 I1 I2 t/m I4 (bij multicenter onderzoek per centrum een volledig pakket zie hieronder bij beoordeling van een deelnemend centrum - aanleveren binnen 14 dagen na eerste indiening; indien later ingediend of later volledig, dan wordt deelname van het centrum na de primaire beoordeling per amendement beoordeeld) J1, J2 (indien dit niet is vermeld in het ABR-formulier) K1 t/m K6 (wanneer van toepassing) K3 Onderzoekscontract of K3 Toekenning subsidie (Let op: altijd van toepassing bij een sponsor of een grant/subsidiegever de METC kan uw onderzoek niet beoordelen zonder bewijs van de afspraken die zijn gemaakt voor financiering; bij multicenter: contract per centrum of een verklaring van de sponsor dat de contracten met de andere centra niet afwijken van het ingediende contract met UMC Utrecht) K6 afspraken met afdeling/divisie (wanneer van toepassing binnen de instelling) K6 monitoringplan (verplicht bij onderzoeker geïnitieerd onderzoek, uitgevoerd in het UMC Utrecht) 3.2 (extra bij primaire toetsing geneesmiddelenonderzoek) Documenten extra nodig bij WMO toetsing geneesmiddelen onderzoek* Aan bovengenoemde lijst voor toetsing niet geneesmiddelenonderzoek toevoegen: A3 B3 D1 D2 (IMPD of SPC) D3 Voorbeeldetiketten versie (in het Nederlands) D4 t/m D6 (wanneer van toepassing) K2 (verplicht bij geneesmiddelenonderzoek indien internationaal onderzoek) *Let op: bij geneesmiddelenonderzoek dient u het dossier ook in te dienen bij de CCMO als Bevoegde Instantie voor het verkrijgen van een verklaring geen bezwaar (zie (reactie op vragen van de METC tijdens WMO toetsing) Voor zowel reactie op vragen bij primaire toetsing als bij toetsing van amendementen bij WMO-plichtig onderzoek geldt: A1 (Model Reactiebrief, te downloaden van de METC website onder + documenten die wijzigen als gevolg van het beantwoorden van de vragen van de METC. METC UMC Utrecht, versiedatum
7 3.4 (toetsing amendementen niet geneesmiddelenonderzoek) Documenten nodig bij WMO toetsing amendementen niet geneesmiddelen onderzoek ingediend na 01 maart 2006 B1 (indien gewijzigd) + documenten die wijzigen als gevolg van het amendement Documenten nodig bij WMO toetsing amendementen niet geneesmiddelen onderzoek ingediend voor 01 maart documenten die wijzigen als gevolg van het amendement 3.5 (toetsing amendementen geneesmiddelenonderzoek) Documenten nodig bij WMO toetsing amendementen geneesmiddelen* onderzoek ingediend voor 01 maart 2006 en als het onderzoek uitsluitend in Nederland plaatsvindt of het amendement alleen voor Nederland geldt (nieuw centrum toegevoegd bijv.) B1 (indien gewijzigd) + documenten die wijzigen als gevolg van het amendement *Let op: u dient A1, A2 en eventueel A3 (indien gewijzigd) ook voor te leggen aan de CCMO als Bevoegde Instantie voor het verkrijgen van een verklaring geen bezwaar. Documenten nodig bij WMO toetsing amendementen geneesmiddelen* onderzoek ingediend na 01 maart 2006 (of voor 2006 betreffende een internationale studie in de EU)* B1 (indien gewijzigd) B3 B5 C2 + documenten die wijzigen als gevolg van het amendement *Let op: u dient A1, A2 en eventueel A3 (indien gewijzigd) ook voor te leggen aan de CCMO als Bevoegde Instantie voor het verkrijgen van een verklaring geen bezwaar. METC UMC Utrecht, versiedatum
8 3.6 (beoordeling van een deelnemend centrum) Documenten nodig voor het beoordelen van deelname van een centrum kunnen bij de primaire toetsing worden ingediend (1) of als amendement (2). (1) Indien de documenten van een centrum binnen 14 dagen na de eerste indiening voor primaire toetsing volledig zijn ingediend, dan wordt het centrum meegenomen in het primaire besluit. Zo niet, dan wordt het centrum later als amendement beoordeeld. (2) indien centra als apart amendement worden toegevoegd, ook de documenten voor een amendement toevoegen zoals hierboven aangegeven*. Onderzoeksdossier, A1. Aanbiedingsbrief, bij een eerste indiening of Model Reactiebrief als u reageert op vragen van de METC) G1 (indien niet verzekerd door de verrichter van de studie) G2 (indien de aanwezigheid van een aansprakelijkheidsverzekering niet al in de onderzoeksverklaring is bevestigd) I2 I3 CV hoofdonderzoeker [naam onderzoeker] [naam centrum] dd dd-mm-jj I3 CV onafh. arts [naam arts] dd dd-mm-jj I4 Informatiebrief versie (of bevestiging dat deze, behoudens lokale aspecten, identiek is aan het hoofddocument) I4 Toestemmingsformulier versie (of bevestiging dat deze, behoudens lokale aspecten, identiek is aan het hoofddocument) I4 Onderzoekscontract dd dd-mm-jj (Onderzoekscontract van verrichter met de onderzoeker en/of instelling, of bevestiging dat deze identiek is aan het binnen dit dossier reeds goedgekeurd document) *Let op: bij geneesmiddelenonderzoek geldt voor deze amendementen ook het voorleggen aan de CCMO als Bevoegde Instantie. 3.7 (voortgangsrapportage) Documenten nodig bij het indienen van een voortgangsrapportage bij WMOplichtig onderzoek. M1 (Formulier voortgangsrapportage: deze is te downloaden van de METC-website, onder Onderzoeksdossier, M1. Voortgangsrapportage) M1 (Interimanalyse indien van toepassing) M2 (wanneer van toepassing) M3 (wanneer van toepassing) 3.8 (veiligheidsmeldingen en periodieke- veiligheidsrapportages) Documenten nodig bij het indienen van veiligheidsmeldingen en (periodieke) veiligheidsrapportages. L1 (indien van toepassing) L2 (indien van toepassing) L3 (indien van toepassing) L4 (indien van toepassing) L5 (indien van toepassing) L6 (indien van toepassing) METC UMC Utrecht, versiedatum
9 3.9 (melding einddatum) Bij WMO-plichtig onderzoek waarbij de METC UMC Utrecht niet de toetsende commissie was volstaat het melden van de einddatum van de studie in het UMC Utrecht samen met het aantal proefpersonen dat in totaal in het UMC Utrecht geïncludeerd is geweest, per aan Heeft de METC UMC Utrecht het onderzoek getoetst aan de WMO dan ontvangt de commissie graag een ingevuld formulier voortgangsrapportage waarin de einddatum van de studie verwerkt kan worden. M1 Voortgangsrapportage (dit formulier is te downloaden van de METC website onder Onderzoeksdossier, M1 Voortgangsrapportage) + bijlagen indien van toepassing: M1 (Interimanalyse indien van toepassing) M2 (wanneer van toepassing) M3 (wanneer van toepassing) 3.10 (eindresultaten) Documenten bij het melden van de eindresultaten. M1 Formulier voortgangsrapportage (indien u deze niet al bij het melden van de einddatum of daarna heeft ingediend, of indien de inhoud van deze rapportage toch is gewijzigd na de laatste voortgangsrapportage) Minstens één van de volgende documenten waarin de eindresultaten worden weergegeven. M2 Samenvatting studieresultaten dd dd-mm-jj M2 Wetenschappelijke publicatie dd dd-mm-jj M3 Studierapport dd dd-mm-jj 3.11 (vraag om advies betreffende mogelijke WMO-plichtigheid / aanvraag verklaring niet WMO-plichtig) Documenten nodig voor de METC om te bepalen of een onderzoeksvoorstel wel of niet aan de WMO getoetst zal moeten worden. A1 Formulier niet-wmo dd dd-mm-jj (te downloaden in WORD formaat van de METC website onder Toetsing, Moet het onderzoek worden getoetst? ; Let op: na invullen ook dit bestand converteren naar PDF formaat alvorens in te dienen!) E1 (wanneer van toepassing) E2 (wanneer van toepassing) F1 (wanneer van toepassing) F2 (wanneer van toepassing) METC UMC Utrecht, versiedatum
Inhoud onderzoeksdossier
 Inhoud onderzoeksdossier (documenten in de witte box zijn nodig voor de primaire beoordeling) A. Brieven B. Formulieren C. Onderzoeksprotocol en protocolamendementen D. Productinformatie E. Informatie
Inhoud onderzoeksdossier (documenten in de witte box zijn nodig voor de primaire beoordeling) A. Brieven B. Formulieren C. Onderzoeksprotocol en protocolamendementen D. Productinformatie E. Informatie
CCMO Structuur documenten Technische Toetsing (ass.secr.) Inhoudelijke Toetsing (secretaris)
 CHECKLIST WMO Primaire indieningsproces WMO in METC Management, screening door Assistent Secretaris. Hieronder staan de generieke uitgangspunten en is toegelicht hoe de primaire toetsing indiening WMO
CHECKLIST WMO Primaire indieningsproces WMO in METC Management, screening door Assistent Secretaris. Hieronder staan de generieke uitgangspunten en is toegelicht hoe de primaire toetsing indiening WMO
Checklist (en toelichting) bij het indienen van een WMO-plichtig onderzoeksdossier
 Checklist (en toelichting) bij het indienen van een WMO-plichtig onderzoeksdossier In onderstaande tabel staan de documenten die u moet indienen als u een onderzoek wilt laten beoordelen door de METC-WU.
Checklist (en toelichting) bij het indienen van een WMO-plichtig onderzoeksdossier In onderstaande tabel staan de documenten die u moet indienen als u een onderzoek wilt laten beoordelen door de METC-WU.
Checklist (en toelichting) bij het indienen van een WMO-plichtig onderzoeksdossier
 Checklist (en toelichting) bij het indienen van een WMO-plichtig onderzoeksdossier In onderstaande tabel staan de documenten die u moet indienen als u een onderzoek wilt laten beoordelen door de METC-WU.
Checklist (en toelichting) bij het indienen van een WMO-plichtig onderzoeksdossier In onderstaande tabel staan de documenten die u moet indienen als u een onderzoek wilt laten beoordelen door de METC-WU.
Checklist en toelichting indienen Lokale Uitvoerbaarheid
 Checklist en toelichting indienen Lokale Uitvoerbaarheid In onderstaande tabel staan de documenten die u moet indienen als u toestemming wilt van de Raad van Bestuur VUmc voor uitvoering van uw onderzoek
Checklist en toelichting indienen Lokale Uitvoerbaarheid In onderstaande tabel staan de documenten die u moet indienen als u toestemming wilt van de Raad van Bestuur VUmc voor uitvoering van uw onderzoek
Checklist en toelichting indienen Lokale Uitvoerbaarheid
 Checklist en toelichting indienen Lokale Uitvoerbaarheid In onderstaande tabel staan de documenten die u moet indienen als u toestemming wilt van de Raad van Bestuur VUmc voor uitvoering van uw onderzoek
Checklist en toelichting indienen Lokale Uitvoerbaarheid In onderstaande tabel staan de documenten die u moet indienen als u toestemming wilt van de Raad van Bestuur VUmc voor uitvoering van uw onderzoek
Checklist Lokale Uitvoerbaarheid
 Primaire indieningsproces Lokale Uitvoerbaarheid in METC Management, screening door Assistent Secretaris. Hieronder staan de generieke uitgangspunten en is toegelicht hoe de toetsing indiening Lokale Uitvoerbaarheid
Primaire indieningsproces Lokale Uitvoerbaarheid in METC Management, screening door Assistent Secretaris. Hieronder staan de generieke uitgangspunten en is toegelicht hoe de toetsing indiening Lokale Uitvoerbaarheid
Checklist en toelichting indienen WMO amendement uitbreiding centrum
 Checklist en toelichting indienen WMO amendement uitbreiding centrum In onderstaande tabel staan de documenten die u moet indienen als u een amendement uitbreiding centrum wilt laten beoordelen door de
Checklist en toelichting indienen WMO amendement uitbreiding centrum In onderstaande tabel staan de documenten die u moet indienen als u een amendement uitbreiding centrum wilt laten beoordelen door de
Danazol voor idiopathische pulmonale fibrose
 Danazol voor idiopathische pulmonale fibrose Thijs W. Hoffman 18-04-2018 Idiopathische pulmonale fibrose (IPF) Normaal Ernstige interstitiële longziekte Ca. 3000 patiënten in NL Verlittekening van de longen
Danazol voor idiopathische pulmonale fibrose Thijs W. Hoffman 18-04-2018 Idiopathische pulmonale fibrose (IPF) Normaal Ernstige interstitiële longziekte Ca. 3000 patiënten in NL Verlittekening van de longen
Formulier Voortgangsrapportage
 Formulier Voortgangsrapportage De METC azm/um wil van al het door haar beoordeelde WMO-onderzoek jaarlijks een voortgangsrapportage zien. Zij heeft deze eis daartoe opgenomen in de tekst van haar eigen
Formulier Voortgangsrapportage De METC azm/um wil van al het door haar beoordeelde WMO-onderzoek jaarlijks een voortgangsrapportage zien. Zij heeft deze eis daartoe opgenomen in de tekst van haar eigen
Checklist en toelichting indienen WMO Oordeel
 Checklist en toelichting indienen WMO Oordeel In onderstaande tabel staan de documenten die u moet indienen als u een onderzoek wilt laten beoordelen door de METc VUmc. Onderscheiden worden monoen multionderzoek
Checklist en toelichting indienen WMO Oordeel In onderstaande tabel staan de documenten die u moet indienen als u een onderzoek wilt laten beoordelen door de METc VUmc. Onderscheiden worden monoen multionderzoek
Handleiding Goedkeuringsprocedure Raad van Bestuur Zuyderland wetenschappelijk onderzoek
 Handleiding Goedkeuringsprocedure Raad van Bestuur Zuyderland wetenschappelijk onderzoek INLEIDING oor al het onderzoek dat binnen Zuyderland wordt uitgevoerd moet goedkeuring worden verkregen van de Raad
Handleiding Goedkeuringsprocedure Raad van Bestuur Zuyderland wetenschappelijk onderzoek INLEIDING oor al het onderzoek dat binnen Zuyderland wordt uitgevoerd moet goedkeuring worden verkregen van de Raad
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek
 Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
Checklist en toelichting indienen WMO Oordeel
 Checklist en toelichting indienen WMO Oordeel In onderstaande tabel staan de documenten die u moet indienen als u een onderzoek wil laten beoordelen door de METc VUmc. Onderscheiden worden mono- en multionderzoek
Checklist en toelichting indienen WMO Oordeel In onderstaande tabel staan de documenten die u moet indienen als u een onderzoek wil laten beoordelen door de METc VUmc. Onderscheiden worden mono- en multionderzoek
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VC9 Proefpersonen- en aansprakelijkheidsverzekering (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure STZ SOP: VC9 Proefpersonen- en aansprakelijkheidsverzekering (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
INDIENEN NIEUWE AANVRAAG
 INDIENEN NIEUWE AANVRAAG Inleiding instructie CMO-Online: voor nieuwe aanvragen CMO-Online is de digitale portal van de Commissie Mensgebonden Onderzoek Alle bestaande en nieuwe dossiers staan in de portal
INDIENEN NIEUWE AANVRAAG Inleiding instructie CMO-Online: voor nieuwe aanvragen CMO-Online is de digitale portal van de Commissie Mensgebonden Onderzoek Alle bestaande en nieuwe dossiers staan in de portal
INSTRUCTIE VOOR BESTAANDE ONDERZOEKSDOSSIERS (die al bij de CMO bekend zijn en een registratienummer hebben
 INSTRUCTIE VOOR BESTAANDE ONDERZOEKSDOSSIERS (die al bij de CMO bekend zijn en een registratienummer hebben Inleiding instructie CMO-Online voor bestaande dossiers CMO-Online is de digitale portal van
INSTRUCTIE VOOR BESTAANDE ONDERZOEKSDOSSIERS (die al bij de CMO bekend zijn en een registratienummer hebben Inleiding instructie CMO-Online voor bestaande dossiers CMO-Online is de digitale portal van
Standaard onderzoeksdossier voor indiening van een onderzoeksvoorstel bij een WMO-toetsingscommissie en/of de bevoegde instantie
 Standaard onderzoeksdossier voor indiening van een onderzoeksvoorstel bij een WMO-toetsingscommissie en/of de bevoegde instantie A. Brieven A1: Aanbiedingsbrief aan toetsingscommissie en bevoegde instantie
Standaard onderzoeksdossier voor indiening van een onderzoeksvoorstel bij een WMO-toetsingscommissie en/of de bevoegde instantie A. Brieven A1: Aanbiedingsbrief aan toetsingscommissie en bevoegde instantie
SOP aanleveren en afhandelen WMO onderzoek METC Onze Lieve Vrouwe Gasthuis, versie 1, juli
 Aanmelden en afhandelen medisch-wetenschappelijk onderzoek met mensen (WMO-onderzoek) Medisch-ethische toetsingscommissie (METC) Onze Lieve Vrouwe Gasthuis Hieronder treft u aan de procedure van aanmelding
Aanmelden en afhandelen medisch-wetenschappelijk onderzoek met mensen (WMO-onderzoek) Medisch-ethische toetsingscommissie (METC) Onze Lieve Vrouwe Gasthuis Hieronder treft u aan de procedure van aanmelding
Procedure multicenter WMO-plichtig klinisch wetenschappelijk onderzoek geïnitieerd vanuit het Elisabeth-TweeSteden Ziekenhuis
 Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure multicenter WMO-plichtig klinisch wetenschappelijk onderzoek geïnitieerd vanuit het Elisabeth-TweeSteden Ziekenhuis Bij dit type
Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure multicenter WMO-plichtig klinisch wetenschappelijk onderzoek geïnitieerd vanuit het Elisabeth-TweeSteden Ziekenhuis Bij dit type
Handleiding Study Management voor onderzoeker
 Handleiding Study Management voor onderzoeker Onderdeel van Research Manager Handleiding Research Manager onderdeel Study Management 21-07-2017 1 Inhoudsopgave Hoofdstuk: Pagina: 1. Gebruik Study Management
Handleiding Study Management voor onderzoeker Onderdeel van Research Manager Handleiding Research Manager onderdeel Study Management 21-07-2017 1 Inhoudsopgave Hoofdstuk: Pagina: 1. Gebruik Study Management
Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis. Procedure niet-wmo-plichtig klinisch wetenschappelijk onderzoek
 Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure niet-wmo-plichtig klinisch wetenschappelijk onderzoek Deze procedure geldt voor niet-wmo-plichtig onderzoek dat of: a) enkel
Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure niet-wmo-plichtig klinisch wetenschappelijk onderzoek Deze procedure geldt voor niet-wmo-plichtig onderzoek dat of: a) enkel
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik
 EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor onderzoekers- Paula Vossebeld Symposium van de V&VN RP 10 november 2015 Verordening
Procedure aanvraag voor het verrichten van wetenschappelijk onderzoek in Meander Medisch Centrum
 Procedure aanvraag voor het verrichten van wetenschappelijk onderzoek in Meander Medisch Centrum Commissie Toetsing Wetenschappelijk Onderzoek (TWO) I II Algemeen 1. Alvorens onderzoek in Meander MC van
Procedure aanvraag voor het verrichten van wetenschappelijk onderzoek in Meander Medisch Centrum Commissie Toetsing Wetenschappelijk Onderzoek (TWO) I II Algemeen 1. Alvorens onderzoek in Meander MC van
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: U11 Voortgangsrapportage Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: U11 Voortgangsrapportage Distributielijst : STZ Datum : 19-06-2014 Revisiedatum : 19-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Handleiding Goedkeuringsprocedure Raad van Bestuur Zuyderland voor wetenschappelijk onderzoek
 Handleiding Goedkeuringsprocedure Raad van Bestuur Zuyderland voor wetenschappelijk onderzoek Deze handleiding wordt voortdurend geupdate naar aanleiding van de meest recente wet- en regelgeving en wijzigingen
Handleiding Goedkeuringsprocedure Raad van Bestuur Zuyderland voor wetenschappelijk onderzoek Deze handleiding wordt voortdurend geupdate naar aanleiding van de meest recente wet- en regelgeving en wijzigingen
Procedure deelnemend aan multicenter WMO-plichtig klinisch wetenschappelijk onderzoek
 Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure deelnemend aan multicenter WMO-plichtig klinisch wetenschappelijk onderzoek Bij dit type onderzoek neemt de onderzoeker van het
Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure deelnemend aan multicenter WMO-plichtig klinisch wetenschappelijk onderzoek Bij dit type onderzoek neemt de onderzoeker van het
Bijgaand ontvangt u het primair besluit van de commissie over het hierna vermelde onderzoek.
 Medisch To e ts ingsco mmiss ie Noord-Holland Noordwest Ziekenhuisgroep Dhr. F. Hagemans Afdeling Orthopedie Wilhelminalaan 12 1815 JD Alkmaar datum 7 juni 2016 kenmerk NH017.140 METC- registratie M016-030
Medisch To e ts ingsco mmiss ie Noord-Holland Noordwest Ziekenhuisgroep Dhr. F. Hagemans Afdeling Orthopedie Wilhelminalaan 12 1815 JD Alkmaar datum 7 juni 2016 kenmerk NH017.140 METC- registratie M016-030
Praktisch: Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis. Procedure niet-wmo-plichtig klinisch wetenschappelijk onderzoek
 Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure niet-wmo-plichtig klinisch wetenschappelijk onderzoek Deze procedure geldt voor niet-wmo-plichtig onderzoek dat of: a) enkel
Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure niet-wmo-plichtig klinisch wetenschappelijk onderzoek Deze procedure geldt voor niet-wmo-plichtig onderzoek dat of: a) enkel
Bijgaand ontvangt u het primaire besluit van de commissie over het hierna vermelde onderzoek.
 Medisch :' i < r. c Toetsingscommissie Noord-Holland t AMC Orthopedie A.J. Kievit Staalmeesterslaan 271 1057 NZ Amsterdam datum kenmerk METC- registratie CCMO-registratie EudraCTnummer 30 oktober 2012
Medisch :' i < r. c Toetsingscommissie Noord-Holland t AMC Orthopedie A.J. Kievit Staalmeesterslaan 271 1057 NZ Amsterdam datum kenmerk METC- registratie CCMO-registratie EudraCTnummer 30 oktober 2012
Handleiding Study Management voor afstudeeronderzoek
 Handleiding Study Management voor afstudeeronderzoek Onderdeel van Research Manager Handleiding Research Manager onderdeel Study Management 12-10-2018 1 Inhoudsopgave Hoofdstuk: Pagina: 1. Gebruik Study
Handleiding Study Management voor afstudeeronderzoek Onderdeel van Research Manager Handleiding Research Manager onderdeel Study Management 12-10-2018 1 Inhoudsopgave Hoofdstuk: Pagina: 1. Gebruik Study
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen. Farmaceutische Bedrijven Deelteam Klinisch Onderzoek
 Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VC8 Beoordeling amendement toetsende commissie (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Standard Operating Procedure STZ SOP: VC8 Beoordeling amendement toetsende commissie (centraal) Distributielijst : STZ Datum : 10-03-2014 Revisiedatum : 10-03-2015 Veranderingen ten opzichte van eerdere
Jouw GCP up-to-date in 45 minuten. Marieke Meulemans, oprichter GCP Central
 Jouw GCP up-to-date in 45 minuten Marieke Meulemans, oprichter GCP Central Waarom een GCP update tijdens de CRA dag? Gedreven Meesterschap. Meesterschap is vakmanschap. Vakmanschap is beheersing van het
Jouw GCP up-to-date in 45 minuten Marieke Meulemans, oprichter GCP Central Waarom een GCP update tijdens de CRA dag? Gedreven Meesterschap. Meesterschap is vakmanschap. Vakmanschap is beheersing van het
5. Goedkeuring deelname door de toetsende METC 6. Start- en einddatum onderzoek 7. Rekening
 Aanleveren documenten voor het uitbrengen van advies over lokale uitvoerbaarheid bij de Medisch-ethische toetsingscommissie (METC) in het Onze Lieve Vrouwe Gasthuis Mocht u nog vragen hebben naar aanleiding
Aanleveren documenten voor het uitbrengen van advies over lokale uitvoerbaarheid bij de Medisch-ethische toetsingscommissie (METC) in het Onze Lieve Vrouwe Gasthuis Mocht u nog vragen hebben naar aanleiding
Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek
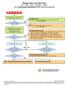 Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek Melding voorval proefpersoon aan onderzoeker/arts 1 Rapportage voorval door onderzoeker/arts in patiëntenstatus
Ongewenste voorvallen flow AE SAE SAR SUSAR SADE voor onderzoeker geïnitieerd WMO-plichtig onderzoek Melding voorval proefpersoon aan onderzoeker/arts 1 Rapportage voorval door onderzoeker/arts in patiëntenstatus
Bij dit type onderzoek vindt het WMO-plichtig onderzoek enkel plaats in het Elisabeth-TweeSteden Ziekenhuis.
 Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure monocenter WMO-plichtig klinisch wetenschappelijk onderzoek Bij dit type onderzoek vindt het WMO-plichtig onderzoek enkel plaats
Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure monocenter WMO-plichtig klinisch wetenschappelijk onderzoek Bij dit type onderzoek vindt het WMO-plichtig onderzoek enkel plaats
Kenmerk: V /R17.001/dj/ld Datum:
 Meander Medisch Centrum T.a.v. dr. P.H.G. Hogeman, kinderarts Postbus 1502 3800 BM AMERSFOORT Kenmerk: V.112232/R17.001/dj/ld Datum: 7-8-2017 Betreft: besluit NL59723.100.16 R17.001/PREP cariesrisk Geachte
Meander Medisch Centrum T.a.v. dr. P.H.G. Hogeman, kinderarts Postbus 1502 3800 BM AMERSFOORT Kenmerk: V.112232/R17.001/dj/ld Datum: 7-8-2017 Betreft: besluit NL59723.100.16 R17.001/PREP cariesrisk Geachte
Procedure monocenter WMO-plichtig klinisch wetenschappelijk onderzoek
 Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure monocenter WMO-plichtig klinisch wetenschappelijk onderzoek Bij dit type onderzoek vindt het WMO-plichtig onderzoek enkel plaats
Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure monocenter WMO-plichtig klinisch wetenschappelijk onderzoek Bij dit type onderzoek vindt het WMO-plichtig onderzoek enkel plaats
website www.nvmetc.nl
 Verslag NVMETC secretarissenoverleg 19 juni 2014 1. Opening en vaststelling agenda Dhr. Davids geeft aan, dat een belangrijke reden van dit secretarissenoverleg is, dat we van elkaar horen wat er speelt
Verslag NVMETC secretarissenoverleg 19 juni 2014 1. Opening en vaststelling agenda Dhr. Davids geeft aan, dat een belangrijke reden van dit secretarissenoverleg is, dat we van elkaar horen wat er speelt
Procedure multicenter WMO-plichtig klinisch wetenschappelijk onderzoek geïnitieerd vanuit het Elisabeth-TweeSteden Ziekenhuis
 Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure multicenter WMO-plichtig klinisch wetenschappelijk onderzoek geïnitieerd vanuit het Elisabeth-TweeSteden Ziekenhuis Bij dit type
Wetenschappelijk onderzoek in het Elisabeth-TweeSteden Ziekenhuis Procedure multicenter WMO-plichtig klinisch wetenschappelijk onderzoek geïnitieerd vanuit het Elisabeth-TweeSteden Ziekenhuis Bij dit type
Revalidatie & MS Centrum vzw. V. Cuyvers Uitgavedatum: 12.05.2015 Pagina: 1 van 5
 Pagina: 1 van 5 Het ondervragen van patiënten in het kader van een eindwerk voor het bekomen van een graad van bachelor of bachelor na bachelor komt neer op een prospectieve verzameling van gegevens met
Pagina: 1 van 5 Het ondervragen van patiënten in het kader van een eindwerk voor het bekomen van een graad van bachelor of bachelor na bachelor komt neer op een prospectieve verzameling van gegevens met
Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen
 Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen Afdeling Farmaceutische Bedrijven, Klinisch Onderzoek Good Clinical Practice Inhoud Wat doet de IGJ aan toezicht op klinisch
Toezicht op klinisch onderzoek: bevindingen uit inspecties bij GGZ instellingen Afdeling Farmaceutische Bedrijven, Klinisch Onderzoek Good Clinical Practice Inhoud Wat doet de IGJ aan toezicht op klinisch
Handleiding Goedkeuringsprocedure Raad van Bestuur Zuyderland voor wetenschappelijk onderzoek - Handleiding voor externe onderzoekers -
 Handleiding Goedkeuringsprocedure Raad van Bestuur Zuyderland voor wetenschappelijk onderzoek - Handleiding voor externe onderzoekers - Deze handleiding wordt voortdurend geupdate naar aanleiding van de
Handleiding Goedkeuringsprocedure Raad van Bestuur Zuyderland voor wetenschappelijk onderzoek - Handleiding voor externe onderzoekers - Deze handleiding wordt voortdurend geupdate naar aanleiding van de
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik
 EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor CCMO, METC s en onderzoekers- Paula Vossebeld DCTF jaarcongres 7 oktober 2015 Verordening
EU verordening no 536/2014 betreffende klinische proeven met geneesmiddelen voor menselijk gebruik -Implicaties voor CCMO, METC s en onderzoekers- Paula Vossebeld DCTF jaarcongres 7 oktober 2015 Verordening
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL5 Protocolamendement (lokaal) Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: VL5 Protocolamendement (lokaal) Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Handleiding/stroomschema gebruik TLV applicatie SWV Passend onderwijs PO Eindhoven
 Handleiding/stroomschema gebruik TLV applicatie SWV Passend onderwijs PO Eindhoven Ga naar tlv.po-eindhoven.nl Bij bestaande account: Inloggen met: e-mailadres wachtwoord Bij nieuwe account: 1. Klik op
Handleiding/stroomschema gebruik TLV applicatie SWV Passend onderwijs PO Eindhoven Ga naar tlv.po-eindhoven.nl Bij bestaande account: Inloggen met: e-mailadres wachtwoord Bij nieuwe account: 1. Klik op
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL2 Aanpassen proefpersoneninformatie / toestemmingsformulier aan lokale situatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen
Standard Operating Procedure STZ SOP: VL2 Aanpassen proefpersoneninformatie / toestemmingsformulier aan lokale situatie Distributielijst : STZ Datum : 20-03-2014 Revisiedatum : 20-03-2015 Veranderingen
KLINISCH GENEESMIDDELEN- ONDERZOEK
 KLINISCH GENEESMIDDELEN- ONDERZOEK HET PROCES VAN HET OPSTARTEN VAN KLINISCH ONDERZOEK MET GENEESMIDDELEN GAAT VERANDEREN De ECTR verandert het klinisch onderzoek met geneesmiddelen in Europa. Dit heeft
KLINISCH GENEESMIDDELEN- ONDERZOEK HET PROCES VAN HET OPSTARTEN VAN KLINISCH ONDERZOEK MET GENEESMIDDELEN GAAT VERANDEREN De ECTR verandert het klinisch onderzoek met geneesmiddelen in Europa. Dit heeft
Op naar het snel opstarten van klinisch onderzoek in Nederland!
 Op naar het snel opstarten van klinisch onderzoek in Nederland! Marika Trieling Voorzitter DCRF werkgroep Lokale uitvoerbaarheid 12 februari 2019 Wat is er in Nederland nodig? Verkorten tijdslijnen van
Op naar het snel opstarten van klinisch onderzoek in Nederland! Marika Trieling Voorzitter DCRF werkgroep Lokale uitvoerbaarheid 12 februari 2019 Wat is er in Nederland nodig? Verkorten tijdslijnen van
HANDLEIDING WMO- BEOORDELING VOOR EEN INTERNE INDIENER. Werken in het METC Management-Systeem METC Erasmus MC
 HANDLEIDING WMO- BEOORDELING VOOR EEN INTERNE Werken in het METC Management-Systeem versie augustus 2018 1 Inhoud 2 Inleiding... 2 3 Toegang tot het METC Managementsysteem... 2 3.1 Account aanvragen interne
HANDLEIDING WMO- BEOORDELING VOOR EEN INTERNE Werken in het METC Management-Systeem versie augustus 2018 1 Inhoud 2 Inleiding... 2 3 Toegang tot het METC Managementsysteem... 2 3.1 Account aanvragen interne
Aanmelden medischwetenschappelijk
 Aanmelden medischwetenschappelijk onderzoek SOP Aanmelden WMO-plichtig onderzoek_versie juli 2016.doc Pagina 1 van 10 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd
Aanmelden medischwetenschappelijk onderzoek SOP Aanmelden WMO-plichtig onderzoek_versie juli 2016.doc Pagina 1 van 10 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd
PATIËNTENINFORMATIE TRACING. Registratie van real time continue glucose monitoring in Nederland (TRACING)
 PATIËNTENINFORMATIE TRACING Registratie van real time continue glucose monitoring in Nederland (TRACING) Geachte heer/mevrouw, Bij de behandeling van uw diabetes gebruikt u op dit moment de real time continue
PATIËNTENINFORMATIE TRACING Registratie van real time continue glucose monitoring in Nederland (TRACING) Geachte heer/mevrouw, Bij de behandeling van uw diabetes gebruikt u op dit moment de real time continue
WinGym Maak uw eigen brieven. Via Management, Diverse brieven komt u in het scherm waarin u zelf uw eigen brieven kunt samenstellen.
 WinGym Maak uw eigen brieven Via Management, Diverse brieven komt u in het scherm waarin u zelf uw eigen brieven kunt samenstellen. U kunt zelf een sjabloon maken waarin u uw eigen huisstijl kunt ontwerpen.
WinGym Maak uw eigen brieven Via Management, Diverse brieven komt u in het scherm waarin u zelf uw eigen brieven kunt samenstellen. U kunt zelf een sjabloon maken waarin u uw eigen huisstijl kunt ontwerpen.
nwmo toetsingskader Eveline Loriaux projectleider 4 oktober 2017 Jaarcongres DCRF
 nwmo toetsingskader Eveline Loriaux projectleider 4 oktober 2017 Jaarcongres DCRF Zien we door de bomen nog het bos? nwmo Toetsingskader Overzicht Start: juli 2015 In 2017 zijn 39 aanvragen ingediend
nwmo toetsingskader Eveline Loriaux projectleider 4 oktober 2017 Jaarcongres DCRF Zien we door de bomen nog het bos? nwmo Toetsingskader Overzicht Start: juli 2015 In 2017 zijn 39 aanvragen ingediend
Standaard onderzoeksdossier voor indiening van een onderzoeksvoorstel bij een WMO toetsingscommissie en/of de bevoegde instantie
 Standaard onderzoeksdossier voor indiening van een onderzoeksvoorstel bij een WMO toetsingscommissie en/of de bevoegde instantie A. Brieven A1: Aanbiedingsbrief aan toetsingscommissie en bevoegde instantie
Standaard onderzoeksdossier voor indiening van een onderzoeksvoorstel bij een WMO toetsingscommissie en/of de bevoegde instantie A. Brieven A1: Aanbiedingsbrief aan toetsingscommissie en bevoegde instantie
ETHISCH COMITÉ PZ HF KORTRIJK - PC MENEN
 ETHISCH COMITÉ PZ HF KORTRIJK - PC MENEN Aanvraagformulier Ethisch advies voor experimenten op de menselijke persoon Richtlijnen Ethische comités hebben een beperkte tijd om dossiers te evalueren en hun
ETHISCH COMITÉ PZ HF KORTRIJK - PC MENEN Aanvraagformulier Ethisch advies voor experimenten op de menselijke persoon Richtlijnen Ethische comités hebben een beperkte tijd om dossiers te evalueren en hun
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Tijdelijke procedure voor het indienen van facturen bij de RIGG voor tarief-gefinancierde zorgaanbieders. (versie 1.03 dd 10 maart 2013)
 Tijdelijke procedure voor het indienen van facturen bij de RIGG voor tarief-gefinancierde zorgaanbieders. (versie 1.03 dd 10 maart 2013) Voor het indienen van declaraties voor jeugdhulp wordt gebruik gemaakt
Tijdelijke procedure voor het indienen van facturen bij de RIGG voor tarief-gefinancierde zorgaanbieders. (versie 1.03 dd 10 maart 2013) Voor het indienen van declaraties voor jeugdhulp wordt gebruik gemaakt
AMC Uitvoeringsrichtlijnen: Goedkeuring medisch-wetenschappelijk onderzoek door de Raad van Bestuur
 AMC Uitvoeringsrichtlijnen: Goedkeuring medisch-wetenschappelijk onderzoek door de Raad van Bestuur en Deelname van personeelsleden en studenten aan medisch-wetenschappelijk onderzoek Versie 1.1 Dit document
AMC Uitvoeringsrichtlijnen: Goedkeuring medisch-wetenschappelijk onderzoek door de Raad van Bestuur en Deelname van personeelsleden en studenten aan medisch-wetenschappelijk onderzoek Versie 1.1 Dit document
Monitorplan voorbeeld
 Monitorplan voorbeeld Protocol Er moet in het protocol beschreven worden dat er monitoring plaatsvindt (zie ook CCMO voorbeeld template). Het monitoringplan mag als bijlage worden toegevoegd (in dat geval
Monitorplan voorbeeld Protocol Er moet in het protocol beschreven worden dat er monitoring plaatsvindt (zie ook CCMO voorbeeld template). Het monitoringplan mag als bijlage worden toegevoegd (in dat geval
De invloed van een uitwendige kracht op de oogdruk.
 1 www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie) naar de invloed die een uitwendige kracht heeft
1 www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie) naar de invloed die een uitwendige kracht heeft
Betreft: Uitnodiging SCORE-onderzoek. Geachte heer/mevrouw,
 Betreft: Uitnodiging SCORE-onderzoek. Geachte heer/mevrouw, Met deze brief willen we u uitnodigen om deel te nemen aan het SCORE-onderzoek. Dit onderzoek gaat over de inhoud van revalidatie na een beroerte,
Betreft: Uitnodiging SCORE-onderzoek. Geachte heer/mevrouw, Met deze brief willen we u uitnodigen om deel te nemen aan het SCORE-onderzoek. Dit onderzoek gaat over de inhoud van revalidatie na een beroerte,
Informatiebrief deelnemers MIND-TIA: De waarde van een bloedtest bij verdenking op een TIA
 Informatiebrief deelnemers MIND-TIA: De waarde van een bloedtest bij verdenking op een TIA Julius Centrum UMC Utrecht Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Informatiebrief deelnemers MIND-TIA: De waarde van een bloedtest bij verdenking op een TIA Julius Centrum UMC Utrecht Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Plaatsing van voedingssondes in de dunne darm via elektromagnetische geleiding op de verpleegafdeling of via kijkonderzoek op de endoscopie-afdeling
 Patiënt informatiebrief Plaatsing van voedingssondes in de dunne darm via elektromagnetische geleiding op de verpleegafdeling of via kijkonderzoek op de endoscopie-afdeling Geachte heer/mevrouw, Wij vragen
Patiënt informatiebrief Plaatsing van voedingssondes in de dunne darm via elektromagnetische geleiding op de verpleegafdeling of via kijkonderzoek op de endoscopie-afdeling Geachte heer/mevrouw, Wij vragen
 ------------------------------------------------------------------------------------------------------------------------------------------- Concept Procedure Lokale Haalbaarheid klinisch geneesmiddelenonderzoek
------------------------------------------------------------------------------------------------------------------------------------------- Concept Procedure Lokale Haalbaarheid klinisch geneesmiddelenonderzoek
Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) Team Klinisch Onderzoek
 Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) 2014-2016 Team Klinisch Onderzoek Toezicht op IIT 2014-2016 Aanleiding en werkwijze Bevindingen vanuit de praktijk Conclusies en aandachtspunten
Toezicht op onderzoeker geïnitieerd klinisch onderzoek (IIT) 2014-2016 Team Klinisch Onderzoek Toezicht op IIT 2014-2016 Aanleiding en werkwijze Bevindingen vanuit de praktijk Conclusies en aandachtspunten
Patiëntinformatieformulier LOGICA-trial
 Informatiebrief LOGICA trial: Laparoscopische versus Open Maag Operatie Datum: Onderwerp Telefoon E-mail 1 november 2015 LOGICA trial 088-005 6908 espillenaarbilgen@rijnstate.nl Geachte heer/mevrouw, U
Informatiebrief LOGICA trial: Laparoscopische versus Open Maag Operatie Datum: Onderwerp Telefoon E-mail 1 november 2015 LOGICA trial 088-005 6908 espillenaarbilgen@rijnstate.nl Geachte heer/mevrouw, U
T.b.v. het lokale advies bij medisch wetenschappelijke studievoorstellen
 Versie oktober 2007 Algemene informatie Voor een advies inzake de lokale uitvoerbaarheid van een onderzoek in het OLVG dat reeds door een erkende METC beoordeeld is, dient u het onderzoek bij de MEC van
Versie oktober 2007 Algemene informatie Voor een advies inzake de lokale uitvoerbaarheid van een onderzoek in het OLVG dat reeds door een erkende METC beoordeeld is, dient u het onderzoek bij de MEC van
Berichtenbox. Auteur : Rakesh Poeran Datum : 19 mei 2015 Versie : 2014.5 Documentnaam : Berichtenbox
 Berichtenbox Auteur : Rakesh Poeran Datum : 19 mei 2015 Versie : 2014.5 Documentnaam : Berichtenbox Inhoud 1. Inleiding 3 2. Inloggen op de berichtenbox 4 3. Lay-out van de berichtenbox 6 3.1 Linker menu
Berichtenbox Auteur : Rakesh Poeran Datum : 19 mei 2015 Versie : 2014.5 Documentnaam : Berichtenbox Inhoud 1. Inleiding 3 2. Inloggen op de berichtenbox 4 3. Lay-out van de berichtenbox 6 3.1 Linker menu
Veel gestelde vragen Medisch-wetenschappelijk onderzoek met medische hulpmiddelen 1
 Veel gestelde vragen Medisch-wetenschappelijk onderzoek met medische hulpmiddelen 1 1. Wat is een medisch hulpmiddel? De wettelijke definitie 2 van een medisch hulpmiddel luidt: Een medisch hulpmiddel
Veel gestelde vragen Medisch-wetenschappelijk onderzoek met medische hulpmiddelen 1 1. Wat is een medisch hulpmiddel? De wettelijke definitie 2 van een medisch hulpmiddel luidt: Een medisch hulpmiddel
Werkervaring zzp er handleiding
 Werkervaring zzp er handleiding Deze korte handleiding geeft stap voor stap uitleg hoe u als jeugd- en gezinsprofessional uw werkervaring als zzp er kunt indienen in Mijn SKJ. Lees deze goed door alvorens
Werkervaring zzp er handleiding Deze korte handleiding geeft stap voor stap uitleg hoe u als jeugd- en gezinsprofessional uw werkervaring als zzp er kunt indienen in Mijn SKJ. Lees deze goed door alvorens
Een onderzoek naar de werkzaamheid van assisted hatching
 Een onderzoek naar de werkzaamheid van assisted hatching Inleiding Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek naar de werkzaamheid van assisted
Een onderzoek naar de werkzaamheid van assisted hatching Inleiding Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek naar de werkzaamheid van assisted
MDR (2017/745) en klinisch onderzoek - Implementatie in Nederland -
 MDR (2017/745) en klinisch onderzoek - Implementatie in Nederland - DCRF 26 september 2018 Monique Al Teamcoördinator Landelijk Bureau CCMO MDR: Drie hoofdcategoriën klinisch onderzoek I II III Klinisch
MDR (2017/745) en klinisch onderzoek - Implementatie in Nederland - DCRF 26 september 2018 Monique Al Teamcoördinator Landelijk Bureau CCMO MDR: Drie hoofdcategoriën klinisch onderzoek I II III Klinisch
Aanmelden WMO-plichtig onderzoek
 Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd wordt bij het aanmelden van onderzoek dat onder de WMO valt en waarbij ZGV optreedt als deelnemend centrum. Voordat
Aanmelden WMO-plichtig onderzoek 1. Doel Het beschrijven van de procedure die gevolgd wordt bij het aanmelden van onderzoek dat onder de WMO valt en waarbij ZGV optreedt als deelnemend centrum. Voordat
Drie-dimensionale echografie voor het verbeteren van cosmetisch resultaat bij borstkanker patiënten; TURACOS trial
 Drie-dimensionale echografie voor het verbeteren van cosmetisch resultaat bij borstkanker patiënten; Geachte mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek
Drie-dimensionale echografie voor het verbeteren van cosmetisch resultaat bij borstkanker patiënten; Geachte mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Routine versus op indicatie verwijderen van de stelschroef Routinematig versus op indicatie verwijderen van de stelschroef:
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Routine versus op indicatie verwijderen van de stelschroef Routinematig versus op indicatie verwijderen van de stelschroef:
Digitaal Aanvraag Formulier Tijdelijke Verkeersmaatregelen
 Digitaal Aanvraag Formulier Tijdelijke Verkeersmaatregelen 1 Hoofdmenu... 2 2 Nieuwe Aanvraag... 2 1 Kaart... 3 2 Locatie... 4 3 Aanvrager... 5 4 Opdrachtgever... 5 5 Tijdsbepaling... 5 6 Maatregelen...
Digitaal Aanvraag Formulier Tijdelijke Verkeersmaatregelen 1 Hoofdmenu... 2 2 Nieuwe Aanvraag... 2 1 Kaart... 3 2 Locatie... 4 3 Aanvrager... 5 4 Opdrachtgever... 5 5 Tijdsbepaling... 5 6 Maatregelen...
Klinische keuzes bij patiënten met staar en hoornvliesdystrofie van Fuchs
 Schiedamse Vest 180 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie)
Schiedamse Vest 180 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie)
Aanvraagformulier REGISTRATIE centraal oncologie datamanager
 Aanvraagformulier REGISTRATIE centraal oncologie datamanager 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:... Geboorteplaats:... Werkzaam bij: Organisatie
Aanvraagformulier REGISTRATIE centraal oncologie datamanager 1. Gegevens aanvrager Naam + Voorletters:... Adres:... Postcode + Woonplaats:.... Geboortedatum:... Geboorteplaats:... Werkzaam bij: Organisatie
Veiligheid en methodologie of Waarom voortijdig stoppen? Job van der Palen METC Twente
 Veiligheid en methodologie of Waarom voortijdig stoppen? Job van der Palen METC Twente Waarom voortijdig stoppen? Veiligheid Effectiviteit Futiliteit Andere redenen Veiligheid (1) Data and Safety Monitoring
Veiligheid en methodologie of Waarom voortijdig stoppen? Job van der Palen METC Twente Waarom voortijdig stoppen? Veiligheid Effectiviteit Futiliteit Andere redenen Veiligheid (1) Data and Safety Monitoring
Standard Operating Procedure
 Standard Operating Procedure STZ SOP: VL4 Investigator Site File Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Standard Operating Procedure STZ SOP: VL4 Investigator Site File Distributielijst : STZ Datum : 03-06-2014 Revisiedatum : 03-06-2015 Veranderingen ten opzichte van eerdere versies Versiedatum Opmerkingen
Handleiding Mobility Online online application Non-Erasmus Placement
 Handleiding Mobility Online online application Non-Erasmus Placement Alle studenten die naar het buitenland gaan voor een stage moeten een dossier aanmaken in Mobility Online. Meer info over de procedures
Handleiding Mobility Online online application Non-Erasmus Placement Alle studenten die naar het buitenland gaan voor een stage moeten een dossier aanmaken in Mobility Online. Meer info over de procedures
Berichtenbox. Auteur : Rakesh Poeran Datum : 16 juli 2015 Versie : 2014.6 Documentnaam : Berichtenbox
 Berichtenbox Auteur : Rakesh Poeran Datum : 16 juli 2015 Versie : 2014.6 Documentnaam : Berichtenbox Inhoud 1. Inleiding 3 2. Inloggen op de berichtenbox 4 3. Lay-out van de berichtenbox 6 3.1 Linker menu
Berichtenbox Auteur : Rakesh Poeran Datum : 16 juli 2015 Versie : 2014.6 Documentnaam : Berichtenbox Inhoud 1. Inleiding 3 2. Inloggen op de berichtenbox 4 3. Lay-out van de berichtenbox 6 3.1 Linker menu
Bijlage 2 bij het Convenant PSI Samenstelling en werkwijze toetsingscommissie
 Bijlage 2 bij het Convenant PSI Samenstelling en werkwijze toetsingscommissie 1. Samenstelling toetsingscommissie De kerncommissie betstaat uit leden met ten minste de volgende specialismes 1 : Arts of
Bijlage 2 bij het Convenant PSI Samenstelling en werkwijze toetsingscommissie 1. Samenstelling toetsingscommissie De kerncommissie betstaat uit leden met ten minste de volgende specialismes 1 : Arts of
Monitoring van Investigator Initiated onderzoek
 Monitoring van Investigator Initiated onderzoek V1.0 Angela Vlug Clinical Research Bureau VUmc Wat is een IIS (volgens de NFU) Onderzoek waarvoor de raad van bestuur van een (universitair) medisch centrum
Monitoring van Investigator Initiated onderzoek V1.0 Angela Vlug Clinical Research Bureau VUmc Wat is een IIS (volgens de NFU) Onderzoek waarvoor de raad van bestuur van een (universitair) medisch centrum
HOVON 141 CLL. Instructies voor de deelnemende site: ICF studie template aanpassen naar een lokaal biobank ICF
 Instructies voor de deelnemende site: ICF studie template aanpassen naar een lokaal biobank ICF Doel van deze studie template Deze studie template is bestemd voor de deelnemende sites in Nederland van
Instructies voor de deelnemende site: ICF studie template aanpassen naar een lokaal biobank ICF Doel van deze studie template Deze studie template is bestemd voor de deelnemende sites in Nederland van
Titel van het onderzoek: Bepaling van Zink en het Ontstekingseiwit PTX3 bij Patiënten met Sikkelcelziekte (ZIP studie)
 INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR PATIËNTEN Titel van het onderzoek: Bepaling van Zink en het Ontstekingseiwit PTX3 bij Patiënten met Sikkelcelziekte () Geachte heer/mevrouw, Wij vragen u om
INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR PATIËNTEN Titel van het onderzoek: Bepaling van Zink en het Ontstekingseiwit PTX3 bij Patiënten met Sikkelcelziekte () Geachte heer/mevrouw, Wij vragen u om
Voor$jdig stoppen van studies Job van der Palen METC Twente
 Voor$jdig stoppen van studies Job van der Palen METC Twente Waarom voor$jdig stoppen? Veiligheid Effec9viteit Fu9liteit Andere redenen Veiligheid (1) Data and Safety Monitoring Board (DSMB) OnaEankelijk!
Voor$jdig stoppen van studies Job van der Palen METC Twente Waarom voor$jdig stoppen? Veiligheid Effec9viteit Fu9liteit Andere redenen Veiligheid (1) Data and Safety Monitoring Board (DSMB) OnaEankelijk!
Handleiding website. Nieuwe of Littéraire Sociëteit De Witte, opgericht in 1802
 Handleiding website Nieuwe of Littéraire Sociëteit De Witte, opgericht in 1802 In deze handleiding website wordt stapsgewijs uitgelegd hoe u als lid kunt inloggen op de website van Sociëteit De Witte alsmede
Handleiding website Nieuwe of Littéraire Sociëteit De Witte, opgericht in 1802 In deze handleiding website wordt stapsgewijs uitgelegd hoe u als lid kunt inloggen op de website van Sociëteit De Witte alsmede
POLYP: een onderzoek naar de behandeling van galblaaspoliepen
 POLYP: een onderzoek naar de behandeling van galblaaspoliepen Geachte heer/mevrouw, Versie 2, 05-04-2018 Bij u is vastgesteld dat u een poliep heeft in de galblaas. In Nederland wordt landelijk onderzoek
POLYP: een onderzoek naar de behandeling van galblaaspoliepen Geachte heer/mevrouw, Versie 2, 05-04-2018 Bij u is vastgesteld dat u een poliep heeft in de galblaas. In Nederland wordt landelijk onderzoek
1. Het verzoek en hetgeen daaraan ten grondslag wordt gelegd
 15 januari 2013 ADVIES (AA12.109) van de Codecommissie op verzoek van [X] op de voet van artikel 59 van het Reglement van de Codecommissie en de Commissie van Beroep van de Stichting Code Geneesmiddelenreclame,
15 januari 2013 ADVIES (AA12.109) van de Codecommissie op verzoek van [X] op de voet van artikel 59 van het Reglement van de Codecommissie en de Commissie van Beroep van de Stichting Code Geneesmiddelenreclame,
nwmo toetsingskader Eveline Loriaux - projectleider Kennisatelier 10 mei 2017 Vereniging Innovatieve Geneesmiddelen
 nwmo toetsingskader Eveline Loriaux - projectleider Kennisatelier 10 mei 2017 Vereniging Innovatieve Geneesmiddelen Zien we door de bomen nog het bos? 1 Overzicht nwmo Toetsingskader Start: juli 2015 Sinds
nwmo toetsingskader Eveline Loriaux - projectleider Kennisatelier 10 mei 2017 Vereniging Innovatieve Geneesmiddelen Zien we door de bomen nog het bos? 1 Overzicht nwmo Toetsingskader Start: juli 2015 Sinds
Handleiding Mobility Online online application Erasmus Placement
 Handleiding Mobility Online online application Erasmus Placement Deadlines Dossier Mobility Online In geval van Erasmus Placement moet je dossier in Mobility Online volledig in orde zijn tegen de volgende
Handleiding Mobility Online online application Erasmus Placement Deadlines Dossier Mobility Online In geval van Erasmus Placement moet je dossier in Mobility Online volledig in orde zijn tegen de volgende
GAIA handleiding aanbieder verkorte versie INHOUD
 INHOUD AANBIEDER 1 GAIA account aanmaken en autorisatie aanvragen (eenmalig)... 2 AANBIEDER 2 Korte instructie accreditatie aanvragen... 3 AANBIEDER 3 - instructie facturering binnen GAIA... 4 AANBIEDER
INHOUD AANBIEDER 1 GAIA account aanmaken en autorisatie aanvragen (eenmalig)... 2 AANBIEDER 2 Korte instructie accreditatie aanvragen... 3 AANBIEDER 3 - instructie facturering binnen GAIA... 4 AANBIEDER
Patiënteninformatieformulier imprint studie
 Patiënteninformatieformulier imprint studie (imaging of PSMA: Registratie en Inventarisatie voor Nederlandse Toepassing) Inleiding Uw arts heeft voorgesteld een aanvraag te doen voor een PSMA-PET-scan.
Patiënteninformatieformulier imprint studie (imaging of PSMA: Registratie en Inventarisatie voor Nederlandse Toepassing) Inleiding Uw arts heeft voorgesteld een aanvraag te doen voor een PSMA-PET-scan.
Informatiebrief. Kies Gerust op maat. Versie 11 oktober 2016
 Informatiebrief Kies Gerust op maat Versie 11 oktober 2016 Inhoud 1. Wat is het doel van het onderzoek? 2. Hoe wordt de zorg vanuit de huisarts onderzocht? 3. Hoe wordt het onderzoek uitgevoerd? 4. Wat
Informatiebrief Kies Gerust op maat Versie 11 oktober 2016 Inhoud 1. Wat is het doel van het onderzoek? 2. Hoe wordt de zorg vanuit de huisarts onderzocht? 3. Hoe wordt het onderzoek uitgevoerd? 4. Wat
Mutatieprocedure per aangetekende
 Mutatieprocedure per aangetekende e-mail Inhoudsopgave 1.... Algemeen principe en voorwaarden... 3 2.... Procedure... 4 3.... Handleiding... 5 Mutatieprocedure per aangetekende e-mail 1. Algemeen principe
Mutatieprocedure per aangetekende e-mail Inhoudsopgave 1.... Algemeen principe en voorwaarden... 3 2.... Procedure... 4 3.... Handleiding... 5 Mutatieprocedure per aangetekende e-mail 1. Algemeen principe
Nieuwe ontwikkelingen in regelgeving
 Nieuwe ontwikkelingen in regelgeving klinisch i onderzoek Monique Al NVMETC scholingsdagen 2015 Zwolle/Amsterdam Nieuwe en toekomstige wijzigingen WMO 1. Verzekeringsbesluit en CCMO richtlijn externe toetsing
Nieuwe ontwikkelingen in regelgeving klinisch i onderzoek Monique Al NVMETC scholingsdagen 2015 Zwolle/Amsterdam Nieuwe en toekomstige wijzigingen WMO 1. Verzekeringsbesluit en CCMO richtlijn externe toetsing
EU verordening geneesmiddelenonderzoek
 EU verordening geneesmiddelenonderzoek Beoordelingen Europese s/jl mul/na/onaal vs. na/onale aanvraag Let op: de beoordeling wordt niet bij u ingediend maar in Europa via een Europese portal De beoordeling
EU verordening geneesmiddelenonderzoek Beoordelingen Europese s/jl mul/na/onaal vs. na/onale aanvraag Let op: de beoordeling wordt niet bij u ingediend maar in Europa via een Europese portal De beoordeling
