Xiapex 0,9 mg poeder en oplosmiddel voor oplossing voor injectie. (Collagenase clostridium histolyticum)
|
|
|
- Marina Wauters
- 7 jaren geleden
- Aantal bezoeken:
Transcriptie
1 De Europese gezondheidsautoriteiten hebben bepaaide voorwaarden verbonden aan het in de handel brengen van het geneesmiddel XIAPEX. Het verplichte plan voor risicobeperking in Belgie, waarvan deze informatie deel uitmaakt, is een maatregel genomen om een veilig en doeltreffend gebruik van XIAPEX te waarborgen (RMA aangepaste versie 05/2016). Xiapex 0,9 mg poeder en oplosmiddel voor oplossing voor injectie. (Collagenase clostridium histolyticum) Informatieprogramma voor de artsen bij de behandeling van de ziekte van Dupuytren Dit materiaal bevat niet alle informatie. Voor de volledige informatie: Lees aandachtig de SKP vooraleer XIAPEX voor te schrijven (of te gebruiken). De volledige en geactualiseerde tekst van deze SKP is beschikbaar op de website rubriek "Bijsluiter en SKP van een geneesmiddel" Vergunninghouder : Swedish Orphan Biovitrum AB 1
2 Doel van het materiaal De houder van de vergunning voor het in de handel brengen zal erop toezien dat alle artsen die naar verwachting Xiapex zullen voorschrijven/gebruiken, goed voorgelicht worden over de juiste toediening van het geneesmiddel en dat zij ervaring hebben in de diagnose en behandeling van de contractuur van Dupuytren en van de ziekte van Peyronie. De houder van de vergunning voor het in de handel brengen zal, in overeenstemming met de bevoegde instanties in de lidstaten, vóór de introductie een voorlichtingsprogramma voor artsen implementeren om ervoor te zorgen - dat het injecteren op de juiste wijze wordt uitgevoerd om het optreden van injectiegerelateerde bijwerkingen te minimaliseren en - om hen te informeren over, met de behandeling samenhangende, verwachte en potentiële risico s. Het voorlichtingsprogramma voor artsen zal uit de volgende belangrijke onderdelen bestaan: Injectietechniek en doseringsinterval. De juiste volumina voor zowel de reconstitutie- als de injectieverschillen tussen de metacarpofalangeale (MP) en proximale interfalangeale (PIP) gewrichten voor contractuur van Dupuytren en voor plaque van de ziekte van Peyronie. Herkenning en behandeling van ernstige immunologische reacties, met inbegrip van anafylaxie. Informatie over de kans op bloedingen bij patiënten met stollingsstoornissen, waaronder patiënten die gelijktijdig anticoagulantia gebruiken. Informatie over het potentiële risico van kruisreactiviteit met matrixmetalloproteïnase- (MMP), waaronder de ontwikkeling van het musculoskeletaal syndroom en de exacerbatie/initiatie van auto-immuunstoornissen. Herinnering aan de noodzaak om bijwerkingen, inclusief medicatiefouten, te melden. De noodzaak de patiënt op de hoogte te stellen van de met de behandeling samenhangende verschijnselen en symptomen en wanneer hulp van een zorgverlener moet worden ingeroepen. Belangrijke productinformatie Therapeutische indicaties (vanaf 18 jaar) XIAPEX is geïndiceerd voor de behandeling van contractuur van Dupuytren bij volwassenen met een palpabele streng. Xiapex is ook geïndiceerd voor de behandeling van volwassen mannen met de ziekte van Peyronie met een palpabele plaque en kromstand van ten minste 30 graden bij het begin van de therapie, maar deze indicatie maakt deel uit van een ander RMA programma Dosering en wijze van toediening Xiapex moet worden toegediend door een arts 1. die voldoende getraind is in de correcte toediening van het product 2. en die ervaring heeft met het diagnosticeren en behandelen van de ziekte van Dupuytren. Dosering De aanbevolen dosering is 0,58 mg Xiapex per injectie in een palpabele streng bij de ziekte van Dupuytren. Het volume van gereconstitueerd Xiapex dat moet worden toegediend in de streng van Dupuytren verschilt, afhankelijk van het type gewricht dat wordt behandeld (zie Tabel 1). Ongeveer uur na de injectie kan, voor zover nodig, geprobeerd worden de vinger(s) te strekken (vingerstrekprocedure) om disruptie van de streng te vergemakkelijken. 2
3 Als er geen bevredigende respons wordt bereikt, kunnen de injectie en de vingerstrekprocedures na ongeveer 4 weken worden herhaald. Met tussenpozen van ongeveer 4 weken kan tot 3 keer per streng een injectie worden toegediend en een vingerstrekprocedure worden verricht. Ervaring met Xiapex in klinisch onderzoek is momenteel beperkt tot maximaal 3 injecties per streng en tot maximaal 8 injecties in totaal. Als de ziekte heeft geleid tot meervoudige contracturen, moet de behandeling van elke streng in een sequentiële volgorde behandeld worden zoals bepaald door de arts. Ervaring met Xiapex in klinisch onderzoek is momenteel beperkt tot maximaal 3 injecties per streng en tot maximaal 8 injecties in totaal. In maximaal twee strengen of twee aangetaste gewrichten in dezelfde hand kunnen tijdens een behandelbezoek injecties worden toegediend overeenkomstig de injectieprocedure. Tijdens een behandelbezoek kan een injectie worden toegediend in twee palpabele strengen die twee gewrichten hebben aangetast, of kan in één palpabele streng die twee gewrichten heeft aangetast in dezelfde vinger een injectie op twee plaatsen worden toegediend. Elke injectie bevat een dosis van 0,58 mg. Als de ziekte heeft geleid tot meervoudige contracturen, kunnen bijkomende strengen worden behandeld tijdens andere behandelbezoeken met een tussenperiode van ongeveer 4 weken. Vingerstrekprocedure (24-72h na de XIAPEX-injectie) Patiënten dienen geïnstrueerd te worden om ongeveer uur na de injectie bij hun arts langs te gaan voor een onderzoek van de behandelde hand en een vingerstrekprocedure, om de streng te breken. voor een onderzoek van de behandelde hand en een vingerstrekprocedure, die de disruptie van de streng vergemakkelijkt. Wijze van toediening Intralaesionaal gebruik. Uitsluitend bestemd voor éénmalig gebruik. Volume voor reconstitutie Xiapex moet vóór gebruik uitsluitend met het meegeleverde oplosmiddel en tot het juiste volume worden gereconstitueerd: Gebruik 0,39 ml oplosmiddel voor metacarpofalangeale gewrichten (MP-gewrichten). Gebruik 0,31 ml oplosmiddel voor proximale interfalangeale gewrichten (PIP-gewrichten), (zie Tabel 1). Volume voor injectie Voor strengen die MP-gewrichten hebben aangetast wordt elke dosering toegediend in een injectievolume van 0,25 ml. Voor strengen die PIP-gewrichten hebben aangetast wordt elke dosering toegediend in een injectievolume van 0,20 ml. 3
4 Tabel 1 Benodigde volumes voor reconstitutie en toediening Te behandelen gewricht Vereiste oplosmiddel voor reconstitutie Injectievolume om dosering van 0,58 mg Xiapex toe te dienen MP-gewrichten 0,39 ml 0,25 ml PIP-gewrichten 0,31 ml 0,20 ml Merk op dat het injectievolume voor toediening van een dosering van 0,58 mg minder is dan het totale volume van het oplosmiddel dat wordt gebruikt voor reconstitutie. Patiënten dienen de volgende instructies te krijgen: Om extravasatie van XIAPEX uit de streng te voorkomen, mogen de vingers van de behandelde hand pas worden gebogen of gestrekt nadat de vingerstrekprocedure is verricht (volgende dag). De patiënt mag op geen enkel moment proberen zelf de behandelde streng te breken De behandelde hand moet tot de dag na de vingerstrekprocedure zoveel mogelijk omhoog worden gehouden Zie voor gedetailleerde instructies voor de arts voor het bereiden van het geneesmiddel voor injectie (reconstitutieprocedure) rubriek 6.6 Instructies voor gebruik en handelen Bereiding - Reconstitutieprocedure De injectieflacon met één dosering Xiapex en de injectieflacon met één dosering oplosmiddel voor oplossing voor injectie voor reconstitutie moeten in de koelkast bewaard worden. Neem vóór gebruik de injectieflacon met het gevriesdroogde Xiapex-poeder en de injectieflacon met het verdunningsmiddel voor reconstitutie uit de koelkast en laat de twee injectieflacons gedurende ten minste 15 minuten, maar niet langer dan 60 minuten, op kamertemperatuur staan. De procedure voor reconstitutie moet op volgende wijze aseptisch gebeuren: 1. Controleer welk gewricht moet worden behandeld (metacarpofalangeale [MP] of proximale interfalangeale [PIP]), want het volume van het oplosmiddel dat nodig is voor reconstitutie wordt bepaald door het type gewricht (bij een PIP-gewricht is een kleiner volume voor injectie nodig). 2. Veeg, na het verwijderen van de flip-off -dop van beide injectieflacons, met een watje met steriele alcohol (er mogen geen andere ontsmettingsmiddelen worden gebruikt) en met gebruikmaking van een aseptische techniek de rubberen stop en het gebied daaromheen van de injectieflacon die Xiapex bevat en de injectieflacon die het verdunningsmiddel voor reconstitutie bevat schoon. 3. Gebruik uitsluitend het meegeleverde verdunningsmiddel voor reconstitutie; het verdunningsmiddel bevat calcium dat nodig is voor de werking van Xiapex. Gebruik een injectiespuit van 1 ml met een schaalverdeling van 0,01 ml en zuig het juiste volume van het meegeleverde verdunningsmiddel op: 0,39 ml oplosmiddel voor een streng die een MP-gewricht heeft aangetast 0,31 ml oplosmiddel voor een streng die een PIP-gewricht heeft aangetast 4. Injecteer het verdunningsmiddel langzaam langs de zijkanten van de injectieflacon met het gevriesdroogde poeder van Xiapex. Keer de injectieflacon niet om en schud de oplossing ook niet. Zwenk de oplossing langzaam, zodat alle gevriesdroogde poeder wordt opgenomen in de oplossing. 5. De gereconstitueerde Xiapex-oplossing moet helder zijn. Controleer de oplossing vóór toediening visueel op vreemde deeltjes en verkleuring. Als de oplossing deeltjes bevat, troebel is of verkleurd is, mag de gereconstitueerde oplossing niet worden geïnjecteerd. 4
5 6. De gereconstitueerde Xiapex-oplossing kan vóór toediening maximaal één uur bij kamertemperatuur (20 C tot 25 C) en maximaal 4 uur in de koelkast (2 C tot 8 C) worden bewaard. In de koelkast bewaarde gereconstitueerde Xiapex-oplossing moet gedurende ongeveer 15 minuten vóór gebruik weer op kamertemperatuur komen. Elke Xiapex-injectieflacon en steriel oplosmiddel voor reconstitutie dient alleen te worden gebruikt voor een enkele injectie. Indien strengen van twee aangetaste gewrichten van dezelfde hand moeten worden behandeld tijdens een behandelbezoek, dienen voor elke reconstitutie en injectie afzonderlijke injectieflacons en spuiten te worden gebruikt. Injectieprocedure Toediening van een lokaal anestheticum voorafgaande aan de injectie van Xiapex wordt afgeraden, want dit kan de juiste plaatsing van de injectie belemmeren. 1. Herbevestig de te behandelen streng. De gekozen plaats voor injectie moet het gebied zijn waar de streng maximaal gescheiden is van de onderliggende flexorpezen en waar de huid niet stevig aan de streng vastzit. 2. Breng een ontsmettingsmiddel aan op de plaats van injectie en laat de huid opdrogen. 3. Zuig met een nieuwe, steriele, hubless injectiespuit met 0,01 ml schaalverdeling en een permanent aangebrachte naald met een diameter van 26 of 27 gauge en een lengte van 12 of 13 mm (wordt niet meegeleverd) de juiste hoeveelheid gereconstitueerde oplossing op voor een 0,58 mg dosering van Xiapex die nodig is voor de injectie. 0,25 ml gereconstitueerd Xiapex voor een streng die een MP-gewricht heeft aangetast, of 0,20 ml gereconstitueerd Xiapex voor een streng die een PIP-gewricht heeft aangetast. 4. Wees voorzichtig met strengen die dicht bij het PIP-flexorplooigebied liggen. Bij het injecteren in een streng die een PIP-gewricht van de vijfde vinger (pink) heeft aangetast, moet dit zo dicht mogelijk bij de plooi tussen vinger en handpalm gebeuren en moet de naald niet dieper dan 2 tot 3 mm worden ingebracht. Injecteer voor PIP-gewrichten niet verder dan 4 mm distaal van de plooi tussen vinger en handpalm. 5. Fixeer met uw niet-dominante hand de te behandelen hand van de patiënt en houd tegelijkertijd de streng onder spanning. Plaats met uw dominante hand de naald in de streng, waarbij u ervoor moet zorgen dat de naald in de streng blijft. Vermijd dat de naaldpunt helemaal door de streng heen wordt gestoken om het risico dat Xiapex in andere weefsels dan de streng wordt geïnjecteerd tot een minimum te beperken. Als u na het plaatsen van de naald vreest dat de naald zich mogelijk in de flexorpees bevindt, pas dan enige passieve beweging van het distale interfalangeale gewricht (DIP-gewricht) toe. Indien wordt vermoed dat de naald in een pees is ingebracht of als de patiënt paresthesie ervaart, moet u de naald terugtrekken en opnieuw in de streng plaatsen. Als de naald zich op de juiste plaats bevindt, zal er enige weerstand worden gevoeld tijdens de injectieprocedure. Zie Afbeelding 1 hieronder voor een illustratie van de injectietechniek. 6. Nadat u hebt gecontroleerd of de naald zich correct in de streng bevindt, injecteert u ongeveer een derde van de dosering. 7. Trek de naaldpunt vervolgens uit de streng en breng deze ongeveer 2 à 3 mm distaal van de oorspronkelijke injectieplaats weer in de streng in en injecteer nogmaals een derde van de dosering. Houd hierbij de naaldpunt te allen tijde onder de huid. 8. Trek de naaldpunt vervolgens opnieuw uit de streng en breng deze nu ongeveer 2 à 3 mm proximaal van de oorspronkelijke injectieplaats weer in de streng in en injecteer de overblijvende portie van de dosering in de streng. Houd hierbij de naaldpunt te alle tijde onder de huid. (zie Afbeelding 2) Afbeeldingen 1 en 2 hieronder zijn uitsluitend bedoeld voor illustratieve doeleinden en zijn mogelijk niet representatief voor de precieze locatie van anatomische structuren bij een individuele patiënt. 5
6 9. Wikkel een zacht, dik gaasverband om de behandelde hand van de patiënt. 10. Gooi het ongebruikte deel van de gereconstitueerde oplossing en oplosmiddel na injectie weg. Bewaar, meng of gebruik geen injectieflacons die ongebruikte gereconstitueerde oplossing of oplosmiddel bevatten. 11. Patiënten dienen de volgende instructies te krijgen: Om extravasatie van Xiapex uit de streng te voorkomen, mogen de vingers van de hand waarin de injectie is toegediend pas worden gebogen of gestrekt als de vingerstrekprocedure is voltooid. Probeer op geen enkel moment zelf de streng te breken. Houd de hand waarin de injectie is toegediend tot de dag na de vingerstrekprocedure zoveel mogelijk omhoog. Vingerstrekprocedure Neem onmiddellijk contact op met de arts als er aanwijzingen zijn voor een infectie (bijvoorbeeld koorts, koude rillingen, toenemende roodheid of vochtophoping) of als de vinger moeilijk gebogen kan worden nadat de zwelling is verminderd (symptoom van peesruptuur) uur na de behandeling moet de patiënt bij zijn/haar arts langsgaan voor een onderzoek van de behandelde hand en mogelijk een vingerstrekprocedure om disruptie van de streng te faciliteren. 1. Stel tijdens het controlebezoek uur na de injectie vast of de contractuur is verdwenen. Als deze niet is verdwenen, zal een passieve vingerstrekprocedure uitgevoerd worden om te proberen de structuur van de streng te verstoren. 2. Indien nodig kan de vingerstrekprocedure onder plaatselijke verdoving worden verricht. 3. Zorg dat de pols van de patiënt in de gebogen stand staat en pas belasting toe op de behandelde streng door de vinger ongeveer 10 à 20 seconden met matige kracht te strekken. Zorg dat het MP-gewricht in de gebogen stand staat wanneer de vingerstrekprocedure wordt uitgevoerd bij een streng die het PIP-gewricht heeft aangetast. 6
7 4. Als de eerste vingerstrekprocedure geen disruptie van de streng tot gevolg heeft, kan een tweede of derde poging worden gedaan met tussenpozen van 5 à 10 minuten. Het wordt afgeraden om meer dan drie strekpogingen te doen, per aangetast gewricht. 5. Als de streng na 3 strekpogingen nog niet is onderbroken, kan een controlebezoek worden gepland dat ongeveer 4 weken na de injectie plaatsvindt. Als de streng ook tijdens dat bezoek niet verdwenen blijkt te zijn, kan een aanvullende injectie en vingerstrekprocedure worden verricht. Indien strengen van twee aangetaste gewrichten in één vinger worden behandeld, voer dan de vingerstrekprocedure uit op de streng die het MPgewricht aantast voordat de procedure wordt uitgevoerd op de streng die het PIP gewricht aantast 6. Nadat de vingerstrekprocedure(s) is/zijn verricht en bij de patiënt een spalk is aangelegd (met het behandelde gewricht in maximaal gestrekte stand), dient de patiënt de volgende instructies te worden gegeven: Ontzie de behandelde hand en belast deze pas weer normaal als u daar toestemming voor krijgt. Draag de spalk s nachts tot 4 maanden. Voer gedurende enkele maanden enkele keren per dag een reeks vingerbuig- en vingerstrekoefeningen uit. Bijzondere waarschuwingen en voorzorgen bij gebruik Allergische reacties Na injectie van Xiapex kan een hevige allergische reactie optreden en patiënten moeten gedurende 30 minuten worden geobserveerd voordat ze de kliniek verlaten om te controleren op eventuele klachten of symptomen van een ernstige allergische reactie, bijvoorbeeld uitgebreide roodheid of uitslag, zwelling, benauwd gevoel in de keel of ademhalingsproblemen. Patiënten moeten de instructie krijgen om onmiddellijk een arts te raadplegen als zij een van deze klachten of symptomen hebben. Medicatie voor spoedeisende gevallen voor behandeling van mogelijke allergische reacties moet beschikbaar zijn. Een anafylactische reactie is gemeld in een klinische postmarketingstudie bij een patiënt die eerder was blootgesteld aan Xiapex voor de behandeling van een contractuur van Dupuytren, waaruit blijkt dat ernstige reacties, waaronder anafylaxie, kunnen optreden na injecties met Xiapex. Sommige patiënten met een contractuur van Dupuytren ontwikkelden IgE-antilichamen tegen het geneesmiddel in grotere percentages en hogere titers bij opeenvolgende injecties van Xiapex Patiënten met een contractuur van Dupuytren die is verkleefd met de huid kunnen een verhoogd risico op huidbeschadiging hebben als gevolg van het farmacologisch effect van Xiapex en de vingerstrekprocedure op de huid boven de te behandelen streng. Herkenning en behandeling van ernstige immunologische reacties, met inbegrip van anafylaxie Wegens het risico op ernstige immunologische reacties, waaronder een mogelijke anafylactische shock, moet de patiënt, na de XIAPEX -injectie, 30 minuten geobserveerd worden. Na de observatieperiode kan de patiënt de kliniek verlaten mits hij/zij stabiel is en geen tekenen van systemische overgevoeligheid of andere systemische bijwerkingen heeft vertoond. Als hij tekenen of symptomen van een ernstige allergische reactie ervaart, bijvoorbeeld roodheid of uitslag over een groot gebied, zwelling dichtgeknepen keel (moeilijkheden met slikken of borstbeklemming) of ademhalingsproblemen. (andere voorbeelden: herhaald niezen, duizeligheid, syncope...) 7
8 Peesruptuur of ander ernstig letsel aan de behandelde extremiteit XIAPEX mag uitsluitend worden geïnjecteerd in een bindweefselstreng die het gevolg is van de ziekte van Dupuytren. Omdat XIAPEX collageen oplost, moet voorzichtigheid worden betracht om te vermijden dat in pezen, zenuwen, bloedvaten of andere collageen bevattende structuren van de hand wordt geïnjecteerd. Injectie van XIAPEX in collageen bevattende structuren kan schade aan die structuren tot gevolg hebben en mogelijk permanent letsel, zoals een peesruptuur of schade aan ligamenten. Wanneer wordt geïnjecteerd in een streng die een PIPgewricht van de vijfde vinger heeft aangetast, mag de naald niet dieper worden ingebracht dan 2 tot 3 mm en niet verder dan 4 mm distaal van de plooi tussen handpalm en vinger. Patiënten dienen de instructie te krijgen dat ze onmiddellijk contact met de arts opnemen als ze de vinger niet goed kunnen buigen nadat de zwelling is verminderd (symptomen van peesruptuur). Patiënten met een contractuur van Dupuytren die is verkleefd met de huid kunnen een verhoogd risico op huidbeschadiging hebben als gevolg van het farmacologisch effect van XIAPEX en de vingerstrekprocedure op de huid boven de te behandelen streng. Postmarketing zijn gevallen van huidlaceratie gemeld waarbij een huidtransplantatie noodzakelijk was na vingerstrekprocedures. Klachten of symptomen die kunnen duiden op ernstig letsel van de behandelde vinger/hand na injectie of manipulatie moeten onmiddellijk worden geëvalueerd, omdat een chirurgische ingreep noodzakelijk kan zijn. In een gecontroleerd postmarketingonderzoek is een hoger percentage voor huidlaceratie voorgekomen na twee gelijktijdige injecties in dezelfde hand Gebruik bij patiënten met stollingsstoornissen XIAPEX moet voorzichtig worden gebruikt bij patiënten met stollingsstoornissen of bij hen die antistollingsmiddelen gebruiken. Bij de drie dubbelblinde, placebo-gecontroleerde, fase 3-onderzoeken, maakte 73% van de met XIAPEX behandelde patiënten melding van een ecchymose of een contusie en 38% van een bloeding op de injectieplaats. De werkzaamheid en veiligheid van XIAPEX is niet bekend bij patiënten die voorafgaand aan toediening van XIAPEX andere antistollingsmiddelen krijgen dan maximaal 150 mg acetylsalicylzuur per dag. Het gebruik van XIAPEX wordt afgeraden bij patiënten die binnen 7 dagen voorafgaand aan de toediening van een injectie met XIAPEX antistollingsmiddelen hebben gekregen (met uitzondering van maximaal 150 mg Acetylsalicylzuur per dag). Immunogeniteit Zoals bij het gebruik van elk geneesmiddel met niet-menselijk eiwit kunnen patiënten als reactie op het therapeutische eiwit antilichamen aanmaken. Tijdens klinische onderzoeken zijn bloedmonsters van patiënten met een contractuur van Dupuytren op meerdere tijdstippen onderzocht op antilichamen gericht tegen de eiwitbestanddelen van het geneesmiddel (AUX-I en AUX-II). Dertig dagen na de eerste injectie had 92% van de patiënten antilichamen gevormd tegen AUX-I en 86% van de patiënten tegen AUX-II. Er werd geen aanwijsbare correlatie waargenomen tussen de vorming van antilichamen en de klinische respons of bijwerkingen. Aangezien de enzymen in XIAPEX enige sequentiehomologie hebben met humane matrix metalloproteïnasen (MMP s), zouden antilichamen gericht tegen het geneesmiddel in theorie kunnen interfereren met 8
9 humane MMP s. Er zijn geen veiligheidsproblemen gerelateerd aan de remming van endogene MMP s waargenomen, in het bijzonder geen bijwerkingen die wijzen op het ontstaan of verergeren van auto-immuunziekten of het ontstaan van een musculoskeletaal syndroom (MSS). Hoewel er op basis van de huidige veiligheidsgegevens geen klinische aanwijzingen zijn dat een musculoskeletaal syndroom het gevolg kan zijn van toediening van XIAPEX, kan de mogelijkheid hiervan niet worden uitgesloten. Als dit syndroom zou ontstaan dan zou dit geleidelijk gebeuren, waarbij een of meer van de volgende tekenen en symptomen kenmerkend zijn: Artralgie Myalgie Gewrichtsstijfheid Stijfheid van de schouders Oedeem in de hand Palmaire fibrose Verdikking of vorming van nodules in de pezen Zelfs na de vingerstrekprocedure de patiënt op het volgende wijzen: Ontzie de behandelde hand en belast deze pas weer normaal als u daar toestemming voor krijgt. Draag de spalk s nachts tot 4 maanden. Voer gedurende enkele maanden enkele keren per dag een reeks vingerbuig- en vingerstrekoefeningen uit. Bijwerkingen De meest gemelde bijwerkingen tijdens klinisch onderzoek naar XIAPEX waren lokale reacties op de injectieplaats, zoals perifeer oedeem (rond de injectieplaats), contusie (waaronder ecchymose), bloeding op injectieplaats en pijn op injectieplaats. Reacties op de injectieplaats kwamen zeer vaak voor en traden bij de overgrote meerderheid van de patiënten op. De reacties waren meestal licht tot matig van ernst en verdwenen over het algemeen binnen 1 tot 2 weken na de injectie. De ernstige bijwerkingen die met betrekking tot het geneesmiddel werden gerapporteerd waren 6 gevallen van peesruptuur, 1 geval van tendinitis, 2 gevallen van ander ligamentletsel 2 gevallen van complex regionaal pijnsyndroom 1 geval van complex regionaal pijnsyndroom Anafylactische reactie werd gemeld bij een patiënt die eerder werd behandeld met Xiapex (1 geval) 9
10 Melden van bijwerkingen De gezondheidszorgbeoefenaars worden verzocht bijwerkingen van XIAPEX te melden aan het Belgisch Centrum voor Geneesmiddelenbewaking voor geneesmiddelen voor humaan gebruik (BCGH) van het FAGG. Het melden kan online gebeuren via of via de papieren gele fiche beschikbaar via het Gecommentarieerd Geneesmiddelenrepertorium en drie maal per jaar via de Folia Pharmacotherapeutica. De gele fiche kan worden verzonden naar het BCGH per post naar het adres FAGG BCGH Eurostation II Victor Hortaplein 40/ Brussel, per fax op het nummer 02/ , of per mail naar: 10
11 Informatie voor de patiënt De Patiënt moet ingelicht worden dat bijwerkingen kunnen en dat hij onmiddellijk zijn arts moet contacteren als hij tekenen of symptomen van een ernstige allergische reactie ervaart, bijvoorbeeld roodheid of uitslag over een groot gebied, zwelling dichtgeknepen keel (moeilijkheden met slikken of borstbeklemming) of ademhalingsproblemen. (andere voorbeelden: herhaald niezen, duizeligheid, syncope...) Andere bijwerkingen kunnen zich voordoen : De meest gemelde bijwerkingen tijdens klinisch onderzoek naar XIAPEX waren lokale reacties op de injectieplaats, zoals perifeer oedeem (rond de injectieplaats), contusie (waaronder ecchymose), bloeding op injectieplaats en pijn op injectieplaats. Reacties op de injectieplaats kwamen zeer vaak voor en traden bij de overgrote meerderheid van de patiënten op. De reacties waren meestal licht tot matig van ernst en verdwenen over het algemeen binnen 1 tot 2 weken na de injectie. Patiënten moeten de instructie worden gegeven om potentieel gevaarlijke activiteiten te vermijden, zoals autorijden of machines bedienen, totdat het veilig is om dat te doen of zoals geadviseerd door de arts 11
Bijsluiter: informatie voor de gebruiker. Xiapex 0,9 mg poeder en oplosmiddel voor oplossing voor injectie collagenase clostridium histolyticum
 Bijsluiter: informatie voor de gebruiker Xiapex 0,9 mg poeder en oplosmiddel voor oplossing voor injectie collagenase clostridium histolyticum Dit geneesmiddel is onderworpen aan aanvullende monitoring.
Bijsluiter: informatie voor de gebruiker Xiapex 0,9 mg poeder en oplosmiddel voor oplossing voor injectie collagenase clostridium histolyticum Dit geneesmiddel is onderworpen aan aanvullende monitoring.
RECONSTITUTIE, DOSERING EN TOEDIENING
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VELCADE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VELCADE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Xiapex 0,9 mg poeder en oplosmiddel voor oplossing voor injectie. (Collagenase clostridium histolyticum)
 De Europese gezondheidsautoriteiten hebben bepaaide voorwaarden verbonden aan het in de handel brengen van het geneesmiddel XIAPEX. Het verplichte plan voor risicobeperking in Belgie, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaaide voorwaarden verbonden aan het in de handel brengen van het geneesmiddel XIAPEX. Het verplichte plan voor risicobeperking in Belgie, waarvan deze informatie
CINRYZE (C1-REMMER [HUMAAN])
![CINRYZE (C1-REMMER [HUMAAN]) CINRYZE (C1-REMMER [HUMAAN])](/thumbs/66/54698885.jpg) De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CINRYZE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CINRYZE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Mysimba 8 mg/90 mg tabletten met verlengde afgifte. (naltrexonhydrochloride en bupropionhydrochloride)
 1 De Europese gezondheidsautoriteiten hebben bepaaide voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Mysimba 8 mg/90 mg tabletten met verlengde afgifte. Het verplichte plan voor
1 De Europese gezondheidsautoriteiten hebben bepaaide voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Mysimba 8 mg/90 mg tabletten met verlengde afgifte. Het verplichte plan voor
VISTABEL (botulinum toxine type A) Educatieve brochure voor artsen. 50 Allerganeenheden Poeder voor oplossing voor injectie
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VISTABEL. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VISTABEL. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Checklist voor voorschrijvers
 De Nederlandse en Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Jext. Het verplicht plan voor risicobeperking in Nederland en
De Nederlandse en Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Jext. Het verplicht plan voor risicobeperking in Nederland en
FLOLAN INFORMATIEGIDS VOOR PATIENTEN - FLOLAN
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
RECONSTITUTIE, DOSERING EN TOEDIENING
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VELCADE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VELCADE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
ZypAdhera. Informatie bestemd voor professionelen uit de gezondheidszorg en verpleegkundigen Risicobeleidsplan
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ZypAdhera. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ZypAdhera. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Belangrijke informatie voor zorgverleners over de nieuwe formulering van FLOLAN
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
NEBIDO (TESTOSTERONUNDECANOAAT) 1000 mg/4 ml oplossing voor injectie GIDS VOOR DE VOORSCHRIJVER
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nebido. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nebido. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
BROCHURE VOOR RECONSTITUTIE, DOSERING EN TOEDIENING
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Bortezomib Sandoz 3,5 mg poeder voor oplossing voor injectie. Het verplicht
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Bortezomib Sandoz 3,5 mg poeder voor oplossing voor injectie. Het verplicht
Informatiefiche voor artsen voor een veilig en doeltreffend gebruik van het geneesmiddel
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de
VALDOXAN. (agomelatine) Informatie voor beroepsbeoefenaren in de gezondheidszorg: Aanbevelingen met betrekking tot:
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Valdoxan 25 mg. Het verplicht plan voor risicobeperking in België, waarvan deze
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Valdoxan 25 mg. Het verplicht plan voor risicobeperking in België, waarvan deze
Gelieve de patiëntenwaarschuwingskaart van Entyvio in te vullen en te overhandigen aan elke patiënt.
 Deze informatie maakt deel uit van het Belgische en Luxemburgse risicobeheerplan, dat informatiemateriaal beschikbaar stelt aan gezondheidszorgbeoefenaars (en patiënten). Deze bijkomende risicobeperkende
Deze informatie maakt deel uit van het Belgische en Luxemburgse risicobeheerplan, dat informatiemateriaal beschikbaar stelt aan gezondheidszorgbeoefenaars (en patiënten). Deze bijkomende risicobeperkende
Dit geneesmiddel is onderworpen aan aanvullende monitoring
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Alofisel. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Alofisel. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
VOORLICHTINGSBROCHURE VOOR DE GEZONDHEIDSZORGBEOEFENAAR
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ACCUSOL 35. Het verplicht plan voor risicobeperking in België, waarvan deze
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ACCUSOL 35. Het verplicht plan voor risicobeperking in België, waarvan deze
BOTOX (botulinum toxine type A) Educatieve brochure voor artsen. 100 Allerganeenheden Poeder voor oplossing voor injectie
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel BOTOX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel BOTOX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Jext : Instructies voor gebruik
 RMA versie 06/2017 Jext : Instructies voor gebruik 1 2 3 4 Ik heb een risico op anafylaxie, een levensbedreigende allergische reactie op: Als ik niet in staat ben om mezelf te helpen, volg dan de instructies
RMA versie 06/2017 Jext : Instructies voor gebruik 1 2 3 4 Ik heb een risico op anafylaxie, een levensbedreigende allergische reactie op: Als ik niet in staat ben om mezelf te helpen, volg dan de instructies
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL Xiapex 0,9 mg poeder en oplosmiddel voor oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke injectieflacon
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL Xiapex 0,9 mg poeder en oplosmiddel voor oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke injectieflacon
Selectie en training van patiënten voor thuistoediening van Nplate
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Dit verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Dit verplicht plan voor risicobeperking in België, waarvan deze informatie
LEIDRAAD VOOR BEROEPSBEOEFENAREN IN DE GEZONDHEIDSZORG
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel KANUMA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel KANUMA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
In geval van vermoedelijke onjuiste toediening van Depo-Eligard moeten de testosteronespiegels bepaald worden.
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
CINRYZE (C1-REMMER [HUMAAN])
![CINRYZE (C1-REMMER [HUMAAN]) CINRYZE (C1-REMMER [HUMAAN])](/thumbs/66/54698857.jpg) De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CINRYZE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CINRYZE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Servier Benelux S.A. PROTELOS. (strontiumranelaat) GIDS EN CHECKLIST VOOR DE ARTS
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Protelos 2 g. Het verplicht plan voor risicobeperking in België, waarvan deze
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Protelos 2 g. Het verplicht plan voor risicobeperking in België, waarvan deze
Educatief materiaal. EFIENT (Prasugrel) Dit geneesmiddel is onderworpen aan aanvullende monitoring.
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel EFIENT. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel EFIENT. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
VALDOXAN (agomelatine) Informatie voor beroepsbeoefenaren in de gezondheidszorg. Aanbevelingen met betrekking tot:
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Valdoxan 25 mg. Het verplicht plan voor risicobeperking in België, waarvan deze
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Valdoxan 25 mg. Het verplicht plan voor risicobeperking in België, waarvan deze
EDUCATIEVE INFORMATIE VOOR PATIËNTEN
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel BOCOUTURE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel BOCOUTURE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
NEBIDO (TESTOSTERONUNDECANOAAT) 1000 mg/4 ml oplossing voor injectie
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nebido. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nebido. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Postdatum. Geachte Dokter,
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Quetiapine Krka 50 mg / 200 mg / 300 mg/400 mg tabletten met verlengde afgifte.
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Quetiapine Krka 50 mg / 200 mg / 300 mg/400 mg tabletten met verlengde afgifte.
Vectibix (panitumumab) Educatief materiaal voor de arts
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Vectibix. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Vectibix. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Directe communicatie aan gezondheidszorgbeoefenaars over de associatie van Sprycel (dasatinib) met Pulmonaire Arteriële Hypertensie (PAH)
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Informatie verspreid onder het gezag van het federaal agentschap voor geneesmiddelen en gezondheidsproducten
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Kyleena (19,5 mg levonorgestrel) afleveringsysteem voor intra-uterien gebruik
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Kyleena. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Kyleena. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Handleiding voor zorgverleners
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel Toujeo. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel Toujeo. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
BIJSLUITER: INFORMATIE VOOR DE PATIËNT
 BIJSLUITER: INFORMATIE VOOR DE PATIËNT, gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt want er staat belangrijke informatie voor u in. Bewaar deze bijsluiter. Misschien heeft
BIJSLUITER: INFORMATIE VOOR DE PATIËNT, gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt want er staat belangrijke informatie voor u in. Bewaar deze bijsluiter. Misschien heeft
Risico minimalisatie materiaal betreffende testosteronundecanoaat voor beroepsbeoefenaren in de gezondheidszorg
 Risico minimalisatie materiaal betreffende testosteronundecanoaat voor beroepsbeoefenaren in de gezondheidszorg De risico minimalisatie materialen voor testosteronundecanoaat zijn beoordeeld door het College
Risico minimalisatie materiaal betreffende testosteronundecanoaat voor beroepsbeoefenaren in de gezondheidszorg De risico minimalisatie materialen voor testosteronundecanoaat zijn beoordeeld door het College
Samenvatting. 26 juni 2015
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
ENKEL VOOR NON HODGKIN LYMFOOM (NHL)
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel MabThera oplossing voor subcutane injectie (SC). Het verplicht plan voor risicobeperking
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel MabThera oplossing voor subcutane injectie (SC). Het verplicht plan voor risicobeperking
Capecitabine Accord moet permanent worden stopgezet bij patiënten die een ernstige huidreactie hebben gehad tijdens de behandeling.
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Onderwerp: Ernstige huidreacties geassocieerd met Capecitabine (Xeloda )
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Educatief materiaal voor gezondheidsbeoefenaars (Powerpointpresentatie)
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel BOCOUTURE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel BOCOUTURE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
(asfotase alfa) 40 mg/ml 100 mg/ml oplossing voor injectie (asfotase-alfa) INJECTIEHANDLEIDING. Ouders/zorgverleners van jonge patiënten
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel STRENSIQ. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel STRENSIQ. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
PATIËNTENHANDLEIDING VOOR ZELFINJECTIE
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel STRENSIQ. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel STRENSIQ. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Belangrijke informatie voor beroepsbeoefenaren
 De gezondheidsautoriteiten van de Europese Unie hebben het in de handel brengen van het geneesmiddel Kadcyla verbonden aan bepaalde voorwaarden. Het verplichte farmacovigilantieplan ter minimalisatie van
De gezondheidsautoriteiten van de Europese Unie hebben het in de handel brengen van het geneesmiddel Kadcyla verbonden aan bepaalde voorwaarden. Het verplichte farmacovigilantieplan ter minimalisatie van
INSTRUCTIES VOOR HET BEREIDEN EN TOEDIENEN VAN DE SOMAVERT INJECTIE
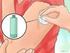 INSTRUCTIES VOOR HET BEREIDEN EN TOEDIENEN VAN DE SOMAVERT INJECTIE Inleiding In de volgende instructies wordt uitgelegd hoe SOMAVERT moet worden bereid en geïnjecteerd. Lees deze instructies aandachtig
INSTRUCTIES VOOR HET BEREIDEN EN TOEDIENEN VAN DE SOMAVERT INJECTIE Inleiding In de volgende instructies wordt uitgelegd hoe SOMAVERT moet worden bereid en geïnjecteerd. Lees deze instructies aandachtig
INFORMATIE VOOR DE ARTS
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Azzalure. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Azzalure. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
RECONSTITUTIE, DOSERING EN TOEDIENING
 Additioneel risico minimalisatie materiaal betreffende bortezomib voor beroepsbeoefenaren in de gezondheidszorg Belangrijke informatie over de RECONSTITUTIE, DOSERING EN TOEDIENING van bortezomib 3,5 mg
Additioneel risico minimalisatie materiaal betreffende bortezomib voor beroepsbeoefenaren in de gezondheidszorg Belangrijke informatie over de RECONSTITUTIE, DOSERING EN TOEDIENING van bortezomib 3,5 mg
GIDS VOOR DE VOORSCHRIJVER
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel Cerdelga. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel Cerdelga. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
BIJSLUITER: INFORMATIE VOOR DE PATIËNT
 BIJSLUITER 1 BIJSLUITER: INFORMATIE VOOR DE PATIËNT PURETHAL Pollen, suspensie voor injectie voor subcutaan gebruik Gezuiverde allergenen uit een mengsel van 10 grassen Lees goed de hele bijsluiter voordat
BIJSLUITER 1 BIJSLUITER: INFORMATIE VOOR DE PATIËNT PURETHAL Pollen, suspensie voor injectie voor subcutaan gebruik Gezuiverde allergenen uit een mengsel van 10 grassen Lees goed de hele bijsluiter voordat
CEREZYME (imiglucerase)
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CEREZYME. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CEREZYME. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
INFORMATIE VOOR DE PATIËNT
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Azzalure. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Azzalure. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
1. WAT IS ORGALUTRAN EN WAARVOOR WORDT HET GEBRUIKT?
 In deze bijsluiter komen de volgende onderdelen aan bod: 1. Wat is Orgalutran en waarvoor wordt het gebruikt? 2. Wat u moet weten voordat u Orgalutran gebruikt 3. Hoe wordt Orgalutran gebruikt? 4. Mogelijke
In deze bijsluiter komen de volgende onderdelen aan bod: 1. Wat is Orgalutran en waarvoor wordt het gebruikt? 2. Wat u moet weten voordat u Orgalutran gebruikt 3. Hoe wordt Orgalutran gebruikt? 4. Mogelijke
BIJSLUITER: INFORMATIE VOOR DE PATIËNT. Aprokam 50 mg poeder voor oplossing voor injectie. Cefuroxim
 BIJSLUITER: INFORMATIE VOOR DE PATIËNT Aprokam 50 mg poeder voor oplossing voor injectie Cefuroxim Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
BIJSLUITER: INFORMATIE VOOR DE PATIËNT Aprokam 50 mg poeder voor oplossing voor injectie Cefuroxim Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING. Vi-polysaccharide van Salmonella typhi (Ty2 stam)
 1. NAAM VAN HET GENEESMIDDEL Typherix, oplossing voor injectie in een voorgevulde spuit Tyfus polysaccharidevaccin 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke dosis vaccin à 0,5 ml bevat: Vi-polysaccharide
1. NAAM VAN HET GENEESMIDDEL Typherix, oplossing voor injectie in een voorgevulde spuit Tyfus polysaccharidevaccin 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke dosis vaccin à 0,5 ml bevat: Vi-polysaccharide
MEDICA KEELSPRAY MENTHOL, 20 mg/10 ml; 5 mg/10 ml, spray voor oromucosaal gebruik Chloorhexidine gluconaat - Lidocaïne hydrochloride
 MEDICA KEELSPRAY MENTHOL, 20 mg/10 ml; 5 mg/10 ml, spray voor oromucosaal gebruik Chloorhexidine gluconaat - Lidocaïne hydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken,
MEDICA KEELSPRAY MENTHOL, 20 mg/10 ml; 5 mg/10 ml, spray voor oromucosaal gebruik Chloorhexidine gluconaat - Lidocaïne hydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken,
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING. Actief bestanddeel: Gezuiverd capsulair Vi polyoside van Salmonella typhi (stam Ty2): 25 microgram
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL TYPHIM Vi, 25 microgram/dosis, oplossing voor injectie Polyoside buiktyfusvaccin 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Eén dosis
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL TYPHIM Vi, 25 microgram/dosis, oplossing voor injectie Polyoside buiktyfusvaccin 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Eén dosis
1. WAT IS DURATEARS EN WAARVOOR WORDT DIT MIDDEL GEBRUIKT?
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER DURATEARS Oogzalf Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor u. Gebruik dit geneesmiddel
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER DURATEARS Oogzalf Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor u. Gebruik dit geneesmiddel
Het gebruik van APIDRA in injectieflacon
 EEN GIDS VOOR ALS U BEGINT MET APIDRA (insuline glulisine) 1x 10ML INJECTIEFLACON (100 Eenheden/ml) De Apidra 100 eenheden/ml oplossing voor injectie (in injectieflacon) wordt in een injectieflacon geleverd
EEN GIDS VOOR ALS U BEGINT MET APIDRA (insuline glulisine) 1x 10ML INJECTIEFLACON (100 Eenheden/ml) De Apidra 100 eenheden/ml oplossing voor injectie (in injectieflacon) wordt in een injectieflacon geleverd
VICTRELIS Boceprevir
 De gezondheidsautoriteiten van de EU hebben een aantal voorwaarden gekoppeld aan het in de handel brengen van het geneesmiddel VICTRELIS. Het verplichte plan voor risicobeperking in België, waarvan deze
De gezondheidsautoriteiten van de EU hebben een aantal voorwaarden gekoppeld aan het in de handel brengen van het geneesmiddel VICTRELIS. Het verplichte plan voor risicobeperking in België, waarvan deze
Selectie en training van volwassen * patiënten voor thuistoediening van Nplate
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
INFORMATIEGIDS VOOR PATIENTEN
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
INJECTIEHANDLEIDING BETREFFENDE ASFOTASE-ALFA VOOR OUDERS EN ZORGVERLENERS VAN JONGE PATIËNTEN
 INJECTIEHANDLEIDING BETREFFENDE ASFOTASE-ALFA VOOR OUDERS EN ZORGVERLENERS VAN JONGE PATIËNTEN Lees aandachtig de bijsluiter alvorens u asfotase-alfa gebruikt. Versie 1 - januari 2018 Inleiding Deze materialen
INJECTIEHANDLEIDING BETREFFENDE ASFOTASE-ALFA VOOR OUDERS EN ZORGVERLENERS VAN JONGE PATIËNTEN Lees aandachtig de bijsluiter alvorens u asfotase-alfa gebruikt. Versie 1 - januari 2018 Inleiding Deze materialen
RECONSTITUTIE, DOSERING EN TOEDIENING
 Belangrijke informatie over de RECONSTITUTIE, DOSERING EN TOEDIENING van bortezomib 3,5 mg injectieflacon voor subcutaan (SC) en intraveneus (IV) gebruik Teva Nederland BV Swensweg 5 Postbus 552 2003 RN
Belangrijke informatie over de RECONSTITUTIE, DOSERING EN TOEDIENING van bortezomib 3,5 mg injectieflacon voor subcutaan (SC) en intraveneus (IV) gebruik Teva Nederland BV Swensweg 5 Postbus 552 2003 RN
Kineret (anakinra) Educatief materiaal voor beroepsbeoefenaren in de gezondheidszorg
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Kineret. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Kineret. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Inhoud: 1) Informatiefolder voor de patiënt (met bijgevoegde audio-cd) 2) Bijsluiter: informatie voor gebruikers
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel OZURDEX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel OZURDEX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Hemlibra (emicizumab) Subcutane injectie Dit geneesmiddel is onderworpen aan aanvullende monitoring. Informatiebrochure voor de patiënt/verzorger
 Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel Hemlibra, om voor een goed gebruik ervan te zorgen en om de ongewenste effecten ervan te beperken, zijn er bepaalde
Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel Hemlibra, om voor een goed gebruik ervan te zorgen en om de ongewenste effecten ervan te beperken, zijn er bepaalde
Bijsluiter: informatie voor de gebruiker. Neurobion 100 mg 100 mg 1 mg / 3 ml oplossing voor injectie Vitaminen B 1 + B 6 + B 12
 Bijsluiter: informatie voor de gebruiker Neurobion 100 mg 100 mg 1 mg / 3 ml oplossing voor injectie Vitaminen B 1 + B 6 + B 12 Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want
Bijsluiter: informatie voor de gebruiker Neurobion 100 mg 100 mg 1 mg / 3 ml oplossing voor injectie Vitaminen B 1 + B 6 + B 12 Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want
Ustekinumab. (Stelara) Dermatologie
 Ustekinumab (Stelara) Dermatologie Inhoudsopgave Inleiding 4 1. Hoe werkt Ustekinumab (Stelara) 4 2. Wat moet u weten voordat u Ustekinumab (Stelara) gebruikt 5 Gebruik Ustekinumab (Stelara) niet 5 Wees
Ustekinumab (Stelara) Dermatologie Inhoudsopgave Inleiding 4 1. Hoe werkt Ustekinumab (Stelara) 4 2. Wat moet u weten voordat u Ustekinumab (Stelara) gebruikt 5 Gebruik Ustekinumab (Stelara) niet 5 Wees
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Cluvot 250 IE Cluvot 1250 IE Poeder en oplosmiddel voor oplossing voor injectie of infusie. Humane plasmastollingsfactor XIII-concentraat Dit geneesmiddel is onderworpen
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Cluvot 250 IE Cluvot 1250 IE Poeder en oplosmiddel voor oplossing voor injectie of infusie. Humane plasmastollingsfactor XIII-concentraat Dit geneesmiddel is onderworpen
Een illustratief hulpmiddel voor het thuis toedienen van Nplate
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Dit verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Dit verplicht plan voor risicobeperking in België, waarvan deze informatie
ACTYNOX 50%/50% v/v Distikstofoxide (N 2 O) en Zuurstof (O 2 ) Medicinaal gas, samengeperst
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ACTYNOX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ACTYNOX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Bijwerking van bijzonder belang Bloedbaaninfecties geassocieerd met Remodulin intraveneus
 De Belgische gezondheidsautoriteiten hebben enkele voorwaarden gesteld aan het in de handel brengen van het geneesmiddel Remodulin. Het verplichte plan om risico s in België te minimaliseren, waarvan deze
De Belgische gezondheidsautoriteiten hebben enkele voorwaarden gesteld aan het in de handel brengen van het geneesmiddel Remodulin. Het verplichte plan om risico s in België te minimaliseren, waarvan deze
Informatiebrochure voor laboratoriumpersoneel
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel hemlibra. Het verplicht plan voor risicobeperking in België en het Groothertogdom
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel hemlibra. Het verplicht plan voor risicobeperking in België en het Groothertogdom
BIJSLUITER: INFORMATIE VOOR DE PATIËNT. FLUORESCEINE 10% Faure oplossing voor injectie natriumfluoresceïne
 BIJSLUITER: INFORMATIE VOOR DE PATIËNT FLUORESCEINE 10% Faure oplossing voor injectie natriumfluoresceïne Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat belangrijke
BIJSLUITER: INFORMATIE VOOR DE PATIËNT FLUORESCEINE 10% Faure oplossing voor injectie natriumfluoresceïne Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat belangrijke
BIJSLUITER: INFORMATIE VOOR DE PATIËNT. Bleu Patente V, oplossing voor injectie 25 mg/ml
 BIJSLUITER: INFORMATIE VOOR DE PATIËNT Bleu Patente V, oplossing voor injectie 25 mg/ml Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt want er staat belangrijke informatie voor u in. Bewaar
BIJSLUITER: INFORMATIE VOOR DE PATIËNT Bleu Patente V, oplossing voor injectie 25 mg/ml Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt want er staat belangrijke informatie voor u in. Bewaar
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Patiëntenfolder
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER, 25 microgram / dosis, oplossing voor injectie Polyoside buiktyfusvaccin Lees de hele bijsluiter zorgvuldig door voordat u of uw kind wordt gevaccineerd want
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER, 25 microgram / dosis, oplossing voor injectie Polyoside buiktyfusvaccin Lees de hele bijsluiter zorgvuldig door voordat u of uw kind wordt gevaccineerd want
De volgende informatie is alleen bestemd voor artsen of andere beroepsbeoefenaren in de gezondheidszorg.
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Levonortis. Het verplicht plan voor risicobeperking in België, waarvan deze
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Levonortis. Het verplicht plan voor risicobeperking in België, waarvan deze
Bijsluiter: informatie voor de patiënt en gebruiker. Ondexxya 200 mg poeder voor oplossing voor infusie andexanet alfa
 Bijsluiter: informatie voor de patiënt en gebruiker Ondexxya 200 mg poeder voor oplossing voor infusie andexanet alfa Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe
Bijsluiter: informatie voor de patiënt en gebruiker Ondexxya 200 mg poeder voor oplossing voor infusie andexanet alfa Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe
B ijsluiter NL P arvosuin - MR B. BIJSLUITER 1
 B. BIJSLUITER 1 PARVOSUIN- MR Geïnactiveerd vaccin tegen parvovirose en vlekziekte bij varkens. 1. NAAM EN ADRES VAN DE HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EN DE FABRIKANT VERANTWOORDELIJK
B. BIJSLUITER 1 PARVOSUIN- MR Geïnactiveerd vaccin tegen parvovirose en vlekziekte bij varkens. 1. NAAM EN ADRES VAN DE HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EN DE FABRIKANT VERANTWOORDELIJK
ARIPIPRAZOLE TEVA JOUW HANDLEIDING INFORMATIEBROCHURE VOOR PATIËNTEN / VERZORGERS. (door de arts af te geven aan elke patiënt/verzorger)
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ARIPIPRAZOLE TEVA. Het verplicht plan voor risicobeperking in België, waarvan
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ARIPIPRAZOLE TEVA. Het verplicht plan voor risicobeperking in België, waarvan
SAMENVATTING VAN DE PRODUCTKENMERKEN 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET DIERGENEESMIDDEL emulsie voor injectie voor varkens 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke dosis van 2 ml bevat: Werkzaam bestanddeel:
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET DIERGENEESMIDDEL emulsie voor injectie voor varkens 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke dosis van 2 ml bevat: Werkzaam bestanddeel:
Bijsluiter: informatie voor de gebruiker. ALCAINE 0,5% oogdruppels, oplossing. Proxymetacaïnehydrochloride
 Bijsluiter: informatie voor de gebruiker ALCAINE 0,5% oogdruppels, oplossing Proxymetacaïnehydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
Bijsluiter: informatie voor de gebruiker ALCAINE 0,5% oogdruppels, oplossing Proxymetacaïnehydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. PNEUMO 23, oplossing voor injectie Polyosidisch pneumokokkenvaccin
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER PNEUMO 23, oplossing voor injectie Polyosidisch pneumokokkenvaccin Lees goed de hele bijsluiter voordat u wordt gevaccineerd. - Bewaar deze bijsluiter. Misschien
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER PNEUMO 23, oplossing voor injectie Polyosidisch pneumokokkenvaccin Lees goed de hele bijsluiter voordat u wordt gevaccineerd. - Bewaar deze bijsluiter. Misschien
BIJSLUITER INFORMATIE VOOR DE GEBRUIKER. Firazyr 30 mg oplossing voor injectie, voorgevulde spuit Icatibant
 BIJSLUITER INFORMATIE VOOR DE GEBRUIKER Firazyr 30 mg oplossing voor injectie, voorgevulde spuit Icatibant Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
BIJSLUITER INFORMATIE VOOR DE GEBRUIKER Firazyr 30 mg oplossing voor injectie, voorgevulde spuit Icatibant Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
BENEPALI SNELGIDS. Benepali Voorgevulde injectiespuit (PFSyringe) NL v3.0 Goedgekeurd: 04/2019
 BENEPALI SNELGIDS Benepali Voorgevulde injectiespuit (PFSyringe) NL v3.0 A. Voordat u begint B. Injectiestappen Deze handleiding is bedoeld als snelle aanwijzing over hoe u op een veilige en effectieve
BENEPALI SNELGIDS Benepali Voorgevulde injectiespuit (PFSyringe) NL v3.0 A. Voordat u begint B. Injectiestappen Deze handleiding is bedoeld als snelle aanwijzing over hoe u op een veilige en effectieve
INFORMATIEBROCHURE VOOR PATIËNTEN / VERZORGERS
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ARIPIPRAZOLE EG 10 mg 15 mg 30 mg tabletten. Het verplicht plan voor risicobeperking
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ARIPIPRAZOLE EG 10 mg 15 mg 30 mg tabletten. Het verplicht plan voor risicobeperking
Urologie. Patiënteninformatie. Zelfinjectie bij erectiestoornissen. Slingeland Ziekenhuis
 Urologie Zelfinjectie bij erectiestoornissen i Patiënteninformatie Slingeland Ziekenhuis Algemeen In overleg met uw uroloog hebt u gekozen voor zelfinjectie om een erectiestoornis te behandelen. In deze
Urologie Zelfinjectie bij erectiestoornissen i Patiënteninformatie Slingeland Ziekenhuis Algemeen In overleg met uw uroloog hebt u gekozen voor zelfinjectie om een erectiestoornis te behandelen. In deze
YERVOY. (ipilimumab) Concentraat voor oplossing voor infusie Dit geneesmiddel is onderworpen aan aanvullende monitoring.
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Ustekinumab. (Stelara )
 Ustekinumab (Stelara ) Inhoud Inleiding 3 Wanneer wordt ustekinumab gebruikt en hoe werkt het? 3 Hoe wordt het gebruikt? 3 Mogelijke bijwerkingen 4 Zwangerschap, borstvoeding en vruchtbaarheid 5 Andere
Ustekinumab (Stelara ) Inhoud Inleiding 3 Wanneer wordt ustekinumab gebruikt en hoe werkt het? 3 Hoe wordt het gebruikt? 3 Mogelijke bijwerkingen 4 Zwangerschap, borstvoeding en vruchtbaarheid 5 Andere
INSTRUCTIEKAART VOOR DE PATiËNT
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ZypAdhera. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ZypAdhera. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
STAPPENGIDS VOOR BEREIDING EN TOEDIENING VAN DE NPLATE (ROMIPLOSTIM)-INJECTIE
 STAPPENGIDS VOOR BEREIDING EN TOEDIENING VAN DE NPLATE (ROMIPLOSTIM)-INJECTIE Een illustratief hulpmiddel voor het thuis toedienen van romiplostim Dit boekje leidt u langs alle stappen die u moet uitvoeren
STAPPENGIDS VOOR BEREIDING EN TOEDIENING VAN DE NPLATE (ROMIPLOSTIM)-INJECTIE Een illustratief hulpmiddel voor het thuis toedienen van romiplostim Dit boekje leidt u langs alle stappen die u moet uitvoeren
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. ALCON EYE GEL 3 mg/g ooggel Carbomeer
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER ALCON EYE GEL 3 mg/g ooggel Carbomeer Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor u. Gebruik
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER ALCON EYE GEL 3 mg/g ooggel Carbomeer Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor u. Gebruik
BYDUREON 2 mg poeder en oplosmiddel voor suspensie voor injectie met verlengde afgifte
 INSTRUCTIES VOOR DE GEBRUIKER Uw stap voor stap handleiding BYDUREON 2 mg poeder en oplosmiddel voor suspensie voor injectie met verlengde afgifte Heeft u vragen over het gebruik van BYDUREON? Zie de veel
INSTRUCTIES VOOR DE GEBRUIKER Uw stap voor stap handleiding BYDUREON 2 mg poeder en oplosmiddel voor suspensie voor injectie met verlengde afgifte Heeft u vragen over het gebruik van BYDUREON? Zie de veel
BEKNOPTE LEIDRAAD VOOR THUISTOEDIENING VAN NPLATE (ROMIPLOSTIM)
 BEKNOPTE LEIDRAAD VAN NPLATE (ROMIPLOSTIM) Voor volwassen patiënten die hebben besloten zichzelf thuis romiplostim injecties toe te dienen. De materialen in dit trainingspakket voor thuistoediening zorgen
BEKNOPTE LEIDRAAD VAN NPLATE (ROMIPLOSTIM) Voor volwassen patiënten die hebben besloten zichzelf thuis romiplostim injecties toe te dienen. De materialen in dit trainingspakket voor thuistoediening zorgen
Brochure voor de professionele zorgverleners
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Mitoxantrone Sandoz. Het verplicht plan voor risicobeperking in België, waarvan
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Mitoxantrone Sandoz. Het verplicht plan voor risicobeperking in België, waarvan
TETRAVAC Geadsorbeerd difterie-, tetanus-, acellulair kinkhoest- en geïnactiveerd poliovaccin
 BIJSLUITER Lees de hele bijsluiter aandachtig door voordat u uw kind laat vaccineren. - Bewaar deze bijsluiter totdat het vaccinatieprogramma is afgerond. Het kan nodig zijn om de bijsluiter nogmaals door
BIJSLUITER Lees de hele bijsluiter aandachtig door voordat u uw kind laat vaccineren. - Bewaar deze bijsluiter totdat het vaccinatieprogramma is afgerond. Het kan nodig zijn om de bijsluiter nogmaals door
