CCaLC, Carbon Calculations over the Life Cycle of Industrial Activities (CCaLC). (accessed, 12 oktober 2012)
|
|
|
- Leo de Graaf
- 6 jaren geleden
- Aantal bezoeken:
Transcriptie
1 BIJLAGEN Paper 5, microschaalpracticum zoutjes. 1. References: Beroepsvereniging voor Zorgprofessionals (V&VN), Bijlage 3. Reken-sjablonen. (accessed 22 oktober 2012). CCaLC, Carbon Calculations over the Life Cycle of Industrial Activities (CCaLC). (accessed, 12 oktober 2012) Centraal Bureau voor de Statistiek (CBS), Planbureau voor de Leefomgeving (PBL) en Wageningen UR, 2012 Broeikasgas en CO2-intensiteit bedrijven, (indicator 0542, versie 05, 10 april 2012). CBS, Den Haag; Planbureau voor de Leefomgeving, Den Haag/Bilthoven en Wageningen UR, Wageningen. Centraal Bureau voor de Statistiek (CBS), Statline: Producentenprijzen; SBI'93, afzet en invoer, index 2000 = 100 vanaf Voorburg. Janssen, T, Het Learner Report als onderzoeksinstrument. ILO-UvA, repository. Kramer, K.J Food Matters. On reducing energy use and greenhouse gas emissions from household food consumption. PhD-thesis, Rijksuniversiteit Groningen (RUG). Kok, R., Benders, R en H. Moll, 200. Energie-intensiteiten van de Nederlandse consumptieve bestedingen anno Vakgroep Energie en Milieukunde (IVEM), Rijksuniversiteit Groningen, rapportnr Groningen, Nederland. 1
2 Bijlage 2. Opgaven SO, bonustoets, 1. Beschrijf een methode om het Cu 2+- ion te verwijderen uit een oplossing van koper(ii)chloride en calciumchloride. Geef ook de reactievergelijking. 2. Tijdens een practicum krijgt Pietje Puk een reageerbuis met daarin een vaste stof. Deze stof kan zijn: calciumsulfiet, bariumhydroxide, natriumcarbonaat, kopernitraat, zinkchloride of kaliumsulfaat. Hij moet vaststellen welke stof er in de reageerbuis zit. PP voegt water toe aan de vaste stof waarna er een oplossing ontstaat. a. Kan PP al een stof wegstrepen? Zo ja, welke en waarom? Vervolgens wordt de oplossing verdeeld over twee reageerbuizen. Aan de ene reageerbuis voegt PP een oplossing van ijzer(ii)nitraat, er ontstaat een oplossing (moet zijn neerslag). Aan de andere reageerbuis wordt natriumsulfaat-oplossing toegevoegd. Er ontstaat geen neerslag. b. Verklaar aan de hand van deze gegevens welke stof zich in de beginsituatie in de reageerbuis bevond. Uitwerkmodel Vraag 1. Er moet een zout (oplossing) worden toegevoegd die aan twee eisen moet voldoen: 1. Het zout moet oplosbaar zijn. 2. Het moet een neerslag vormen met Cu 2+ maar niet met Ca 2+. Cu 2+ verwijderen. De toegevoegde oplossing moet met Cu 2+ moet dus een neerslag geven en niet met Ca 2+. Dit kan door een oplossing toe te voegen met niet al te grote concentraties OH -. Bijv, NaOH. (KOH-, NH 4 OH-oplossing) of De volgende reactie zal dan plaatsvinden: Cu 2+ (aq) + 2 OH - (aq) Cu(OH) 2 (s) Vraag 2 a. Ja, calciumsulfiet, Calciumsulfiet is niet/slecht oplosbaar in water. b. IJzer(II)nitraat-oplossing kan een neerslag geven met een bariumhydroxide-oplossing en met een natriumcarbonaat-oplossing. Sulfaat kan slechts een neerslag geven met een bariumhydroxide-oplossing. Er is vermeld dat er bij toevoeging van een natriumsulfaatoplossing geen neerslag ontstaat; de reageerbuis in de beginsituatie bevat derhalve natriumcarbonaat. Waardering: Vraag 1: 5 punten Vraag 2a: 2 punten (1 voor naam zout en 1 voor verklaring Vraag 2b: 6 punten (3 voor neerslag met bariumhydroxide-oplossing en met een natriumcarbonaat-oplossing en 3 voor overige mogelijkheden: kopernitraat, zinkchloride of kaliumsulfaat). Door de fout in de opgave is vraag 2b niet meegeteld in de beoordeling, als het wel goed was beantwoord dan kreeg de leerling bonuspunten (max 6). 2
3 Bijlage 3. Learner Report Vragenlijst leerlingen microschaalpracticum Zouten Castricum, november 2012 We willen graag van je weten wat je zelf vindt dat je geleerd hebt in het Microschaalpracticum Zouten. Daarom vind je hieronder een aantal uitspraken over wat je gedurende het microschaalpracticum geleerd kunt hebben. Geef aan of je het met deze uitspraken eens bent door eerst een hokje aan te kruisen en daarna je antwoord toe te lichten. Je krijgt er geen cijfer of beoordeling voor! Het gaat erom dat we graag willen van jou horen wat jij van het microschaalpracticum geleerd hebt tot nu toe. 1. Ik heb meer zelfvertrouwen gekregen. Dat werd me duidelijk toen 2. Ik heb geleerd zelfstandig te werken. Ik heb dat ontdekt toen ik 3. Ik heb geleerd kritisch ten opzichte van mijn eigen prestaties te staan. Dat werd me duidelijk doordat ik 3
4 4. Ik heb door het microschaalpracticum Zouten nieuwe onverwachte eigenschappen van mezelf ontdekt. Ik heb dat gemerkt toen ik 5. Ik ben erachter gekomen dat ik graag in een team samenwerk. Dat heb ik ontdekt toen ik 6. Ik heb ontdekt dat ik niet met iedereen goed kan samenwerken. Dat werd me duidelijk toen 4
5 7. Bij het microschaalpracticum Zouten leer ik dingen waar ik later niets aan heb. Dat blijkt uit 8. Door het microschaalpracticum kijk ik anders aan tegen scheikundepractica Dat blijkt uit 9. Door het microschaalpracticum snap ik de theorie achter zouten/neerslagreactie beter Omdat Wil je de volgende zinnen afmaken? Ik heb geleerd / gemerkt / ontdekt dat [ 5
6 Ik heb geleerd / gemerkt / ontdekt dat het niet zo is dat Ik heb geleerd / gemerkt / ontdekt dat ik Ik heb geleerd / gemerkt / ontdekt dat ik niet. Dit is het einde van de vragenlijst. Hartelijk dank voor je medewerking! 6
7 Bijlage 4. Observatieformulier. Vijf leerlingen observeren op de volgende terreinen: Taak: Werkt aan opgedragen taak Vraagt hulp (medeleerlingen/toa/docent) Kijkt in het rond Loopt weg voor iets anders Praat met anderen over iets anders dan de opdracht Helpt medeleerlingen Leerling 1 Leerling 2 Leerling 3 Leerling 4 Leerling 5 Beoordelingen: 1: heel weinig 2: weinig 3: niet veel/niet weinig 4: veel 5: heel veel Veiligheid: Tafel droog en netjes Leerling 1 Leerling 2 Leerling 3 Leerling 4 Leerling 5 Algemeen: Labjas dicht Bril op Opruimen Beoordelingen: 1: goed 2: niet goed/niet slecht 3: slecht Per klas worden 5 leerlingen geselecteerd waarbij de observaties uitgevoerd worden. 7
8 BIJLAGE 5. Vragenlijst TOA 1. Voorbereiding Wat zijn de belangrijkste verschillen voor een TOA in de werkzaamheden als voorbereiding van een microschaalpracticum zouten vergeleken met een reageerbuispracticum zouten? (tijd, chemicaliën, etc) 2. Uitvoering Wat zijn de belangrijkste verschillen voor een TOA tijdens de uitvoering van een microschaalpracticum zouten door leerlingen vergeleken met een reageerbuispracticum zouten? (uitvoering door leerlingen, vragen van leerlingen, vaardigheden voordoen, uitleggen etc) 3. Afhandeling Wat zijn de belangrijkste verschillen voor een TOA in de afhandeling van een microschaalpracticum zouten vergeleken met een reageerbuispracticum zouten? (tijd, afval, schoonmaken etc). 8
Bijlage Paper 2 zouten, K.J Kramer ( ) 1. Lesplannen
 Bijlage Paper 2 zouten, K.J Kramer (10314997) 1. Lesplannen 2. Leerlingenmateriaal 2.1 Experiment-voorschrift druppelpracticum zoutoplossingen mengen 2.2 Verwerkingsbladen microschaalpracticum zoutoplossingen
Bijlage Paper 2 zouten, K.J Kramer (10314997) 1. Lesplannen 2. Leerlingenmateriaal 2.1 Experiment-voorschrift druppelpracticum zoutoplossingen mengen 2.2 Verwerkingsbladen microschaalpracticum zoutoplossingen
Samenvatting: Scheikunde H4 Reacties met zoutoplossingen. Don van Baar Murmelliusgymnasium Leerjaar
 Samenvatting: Scheikunde H4 Reacties met zoutoplossingen Don van Baar Murmelliusgymnasium Leerjaar 2011-2012 Murmellius2014 www.compudo.nl/murmellius2014 Scheikunde H4: Reacties met zoutoplossingen Samenvatting
Samenvatting: Scheikunde H4 Reacties met zoutoplossingen Don van Baar Murmelliusgymnasium Leerjaar 2011-2012 Murmellius2014 www.compudo.nl/murmellius2014 Scheikunde H4: Reacties met zoutoplossingen Samenvatting
Practicum Zouten 2 VMBO 4 Zouten Zoutoplossingen bij elkaar Slecht oplosbare zouten maken Ionen verwijderen Herkennen van een zout
 Practicum Zouten 2 Niveau: VMBO 4 Onderdeel: Zouten Proeven: Zoutoplossingen bij elkaar Slecht oplosbare zouten maken Ionen verwijderen Herkennen van een zout 1 Proef 1 Zoutoplossingen bij elkaar Nodig:
Practicum Zouten 2 Niveau: VMBO 4 Onderdeel: Zouten Proeven: Zoutoplossingen bij elkaar Slecht oplosbare zouten maken Ionen verwijderen Herkennen van een zout 1 Proef 1 Zoutoplossingen bij elkaar Nodig:
H4SK-H4. Willem de Zwijgerteam. CC Naamsvermelding-GelijkDelen 3.0 Nederland licentie. https://maken.wikiwijs.nl/66747
 Auteur Laatst gewijzigd Licentie Webadres Willem de Zwijgerteam 29 augustus 2017 CC Naamsvermelding-GelijkDelen 3.0 Nederland licentie https://maken.wikiwijs.nl/66747 Dit lesmateriaal is gemaakt met Wikiwijs
Auteur Laatst gewijzigd Licentie Webadres Willem de Zwijgerteam 29 augustus 2017 CC Naamsvermelding-GelijkDelen 3.0 Nederland licentie https://maken.wikiwijs.nl/66747 Dit lesmateriaal is gemaakt met Wikiwijs
PbSO 4(s) d NH 4Cl + KOH KCl + H 2O + NH 3(g) NH 4. + OH - NH 3(g) + H 2O e 2 NaOH + CuCl 2 Cu(OH) 2(s) + 2 NaCl
 Hoofdstuk 11 Chemische reacties bladzijde 1 Opgave 1 De ionen die in water ontstaan: a NaCl Na Cl - b AgNO 3 Ag - NO 3 c (NH 4) 2SO 4 2 NH 4 SO 4 d KOH K OH - e NiSO 4 Ni 2 SO 4 Opgave 2 Schrijf de volgende
Hoofdstuk 11 Chemische reacties bladzijde 1 Opgave 1 De ionen die in water ontstaan: a NaCl Na Cl - b AgNO 3 Ag - NO 3 c (NH 4) 2SO 4 2 NH 4 SO 4 d KOH K OH - e NiSO 4 Ni 2 SO 4 Opgave 2 Schrijf de volgende
ßCalciumChloride oplossing
 Samenvatting door R. 1673 woorden 17 februari 2013 8 1 keer beoordeeld Vak Methode Scheikunde Pulsar chemie Additiereactie Bij een reactie tussen hexeen en broom springt de C=C binding open. Aan het molecuul
Samenvatting door R. 1673 woorden 17 februari 2013 8 1 keer beoordeeld Vak Methode Scheikunde Pulsar chemie Additiereactie Bij een reactie tussen hexeen en broom springt de C=C binding open. Aan het molecuul
Proef Scheikunde PH-bepaling
 Proef Scheikunde PH-bepaling Proef door een scholier 924 woorden 27 mei 2001 4,9 57 keer beoordeeld Vak Scheikunde Inleiding De opdracht voor de eerste module was een vaardigheidspracticum. In dit practicum
Proef Scheikunde PH-bepaling Proef door een scholier 924 woorden 27 mei 2001 4,9 57 keer beoordeeld Vak Scheikunde Inleiding De opdracht voor de eerste module was een vaardigheidspracticum. In dit practicum
Wet van Behoud van Massa
 Les 3 E42 Wet van Behoud van Massa In 1789 door Antoine Lavoiser ontdekt dat : De totale massa tijdens een reactie altijd gelijk blijft. Bij chemische reacties worden moleculen dus veranderd in andere
Les 3 E42 Wet van Behoud van Massa In 1789 door Antoine Lavoiser ontdekt dat : De totale massa tijdens een reactie altijd gelijk blijft. Bij chemische reacties worden moleculen dus veranderd in andere
OEFENOPGAVEN VWO EVENWICHTEN
 OPGAVE 1 OEFENOPGAVEN VWO EVENWICHTEN In een ruimte van 5,00 liter brengt men 9,50 mol HCl(g) en 2,60 mol O 2 (g). Na evenwichtsinstelling is 40,0% van de beginstoffen omgezet en is er Cl 2 (g) en H 2
OPGAVE 1 OEFENOPGAVEN VWO EVENWICHTEN In een ruimte van 5,00 liter brengt men 9,50 mol HCl(g) en 2,60 mol O 2 (g). Na evenwichtsinstelling is 40,0% van de beginstoffen omgezet en is er Cl 2 (g) en H 2
Grafieken, samenwerkend leren, hardop denken, stappenplan
 PAPER 3 ONTWERPRAPPORT Naam auteur(s) Vakgebied Titel Onderwerp Opleiding Doelgroep Sleuteltermen Bibliografische referentie Marlinda van Rooijen Steltenpool, drs Economie Grafieken en betekenis Marktvraag
PAPER 3 ONTWERPRAPPORT Naam auteur(s) Vakgebied Titel Onderwerp Opleiding Doelgroep Sleuteltermen Bibliografische referentie Marlinda van Rooijen Steltenpool, drs Economie Grafieken en betekenis Marktvraag
6 VWO SK Extra (reken)opgaven Buffers.
 6 VWO SK Extra (reken)opgaven Buffers. Opgave I. 1 Je wilt een buffermengsel maken met ph = 4,20. Welke stoffen kun je het beste als uitgangsstoffen nemen? Opgave II. 2 In 1,00 liter water is opgelost
6 VWO SK Extra (reken)opgaven Buffers. Opgave I. 1 Je wilt een buffermengsel maken met ph = 4,20. Welke stoffen kun je het beste als uitgangsstoffen nemen? Opgave II. 2 In 1,00 liter water is opgelost
OEFENOPGAVEN VWO ZUREN EN BASEN + ph-berekeningen
 OEFENOPGAVEN VWO ZUREN EN BASEN + ph-berekeningen OPGAVE 1 01 Bereken hoeveel mmol HCOOH is opgelost in 40 ml HCOOH oplossing met ph = 3,60. 02 Bereken ph van 0,300 M NaF oplossing. 03 Bereken hoeveel
OEFENOPGAVEN VWO ZUREN EN BASEN + ph-berekeningen OPGAVE 1 01 Bereken hoeveel mmol HCOOH is opgelost in 40 ml HCOOH oplossing met ph = 3,60. 02 Bereken ph van 0,300 M NaF oplossing. 03 Bereken hoeveel
Kaliumaluminiumsulfaat is een dubbelzout met drie ionsoorten, twee positieve monoatomische en één negatief polyatomisch.
 Chemie Vraag 1 Kaliumaluminiumsulfaat is een dubbelzout met drie ionsoorten, twee positieve monoatomische en één negatief polyatomisch. Wat is de juiste formule van dit dubbelzout? KAlSO4 KAl(SO4)2 K3Al(SO4)2
Chemie Vraag 1 Kaliumaluminiumsulfaat is een dubbelzout met drie ionsoorten, twee positieve monoatomische en één negatief polyatomisch. Wat is de juiste formule van dit dubbelzout? KAlSO4 KAl(SO4)2 K3Al(SO4)2
Kaliumaluminiumsulfaat is een dubbelzout met drie ionsoorten, twee positieve monoatomische en één negatief polyatomisch.
 Chemie Vraag 1 Kaliumaluminiumsulfaat is een dubbelzout met drie ionsoorten, twee positieve monoatomische en één negatief polyatomisch. Wat is de juiste formule van dit dubbelzout? K3AlSO4 K3Al(SO4)2 KAl(SO4)2
Chemie Vraag 1 Kaliumaluminiumsulfaat is een dubbelzout met drie ionsoorten, twee positieve monoatomische en één negatief polyatomisch. Wat is de juiste formule van dit dubbelzout? K3AlSO4 K3Al(SO4)2 KAl(SO4)2
Ontwerponderzoek Paper 3 Onderzoeksinstrumenten
 Ontwerponderzoek Paper 3 Onderzoeksinstrumenten Student Graziella de Guytenaere (studentnummer: 0409170) Docenten Abdul A. Rezaei Vakdidacticus Jannet P. van Drie Onderwijskundige Femke Boesenkool - Onderwijskundige
Ontwerponderzoek Paper 3 Onderzoeksinstrumenten Student Graziella de Guytenaere (studentnummer: 0409170) Docenten Abdul A. Rezaei Vakdidacticus Jannet P. van Drie Onderwijskundige Femke Boesenkool - Onderwijskundige
Basisscheikunde voor het hbo ISBN e druk Uitgeverij Syntax media
 Hoofdstuk 5 Chemische reacties bladzijde 1 Opgave 1 Maak de volgende reactievergelijkingen kloppend: a C 3H 8O 2 4 O 2 3 CO 2 4 H 2O b P 4 5 O 2 6 H 2O 4 H 3PO 4 c 4 Al 3 O 2 2 Al 2O 3 d 2 Fe 3 Cl 2 2
Hoofdstuk 5 Chemische reacties bladzijde 1 Opgave 1 Maak de volgende reactievergelijkingen kloppend: a C 3H 8O 2 4 O 2 3 CO 2 4 H 2O b P 4 5 O 2 6 H 2O 4 H 3PO 4 c 4 Al 3 O 2 2 Al 2O 3 d 2 Fe 3 Cl 2 2
Interfacultaire Lerarenopleidingen, Universiteit van Amsterdam
 Paper 3: Onderzoeksinstrumenten Aantal woorden (exclusief bijlage, literatuur en samenvatting): 581 Jeffrey de Jonker Naam auteur(s) Vakgebied Titel Onderwerp Opleiding Jeffrey de Jonker Biologie Differentiëren
Paper 3: Onderzoeksinstrumenten Aantal woorden (exclusief bijlage, literatuur en samenvatting): 581 Jeffrey de Jonker Naam auteur(s) Vakgebied Titel Onderwerp Opleiding Jeffrey de Jonker Biologie Differentiëren
OEFENTOETS Zuren en basen 5 VWO
 OEFENTOETS Zuren en basen 5 VWO Gesloten vragen 1. Carolien wil de zuurgraad van een oplossing onderzoeken met twee verschillende zuur-baseindicatoren en neemt hierbij het volgende waar: I de oplossing
OEFENTOETS Zuren en basen 5 VWO Gesloten vragen 1. Carolien wil de zuurgraad van een oplossing onderzoeken met twee verschillende zuur-baseindicatoren en neemt hierbij het volgende waar: I de oplossing
36ste Vlaamse Chemieolympiade
 36ste Vlaamse Chemieolympiade 2018-2019 2de ronde 27 februari 2019 Je naam en voornaam: Je adres: De naam van je school: Het adres van je school: Je leerjaar: antal lesuren chemie per week die je dit schooljaar
36ste Vlaamse Chemieolympiade 2018-2019 2de ronde 27 februari 2019 Je naam en voornaam: Je adres: De naam van je school: Het adres van je school: Je leerjaar: antal lesuren chemie per week die je dit schooljaar
Zouten versie
 Zouten versie 16-02-2016 Je kunt bij een onderwerp komen door op de gewenste rubriek in de inhoud te klikken. Wil je vanuit een rubriek terug naar de inhoud, klik dan op de tekst van de rubriek waar je
Zouten versie 16-02-2016 Je kunt bij een onderwerp komen door op de gewenste rubriek in de inhoud te klikken. Wil je vanuit een rubriek terug naar de inhoud, klik dan op de tekst van de rubriek waar je
5-1 Moleculen en atomen
 5-1 Moleculen en atomen Vraag 1. Uit hoeveel soorten moleculen bestaat een zuivere stof? Vraag 2. Wat is een molecuul? Vraag 3. Wat is een atoom? Vraag 4. Van welke heb je er het meeste: moleculen of atomen?
5-1 Moleculen en atomen Vraag 1. Uit hoeveel soorten moleculen bestaat een zuivere stof? Vraag 2. Wat is een molecuul? Vraag 3. Wat is een atoom? Vraag 4. Van welke heb je er het meeste: moleculen of atomen?
Samenvatting Scheikunde Hoofdstuk 9, 10, 11 Zuren/Basen, Evenwichtsconstanten
 Samenvatting Scheikunde Hoofdstuk 9, 10, 11 Zuren/Basen, Evenwichtsconstanten Samenvatting door een scholier 1087 woorden 22 januari 2009 6 42 keer beoordeeld Vak Methode Scheikunde Pulsar chemie Scheikunde
Samenvatting Scheikunde Hoofdstuk 9, 10, 11 Zuren/Basen, Evenwichtsconstanten Samenvatting door een scholier 1087 woorden 22 januari 2009 6 42 keer beoordeeld Vak Methode Scheikunde Pulsar chemie Scheikunde
Reacties met een kleurtje
 Supplement bij: Offereins, M. en J.R. Bette (2008). Een uitje met een DOEL. NVOX, 33(10), 442-443. Reacties met een kleurtje DATUM UITVOERING: Afdeling Laboratoriumtechniek Algemene informatie Doel: het
Supplement bij: Offereins, M. en J.R. Bette (2008). Een uitje met een DOEL. NVOX, 33(10), 442-443. Reacties met een kleurtje DATUM UITVOERING: Afdeling Laboratoriumtechniek Algemene informatie Doel: het
25 ste Vlaamse Chemie-Olympiade 2008
 25 ste Vlaamse Chemie-Olympiade 2008 Schiftingsproef 13 februari 2008 Je naam en voornaam: Je adres: De naam van je school: Het adres van je school: Je leerjaar: Aantal uur chemie dat je dit schooljaar
25 ste Vlaamse Chemie-Olympiade 2008 Schiftingsproef 13 februari 2008 Je naam en voornaam: Je adres: De naam van je school: Het adres van je school: Je leerjaar: Aantal uur chemie dat je dit schooljaar
Opgaven zuurgraad (ph) berekenen. ph = -log [H + ] poh = -log [OH - ] [H + ] = 10 -ph [OH - ] = 10 -poh. ph = 14 poh poh = 14 ph ph + poh = 14
![Opgaven zuurgraad (ph) berekenen. ph = -log [H + ] poh = -log [OH - ] [H + ] = 10 -ph [OH - ] = 10 -poh. ph = 14 poh poh = 14 ph ph + poh = 14 Opgaven zuurgraad (ph) berekenen. ph = -log [H + ] poh = -log [OH - ] [H + ] = 10 -ph [OH - ] = 10 -poh. ph = 14 poh poh = 14 ph ph + poh = 14](/thumbs/82/85039734.jpg) Opgaven zuurgraad (ph) berekenen Met behulp van deze formules dien je berekeningen te kunnen uitvoeren. Deze hoef je niet uit je hoofd te leren, maar je moet ze wel kunnen toepassen. Bij een toets zullen
Opgaven zuurgraad (ph) berekenen Met behulp van deze formules dien je berekeningen te kunnen uitvoeren. Deze hoef je niet uit je hoofd te leren, maar je moet ze wel kunnen toepassen. Bij een toets zullen
Oefenopgaven REDOX vwo
 Oefenopgaven REDOX vwo OPGAVE 1 Geef de halfreactie waarbij 01 P 2 O 5 wordt omgezet in PH 3. 02 Jodaat, IO 3 - in neutraal milieu wordt omgezet in H 5 IO 6. 03 Methanol in zuur milieu wordt omgezet in
Oefenopgaven REDOX vwo OPGAVE 1 Geef de halfreactie waarbij 01 P 2 O 5 wordt omgezet in PH 3. 02 Jodaat, IO 3 - in neutraal milieu wordt omgezet in H 5 IO 6. 03 Methanol in zuur milieu wordt omgezet in
Oefenopgaven REDOXREACTIES vwo Reactievergelijkingen en halfreacties
 Oefenopgaven REDOXREACTIES vwo Reactievergelijkingen en halfreacties OPGAVE 1 Geef de halfreactie waarbij 01 P 2 O 5 wordt omgezet in PH 3. 02 Jodaat, IO 3 - in neutraal milieu wordt omgezet in H 5 IO
Oefenopgaven REDOXREACTIES vwo Reactievergelijkingen en halfreacties OPGAVE 1 Geef de halfreactie waarbij 01 P 2 O 5 wordt omgezet in PH 3. 02 Jodaat, IO 3 - in neutraal milieu wordt omgezet in H 5 IO
Reacties en stroom 1
 Reacties en stroom 1 Elektronenoverdracht (1) Een bekende reactie is: 2 Na(s) + Cl 2 (g) 2 NaCl(s) (oude notatie: Na + Cl - ) Hierbij is sprake van elektronenoverdracht. Dit kan als volgt worden voorgesteld:
Reacties en stroom 1 Elektronenoverdracht (1) Een bekende reactie is: 2 Na(s) + Cl 2 (g) 2 NaCl(s) (oude notatie: Na + Cl - ) Hierbij is sprake van elektronenoverdracht. Dit kan als volgt worden voorgesteld:
Colorimetrische bepaling van het kopergehalte van euromunten experiment 5+
 Practicum W22 Colorimetrische bepaling van het kopergehalte van euromunten experiment 5+ In experiment 5, blz 102, moet je de kleur van een muntoplossing vergelijken met een aantal buizen met bekende concentratie.
Practicum W22 Colorimetrische bepaling van het kopergehalte van euromunten experiment 5+ In experiment 5, blz 102, moet je de kleur van een muntoplossing vergelijken met een aantal buizen met bekende concentratie.
Vragenlijst leerlingen Eureka! Oberon & Eureka!, januari 2012
 Vragenlijst leerlingen Eureka! Oberon & Eureka!, januari 2012 Toelichting Beste leerling, Jij zit in de Eureka!-klas. We zijn benieuwd naar jouw mening. Die kun je geven in deze vragenlijst. Die bestaat
Vragenlijst leerlingen Eureka! Oberon & Eureka!, januari 2012 Toelichting Beste leerling, Jij zit in de Eureka!-klas. We zijn benieuwd naar jouw mening. Die kun je geven in deze vragenlijst. Die bestaat
Emissies van broeikasgassen door de land- en tuinbouw,
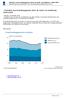 Emissies van broeikasgassen door de land- en tuinbouw, 1990-2009 Indicator 19 oktober 2010 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens
Emissies van broeikasgassen door de land- en tuinbouw, 1990-2009 Indicator 19 oktober 2010 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens
Samenvatting Scheikunde Hoofdstuk 3
 Samenvatting Scheikunde Hoofdstuk 3 Samenvatting door een scholier 1766 woorden 20 januari 2009 6,1 63 keer beoordeeld Vak Methode Scheikunde Chemie overal 3.1: Inleiding: Zouten zijn stoffen die veel
Samenvatting Scheikunde Hoofdstuk 3 Samenvatting door een scholier 1766 woorden 20 januari 2009 6,1 63 keer beoordeeld Vak Methode Scheikunde Chemie overal 3.1: Inleiding: Zouten zijn stoffen die veel
OEFENOPGAVEN MOLBEREKENINGEN
 OEFENOPGAVEN MOLBEREKENINGEN * = voor VWO Salmiak, NH 4 Cl(s), kan gemaakt worden door waterstofchloride, HCl(g), te laten reageren met ammoniak, NH 3 (g) 01 Wat is de chemische naam voor salmiak? 02 Geef
OEFENOPGAVEN MOLBEREKENINGEN * = voor VWO Salmiak, NH 4 Cl(s), kan gemaakt worden door waterstofchloride, HCl(g), te laten reageren met ammoniak, NH 3 (g) 01 Wat is de chemische naam voor salmiak? 02 Geef
30 ste Vlaamse Chemie Olympiade
 30 ste Vlaamse Chemie Olympiade 2012-2013 2 de ronde 20 februari 2013 Je naam en voornaam: E-mail: Je adres: De naam van je school: Het adres van je school: Je leerjaar: Aantal lesuren chemie per week
30 ste Vlaamse Chemie Olympiade 2012-2013 2 de ronde 20 februari 2013 Je naam en voornaam: E-mail: Je adres: De naam van je school: Het adres van je school: Je leerjaar: Aantal lesuren chemie per week
1 Onderzoeksinstrument A en B 2 A. Resultaten diagnostiche toets 3 B. Gesloten vragenlijst - uitkomsten 4 Leerling 5 Ik weet wat inkomstenbelasting
 1 Onderzoeksinstrument A en B 2 A. Resultaten diagnostiche toets 3 B. Gesloten vragenlijst - uitkomsten 4 Leerling H S R W A T E J M 5 Ik weet wat inkomstenbelasting is 4 3 4 4 3 4 4 4 4 4 3 4 4 2 4 4
1 Onderzoeksinstrument A en B 2 A. Resultaten diagnostiche toets 3 B. Gesloten vragenlijst - uitkomsten 4 Leerling H S R W A T E J M 5 Ik weet wat inkomstenbelasting is 4 3 4 4 3 4 4 4 4 4 3 4 4 2 4 4
Uitwerkingen van de opgaven uit: CHEMISCHE ANALYSE ISBN , 1 e druk, Uitgeverij Syntax Media Hoofdstuk 5 Argentometrie bladzijde 1
 Hoofdstuk 5 Argentometrie bladzijde 1 Opgave 1 Bereken met behulp van het oplosbaarheidsproduct de oplosbaarheid (g/l) in zuiver water bij kamertemperatuur, van: a CuBr K s = 5,2 x 10-9 CuBr Cu + + Br
Hoofdstuk 5 Argentometrie bladzijde 1 Opgave 1 Bereken met behulp van het oplosbaarheidsproduct de oplosbaarheid (g/l) in zuiver water bij kamertemperatuur, van: a CuBr K s = 5,2 x 10-9 CuBr Cu + + Br
MAVO- C I CENTRALE EXAMENCOMMISSIE VASTSTELLING OPGAVEN CORRECTIEVOORSCHRIFT bij het examen SCHEIKUNDE MAVO-C Eerste tijdvak F -C
 MAVO- C I CENTRALE EXAMENCOMMISSIE VASTSTELLING OPGAVEN CORRECTIEVOORSCHRIFT 984 bij het examen SCHEIKUNDE MAVO-C Eerste tijdvak 48 7 F -C Bindende normen voor de beoordeling van het schriftelijk werk,
MAVO- C I CENTRALE EXAMENCOMMISSIE VASTSTELLING OPGAVEN CORRECTIEVOORSCHRIFT 984 bij het examen SCHEIKUNDE MAVO-C Eerste tijdvak 48 7 F -C Bindende normen voor de beoordeling van het schriftelijk werk,
kleurveranderingen en reactiesoorten met soda
 kleurveranderingen en reactiesoorten met soda 1. Onderzoeksvraag Welke soorten reacties kunnen aangetoond worden met behulp van soda? 2. Voorbereiding a. Begrippen als achtergrond voor experiment Gasvormingsreactie
kleurveranderingen en reactiesoorten met soda 1. Onderzoeksvraag Welke soorten reacties kunnen aangetoond worden met behulp van soda? 2. Voorbereiding a. Begrippen als achtergrond voor experiment Gasvormingsreactie
Fosfor kan met waterstof reageren. d Geef de vergelijking van de reactie van fosfor met waterstof.
 1 Een oplossing van zwavelzuur en een oplossing van bariumhydroxide geladen beide elektriciteit. Wordt bij de zwavelzuuroplossing een oplossing van bariumhydroxide gedruppeld, dan neemt het elektrisch
1 Een oplossing van zwavelzuur en een oplossing van bariumhydroxide geladen beide elektriciteit. Wordt bij de zwavelzuuroplossing een oplossing van bariumhydroxide gedruppeld, dan neemt het elektrisch
Gegeven is volgende niet-uitgebalanceerde reactievergelijking waarin X de formule van een verbinding voorstelt:
 Chemie Vraag 1 Gegeven is volgende niet-uitgebalanceerde reactievergelijking waarin X de formule van een verbinding voorstelt: CS2 + X + KOH K2SO4 + K2CO3 + KCl + H2O De hoeveelheden (in mol) van de betrokken
Chemie Vraag 1 Gegeven is volgende niet-uitgebalanceerde reactievergelijking waarin X de formule van een verbinding voorstelt: CS2 + X + KOH K2SO4 + K2CO3 + KCl + H2O De hoeveelheden (in mol) van de betrokken
Het is echter waarschijnlijker dat rood kwik bestaat uit Hg 2+ ionen en het biantimonaation met de formule Sb2O7 4.
 Lyceum Oudehoven Hoefslag 4 4205 NK Gorinchem Schoolexamen Leerjaar: 4 Vak: Scheikunde Datum: 26-06-2013 Tijd: 13.00 14.30 uur Uitdelen: opgavenvellen + proefwerkpapier Toegestaan: rekenmachine, potlood,
Lyceum Oudehoven Hoefslag 4 4205 NK Gorinchem Schoolexamen Leerjaar: 4 Vak: Scheikunde Datum: 26-06-2013 Tijd: 13.00 14.30 uur Uitdelen: opgavenvellen + proefwerkpapier Toegestaan: rekenmachine, potlood,
Oplossingen oefeningenreeks 1
 Oplossingen oefeningenreeks 1 4. Door diffractie van X-stralen in natriumchloride-kristallen stelt men vast dat de eenheidscel van dit zout een kubus is waarvan de ribbe een lengte heeft van 5.64 10-10
Oplossingen oefeningenreeks 1 4. Door diffractie van X-stralen in natriumchloride-kristallen stelt men vast dat de eenheidscel van dit zout een kubus is waarvan de ribbe een lengte heeft van 5.64 10-10
Ontwerp Onderzoek: Paper 3: Onderzoeksinstrumenten. Leraren Opleiding. Management & Organisatie
 Ontwerp Onderzoek: Paper 3: Onderzoeksinstrumenten Leraren Opleiding Management & Organisatie Naam auteur(s) Vakgebied Bart Deelen M&O Student nr 10761799 Titel Onderwerp Opleiding Doelgroep Procent rekenen
Ontwerp Onderzoek: Paper 3: Onderzoeksinstrumenten Leraren Opleiding Management & Organisatie Naam auteur(s) Vakgebied Bart Deelen M&O Student nr 10761799 Titel Onderwerp Opleiding Doelgroep Procent rekenen
Belasting van het milieu door gewasbeschermingsmiddelen,
 Belasting van het milieu door gewasbeschermingsmiddelen, 1998-2008 Indicator 17 december 2010 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens
Belasting van het milieu door gewasbeschermingsmiddelen, 1998-2008 Indicator 17 december 2010 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens
Exo-energetische reactie: Een chemische reactie waarbij energie vrijgegeven wordt.
 Onweer onder water 1. Onderzoeksvraag Hoe kunnen we een onweer onder water nabootsen? 2. Voorbereiding a. Begrippen als achtergrond voor experiment Redoxreactie: Een reactie tussen atomen, moleculen en/of
Onweer onder water 1. Onderzoeksvraag Hoe kunnen we een onweer onder water nabootsen? 2. Voorbereiding a. Begrippen als achtergrond voor experiment Redoxreactie: Een reactie tussen atomen, moleculen en/of
Een reactie blijkt bij verdubbeling van alle concentraties 8 maal zo snel te verlopen. Van welke orde zou deze reactie zijn?
 Hoofdstuk 19 Reactiesnelheid en evenwicht bladzijde 1 Opgave 1 Voor de volgende reactie: 4 NH 3(g) + 5 O 2(g) 4 NO(g) + 6 H 2O(g) blijkt onder bepaalde omstandigheden: S = 2,5 mol/l s. Hoe groot zijn:
Hoofdstuk 19 Reactiesnelheid en evenwicht bladzijde 1 Opgave 1 Voor de volgende reactie: 4 NH 3(g) + 5 O 2(g) 4 NO(g) + 6 H 2O(g) blijkt onder bepaalde omstandigheden: S = 2,5 mol/l s. Hoe groot zijn:
Hoofdstuk 3-5. Reacties. Klas
 Hoofdstuk 3-5 Reacties Klas 3 MOLECUULFORMULES OPDRACHT 1: MOLECUULFORMULES LEVEL 1 A H 2O C 2H 6 C C 2H 6O D CO 2 E F C 4H 8O CHN OPDRACHT 2: MOLECUULFORMULES LEVEL 1 A HNO C 3H 6O C C 2H 2 D C 6H 5NO
Hoofdstuk 3-5 Reacties Klas 3 MOLECUULFORMULES OPDRACHT 1: MOLECUULFORMULES LEVEL 1 A H 2O C 2H 6 C C 2H 6O D CO 2 E F C 4H 8O CHN OPDRACHT 2: MOLECUULFORMULES LEVEL 1 A HNO C 3H 6O C C 2H 2 D C 6H 5NO
Natuurlijk heb je nu nog géén massa s berekend. Maar dat kan altijd later nog. En dan kun je mooi kiezen, van welke stoffen je de massa wil berekenen.
 Hoofdstuk 17: Rekenen in molverhoudingen 17.1 Rekenen aan reacties: een terugblik én een alternatief In hoofdstuk 11 hebben we gerekend aan reacties. Het achterliggende idee was vaak, dat je bij een reactie
Hoofdstuk 17: Rekenen in molverhoudingen 17.1 Rekenen aan reacties: een terugblik én een alternatief In hoofdstuk 11 hebben we gerekend aan reacties. Het achterliggende idee was vaak, dat je bij een reactie
Hoofdstuk 3: Zuren en basen
 Hoofdstuk 3: Zuren en basen Scheikunde VWO 2011/2012 www.lyceo.nl Onderwerpen Scheikunde 2011 2012 Stoffen, structuur en binding Kenmerken van Reacties Zuren en base Redox Chemische technieken Koolstofchemie
Hoofdstuk 3: Zuren en basen Scheikunde VWO 2011/2012 www.lyceo.nl Onderwerpen Scheikunde 2011 2012 Stoffen, structuur en binding Kenmerken van Reacties Zuren en base Redox Chemische technieken Koolstofchemie
Hulpmiddelen: Binas T99, T40A. Hulpmiddelen: Binas T99, T40A
 NAAMGEVING IONEN EINDBAAS A LEVEL 2 NAAMGEVING IONEN EINDBAAS C LEVEL 2 A Hoe heet het ion van broom met een lading van 1-? B Wat zijn de namen van de verschillende ijzer-ionen? C Hoe heet het ion van
NAAMGEVING IONEN EINDBAAS A LEVEL 2 NAAMGEVING IONEN EINDBAAS C LEVEL 2 A Hoe heet het ion van broom met een lading van 1-? B Wat zijn de namen van de verschillende ijzer-ionen? C Hoe heet het ion van
SCHEIKUNDE KLAS 3 REACTIES SKILL TREE
 SKILL TREE MOLECUULFORMULES OPDRACHT 1: MOLECUULFORMULES LEVEL 1 A H 2 O C 2 H 6 C C 2 H 6 O D CO 2 E F C 4 H 8 O CHN OPDRACHT 2: MOLECUULFORMULES LEVEL 1 A HNO C 3 H 6 O C C 2 H 2 D C 6 H 5 NO E C 5 H
SKILL TREE MOLECUULFORMULES OPDRACHT 1: MOLECUULFORMULES LEVEL 1 A H 2 O C 2 H 6 C C 2 H 6 O D CO 2 E F C 4 H 8 O CHN OPDRACHT 2: MOLECUULFORMULES LEVEL 1 A HNO C 3 H 6 O C C 2 H 2 D C 6 H 5 NO E C 5 H
namen formules ionogene stoffen van Als je de negatieve ionen (behalve OH - ) koppelt aan H + - ionen ontstaan verbindingen die men zuren noemt.
 namen en formules van ionogene stoffen CH 3 COO - acetaat afkomstig van azijnzuur (ethaanzuur) C 2 O 4 samengestelde ionen HC 2 O 4 - oxalaat beide afkomstig van oxaalzuur (ethaandizuur) waterstofoxalaat
namen en formules van ionogene stoffen CH 3 COO - acetaat afkomstig van azijnzuur (ethaanzuur) C 2 O 4 samengestelde ionen HC 2 O 4 - oxalaat beide afkomstig van oxaalzuur (ethaandizuur) waterstofoxalaat
PORTFOLIO SKI- OF SNOWBOARD INSTRUCTEUR NIVEAU 2 NAAM: DATUM:
 PORTFOLIO SKI- OF SNOWBOARD INSTRUCTEUR NIVEAU 2 NAAM: DATUM: INHOUDSOPGAVE DAGVERSLAG CURSUSDAG 1 3 DAGVERSLAG CURSUSDAG 2 4 DAGVERSLAG CURSUSDAG 3 5 VIDEO ANALYSE 6 FEEDBACK OP JE LES & LVF 7 LVF (KOPIE
PORTFOLIO SKI- OF SNOWBOARD INSTRUCTEUR NIVEAU 2 NAAM: DATUM: INHOUDSOPGAVE DAGVERSLAG CURSUSDAG 1 3 DAGVERSLAG CURSUSDAG 2 4 DAGVERSLAG CURSUSDAG 3 5 VIDEO ANALYSE 6 FEEDBACK OP JE LES & LVF 7 LVF (KOPIE
NATIONALE SCHEIKUNDEOLYMPIADE
 NATIONALE SCHEIKUNDEOLYMPIADE CORRECTIEMODEL VOORRONDE 1 af te nemen in de periode van woensdag 5 januari 01 tot en met woensdag 1 februari 01 Deze voorronde bestaat uit 4 meerkeuzevragen verdeeld over
NATIONALE SCHEIKUNDEOLYMPIADE CORRECTIEMODEL VOORRONDE 1 af te nemen in de periode van woensdag 5 januari 01 tot en met woensdag 1 februari 01 Deze voorronde bestaat uit 4 meerkeuzevragen verdeeld over
Chemie: oefeningen zuren, hydroxiden en zouten
 Chemie: oefeningen zuren, hydroxiden en zouten Teken de structuurformule van salpeterigzuur HNO 2 en van salpeterzuur HNO 3 : Doevoor jezelf telkens ook de controles! Controles HNO 2 : - 2x6 e - (2 O)
Chemie: oefeningen zuren, hydroxiden en zouten Teken de structuurformule van salpeterigzuur HNO 2 en van salpeterzuur HNO 3 : Doevoor jezelf telkens ook de controles! Controles HNO 2 : - 2x6 e - (2 O)
Het leren van de uitspraak van onbekende klanken van Arabische letters. Interfacultaire Lerarenopleidingen, Universiteit van Amsterdam
 ONTWERPONDERZOEK - PAPER 3 ONDERZOEKSINSTRUMENTEN Naam auteur M.H.J. (Mariska) Verbeek-Keizer MA Vakgebied Arabisch Titel صوت العربية / Arabisch De klank van het Onderwerp Het leren van de uitspraak van
ONTWERPONDERZOEK - PAPER 3 ONDERZOEKSINSTRUMENTEN Naam auteur M.H.J. (Mariska) Verbeek-Keizer MA Vakgebied Arabisch Titel صوت العربية / Arabisch De klank van het Onderwerp Het leren van de uitspraak van
De waterconstante en de ph
 EVENWICHTEN BIJ PROTOLYSEREACTIES De waterconstante en de ph Water is een amfotere stof, dat wil zeggen dat het zowel zure als basische eigenschappen heeft. In zuiver water treedt daarom een reactie van
EVENWICHTEN BIJ PROTOLYSEREACTIES De waterconstante en de ph Water is een amfotere stof, dat wil zeggen dat het zowel zure als basische eigenschappen heeft. In zuiver water treedt daarom een reactie van
5 VWO. H8 zuren en basen
 5 VWO H8 zuren en basen Inleiding Opdracht 1, 20 min in tweetallen Nakijken; eventueel vragen stellen 8.2 Zure, neutrale en basische oplossingen 8.2 Zure, neutrale en Indicator (tabel 52A) Zuurgraad 0-14?
5 VWO H8 zuren en basen Inleiding Opdracht 1, 20 min in tweetallen Nakijken; eventueel vragen stellen 8.2 Zure, neutrale en basische oplossingen 8.2 Zure, neutrale en Indicator (tabel 52A) Zuurgraad 0-14?
Wat is de formule van het metaalchloride waarin M het symbool van het metaal voorstelt?
 Chemie Vraag 1 5,0.10-4 mol van een metaalchloride wordt opgelost in water. Er is 60 ml van een 2,5.10-2 mol.l -1 zilvernitraatoplossing nodig om alle chlorideionen neer te slaan onder de vorm van zilverchloride.
Chemie Vraag 1 5,0.10-4 mol van een metaalchloride wordt opgelost in water. Er is 60 ml van een 2,5.10-2 mol.l -1 zilvernitraatoplossing nodig om alle chlorideionen neer te slaan onder de vorm van zilverchloride.
Wat is de formule van het metaalchloride waarin M het symbool van het metaal voorstelt?
 Chemie Vraag 1 5,0.10-4 mol van een metaalchloride wordt opgelost in water. Er is 60 ml van een 2,5.10-2 mol.l -1 zilvernitraatoplossing nodig om alle chlorideionen neer te slaan onder de vorm van zilverchloride.
Chemie Vraag 1 5,0.10-4 mol van een metaalchloride wordt opgelost in water. Er is 60 ml van een 2,5.10-2 mol.l -1 zilvernitraatoplossing nodig om alle chlorideionen neer te slaan onder de vorm van zilverchloride.
NATIONALE SCHEIKUNDEOLYMPIADE
 NATIONALE SCHEIKUNDEOLYMPIADE CORRECTIEMODEL VOORRONDE af te nemen in de periode van januari tot en met 5 februari 04 Deze voorronde bestaat uit 0 meerkeuzevragen verdeeld over 8 onderwerpen en open opgaven
NATIONALE SCHEIKUNDEOLYMPIADE CORRECTIEMODEL VOORRONDE af te nemen in de periode van januari tot en met 5 februari 04 Deze voorronde bestaat uit 0 meerkeuzevragen verdeeld over 8 onderwerpen en open opgaven
Practicum 3 Verf: kleurrijke chemie
 Practicum 3 Verf: kleurrijke chemie 3.1 In de volgende opdrachten ga je je kennis over evenwichten en andere chemische begrippen toepassen en uitbreiden. Je gaat dat doen in de context van verf. Bekijk
Practicum 3 Verf: kleurrijke chemie 3.1 In de volgende opdrachten ga je je kennis over evenwichten en andere chemische begrippen toepassen en uitbreiden. Je gaat dat doen in de context van verf. Bekijk
In de natuur komen voor Cu en Cl respectievelijk de isotopen 63 Cu, 65 Cu en 35 Cl, 37 Cl voor.
 Chemie Vraag 1 In de natuur komen voor Cu en Cl respectievelijk de isotopen 63 Cu, 65 Cu en 35 Cl, 37 Cl voor. Nuclide Nuclidemassa (u) 63 Cu 62,93 65 Cu 64,93 35 Cl 34,97 37 Cl 36,95 Wat is de verhouding
Chemie Vraag 1 In de natuur komen voor Cu en Cl respectievelijk de isotopen 63 Cu, 65 Cu en 35 Cl, 37 Cl voor. Nuclide Nuclidemassa (u) 63 Cu 62,93 65 Cu 64,93 35 Cl 34,97 37 Cl 36,95 Wat is de verhouding
Onderzoekscompetenties. 3 de jaar. Hoe verlopen chemische reacties? A Tekst leerlingen: leerwerkboek
 Onderzoekscompetenties 3 de jaar Hfdst 4 Hoe verlopen chemische reacties? A Tekst leerlingen: leerwerkboek Onderzoek: het behoud van atoomsoorten in een reactiereeks Werkmethode 1. Wat onderzoeken? Probleemstelling
Onderzoekscompetenties 3 de jaar Hfdst 4 Hoe verlopen chemische reacties? A Tekst leerlingen: leerwerkboek Onderzoek: het behoud van atoomsoorten in een reactiereeks Werkmethode 1. Wat onderzoeken? Probleemstelling
Uitwerkingen van de opgaven uit: BASISCHEMIE voor het MLO ISBN , 3 e druk, Uitgeverij Syntax Media Hoofdstuk 14 Zouten bladzijde 1
 BASISCHEMIE het MLO ISBN 9789077423875, 3 e druk, Uitgeverij Syntax Media Hoofdstuk 14 Zouten bladzijde 1 Opgave 1 Van onderstaande zouten worden steeds waterige oplossingen samengevoegd. Welk slecht oplosbare
BASISCHEMIE het MLO ISBN 9789077423875, 3 e druk, Uitgeverij Syntax Media Hoofdstuk 14 Zouten bladzijde 1 Opgave 1 Van onderstaande zouten worden steeds waterige oplossingen samengevoegd. Welk slecht oplosbare
scheikunde oude stijl havo 2015-I
 Snelle auto's 1 maximumscore 2 Voorbeelden van een juist antwoord zijn: De molecuulformule C 7 H 12 voldoet niet aan de algemene formule voor alkanen: C n H 2n+2. Het mengsel bestaat dus niet uitsluitend
Snelle auto's 1 maximumscore 2 Voorbeelden van een juist antwoord zijn: De molecuulformule C 7 H 12 voldoet niet aan de algemene formule voor alkanen: C n H 2n+2. Het mengsel bestaat dus niet uitsluitend
universele gasconstante: R = 8,314 J K -1 mol -1 Avogadroconstante: N A = 6,022 x 10 23 mol -1 normomstandigheden:
 Nuttige gegevens: universele gasconstante: R = 8,314 J K -1 mol -1 vogadroconstante: N = 6,022 x 10 23 mol -1 normomstandigheden: θ = 0 p = 1013 hpa molair volume van een ideaal gas onder normomstandigheden:
Nuttige gegevens: universele gasconstante: R = 8,314 J K -1 mol -1 vogadroconstante: N = 6,022 x 10 23 mol -1 normomstandigheden: θ = 0 p = 1013 hpa molair volume van een ideaal gas onder normomstandigheden:
Correctievoorschrift VMBO-GL en TL 2005
 Correctievoorschrift VMBO-GL en TL 2005 tijdvak 2 NATUUR- EN SCHEIKUNDE 2 CSE GL EN TL Het correctievoorschrift bestaat uit: 1 Regels voor de beoordeling 2 Algemene regels 3 Vakspecifieke regels 4 Beoordelingsmodel
Correctievoorschrift VMBO-GL en TL 2005 tijdvak 2 NATUUR- EN SCHEIKUNDE 2 CSE GL EN TL Het correctievoorschrift bestaat uit: 1 Regels voor de beoordeling 2 Algemene regels 3 Vakspecifieke regels 4 Beoordelingsmodel
TF5 Scheikunde 4 VWO H 8 en H 9 16 juni 2011
 TF5 Scheikunde 4 VWO H 8 en H 9 16 juni 2011 Deze toets bestaat uit 28 onderdelen. Hiervoor zijn in totaal X punten te behalen. Kalkwater Calciumhydroxide, Ca(OH) 2 (s) is matig oplosbaar in water. Als
TF5 Scheikunde 4 VWO H 8 en H 9 16 juni 2011 Deze toets bestaat uit 28 onderdelen. Hiervoor zijn in totaal X punten te behalen. Kalkwater Calciumhydroxide, Ca(OH) 2 (s) is matig oplosbaar in water. Als
Wat is de verhouding tussen de aantallen atomen van de elementen Mg, P en O in magnesiumfosfaat?
 Chemie Vraag 1 Wat is de verhouding tussen de aantallen atomen van de elementen Mg, P en O in magnesiumfosfaat? 1 : 1 : 4 2 : 1 : 4 2 : 3 : 12 3 : 2 : 8 Chemie: vraag 1 Chemie Vraag 2 Welke
Chemie Vraag 1 Wat is de verhouding tussen de aantallen atomen van de elementen Mg, P en O in magnesiumfosfaat? 1 : 1 : 4 2 : 1 : 4 2 : 3 : 12 3 : 2 : 8 Chemie: vraag 1 Chemie Vraag 2 Welke
Wat is de verhouding tussen de aantallen atomen van de elementen Mg, P en O in magnesiumfosfaat?
 Chemie Vraag 1 Wat is de verhouding tussen de aantallen atomen van de elementen Mg, P en O in magnesiumfosfaat? 3 : 2 : 8 2 : 3 : 12 2 : 1 : 4 1 : 1 : 4 Chemie: vraag 1 Chemie Vraag 2 Welke
Chemie Vraag 1 Wat is de verhouding tussen de aantallen atomen van de elementen Mg, P en O in magnesiumfosfaat? 3 : 2 : 8 2 : 3 : 12 2 : 1 : 4 1 : 1 : 4 Chemie: vraag 1 Chemie Vraag 2 Welke
Project Verwenmorgen voor ouderen organiseren Groepen van 5 leerlingen Totaal: 560 minuten
 Project Verwenmorgen voor ouderen organiseren Groepen van 5 leerlingen Totaal: 560 minuten Inleiding en werkwijze: De meeste ouderen vinden het leuk om samen met jongeren iets te doen. Op deze manier hebben
Project Verwenmorgen voor ouderen organiseren Groepen van 5 leerlingen Totaal: 560 minuten Inleiding en werkwijze: De meeste ouderen vinden het leuk om samen met jongeren iets te doen. Op deze manier hebben
Oefenopgaven ENERGIE, REACTIESNELHEID en EVENWICHT
 Oefenopgaven vwo ENERGIE, REACTIESNELHEID en EVENWICHT OPGAVE 1 Happy en Fifax zijn merknamen van middelen die verstopte afvoeren weer ontstoppen. De inhoud van de verpakkingen blijkt te bestaan uit korrels
Oefenopgaven vwo ENERGIE, REACTIESNELHEID en EVENWICHT OPGAVE 1 Happy en Fifax zijn merknamen van middelen die verstopte afvoeren weer ontstoppen. De inhoud van de verpakkingen blijkt te bestaan uit korrels
SCHEIKUNDEOLYMPIADE 2017
 SCHEIKUNDEOLYMPIADE 2017 CORRECTIEMODEL VOORRONDE 1 af te nemen in de periode van 18 tot en met 25 januari 2017 Deze voorronde bestaat uit 20 meerkeuzevragen verdeeld over 8 onderwerpen en 2 opgaven met
SCHEIKUNDEOLYMPIADE 2017 CORRECTIEMODEL VOORRONDE 1 af te nemen in de periode van 18 tot en met 25 januari 2017 Deze voorronde bestaat uit 20 meerkeuzevragen verdeeld over 8 onderwerpen en 2 opgaven met
Oefenopgaven ZUREN en BASEN havo
 Oefenopgaven ZUREN en BASEN havo OPGAVE 1 Men lost de volgende zouten op in water: (i) ammoniumnitraat (ii) kaliumsulfide (iii) natriumwaterstofsulfaat 01 Geef voor elk van deze zouten de oplosvergelijking.
Oefenopgaven ZUREN en BASEN havo OPGAVE 1 Men lost de volgende zouten op in water: (i) ammoniumnitraat (ii) kaliumsulfide (iii) natriumwaterstofsulfaat 01 Geef voor elk van deze zouten de oplosvergelijking.
Lesplanformulier. Les wordt gegeven in een open ruimte met ronde tafels en een computergedeelte. Een les duurt 50 minuten
 Lesplanformulier naam student : Aukelien Stalman opleiding : docent GZW jaar : 3 naam school : Gomarus College Assen coach : klas : 1 datum van de les: mei 2017 Lesonderwerp: Biologie stevigheid en beweging
Lesplanformulier naam student : Aukelien Stalman opleiding : docent GZW jaar : 3 naam school : Gomarus College Assen coach : klas : 1 datum van de les: mei 2017 Lesonderwerp: Biologie stevigheid en beweging
Curie Hoofdstuk 6 HAVO 4
 Rekenen aan reacties Curie Hoofdstuk 6 HAVO 4 6.1 Rekenen met de mol 6.2 Rekenen met massa s 6.3 Concentratie 6.4 SPA en Stappenplan 6.1 Rekenen met de mol Eenheden en grootheden 1d dozijn potloden 12
Rekenen aan reacties Curie Hoofdstuk 6 HAVO 4 6.1 Rekenen met de mol 6.2 Rekenen met massa s 6.3 Concentratie 6.4 SPA en Stappenplan 6.1 Rekenen met de mol Eenheden en grootheden 1d dozijn potloden 12
Werkgelegenheid en verhouding wonen en werken per gemeente, 2013
 Werkgelegenheid en verhouding wonen en werken per gemeente, 2013 Indicator 10 september 2014 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens
Werkgelegenheid en verhouding wonen en werken per gemeente, 2013 Indicator 10 september 2014 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens
Gft-afval verwerkers,
 Indicator 10 januari 2012 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens kunt u via deze link [1] bekijken. De hoeveelheid groente-, fruit-
Indicator 10 januari 2012 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens kunt u via deze link [1] bekijken. De hoeveelheid groente-, fruit-
EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN Dit examen bestaat voor iedere kandidaat uit 5 OPGAVEN
 MAVO-4 II EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN 1974 MAVO-4 Dinsdag 11 juni, 9.00 11.00 NATUUR-EN SCHEIKUNDE II (Scheikunde) OPEN VRAGEN Dit examen bestaat voor iedere kandidaat uit 5 OPGAVEN
MAVO-4 II EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN 1974 MAVO-4 Dinsdag 11 juni, 9.00 11.00 NATUUR-EN SCHEIKUNDE II (Scheikunde) OPEN VRAGEN Dit examen bestaat voor iedere kandidaat uit 5 OPGAVEN
Zouten. Pagina 1 van 11
 Zouten Pagina 1 van 11 Hoofdstuk 7: Zouten 7.1 Inleiding Tot op heden hebben we steeds gezegd dat alle stoffen uit moleculen bestaan. In dit hoofdstuk laten we zien dat dit niet helemaal waar is. Alle
Zouten Pagina 1 van 11 Hoofdstuk 7: Zouten 7.1 Inleiding Tot op heden hebben we steeds gezegd dat alle stoffen uit moleculen bestaan. In dit hoofdstuk laten we zien dat dit niet helemaal waar is. Alle
Dit examen bestaat voor iedere kandidaat uit 20 vragen
 MAVO-4 II EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN 1983 MAVO-C Woensdag 15 juni, 9.00 11.00 NATUUR-EN SCHEIKUNDE II (Scheikunde) MEERKEUZETOETS Dit examen bestaat voor iedere kandidaat uit 20
MAVO-4 II EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN 1983 MAVO-C Woensdag 15 juni, 9.00 11.00 NATUUR-EN SCHEIKUNDE II (Scheikunde) MEERKEUZETOETS Dit examen bestaat voor iedere kandidaat uit 20
5 Water, het begrip ph
 5 Water, het begrip ph 5.1 Water Waterstofchloride is een sterk zuur, het reageert als volgt met water: HCI(g) + H 2 0(I) Cl (aq) + H 3 O + (aq) z b Hierbij reageert water als base. Ammoniak is een zwakke
5 Water, het begrip ph 5.1 Water Waterstofchloride is een sterk zuur, het reageert als volgt met water: HCI(g) + H 2 0(I) Cl (aq) + H 3 O + (aq) z b Hierbij reageert water als base. Ammoniak is een zwakke
Oefentoets zuren en basen havo
 Oefentoets zuren en basen havo Opgave 1 Melk en yoghurt Zweedse voedingswetenschappers hebben in 2014 bij meer dan 10000 mensen onderzocht of melk en melkproducten gezond zijn. Het doel van het onderzoek
Oefentoets zuren en basen havo Opgave 1 Melk en yoghurt Zweedse voedingswetenschappers hebben in 2014 bij meer dan 10000 mensen onderzocht of melk en melkproducten gezond zijn. Het doel van het onderzoek
Deel 1: traditionele kalkwater met koolstofdioxide test.
 Bereiding en eigenschappen van CO 2 Deel 1: traditionele kalkwater met koolstofdioxide test. 1.1 Onderzoeksvraag Hoe kunnen we CO 2 aantonen? 1.2 Mogelijke hypothesen 1.2.1 Geen interactie: Er vormt zich
Bereiding en eigenschappen van CO 2 Deel 1: traditionele kalkwater met koolstofdioxide test. 1.1 Onderzoeksvraag Hoe kunnen we CO 2 aantonen? 1.2 Mogelijke hypothesen 1.2.1 Geen interactie: Er vormt zich
Verkoopprijs woningen, 2010
 Indicator 30 augustus 2011 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens kunt u via deze link [1] bekijken. De gemiddelde verkoopprijs
Indicator 30 augustus 2011 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens kunt u via deze link [1] bekijken. De gemiddelde verkoopprijs
Tijdreeks huishoudelijke energieconsumptie 1980-1995
 Tijdreeks huishoudelijke energieconsumptie 1980-1995 Notitie in opdracht van het RIVM Kees Vringer. Vakgroep Natuurwetenschappen en Samenleving (NW&S). Universiteit Utrecht. Utrecht, Mei 1998. Nummer:
Tijdreeks huishoudelijke energieconsumptie 1980-1995 Notitie in opdracht van het RIVM Kees Vringer. Vakgroep Natuurwetenschappen en Samenleving (NW&S). Universiteit Utrecht. Utrecht, Mei 1998. Nummer:
Verkoopprijs woningen, 2013
 Indicator 29 augustus 2014 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens kunt u via deze link [1] bekijken. De prijzen van bestaande koopwoningen
Indicator 29 augustus 2014 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens kunt u via deze link [1] bekijken. De prijzen van bestaande koopwoningen
Composteer- en vergistingsinstallaties voor gft-afval,
 Composteer- en vergistingsinstallaties voor gft-afval, 1989-2015 Indicator 1 juni 2017 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens kunt
Composteer- en vergistingsinstallaties voor gft-afval, 1989-2015 Indicator 1 juni 2017 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens kunt
Hoofdstuk 8. Opgave 2. Opgave 1. Oefenvragen scheikunde, hoofdstuk 8 en 10, 5 VWO,
 Oefenvragen scheikunde, hoofdstuk 8 en 10, 5 VWO, Hoofdstuk 8 Opgave 1 Bruistabletten bevatten onder andere natriumwaterstofcarbonaat. Als je deze tabletten in water brengt, treedt een reactie op waarbij
Oefenvragen scheikunde, hoofdstuk 8 en 10, 5 VWO, Hoofdstuk 8 Opgave 1 Bruistabletten bevatten onder andere natriumwaterstofcarbonaat. Als je deze tabletten in water brengt, treedt een reactie op waarbij
(g) (g) (g) NH 3. (aq) + Cl - (aq)
 OPGAVE 1 In onderstaand schema is het technische proces voor de bereiding van soda (natriumcarbonaat) weergegeven. De blokken 1, 2, 3 en 4 stellen reactorvaten voor. Door middel van pijlen is aangegeven
OPGAVE 1 In onderstaand schema is het technische proces voor de bereiding van soda (natriumcarbonaat) weergegeven. De blokken 1, 2, 3 en 4 stellen reactorvaten voor. Door middel van pijlen is aangegeven
3. Welke van onderstaande formules geeft een zout aan? A. Al 2O 3 B. P 2O 3 C. C 2H 6 D. NH 3
 Toelatingsexamens en Ondersteunend Onderwijs VOORBLAD EXAMENOPGAVEN Toetsdatum: n.v.t. Vak: Scheikunde voorbeeldexamen 2015 Tijdsduur: 2 uur en 30 minuten De volgende hulpmiddelen zijn toegestaan bij het
Toelatingsexamens en Ondersteunend Onderwijs VOORBLAD EXAMENOPGAVEN Toetsdatum: n.v.t. Vak: Scheikunde voorbeeldexamen 2015 Tijdsduur: 2 uur en 30 minuten De volgende hulpmiddelen zijn toegestaan bij het
Uitwerkingen van de opgaven uit: BASISCHEMIE voor het MLO ISBN , 3 e druk, Uitgeverij Syntax Media Hoofdstuk 18 Oxidimetrie bladzijde 1
 Hoofdstuk 18 Oxidimetrie bladzijde 1 Opgave 1 Bepaal met behulp van tabel II de reactie tussen kaliumpermanganaat in zuur milieu met: a Sn 2+ ionen MnO 4 + 8 H 3O + + 5 e Mn 2+ + 12 H 2O x 2 Sn 2+ Sn 4+
Hoofdstuk 18 Oxidimetrie bladzijde 1 Opgave 1 Bepaal met behulp van tabel II de reactie tussen kaliumpermanganaat in zuur milieu met: a Sn 2+ ionen MnO 4 + 8 H 3O + + 5 e Mn 2+ + 12 H 2O x 2 Sn 2+ Sn 4+
Voorbereiding toelatingsexamen arts/tandarts
 Voorbereiding toelatingsexamen arts/tandarts Oplossingen van 2018 Arts Geel 29 september 2018 Brenda Casteleyn, PhD Vraag 1 Welke waarden moeten worden toegekend aan x en y in de onderstaande reactievergelijking
Voorbereiding toelatingsexamen arts/tandarts Oplossingen van 2018 Arts Geel 29 september 2018 Brenda Casteleyn, PhD Vraag 1 Welke waarden moeten worden toegekend aan x en y in de onderstaande reactievergelijking
Werkplek H >> Startprojectboek Tendens
 H >> Startprojectboek Tendens Werkplek H >> Startprojectboek Tendens Mijn lesplanning bij deze werkplek 1 Is dit de eerste werkplek die je doet? Haal dan de differentiatieopdracht die bij deze werkplek
H >> Startprojectboek Tendens Werkplek H >> Startprojectboek Tendens Mijn lesplanning bij deze werkplek 1 Is dit de eerste werkplek die je doet? Haal dan de differentiatieopdracht die bij deze werkplek
Omschrijven, formules, natuurkunde, stappenplan, begripspracticum
 ONTWERP ONDERZOEK FORMULES OMSCHRIJVEN BIJ NATUURKUNDE IN 3 VWO Naam auteur Margriet van der Laan, Msc Vakgebied Natuurkunde Titel & onderwerp Formules omschrijven bij natuurkunde Opleiding Interfacultaire
ONTWERP ONDERZOEK FORMULES OMSCHRIJVEN BIJ NATUURKUNDE IN 3 VWO Naam auteur Margriet van der Laan, Msc Vakgebied Natuurkunde Titel & onderwerp Formules omschrijven bij natuurkunde Opleiding Interfacultaire
Hoofdstuk 6: Zure en base oplossingen / ph
 Hoofdstuk 6: Zure en base oplossingen / ph 6.1 Herhaling: zure en basische oplossingen Arrhenius definieerde zuren als volgt: zuren zijn polaire covalente verbindingen die bij het oplossen in water H +
Hoofdstuk 6: Zure en base oplossingen / ph 6.1 Herhaling: zure en basische oplossingen Arrhenius definieerde zuren als volgt: zuren zijn polaire covalente verbindingen die bij het oplossen in water H +
Verkoopprijs woningen, 2011
 Indicator 25 mei 2012 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens kunt u via deze link [1] bekijken. De gemiddelde verkoopprijs van bestaande
Indicator 25 mei 2012 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens kunt u via deze link [1] bekijken. De gemiddelde verkoopprijs van bestaande
Verkoopprijs woningen, 2012
 Indicator 28 juni 2013 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens kunt u via deze link [1] bekijken. De gemiddelde verkoopprijs van
Indicator 28 juni 2013 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens kunt u via deze link [1] bekijken. De gemiddelde verkoopprijs van
Emissies naar lucht door de energievoorziening,
 Indicator 1 mei 2012 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens kunt u via deze link [1] bekijken. De emissies van vrijwel alle belangrijke
Indicator 1 mei 2012 U bekijkt op dit moment een archiefversie van deze indicator. De actuele indicatorversie met recentere gegevens kunt u via deze link [1] bekijken. De emissies van vrijwel alle belangrijke
