DRINGEND VEILIGHEIDSBERICHT
|
|
|
- Wouter Goossens
- 5 jaren geleden
- Aantal bezoeken:
Transcriptie
1 [Contact Name] [Department/Title] [Hospital Name] [Address Line 1] [Town/City] [Postal Code] [Country] [Date] Referentie: FA DRINGEND VEILIGHEIDSBERICHT KENNISGEVING OVER UPDATE VAN LIFESTREAM-ETIKETTERING Geachte klant, Met deze brief willen wij u informeren over een corrigerend veiligheidsbericht. Deze corrigerende veiligheidsmaatregel, geïnitieerd door ClearStream Technologies (BD), heeft betrekking op de LifeStream ballonexpandeerbare beklede vasculaire stent. Reden voor dit bericht inzake dit veiligheidsbericht Er zijn klachten gemeld met betrekking tot restenose na implantatie van de LifeStream ballonexpandeerbare beklede vasculaire stent. Deze klachten werden gemeld na normaal klinisch gebruik en ook bij de follow-up van het klinische onderzoek naar het gebruik van de BARD LIFESTREAM ballonexpandeerbare beklede vasculaire stent bij de behandeling van vaatlijden door aorta iliacale occlusie (BOLSTER). Er zijn geen meldingen van patiëntletsel. Het klachtenpercentage voor restenose (0,04%) is hoger dan het percentage dat is gemeld in de FMEA (Failure Modes and Effects Analysis) (0,01%). Met dit bericht inzake de veiligheid in het veld wil ClearStream Technologies gebruikers op de hoogte brengen van het percentage voor restenose en van een update van de gebruiksaanwijzing voor de LifeStream ballonexpandeerbare beklede vasculaire stent. Zie hiervoor de bijgesloten etiketteringsupdate (bijlage 1). Deze informatie zal voortaan in de etikettering van alle toekomstige, door ClearStream (BD) gedistribueerde eenheden worden vermeld. De etiketteringsupdate bevat informatie over de huidige klinische onderzoeksresultaten van de BARD LIFESTREAM ballonexpandeerbare beklede vasculaire stent bij de behandeling van vaatlijden door aorta iliacale occlusie (BOLSTER). Pagina 1 van 12
2 Dit betreft geen terugroeping van het product en dit is ook geen verzoek van ClearStream om naar aanleiding van deze kennisgeving eenheden te retourneren. Uit onze gegevens blijkt dat uw instelling een of meerdere exemplaren heeft aangeschaft van het product waarop dit veiligheidsbericht betrekking heeft, zie Tabel 1 hieronder. Onderdeelnummer Diameter ballon Lengte ballon Lengte schacht LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM Pagina 2 van 12
3 Onderdeelnummer Diameter ballon Lengte ballon Lengte schacht LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM LSM Tabel 1: Betreffende productcodes Pagina 3 van 12
4 Hou er rekening mee dat uw bevoegde autoriteit in kennis wordt gesteld van deze corrigerende veiligheidsactie. Als onderdeel van deze actie vragen wij u om de onderstaande aanwijzingen te volgen en Bard Benelux in kennis te stellen van het door u uitvoeren van de maatregelen van deze corrigerende veiligheidsactie. De door u en uw zorginstelling vereiste actie in verband met dit VB 1. Geef dit veiligheidsbericht door aan alle medewerkers die betrokken zijn bij het gebruik van het LifeStream ballonexpandeerbare vasculaire beklede stent-systeem. 2. Zorg ervoor dat de betrokken medewerkers de inhoud van dit Veiligheidsbericht begrijpen. 3. De bijgevoegde aanpassing van de etikettering (Bijlage 1) moet voor alle LifeStreaminstrumenten die momenteel zijn verspreid worden gebruikt in combinatie met de gebruiksaanwijzing voor de LifeStream ballonexpandeerbare beklede vasculaire stent. 4. Indien u dit product verder verspreid heeft, ga dan na aan welke organisatie dit is gebeurd en stel deze organisatie onmiddellijk op de hoogte van dit bericht. In uw kennisgeving kunt u een kopie van deze brief opnemen. 5. Wij verzoeken u om het bijgevoegd Antwoordformulier effectiviteitscontrole in te vullen en dit terug te sturen naar Bard Benelux NV per [FAX +32(0) of per aan evelyn.triest@crbard.com Opmerking: Hoewel dit veiligheidsbericht niet vereist dat het product wordt geretourneerd, is het wel uiterst belangrijk dat we het door u ingevulde Antwoordformulier effectiviteitscontrole zo snel mogelijk ontvangen. Wij stellen uw medewerking en hulp bij de deze kwestie op prijs, en bieden u onze welgemeende excuses aan voor eventueel ongemak dat uit deze actiekan voortvloeien. Indien u nog vragen hebt of hulp nodig hebt, neem dan contact op met uw locale verkoopsspecialist of locale vertegenwoordiger van de Bard klantenservice via 014/ Met vriendelijke groet Evelyn Triest, RA QA Dept. 1. Bijlage 1: Tekst die moet worden toegevoegd aan gebruiksaanwijzing van LifeStream Pagina 4 van 12
5 REFERENTIE: FA ANTWOORDFORMULIER EFFECTIVITEITSCONTROLE LifeStream ballonexpandeerbare beklede vasculaire stent Door onderstaande informatie in te vullen, bevestigt u dat de corrigerende maatregel inzake de veiligheid in het veld met referentienummer is ontvangen door uw zorginstelling of organisatie, dat deze is gelezen en begrepen en dat de verzochte acties zijn uitgevoerd. Schrijf uw contactgegevens in BLOKLETTERS op en vul het formulier volledig in Naam Functie Naam van klant/ziekenhuis [Vooraf ingevuld veld] Telefoonnummer contactpersoon Handtekening Datum Het volledig ingevulde formulier sturen naar: Evelyn Triest QA coordinator Bard Benelux NV Hagelberg Olen België Tel: +32 (0) Fax: +32 (0) evelyn.triest@crbard.com Pagina 5 van 12
6 Bijlage 1 - Voorgestelde aanvullende tekst die moet worden toegevoegd aan de LifeStream etikettering Samenvatting van klinische studie Er werden in totaal 155 patiënten behandeld in 17 onderzoekscentra in de Verenigde Staten, Europa en Nieuw-Zeeland in de prospectieve, multicentrum, niet-gerandomiseerde, eenarmige studie van de Bard LifeStream ballonexpandeerbare beklede vasculaire stent in de behandeling van aortailicaleocclusies (BOLSTER). In totaal werden 228 proefpersonen opgenomen in de studie, waarvan 155 werden behandeld met het onderzoeksinstrument en werden opgenomen als De Behandelde Populatie. Het doel van deze studie was het beoordelen van de veiligheid en effectiviteit van de Bard LifeStream ballonexpandeerbare beklede vasculaire stent in de behandeling van atherosclerotische laesies van gemeenschappelijke of externe iliacale slagaders. Een gecombineerd eindpunt voor de veiligheid en effectiviteit voor personen die behandeld werden met de Bard LifeStream ballonexpandeerbare vasculaire stent werd vergeleken met een prestatiedoel ontleend aan de gepubliceerde literatuur over iliacale stents. Ten tijde van deze analyse hadden 155 proefpersonen hun controle 9 maanden na de behandeling ondergaan en waren beoordeeld op de primaire en secundaire eindpunten. Patiënten zullen worden gevolgd voor een periode van 36 maanden. Eindpunten van de studie Het primaire eindpunt van de studie is een gecombineerd eindpunt voor de veiligheid en effectiviteit, gedefinieerd als overlijden gerelateerd aan het instrument en/of de behandeling of myocardinfarct (MI) over een periode van 30 dagen, of een targetlaesie-revascularisatie (TLR), majeure amputatie van (een) doelwit-ledema(a)t(en) of restenose over een periode van 9 maanden na de indexprocedure. Overlijden gerelateerd aan het instrument en/of de behandeling, MI, en majeure amputatie van (een) doelwit-ledema(a)t(en) worden beoordeeld door een Clinical Events Committee (CEC -Commissie klinische gebeurtenissen). TLR wordt gedefinieerd als de eerste revascularisatie-behandeling (bijv. PTA, atherectomie, enz.) van de targetlaesie(s) na de indexprocedure, zoals bepaald door een onafhankelijk Angiografisch Centraal Laboratorium (of CEC, indien nodig). Restenose wordt beoordeeld door echo-doppler-onderzoek (EDO), waarbij de targetlaesie(s) een pieksystolische snelheidsverhouding heeft van (PSSR) > 2,4 met post-stenotische turbulentie, zoals bepaald door een onafhankelijk EDO Centraal Laboratorium. In deze studie wijst een PSSR van > 2,4 op > 50% restenose. Secundaire eindpunten waren de volgende, die op verschillende timepoints in de studie werden onderzocht: (1) Aantal ernstige ongewenste voorvallen (MAE s - Major Adverse Events), (2) Onmiddellijk laesie-succes (3) Onmiddellijk behandelingsschema, (4) Onmiddellijk technisch succes, (5) targetlaesie revascularisatie (TLR) (6) target vessel revascularisatie (TVR), (7) Aanhoudend klinisch succes, (8) Primaire doorgankelijkheid (9) Primaire ondersteunde doorgankelijkheid (10) Secundaire doorgankelijkheid en (11) Levenskwaliteit. Onderzochte patiënten In aanmerking komende patiënten hadden intermitterende claudicatio of ischemische rustpijnen angiografische bevestiging van de novo of restenotische (niet-gestente) leasie(s) 50% (inclusief totale occlusies) in de gemeenschappelijke en/of externe iliacale slagaders. Om opgenomen te worden in de studie, moest de diameter van de/het referentievat(en) tussen 4,5 en 12,0 mm zijn en de doellaesie(s) 100 mm totale lengte (per zijde). De patiënten moesten angiografisch bewijs van Pagina 6 van 12
7 een doorgankelijke profunda en/of oppervlakkige? liesslagader hebben. Patiënten werden uitgesloten van de studie als bij hen eerder een vasculaire prothese in het oorspronkelijke iliacale bloedvat was geplaatst, of als de proefpersoon een hersenbloeding of transiënte ischemische aanval (TIA) had gehad binnen drie maanden voorafgaand aan de indexprocedure. Methoden In aanmerking komende proefpersonen werden beschouwd als in het onderzoek opgenomen nadat ze hadden ingestemd met deelname en geïnformeerde toestemming hadden verstrekt. Na de behandeling met de LifeStream ballonexpandeerbare beklede vasculaire stent, vond klinische follow-up plaats bij ontslag, na 30 dagen en 9, 12, 24 en 36 na de indexprocedure. Follow-up controles omvatten onder meer een uitgebreid lichamelijk onderzoek, echo-doppler, Rutherfordclassificatie, ABI-meting en beoordeling van de levenskwaliteit. Zes maanden na de indexprocedure vond een telefonische controle plaats van alle behandelde proefpersonen. Een onafhankelijke Clinical Events Committee (CEC - Commissie klinische gebeurtenissen) heeft alle ongewenste voorvallen gecontroleerd en alle ernstige, onverwachte en aan het instrument gerelateerde ongewenste voorvallen beoordeeld. Daarnaast heeft een onafhankelijk Data Safety Monitoring Board (DSMB - Toezichtscommissie informatie en veiligheid) de veiligheidsinformatie onderzocht, waaronder door de centra gemelde gebeurtenissen en samenvattingen van door de CEC uitgevoerde beoordelingsactiviteiten. De DSMB heeft vastgesteld dat de studie door moet gaan overeenkomstig de beschrijving en aanbevelingen verstrekt over eventueel aan te brengen wijzigingen. Resultaten Patiëntgegevens De Tabellen 1-4 geven een overzicht van de patiëntgegevens, medische geschiedenis, baselinekenmerken en behandelde doelwit-laesies. Tabel 1: Patiëntgegevens Bolster (N=155) Leeftijd (jaar) N 155 Gemiddelde (SD) 64,3 (9,75) Min - Max 42,0 86,0 Geslacht Man 107 (69,0%) Vrouw 48 (31,0%) Gewicht (kg) N 151 Gemiddelde (SD) 79,6 (16,60) Lengte (cm) N 154 Gemiddelde (SD) 170,7 (8,80) BMI (kg/m2) N 151 Gemiddelde (SD) 27,2 (4,81) Tabel 2: Medische geschiedenis patiënt Pagina 7 van 12
8 Categorie Termijn Bolster (N=155) Hart- en vaatziekten Totaal 142 (91,6%) AAA 7 (4,5%) Angina 11 (7,1%) Ziekte van de aorta 7 (4,5%) Atriumfibrilleren (A-FIB) 12 (7,7%) Congestief hartfalen (CHF) 9 (5,8%) Ischemische hartklachten 49 (31,6%) Dyslipidemie 101 (65,2%) Hypertensie 117 (75,5%) Myocardinfarct (MI) 21 (13,5%) Beroerte 8 (5,2%) Overig 54 (34,8%) Nierziekte Totaal 27 (17,4%) Hemodialyse 1 (0,6%) Nierfalen 3 (1,9%) Overig 27 (17,4%) Andere ziekte Totaal 152 (98,1%) Kanker 13 (8,4%) Roken van sigaretten 132 (85,2%) Diabetes 50 (32,3%) Maag-darmstoornissen 17 (11,0%) Ademhalingsstoornissen 23 (14,8%) Overig 78 (50,3%) Opmerking: Een proefpersoon kan meerdere medicijnen gebruiken Tabel 3: Samenvatting van de baseline-kenmerken per proefpersoon Behandelde ledemaat Bolster (N=155) Bilateraal 34 (21,9%) Linkerbeen 72 (46,5%) Rechterbeen 49 (31,6%) Aantal doelwit-laesies (75,5%) 2 34 (21,9%) 3 4 (2,6%) Locatie doelwit-laesie Gemeenschappelijke iliacale slagader 103 (66,5%) Externe iliacale slagader 36 (23,2%) Zowel gemeenschappelijke als externe iliacale slagader Aantal behandelde laesielocaties 16 (10,3%) (71,6%) 2 40 (25,8%) 3 4 (2,6%) Behandelde laesie-locatie Linker gemeenschappelijke iliacale 83 (53,5%) slagader Rechter gemeenschappelijke iliacale 65 (41,9%) slagader Linker externe iliacale slagader 30 (19,4%) Rechter externe iliacale slagader 25 (16,1%) Stenose baseline/vóór behandeling 1 Occlusie 21 (13,5%) Stenose 134 (86,5%) Baseline TASC-score 2 A 96 (61,9%) B 42 (27,1%) C 15 (9,7%) D 2 (1,3%) 1,2 Indien een proefpersoon meer dan één laesie heeft, wordt het ernstigste type gebruikt als categorie voor de Stenose baseline/vóór behandeling en de Baseline TASC-score. Ten tijde van deze analyse werden de 197 laesies behandeld met de LifeStream ballonexpandeerbare beklede vasculaire stent. Tabel 4 toont de kenmerken van de behandelde laesies. Pagina 8 van 12
9 Tabel 4: Samenvatting van doelwit-laesies Mate van verkalking Bolster (N=155) Geen 19 / 197 (9,6%) Licht 51 / 197 (25,9%) Matig 89 / 197 (45,2%) Ernstig 38 / 197 (19,3%) Lengte doelwit-laesie (mm) N 197 Gemiddelde (SD) 30,7 (17,35) Min Max 3,0-100,0 Diameter referentievat (mm) N 197 Gemiddelde (SD) 8,0 (1,27) Min Max 5,0-12,0 Stenose doelwit-laesie (voorafgaand aan behandeling) % N 197 Gemiddelde (SD) 80,3 (13,60) Min Max 30,0-100,0 Zoals gemeld door het onderzoekscentrum. Rapportage patiënten De onderzoekers behandelden 155 patiënten op 17 locaties. In een vooraf vastgestelde analyse, konden op het 9 maanden timepoint 130 proefpersonen worden beoordeeld. Er werd een post-hoc analyse uitgevoerd op basis van 138 proefpersonen. Primaire effectiviteitsresultaten Het primaire eindpunt van de studie is een gecombineerd eindpunt voor de veiligheid en effectiviteit, gedefinieerd als overlijden gerelateerd aan het instrument en/of de behandeling of myocardinfarct (MI) over een periode van 30 dagen, of een targetlaesie-revascularisatie (TLR), majeure amputatie van (een) doelwit-ledema(a)t(en) of restenose over een periode van 9 maanden na de indexprocedure. Het primair gecombineerd eindpunt werd per proefpersoon geanalyseerd. Het aandeel proefpersonen met deze effectiviteits-gebeurtenissen werd vergeleken met het prestatiedoel van 19,5%. Restenose werd door het DUS Core Lab bepaald op basis van objectieve metingen van DUSbeeldvorming, zonder dat andere methoden voor beeldvorming, de noodzaak van een nieuwe behandeling of andere klinische factoren in beschouwing werden genomen om de doorgankelijkheid van de met het LifeStream -instrument behandelde laesies te bepalen. In een vooraf vastgestelde analyse van de 155 proefpersonen die in de studie werden behandeld, werden 25 proefpersonen uitgesloten van de 9-maanden-analyse. Van deze proefpersonen werden 17 uitgesloten om redenen zoals niet te beoordelen beeldvorming, verloren gegaan voor follow-up na 9 maanden, of vroegtijdige beëindiging van deelname aan het onderzoek. Er waren 8 proefpersonen waarvan geen beeldvorming werd uitgevoerd of waarvan de beeldvorming niet beoordeeld kon worden tijdens de controle na 9 maanden. Op het moment van deze analyse hebben zij hun controle na 12 maanden afgerond. Pagina 9 van 12
10 Tabel 5: Primaire gecombineerde eindpuntresultaten (Vooraf vastgestelde analyse) Bolster (N=155) 93,3% Betrouwbaarheidsinterval Proefpersonen met de samengestelde gebeurtenissen 21/130 (16,2%) (10,6%, 23,2%) Proefpersonen behalen resultaten niet tengevolge van Gerelateerd aan instrument en/of behandeling overlijden (<=30 dagen) 0 / 130 (0,0%) Gerelateerd aan instrument en/of behandeling MI (<= 30 dagen) 0 / 130 (0,0%) Majeure amputatie doelwit-ledema(a)t(en) gedurende 9 maanden* 1/ 130 (0,8%) TLR gedurende 9 maanden 6 / 130 (4,6%) Restenose gedurende 9 maanden 15 / 130 (11,5%) * Niet gerelateerd aan instrument en/of behandeling Zoals geanalyseerd op een vooraf gedefinieerde basis, was het primaire gecombineerd eindpuntresultaat 16,2% (p-waarde 0,1987) en behaalde niet het vooraf gedefinieerde statistische prestatiedoel. Er werd een post-hoc analyse uitgevoerd. Deze analyse omvatte de 8 proefpersonen die bij hun controle na 9 maanden geen of geen beoordeelbare beeldvorming hadden, maar tijdens hun controle na 12 maanden wel konden worden beoordeeld. Alle 8 werden vervolgens beoordeeld door het DUS Centraal Laboratorium. Daarnaast werden 5 proefpersonen tijdens het onderzoek na 9 maanden door de voorzitter van de CEC als doorgankelijk beschouwd op basis van DUS-beeldvorming en indien beschikbaar aanvullende beeldvorming, status betreffende nieuwe behandeling, verbetering in Rutherford-classificatie en andere klinische factoren. In Tabel 6 zijn de resultaten van deze post-hoc analyse opgenomen, waarin alle 13 proefpersonen als doorgankelijk werden beschouwd. Tabel 6: Primaire gecombineerde eindpuntresultaten (post-hoc analyse) Bolster (N=155) 93,3% Betrouwbaarheidsinterval 1 Proefpersonen met de gecombineerdegebeurtenissen 16 / 138 (11,6%) (7,0%, 17,8%) Proefpersonen behalen resultaten niet tengevolge van Gerelateerd aan instrument en/of behandeling overlijden (<=30 dagen) 0 / 138 (0,0%) Gerelateerd aan instrument en/of behandeling MI (<= 30 dagen) 0 / 138 (0,0%) Majeure amputatie doelwit-ledema(a)t(en) gedurende 9 maanden 2 1/ 138 (0,7%) TLR gedurende 9 maanden 6 / 138 (4,3%) Restenose gedurende 9 maanden 10 / 138 (7,2%) 1 De betrouwbaarheidsintervallen zijn niet gecorrigeerd voor multipliciteit en zijn bedoeld ter illustratie van de variabiliteit van de bijbehorende samenvattende statistische gegevens. Ze mogen niet worden gebruikt voor het maken van waarschijnlijkheidsberekeningen. 2 Niet gerelateerd aan instrument en/of behandeling Het primaire gecombineerde eindpunt gebaseerd op de post-hoc analyse met gebruik van de controles na 12 maanden en aanvullende klinische factoren was 11,6%. Analyse per ledemaat Op een vooraf gedefinieerde grondslag was het primaire gecombineerd eindpunt per ledemaat bepaald op 21/157 = 13,4%. Zoals geanalyseerd op een post-hoc per ledemaat-basis, wordt het primaire eindpunt bepaald op 16/168 = 9,5%. Secundaire effectiviteitsresultaten De onderstaande Tabel 7 en 8 geven een overzicht van de secundaire effectiviteitseindpunten op het Pagina 10 van 12
11 moment van deze analyse. Tabel 7: Secondaire effectiviteitsresultaten (vooraf gedefinieerde analyse) Resultaat N 95% Betrouwbaarheidsinterval 1 Aantal ernstige ongewenste voorvallen (MAE's) 4,7% (1,9%, 9,4%) Onmiddellijk laesie-succes 98,4% (95,5%, 99,7%) Onmiddellijk behandelingssucces 97,4% (93,4%, 99,3%) Onmiddellijk technisch succes 98,3% (95,6%, 99,5%) Doelwitlaesie revascularisatie (TLR 4,0% (1,5%, 8,5%) Target vessel revascularisatie TVT) 4,0% (1,5%, 8,5%) Aanhoudend klinisch succes 90,5% (84,3%, 94,9%) Primaire doorgankelijkheid 84,5% (77,1%, 90,3%) Primaire ondersteunde doorgankelijkheid 85,3% (78,0%, 90,9%) Secundaire doorgankelijkheid 87,5% (80,5%, 92,7%) Tabel 8: Secondaire effectiviteitseindpunten (post-hoc analyse) Resultaat N 95% Betrouwbaarheidsinterval 1 Primaire doorgankelijkheid 89,1% (82,6%, 93,7%) Primaire ondersteunde doorgankelijkheid 89,8% (83,4%, 94,3%) Secundaire Doorgankelijkheid 91,9% (86,0%, 95,9%) 1 De betrouwbaarheidsintervallen zijn niet gecorrigeerd voor multipliciteit en zijn bedoeld ter illustratie van de variabiliteit van de bijbehorende samenvattende statistische gegevens. Ze mogen niet worden gebruikt voor het maken van waarschijnlijkheidsberekeningen. 2 Alle proefpersonen gevolgd tot dag Alle behandelde laesies/proefpersonen/stents met beoordeelbare angiografische beeldvorming bij implantaat 4 Alle proefpersonen die de controle na 9 maanden ondergingen waarbij de Rutherford-classificatie door de onderzoeker werd beoordeeld 5 Alle personen die de controle na 9 maanden ondergingen met beoordeelbare echo-doppler-beeldvorming 6 Alle proefpersonen die de controle na 9 maanden en/of 12 maanden ondergingen met beoordeelbare echo-doppler-beeldvorming Er werd een Kaplan-Meier analyse van RDL per proefpersoon uitgevoerd; de resultaten zijn weergegeven in Afbeelding 3. De Kaplan-Meier schatting van de incidentie van RDL? na 9 maanden (dag 300) was 3,9% (95% CI 1,8%, 8,6%). Afbeelding 3: Kaplan-Meier Analyse van RDL per proefpersoon (als behandelde populatie) Overlevingskans Tijd tot gebeurtenis (dagen) De levenskwaliteit werd beoordeeld met behulp van de Vragenlijst loopbeperking (VLP). De gemiddelde totaalscore op baseline was 32,0. Na 9 maanden was de gemiddelde totaalscore 64,7, hetgeen neerkomt op een stijging ten opzichte van baseline van 32,7. In het algemeen werden verbeteringen waargenomen op elk gebied van de VLP. Samenvatting betreffende veiligheid Pagina 11 van 12
12 Van de 155 proefpersonen meldden 110 proefpersonen (71,0%) 299 ongewenste voorvallen (adverse events - AE s.) Zestig (60) proefpersonen melden ernstige ongewenste voorvallen (60/110 = 54,5%). Het merendeel van de proefpersonen ondervond AE s die niet gerelateerd waren aan het instrument (86/110; 78,2%) en/of de procedures (81/110; 73,6%). Er werden geen onverwachte ongewenste apparaat-effecten (UADE s - unanticipated adverse device effects) gemeld. Tabel 9: Samenvatting betreffende veiligheid Totaal aantal voorvallen 299 Totaal aantal proefpersonen met ten minste één AE 110 (71,0%) Gerelateerd aan instrument 1, 2 Zeker gerelateerd 8 (7,3%) Mogelijk gerelateerd 16 (14,5%) Niet gerelateerd 86 (78,2%) Gerelateerd aan procedure 1, 2 Zeker gerelateerd 20 (18,2%) Mogelijk gerelateerd 9 (8,2%) Niet gerelateerd 81 (73,6%) Ernstige AE (SAE) 1 60 (54,5%) SAE Zeker of mogelijk gerelateerd aan instrument 9 (15,0%) SAE Niet gerelateerd aan instrument 51 (85,0%) Bolster (N=155) Door de onderzoekcentra gemeld 1 Proefpersonen worden slechts eenmaal geteld, met het hoogste niveau van gerelateerdheid. 2 De percentages zijn gebaseerd op de grootste gemene deler van 110, het totaal aantal proefpersonen met minstens 1 AE De typen veiligheidsgebeurtenissen die in de studie zijn ondervonden, worden ook verwacht voor deze patiëntenpopulatie. Alle gemelde ongewenste voorvallen gerelateerd aan het instrument waren in overeenstemming met de AE s die opgenomen zijn in deel F Mogelijke ongewenste voorvallen. Over het algemeen lijken de profielen van ongewenste voorvallen vergelijkbaar met de zorgstandaard voor PTA en het plaatsen van een stent in de iliacale slagaderen. Overzicht sterfgevallen patiënten Op de datum van dit verslag waren vijf proefpersonen overleden. Geen van de sterfgevallen werden beschouwd als verband houdend met het onderzoeksinstrument of de onderzoeksbehandeling, zoals door de CEC bepaald. Conclusies uit de studie In het prospectieve, multicentrum, niet-gerandomiseerde, eenarmige studie van de Bard LifeStream ballonexpandeerbare beklede vasculaire stent in de behandeling van aorta iliac occlusie (BOLSTER) werd een gecombineerd eindpunt voor veiligheid en effectiviteit vergeleken met een prestatiedoel ontleend aan de gepubliceerde literatuur over iliacale stents. Ten tijde van deze analyse hadden 155 proefpersonen hun controle 9 maanden na de behandeling ondergaan en waren beoordeeld op de primaire en secundaire eindpunten. De typen veiligheidsgebeurtenissen die in de studie zijn gevonden, worden ook verwacht voor deze patiëntenpopulatie. Over het algemeen lijken de profielen van ongewenste voorvallen vergelijkbaar met de zorgstandaard PTA en het plaatsen van een stent in de iliacale slagaderen. De resultaten van de klinische studie tonen aan dat de LifeStream ballonexpandeerbare beklede vasculaire stent veilige en effectief is voor de behandeling van atherosclerotische laesies van de iliaca communis of externa Pagina 12 van 12
BD staakt de productie en distributie van deze hulpmiddelen en verwijdert deze producten per direct uit ziekenhuizen en distributiecentra.
 DATE CORRECTIEVE ACTIE IN HET VELD KENNISGEVING VOOR PRODUCTVERWIJDERING: BM-RAP-19-001-003 BARD hulpmiddelen van gaas voor verzakking van organen in het bekken en stressincontinentie bij vrouwen Hulpmiddelen
DATE CORRECTIEVE ACTIE IN HET VELD KENNISGEVING VOOR PRODUCTVERWIJDERING: BM-RAP-19-001-003 BARD hulpmiddelen van gaas voor verzakking van organen in het bekken en stressincontinentie bij vrouwen Hulpmiddelen
5-jaars Follow-up van de FAME studie
 5-jaars Follow-up van de FAME studie WCN Congres 2015, Amsterdam 20-11-2015 Drs. L.X. van Nunen namens de FAME studiegroep Potential conflicts of interest Ik, Lokien X. van Nunen, heb GEEN conflicts of
5-jaars Follow-up van de FAME studie WCN Congres 2015, Amsterdam 20-11-2015 Drs. L.X. van Nunen namens de FAME studiegroep Potential conflicts of interest Ik, Lokien X. van Nunen, heb GEEN conflicts of
Cordis roept de genoemde loten vrijwillig terug.
 Ziekenhuis T.a.v. de apotheek Straat Post code Plaats DRINGEND VEILIGHEIDSBULLETIN ( RECALL) Cordis PRECISE PRO RX Nitinol Stent System (Carotid) 16 artikelnummers, 179 lotnummers zie catalogus / lotnummerlijst
Ziekenhuis T.a.v. de apotheek Straat Post code Plaats DRINGEND VEILIGHEIDSBULLETIN ( RECALL) Cordis PRECISE PRO RX Nitinol Stent System (Carotid) 16 artikelnummers, 179 lotnummers zie catalogus / lotnummerlijst
DRINGEND - VEILIGHEIDSKENNISGEVING EINDGEBRUIKERS
 DRINGEND - VEILIGHEIDSKENNISGEVING EINDGEBRUIKERS Handelsnaam: AbViser TM AutoValve TM -instrument voor intra-abdominale drukmeting (zie bijlage 1 voor meer informatie) Uitgiftedatum: 25 april 2018 REF.nr.:
DRINGEND - VEILIGHEIDSKENNISGEVING EINDGEBRUIKERS Handelsnaam: AbViser TM AutoValve TM -instrument voor intra-abdominale drukmeting (zie bijlage 1 voor meer informatie) Uitgiftedatum: 25 april 2018 REF.nr.:
DRINGEND VEILIGHEIDSBULLETIN TERUGROEPACTIE MEDISCH HULPMIDDEL
 DRINGEND VEILIGHEIDSBULLETIN TERUGROEPACTIE MEDISCH HULPMIDDEL MOBICATH tweezijdige geleideschacht productnummers: D140010 en D140011 partijnummers: Zie bijlage Diegem, 28 februari 2017 Ref. FMJR/17-026
DRINGEND VEILIGHEIDSBULLETIN TERUGROEPACTIE MEDISCH HULPMIDDEL MOBICATH tweezijdige geleideschacht productnummers: D140010 en D140011 partijnummers: Zie bijlage Diegem, 28 februari 2017 Ref. FMJR/17-026
BELANGRIJKE VEILIGHEIDSKENNISGEVING
 Pagina 1 van 3 BELANGRIJKE VEILIGHEIDSKENNISGEVING Palindrome Precision SI chronische katheter, Palindrome SI chronische katheter, Palindrome Precision HSI chronische katheter en Palindrome HSI chronische
Pagina 1 van 3 BELANGRIJKE VEILIGHEIDSKENNISGEVING Palindrome Precision SI chronische katheter, Palindrome SI chronische katheter, Palindrome Precision HSI chronische katheter en Palindrome HSI chronische
URGENT - Correctie m.b.t. medisch apparaat IntelliVue MX40 Ontbrekende waarschuwingen in de gebruiksaanwijzing
 Beste klant, Er is een probleem gevonden in de van de Philips IntelliVue MX40 voor softwareversies B.05, B.06 and B.06.5X. U kunt uw IntelliVue MX40 veilig blijven gebruiken. In deze en ontbreken waarschuwingen
Beste klant, Er is een probleem gevonden in de van de Philips IntelliVue MX40 voor softwareversies B.05, B.06 and B.06.5X. U kunt uw IntelliVue MX40 veilig blijven gebruiken. In deze en ontbreken waarschuwingen
Externe stroomadapters Ref voor RENASYS GO
 Smith & Nephew Nederland C.V. Postbus 525, 2130 AM Hoofddorp Kruisweg 637, 2132 NB Hoofddorp T. 020-654 39 99 F. 020-653 20 99 www.smith-nephew.com Naam klant Naam product Straat en huisnummer Postcode
Smith & Nephew Nederland C.V. Postbus 525, 2130 AM Hoofddorp Kruisweg 637, 2132 NB Hoofddorp T. 020-654 39 99 F. 020-653 20 99 www.smith-nephew.com Naam klant Naam product Straat en huisnummer Postcode
Dringende veiligheidsinstructie Terugroeping van de partij van de gabcontrol D-Dimer sneltest (M09DD02) uit de markt
 Am Wassermann 28 50829 Köln Geadresseerde: Gebruikers, exploitanten, distributeurs van de gabcontrol D-Dimer sneltest (M09DD02) Praxis- & Drogendiagnostik Am Wassermann 28 D-50829 Köln Telefoon: +49 221
Am Wassermann 28 50829 Köln Geadresseerde: Gebruikers, exploitanten, distributeurs van de gabcontrol D-Dimer sneltest (M09DD02) Praxis- & Drogendiagnostik Am Wassermann 28 D-50829 Köln Telefoon: +49 221
BELANGRIJK BERICHT VOOR KLANTEN INTREKKING CE , PROMETRA -PROGRAMMEERBARE POMP VAN FLOWONIX MEDICAL
 BELANGRIJK BERICHT VOOR KLANTEN INTREKKING CE 558455, PROMETRA -PROGRAMMEERBARE POMP VAN FLOWONIX MEDICAL Type actie: Bericht aan klant over de intrekking van CE-keurmerk 558455 Productcodes: Prometra-pomp
BELANGRIJK BERICHT VOOR KLANTEN INTREKKING CE 558455, PROMETRA -PROGRAMMEERBARE POMP VAN FLOWONIX MEDICAL Type actie: Bericht aan klant over de intrekking van CE-keurmerk 558455 Productcodes: Prometra-pomp
PRODUCTKENNISGEVING EMEA0759 Homepump C-Series met DEHP-vrije slang niet 5-FU-compatibel
 DOBFAR Eekhorstweg 37 7942 KC, Mepple The Netherlands 3 maart 2017 Geachte klant van Halyard Health, Wat is de reden van deze follow-up van de vrijwillige productkennisgeving? Halyard Health (voorheen
DOBFAR Eekhorstweg 37 7942 KC, Mepple The Netherlands 3 maart 2017 Geachte klant van Halyard Health, Wat is de reden van deze follow-up van de vrijwillige productkennisgeving? Halyard Health (voorheen
10 januari 2018 DRINGEND: BERICHT INZAKE DE VEILIGHEID IN HET VELD VAN TISSU-TRANS-PRODUCTEN
 10 januari 2018 DRINGEND: BERICHT INZAKE DE VEILIGHEID IN HET VELD VAN TISSU-TRANS-PRODUCTEN Geachte klant/distributeur van het hulpmiddel, Het doel van deze brief is u te laten weten dat Shippert Medical
10 januari 2018 DRINGEND: BERICHT INZAKE DE VEILIGHEID IN HET VELD VAN TISSU-TRANS-PRODUCTEN Geachte klant/distributeur van het hulpmiddel, Het doel van deze brief is u te laten weten dat Shippert Medical
URGENT TERUGROEPINGSBERICHT enflow vloeistofverwarmingssysteem - Disposable cassettes
 URGENT TERUGROEPINGSBERICHT enflow vloeistofverwarmingssysteem - Disposable cassettes Let op: Distributeurs en eindgebruikers van het enflow vloeistofverwarmingssysteem. Geachte klant, Het doel van deze
URGENT TERUGROEPINGSBERICHT enflow vloeistofverwarmingssysteem - Disposable cassettes Let op: Distributeurs en eindgebruikers van het enflow vloeistofverwarmingssysteem. Geachte klant, Het doel van deze
Onderwerp: BERICHT INZAKE DE VEILIGHEID IN HET VELD - VERWIJDERING
 11 maart 2015 Aan: Ziekenhuizen en chirurgen Onderwerp: BERICHT INZAKE DE VEILIGHEID IN HET VELD - VERWIJDERING FSN/FSCA: FA 2016-02 Betrokken product: Revitan proximale heupstelen (maat 55-105) en Revitan
11 maart 2015 Aan: Ziekenhuizen en chirurgen Onderwerp: BERICHT INZAKE DE VEILIGHEID IN HET VELD - VERWIJDERING FSN/FSCA: FA 2016-02 Betrokken product: Revitan proximale heupstelen (maat 55-105) en Revitan
KENNISGEVING DRINGENDE PRODUCTVEILIGHEIDSACTIE LFIT TM anatomische CoCr V40 TM femurkop
 KENNISGEVING DRINGENDE PRODUCTVEILIGHEIDSACTIE 11 oktober 2016 Productveiligheidsactienr.: Beschrijving: RA2016-028 Catalogusnr(s): 6260-9-236, 6260-9-240, 6260-9-244, 6260-9-340, 6260-9-344, 6260-9-440,
KENNISGEVING DRINGENDE PRODUCTVEILIGHEIDSACTIE 11 oktober 2016 Productveiligheidsactienr.: Beschrijving: RA2016-028 Catalogusnr(s): 6260-9-236, 6260-9-240, 6260-9-244, 6260-9-340, 6260-9-344, 6260-9-440,
DRINGENDE VEILIGHEIDSMEDEDELING PRODUCT RECALL
 COMMERCIËLE NAAM: NC Trek RX Coronaire dilatatiekatheter NC Traveler RX Coronaire dilatatiekatheter NC Tenku RX PTCA ballonkatheter FSCA-Identificatie: Type Actie: Terugroeping product T.a.v.: Dienst Interventionele
COMMERCIËLE NAAM: NC Trek RX Coronaire dilatatiekatheter NC Traveler RX Coronaire dilatatiekatheter NC Tenku RX PTCA ballonkatheter FSCA-Identificatie: Type Actie: Terugroeping product T.a.v.: Dienst Interventionele
Hoofdstuk 2: Preprocedurele serum waarden van acute-fase reagentia en de prognose na percutane coronaire interventie
 Samenvatting 111 CHAPTER 10 Ondanks verbeteringen in de techniek van percutane coronaire interventie (PCI), blijft restenose een belangrijk probleem. De reactie van de vaatwand op beschadiging speelt een
Samenvatting 111 CHAPTER 10 Ondanks verbeteringen in de techniek van percutane coronaire interventie (PCI), blijft restenose een belangrijk probleem. De reactie van de vaatwand op beschadiging speelt een
Urgent veiligheidsbericht
 Urgent veiligheidsbericht Productnaam: twinsys dubbele offset-adapter FSCA-ID-nr.: FSCA 16/04 Soort maatregel: Terugroeping van betrokken partijnummers Bettlach, 20 juli 2016 Uitgegeven door: Geadresseerde:
Urgent veiligheidsbericht Productnaam: twinsys dubbele offset-adapter FSCA-ID-nr.: FSCA 16/04 Soort maatregel: Terugroeping van betrokken partijnummers Bettlach, 20 juli 2016 Uitgegeven door: Geadresseerde:
Belangrijk - Veiligheidskennisgeving
 Geachte klant, Belangrijk - Als onderdeel van Samsung Electronics continue aandacht voor prestaties en veiligheid, hebben we een mogelijk probleem geïdentificeerd dat van invloed kan zijn op het Samsung
Geachte klant, Belangrijk - Als onderdeel van Samsung Electronics continue aandacht voor prestaties en veiligheid, hebben we een mogelijk probleem geïdentificeerd dat van invloed kan zijn op het Samsung
DRINGEND: Veiligheidsbulletin. LFIT V40 conussen, V40 conussen en PCA conussen Vitallium femurkoppen
 Ikaroslaan 12 1930 Zaventem Tel: +32 (0)2 717 92 10 Fax: +32 (0)2 725 11 78 DRINGEND: Veiligheidsbulletin FSCA-nummer: Soort actie: Omschrijving: Productveiligheidsactie RA2014-170ext Corrigerende veiligheidsactie:
Ikaroslaan 12 1930 Zaventem Tel: +32 (0)2 717 92 10 Fax: +32 (0)2 725 11 78 DRINGEND: Veiligheidsbulletin FSCA-nummer: Soort actie: Omschrijving: Productveiligheidsactie RA2014-170ext Corrigerende veiligheidsactie:
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk. De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak Officiële titel: De rol van endoscopische echografie
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak Officiële titel: De rol van endoscopische echografie
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk. De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak Officiële titel: De rol van endoscopische echografie
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak Officiële titel: De rol van endoscopische echografie
DRINGENDE VEILIGHEIDSKENNISGEVING UIT DE PRAKTIJK VOOR MEDISCH HULPMIDDEL
 29.03.2017 Aan: Onderwerp: Chirurgen DRINGENDE VEILIGHEIDSKENNISGEVING UIT DE PRAKTIJK VOOR MEDISCH HULPMIDDEL Betreft de volgende producten: Bepaalde loten van de volgende implantaten: Vanguard Rocc,
29.03.2017 Aan: Onderwerp: Chirurgen DRINGENDE VEILIGHEIDSKENNISGEVING UIT DE PRAKTIJK VOOR MEDISCH HULPMIDDEL Betreft de volgende producten: Bepaalde loten van de volgende implantaten: Vanguard Rocc,
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk. De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak Officiële titel: De rol van endoscopische echografie
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak Officiële titel: De rol van endoscopische echografie
DRINGEND: VEILIGHEIDSBERICHT ETHICON Temporary Cardiac Pacing Wire, productcodes TPW10 en TPW30
 DRINGEND: VEILIGHEIDSBERICHT ETHICON Temporary Cardiac Pacing Wire, productcodes TPW10 en Diegem, 7 september 2015 Ref. FMJR\15-281 Geachte heer, mevrouw, ETHICON is van start gegaan met een vrijwillige
DRINGEND: VEILIGHEIDSBERICHT ETHICON Temporary Cardiac Pacing Wire, productcodes TPW10 en Diegem, 7 september 2015 Ref. FMJR\15-281 Geachte heer, mevrouw, ETHICON is van start gegaan met een vrijwillige
URGENT Veiligheidsbericht Correctie medisch apparaat
 Beste klant, Volgens onze gegevens beschikt u over een van de hierboven vermelde V60-beademingsapparaten. Via dit veiligheidsbericht (FSN) willen we u meedelen dat Respironics California, LLC ('Respironics')
Beste klant, Volgens onze gegevens beschikt u over een van de hierboven vermelde V60-beademingsapparaten. Via dit veiligheidsbericht (FSN) willen we u meedelen dat Respironics California, LLC ('Respironics')
DRINGENDE TERUGROEPACTIE VAN MEDISCHE PRODUCTEN
 DRINGENDE TERUGROEPACTIE VAN MEDISCHE PRODUCTEN 2 februari 2016 Biomet France SARL Plateau de Lautagne 26000 Valence, Frankrijk Telefoon: (33) 04 75 75 91 00 Fax: (33) 04 75 75 91 01 Aan: Tandartsen en
DRINGENDE TERUGROEPACTIE VAN MEDISCHE PRODUCTEN 2 februari 2016 Biomet France SARL Plateau de Lautagne 26000 Valence, Frankrijk Telefoon: (33) 04 75 75 91 00 Fax: (33) 04 75 75 91 01 Aan: Tandartsen en
Belangrijke Veiligheidsinformatie over EFIENT (prasugrel)
 Belangrijke Veiligheidsinformatie over EFIENT (prasugrel) EFIENT (prasugrel) behoort tot de farmacotherapeutische groep van de bloedplaatjesaggregatieremmers (heparine niet meegerekend), een groep waaronder
Belangrijke Veiligheidsinformatie over EFIENT (prasugrel) EFIENT (prasugrel) behoort tot de farmacotherapeutische groep van de bloedplaatjesaggregatieremmers (heparine niet meegerekend), een groep waaronder
DRINGENDE VEILIGHEIDSINFORMATIE PAS
 DRINGENDE VEILIGHEIDSINFORMATIE PAS-016-841 BD Vacutainer Push Button Bloedafnameset : 367342, s: 5355533 en 5356681 17 augustus 2016 Aan: Verantwoordelijke voor Veiligheid van Medische Hulpmiddelen, Risicomanager,
DRINGENDE VEILIGHEIDSINFORMATIE PAS-016-841 BD Vacutainer Push Button Bloedafnameset : 367342, s: 5355533 en 5356681 17 augustus 2016 Aan: Verantwoordelijke voor Veiligheid van Medische Hulpmiddelen, Risicomanager,
Indicatorensets Meetbaar Beter
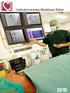 Indicatorensets Meetbaar Beter 2015 Uitkomstindicatoren Uitkomstindicator Definitie Coronairlijden Aortakleplijden Atriumfibrilleren PCI CB AVR TAVI CB Procedurele 30-daagse 120-daagse 1-jaars 30-daagse
Indicatorensets Meetbaar Beter 2015 Uitkomstindicatoren Uitkomstindicator Definitie Coronairlijden Aortakleplijden Atriumfibrilleren PCI CB AVR TAVI CB Procedurele 30-daagse 120-daagse 1-jaars 30-daagse
Nederlandse samenvatting
 198 Het eerste deel van dit proefschrift beschrijft de effectiviteit van clopidogrel en tirofiban in patiënten met een acuut hart infarct verwezen voor een spoed dotter behandeling. In hoofdstuk 1 werd
198 Het eerste deel van dit proefschrift beschrijft de effectiviteit van clopidogrel en tirofiban in patiënten met een acuut hart infarct verwezen voor een spoed dotter behandeling. In hoofdstuk 1 werd
Formulier Voortgangsrapportage
 Formulier Voortgangsrapportage De METC azm/um wil van al het door haar beoordeelde WMO-onderzoek jaarlijks een voortgangsrapportage zien. Zij heeft deze eis daartoe opgenomen in de tekst van haar eigen
Formulier Voortgangsrapportage De METC azm/um wil van al het door haar beoordeelde WMO-onderzoek jaarlijks een voortgangsrapportage zien. Zij heeft deze eis daartoe opgenomen in de tekst van haar eigen
BELANGRIJKE VEILIGHEIDSKENNISGEVING
 +44 (0) 2920 854 390 +44 (0) 2920 854 395 BRUNEL WAY, BAGLAN ENERGY PARK, NEATH, SA11 2GA, UK www.ecolabcc.com infocc@ecolab.com BELANGRIJKE VEILIGHEIDSKENNISGEVING Overeenkomstig MEDDEV 2.12/1 rev. 8
+44 (0) 2920 854 390 +44 (0) 2920 854 395 BRUNEL WAY, BAGLAN ENERGY PARK, NEATH, SA11 2GA, UK www.ecolabcc.com infocc@ecolab.com BELANGRIJKE VEILIGHEIDSKENNISGEVING Overeenkomstig MEDDEV 2.12/1 rev. 8
Kennisgeving veiligheid Belangrijke informatie betreffende medisch instrument Imager II Angiographic Catheter
 Boston Scientific International S.A. ZAC Paris Nord II/Bât Emerson - 33 rue des Vanesses 93420 Villepinte Siège social : Parc du Val Saint Quentin 2 rue René Caudron 78960 Voisins le Bretonneux France
Boston Scientific International S.A. ZAC Paris Nord II/Bât Emerson - 33 rue des Vanesses 93420 Villepinte Siège social : Parc du Val Saint Quentin 2 rue René Caudron 78960 Voisins le Bretonneux France
Stereotactische radiochirurgie bij hersenmetastasen in het ARTI De resultaten met betrekking tot de overleving en de mate van lokale controle
 Stereotactische radiochirurgie bij hersenmetastasen in het ARTI De resultaten met betrekking tot de overleving en de mate van lokale controle Nurer Gergin Radiotherapeutisch Laborant, UMC Utrecht Cancer
Stereotactische radiochirurgie bij hersenmetastasen in het ARTI De resultaten met betrekking tot de overleving en de mate van lokale controle Nurer Gergin Radiotherapeutisch Laborant, UMC Utrecht Cancer
DRINGENDE VEILIGHEIDSWAARSCHUWING
 «IA_Customer_Name» «IA_Facility_Site» «IA_Street_Address» «IA_City», «IA_State» «IA_Zip_Code» Beste klant, Met deze dringende veiligheidswaarschuwing willen we u over het volgende informeren: wat het probleem
«IA_Customer_Name» «IA_Facility_Site» «IA_Street_Address» «IA_City», «IA_State» «IA_Zip_Code» Beste klant, Met deze dringende veiligheidswaarschuwing willen we u over het volgende informeren: wat het probleem
Nederlanse Samenvatting. Nederlandse Samenvatting
 Nederlandse Samenvatting 197 198 Samenvatting In het proefschrift worden diverse klinische aspecten van primaire PCI (Primaire Coronaire Interventie) voor de behandeling van een hartinfarct onderzocht.
Nederlandse Samenvatting 197 198 Samenvatting In het proefschrift worden diverse klinische aspecten van primaire PCI (Primaire Coronaire Interventie) voor de behandeling van een hartinfarct onderzocht.
BELANGRIJKE VEILIGHEIDSWAARSCHUWING
 BELANGRIJKE VEILIGHEIDSWAARSCHUWING Productnaam: Secundaire sets met terugslagklep Productcodes: 72951NE, 72947NE, 72948NE, 72949NE, 72987NE FSCA-identificeerder: RA-2016-12-02 Datum: 14 april 2017 Type
BELANGRIJKE VEILIGHEIDSWAARSCHUWING Productnaam: Secundaire sets met terugslagklep Productcodes: 72951NE, 72947NE, 72948NE, 72949NE, 72987NE FSCA-identificeerder: RA-2016-12-02 Datum: 14 april 2017 Type
Philips Healthcare - 1/8 - FSN A Juni 2019
 Philips Healthcare - 1/8 - FSN86100188A Beste klant, Philips heeft vastgesteld dat de M3539A netvoedingsmodule voor de HeartStart MRxmonitor/defibrillator mogelijk sneller defect kan raken dan verwacht.
Philips Healthcare - 1/8 - FSN86100188A Beste klant, Philips heeft vastgesteld dat de M3539A netvoedingsmodule voor de HeartStart MRxmonitor/defibrillator mogelijk sneller defect kan raken dan verwacht.
Samenvatting*en*conclusies* *
 Samenvatting*en*conclusies* * Kwaliteitscontrole-in-vaatchirurgie.-Samenvattinginhetnederlands. Inditproefschriftstaankwaliteitvanzorgenkwaliteitscontrolebinnende vaatchirurgie zowel vanuit het perspectief
Samenvatting*en*conclusies* * Kwaliteitscontrole-in-vaatchirurgie.-Samenvattinginhetnederlands. Inditproefschriftstaankwaliteitvanzorgenkwaliteitscontrolebinnende vaatchirurgie zowel vanuit het perspectief
Onderstaande vragen zijn van toepassing op de periode 6-12 maanden postoperatief
 9. Follow-up Aantal maanden? Datum: Setting: O klinisch O poliklinisch Beoordelaar: (naam) Algemeen Onderstaande vragen zijn van toepassing op de periode 6- postoperatief Is de patient opgenomen geweest
9. Follow-up Aantal maanden? Datum: Setting: O klinisch O poliklinisch Beoordelaar: (naam) Algemeen Onderstaande vragen zijn van toepassing op de periode 6- postoperatief Is de patient opgenomen geweest
Art.nr Beschrijving Batchnr.
 Smith & Nephew Nederland C.V. T 020-654 39 99 Postbus 525, 2130 AM Hoofddorp F 020-653 20 99 Kruisweg 637, 2132 NB Hoofddorp www.smith-nephew.nl «Instelling» «TAV» «Afdeling» «Adres» «PC» «Plaats» 7 april
Smith & Nephew Nederland C.V. T 020-654 39 99 Postbus 525, 2130 AM Hoofddorp F 020-653 20 99 Kruisweg 637, 2132 NB Hoofddorp www.smith-nephew.nl «Instelling» «TAV» «Afdeling» «Adres» «PC» «Plaats» 7 april
Onderwerp: DRINGENDE VEILIGHEIDSKENNISGEVING UIT DE PRAKTIJK VOOR MEDISCH HULPMIDDEL - CORRECTIE
 13 augustus 2017 Aan: Clinicus Onderwerp: DRINGENDE VEILIGHEIDSKENNISGEVING UIT DE PRAKTIJK VOOR MEDISCH HULPMIDDEL - CORRECTIE Betrokken product: Verscheidene tandheelkundige producten, zie bijlage 2
13 augustus 2017 Aan: Clinicus Onderwerp: DRINGENDE VEILIGHEIDSKENNISGEVING UIT DE PRAKTIJK VOOR MEDISCH HULPMIDDEL - CORRECTIE Betrokken product: Verscheidene tandheelkundige producten, zie bijlage 2
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Observationeel onderzoek van de BioMimics 3D-stent bij de behandeling van perifeer vaatlijden Officiële titel: Een prospectief,
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Observationeel onderzoek van de BioMimics 3D-stent bij de behandeling van perifeer vaatlijden Officiële titel: Een prospectief,
Urgente Field Safety Notice (Terugroepactie)
 Urgente Field Safety Notice (Terugroepactie) Cordis Vista Brite Tip & ADROIT TM Guiding Catheters Februari 07, 2019, bijgewerkt Maart 06, 2019 Zeer gewaardeerde klant, Het doel van dit schrijven is om
Urgente Field Safety Notice (Terugroepactie) Cordis Vista Brite Tip & ADROIT TM Guiding Catheters Februari 07, 2019, bijgewerkt Maart 06, 2019 Zeer gewaardeerde klant, Het doel van dit schrijven is om
INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN LONGEMBOLIE
 INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN LONGEMBOLIE Hokusai post VTE studie: Lange termijn uitkomst na edoxaban versus warfarine voor
INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN LONGEMBOLIE Hokusai post VTE studie: Lange termijn uitkomst na edoxaban versus warfarine voor
DRINGEND VEILIGHEIDSBERICHT
 Smiths Medical ASD / Smiths Medical Nederland BV DRINGEND VEILIGHEIDSBERICHT Smiths Medical ASD CADD -toedieningssets met Flow Stop 18 mei 2016 Aanvullende instructies Bestemd voor: Clinici die toezien
Smiths Medical ASD / Smiths Medical Nederland BV DRINGEND VEILIGHEIDSBERICHT Smiths Medical ASD CADD -toedieningssets met Flow Stop 18 mei 2016 Aanvullende instructies Bestemd voor: Clinici die toezien
Belangrijke Veiligheidsinformatie over prasugrel
 Belangrijke Veiligheidsinformatie over prasugrel Prasugrel behoort tot de farmacotherapeutische groep van de bloedplaatjesaggregatieremmers (heparine niet meegerekend), een groep waaronder ook clopidogrel
Belangrijke Veiligheidsinformatie over prasugrel Prasugrel behoort tot de farmacotherapeutische groep van de bloedplaatjesaggregatieremmers (heparine niet meegerekend), een groep waaronder ook clopidogrel
Dringende veiligheidsmededeling. BIRMINGHAM HIP RESURFACING (BHR) SYSTEM FSCA-referentie:
 Dringende veiligheidsmededeling 5 juni 2015 Betrokken product: BIRMINGHAM HIP RESURFACING (BHR) SYSTEM FSCA-referentie: R-2015-08 FSCA-actie: Aanpassingen m.b.t. BHR en uit de handel nemen van het hulpmiddel
Dringende veiligheidsmededeling 5 juni 2015 Betrokken product: BIRMINGHAM HIP RESURFACING (BHR) SYSTEM FSCA-referentie: R-2015-08 FSCA-actie: Aanpassingen m.b.t. BHR en uit de handel nemen van het hulpmiddel
Kimal plc: DRINGEND BERICHT INZAKE DE VEILIGHEID IN HET VELD Corrigerende actie in verband met de veiligheid in het veld ONMIDDELLIJKE ACTIE VEREIST
 Kimal plc: DRINGEND BERICHT INZAKE DE VEILIGHEID IN HET VELD Corrigerende actie in verband met de veiligheid in het veld ONMIDDELLIJKE ACTIE VEREIST Procedurepakketten met specifieke introducers (met en
Kimal plc: DRINGEND BERICHT INZAKE DE VEILIGHEID IN HET VELD Corrigerende actie in verband met de veiligheid in het veld ONMIDDELLIJKE ACTIE VEREIST Procedurepakketten met specifieke introducers (met en
DRINGENDE KENNISGEVING: RECALL MEDISCH HULPMIDDEL ETHICON PHYSIOMESH Flexible Composite Mesh (Alle productcodes)
 DRINGENDE KENNISGEVING: RECALL MEDISCH HULPMIDDEL Flexible Composite Mesh (Alle productcodes) Ziekenhuis T.a.v. de Directie Straat Post code Plaats Diegem, 31 mei 2016 Ref. FMJR\16-077 Geachte heer, mevrouw,
DRINGENDE KENNISGEVING: RECALL MEDISCH HULPMIDDEL Flexible Composite Mesh (Alle productcodes) Ziekenhuis T.a.v. de Directie Straat Post code Plaats Diegem, 31 mei 2016 Ref. FMJR\16-077 Geachte heer, mevrouw,
Lange-termijnervaringen met abatacept sc in de dagelijkse klinische praktijk
 PATIËNTENINFORMATIE EN TOESTEMMINGSFORMULIER Lange-termijnervaringen met abatacept sc in de dagelijkse klinische praktijk Geachte heer, mevrouw, U wordt uitgenodigd om deel te nemen aan een observationele
PATIËNTENINFORMATIE EN TOESTEMMINGSFORMULIER Lange-termijnervaringen met abatacept sc in de dagelijkse klinische praktijk Geachte heer, mevrouw, U wordt uitgenodigd om deel te nemen aan een observationele
Dringende vrijwillige veiligheidsmededeling
 Pagina 1 van 6 [Naam en adres van de geadresseerde] Dringende vrijwillige veiligheidsmededeling Lis Referentie: R517 Doel U ontvangt deze veiligheidsmededeling in verband met een vrijwillige terugroeping
Pagina 1 van 6 [Naam en adres van de geadresseerde] Dringende vrijwillige veiligheidsmededeling Lis Referentie: R517 Doel U ontvangt deze veiligheidsmededeling in verband met een vrijwillige terugroeping
Aanmeldformulier bariatrische chirurgie (deel 1)
 Aanmeldformulier bariatrische chirurgie (deel 1) Het ingevulde aanmeldformulier kunt u samen met de gevraagde relevante aanvullende informatie* en de ingevulde toestemmingsverklaring opsturen naar Vitalys
Aanmeldformulier bariatrische chirurgie (deel 1) Het ingevulde aanmeldformulier kunt u samen met de gevraagde relevante aanvullende informatie* en de ingevulde toestemmingsverklaring opsturen naar Vitalys
Bijlage I DRINGEND: RECALL. ARB Medical LLC Rebound HRD implantaat
 Bijlage I DRINGEND: RECALL ARB Medical LLC Rebound HRD implantaat Duo-Med N.V. stuurt u dit bericht ter kennisgeving van de terugroeping van de Rebound HRD implantaten van ARB Medical LLC. Hieronder vindt
Bijlage I DRINGEND: RECALL ARB Medical LLC Rebound HRD implantaat Duo-Med N.V. stuurt u dit bericht ter kennisgeving van de terugroeping van de Rebound HRD implantaten van ARB Medical LLC. Hieronder vindt
Transient neurological attacks. Schoppen tegen een heilig huisje?
 Transient neurological attacks Schoppen tegen een heilig huisje? Frank van Rooij 18 april 2019 Transient ischemic attack (TIA) Transient ischemic attack (TIA) Transient ischemic attack (TIA) TIA? TIA?
Transient neurological attacks Schoppen tegen een heilig huisje? Frank van Rooij 18 april 2019 Transient ischemic attack (TIA) Transient ischemic attack (TIA) Transient ischemic attack (TIA) TIA? TIA?
Proefpersoneninformatie
 Proefpersoneninformatie Titel van het onderzoek: Implementatie van de keuzehulp bestraling bij borstkanker en DCIS: een pre- en post-interventie studie. Geachte mevrouw, Uw behandelend arts heeft met u
Proefpersoneninformatie Titel van het onderzoek: Implementatie van de keuzehulp bestraling bij borstkanker en DCIS: een pre- en post-interventie studie. Geachte mevrouw, Uw behandelend arts heeft met u
Software-update controller
 7 januari 2016 BELANGRIJKE VEILIGHEIDSAANKONDIGING HeartWare HVAD controllersoftware, stroomadapter, en batterij Soort actie: HeartWare Software-update HVAD controller (modificatie apparaat), HeartWare
7 januari 2016 BELANGRIJKE VEILIGHEIDSAANKONDIGING HeartWare HVAD controllersoftware, stroomadapter, en batterij Soort actie: HeartWare Software-update HVAD controller (modificatie apparaat), HeartWare
DISTRICTS. Case Record Form Baseline meting arts VERTROUWELIJK. Versie 1.7. Contactinformatie: Wijnand Palmbergen, uitvoerend onderzoeker
 Studienummer: Pagina 1 van 10 DISTRICTS Case Record Form Baseline meting arts Versie 1.7 VERTROUWELIJK DISTRICTS studienummer: (wordt gegenereerd) Contactinformatie: Wijnand Palmbergen, uitvoerend onderzoeker
Studienummer: Pagina 1 van 10 DISTRICTS Case Record Form Baseline meting arts Versie 1.7 VERTROUWELIJK DISTRICTS studienummer: (wordt gegenereerd) Contactinformatie: Wijnand Palmbergen, uitvoerend onderzoeker
Informatiebrief en toestemmingsformulier registratie facioscapulohumerale spierdystrofie voor mensen van 16 jaar en ouder
 16+ jr Informatiebrief en toestemmingsformulier registratie facioscapulohumerale spierdystrofie voor mensen van 16 jaar en ouder Geachte mevrouw, meneer, Wij willen u vragen deel te nemen aan de landelijke
16+ jr Informatiebrief en toestemmingsformulier registratie facioscapulohumerale spierdystrofie voor mensen van 16 jaar en ouder Geachte mevrouw, meneer, Wij willen u vragen deel te nemen aan de landelijke
Chapter 9. Samenvatting
 Chapter 9 Samenvatting 130 Samenvatting 131 Samenvatting Complicaties van de onderste extremiteit, in het bijzonder voetulcera (voetwonden), veroorzaken een zeer grote ziektelast en een grote mate van
Chapter 9 Samenvatting 130 Samenvatting 131 Samenvatting Complicaties van de onderste extremiteit, in het bijzonder voetulcera (voetwonden), veroorzaken een zeer grote ziektelast en een grote mate van
URGENT FIELD SAFETY NOTICE. 1: Informatie over de VF inductie test door middel van een stimulatieburst van 30 Hz met RF-telemetrie
 HOSPITAL NAME Cardioloog ADDRESS 27 juli 2016 URGENT FIELD SAFETY NOTICE Betreft PLATINIUM-apparaten geproduceerd door Sorin Group Italia S.r.l. 1: Informatie over de VF inductie test door middel van een
HOSPITAL NAME Cardioloog ADDRESS 27 juli 2016 URGENT FIELD SAFETY NOTICE Betreft PLATINIUM-apparaten geproduceerd door Sorin Group Italia S.r.l. 1: Informatie over de VF inductie test door middel van een
BELANGRIJK VEILIGHEIDSBERICHT HeartSine Technologies samaritan PAD 500P (defibrillator voor openbare ruimte) Software-upgrade
 BELANGRIJK VEILIGHEIDSBERICHT HeartSine Technologies samaritan PAD 500P (defibrillator voor openbare ruimte) Software-upgrade Geachte eigenaren van de samaritan PAD 500P, Met deze brief willen we u op
BELANGRIJK VEILIGHEIDSBERICHT HeartSine Technologies samaritan PAD 500P (defibrillator voor openbare ruimte) Software-upgrade Geachte eigenaren van de samaritan PAD 500P, Met deze brief willen we u op
Toestemmingsformulier Nederlandse Hersenbank
 Print Form ToestemmingsformulierNederlandseHersenbank Voorvertegenwoordigersvanwilsonbekwamepersonen Nietinvullen Codicilcode: Codicilnummer: Naamdonor Man Vrouw Voornamen Geboortedatum Naamverblijfplaats
Print Form ToestemmingsformulierNederlandseHersenbank Voorvertegenwoordigersvanwilsonbekwamepersonen Nietinvullen Codicilcode: Codicilnummer: Naamdonor Man Vrouw Voornamen Geboortedatum Naamverblijfplaats
Informatiebrochure. Een onderzoek van Afdeling Humane Voeding, Wageningen Universiteit
 Informatiebrochure Een onderzoek van Afdeling Humane Voeding, Wageningen Universiteit Inhoudsopgave Inhoudsopgave... 2 Contactinformatie onderzoekers... 3 Plattegrond locatie... 4 Voorwoord... 5 Het onderzoek...
Informatiebrochure Een onderzoek van Afdeling Humane Voeding, Wageningen Universiteit Inhoudsopgave Inhoudsopgave... 2 Contactinformatie onderzoekers... 3 Plattegrond locatie... 4 Voorwoord... 5 Het onderzoek...
16 februari 2018 FSN Terugroepactie/bericht medisch apparaat HeartStart FRx, HeartStart Home en HeartStart OnSite AED's
 16 februari 2018 FSN86100186 Terugroepactie/bericht medisch apparaat HeartStart FRx, HeartStart Home en HeartStart OnSite AED's Geachte HeartStart AED-eigenaar, We nemen contact met u op, omdat uit onze
16 februari 2018 FSN86100186 Terugroepactie/bericht medisch apparaat HeartStart FRx, HeartStart Home en HeartStart OnSite AED's Geachte HeartStart AED-eigenaar, We nemen contact met u op, omdat uit onze
URGENTE PRODUCT RECALL MEDICAL DEVICE FIELD CORRECTION
 April 2016 URGENTE PRODUCT RECALL MEDICAL DEVICE FIELD CORRECTION Maquet CARDIOSAVE Hybrid Intra-Aortale Ballonpomp (IABP) Maquet CARDIOSAVE Rescue Intra-Aortale Ballonpomp (IABP) BETROKKEN PRODUCT ARTIKELNUMMER
April 2016 URGENTE PRODUCT RECALL MEDICAL DEVICE FIELD CORRECTION Maquet CARDIOSAVE Hybrid Intra-Aortale Ballonpomp (IABP) Maquet CARDIOSAVE Rescue Intra-Aortale Ballonpomp (IABP) BETROKKEN PRODUCT ARTIKELNUMMER
Indicatorensets Meetbaar Beter
 Indicatorensets Meetbaar Beter 2016 2015 Uitkomstindicatoren Uitkomstindicator PCI CB AVR TAVI CB Procedurele mortaliteit 30-daagse mortaliteit 120-daagse mortaliteit 1-jaars mortaliteit Lange-termijn
Indicatorensets Meetbaar Beter 2016 2015 Uitkomstindicatoren Uitkomstindicator PCI CB AVR TAVI CB Procedurele mortaliteit 30-daagse mortaliteit 120-daagse mortaliteit 1-jaars mortaliteit Lange-termijn
Onderstaande vragen zijn van toepassing op de periode maanden postoperatief
 9. Follow-up Aantal maanden? Datum: Setting: O klinisch O poliklinisch Beoordelaar: (naam) Algemeen Onderstaande vragen zijn van toepassing op de periode 12- postoperatief Is de patient opgenomen geweest
9. Follow-up Aantal maanden? Datum: Setting: O klinisch O poliklinisch Beoordelaar: (naam) Algemeen Onderstaande vragen zijn van toepassing op de periode 12- postoperatief Is de patient opgenomen geweest
Dringend veiligheidsbulletin
 Dringend veiligheidsbulletin Dit is een dringend veiligheidsbulletin betreffende het gebruik van de Welch Allyn Automatische externe defibrillator, AED 10 en MRL Jumpstart. Opmerking: Deze veiligheidskennisgeving
Dringend veiligheidsbulletin Dit is een dringend veiligheidsbulletin betreffende het gebruik van de Welch Allyn Automatische externe defibrillator, AED 10 en MRL Jumpstart. Opmerking: Deze veiligheidskennisgeving
PCI of complex coronary lesions, new stent technologies, and clinical outcomes Beijk, M.A.M.
 UvA-DARE (Digital Academic Repository) PCI of complex coronary lesions, new stent technologies, and clinical outcomes Beijk, M.A.M. Link to publication Citation for published version (APA): Beijk, M. A.
UvA-DARE (Digital Academic Repository) PCI of complex coronary lesions, new stent technologies, and clinical outcomes Beijk, M.A.M. Link to publication Citation for published version (APA): Beijk, M. A.
Summery. Effectiviteit van een interventieprogramma op arm-, schouder- en nekklachten bij beeldschermwerkers
 ummery amenvatting Effectiviteit van een interventieprogramma op arm-, schouder- en nekklachten bij beeldschermwerkers 207 Algemene introductie Werkgerelateerde arm-, schouder- en nekklachten zijn al eeuwen
ummery amenvatting Effectiviteit van een interventieprogramma op arm-, schouder- en nekklachten bij beeldschermwerkers 207 Algemene introductie Werkgerelateerde arm-, schouder- en nekklachten zijn al eeuwen
URGENTE VEILIGHEIDSWAARSCHUWING
 08.01.2015 Product: HeartWare -controller Soort actie: Terughalen van HeartWare Controller Productcodes: 1400, 1401XX Serienummers: CON000001 t/m CON005472 Geachte arts van HeartWare, In 2013 adviseerde
08.01.2015 Product: HeartWare -controller Soort actie: Terughalen van HeartWare Controller Productcodes: 1400, 1401XX Serienummers: CON000001 t/m CON005472 Geachte arts van HeartWare, In 2013 adviseerde
Informatiebrief voor de vertegenwoordiger
 Informatiebrief voor de vertegenwoordiger Preventive Antibiotics in Stroke Study (PASS) Informatiebrief over de studie naar preventief gebruik van antibiotica bij patiënten met een herseninfarct of hersenbloeding.
Informatiebrief voor de vertegenwoordiger Preventive Antibiotics in Stroke Study (PASS) Informatiebrief over de studie naar preventief gebruik van antibiotica bij patiënten met een herseninfarct of hersenbloeding.
Informatie voor de wettelijke vertegenwoordiger voor deelname aan het onderzoek
 PAIS2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden of hoger Geachte heer/ mevrouw, Uw partner/familielid is in ons ziekenhuis
PAIS2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden of hoger Geachte heer/ mevrouw, Uw partner/familielid is in ons ziekenhuis
Urgent bericht voor veiligheid in de praktijk
 TRUMPF Medizin Systeme GmbH + Co. KG P.O. box 24 44 07310 Saalfeld Germany TRUMPF Medizin Systeme GmbH + Co. KG Carl-Zeiss-Straße 7-9 07318 Saalfeld Telefoon +49 3671 586-0 Fax +49 3671 586-41 105 med@trumpfmedical.com
TRUMPF Medizin Systeme GmbH + Co. KG P.O. box 24 44 07310 Saalfeld Germany TRUMPF Medizin Systeme GmbH + Co. KG Carl-Zeiss-Straße 7-9 07318 Saalfeld Telefoon +49 3671 586-0 Fax +49 3671 586-41 105 med@trumpfmedical.com
Belangrijk veiligheidsbericht
 Belangrijk veiligheidsbericht Handelsnaam/model: Beneview T1-patiëntenmonitor FSCA-identificatie: CP17-JH0008 Type actie: Vervanging apparaat - April 2017 Let op: [naam ziekenhuis/distributeur] Geachte
Belangrijk veiligheidsbericht Handelsnaam/model: Beneview T1-patiëntenmonitor FSCA-identificatie: CP17-JH0008 Type actie: Vervanging apparaat - April 2017 Let op: [naam ziekenhuis/distributeur] Geachte
DRINGENDE VEILIGHEIDSMEDEDELING: Corrigerende veiligheidsactie/terugroeping medisch hulpmiddel
 Smith & Nephew Inc T +1 901-396-2121 1450 Brooks Road www.smith-nephew.com Memphis, TN 38116 [Adres ontvanger] 16 november 2016 DRINGENDE VEILIGHEIDSMEDEDELING: Corrigerende veiligheidsactie/terugroeping
Smith & Nephew Inc T +1 901-396-2121 1450 Brooks Road www.smith-nephew.com Memphis, TN 38116 [Adres ontvanger] 16 november 2016 DRINGENDE VEILIGHEIDSMEDEDELING: Corrigerende veiligheidsactie/terugroeping
University of Groningen. Restenosis in clinical practice Rahel, Braim Mohammed
 University of Groningen Restenosis in clinical practice Rahel, Braim Mohammed IMPORTANT NOTE: You are advised to consult the publisher's version (publisher's PDF) if you wish to cite from it. Please check
University of Groningen Restenosis in clinical practice Rahel, Braim Mohammed IMPORTANT NOTE: You are advised to consult the publisher's version (publisher's PDF) if you wish to cite from it. Please check
Informatie verstrekt onder het gezag van het FAGG. Rechtstreekse mededeling aan de Gezondheidszorgbeoefenaars
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Informatiebrief. Kies Gerust op maat. Versie 11 oktober 2016
 Informatiebrief Kies Gerust op maat Versie 11 oktober 2016 Inhoud 1. Wat is het doel van het onderzoek? 2. Hoe wordt de zorg vanuit de huisarts onderzocht? 3. Hoe wordt het onderzoek uitgevoerd? 4. Wat
Informatiebrief Kies Gerust op maat Versie 11 oktober 2016 Inhoud 1. Wat is het doel van het onderzoek? 2. Hoe wordt de zorg vanuit de huisarts onderzocht? 3. Hoe wordt het onderzoek uitgevoerd? 4. Wat
CEL 2010 0049. Indicatorenset DM
 CEL 2010 0049 Indicatorenset DM Deze indicatorenset Diabetes Melitus is vervaardigd in opdracht van ZN en wordt ingebracht bij Zichtbare Zorg als de door zorgverzekeraars gewenste indicatorenset. Zorgverzekeraars
CEL 2010 0049 Indicatorenset DM Deze indicatorenset Diabetes Melitus is vervaardigd in opdracht van ZN en wordt ingebracht bij Zichtbare Zorg als de door zorgverzekeraars gewenste indicatorenset. Zorgverzekeraars
Uitgevoerd onderzoek in de huisartsenpraktijk
 Uitgevoerd onderzoek in de huisartsenpraktijk ELLEN BANIERINK ANIOS INTERNE GENEESKUNDE 06-12-2016 Inhoud Aanleiding Vorming onderzoeksvoorstel Het onderzoek Praktisch gezien Planning Verloop Problemen
Uitgevoerd onderzoek in de huisartsenpraktijk ELLEN BANIERINK ANIOS INTERNE GENEESKUNDE 06-12-2016 Inhoud Aanleiding Vorming onderzoeksvoorstel Het onderzoek Praktisch gezien Planning Verloop Problemen
Patiëntinformatie TES
 Patiëntinformatie TES Datum: 6 november 2013 Onderwerp: Proefpersoneninformatie Geachte heer / mevrouw, U bent gevraagd om mee te doen aan een onderzoek naar de behoefte aan ondersteuning bij zorgen over
Patiëntinformatie TES Datum: 6 november 2013 Onderwerp: Proefpersoneninformatie Geachte heer / mevrouw, U bent gevraagd om mee te doen aan een onderzoek naar de behoefte aan ondersteuning bij zorgen over
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek Fysiotherapie na een totale knie of heup prothese, de PATIO studie Inleiding Geachte heer/mevrouw, Wij
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek Fysiotherapie na een totale knie of heup prothese, de PATIO studie Inleiding Geachte heer/mevrouw, Wij
Spoelen of darm verwijderen voor geperforeerde diverticulitis
 Spoelen of darm verwijderen voor geperforeerde diverticulitis Geachte mevrouw, mijnheer, Bij u is vastgesteld, dat er mogelijk sprake is van een perforatie (gaatje) van de dikke darm ten gevolge van divertikels
Spoelen of darm verwijderen voor geperforeerde diverticulitis Geachte mevrouw, mijnheer, Bij u is vastgesteld, dat er mogelijk sprake is van een perforatie (gaatje) van de dikke darm ten gevolge van divertikels
Onderzoek naar kwaliteit van antistolling bij ouderen met een lage dosering acenocoumarol, en de invloed van preciezer doseren
 Onderzoek naar kwaliteit van antistolling bij ouderen met een lage dosering acenocoumarol, en de invloed van preciezer doseren Officiële titel: More precise dosing of acenocoumarol in patients aged 80
Onderzoek naar kwaliteit van antistolling bij ouderen met een lage dosering acenocoumarol, en de invloed van preciezer doseren Officiële titel: More precise dosing of acenocoumarol in patients aged 80
Informatiebrief en toestemmingsformulier registratie facioscapulohumerale spierdystrofie voor kinderen tot 12 jaar
 tot 12 jr Informatiebrief en toestemmingsformulier registratie facioscapulohumerale spierdystrofie voor kinderen tot 12 jaar Geachte mevrouw, mijnheer, Wij willen u om toestemming vragen voor deelname
tot 12 jr Informatiebrief en toestemmingsformulier registratie facioscapulohumerale spierdystrofie voor kinderen tot 12 jaar Geachte mevrouw, mijnheer, Wij willen u om toestemming vragen voor deelname
DRINGENDE VEILIGHEIDSNOTA. Catalogusnr. Zie bijgevoegde lijst. Beschrijving van het probleem en gezondheidsrisico s
 DRINGENDE VEILIGHEIDSNOTA Datum: 15 januari 2018 Naam Product BD Phoenix Gram Negative Panels met colistine Product Catalogusnr. Zie bijgevoegde lijst Lotnr. Alle Vervaldatum (YYYYMMDD) Varia Ter attentie
DRINGENDE VEILIGHEIDSNOTA Datum: 15 januari 2018 Naam Product BD Phoenix Gram Negative Panels met colistine Product Catalogusnr. Zie bijgevoegde lijst Lotnr. Alle Vervaldatum (YYYYMMDD) Varia Ter attentie
Spoelen of darm verwijderen voor geperforeerde diverticulitis
 Geachte mevrouw, mijnheer, Bij u is vastgesteld, dat er mogelijk sprake is van een perforatie (gaatje) van de dikke darm ten gevolge van divertikels (uitstulpingen). Doordat ontlasting de buik in gekomen
Geachte mevrouw, mijnheer, Bij u is vastgesteld, dat er mogelijk sprake is van een perforatie (gaatje) van de dikke darm ten gevolge van divertikels (uitstulpingen). Doordat ontlasting de buik in gekomen
Prospectieve registratie studie voor de diagnose en behandeling van borstkanker tijdens zwangerschap (BOOG ) PATIENTENINFORMATIE
 Prospectieve registratie studie voor de diagnose en behandeling van borstkanker tijdens zwangerschap (BOOG 2003-04) PATIENTENINFORMATIE Geachte mevrouw, Uw behandelend arts heeft u geïnformeerd over bovengenoemd
Prospectieve registratie studie voor de diagnose en behandeling van borstkanker tijdens zwangerschap (BOOG 2003-04) PATIENTENINFORMATIE Geachte mevrouw, Uw behandelend arts heeft u geïnformeerd over bovengenoemd
Onderwerp: DRINGENDE TERUGROEPING VAN MEDISCH HULPMIDDEL - LOTGEBONDEN
 28 februari 2017 Aan: Risicomanagers Onderwerp: DRINGENDE TERUGROEPING VAN MEDISCH HULPMIDDEL - LOTGEBONDEN Betrokken product: Vanguard Open Box Femoral Components Zie Bijlage 2 Lijst met de betrokken
28 februari 2017 Aan: Risicomanagers Onderwerp: DRINGENDE TERUGROEPING VAN MEDISCH HULPMIDDEL - LOTGEBONDEN Betrokken product: Vanguard Open Box Femoral Components Zie Bijlage 2 Lijst met de betrokken
Brief 1: Bevestiging geen deelname zorgprogramma
 Brief 1: Bevestiging geen deelname zorgprogramma Datum Onderwerp: bevestiging afzien van ketenzorg voor Diabetes / COPD / Astma / CVRM Geachte heer/ mevrouw, Inleiding Voor patiënten met Diabetes / COPD
Brief 1: Bevestiging geen deelname zorgprogramma Datum Onderwerp: bevestiging afzien van ketenzorg voor Diabetes / COPD / Astma / CVRM Geachte heer/ mevrouw, Inleiding Voor patiënten met Diabetes / COPD
Informatie over dit wetenschappelijk onderzoek
 Proefpersoneninformatie / Toestemmingsverklaring voor langetermijn opslag van lichaamsmateriaal Een multi-nationaal onderzoek naar de veiligheid en effectiviteit, inclusief farmacokinetiek, van NNC-0129-0000-1003
Proefpersoneninformatie / Toestemmingsverklaring voor langetermijn opslag van lichaamsmateriaal Een multi-nationaal onderzoek naar de veiligheid en effectiviteit, inclusief farmacokinetiek, van NNC-0129-0000-1003
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Haalbaarheidsstudie naar het thuis meten van de bloeddruk bij patiënten met een hoge bloeddruk Geachte heer/mevrouw, Wij vragen
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Haalbaarheidsstudie naar het thuis meten van de bloeddruk bij patiënten met een hoge bloeddruk Geachte heer/mevrouw, Wij vragen
PATIËNTEN INFORMATIE
 LIMERIC-studie PATIËNTEN INFORMATIE Gelimiteerde wigresectie van poliepen in de darm (LIMERIC) Geachte heer/mevrouw, Uw arts heeft u gevraagd mee te doen aan een medisch-wetenschappelijk onderzoek (zie
LIMERIC-studie PATIËNTEN INFORMATIE Gelimiteerde wigresectie van poliepen in de darm (LIMERIC) Geachte heer/mevrouw, Uw arts heeft u gevraagd mee te doen aan een medisch-wetenschappelijk onderzoek (zie
Spoelen of darm verwijderen voor geperforeerde diverticulitis
 Spoelen of darm verwijderen voor geperforeerde diverticulitis Geachte mevrouw, mijnheer, Bij u is vastgesteld, dat er mogelijk sprake is van een perforatie (gaatje) van de dikke darm ten gevolge van divertikels
Spoelen of darm verwijderen voor geperforeerde diverticulitis Geachte mevrouw, mijnheer, Bij u is vastgesteld, dat er mogelijk sprake is van een perforatie (gaatje) van de dikke darm ten gevolge van divertikels
