FIRMAGON (degarelix) Productinformatie voor gezondheidszorgbeoefenaars
|
|
|
- Erik de Smedt
- 8 jaren geleden
- Aantal bezoeken:
Transcriptie
1 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FIRMAGON. Het verplicht plan voor risicobeperking in België, waarvan deze informatie deel uitmaakt, is een maatregel genomen om een veilig en doeltreffend gebruik van FIRMAGON te waarborgen. (RMA gewijzigde versie 05/2015) FIRMAGON (degarelix) Productinformatie voor gezondheidszorgbeoefenaars Dit materiaal bevat niet alle informatie. Voor de volledige informatie: Lees aandachtig de SKP (in bijlage) vooraleer FIRMAGON voor te schrijven (en/of te gebruiken en/of af te leveren). De volledige en geactualiseerde tekst van deze SKP is beschikbaar op de website rubriek BIJSLUITER en SKP van een geneesmiddel. Ferring nv - Capucienenlaan 93C - B-9300 Aalst Tel.: +32(0)53/ Fax: +32(0)53/
2 Doel van dit materiaal (RMA of Risk Minimisation Activities) Deze informatie maakt deel uit van het Belgische risicobeheerplan, dat informatiemateriaal beschikbaar stelt aan gezondheidszorgbeoefenaars. Deze bijkomende risicobeperkende activiteiten hebben als doel een veilig en doeltreffend gebruik van FIRMAGON te waarborgen en moeten volgende belangrijke onderdelen bevatten: Dosering Toedieningsinstructies Informatie over de vorming van een geldepot met gecontroleerde afgifte en mogelijke reacties op de plaats van injectie Informatie over geïdentificeerde en mogelijke risico s Inhoudsopgave Inleiding 3 Hoe werkt FIRMAGON? 3 Wat is het verschil tussen FIRMAGON en GnRH-agonisten? 4 Hoe effectief is FIRMAGON bij prostaatkanker? 4 Dosering 5 Wijze van toediening 5 Inhoud van de verpakking 6 Reconstitutiemethode voor de FIRMAGON aanvangsdosis (2 x 120 mg) 7 Reconstitutiemethode voor de FIRMAGON onderhoudsdosis (80 mg) 9 Doseringskaart 11 Geen reden voor antiandrogeentherapie 11 Bijwerkingen 11 Advies aan patiënten over mogelijke bijwerkingen 12 Voorzorgen bij gebruik 14 Bewaarcondities 14 2
3 FIRMAGON Inleiding FIRMAGON (degarelix) is een gonadotrophin releasing hormone (GnRH)-antagonist voor de behandeling van volwassen mannelijke patiënten met hormoonafhankelijke prostaatkanker in een vergevorderd stadium. Dit document voorziet u als beroepsbeoefenaar van praktische informatie over FIRMAGON waaronder de reconstitutie en toediening ervan, kenmerkende fysiologische eigenschappen, alsmede de belangrijkste veiligheidsissues en tips om uw patiënt bewust te maken van de bijwerkingen en de risico's van de behandeling. Hoe werkt FIRMAGON? Degarelix is een selectieve gonadotrophin releasing hormone (GnRH)-antagonist die zich competitief en reversibel aan de GnRH-receptoren in de hypofyse bindt. Dit veroorzaakt een snelle afname van de gonadotrofines, het luteïniserend hormoon (LH) en het follikelstimulerend hormoon (FSH). Hierdoor neemt de testosteron (T)-afscheiding door de Leydigcellen van de teelballen af tot het niveau van medische castratie. FIRMAGON vormt bij subcutane injectie een gelachtig depot in de lichaamsweefsels van waaruit de werkzame stof degarelix langzaam en gestaag in de circulatie vrijkomt, maar wel met voldoende snelheid om de testosteronafscheiding snel te onderdrukken tot het niveau van medische castratie. FIRMAGON bevat deeltjes (aggregatiekernen) die ervoor zorgen dat het gelachtige depot wordt gevormd zodra contact wordt gemaakt met het subcutane weefsel. Het depot verdwijnt na verloop van tijd uit de injectieplaats. 3
4 Wat is het verschil tussen FIRMAGON en GnRH-agonisten? FIRMAGON is een GnRH-antagonist en werkt dus op een andere manier dan de GnRH-agonisten die momenteel voor prostaatkanker worden ingezet. In tegenstelling tot GnRH-agonisten veroorzaken GnRH-antagonisten (zoals FIRMAGON ) na aanvang van de behandeling geen LH-piek met achtereenvolgende testosteronpiek/stimulatie van de tumor en mogelijke symptomatische opvlamming. Hoe effectief is FIRMAGON bij prostaatkanker? Het is aangetoond dat FIRMAGON een snellere onderdrukking teweegbrengt van de testosteronafscheiding en PSA-spiegels in vergelijking met leuproreline. In een gerandomiseerd klinisch onderzoek (n = 620) bereikten 52% en 96% van de met FIRMAGON behandelde patiënten op respectievelijk dag 1 en dag 3 het niveau van medische castratie (testosteron 0,5 ng/ml). PSA-spiegels waren op dag 14 en 28 beduidend lager bij patiënten in de FIRMAGON -groep vergeleken met patiënten in de leuprorelinegroep. De onderdrukking van de testosteronafscheiding bewerkstelligd door FIRMAGON hield gedurende de hele studieperiode aan (1 jaar). 4
5 Dosering FIRMAGON is beschikbaar als een gevriesdroogd poeder in een injectieflacon en een oplosmiddel (water voor injecties) in een voorgevulde spuit. Voordat het diep subcutaan wordt geïnjecteerd, moet het poeder worden opgelost. De aanbevolen dosering van FIRMAGON is één injectie per maand. De aanvangsdosis, eenmalig aan het begin van de therapie toe te dienen, bedraagt 240 mg. Wegens het te grote injectievolume bestaat de aanvangsdosis uit twee injecties van 120 mg in 3 ml oplosmiddel die als een diepe subcutane injectie moeten worden gegeven. De twee injecties moeten onmiddellijk na elkaar, zonder interval, worden toegediend. De onderhoudsdosis, die iedere maand moet worden toegediend, bestaat uit een diepe subcutane injectie van 80 mg in 4 ml oplosmiddel. Injectieschema Aanvangsdosis Onderhoudsdosis Wijze van toediening FIRMAGON wordt als een diepe subcutane injectie gegeven in de buikstreek. Hierbij wordt gebruikgemaakt van een dunne injectienaald (25G 0,5 x 25 mm). Zoals gebruikelijk bij injecteren, wordt met een antiseptisch doekje de huid schoongemaakt. De plaats van injectie moet variëren. De injectie moet worden gegeven op een plaats waar de patiënt geen druk ervaart, dus niet bij de riem of tailleband of vlak bij de ribben. 5
6 Inhoud van de verpakking Aanvangsdosis 1 verpakking FiRMAgOn 120 mg poeder en oplosmiddel voor injectie bevat: 2 injectieflacons met 120 mg poeder voor oplossing voor injectie 2 voorgevulde spuiten met 3 ml oplosmiddel (lijnmarkering bij 3 ml) 2 zuigers 2 flaconadapters 2 injectienaalden (25G 0,5 x 25 mm) Onderhoudsdosis 1 verpakking FiRMAgOn 80 mg poeder en oplosmiddel voor injectie bevat: 1 injectieflacon met 80 mg poeder voor oplossing voor injectie 1 voorgevulde spuit met 4,2 ml oplosmiddel (lijnmarkering bij 4 ml) 1 zuiger 1 flaconadapter 1 injectienaald (25G 0,5 x 25 mm) 6
7 Reconstitutiemethode voor de FIRMAGON aanvangsdosis (2 x 120 mg) De verpakking bevat twee injectieflacons met poeder en twee voorgevulde spuiten met oplosmiddel die voorbereid moeten worden voor diep subcutane injectie. Daarom moeten onderstaande instructies tweemaal herhaald worden. De reconstitutie van de oplossing duurt enkele minuten. De oplossing moet onmiddellijk na reconstitutie worden toegediend. OPMERKing: DE injectieflacons MOgEn niet worden geschud. 1. Haal de flaconadapter uit de verpakking. Maak de adapter vast aan de injectieflacon met poeder door de adapter naar beneden te drukken totdat de punt door de rubberen dop van de injectieflacon wordt geduwd en de adapter vastklikt. 2. Maak de zuiger vast aan de voorgevulde spuit. 3. Haal het dopje van de voorgevulde spuit. Maak de spuit vast aan de poederflacon door deze op de adapter te draaien. Breng al het oplosmiddel over in de poederflacon. 7
8 4. Draai de injectieflacon voorzichtig rond terwijl de spuit nog steeds aan de adapter zit, totdat de vloeistof helder en zonder onopgelost poeder of deeltjes is. Indien het poeder zich aan de flaconwand hecht boven het vloeistofniveau, moet de injectieflacon iets schuin worden gehouden. niet schudden, om schuimvorming te voorkomen. Een randje met kleine luchtbelletjes rond het vloeistofoppervlak is acceptabel. De oplosprocedure duurt doorgaans maar een paar minuten, maar kan in sommige gevallen 15 minuten duren. 5. Draai de injectieflacon ondersteboven en trek vloeistof op tot aan de markering op de spuit. Verzeker u er altijd van het exacte volume op te trekken en corrigeer voor eventuele luchtbellen. 6. Haal de spuit van de flaconadapter en zet de injectienaald voor diepe subcutane injectie op de spuit. 7. Dien een diepe subcutane injectie toe. Pak hiervoor een huidplooi van de buik en trek het subcutane weefsel omhoog. Breng de injectienaald diep in onder een hoek van minimaal 45 graden. Injecteer langzaam 3 ml FiRMAgOn 120 mg direct na reconstitutie.* 8. De injecties mogen niet worden toegediend op plaatsen waar de patiënt aan druk wordt blootgesteld, zoals dicht bij de riem of tailleband of vlak bij de ribben. Zet de injectie niet direct in een ader. Trek de zuiger voorzichtig terug om te controleren of er bloed geaspireerd wordt. Indien er bloed in de spuit terechtkomt, kan het geneesmiddel niet langer gebruikt worden. Breek de procedure af en verwijder de spuit en de injectienaald. (Los een nieuwe dosis op voor de patiënt.) 9. Herhaal de oplosprocedure voor de tweede dosis. Kies een andere injectieplaats en injecteer 3 ml. 8 * Aangetoond fysisch-chemisch stabiel gedurende twee uur bij 25 C. Vanuit microbiologisch oogpunt dient het product direct te worden gebruikt, tenzij het risico op microbiële infecties door de reconstitutiemethode wordt uitgesloten. Indien het product niet direct gebruikt wordt zijn de bewaartijd en -omstandigheden de verantwoordelijkheid van de gebruiker.
9 Reconstitutiemethode voor de FIRMAGON onderhoudsdosis (80 mg) De verpakking bevat één injectieflacon met poeder en één voorgevulde spuit met oplosmiddel die voorbereid moet worden voor diep subcutane injectie. De reconstitutie van de oplossing duurt enkele minuten. De oplossing moet onmiddellijk na reconstitutie worden toegediend. OPMERKing: DE injectieflacons MOgEn niet worden geschud. 1. Haal de flaconadapter uit de verpakking. Maak de adapter vast aan de injectieflacon met poeder door de adapter naar beneden te drukken totdat de punt door de rubberen dop van de injectieflacon wordt geduwd en de adapter vastklikt. 2. Maak de zuiger vast aan de voorgevulde spuit. 3. Haal het dopje van de voorgevulde spuit. Maak de spuit vast aan de poederflacon door deze op de adapter te draaien. Breng al het oplosmiddel over in de poederflacon. 9
10 4. Draai de injectieflacon voorzichtig rond terwijl de spuit nog steeds aan de adapter zit, totdat de vloeistof helder en zonder onopgelost poeder of deeltjes is. Indien het poeder zich aan de flaconwand hecht boven het vloeistofniveau, moet de injectieflacon iets schuin worden gehouden. niet schudden, om schuimvorming te voorkomen. Een randje met kleine luchtbelletjes rond het vloeistofoppervlak is acceptabel. De oplosprocedure duurt doorgaans maar een paar minuten, maar kan in sommige gevallen 15 minuten duren. 5. Draai de injectieflacon ondersteboven en trek vloeistof op tot aan de markering op de spuit. Verzeker u er altijd van het exacte volume op te trekken en corrigeer voor eventuele luchtbellen. 6. Haal de spuit van de flaconadapter en zet de injectienaald voor diepe subcutane injectie op de spuit. 7. Dien een diepe subcutane injectie toe. Pak hiervoor een huidplooi van de buik en trek het subcutane weefsel omhoog. Breng de injectienaald diep in onder een hoek van minimaal 45 graden. Injecteer langzaam 4 ml FiRMAgOn 80 mg direct na reconstitutie.* 8. De injecties mogen niet worden toegediend op plaatsen waar de patiënt aan druk wordt blootgesteld, zoals dicht bij de riem of tailleband of vlak bij de ribben. Zet de injectie niet direct in een ader. Trek de zuiger voorzichtig terug om te controleren of er bloed geaspireerd wordt. Indien er bloed in de spuit terechtkomt, kan het geneesmiddel niet langer gebruikt worden. Breek de procedure af en verwijder de spuit en de injectienaald. (Los een nieuwe dosis op voor de patiënt.) 10 * Aangetoond fysisch-chemisch stabiel gedurende twee uur bij 25 C. Vanuit microbiologisch oogpunt dient het product direct te worden gebruikt, tenzij het risico op microbiële infecties door de reconstitutiemethode wordt uitgesloten. Indien het product niet direct gebruikt wordt zijn de bewaartijd en -omstandigheden de verantwoordelijkheid van de gebruiker.
11 Doseringskaart Benodigde hoeveelheid oplosmiddel Injectievolume Aanvangsdosis (120 mg x 2) 3,0 ml x 2 3,0 ml x 2 Onderhoudsdosis (80 mg) 4,2 ml 4,0 ml Geen reden voor antiandrogeentherapie Aangezien FIRMAGON geen initiële testosteronpiek veroorzaakt, is er geen reden om een antiandrogeentherapie te starten aan het begin van de behandeling. Bijwerkingen De meest voorkomende bijwerkingen tijdens de behandeling met FIRMAGON zijn te wijten aan de verwachte fysiologische effecten van de onderdrukking van de testosteronafscheiding, waaronder opvliegers (25%) en gewichtstoename (7%). Inherent aan een subcutane injectie kan FIRMAGON bijwerkingen op de plaats van injectie veroorzaken die voornamelijk bestaan uit pijn (28%), erytheem (17%) en zwelling (6%). Deze bijwerkingen treden met name op bij de aanvangsdosis, terwijl bij de onderhoudsdosis van 80 mg de incidentie van deze bijwerkingen per 100 injecties uitkwam op 3% voor pijn en < 1% voor erytheem, zwelling, plaatselijke verharding (4%) en knobbels (3%). De gemelde bijwerkingen waren grotendeels tijdelijk en van lichte tot matige intensiteit, en leidden zeer zelden tot het beëindigen van de behandeling (< 1%). Lichte overgevoeligheidsreacties zoals urticaria en uitslag zijn gemeld door minder dan 1% van de patiënten die behandeld zijn met FIRMAGON. In klinische studies zijn geen meldingen geweest van anafylactoïde reacties. Veranderingen in de ecg-metingen die tijdens één behandeljaar werden geconstateerd, waren vergelijkbaar voor degarelix en een GnRH-agonist (leuproreline) die als comparator werd gebruikt. Drie (< 1%) van de 409 patiënten in de degarelixgroep en vier (2%) van de 201 patiënten in de leuprorelinegroep (7,5 mg) hadden een QTcF 500 ms. Van het begin tot het eind van het onderzoek bedroeg de gemiddelde verandering 12,0 ms voor degarelix en 16,7 ms voor leuproreline. 11
12 Androgeendeprivatietherapie kan het cardiovasculair systeem negatief beïnvloeden door een verlenging van het QT-interval. Ongeveer 20% van de patiënten die gedurende één jaar behandeld werden met FIRMAGON of leuproreline, vertoonden een verlenging van het QT/QTc-interval van meer dan 450 ms en 1% in de FIRMAGON -groep vertoonden een QT/QTc-intervalverlenging van meer dan 500 ms versus 2% in de leuprorelinegroep. Bij ongeveer 10% van de patiënten die gedurende één jaar werden behandeld met FIRMAGON, is een ontwikkeling van antilichamen tegen degarelix gezien. Er zijn echter geen aanwijzingen dat de effectiviteit of de veiligheid in het gedrang komt door de aanwezigheid van deze antilichamen tegen degarelix. Melden van bijwerkingen De gezondheidszorgbeoefenaars worden verzocht bijwerkingen van FIRMAGON te melden aan het Belgisch Centrum voor Geneesmiddelenbewaking voor geneesmiddelen voor humaan gebruik (BCGH) van het FAGG. Het melden kan online gebeuren via of via de papieren gele fiche beschikbaar via het Gecommentarieerd Geneesmiddelenrepertorium en driemaal per jaar via de Folia Pharmacotherapeutica. De gele fiche kan worden verzonden naar het BCGH per post naar het adres FAGG BCGH Eurostation II Victor Hortaplein 40/ Brussel, per fax op het nummer 02/ , of per mail naar Advies aan patiënten over mogelijke bijwerkingen Het is van belang uw patiënten goed te informeren over het feit dat regelmatig hormonale bijwerkingen kunnen optreden. Neem er de tijd voor deze bijwerkingen te bespreken zodat het hen helpt eventuele symptomen beter te begrijpen en de behandeling beter te accepteren. Moedig uw patiënten aan bijwerkingen te melden en stel met hen een plan samen om de impact van bijwerkingen zo klein mogelijk te laten zijn. Opvliegers komen regelmatig voor als bijwerking van androgeendeprivatietherapie (ADT). Van de patiënten die ADT ondergaan, kunnen 80% hiervan last krijgen. Opvliegers kunnen veel ongemak veroorzaken, zeker wanneer het gepaard gaat met transpireren, slecht slapen en een verminderde kwaliteit van leven. U kunt uw patiënten wijzen op beschikbare therapeutische mogelijkheden om hen te helpen opvliegers tijdens ADT beter te controleren. Ook enkele simpele levensstijlaanpassingen zoals minder roken en alcoholische en caffeïnebevattende dranken vermijden, kunnen helpen de frequentie van opvliegers te verminderen. seksuele functiestoornissen zoals een verminderd libido is een vaak voorkomende bijwerking gerelateerd aan ADT en is een belangrijk aspect van aandacht bij deze behandeling. 12
13 Ook hier kunnen therapeutische mogelijkheden met de patiënt die daarom vraagt, besproken worden. Een alternatieve benadering kan bestaan uit adviezen over de levensstijl. Zo kunnen handhaving van een gezond gewicht en fysiek actief blijven patiënten met seksuele functiestoornissen helpen. In de medische literatuur wordt melding gemaakt van een verminderde botdichtheid bij mannen die een orchidectomie ondergaan hebben of die behandeld zijn met een GnRH-agonist. Lange periodes van testosterononderdrukking bij mannen zullen naar verwachting gevolgen hebben voor de botdichtheid. De botdichtheid is niet gemeten tijdens de behandeling met degarelix. U kunt uw patiënten adviseren over calcium- en vitamine D-supplementen. Het is ook bekend dat uithoudingsoefeningen botverlies verminderen. Osteoporosebehandelingen kunnen heilzaam zijn. Veel patiënten die ADT ondergaan, komen bij in gewicht. Naast meer lichaamsvet zijn ook metabole veranderingen waargenomen zoals een verhoging van de totale cholesterol, LDL-cholesterolconcentraties, plasmatriglyceriden, insulinespiegels en bloeddruk. Begeleiding van de patiënten bij stoppen met roken, goede voeding en/of een dieet en fysieke activiteit kan hen helpen deze lichamelijke veranderingen te minimaliseren en cardiovasculaire aandoeningen te voorkomen. De emotionele impact gerelateerd aan prostaatkanker en ADT is substantieel. Het is normaal dat de patiënt zich depressief voelt en zich zorgen maakt. Sommige patiënten kroppen hun gevoelens op en het kan daarom van belang zijn toch vragen te stellen over hun gevoelens zonder daarin te indringend te zijn. In de medische literatuur wordt melding gemaakt van cardiovasculaire aandoeningen zoals een hersen- of hartinfarct, bij patienten die androgeendeprivatietherapie ondergaan. Daarom moeten alle cardiovasculaire risicofactoren in acht worden genomen, ongeacht het product. Begeleidingsprogramma s voor patiënten met prostaatkanker moedigen hen aan hun leven en ziekte in eigen handen te nemen met behulp van regelmatige lichaamsbeweging en speciaal voor hen ontworpen oefeningen, een goede voedingshygiëne en een proactieve benadering van de bijwerkingen van de behandeling. 13
14 Voorzorgen bij gebruik Bij sommige patiëntgroepen zijn voorzorgen of waarschuwingen van toepassing om de volgende mogelijke risico s te voorkomen of te verminderen: Overgevoeligheid FIRMAGON is niet onderzocht bij patiënten met een voorgeschiedenis van ernstige, onbehandelde astma, anafylactische reacties en ernstige netelroos of angio-oedeem. Daarom moet voorzichtigheid worden betracht bij deze patiënten. Verhoging van leverenzymen Er is een lichte, tijdelijke toename van ALT en AST geconstateerd tijdens klinische studies. Deze vielen niet samen met een toename van bilirubine of klinische symptomen. Het monitoren van de leverfunctie bij patiënten met een vermoedelijke of bekende leveraandoening strekt daarom tot aanbeveling tijdens de behandeling met FIRMAGON. Verlengd QT-interval Er is geen onderzoek gedaan naar FIRMAGON bij patiënten met een gecorrigeerd QTinterval > 450 ms, bij patiënten met een voorgeschiedenis van of risico op torsades de pointes en bij patiënten die gelijktijdig geneesmiddelen gebruiken die het QT-interval kunnen verlengen (zoals klasse IA- of klasse III-antiaritmica). Daarom moet u bij dergelijke patiënten de risico-batenverhouding zorgvuldig afwegen. Bewaarcondities Er zijn geen speciale bewaarcondities voor FIRMAGON. Na reconstitutie van de oplossing is deze fysisch-chemisch stabiel gedurende twee uur bij 25ºC. Het is aan te bevelen FIRMAGON onmiddellijk na reconstitutie te gebruiken. 14
15 Ferring nv - Capucienenlaan 93C - B-9300 Aalst Tel.: +32(0)53/ Fax: +32(0)53/
Risico minimalisatie materiaal betreffende degarelix voor voorschrijvers. Ferring BV., Polarisavenue 130, 2132 JX Hoofddorp
 Risico minimalisatie materiaal betreffende degarelix voor voorschrijvers Ferring BV., Polarisavenue 130, 2132 JX Hoofddorp Inhoudsopgave: Inleiding... 3 Samenvatting... 3 Hoe werkt degarelix?... 3 Dosering...
Risico minimalisatie materiaal betreffende degarelix voor voorschrijvers Ferring BV., Polarisavenue 130, 2132 JX Hoofddorp Inhoudsopgave: Inleiding... 3 Samenvatting... 3 Hoe werkt degarelix?... 3 Dosering...
Inleiding. Inhoudsopgave
 Productinformatie Inhoudsopgave Inleiding 3 Hoe werkt Firmagon? 4 Wat is het verschil tussen Firmagon en LHRH-Agonisten? 4 Hoe effectief is Firmagon bij prostaatkanker? 5 Dosering 5 Toepassing 6 Inhoud
Productinformatie Inhoudsopgave Inleiding 3 Hoe werkt Firmagon? 4 Wat is het verschil tussen Firmagon en LHRH-Agonisten? 4 Hoe effectief is Firmagon bij prostaatkanker? 5 Dosering 5 Toepassing 6 Inhoud
VALDOXAN. (agomelatine) Informatie voor beroepsbeoefenaren in de gezondheidszorg: Aanbevelingen met betrekking tot:
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Valdoxan 25 mg. Het verplicht plan voor risicobeperking in België, waarvan deze
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Valdoxan 25 mg. Het verplicht plan voor risicobeperking in België, waarvan deze
RECONSTITUTIE, DOSERING EN TOEDIENING
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VELCADE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VELCADE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
VISTABEL (botulinum toxine type A) Educatieve brochure voor artsen. 50 Allerganeenheden Poeder voor oplossing voor injectie
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VISTABEL. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VISTABEL. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
VALDOXAN (agomelatine) Informatie voor beroepsbeoefenaren in de gezondheidszorg. Aanbevelingen met betrekking tot:
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Valdoxan 25 mg. Het verplicht plan voor risicobeperking in België, waarvan deze
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Valdoxan 25 mg. Het verplicht plan voor risicobeperking in België, waarvan deze
Belangrijke informatie voor zorgverleners over de nieuwe formulering van FLOLAN
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
NEBIDO (TESTOSTERONUNDECANOAAT) 1000 mg/4 ml oplossing voor injectie GIDS VOOR DE VOORSCHRIJVER
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nebido. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nebido. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
CINRYZE (C1-REMMER [HUMAAN])
![CINRYZE (C1-REMMER [HUMAAN]) CINRYZE (C1-REMMER [HUMAAN])](/thumbs/66/54698885.jpg) De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CINRYZE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CINRYZE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Informatiefiche voor artsen voor een veilig en doeltreffend gebruik van het geneesmiddel
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Mysimba 8 mg/90 mg tabletten met verlengde afgifte. (naltrexonhydrochloride en bupropionhydrochloride)
 1 De Europese gezondheidsautoriteiten hebben bepaaide voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Mysimba 8 mg/90 mg tabletten met verlengde afgifte. Het verplichte plan voor
1 De Europese gezondheidsautoriteiten hebben bepaaide voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Mysimba 8 mg/90 mg tabletten met verlengde afgifte. Het verplichte plan voor
Postdatum. Geachte Dokter,
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Quetiapine Krka 50 mg / 200 mg / 300 mg/400 mg tabletten met verlengde afgifte.
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Quetiapine Krka 50 mg / 200 mg / 300 mg/400 mg tabletten met verlengde afgifte.
BROCHURE VOOR RECONSTITUTIE, DOSERING EN TOEDIENING
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Bortezomib Sandoz 3,5 mg poeder voor oplossing voor injectie. Het verplicht
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Bortezomib Sandoz 3,5 mg poeder voor oplossing voor injectie. Het verplicht
Educatief materiaal. EFIENT (Prasugrel) Dit geneesmiddel is onderworpen aan aanvullende monitoring.
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel EFIENT. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel EFIENT. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
FLOLAN INFORMATIEGIDS VOOR PATIENTEN - FLOLAN
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Servier Benelux S.A. PROTELOS. (strontiumranelaat) GIDS EN CHECKLIST VOOR DE ARTS
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Protelos 2 g. Het verplicht plan voor risicobeperking in België, waarvan deze
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Protelos 2 g. Het verplicht plan voor risicobeperking in België, waarvan deze
VOORLICHTINGSBROCHURE VOOR DE GEZONDHEIDSZORGBEOEFENAAR
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ACCUSOL 35. Het verplicht plan voor risicobeperking in België, waarvan deze
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ACCUSOL 35. Het verplicht plan voor risicobeperking in België, waarvan deze
Selectie en training van patiënten voor thuistoediening van Nplate
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Dit verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Dit verplicht plan voor risicobeperking in België, waarvan deze informatie
Checklist voor voorschrijvers
 De Nederlandse en Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Jext. Het verplicht plan voor risicobeperking in Nederland en
De Nederlandse en Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Jext. Het verplicht plan voor risicobeperking in Nederland en
RECONSTITUTIE, DOSERING EN TOEDIENING
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VELCADE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VELCADE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Belangrijke informatie voor beroepsbeoefenaren
 De gezondheidsautoriteiten van de Europese Unie hebben het in de handel brengen van het geneesmiddel Kadcyla verbonden aan bepaalde voorwaarden. Het verplichte farmacovigilantieplan ter minimalisatie van
De gezondheidsautoriteiten van de Europese Unie hebben het in de handel brengen van het geneesmiddel Kadcyla verbonden aan bepaalde voorwaarden. Het verplichte farmacovigilantieplan ter minimalisatie van
Vectibix (panitumumab) Educatief materiaal voor de arts
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Vectibix. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Vectibix. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Gelieve de patiëntenwaarschuwingskaart van Entyvio in te vullen en te overhandigen aan elke patiënt.
 Deze informatie maakt deel uit van het Belgische en Luxemburgse risicobeheerplan, dat informatiemateriaal beschikbaar stelt aan gezondheidszorgbeoefenaars (en patiënten). Deze bijkomende risicobeperkende
Deze informatie maakt deel uit van het Belgische en Luxemburgse risicobeheerplan, dat informatiemateriaal beschikbaar stelt aan gezondheidszorgbeoefenaars (en patiënten). Deze bijkomende risicobeperkende
Kyleena (19,5 mg levonorgestrel) afleveringsysteem voor intra-uterien gebruik
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Kyleena. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Kyleena. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Bijsluiter: informatie voor de gebruiker. FIRMAGON 120 mg poeder en oplosmiddel voor oplossing voor injectie Degarelix
 Bijsluiter: informatie voor de gebruiker FIRMAGON 120 mg poeder en oplosmiddel voor oplossing voor injectie Degarelix Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat
Bijsluiter: informatie voor de gebruiker FIRMAGON 120 mg poeder en oplosmiddel voor oplossing voor injectie Degarelix Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat
GIDS VOOR DE VOORSCHRIJVER
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel Cerdelga. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel Cerdelga. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Handleiding voor zorgverleners
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel Toujeo. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel Toujeo. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Risico minimalisatie materiaal betreffende testosteronundecanoaat voor beroepsbeoefenaren in de gezondheidszorg
 Risico minimalisatie materiaal betreffende testosteronundecanoaat voor beroepsbeoefenaren in de gezondheidszorg De risico minimalisatie materialen voor testosteronundecanoaat zijn beoordeeld door het College
Risico minimalisatie materiaal betreffende testosteronundecanoaat voor beroepsbeoefenaren in de gezondheidszorg De risico minimalisatie materialen voor testosteronundecanoaat zijn beoordeeld door het College
CAPRELSA (vandetanib)
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CAPRELSA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CAPRELSA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
ZypAdhera. Informatie bestemd voor professionelen uit de gezondheidszorg en verpleegkundigen Risicobeleidsplan
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ZypAdhera. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ZypAdhera. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
NEBIDO (TESTOSTERONUNDECANOAAT) 1000 mg/4 ml oplossing voor injectie
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nebido. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nebido. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
INFORMATIE VOOR DE PATIËNT
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Azzalure. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Azzalure. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
LEIDRAAD VOOR BEROEPSBEOEFENAREN IN DE GEZONDHEIDSZORG
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel KANUMA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel KANUMA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
BOTOX (botulinum toxine type A) Educatieve brochure voor artsen. 100 Allerganeenheden Poeder voor oplossing voor injectie
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel BOTOX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel BOTOX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
In geval van vermoedelijke onjuiste toediening van Depo-Eligard moeten de testosteronespiegels bepaald worden.
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Het gebruik van APIDRA in injectieflacon
 EEN GIDS VOOR ALS U BEGINT MET APIDRA (insuline glulisine) 1x 10ML INJECTIEFLACON (100 Eenheden/ml) De Apidra 100 eenheden/ml oplossing voor injectie (in injectieflacon) wordt in een injectieflacon geleverd
EEN GIDS VOOR ALS U BEGINT MET APIDRA (insuline glulisine) 1x 10ML INJECTIEFLACON (100 Eenheden/ml) De Apidra 100 eenheden/ml oplossing voor injectie (in injectieflacon) wordt in een injectieflacon geleverd
VICTRELIS Boceprevir
 De gezondheidsautoriteiten van de EU hebben een aantal voorwaarden gekoppeld aan het in de handel brengen van het geneesmiddel VICTRELIS. Het verplichte plan voor risicobeperking in België, waarvan deze
De gezondheidsautoriteiten van de EU hebben een aantal voorwaarden gekoppeld aan het in de handel brengen van het geneesmiddel VICTRELIS. Het verplichte plan voor risicobeperking in België, waarvan deze
1. WAT IS ORGALUTRAN EN WAARVOOR WORDT HET GEBRUIKT?
 In deze bijsluiter komen de volgende onderdelen aan bod: 1. Wat is Orgalutran en waarvoor wordt het gebruikt? 2. Wat u moet weten voordat u Orgalutran gebruikt 3. Hoe wordt Orgalutran gebruikt? 4. Mogelijke
In deze bijsluiter komen de volgende onderdelen aan bod: 1. Wat is Orgalutran en waarvoor wordt het gebruikt? 2. Wat u moet weten voordat u Orgalutran gebruikt 3. Hoe wordt Orgalutran gebruikt? 4. Mogelijke
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL FIRMAGON 80 mg poeder en oplosmiddel voor oplossing voor injectie. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke flacon
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL FIRMAGON 80 mg poeder en oplosmiddel voor oplossing voor injectie. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke flacon
ENKEL VOOR NON HODGKIN LYMFOOM (NHL)
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel MabThera oplossing voor subcutane injectie (SC). Het verplicht plan voor risicobeperking
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel MabThera oplossing voor subcutane injectie (SC). Het verplicht plan voor risicobeperking
Testosteronundecanoaat
 Testosteronundecanoaat Succesvolle toediening van Nebido (injectieflacon) Informatiebrochure voor beroepsbeoefenaren in de gezondheidszorg Deze brochure geeft informatie over de toediening van Nebido met
Testosteronundecanoaat Succesvolle toediening van Nebido (injectieflacon) Informatiebrochure voor beroepsbeoefenaren in de gezondheidszorg Deze brochure geeft informatie over de toediening van Nebido met
INSTRUCTIES VOOR HET BEREIDEN EN TOEDIENEN VAN DE SOMAVERT INJECTIE
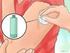 INSTRUCTIES VOOR HET BEREIDEN EN TOEDIENEN VAN DE SOMAVERT INJECTIE Inleiding In de volgende instructies wordt uitgelegd hoe SOMAVERT moet worden bereid en geïnjecteerd. Lees deze instructies aandachtig
INSTRUCTIES VOOR HET BEREIDEN EN TOEDIENEN VAN DE SOMAVERT INJECTIE Inleiding In de volgende instructies wordt uitgelegd hoe SOMAVERT moet worden bereid en geïnjecteerd. Lees deze instructies aandachtig
Bijsluiter: informatie voor de gebruiker. FIRMAGON 80 mg poeder en oplosmiddel voor oplossing voor injectie
 FIRMAGON Bijsluiter: informatie voor de gebruiker FIRMAGON 80 mg poeder en oplosmiddel voor oplossing voor injectie Degarelix Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want
FIRMAGON Bijsluiter: informatie voor de gebruiker FIRMAGON 80 mg poeder en oplosmiddel voor oplossing voor injectie Degarelix Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want
Jext : Instructies voor gebruik
 RMA versie 06/2017 Jext : Instructies voor gebruik 1 2 3 4 Ik heb een risico op anafylaxie, een levensbedreigende allergische reactie op: Als ik niet in staat ben om mezelf te helpen, volg dan de instructies
RMA versie 06/2017 Jext : Instructies voor gebruik 1 2 3 4 Ik heb een risico op anafylaxie, een levensbedreigende allergische reactie op: Als ik niet in staat ben om mezelf te helpen, volg dan de instructies
Dit geneesmiddel is onderworpen aan aanvullende monitoring
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Alofisel. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Alofisel. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
CINRYZE (C1-REMMER [HUMAAN])
![CINRYZE (C1-REMMER [HUMAAN]) CINRYZE (C1-REMMER [HUMAAN])](/thumbs/66/54698857.jpg) De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CINRYZE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CINRYZE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
ACTYNOX 50%/50% v/v Distikstofoxide (N 2 O) en Zuurstof (O 2 ) Medicinaal gas, samengeperst
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ACTYNOX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ACTYNOX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Testosteronundecanoaat
 Testosteronundecanoaat Succesvolle toediening van Nebido (injectieflacon) Informatiebrochure voor beroepsbeoefenaren in de gezondheidszorg Deze brochure geeft informatie over de toediening van Nebido met
Testosteronundecanoaat Succesvolle toediening van Nebido (injectieflacon) Informatiebrochure voor beroepsbeoefenaren in de gezondheidszorg Deze brochure geeft informatie over de toediening van Nebido met
PATIËNTENHANDLEIDING VOOR ZELFINJECTIE
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel STRENSIQ. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel STRENSIQ. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
(asfotase alfa) 40 mg/ml 100 mg/ml oplossing voor injectie (asfotase-alfa) INJECTIEHANDLEIDING. Ouders/zorgverleners van jonge patiënten
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel STRENSIQ. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel STRENSIQ. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
MYCOFENOLAATHOUDENDE GENEESMIDDELEN Informatiegids voor de gezondheidszorgbeoefenaars TERATOGEEN RISICO
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van geneesmiddelen die mycofenolaat bevatten. Het verplicht plan voor risicobeperking in België, waarvan
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van geneesmiddelen die mycofenolaat bevatten. Het verplicht plan voor risicobeperking in België, waarvan
Inhoud: 1) Informatiefolder voor de patiënt (met bijgevoegde audio-cd) 2) Bijsluiter: informatie voor gebruikers
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel OZURDEX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel OZURDEX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Brochure voor de professionele zorgverleners
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Mitoxantrone Sandoz. Het verplicht plan voor risicobeperking in België, waarvan
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Mitoxantrone Sandoz. Het verplicht plan voor risicobeperking in België, waarvan
Houder van de vergunning voor het in de handel brengen: Serono Europe Limited 56, Marsh Wall London E14 9TP Verenigd Koninkrijk
 Lees de hele bijsluiter aandachtig door alvorens dit geneesmiddel te gebruiken. Bewaar deze bijsluiter. Misschien heeft u hem nog een keer nodig. Raadpleeg uw arts of apotheker, als u aanvullende vragen
Lees de hele bijsluiter aandachtig door alvorens dit geneesmiddel te gebruiken. Bewaar deze bijsluiter. Misschien heeft u hem nog een keer nodig. Raadpleeg uw arts of apotheker, als u aanvullende vragen
Rechtstreekse mededeling aan de Gezondheidszorgbeoefenaars
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
ARIPIPRAZOLE TEVA JOUW HANDLEIDING INFORMATIEBROCHURE VOOR PATIËNTEN / VERZORGERS. (door de arts af te geven aan elke patiënt/verzorger)
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ARIPIPRAZOLE TEVA. Het verplicht plan voor risicobeperking in België, waarvan
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ARIPIPRAZOLE TEVA. Het verplicht plan voor risicobeperking in België, waarvan
Informatie verspreid onder het gezag van het federaal agentschap voor geneesmiddelen en gezondheidsproducten
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Directe communicatie aan gezondheidszorgbeoefenaars over de associatie van Sprycel (dasatinib) met Pulmonaire Arteriële Hypertensie (PAH)
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
INFORMATIE VOOR DE PATIENT
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Increlex. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Increlex. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Hemlibra (emicizumab) Subcutane injectie Dit geneesmiddel is onderworpen aan aanvullende monitoring. Informatiebrochure voor de patiënt/verzorger
 Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel Hemlibra, om voor een goed gebruik ervan te zorgen en om de ongewenste effecten ervan te beperken, zijn er bepaalde
Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel Hemlibra, om voor een goed gebruik ervan te zorgen en om de ongewenste effecten ervan te beperken, zijn er bepaalde
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL FIRMAGON 80 mg poeder en oplosmiddel voor oplossing voor injectie. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke ampul
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL FIRMAGON 80 mg poeder en oplosmiddel voor oplossing voor injectie. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke ampul
Samenstelling HMG : Poeder voor injectievloeistof (+ toedieningsset): 75 IE follikel-stimulerend hormoon (FSH) + 75 IE luteïniserend hormoon (= LH)
 Menogon /HMG /Pergonal Samenstelling HMG : Poeder voor injectievloeistof (+ toedieningsset): 75 IE follikel-stimulerend hormoon (FSH) + 75 IE luteïniserend hormoon (= LH) Samenstelling Menogon : Poeder
Menogon /HMG /Pergonal Samenstelling HMG : Poeder voor injectievloeistof (+ toedieningsset): 75 IE follikel-stimulerend hormoon (FSH) + 75 IE luteïniserend hormoon (= LH) Samenstelling Menogon : Poeder
BYDUREON 2 mg poeder en oplosmiddel voor suspensie voor injectie met verlengde afgifte
 INSTRUCTIES VOOR DE GEBRUIKER Uw stap voor stap handleiding BYDUREON 2 mg poeder en oplosmiddel voor suspensie voor injectie met verlengde afgifte Heeft u vragen over het gebruik van BYDUREON? Zie de veel
INSTRUCTIES VOOR DE GEBRUIKER Uw stap voor stap handleiding BYDUREON 2 mg poeder en oplosmiddel voor suspensie voor injectie met verlengde afgifte Heeft u vragen over het gebruik van BYDUREON? Zie de veel
BIJSLUITER: INFORMATIE VOOR DE PATIËNT
 BIJSLUITER: INFORMATIE VOOR DE PATIËNT, gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt want er staat belangrijke informatie voor u in. Bewaar deze bijsluiter. Misschien heeft
BIJSLUITER: INFORMATIE VOOR DE PATIËNT, gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt want er staat belangrijke informatie voor u in. Bewaar deze bijsluiter. Misschien heeft
INFORMATIEGIDS VOOR PATIENTEN
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Capecitabine Accord moet permanent worden stopgezet bij patiënten die een ernstige huidreactie hebben gehad tijdens de behandeling.
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
YERVOY. (ipilimumab) Concentraat voor oplossing voor infusie Dit geneesmiddel is onderworpen aan aanvullende monitoring.
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
INFORMATIEBROCHURE VOOR BEROEPSBEOEFENAARS IN DE GEZONDHEIDSZORG
 De gezondheidsinstanties van de Europese Unie hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel OPSUMIT. Het verplicht plan voor risicobeperking in België, waarvan deze
De gezondheidsinstanties van de Europese Unie hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel OPSUMIT. Het verplicht plan voor risicobeperking in België, waarvan deze
Titratiegids voor patiënten
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan hetin de handel brengen van het geneesmiddel Uptravi. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan hetin de handel brengen van het geneesmiddel Uptravi. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
INFORMATIEBROCHURE VOOR PATIËNTEN / VERZORGERS
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ARIPIPRAZOLE EG 10 mg 15 mg 30 mg tabletten. Het verplicht plan voor risicobeperking
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ARIPIPRAZOLE EG 10 mg 15 mg 30 mg tabletten. Het verplicht plan voor risicobeperking
Educatieve PrEP-brochure voor voorschrijvers 1
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Emtricitabine/Tenofovirdisoproxil Mylan 200 mg/245 mg filmomhulde tabletten.
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Emtricitabine/Tenofovirdisoproxil Mylan 200 mg/245 mg filmomhulde tabletten.
Informatiebrochure voor laboratoriumpersoneel
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel hemlibra. Het verplicht plan voor risicobeperking in België en het Groothertogdom
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel hemlibra. Het verplicht plan voor risicobeperking in België en het Groothertogdom
Gebruikershandleiding. Taltz 80mg oplossing voor injectie in voorgevulde injectiespuit. Ixekizumab
 Gebruikershandleiding Taltz 80mg oplossing voor injectie in voorgevulde injectiespuit Ixekizumab Voordat u uw voorgevulde injectiespuit gebruikt: Belangrijk om te weten Lees voordat u de Taltz voorgevulde
Gebruikershandleiding Taltz 80mg oplossing voor injectie in voorgevulde injectiespuit Ixekizumab Voordat u uw voorgevulde injectiespuit gebruikt: Belangrijk om te weten Lees voordat u de Taltz voorgevulde
Gids voor gezondheidszorgbeoefenaars
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Lariam. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Lariam. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
INFORMATIEBROCHURE VOOR PATIËNTEN / VERZORGERS
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ABILIFY. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ABILIFY. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
RECONSTITUTIE, DOSERING EN TOEDIENING
 Additioneel risico minimalisatie materiaal betreffende bortezomib voor beroepsbeoefenaren in de gezondheidszorg Belangrijke informatie over de RECONSTITUTIE, DOSERING EN TOEDIENING van bortezomib 3,5 mg
Additioneel risico minimalisatie materiaal betreffende bortezomib voor beroepsbeoefenaren in de gezondheidszorg Belangrijke informatie over de RECONSTITUTIE, DOSERING EN TOEDIENING van bortezomib 3,5 mg
De volgende informatie is alleen bestemd voor artsen of andere beroepsbeoefenaren in de gezondheidszorg.
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Levonortis. Het verplicht plan voor risicobeperking in België, waarvan deze
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Levonortis. Het verplicht plan voor risicobeperking in België, waarvan deze
INSTRUCTIEBROCHURE. voor mensen die Metoject 50 mg/ml gebruiken
 INSTRUCTIEBROCHURE voor mensen die Metoject 50 mg/ml gebruiken Inhoud Pagina Inleiding 3 Hoe wordt Metoject 50 mg/ml gebruikt? 4 Het vermijden van plaatselijke huidirritatie 7 Het vermijden van verharding
INSTRUCTIEBROCHURE voor mensen die Metoject 50 mg/ml gebruiken Inhoud Pagina Inleiding 3 Hoe wordt Metoject 50 mg/ml gebruikt? 4 Het vermijden van plaatselijke huidirritatie 7 Het vermijden van verharding
Cetrotide 0,25 mg poeder en oplosmiddel voor oplossing voor injectie Cetrorelixacetaat
 CETROTIDE Bijsluiter: informatie voor de gebruiker Cetrotide 0,25 mg poeder en oplosmiddel voor oplossing voor injectie Cetrorelixacetaat Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
CETROTIDE Bijsluiter: informatie voor de gebruiker Cetrotide 0,25 mg poeder en oplosmiddel voor oplossing voor injectie Cetrorelixacetaat Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
INFORMATIE VOOR DE PATIENT
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Increlex. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Increlex. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Dit geneesmiddel is onderworpen aan aanvullende monitoring.
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Erivedge. Het verplicht plan voor risicobeperking in België, waar deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Erivedge. Het verplicht plan voor risicobeperking in België, waar deze informatie
MAVENCLAD (Cladribine)
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel MAVENCLAD. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel MAVENCLAD. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Educatief materiaal voor gezondheidsbeoefenaars (Powerpointpresentatie)
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel BOCOUTURE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel BOCOUTURE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
ISOCURAL zachte capsules, oraal (isotretinoïne)
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ISOCURAL. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ISOCURAL. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Selectie en training van volwassen * patiënten voor thuistoediening van Nplate
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Onderwerp: Ernstige huidreacties geassocieerd met Capecitabine (Xeloda )
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een illustratief hulpmiddel voor het thuis toedienen van Nplate
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Dit verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Dit verplicht plan voor risicobeperking in België, waarvan deze informatie
Risico minimalisatie materialen betreffende Inflectra (infliximab) voor de voorschrijvers
 Inflectra (infliximab) Dit geneesmiddel is onderworpen aan aanvullende monitoring Risico minimalisatie materialen betreffende Inflectra (infliximab) voor de voorschrijvers De risico minimalisatie materialen
Inflectra (infliximab) Dit geneesmiddel is onderworpen aan aanvullende monitoring Risico minimalisatie materialen betreffende Inflectra (infliximab) voor de voorschrijvers De risico minimalisatie materialen
BIJSLUITER Atosiban Devrimed 6,75 mg/0,9 ml
 BIJSLUITER Atosiban Devrimed 6,75 mg/0,9 ml 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Atosiban Devrimed 6,75 mg/0,9 ml oplossing voor injectie Atosiban Lees goed de hele bijsluiter voordat u dit geneesmiddel
BIJSLUITER Atosiban Devrimed 6,75 mg/0,9 ml 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Atosiban Devrimed 6,75 mg/0,9 ml oplossing voor injectie Atosiban Lees goed de hele bijsluiter voordat u dit geneesmiddel
Fronslijnen behandelen met VISTABEL
 Uw arts heeft u verteld dat u in aanmerking komt voor een behandeling met VISTABEL. In deze folder vindt u extra informatie over deze behandeling en enkele algemene tips voor de verzorging van de huid.
Uw arts heeft u verteld dat u in aanmerking komt voor een behandeling met VISTABEL. In deze folder vindt u extra informatie over deze behandeling en enkele algemene tips voor de verzorging van de huid.
Zelfinjectie bij erectiestoornissen. Poli Urologie
 00 Zelfinjectie bij erectiestoornissen Poli Urologie 1 In overleg met uw uroloog heeft u gekozen om zelf medicijnen te injecteren in het zwellichaam van de penis (auto-injectie therapie). Uw behandelend
00 Zelfinjectie bij erectiestoornissen Poli Urologie 1 In overleg met uw uroloog heeft u gekozen om zelf medicijnen te injecteren in het zwellichaam van de penis (auto-injectie therapie). Uw behandelend
INFORMATIE VOOR DE VOORSCHRIJVER
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Tracleer. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Tracleer. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
METASTRON 37 MBq/ml oplossing voor injectie Strontium [ 89 Sr] chloride
![METASTRON 37 MBq/ml oplossing voor injectie Strontium [ 89 Sr] chloride METASTRON 37 MBq/ml oplossing voor injectie Strontium [ 89 Sr] chloride](/thumbs/88/115148610.jpg) BIJSLUITER: INFORMATIE VOOR DE PATIËNT METASTRON 37 MBq/ml oplossing voor injectie Strontium [ 89 Sr] chloride Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke
BIJSLUITER: INFORMATIE VOOR DE PATIËNT METASTRON 37 MBq/ml oplossing voor injectie Strontium [ 89 Sr] chloride Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke
Bijsluiter: informatie voor de gebruiker. Neurobion 100 mg 100 mg 1 mg / 3 ml oplossing voor injectie Vitaminen B 1 + B 6 + B 12
 Bijsluiter: informatie voor de gebruiker Neurobion 100 mg 100 mg 1 mg / 3 ml oplossing voor injectie Vitaminen B 1 + B 6 + B 12 Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want
Bijsluiter: informatie voor de gebruiker Neurobion 100 mg 100 mg 1 mg / 3 ml oplossing voor injectie Vitaminen B 1 + B 6 + B 12 Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want
Dosisgids bestemd voor de arts voor de behandeling van Reumatoïde Artritis (RA) met RoACTEMRA
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel RoACTEMRA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel RoACTEMRA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Educatieve PrEP-brochure voor voorschrijvers 1
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Emtricitabin/ Tenofovir Disoproxil Sandoz. Het verplicht plan voor risicobeperking
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Emtricitabin/ Tenofovir Disoproxil Sandoz. Het verplicht plan voor risicobeperking
RECONSTITUTIE, DOSERING EN TOEDIENING
 Belangrijke informatie over de RECONSTITUTIE, DOSERING EN TOEDIENING van bortezomib 3,5 mg injectieflacon voor subcutaan (SC) en intraveneus (IV) gebruik Teva Nederland BV Swensweg 5 Postbus 552 2003 RN
Belangrijke informatie over de RECONSTITUTIE, DOSERING EN TOEDIENING van bortezomib 3,5 mg injectieflacon voor subcutaan (SC) en intraveneus (IV) gebruik Teva Nederland BV Swensweg 5 Postbus 552 2003 RN
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Patiëntenfolder
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
EDUCATIEVE INFORMATIE VOOR PATIËNTEN
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel BOCOUTURE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel BOCOUTURE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Patiënten Informatiegids
 Patiënten Informatiegids voor behandeling met Aclasta (zoledroninezuur 5 mg) Acl 117 PatientGids Aanpas.indd 1 23-12-2013 13:24 2 Acl 117 PatientGids Aanpas.indd 2 23-12-2013 13:24 Deze brochure is bestemd
Patiënten Informatiegids voor behandeling met Aclasta (zoledroninezuur 5 mg) Acl 117 PatientGids Aanpas.indd 1 23-12-2013 13:24 2 Acl 117 PatientGids Aanpas.indd 2 23-12-2013 13:24 Deze brochure is bestemd
