Handleiding thuisinfusie voor de patiënt
|
|
|
- Daniël Geerts
- 7 jaren geleden
- Aantal bezoeken:
Transcriptie
1 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel FABRAZYME. Het verplicht plan voor risicobeperking in België, waarvan deze informatie deel uitmaakt, is een maatregel genomen om een veilig en doeltreffend gebruik van FABRAZYME te waarborgen (RMA versie 08/2013). Fabrazyme (agalsidase bèta) Lees aandachtig de bijsluiter voordat u Fabrazyme gaat gebruiken. Lees goed deze informatiebrochure voordat u start met thuisinfusie.
2 INHOUDSTAFEL 1. DOEL VAN DIT EDUCATIEF MATERIAAL UW ZIEKTE, BEHANDELING EN THUISINFUSIE De ziekte van Fabry en behandeling Thuisinfusie Veiligheidsbeoordeling ORGANISATIE THUISINFUSIE Patiënt Behandelende arts Apotheker Thuisverpleegkundige Voorbehandeling en behandeling in noodsituatie Het logboek OPLEIDING IN HET OPLOSSEN EN TOEDIENEN VAN FABRAZYME FABRAZYME BEREIDEN EN TOEDIENEN Benodigdheden Voorbereiding Oplossen Verdunning De infusielijn vullen De naald in de ader brengen Toediening Voorbereiding bij gebruik van een centraal veneuze toegang BIJLAGEN Logboek Bijsluiter - Fabrazyme 5 mg Bijsluiter - Fabrazyme 35 mg
3 1. DOEL VAN DIT EDUCATIEF MATERIAAL Deze informatie maakt deel uit van het Belgische risicobeheerplan, dat informatiemateriaal beschikbaar stelt aan gezondheidszorgbeoefenaars en patiënten. Deze bijkomende risicobeperkende activiteiten hebben als doel een veilig en doeltreffend gebruik van Fabrazyme te waarborgen en moeten volgende belangrijke onderdelen bevatten: Het opleidingspakket dat moet bestaan uit: Handleiding voor thuisinfusie voor de beroepsbeoefenaar in de gezondheidszorg Handleidingen voor thuisinfusie voor patiënten Samenvatting van de productkenmerken en bijsluiter Het opleidingsmateriaal voor patiënten moet informatie over de volgende belangrijke elementen bevatten: - De voorschrijvende arts kan beslissen dat Fabrazyme thuis kan worden toegediend. De vereiste mate van ondersteuning voor thuisinfusies zal worden besproken en overeengekomen door de patiënt en/of zorgverlener en de voorschrijvende arts. - De behandelende arts bepaalt welke patiënten er in aanmerking kunnen komen voor thuisinfusies of zelftoediening van Fabrazyme en treft de nodige regelingen voor thuisbehandeling en voor de opleiding van de patiënt en/of zorgverlener in de specifieke en juiste vaardigheden die hiervoor nodig zijn. - Niet-medisch personeel moet de nodige vaardigheden hebben vergaard voordat Fabrazyme veilig en doeltreffend thuis kan worden toegediend. - Hun voorschrijvende arts zal een training verzorgen over de volgende elementen: o Het is essentieel om strikt de voorgeschreven dosis en infusiesnelheid te volgen o Bereidingsmethode en wijze van toediening van Fabrazyme o Instructie voor het behandelen van mogelijke bijwerkingen o Instructie om dringend medisch hulp in te winnen bij beroepsbeoefenaren in de gezondheidszorg in geval van een bijwerking tijdens een infusie o De vereiste om dringend medische hulp in te winnen in geval er geen veneuze toegang kan worden verkregen of bij gebrek aan effectiviteit 3
4 o De vereiste om een dagboek bij te houden om elke gekregen thuisbehandeling te documenteren en het bij elk bezoek mee te brengen 2. UW ZIEKTE, BEHANDELING EN THUISINFUSIE Samen met uw behandelende arts heeft u beslist om te starten met thuisinfusie met Fabrazyme. Dit document geeft u een leidraad over hoe u Fabrazyme thuis kunt toegediend krijgen. Van uw behandelende arts krijgt u alle informatie die op uw situatie van toepassing is De ziekte van Fabry en behandeling Fabrazyme is aangewezen voor langdurige enzym-substitutietherapie bij patiënten met een bevestigde diagnose van de ziekte van Fabry (αgalactosidase A deficiëntie). Bij patiënten met de ziekte van Fabry ontbreekt de enzymactiviteit van α- galactosidase A of is ze lager dan normaal. Dit enzym zorgt normaal gesproken voor de afbraak van een vetachtige stof, globotriaosylceramide (GL-3). Als u aan de ziekte van Fabry lijdt, wordt deze stof niet uit de cellen van uw lichaam verwijderd en gaat zich ophopen in de wanden van de bloedvaten van uw organen. De belangrijkste symptomen van de ziekte van Fabry, die bij mannen reeds in de kinderjaren optreden, zijn perioden van pijn en een brandend gevoel in handen en voeten, maag-en darm klachten, huiduitslag en een verminderd vermogen tot zweetafscheiding. De ziekte manifesteert zich op volwassen leeftijd meestal in de vorm van hart-, nieren/of neurologische problemen. Bij vrouwen kan het verloop van de ziekte atypische zijn en vaak - niet altijd - minder ernstig dan bij mannen. Fabrazyme bevat het werkzame bestanddeel agalsidase bèta en is aangewezen voor gebruik als langdurige enzymvervangingstherapie bij patiënten bij wie is vastgesteld dat ze aan de ziekte van Fabry lijden. Raadpleeg de bijsluiter van Fabrazyme voor bijkomende informatie (Bijlagen 6.2 en 6.3). 4
5 2.2. Thuisinfusie In sommige landen krijgen mensen die lijden aan de ziekte van Fabry en behandeld worden met Fabrazyme hun infusies thuis. De beslissing om thuis behandeld te worden, moet worden genomen door u en uw behandelende arts. De eerste infusies dienen in het ziekenhuis te gebeuren om te controleren of de infusies goed worden verdragen. Thuisinfusie gebeurt onder de verantwoordelijkheid van uw behandelende arts. Een thuisverpleegkundige, met de geschikte opleiding, zal u en/of uw verzorger aanvankelijk opleiden en bijstaan om een optimale behandeling te garanderen. U bespreekt samen met uw zorgverlener(s) en uw behandelende arts hoeveel ondersteuning voor de thuisinfusie u nodig heeft. Indien u echter de voorkeur geeft aan volledige ondersteuning voor uw infusies thuis, zal de thuisverpleegkundige de volledige procedure uitvoeren. Opmerking: de dosis en infusiesnelheid bij behandeling thuis moeten overeenkomen met de richtlijnen van uw behandelende arts, zoals aangegeven in het logboek (Bijlage 6.1). Hierop mogen geen aanpassingen worden doorgevoerd zonder goedkeuring vooraf van uw behandelende arts en toezicht van de infusieverpleegkundige Veiligheidsbeoordeling Infusie-gerelateerde reacties Zoals bij elk intraveneus eiwitgeneesmiddel kunnen overgevoeligheidsreacties optreden. Sommige patiënten hebben een grotere kans op infusie-gerelateerde bijwerkingen, die gedefinieerd worden als iedere bijwerking die zich op de dag van de infusie voordoet. Deze patiënten dienen voorzichtig behandeld te worden wanneer agalsidase bèta opnieuw wordt toegediend. De meest voorkomende bijwerkingen van infusie met Fabrazyme (bij meer dan 1 op de 10 patiënten) zijn koorts en rillingen. Andere zeer vaak voorkomende bijwerkingen zijn hoofdpijn, abnormaal tastgevoel (spelden- en 5
6 naaldprikken), misselijkheid, braken en koud gevoel. Ernstige allergische reacties zijn gerapporteerd (frequentie niet bekend). Bijwerkingen die bij kinderen zijn gemeld, lijken op de bijwerkingen bij volwassenen. Een volledige lijst met alle bijwerkingen die zijn gemeld voor Fabrazyme, vindt u in rubriek 4 van de bijsluiter (Bijlagen 6.2 en 6.3). De infusie-gerelateerde bijwerkingen kunnen behandeld worden door verlaging van de infusiesnelheid* gecombineerd met toediening van daartoe door de behandelende arts voor u specifiek voorgeschreven geneesmiddelen. Acties in geval van een ernstige infusie-gerelateerde reactie : 1. Stop de infusie 2. Bel de noodtelefoon (100 of 112) 3. Bel de arts *Let wel, De behandelende arts is verantwoordelijk voor de dosering en infusiesnelheid. Deze mag niet gewijzigd worden in de thuisomgeving, tenzij dit nodig is vanuit een veiligheidsoverweging. Elke verandering aan de toediening van Fabrazyme dient duidelijk gedocumenteerd te worden in het logboek (Bijlage 6.1). Wanneer u zich door de medicatie tijdens of vlak na de thuisinfusie niet goed voelt, moet u de medicatie onmiddellijk stopzetten. Neem meteen contact op met de behandelende arts, zijn of haar plaatsvervanger, en/of het noodnummer 100 of 112 (zie de instructies in het logboek in bijlage 6.1). Volgende infusies zullen mogelijks in een klinische omgeving moeten plaatsvinden. Alle symptomen of bijwerkingen moeten ook worden genoteerd in het logboek (Bijlage 6.1). Medicatiefouten Als u merkt dat er een fout is gemaakt bij de voorbereiding en/of toediening van Fabrazyme, moet u de infusieverpleegkundige of de behandelende arts om advies vragen voordat de infusie opnieuw wordt gestart of voortgezet. Zie rubriek 4 van de bijsluiter (Bijlage 6.3) voor de volledige informatie over de veiligheid van Fabrazyme. 6
7 3. ORGANISATIE VAN THUISINFUSIE 3.1. Patiënt U en/of uw verzorger werd(en) geïnformeerd door de behandelende arts over het toedienen van de behandeling thuis, de eraan verbonden risico s, de mogelijke complicaties en de voorziening van medische assistentie thuis. U en/of uw verzorger begrijpt/begrijpen de ziekte van Fabry en is/zijn in staat bijwerkingen te herkennen en begrijpt/begrijpen de procedure die moet worden gevolgd als deze optreden. De thuisomgeving dient gunstig te zijn voor het toedienen van de behandeling met thuisinfusie, waaronder een schone omgeving met elektriciteit- en watervoorziening, telefoonverbinding, koelkast en fysieke ruimte om Fabrazyme en andere infusiebenodigdheden te bewaren. U bent ervan op de hoogte dat de infusie altijd moet worden toegediend in aanwezigheid van een getrainde volwassene (een infusieverpleegkundige of, als u de infusies zelf toedient, een volwassene die goed is ingelicht over de infusieprocedures en is getraind in hoe te handelen in het geval van infusie-gerelateerde bijwerkingen en medicatiefouten, zoals bepaald door de behandelende arts of de infusieverpleegkundige). U moet fysiek en mentaal in staat zijn om de infusie thuis te ondergaan. De behandelende arts is verantwoordelijk voor de indicatie om Fabrazyme -infusies thuis toegediend te krijgen. U heeft toegankelijke aders die het mogelijk maken een infusienaald in te brengen. Wanneer u een centraal veneuze toegang heeft, moet de infusienaald in het systeem ingebracht kunnen worden. U en/of uw verzorger moet(en) ermee instemmen om de behandeling thuis toegediend te krijgen. U en/of uw verzorger heeft/hebben de geschikte opleiding gehad over de procedures voor het oplossen, het verdunnen en de infusie met Fabrazyme. 7
8 3.2. Behandelende arts De behandelende arts is verantwoordelijk voor de initiatie van alle nodige administratieve handelingen, waardoor andere belanghebbenden (thuisverpleegkundige, patiënt, verzorger) hun taken kunnen voortzetten. Thuisinfusie gebeurt onder de verantwoordelijkheid van uw behandelende arts. Het educatief materiaal dient enkel verspreid te worden indien de behandelende arts beslist dat de patiënt in aanmerking komt voor thuisinfusie. Het is de verantwoordelijkheid van de behandelende arts om een veilige toediening te garanderen. Dit moet gecontroleerd en gedocumenteerd worden door de behandelende arts. De behandelende arts is verantwoordelijk voor het duidelijk vermelden in het logboek van de dosering en infusiesnelheid, de behandeling voorafgaand aan de infusie en de behandeling in noodgeval. Eventuele wijzigingen moeten duidelijk aan de patiënt worden gemeld en moeten in het logboek worden beschreven (Bijlagen 6.2 en 6.3). De behandelende arts is verantwoordelijk voor het instellen van communicatielijnen in het geval u onmiddellijk medische hulp nodig heeft. Deze moeten in het logboek worden genoteerd. De behandelende arts en de thuisverpleegkundige stellen een tijdschema op voor regelmatige controle op de infusies die door de patiënt en/of zijn verzorger of door de thuisverpleegkundige worden toegediend Apotheker De behandeling en alle benodigde apparatuur (infusiemateriaal) worden verstrekt door de (ziekenhuis)apotheker op voorlegging van bijhorend voorschrift Thuisverpleegkundige De thuisverpleegkundige bepaalt in overleg met de behandelende arts en de patiënt en/of zorgverlener(s) hoeveel zorg bij de thuisinfusie nodig is. De thuisverpleegkundige heeft samen met de behandelende arts en u en/of uw zorgverlener(s) een coördinerende taak in de organisatie van de behandeling thuis. 8
9 De thuisverpleegkundige is bevoegd om IV-infusies toe te dienen. De thuisverpleegkundige kreeg een opleiding over de toediening van Fabrazyme. De thuisverpleegkundige is zich bewust van de mogelijke bijwerkingen en de acties die moeten worden ondernomen in geval er zich bijwerkingen voordoen. De thuisverpleegkundige zal strikt de voorgeschreven toedieningsmethode, dosis en infusiesnelheid van Fabrazyme volgen zoals vermeld in het logboek (Bijlage 6.1). De thuisverpleegkundige zal elke toediening van Fabrazyme logboek noteren (Bijlage 6.1). in het De behandelende arts en de thuisverpleegkundige stellen een tijdschema op voor regelmatige controle op de infusies die door de patiënt en/of zijn verzorger of door de thuisverpleegkundige worden toegediend. Bij eventuele reactie als gevolg van de infusie moet de thuisverpleegkundige de infusie stopzetten en telefonisch contact opnemen met de behandelende arts en/of het noodnummer 100 of 112 bellen. De behandelende arts en/of het noodnummer 100/112 moeten ook worden gebeld wanneer een infusie-gerelateerde bijwerking vlak na het toedienen van een infusie optreedt. Alle infusie-gerelateerde bijwerkingen moeten worden genoteerd in het logboek (Bijlage 6.1) Voorbehandeling en behandeling in een noodsituatie De behandelende arts zal u indien nodig medicatie voorschrijven die voorafgaand aan de infusie kan ingenomen worden. De behandelende arts noteert informatie over deze medicatie in het logboek. De behandelende arts zal u indien nodig medicatie voor de behandeling van een noodgeval voorschrijven. De behandelende arts noteert informatie over deze medicatie in het logboek. De medicatie voor noodgevallen moet tijdens de thuisinfusies beschikbaar zijn. 9
10 3.6. Het logboek (Bijlage 6.1) Het logboek vormt een communicatiemiddel voor iedereen die betrokken is bij het toedienen van Fabrazyme thuis. Het logboek moet bij u thuis worden bewaard en zal door u, uw verzorger of de thuisverpleegkundige worden bijgewerkt. De voorgeschreven dosis en infusiesnelheid van Fabrazyme zoals vermeld in het logboek moeten strikt worden aangehouden. De behandelende arts vermeldt er duidelijk de dosis, de infusiesnelheid, evenals eventuele wijzigingen. Elke toediening van Fabrazyme moet in het logboek genoteerd worden. U en/of uw verzorger dient/dienen het logboek bij elke afspraak mee te nemen naar het ziekenhuis ter controle en het vervolgens opnieuw mee naar huis te nemen. De thuisverpleegkundige noteert de bevindingen en acties van het initiële gesprek en u, uw verzorger of de thuisverpleegkundige noteert alle relevante informatie van volgende bezoeken in het logboek. In het logboek vermeldt de behandelende arts duidelijk wat er moet gebeuren en wat er moet worden toegediend in geval van een infusiegerelateerde bijwerking. Wanneer een infusie-gerelateerde bijwerking optreedt, moet de infusie worden stopgezet. Alle infusie-gerelateerde bijwerkingen en/of medicatiefouten moeten in het logboek worden vermeld. 4. OPLEIDING IN HET OPLOSSEN EN TOEDIENEN VAN FABRAZYME In principe zullen de initiële instructies in het ziekenhuis worden gegeven. De mate van ondersteuning die vereist is van de thuisverpleegkundige zal met u en/of uw verzorger en uw behandelende arts worden besproken en overeengekomen. 10
11 Uw behandelende arts is verantwoordelijk voor de organisatie van de thuisinfusie en moet goedkeuring geven aan de gevolgde procedure voor thuisinfusie. Indien u verkiest om de procedure zelf uit te voeren of met de hulp van uw verzorger, zult/zullen u en/of uw verzorger opgeleid worden door de thuisverpleegkundige. De thuisverpleegkundige zal de volledige infusieprocedure aan u en/of uw verzorger uitleggen en tonen, inclusief een training in hygiëne van de handen, de juiste ontsmetting en de aseptische maatregelen die bij de bereiding van de infusie moeten worden gevolgd. Tijdens de volgende bezoeken zal de thuisverpleegkundige aanwezig zijn om te helpen indien nodig totdat u zich vertrouwd voelt met de volledige infusieprocedure. Bij het oplossen, verdunnen en toedienen van Fabrazyme moet de procedure die staat beschreven in de bijsluiter, nauwgezet worden gevolgd (Bijlagen 6.2 en 6.3). 5. FABRAZYME BEREIDEN EN TOEDIENEN 5.1. Benodigdheden Op voorlegging van bijhorend voorschrift, afgeleverd door de (ziekenhuis)apotheker aan de patiënt of aan een derde. Flacons met Fabrazyme (5 mg of 35 mg per flacon); moeten worden bewaard bij een temperatuur tussen +2 C and +8 C. Steriel water voor injecties om Fabrazyme op te lossen. Oplossing van 0,9 % NaCl, 2 x 250 ml voor IV-toediening. Oplossing van 0,9 % NaCl, 2 x 50 ml voor het spoelen van de infusielijn vóór en na de infusie. Chloorhexidine 0,5 % in alcohol 70 % (antiseptische oplossing). Correct aantal spuiten van 2 ml, 10 ml en 50 ml, afhankelijk van de dosis Fabrazyme. 11
12 3 x steriele hypodermische naalden (1,1 x 40 mm). 1 x vlindernaald. Inlinefilter van 0,2 micron met lage proteïnebinding. Toedieningsset voor infusie (infusieslang). Kleefband. Mediswabs (alcoholdoekjes) Container voor naalden. Reinigingsmiddel voor handen. Tourniquet. Bijkomende benodigdheden bij gebruik van centraal veneuze toegang: heparine, 0,9% NaCl oplossing, naalden, spuiten, wondverband, steriele handschoenen, grippernaald. Noodmedicatie (zoals beschreven in het logboek) 5.2. Voorbereiding OPMERKING: de instructies voor gebruik (reconstitutie, verdunning en toediening) kunt u vinden in de bijsluiter (Bijlage 6.2 en 6.1). In dit gedeelte vindt u een gedetailleerde beschrijving. 1. Zorg voor een schoon werkvlak en leg alle benodigdheden klaar. 2. De flacons met Fabrazyme moeten ongeveer 30 minuten vóór de bereiding uit de koelkast worden gehaald om op kamertemperatuur te komen. 3. Controleer de vervaldatum die op de onderkant van de flaconverpakking staat gedrukt (Fabrazyme niet gebruiken na de vervaldatum). 4. Controleer of het aantal ontvangen flacons correct is. 5. Bereid enkel het aantal vereiste flacons voor 1 infusie. Opmerking: de bewaarinstructies zoals beschreven in de instructies voor gebruik van de bijsluiter moeten worden opgevolgd. (Bijlagen 6.2 en 6.3). 12
13 5.3. Oplossen 1. Verwijder de flip-offdop van de flacon met Fabrazyme. 2. Ontsmet de rubberen stop van de Fabrazyme -flacon met chloorhexidine en laat drogen aan de lucht. 3. Open het steriele water voor injecties. 4. Trek het vereiste aantal ml steriele water in de spuit. Een flacon van 35 mg wordt gereconstitueerd met 7,2 ml water voor injectie. Een flacon van 5 mg wordt gereconstitueerd met 1,1 ml water voor injectie. 5. Vermijd krachtig spuiten van het water voor injectie uit de spuit op het poeder om schuim in de oplossing te voorkomen. Het water voor injectie dient langzaam druppelsgewijs in de flacon te worden gespoten. Draai de flacon(s) zorgvuldig rond om de oplossing te mengen (vermijd krachtig schudden tijdens het oplossen om schuimvorming te vermijden). 6. Herhaal het proces voor meer Fabrazyme -flacons indien nodig. 7. Er kunnen kleine luchtbellen verschijnen na het mengen. 8. Laat de oplossing gedurende een aantal minuten bezinken om eventuele luchtbellen te laten verdwijnen en te garanderen dat het poeder correct opgelost is. 9. Na oplossen, moet Fabrazyme visueel worden gecontroleerd voorafgaand aan gebruik. Omdat dit een proteïneoplossing is, kan er nu en dan lichte vlokvorming (beschreven als dunne, transparante vezels) voorkomen na oplossen. De oplossing moet helder, kleurloos, vloeibaar en vrij van vreemde deeltjes zijn. 10.Als u vreemde deeltjes in of verkleuring van de vloeistof opmerkt, gebruik het product dan niet en verwittig de thuisverpleegkundige en/of de behandelende arts. 13
14 11.Het wordt aanbevolen om de flacons meteen na de reconstitutie te verdunnen om de vorming van proteïnedeeltjes na verloop van tijd te voorkomen. 12.Alle ongebruikte producten en afvalstoffen moeten worden weggegooid in overeenstemming met de lokale voorschriften Verdunning 1. Ontsmet de dop/opening van 1 of 2 zakken van 0,9 % NaCl-oplossing met chloorhexidine en laat het drogen aan de lucht. 2. Het volume gereconstitueerde Fabrazyme -oplossing moet overeenkomen met het volume dat is voorgeschreven in het logboek (Bijlage 6.1). 3. Steek de naald door de dop van de infusiezak en zuig langzaam een volume NaCl 0,9 %-oplossing uit de zak dat gelijk is aan het volume van de gereconstitueerde Fabrazyme -oplossing die moet worden toegevoegd. Als het voorgeschreven gereconstitueerde volume bijvoorbeeld 14 ml is, zuigt u 14 ml van de NaCl-oplossing op uit de zak met NaCl-oplossing. Verwijder nooit meer dan de helft van de inhoud van de zak NaCl om zeker te zijn dat minstens de helft van de verdunde oplossing uit NaCl bestaat. 4. Verwijder de lucht uit de infusiezak door de lucht op te zuigen in een spuit van 50 ml. Zuig het benodigde volume aan gereconstitueerde oplossing langzaam uit elke flacon totdat het vereiste totaalvolume is bereikt. Op het moment waarop deze hoeveelheden worden opgetrokken, mag het opgeloste product geen schuim bevatten. Let op: Uit een flacon van 35 mg mag slechts 7.0 ml opgezogen worden, uit een flacon van 5 mg, slecths 1.0 ml 5. Injecteer vervolgens het totale volume van Fabrazyme -oplossing langzaam in de zak 0,9 % NaCl-oplossing. 14
15 6. Meng deze Fabrazyme -oplossing voorzichtig door de infusiezak langzaam te draaien of licht te masseren. Vermijd schudden of overmatig bewegen van de infusiezak. 7. De verdunde oplossing moet gefilterd worden door een inlinefilter van 0,2 micron met lage proteïnebinding tijdens de toediening De infusielijn vullen 1. Verwijder het infusiesysteem uit de verpakking en sluit het met de rolklem. Verbind de inlinefilter met de infusielijn. 2. Sluit de insteekpunt in een zak met NaCl 0,9 % die geen Fabrazyme bevat en vul het infusiesysteem door de druppelkamer omgekeerd te houden en de klem te openen. 3. Vul het volledige systeem, verwijder eventuele luchtbellen die aanwezig zijn en sluit de rolklem. 4. Sluit de infusiezak met Fabrazyme aan op het y-systeem. Zorg dat de klem gesloten blijft De naald in de ader brengen Wanneer u zelf de infusie uitvoert, moet de volwassene die bij de infusie aanwezig is adequaat zijn getraind (door de thuisverpleegkundige, behandelende arts, of zijn/haar plaatsvervanger) in de techniek van het inbrengen van naalden. 1. Zorg ervoor dat er een aantal pleisterstrips klaar hangen voor gebruik en dat de start van het infusiesysteem binnen bereik is. Plaats de chloorhexidine binnen handbereik samen met een aantal gaasdoekjes. 2. Verwijder de vlindernaald uit de verpakking. 3. Ga zitten met één arm op de tafel rustend (bij voorkeur op een schone doek). 4. Breng het knelverband aan en desinfecteer de zone waar de naald zal worden ingebracht en laat het drogen. 15
16 5. Trek de huid strak en breng de naald (met het oog naar boven gericht) in een lichte hoek in via de huid en in de ader. Op de plaats waar de naald in de ader gaat, zal er een opwelling van bloed zichtbaar zijn aan het begin van de lijn. 6. Breng de naald ongeveer 0,5 cm in de ader in om zeker te zijn dat ze er niet opnieuw uitspringt. Bevestig de vlindernaald op zijn plaats met behulp van een pleister. Verbind het systeem met de naald. 7. Maak het knelverband los en verwijder de dop van de lijn. De lijn zal nu gevuld worden met bloed. Als dit niet gebeurt, zit de naald niet correct in de ader. Het proces moet worden herhaald met een nieuwe naald. Open de klem voor NaCl 0,9 %-oplossing. 8. Pas de infusiesnelheid aan volgens de aanwijzingen (zie het logboek, bijlage 6.1) en draai het kraantje open. Ga zitten en ontspan terwijl de infusie plaatsvindt. Houd het logboek bij de hand voor het geval u de procedures voor noodgevallen moet raadplegen. Wanneer het inbrengen van de naald in de ader en/of niet lukt of wanneer er zich een technisch probleem met de infusie voordoet, dient er onmiddellijk contact opgenomen te worden met de behandelende arts, de thuisverpleegkundige en/of het noodnummer 100 of Toediening Vanuit microbiologisch oogpunt moet het product onmiddellijk worden gebruikt. Als het product niet meteen wordt gebruikt, zijn de opslag en de condities voor gebruik de verantwoordelijkheid van de gebruiker. Het product dat is verdund in een 0,9 % NaCl-oplossing zal zijn chemische stabiliteit behouden wanneer het maximaal 24 uur wordt bewaard bij een temperatuur tussen 2 C en 8 C en uit het zonlicht. De dosis Fabrazyme, de infusiesnelheid alsook eventuele wijzigingen zullen worden bepaald door de behandelende arts. De behandeling mag in de thuissituatie niet worden gewijzigd, tenzij medisch gerechtvaardigd naar het oordeel van de behandelende arts. 16
17 Na afloop van het Fabrazyme -infuus wordt het systeem gespoeld met 0,9 % NaCl-oplossing bij dezelfde snelheid en wordt de naald verwijderd Voorbereiding bij gebruik van een centraal veneuze toegang Wanneer u over een centraal veneuze toegang beschikt voor de aflevering van Fabrazyme, zal door de verpleegkundige aan u en/of uw verzorger worden getoond hoe dit apparaat moet worden onderhouden en de werking van de katheter demonstreren, als dit nog niet is gebeurd tijdens de infusies in het ziekenhuis. Een correcte thuiszorg voor een apparaat voor veneuze toegang houdt in dat het regelmatig gespoeld moet worden met heparine om klontervorming te voorkomen en dat er aandacht wordt geschonken aan een steriele techniek om het apparaat vrij te houden van besmetting. De volgende stappen zijn noodzakelijk: Wanneer het apparaat in gebruik is, de locatie met transparant occlusief verband bedekken. Geen verband nodig wanneer het apparaat niet in gebruik is. Spoelen met 5 ml zoutoplossing vóór en na elk gebruik. Spoelen met 5 ml heparine (100 E/mL) na elk gebruik. 17
18 6. BIJLAGEN 6.1. Logboek Logboek voor Fabrazyme -thuisinfusie Algemene gegevens Patiënt Naam: Geboortedatum: Adres: Postcode / stad: Telefoon: Thuisverpleegkundige Naam: Organisatie: Telefoon: Behandelende arts Naam: Ziekenhuis: Adres: Postcode / stad: Telefoon: Apotheker Naam: Postcode / stad: Telefoon: Noodtelefoon 100 of
19 Details van toediening (in te vullen door behandelende arts) Fabrazyme toegediend sinds Datum (dd-mmm-yyyy): Eerste infusie thuis Datum (dd-mmm-yyyy): Redenen voor Fabrazyme -infusie thuis Ondersteuning door verpleegkundige is vereist voor Dosis Aantal flacons nodig Flacons van 5 mg : Flacons van 35 mg : Volume steriel water voor injecties toe te voegen Totaal volume Fabrazyme -oplossing op te zuigen Let op: Uit een flacon van 35 mg mag slechts 7.0 ml opgezogen worden, uit een flacon van 5 mg, slechts 1.0 ml Totaal Volume NaCl 0,9 % waaraan de Fabrazyme -oplossing wordt toegevoegd Let op : mag niet minder dan 125 ml zijn; indien dosis dit toch vereist : infusie verdelen over meerdere zakken NaCl 0,9 % Niet vergeten aub: De verdunde oplossing moet tijdens de toediening gefilterd worden door een inlinefilter van 0,2 µ met lage proteïnebinding. Duur van de toediening 1,1 ml x (aantal 5 mg flacons) 7,2 ml x (aantal 35 mg flacons) 1,0 ml x (aantal 5 mg flacons) :.. ml + 7,0 ml x (aantal 35 mg flacons) :...ml. ml Totaal Volume (som):...ml (=250 ml Totaal volume Fabrazyme - oplossing op te zuigen ) Indien meerdere zakken nodig : specifiëer Volume per zak : Toedieningssnelheid 19
20 Details in geval van nood : (noodmedicatie, infusiesnelheid, - In te vullen door de behandelende arts) : Acties in geval van een ernstige infusie-gerelateerde reactie : 1. Stop de infusie 2. Bel de noodtelefoon (100 of 112) 3. Bel de arts 20
21 Infusiegegevens (in te vullen door de thuisverpleegkundige en/of patiënt en/of verzorger) Datum van infusie Algemene gezondheid van de patiënt : specifieke problemen/opmerkingen Dosis Aantal flacons gebruikt Duur van de toediening Toedieningssnelheid Problemen/opmerkingen (gerelateerd aan de infusie vb. bijwerkingen) Gebruikte noodmedicatie Datum (dd-mmm-jjjj): Flacons van 5 mg :.. Flacons van 35 mg :. Datum van infusie Algemene gezondheid van de patiënt : specifieke problemen/opmerkingen Dosis Aantal flacons gebruikt Duur van de toediening Toedieningssnelheid Problemen/opmerkingen (gerelateerd aan de infusie vb. bijwerkingen) Gebruikte noodmedicatie Datum (dd-mmm-jjjj): Flacons van 5 mg :.. Flacons van 35 mg :. Voor bijkomende pagina s bel naar :
22 Infusiegegevens (in te vullen door de thuisverpleegkundige en/of patiënt en/of verzorger) Datum van infusie Algemene gezondheid van de patiënt : specifieke problemen/opmerkingen Dosis Aantal flacons gebruikt Duur van de toediening Toedieningssnelheid Problemen/opmerkingen (gerelateerd aan de infusie vb. bijwerkingen) Gebruikte noodmedicatie Datum (dd-mmm-jjjj): Flacons van 5 mg :.. Flacons van 35 mg :. Datum van infusie Algemene gezondheid van de patiënt : specifieke problemen/opmerkingen Dosis Aantal flacons gebruikt Duur van de toediening Toedieningssnelheid Problemen/opmerkingen (gerelateerd aan de infusie vb. bijwerkingen) Gebruikte noodmedicatie Datum (dd-mmm-jjjj): Flacons van 5 mg :.. Flacons van 35 mg :. Voor bijkomende pagina s: bel naar :
23 23
Thuisinfusie met Fabrazyme (agalsidase beta): Handleiding voor patiënten met de ziekte van Fabry die. thuis infusies krijgen met Fabrazyme
 Thuisinfusie met Fabrazyme (agalsidase beta): Handleiding voor patiënten met de ziekte van Fabry die thuis infusies krijgen met Fabrazyme Versie nr. 1.1: 19 september 2011 De procedures in dit document
Thuisinfusie met Fabrazyme (agalsidase beta): Handleiding voor patiënten met de ziekte van Fabry die thuis infusies krijgen met Fabrazyme Versie nr. 1.1: 19 september 2011 De procedures in dit document
CEREZYME (imiglucerase)
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CEREZYME. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CEREZYME. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
CINRYZE (C1-REMMER [HUMAAN])
![CINRYZE (C1-REMMER [HUMAAN]) CINRYZE (C1-REMMER [HUMAAN])](/thumbs/66/54698885.jpg) De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CINRYZE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CINRYZE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
INFORMATIEGIDS VOOR PATIENTEN
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
RECONSTITUTIE, DOSERING EN TOEDIENING
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VELCADE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VELCADE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
CINRYZE (C1-REMMER [HUMAAN])
![CINRYZE (C1-REMMER [HUMAAN]) CINRYZE (C1-REMMER [HUMAAN])](/thumbs/66/54698857.jpg) De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CINRYZE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CINRYZE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
RECONSTITUTIE, DOSERING EN TOEDIENING
 Additioneel risico minimalisatie materiaal betreffende bortezomib voor beroepsbeoefenaren in de gezondheidszorg Belangrijke informatie over de RECONSTITUTIE, DOSERING EN TOEDIENING van bortezomib 3,5 mg
Additioneel risico minimalisatie materiaal betreffende bortezomib voor beroepsbeoefenaren in de gezondheidszorg Belangrijke informatie over de RECONSTITUTIE, DOSERING EN TOEDIENING van bortezomib 3,5 mg
ZypAdhera. Informatie bestemd voor professionelen uit de gezondheidszorg en verpleegkundigen Risicobeleidsplan
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ZypAdhera. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ZypAdhera. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
(asfotase alfa) 40 mg/ml 100 mg/ml oplossing voor injectie (asfotase-alfa) INJECTIEHANDLEIDING. Ouders/zorgverleners van jonge patiënten
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel STRENSIQ. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel STRENSIQ. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
RECONSTITUTIE, DOSERING EN TOEDIENING
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VELCADE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VELCADE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
BROCHURE VOOR RECONSTITUTIE, DOSERING EN TOEDIENING
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Bortezomib Sandoz 3,5 mg poeder voor oplossing voor injectie. Het verplicht
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Bortezomib Sandoz 3,5 mg poeder voor oplossing voor injectie. Het verplicht
PATIËNTENHANDLEIDING VOOR ZELFINJECTIE
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel STRENSIQ. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel STRENSIQ. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Doel van dit educatief materiaal (RMA of risk minimisation activities)
 Doel van dit educatief materiaal (RMA of risk minimisation activities) Deze informatie maakt deel uit van het Belgische risicobeheerplan, dat informatiemateriaal beschikbaar stelt aan gezondheidszorgbeoefenaars
Doel van dit educatief materiaal (RMA of risk minimisation activities) Deze informatie maakt deel uit van het Belgische risicobeheerplan, dat informatiemateriaal beschikbaar stelt aan gezondheidszorgbeoefenaars
BEKNOPTE LEIDRAAD VOOR THUISTOEDIENING VAN NPLATE (ROMIPLOSTIM)
 BEKNOPTE LEIDRAAD VAN NPLATE (ROMIPLOSTIM) Voor volwassen patiënten die hebben besloten zichzelf thuis romiplostim injecties toe te dienen. De materialen in dit trainingspakket voor thuistoediening zorgen
BEKNOPTE LEIDRAAD VAN NPLATE (ROMIPLOSTIM) Voor volwassen patiënten die hebben besloten zichzelf thuis romiplostim injecties toe te dienen. De materialen in dit trainingspakket voor thuistoediening zorgen
INSTRUCTIES VOOR HET BEREIDEN EN TOEDIENEN VAN DE SOMAVERT INJECTIE
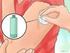 INSTRUCTIES VOOR HET BEREIDEN EN TOEDIENEN VAN DE SOMAVERT INJECTIE Inleiding In de volgende instructies wordt uitgelegd hoe SOMAVERT moet worden bereid en geïnjecteerd. Lees deze instructies aandachtig
INSTRUCTIES VOOR HET BEREIDEN EN TOEDIENEN VAN DE SOMAVERT INJECTIE Inleiding In de volgende instructies wordt uitgelegd hoe SOMAVERT moet worden bereid en geïnjecteerd. Lees deze instructies aandachtig
RECONSTITUTIE, DOSERING EN TOEDIENING
 Belangrijke informatie over de RECONSTITUTIE, DOSERING EN TOEDIENING van bortezomib 3,5 mg injectieflacon voor subcutaan (SC) en intraveneus (IV) gebruik Teva Nederland BV Swensweg 5 Postbus 552 2003 RN
Belangrijke informatie over de RECONSTITUTIE, DOSERING EN TOEDIENING van bortezomib 3,5 mg injectieflacon voor subcutaan (SC) en intraveneus (IV) gebruik Teva Nederland BV Swensweg 5 Postbus 552 2003 RN
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. AQUA STEROP AQUA STEROP FLEXO Oplosmiddel voor parenteraal gebruik. Water voor injectie
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER AQUA STEROP AQUA STEROP FLEXO Oplosmiddel voor parenteraal gebruik Water voor injectie Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER AQUA STEROP AQUA STEROP FLEXO Oplosmiddel voor parenteraal gebruik Water voor injectie Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want
Bijsluiter: informatie voor de patiënt en gebruiker. Ondexxya 200 mg poeder voor oplossing voor infusie andexanet alfa
 Bijsluiter: informatie voor de patiënt en gebruiker Ondexxya 200 mg poeder voor oplossing voor infusie andexanet alfa Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe
Bijsluiter: informatie voor de patiënt en gebruiker Ondexxya 200 mg poeder voor oplossing voor infusie andexanet alfa Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe
BIJSLUITER Atosiban Devrimed 6,75 mg/0,9 ml
 BIJSLUITER Atosiban Devrimed 6,75 mg/0,9 ml 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Atosiban Devrimed 6,75 mg/0,9 ml oplossing voor injectie Atosiban Lees goed de hele bijsluiter voordat u dit geneesmiddel
BIJSLUITER Atosiban Devrimed 6,75 mg/0,9 ml 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Atosiban Devrimed 6,75 mg/0,9 ml oplossing voor injectie Atosiban Lees goed de hele bijsluiter voordat u dit geneesmiddel
INJECTIEHANDLEIDING BETREFFENDE ASFOTASE-ALFA VOOR OUDERS EN ZORGVERLENERS VAN JONGE PATIËNTEN
 INJECTIEHANDLEIDING BETREFFENDE ASFOTASE-ALFA VOOR OUDERS EN ZORGVERLENERS VAN JONGE PATIËNTEN Lees aandachtig de bijsluiter alvorens u asfotase-alfa gebruikt. Versie 1 - januari 2018 Inleiding Deze materialen
INJECTIEHANDLEIDING BETREFFENDE ASFOTASE-ALFA VOOR OUDERS EN ZORGVERLENERS VAN JONGE PATIËNTEN Lees aandachtig de bijsluiter alvorens u asfotase-alfa gebruikt. Versie 1 - januari 2018 Inleiding Deze materialen
INFORMATIE VOOR DE PATIËNT
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Azzalure. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Azzalure. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
CEREZYME (imiglucerase) Thuisinfusie
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CEREZYME. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CEREZYME. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Het gebruik van APIDRA in injectieflacon
 EEN GIDS VOOR ALS U BEGINT MET APIDRA (insuline glulisine) 1x 10ML INJECTIEFLACON (100 Eenheden/ml) De Apidra 100 eenheden/ml oplossing voor injectie (in injectieflacon) wordt in een injectieflacon geleverd
EEN GIDS VOOR ALS U BEGINT MET APIDRA (insuline glulisine) 1x 10ML INJECTIEFLACON (100 Eenheden/ml) De Apidra 100 eenheden/ml oplossing voor injectie (in injectieflacon) wordt in een injectieflacon geleverd
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER. Cerezyme 200 U poeder voor concentraat voor oplossing voor infusie Imiglucerase
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER Cerezyme 200 U poeder voor concentraat voor oplossing voor infusie Imiglucerase Lees de hele bijsluiter zorgvuldig door voordat u start met het gebruik van
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER Cerezyme 200 U poeder voor concentraat voor oplossing voor infusie Imiglucerase Lees de hele bijsluiter zorgvuldig door voordat u start met het gebruik van
BIJSLUITER: INFORMATIE VOOR DE PATIËNT. Aprokam 50 mg poeder voor oplossing voor injectie. Cefuroxim
 BIJSLUITER: INFORMATIE VOOR DE PATIËNT Aprokam 50 mg poeder voor oplossing voor injectie Cefuroxim Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
BIJSLUITER: INFORMATIE VOOR DE PATIËNT Aprokam 50 mg poeder voor oplossing voor injectie Cefuroxim Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
Belangrijke informatie voor zorgverleners over de nieuwe formulering van FLOLAN
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Inhoud: 1) Informatiefolder voor de patiënt (met bijgevoegde audio-cd) 2) Bijsluiter: informatie voor gebruikers
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel OZURDEX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel OZURDEX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. NaCl 0,9% B. Braun, oplossing voor infusie Natriumchloride
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER NaCl 0,9% B. Braun, oplossing voor infusie Natriumchloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER NaCl 0,9% B. Braun, oplossing voor infusie Natriumchloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
Doel van dit educatief materiaal en uitleg over de risico s
 Doel van dit educatief materiaal en uitleg over de risico s Deze informatie maakt deel uit van het Belgische risicobeheerplan, dat informatiemateriaal beschikbaar stelt aan gezondheidszorgbeoefenaars en
Doel van dit educatief materiaal en uitleg over de risico s Deze informatie maakt deel uit van het Belgische risicobeheerplan, dat informatiemateriaal beschikbaar stelt aan gezondheidszorgbeoefenaars en
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER. GlucaGen Hypokit 1 mg Poeder en oplosmiddel voor oplossing voor injectie Glucagon
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER GlucaGen Hypokit 1 mg Poeder en oplosmiddel voor oplossing voor injectie Glucagon Lees de hele bijsluiter zorgvuldig door voordat de injectie van dit geneesmiddel
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER GlucaGen Hypokit 1 mg Poeder en oplosmiddel voor oplossing voor injectie Glucagon Lees de hele bijsluiter zorgvuldig door voordat de injectie van dit geneesmiddel
Baxter S.A. Water voor Injecties (Viaflo) Samenvatting van de productkenmerken 1/6 1. NAAM VAN HET GENEESMIDDEL
 Samenvatting van de productkenmerken 1/6 1. NAAM VAN HET GENEESMIDDEL Water voor Injecties Viaflo, oplosmiddel voor parenteraal gebruik. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke zak bevat 100
Samenvatting van de productkenmerken 1/6 1. NAAM VAN HET GENEESMIDDEL Water voor Injecties Viaflo, oplosmiddel voor parenteraal gebruik. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke zak bevat 100
Selectie en training van patiënten voor thuistoediening van Nplate
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Dit verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Dit verplicht plan voor risicobeperking in België, waarvan deze informatie
BIJSLUITER. Inhoud van deze bijsluiter:
 BIJSLUITER Lees de hele bijsluiter aandachtig door, omdat er voor u belangrijke informatie in staat. Raadpleeg uw arts of apotheker als u aanvullende vragen heeft. Bewaar deze bijsluiter, misschien heeft
BIJSLUITER Lees de hele bijsluiter aandachtig door, omdat er voor u belangrijke informatie in staat. Raadpleeg uw arts of apotheker als u aanvullende vragen heeft. Bewaar deze bijsluiter, misschien heeft
Water voor injecties Bijsluiter 1/6 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Water voor injecties, oplosmiddel voor parenteraal gebruik
 Bijsluiter 1/6 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER, oplosmiddel voor parenteraal gebruik Lees goed de hele bijsluiter voordat u dit geneesmiddel toegediend gaat krijgen want er staat belangrijke informatie
Bijsluiter 1/6 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER, oplosmiddel voor parenteraal gebruik Lees goed de hele bijsluiter voordat u dit geneesmiddel toegediend gaat krijgen want er staat belangrijke informatie
Hygiënische voorzorgsmaatregelen
 Hygiënische voorzorgsmaatregelen Strikte aseptische richtlijnen in overeenstemming met het gangbare protocol binnen uw instelling dienen opgevolgd te worden, voor elke manipulatie van een poortkatheter.
Hygiënische voorzorgsmaatregelen Strikte aseptische richtlijnen in overeenstemming met het gangbare protocol binnen uw instelling dienen opgevolgd te worden, voor elke manipulatie van een poortkatheter.
B. Braun Access Port Systems Easypump
 B. Braun Access Port Systems Easypump Elastomeer infuuspompje Patiënteninformatie Inhoud Inleiding 3 Productomschrijving 4 Woordenlijst 5 Inhoud Bewaren van een gevulde Easypump 6 Hoe sluit u de Easypump
B. Braun Access Port Systems Easypump Elastomeer infuuspompje Patiënteninformatie Inhoud Inleiding 3 Productomschrijving 4 Woordenlijst 5 Inhoud Bewaren van een gevulde Easypump 6 Hoe sluit u de Easypump
Bijsluiter: informatie voor de gebruiker. Replagal, 1 mg/ml, concentraat voor oplossing voor infusie Agalsidase alfa
 Bijsluiter: informatie voor de gebruiker Replagal, 1 mg/ml, concentraat voor oplossing voor infusie Agalsidase alfa Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat
Bijsluiter: informatie voor de gebruiker Replagal, 1 mg/ml, concentraat voor oplossing voor infusie Agalsidase alfa Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat
RECONSTITUTIE, DOSERING EN TOEDIENING
 Risico minimalisatie - materiaal over de risico s van bortezomib voor beroepsbeoefenaren in de gezondheidszorg Belangrijke informatie over de RECONSTITUTIE, DOSERING EN TOEDIENING van Bortezomib 3,5 mg
Risico minimalisatie - materiaal over de risico s van bortezomib voor beroepsbeoefenaren in de gezondheidszorg Belangrijke informatie over de RECONSTITUTIE, DOSERING EN TOEDIENING van Bortezomib 3,5 mg
BIJSLUITER 1. WAT IS DAFALGAN VOLWASSENEN 600 MG EN WAARVOOR WORDT HET GEBRUIKT?
 BIJSLUITER Lees de hele bijsluiter aandachtig door, omdat er voor u belangrijke informatie in staat. Raadpleeg uw arts of apotheker als u aanvullende vragen heeft. Bewaar deze bijsluiter, misschien heeft
BIJSLUITER Lees de hele bijsluiter aandachtig door, omdat er voor u belangrijke informatie in staat. Raadpleeg uw arts of apotheker als u aanvullende vragen heeft. Bewaar deze bijsluiter, misschien heeft
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Cluvot 250 IE Cluvot 1250 IE Poeder en oplosmiddel voor oplossing voor injectie of infusie. Humane plasmastollingsfactor XIII-concentraat Dit geneesmiddel is onderworpen
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Cluvot 250 IE Cluvot 1250 IE Poeder en oplosmiddel voor oplossing voor injectie of infusie. Humane plasmastollingsfactor XIII-concentraat Dit geneesmiddel is onderworpen
Hickmankatheter: informatie voor de thuiszorg
 Hickmankatheter: informatie voor de thuiszorg Beste patiënt, Voor uw behandeling werd beslist om een Hickmankatheter te plaatsen. Deze folder biedt u een eerste antwoord op uw vragen. Ook wensen we uw
Hickmankatheter: informatie voor de thuiszorg Beste patiënt, Voor uw behandeling werd beslist om een Hickmankatheter te plaatsen. Deze folder biedt u een eerste antwoord op uw vragen. Ook wensen we uw
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Glucose 5% g/v, oplossing voor infusie Glucosemonohydraat
 BIJSLUITER 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Glucose 5% g/v, oplossing voor infusie Glucosemonohydraat Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
BIJSLUITER 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Glucose 5% g/v, oplossing voor infusie Glucosemonohydraat Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKERS. Natriumchloride CF 9 mg/ml, injectievloeistof (natriumchloride)
 1.3.1.3 Package leaflet 1.3.1.3-1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKERS Natriumchloride CF 9 mg/ml, injectievloeistof (natriumchloride) Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat
1.3.1.3 Package leaflet 1.3.1.3-1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKERS Natriumchloride CF 9 mg/ml, injectievloeistof (natriumchloride) Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat
Titratiegids voor patiënten
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan hetin de handel brengen van het geneesmiddel Uptravi. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan hetin de handel brengen van het geneesmiddel Uptravi. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
1. WAT IS ORGALUTRAN EN WAARVOOR WORDT HET GEBRUIKT?
 In deze bijsluiter komen de volgende onderdelen aan bod: 1. Wat is Orgalutran en waarvoor wordt het gebruikt? 2. Wat u moet weten voordat u Orgalutran gebruikt 3. Hoe wordt Orgalutran gebruikt? 4. Mogelijke
In deze bijsluiter komen de volgende onderdelen aan bod: 1. Wat is Orgalutran en waarvoor wordt het gebruikt? 2. Wat u moet weten voordat u Orgalutran gebruikt 3. Hoe wordt Orgalutran gebruikt? 4. Mogelijke
BIJSLUITER: INFORMATIE VOOR GEBRUIKERS. VISINE 0,5 mg/ml oogdruppels, oplossing. Tetryzolinehydrochloride
 BIJSLUITER: INFORMATIE VOOR GEBRUIKERS VISINE 0,5 mg/ml oogdruppels, oplossing Tetryzolinehydrochloride Lees goed de hele bijsluiter, want deze bevat belangrijke informatie Dit geneesmiddel kunt u zonder
BIJSLUITER: INFORMATIE VOOR GEBRUIKERS VISINE 0,5 mg/ml oogdruppels, oplossing Tetryzolinehydrochloride Lees goed de hele bijsluiter, want deze bevat belangrijke informatie Dit geneesmiddel kunt u zonder
2. WANNEER MAG U DIT MIDDEL NIET GEBRUIKEN OF MOET U ER EXTRA VOORZICHTIG MEE ZIJN?
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Nefrocarnit 1000 mg/5 ml injectievloeistof 1000 mg/5 ml injectievloeistof Werkzame stof: 200 mg/ml levocarnitine Lees goed de hele bijsluiter voordat u dit geneesmiddel
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Nefrocarnit 1000 mg/5 ml injectievloeistof 1000 mg/5 ml injectievloeistof Werkzame stof: 200 mg/ml levocarnitine Lees goed de hele bijsluiter voordat u dit geneesmiddel
STAPPENGIDS VOOR BEREIDING EN TOEDIENING VAN DE NPLATE (ROMIPLOSTIM)-INJECTIE
 STAPPENGIDS VOOR BEREIDING EN TOEDIENING VAN DE NPLATE (ROMIPLOSTIM)-INJECTIE Een illustratief hulpmiddel voor het thuis toedienen van romiplostim Dit boekje leidt u langs alle stappen die u moet uitvoeren
STAPPENGIDS VOOR BEREIDING EN TOEDIENING VAN DE NPLATE (ROMIPLOSTIM)-INJECTIE Een illustratief hulpmiddel voor het thuis toedienen van romiplostim Dit boekje leidt u langs alle stappen die u moet uitvoeren
Een illustratief hulpmiddel voor het thuis toedienen van Nplate
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Dit verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Dit verplicht plan voor risicobeperking in België, waarvan deze informatie
BYDUREON 2 mg poeder en oplosmiddel voor suspensie voor injectie met verlengde afgifte
 INSTRUCTIES VOOR DE GEBRUIKER Uw stap voor stap handleiding BYDUREON 2 mg poeder en oplosmiddel voor suspensie voor injectie met verlengde afgifte Heeft u vragen over het gebruik van BYDUREON? Zie de veel
INSTRUCTIES VOOR DE GEBRUIKER Uw stap voor stap handleiding BYDUREON 2 mg poeder en oplosmiddel voor suspensie voor injectie met verlengde afgifte Heeft u vragen over het gebruik van BYDUREON? Zie de veel
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER. Novaban 2 mg/2 ml, oplossing voor injectie en infusie Tropisetron
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER 2 mg/2 ml, oplossing voor injectie en infusie Tropisetron Lees de hele bijsluiter zorgvuldig door voordat u start met het gebruik van. - Bewaar deze bijsluiter.
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER 2 mg/2 ml, oplossing voor injectie en infusie Tropisetron Lees de hele bijsluiter zorgvuldig door voordat u start met het gebruik van. - Bewaar deze bijsluiter.
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Uro-tainer chloorhexidinediacetaat 1:5000, spoelvloeistof voor blaas- en katheterspoeling Chloorhexidinediacetaat Lees goed de hele bijsluiter voordat u dit geneesmiddel
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Uro-tainer chloorhexidinediacetaat 1:5000, spoelvloeistof voor blaas- en katheterspoeling Chloorhexidinediacetaat Lees goed de hele bijsluiter voordat u dit geneesmiddel
SELECTIE EN TRAINING VAN VOLWASSEN* PATIËNTEN VOOR THUISTOEDIENING VAN NPLATE (ROMIPLOSTIM)
 SELECTIE EN TRAINING VAN VOLWASSEN* PATIËNTEN VOOR THUISTOEDIENING VAN NPLATE (ROMIPLOSTIM) * Zelftoediening van romiplostim is niet toegestaan voor kinderen. Selectie en training van volwassen patiënten
SELECTIE EN TRAINING VAN VOLWASSEN* PATIËNTEN VOOR THUISTOEDIENING VAN NPLATE (ROMIPLOSTIM) * Zelftoediening van romiplostim is niet toegestaan voor kinderen. Selectie en training van volwassen patiënten
Checklist voor voorschrijvers
 De Nederlandse en Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Jext. Het verplicht plan voor risicobeperking in Nederland en
De Nederlandse en Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Jext. Het verplicht plan voor risicobeperking in Nederland en
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Paracetamol Mylan 500 mg tabletten Paracetamol
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Paracetamol Mylan 500 mg tabletten Paracetamol Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Paracetamol Mylan 500 mg tabletten Paracetamol Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER GlucaGen HypoKit 1 mg (1 IE), poeder en oplosmiddel voor oplossing voor injectie Glucagonhydrochloride
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER GlucaGen HypoKit 1 mg (1 IE), poeder en oplosmiddel voor oplossing voor injectie Glucagonhydrochloride Lees de hele bijsluiter zorgvuldig door voordat deze
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER GlucaGen HypoKit 1 mg (1 IE), poeder en oplosmiddel voor oplossing voor injectie Glucagonhydrochloride Lees de hele bijsluiter zorgvuldig door voordat deze
FLOLAN INFORMATIEGIDS VOOR PATIENTEN - FLOLAN
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Informatieboekje voor patiënten Wat u moet weten
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VOLIBRIS. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VOLIBRIS. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Bijsluiter: informatie voor de gebruiker. VPRIV 400 eenheden poeder voor oplossing voor infusie velaglucerase alfa
 Bijsluiter: informatie voor de gebruiker VPRIV 400 eenheden poeder voor oplossing voor infusie velaglucerase alfa Lees goed de hele bijsluiter voordat dit geneesmiddel wordt gebruikt want er staat belangrijke
Bijsluiter: informatie voor de gebruiker VPRIV 400 eenheden poeder voor oplossing voor infusie velaglucerase alfa Lees goed de hele bijsluiter voordat dit geneesmiddel wordt gebruikt want er staat belangrijke
OptiPen Pro 1. informatiebrochure
 OptiPen Pro 1 informatiebrochure INHOUDSOPGAVE OptiPen Pro 1 instructies 4 Voordat u Lantus toedient met de OptiPen Pro 1 7 Het toedienen van Lantus /Apidra met de OptiPen Pro 1 8 Algemene aanwijzingen
OptiPen Pro 1 informatiebrochure INHOUDSOPGAVE OptiPen Pro 1 instructies 4 Voordat u Lantus toedient met de OptiPen Pro 1 7 Het toedienen van Lantus /Apidra met de OptiPen Pro 1 8 Algemene aanwijzingen
Educatieve PrEP-brochure voor risicopersonen
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Emtricitabine/ Tenofovirdisoproxil Mylan 200 mg/245 mg filmomhulde tabletten.
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Emtricitabine/ Tenofovirdisoproxil Mylan 200 mg/245 mg filmomhulde tabletten.
Instructies voor bereiding van Risperdal Consta
 Instructies voor bereiding van Risperdal Consta De Risperdal Consta kit Risperdal Consta wordt geleverd in een kit, die alle componenten bevat die nodig zijn om een dosis toe te dienen. Risperdal Consta
Instructies voor bereiding van Risperdal Consta De Risperdal Consta kit Risperdal Consta wordt geleverd in een kit, die alle componenten bevat die nodig zijn om een dosis toe te dienen. Risperdal Consta
Therapeutische indicaties en behandelschema s van bortezomib voor de behandeling van multipel myeloom
 Indicatie 3 bortezomib voor behandeling van multipel myeloom Bortezomib als monotherapie of in combinatie met gepegyleerd liposomaal doxorubicine of dexamethason is geïndiceerd voor de behandeling van
Indicatie 3 bortezomib voor behandeling van multipel myeloom Bortezomib als monotherapie of in combinatie met gepegyleerd liposomaal doxorubicine of dexamethason is geïndiceerd voor de behandeling van
SoloStar. informatiebrochure
 SoloStar informatiebrochure 2 Inhoudsopgave Bewaren 4 Belangrijke informatie voor gebruik van de SoloStar 5 Leer uw SoloStar kennen 6 Stap 1. Controleer uw insuline 7 Stap 2. Bevestigen van de naald 7
SoloStar informatiebrochure 2 Inhoudsopgave Bewaren 4 Belangrijke informatie voor gebruik van de SoloStar 5 Leer uw SoloStar kennen 6 Stap 1. Controleer uw insuline 7 Stap 2. Bevestigen van de naald 7
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Apotel 10 mg/ml, oplossing voor infusie Paracetamol
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Apotel 10 mg/ml, oplossing voor infusie Paracetamol Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Apotel 10 mg/ml, oplossing voor infusie Paracetamol Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
dagziekenhuis inwendige geneeskunde Zoledroninezuur
 dagziekenhuis inwendige geneeskunde Zoledroninezuur Inhoud Zoledroninezuur 3 Voorbereiding 3 Rijvaardigheid en gebruik van machines 3 Gebruik bij ouderen 4 Uitzonderingen bij gebruik 4 Combinatie met andere
dagziekenhuis inwendige geneeskunde Zoledroninezuur Inhoud Zoledroninezuur 3 Voorbereiding 3 Rijvaardigheid en gebruik van machines 3 Gebruik bij ouderen 4 Uitzonderingen bij gebruik 4 Combinatie met andere
EDUCATIEVE INFORMATIE VOOR PATIËNTEN
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel BOCOUTURE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel BOCOUTURE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER NATRICLO 585 mg/10ml NATRICLO 1g/10ml NATRICLO 2g/10ml NATRICLO 3g/10ml NATRICLO 4g/20ml NATRICLO 6g/20ml Concentraat voor oplossing voor infusie Natriumchloride
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER NATRICLO 585 mg/10ml NATRICLO 1g/10ml NATRICLO 2g/10ml NATRICLO 3g/10ml NATRICLO 4g/20ml NATRICLO 6g/20ml Concentraat voor oplossing voor infusie Natriumchloride
Patiënteninformatie. Therapie met FOLFUSOR
 Patiënteninformatie Therapie met FOLFUSOR Inhoud Inhoud... 2 Inleiding... 3 Omschrijving van uw therapie met een folfusor pomp.... 4 Hoe ziet een folfusor pomp eruit?... 4 Hoe werkt de folfusorpomp?...
Patiënteninformatie Therapie met FOLFUSOR Inhoud Inhoud... 2 Inleiding... 3 Omschrijving van uw therapie met een folfusor pomp.... 4 Hoe ziet een folfusor pomp eruit?... 4 Hoe werkt de folfusorpomp?...
Methotrexaat (MTX) bij de ziekte van Crohn
 Methotrexaat (MTX) bij de ziekte van Crohn Ziekenhuis Gelderse Vallei Uw behandelend arts en/of verpleegkundige specialist heeft met u gesproken over het gebruik van Methotrexaat (MTX). In deze folder
Methotrexaat (MTX) bij de ziekte van Crohn Ziekenhuis Gelderse Vallei Uw behandelend arts en/of verpleegkundige specialist heeft met u gesproken over het gebruik van Methotrexaat (MTX). In deze folder
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Loperamide EG 2 mg capsules, hard. Loperamidehydrochloride
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Loperamide EG 2 mg capsules, hard Loperamidehydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat innemen want er staat belangrijke informatie
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Loperamide EG 2 mg capsules, hard Loperamidehydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat innemen want er staat belangrijke informatie
Thiamini hydrochloridum 100 mg/ml, oplossing voor injectie thiaminehydrochloride
 1.3.1 : Bijsluiter Bladzijde : 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Thiamini hydrochloridum 100 mg/ml, thiaminehydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
1.3.1 : Bijsluiter Bladzijde : 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Thiamini hydrochloridum 100 mg/ml, thiaminehydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
Gebruikershandleiding. Taltz 80mg oplossing voor injectie in voorgevulde injectiespuit. Ixekizumab
 Gebruikershandleiding Taltz 80mg oplossing voor injectie in voorgevulde injectiespuit Ixekizumab Voordat u uw voorgevulde injectiespuit gebruikt: Belangrijk om te weten Lees voordat u de Taltz voorgevulde
Gebruikershandleiding Taltz 80mg oplossing voor injectie in voorgevulde injectiespuit Ixekizumab Voordat u uw voorgevulde injectiespuit gebruikt: Belangrijk om te weten Lees voordat u de Taltz voorgevulde
BIJSLUITER: INFORMATIE VOOR DE PATIËNT
 BIJSLUITER: INFORMATIE VOOR DE PATIËNT, gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt want er staat belangrijke informatie voor u in. Bewaar deze bijsluiter. Misschien heeft
BIJSLUITER: INFORMATIE VOOR DE PATIËNT, gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt want er staat belangrijke informatie voor u in. Bewaar deze bijsluiter. Misschien heeft
Methotrexaat (MTX) bij de ziekte van Crohn MDL
 Methotrexaat (MTX) bij de ziekte van Crohn MDL Inhoudsopgave Algemeen...4 Werking...4 Gebruik...5 Bijwerkingen...6 Foliumzuur...6 Aanvullende informatie...7 Zwangerschap en borstvoeding...7 Tot slot...8
Methotrexaat (MTX) bij de ziekte van Crohn MDL Inhoudsopgave Algemeen...4 Werking...4 Gebruik...5 Bijwerkingen...6 Foliumzuur...6 Aanvullende informatie...7 Zwangerschap en borstvoeding...7 Tot slot...8
Educatieve PrEP-brochure voor risicopersonen
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Emtricitabin/ Tenofovir Disoproxil Sandoz. Het verplicht plan voor risicobeperking
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Emtricitabin/ Tenofovir Disoproxil Sandoz. Het verplicht plan voor risicobeperking
BIJSLUITER: INFORMATIE VOOR DE PATIËNT. FLUORESCEINE 10% Faure oplossing voor injectie natriumfluoresceïne
 BIJSLUITER: INFORMATIE VOOR DE PATIËNT FLUORESCEINE 10% Faure oplossing voor injectie natriumfluoresceïne Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat belangrijke
BIJSLUITER: INFORMATIE VOOR DE PATIËNT FLUORESCEINE 10% Faure oplossing voor injectie natriumfluoresceïne Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat belangrijke
NutropinAq Pen. instructies voor gebruik samen met NutropinAq
 NutropinAq Pen instructies voor gebruik samen met NutropinAq INJECTEER HET GENEESMIDDEL UITSLUITEND NADAT U MET UW ARTS OF VERPLEEGKUNDIGE DE JUISTE TECHNIEK GOED HEEFT GEOEFEND. Let op: Lees de onderstaande
NutropinAq Pen instructies voor gebruik samen met NutropinAq INJECTEER HET GENEESMIDDEL UITSLUITEND NADAT U MET UW ARTS OF VERPLEEGKUNDIGE DE JUISTE TECHNIEK GOED HEEFT GEOEFEND. Let op: Lees de onderstaande
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Patiëntenfolder
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
VALDOXAN. (agomelatine) Informatie voor beroepsbeoefenaren in de gezondheidszorg: Aanbevelingen met betrekking tot:
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Valdoxan 25 mg. Het verplicht plan voor risicobeperking in België, waarvan deze
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Valdoxan 25 mg. Het verplicht plan voor risicobeperking in België, waarvan deze
Bijsluiter: informatie voor de gebruiker. Glucose 5% B. Braun, oplossing voor infusie Glucose.monohydraat
 Bijsluiter: informatie voor de gebruiker Glucose 5% B. Braun, oplossing voor infusie Glucose.monohydraat Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat belangrijke
Bijsluiter: informatie voor de gebruiker Glucose 5% B. Braun, oplossing voor infusie Glucose.monohydraat Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat belangrijke
Risico minimalisatie materiaal betreffende testosteronundecanoaat voor beroepsbeoefenaren in de gezondheidszorg
 Risico minimalisatie materiaal betreffende testosteronundecanoaat voor beroepsbeoefenaren in de gezondheidszorg De risico minimalisatie materialen voor testosteronundecanoaat zijn beoordeeld door het College
Risico minimalisatie materiaal betreffende testosteronundecanoaat voor beroepsbeoefenaren in de gezondheidszorg De risico minimalisatie materialen voor testosteronundecanoaat zijn beoordeeld door het College
De ampullen bevatten de bestanddelen: natriumcarboxymethylcellulose, mannitol en water.
 Sandostatine LAR Novartis Pharma B.V. Postbus 241 6800 LZ Arnhem Telefoon 026-37 82 111 Informatie voor de patiënt Lees de bijsluiter regelmatig vóór gebruik, ook als u Sandostatine LAR al enige tijd gebruikt.
Sandostatine LAR Novartis Pharma B.V. Postbus 241 6800 LZ Arnhem Telefoon 026-37 82 111 Informatie voor de patiënt Lees de bijsluiter regelmatig vóór gebruik, ook als u Sandostatine LAR al enige tijd gebruikt.
YERVOY. (ipilimumab) Concentraat voor oplossing voor infusie Dit geneesmiddel is onderworpen aan aanvullende monitoring.
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Een injectie Menopur maakt u zelf klaar, waarna u het middel inspuit in de buikplooi.
 Prikinstructie Menopur Algemeen: Menopur is een preparaat dat humaan menopauzaal gonadotrofine (hmg) bevat. Doel: stimuleren van de groei en rijping van follikels in de eierstokken Dosering: individueel.
Prikinstructie Menopur Algemeen: Menopur is een preparaat dat humaan menopauzaal gonadotrofine (hmg) bevat. Doel: stimuleren van de groei en rijping van follikels in de eierstokken Dosering: individueel.
BIJSLUITER: INFORMATIE VOOR GEBRUIKERS. MYCOSTEN 80 mg/g nagellak. Ciclopirox
 BIJSLUITER: INFORMATIE VOOR GEBRUIKERS MYCOSTEN 80 mg/g nagellak Ciclopirox Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor u.gebruik
BIJSLUITER: INFORMATIE VOOR GEBRUIKERS MYCOSTEN 80 mg/g nagellak Ciclopirox Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor u.gebruik
Maag-Darm-Leverziekten. Instructie zelf toedienen van Methotrexaat (MTX)
 Afdeling: Maag-Darm-Leverziekten Onderwerp: Instructie zelf toedienen van Methotrexaat (MTX) Zelf toedienen van Methotrexaat door patiënt of mantelzorger In overleg met uw behandelend arts is besloten
Afdeling: Maag-Darm-Leverziekten Onderwerp: Instructie zelf toedienen van Methotrexaat (MTX) Zelf toedienen van Methotrexaat door patiënt of mantelzorger In overleg met uw behandelend arts is besloten
INSTRUCTIEBROCHURE. voor mensen die Metoject 50 mg/ml gebruiken
 INSTRUCTIEBROCHURE voor mensen die Metoject 50 mg/ml gebruiken Inhoud Pagina Inleiding 3 Hoe wordt Metoject 50 mg/ml gebruikt? 4 Het vermijden van plaatselijke huidirritatie 7 Het vermijden van verharding
INSTRUCTIEBROCHURE voor mensen die Metoject 50 mg/ml gebruiken Inhoud Pagina Inleiding 3 Hoe wordt Metoject 50 mg/ml gebruikt? 4 Het vermijden van plaatselijke huidirritatie 7 Het vermijden van verharding
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Water voor injecties Fresenius Kabi oplosmiddel voor parenteraal gebruik. Water voor injecties
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Water voor injecties Fresenius Kabi oplosmiddel voor parenteraal gebruik Water voor injecties Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Water voor injecties Fresenius Kabi oplosmiddel voor parenteraal gebruik Water voor injecties Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
Workshop verzorgingstechnieken. 24 maart 2017
 Workshop verzorgingstechnieken 24 maart 2017 Wat betekent PICC PICC staat voor peripherally inserted central catheter ofwel perifeer ingebrachte centraal veneuze katheter. Een PICC is een katheter vervaardigd
Workshop verzorgingstechnieken 24 maart 2017 Wat betekent PICC PICC staat voor peripherally inserted central catheter ofwel perifeer ingebrachte centraal veneuze katheter. Een PICC is een katheter vervaardigd
Gebruikershandleiding. Taltz 80mg oplossing voor injectie in voorgevulde pen. Ixekizumab
 Gebruikershandleiding Taltz 80mg oplossing voor injectie in voorgevulde pen Ixekizumab Voordat u uw voorgevulde pen gebruikt: Belangrijk om te weten Lees voordat u de Taltz voorgevulde pen gaat gebruiken
Gebruikershandleiding Taltz 80mg oplossing voor injectie in voorgevulde pen Ixekizumab Voordat u uw voorgevulde pen gebruikt: Belangrijk om te weten Lees voordat u de Taltz voorgevulde pen gaat gebruiken
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER. Helico STATE, poeder voor drank 100 mg/sachet. { 13 C-Ureum}
 BIJSLUITER 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER Helico STATE, poeder voor drank 100 mg/sachet. { 13 C-Ureum} Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken - Bewaar deze
BIJSLUITER 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER Helico STATE, poeder voor drank 100 mg/sachet. { 13 C-Ureum} Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken - Bewaar deze
Behandeling met Entyvio (vedolizumab)
 Praat met uw arts als u graag meer informatie wilt over de behandeling met. Behandeling met (vedolizumab) Meer informatie Deze brochure is een aanvulling op de bijsluiter. We hopen dat de meeste vragen
Praat met uw arts als u graag meer informatie wilt over de behandeling met. Behandeling met (vedolizumab) Meer informatie Deze brochure is een aanvulling op de bijsluiter. We hopen dat de meeste vragen
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Belangrijke informatie voor beroepsbeoefenaren
 De gezondheidsautoriteiten van de Europese Unie hebben het in de handel brengen van het geneesmiddel Kadcyla verbonden aan bepaalde voorwaarden. Het verplichte farmacovigilantieplan ter minimalisatie van
De gezondheidsautoriteiten van de Europese Unie hebben het in de handel brengen van het geneesmiddel Kadcyla verbonden aan bepaalde voorwaarden. Het verplichte farmacovigilantieplan ter minimalisatie van
VORMING. Praktische informatie voor de arts-patiënt. patiëntenbegeleiding bij het opstarten van
 VORMING Praktische informatie voor de arts-patiënt patiëntenbegeleiding bij het opstarten van Simponi Praktische richtlijnen voor het gebruik van Simponi Simponi (golimumab) is een humane monoklonale antistof.
VORMING Praktische informatie voor de arts-patiënt patiëntenbegeleiding bij het opstarten van Simponi Praktische richtlijnen voor het gebruik van Simponi Simponi (golimumab) is een humane monoklonale antistof.
BIJSLUITER: INFORMATIE VOOR DE PATIËNT
 BIJSLUITER: INFORMATIE VOOR DE PATIËNT citroen zuigtabletten amylmetacresol dichloorbenzylalcohol Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat innemen want er staat belangrijke informatie
BIJSLUITER: INFORMATIE VOOR DE PATIËNT citroen zuigtabletten amylmetacresol dichloorbenzylalcohol Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat innemen want er staat belangrijke informatie
Bijsluiter: informatie voor de gebruiker. Simdax 2,5 mg/ml concentraat voor oplossing voor infusie levosimendan
 Bijsluiter: informatie voor de gebruiker Simdax 2,5 mg/ml concentraat voor oplossing voor infusie levosimendan Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
Bijsluiter: informatie voor de gebruiker Simdax 2,5 mg/ml concentraat voor oplossing voor infusie levosimendan Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
BIJLAGE III ETIKETTERING EN BIJSLUITER
 BIJLAGE III ETIKETTERING EN BIJSLUITER B. BIJSLUITER BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER ZOVIRAX Labialis 50 mg/g, crème Aciclovir Lees goed de hele bijsluiter, want deze bevat belangrijke informatie
BIJLAGE III ETIKETTERING EN BIJSLUITER B. BIJSLUITER BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER ZOVIRAX Labialis 50 mg/g, crème Aciclovir Lees goed de hele bijsluiter, want deze bevat belangrijke informatie
Bijsluiter: Informatie voor de gebruiker. GlucaGen 1 mg Poeder en oplosmiddel voor oplossing voor injectie Glucagon
 Bijsluiter: Informatie voor de gebruiker GlucaGen 1 mg Poeder en oplosmiddel voor oplossing voor injectie Glucagon Lees goed de hele bijsluiter voordat men u dit geneesmiddel geeft want er staat belangrijke
Bijsluiter: Informatie voor de gebruiker GlucaGen 1 mg Poeder en oplosmiddel voor oplossing voor injectie Glucagon Lees goed de hele bijsluiter voordat men u dit geneesmiddel geeft want er staat belangrijke
