Nieuwsbulletin van de Nederlandse Vereniging voor Hepatologie. Bestuurszaken Basaal onderzoek Klinisch onderzoek Mededelingen Nieuws Congresagenda
|
|
|
- Karel Maes
- 8 jaren geleden
- Aantal bezoeken:
Transcriptie
1 Nieuwsbulletin van de Nederlandse Vereniging voor Hepatologie I N H O U D Bestuurszaken Basaal onderzoek Klinisch onderzoek Mededelingen Nieuws Congresagenda Jaargang 34, nr.1 Februari 2010
2 Colofon Congresagenda 2010 Nieuwsbrief van de Nederlandse Vereniging voor Hepatologie. Verschijnt vier maal per jaar. De Nederlandse Vereniging voor Hepatologie is opgericht op 30 september Redactie: Dr. L.C. Baak Mw. Dr. S.W.C. van Mil Mw. M. J. van Gijtenbeek Redactie adres: Redactie Nieuwsbrief NVH Postbus RR Haarlem Fax: Bestuur: Prof. dr. H.L.A. Janssen, voorzitter Prof. dr. K.N. Faber, secretaris Dr. J.T. Brouwer, penningmeester Dr. L.C. Baak Prof. dr. J.P.H. Drenth Dr. R.J. de Knegt Dr. G.H. Koek Mw. Dr. S.W.C. van Mil Dr. S.W.M. Olde Damink Dr. C.C. Paulusma Organisatoren van congressen/symposia worden verzocht data tijdig door te geven en zoveel mogelijk rekening te houden met reeds geplande activiteiten. 17 maart Cursorisch onderwijs in Maag-Darm-Leverziekten. Locatie: Koningshof te Veldhoven Inlichtingen: Secretariaat NVMDL, Postbus 657, 2003 RR Haarlem Tel.: , Fax: maart Voorjaarsvergadering NVGE-NVH incl. DEGH-meeting Locatie: Koningshof te Veldhoven Inlichtingen: Secretariaat NVGE, Postbus 657, 2003 RR Haarlem Tel.: , Fax: april 2e ELPAT congres Locatie: World Trade Centre, Rotterdam 8-11 juni Dutch Liver Week / Cursus Klinische Hepatologie Locatie: NH Carlton Amsterdam Inlichtingen: 6 oktober Cursorisch onderwijs in Maag-Darm- Leverziekten. Locatie: Koningshof te Veldhoven Inlichtingen: zie 17 maart oktober Najaarsvergadering NVGE- NVH Locatie: Koningshof te Veldhoven Inlichtingen: zie maart oktober - 2 november The Liver Meeting van AASLD Locatie: Boston, Massachusetts Inlichtingen: Lidmaatschap: aanmeldingen bij de secretaris: Prof. dr. K.N. Faber Postbus RR Haarlem Fax: Omslagfoto: (A) ERCP met multipele ophelderingen in de galwegen passend bij stolsels. (B) Bloed komend uit de papil van vater passend bij hemobilie. Overname van gegevens uit deze nieuwsbrief is toegestaan met bronvermelding. Correspondentie kan worden gestuurd naar het redactieadres. De redactie behoudt zich het recht voor om te bewerken. Vormgeving: Drukkerij Bijto BV, Enkhuizen ISSN nr.: Deze uitgave is mogelijk gemaakt door Bristol-Myers Squibb, Gilead, Roche en Schering Plough Inhoud Congresagenda 2 Bestuurszaken 3 - Van de secretaris Sectie Basale Hepatologie 4 - Dutch Experimental Gastroenterology and Hepatology (DEGH) Meeting Introduction Invited Speakers - Hoe gaat het eigenlijk met... Coen Paulusma Sectie Klinische Hepatologie 7 - In de schijnwerpers: Wendingen in Leiden - Hepatology Alert Lever Casus 11 - Partiële biliaire diversie als behandeling van PFIC type 1 en PFIC type 2 Lever van eigen bodem 14 - Bespreking van artikelen in het afgelopen kwartaal gepubliceerd door NVH-leden Mededelingen 16 - Inschrijving voorjaarsvergadering Informatie bestellen leerboek leverziekten - NVH onderzoeksprijs - Agenda casuïstische conferenties te Utrecht - NVGE-NVH reisstipendia - Lidmaatschap NVH - Proefschriftsponsoring Nieuws 17 Proefschriftsamenvatting 19 - Samenvatting proefschrift Esther van Straaten Metabolic programming of lipid metabolism: Effects of prenatal pharmacological and nutriational interference Proefschriftenservice 19 2
3 Bestuurszaken Van de secretaris Jaarverslag NVH 2009 Het ei is gelegd! Zo zou je 2009 kunnen betitelen, in ieder geval als je de notulen van de NVH bestuursvergaderingen van de afgelopen 10 jaar bekijkt. Wat daar namelijk voordurend in voorbij komt is het onderwerp Nederlands Leerboek Hepatologie. Vele NVH bestuurders hebben hier dus over gediscussieerd, onderwerpen geselecteerd, wetenschappers uitgenodigd voor manuscripten, sponsorgelden geregeld, onderhandelingen met de uitgever gevoerd en wat al niet meer zij. Als redelijk recent NVH bestuurslid heb ik met bewondering de daadkracht van de redacteuren van dit boek aanschouwd. Harry Janssen, Joost Drenth en Bart van Hoek hebben dit project in 2008 ter harte genomen en dit in een jaar succesvol afgerond. Dit jaar (in 2009 dus) is het verschenen onder de titel Leverziekten. Wetenschappers en specialisten uit Nederland en Vlaanderen hebben hieraan meegewerkt en dit 230 pagina s dikke, rijk geïllustreerde state-ofthe-art overzichtswerk is een warm aanbevolen aanvulling voor uw boekenkast. Voor wie dit boek nog niet in bezit heeft: in de bijlagen treft u een bestelformulier aan. Het boek wordt direct na ontvangst van het formulier aan u verzonden. Groei! Dat zit nog steeds in het aantal NVH leden. Zaten we vorig jaar rond de 400, nu zitten we alweer op 470. Dus bijna net zo goed als de AEX, maar dan zonder de 2008 dip. Daarbij is dit een krachtige mix van klinici en basale wetenschappers. Gezond! Zo kan je de financiële positie van de NVH omschrijven. De NVH penningen zijn in goede handen bij Hans Brouwer, jullie penningmeester. Hans heeft de hoofdsponsoren bereid gevonden hun steun aan de NVH ook de komende jaren voort te zetten. Hiermee kan de NVH met een gerust hart de activiteiten voort zetten en daar waar kansen liggen, zelfs uitbouwen. Krant! Saskia van Mil, Bert Baak en Marie José van Gijtenbeek vormen het nieuwe redactie trio van ons nieuwsbulletin Lever. De toegenomen kopij heeft de afgelopen edities geleid tot een uitbreiding van het aantal pagina s dat vooralsnog van blijvende aard lijkt te zijn. Dit komt onder andere door de nieuwe rubriek: Lever van eigen bodem. Hierin krijgen NVH leden de mogelijkheid om hun vers-gepubliceerde werk met een impact factor van >4 kort toe te lichten. In dit nummer staan zelfs 15 artikelen vermeld. Het gaat dus goed met lever onderzoek in Nederland en ons nieuwsblad. Samen! Centrale activiteiten van de NVH zijn de organisatie van de voor- (Dutch Experimental Gastroenterology and Hepatology (DEGH) meeting) en najaarsvergaderingen en de Levercursus. Na de DEGH in 2008, is de levercursus in 2009 in een nieuw jasje ge- stoken, namelijk een Dutch Liver Week. Dit zijn belangrijke ontmoetingsmomenten voor NVH leden, niet alleen om elkaar bij te praten over nieuwe wetenschappelijke en klinische onderwerpen, maar ook om elkaar persoonlijk beter te leren kennen. De eerste edities van de DEGH en de DLW zijn (zeer) succesvol verlopen en het NVH bestuur maakt zich sterk om deze bijeenkomsten ook in de komende jaren blijvend een interessant platform te maken voor haar leden. Toppers! Sinds 2009 heeft de NVH een aantal prijzen voor wetenschappers die zich recent of al langere tijd hebben onderscheiden door publicaties in de Hepatologie. De Young Hepatologist werden tijdens de voorjaarsvergadering voor het eerst uitgereikt aan Martijn Hoeke (Basale Hepatologie) en Erik Buster (Klinische Hepatologie) voor top publicaties in Ook dit jaar zal de NVH deze aanmoedigingprijzen uitreiken. Daarnaast zal dit jaar voor het eerst de Distinghuished Hepatologist prijs toegekend worden. De selectie procedure voor deze 2 à 3-jaarlijkse prijs voor een actieve wetenschapper met een bijzondere track record in de Hepatologie is inmiddels afgerond. In de DEGH bijeenkomst tijdens de voorjaarsvergadering zal deze uitgereikt worden aan... (u bent op 19 maart van harte welkom in de Baroniezaal). Nieuw bloed! Dat heeft een gezonde organisatie steeds nodig en ook het NVH bestuur is in 2009 voorzien van nieuw bloed. Karel van Erpecum (Utrecht) en Jaap Kwekkeboom (Rotterdam) hebben zich 6 jaar lang ingezet voor de NVH. Het reikt te ver om al hun inspanningen hier te benoemen, maar een bedankje in dit jaarverslag is zeker op zijn plek: Bedankt! Saskia van Mil (Utrecht) en Bert Baak (Amsterdam) hebben hun plekken overgenomen en zijn inmiddels op verschillende terreinen actief voor de NVH. Zij ervaren nu ook dat het wel wat tijd kost, maar dat je als bestuurslid ook echt invloed hebt op de NVH-activiteiten. We zullen dus nog van hen horen. Succes! Spinnen! Voor andere zaken is het goed om niet al teveel nieuw bloed in een organisatie te hebben. Heel veel organisatorische zaken worden in overleg, of zelfs ongemerkt door het secretariaat in Haarlem geregeld. Ze zorgen voor een strakke planning van de voor- en najaarsvergaderingen, het drukken van Lever, het innen van de contributie (inclusief herinneringen) en noem maar op. Met andere woorden: de noodzakelijke maar zeer vriendelijke spin(nen) in het web. Bedankt Marie José van Gijtenbeek en Marja Weber. Muziek? De NVH kan als organisatie met vertrouwen naar de toekomst kijken. Maar de muziek, die wordt gemaakt door haar leden. Ik wil u daarom een gezond en succesvol 2010 wensen en wij hopen u bij één van de NVH bijeenkomsten te ontmoeten. Klaas Nico Faber, secretaris NVH Laatste nieuws Bij deze Lever vindt u een bestelformulier voor het Leerboek Leverziekten. Het boek is op voorraad en kan binnen enkele dagen worden toegezonden. 3
4 Sectie Basale Hepatologie coördinatoren: - Coen Paulusma en Saskia van Mil Dutch Experimental Gastroenterology and Hepatology (DEGH) meeting maart, NH KONINGSHOF Veldhoven Tijdens de voorjaarsvergadering van de Nederlandse verenigingen voor Hepatologie en Gastroenterologie op 18 en 19 maart 2010 in Veldhoven zal voor de derde keer de DEGH-meeting gehouden worden. Er zijn voor deze meeting 78 abstracts ingestuurd! De 36 beste abstracts werden geselecteerd voor mondelinge presentatie, waarvan één tijdens de plenaire (President Select) sessie. De auteurs van de andere abstracts zullen de gelegenheid krijgen hun onderzoek toe te lichten tijdens de posterrondes. Aan het einde van de meeting zullen prijzen voor de twee beste abstracts en twee beste posters worden uitgereikt. Tesamen met de vier uitmuntende buitenlandse sprekers, zie hieronder, belooft deze 3e DEGH-meeting een wetenschappelijke bijeenkomst van hoge kwaliteit te worden. We heten alle leden en andere belangstellenden van harte welkom! International Invited Speakers Sponsored by the joint Dutch Experimental Gastroenterology and Hepatology (DEGH) Sections Thursday, March 18th, Baroniezaal h Michael Trauner is Professor of Experimental and Molecular Hepatology at the University of Graz, Austria. In his lecture he will discuss the molecular regulation and pharmacological interventions of transport systems in cholestatic and fatty liver disease h Prof. dr. Jörg-Dieter Schulzke is head of the Department of Pathophy-siology and Enteral Nutrition of the Charite University (Benjamin Franklin) in Berlin. Schulzke will entertain the topic of molecular regulation of Tight-Junctions in the Intestinal Epithelium and their role in the development of GI disease. Friday, March 19th, Baroniezaal h Prof. dr. Scott L. Friedman is Chief of the Division of Liver Diseases at Mount Sinai School of Medicine in New York and 2009 AASLD President. Friedman was the first to isolate and characterize the hepatic stellate cell, the key cell type responsible for scar production in liver. He will discuss molecular mechanisms underlying the development of liver fibrosis h Prof. dr. Elke Cario is working at the Department of Gastroenterology and Hepatology of the University Hospital in Essen. Her specific research interest and topic of the lecture will be on Toll-like receptors in Inflammatory Bowel Disease (IBD). 4
5 Hoe gaat het eigenlijk met.? In deze aflevering van Hoe gaat het eigenlijk met...? komt basaal hepatoloog Coen Paulusma aan het woord, staflid op het Tytgat Instituut voor Darm en Leveronderzoek en NVH-bestuurslid. Hij vertelt over hoe zijn research-carriere tot nu toe is verlopen, en wat zijn plannen zijn voor de toekomst. Met deze rubriek hopen we een goed beeld te krijgen van diverse binnenlandse en buitenlandse hepatologische onder-zoeksgroepen. In het bijzonder hopen we dat jonge onderzoekers door het lezen over de carrière stappen van meer gevorderde basale hepatologen, enthousiast raken voor een verdere carrière in onderzoek en in de hepatologie in het bijzonder. Sinds een aantal jaar werk ik als staflid op het Tytgat Instituut voor Darm- en Leveronderzoek, het voormalig AMC Lever Centrum. Eén van de zwaartepunten van onze onderzoeksgroep is het bestuderen van de pathofysiologie van galvorming. Hierbij kijken we vooral naar transportprocessen die plaatsvinden in het canaliculaire (apicale) membraan van de hepatocyt. Dit membraandomein huist een groot aantal transporteiwitten die essentieel zijn voor de vorming van hepatische gal, bijvoorbeeld BSEP (dé transporter voor galzouten), MDR3 (fosfatidylcholine), MRP2 (bilirubine), ABCG5/G8 heterodimeer (cholesterol), en ATP8B1 (fosfatidylserine). Mutaties in de genen die coderen voor bovengenoemde eiwitten kunnen leiden tot erfelijke cholestatische leverziekten (Figuur 1), welke gekenmerkt worden door een verstoorde uitscheiding van galzouten van de lever naar de gal. De AIO Mijn voorliefde voor dit onderzoek stamt uit de tijd dat ik promotieonderzoek deed bij de afdeling Experimentele Hepatologie van het AMC in de groep van Ronald Oude Elferink. Hier beleefde ik mijn eerste euforie moment, een zeldzaam-voorkomende overdreven, maar zeer kortdurende, mate van opwinding. Peter Jansen en Oude Elferink waren jaren bezig geweest met de functionele karakterisering van een transportdefect in de zogenaamde TR- rat, een natuurlijk voorkomende rattestam met een defect in de uitscheiding van geconjugeerd bilirubine van de lever naar de gal. De TRrat was een diermodel voor het humane Dubin-Johnson syndroom, een zeldzame goedaardige (?) leverafwijking gekarakteriseerd door een chronische geconjugeerde hyperbilirubinemie. Welk(e) eiwit(ten) hiervoor verantwoordelijk was (waren) was onbekend. Aangezien de substraatspecificiteit nogal breed was noemden zij dit transportsysteem cmoat, voor canaliculaire multispecifieke organische anion transporter. Het was mijn taak om het gen (of genen) voor deze cmoat te identificeren. In die tijd was net gepubliceerd dat sommige drugresistente tumorcellen een eiwit overexpresseerden (Multidrug Resistance-Associated Protein 1, MRP1) dat overlappende substraatspecificiteit vertoonde met cmoat. Het eerste stukje cdna sequentie (213-bp) geïsoleerd uit rat hepatocyten vertoonde homologie met MRP1 en leidde tot grote opwinding en gaf genoeg energie om 2 jaar later het volledige cdna voor cmoat, of zoals het nu heet, MRP2, te isoleren (4918-bp). De postdoc Na mijn promotie had ik genoeg van levers en transporters en belandde ik als postdoc in Rotterdam bij de afdeling Celbiologie en Genetica alwaar ik me verdiept heb in de mechanismen die ten grondslag liggen aan het herstel van dubbelstrengsbreuken in DNA via homologe recombinatie. Dat was een enerverende tijd met veel hardcore cel- en biochemie in een zeer stimulerende wetenschappelijke omgeving. Euforiemomenten als wetenschapper heb ik hier niet gekend, wel diverse in mijn (toentertijd) uit de hand gelopen hobby als muzikant, maar dat terzijde. In die tijd heb ik ook een voorliefde voor de stad Rotterdam en de mentaliteit en humor van de autochtone Rotterdammer ontwikkeld (sorry, Amsterdammers). Na mijn eerste postdoc ben ik door Oude Elferink teruggehaald vanuit Rotterdam. Daar onderzocht ik als postdoc de oorzaak van de cholestase in patiënten met ATP8B1 deficiëntie. Mutaties in het ATP8B1 gen leiden tot een spectrum van cholestatische leverziekten variërend van progressief (progressieve familiaire intrahepatische cholestase type 1, PFIC1) tot episodisch (benigne recurrente intrahepatische cholestase type 1, BRIC1, en zwangerschapscholestase). De afgelopen jaren heb ik veel onderzoek gedaan naar de galvorming in ATP8B1 deficiënte muizen. We hebben laten zien dat ATP8B1 belangrijk is voor het in stand houden van de structuur van het canaliculaire membraan, en daarmee essentieel is in de bescherming van dit membraandomein tegen de zeepwerking van galzouten. De aangedane membraanstructuur in ATP8B1 deficiënte muizen leidt tot een grotere gevoeligheid voor galzout-geinduceerde extractie van o.a. cholesterol. Dit laatste leidt tot een aangedane activiteit van transporteiwitten in dit membraan, waaronder BSEP, waarmee wij de cholestase in patiënten konden verklaren. Ik heb ook laten zien dat ATP8B1 een chaperonne-eiwit (CDC50A) nodig heeft om vanuit het endoplasmatisch reticulum op het celmembraan te komen en daar functioneert als een fosfatidylserine flippase, een eiwit dat het transport van fosfatidylserine van het buitenblad naar het binnenblad van de membraan dubbellaag verzorgt. Zeven jaar in een notendop. Zeven jaar van frustratie, euforie, bloed, zweet, tranen, 13 papers en 2 kinderen. Toptijd! De toekomst Recentelijk heeft mijn AIO Dineke Folmer laten zien waarom sommige mutaties in ATP8B1 leiden tot PFIC1 en anderen tot het mildere BRIC1 en momenteel bestudeert mijn andere AIO, Vincent van der Mark, de etiologie van de diarree die in veel PFIC1/ BRIC1 patiënten wordt waargenomen. Dankzij een subsidie van de Maag Lever Darm Stichting ben ik bezig om muismodellen te genereren voor erfelijke cholestatische leverziekten die qua ziektebeeld een betere gelijkenis vertonen met patiënten. In tegenstelling tot mensen, zijn muizen zeer goed in staat om de toxische, hydrofobe, galzouten te ontgiften. Om dit te omzeilen maken we muismodellen voor PFIC1-3 (zie figuur 1) die geen galzouten kunnen ontgiften. Vervolgens installeren we in deze muizen een humane galzout pool. In deze muizen willen we het ziekteverloop van de PFICs bestuderen. Aangezien milde mutaties in deze genen kunnen leiden tot een verhoogde kans op diverse lever- en galweg geassocieerde afwijkingen, zoals zwangerschapscholestase, ontsteking van de galwegen, galstenen en hepatocellulair carcinoom, zijn deze muismodellen breed toepasbaar. Tevens bestudeer ik nieuwe, voor de lever relevante ATP8B1 homologen (er zijn 13 homologen welke tot op heden nauwelijks bestudeerd zijn), en de cellulaire rol van CDC50 eiwitten in relatie tot deze homologen. Uit giststudies is naar voren gekomen dat de familie van eiwitten waar ATP8B1 toe 5
6 CHRONISCHE HEPATITIS B Levenslange therapie of herstel van chronische hepatitis B? Hepatitis vraagt om een krachtige aanpak Zie voor meer productinformatie elders in dit blad. I
7 Verkort Curriculum vitae 1965 Geboren te Sittard Studie Farmacie, Rijksuniversiteit Groningen Studie Biologie, Rijksuniversiteit Utrecht Promotie bij de afdeling Experimentele Hepatologie, AMC, Amsterdam. Co-promotor Ronald Oude Elferink; Promotores Guido Tytgat en Piet Borst Postdoc bij de afdeling Celbiologie en Genetica, Jan Hoeijmakers/Roland Kanaar; Erasmus Universiteit, Rotterdam Postdoc in het AMC Lever Centrum; Ronald Oude Elferink 2006-heden Staflid Tytgat Instituut voor Darm- en Leveronderzoek 3. Paulusma CC, Groen A, Kunne C, Ho-Mok KS, Spijkerboer AL, de Waart DR, Hoek FJ, Vreeling H, Hoeben KA, van Marle J, Pawlikowska L, Bull LN, Hofmann AF, Knisely AS and Oude Elferink RPJ (2006) ATP8B1 deficiency reduces resistance of the canalicular membrane to hydrophobic bile salts and impairs bile salt transport. Hepatology 44: CC Paulusma, MJC Kothe, CTM Bakker, PJ Bosma, I van Bokhoven, J van Marle, U Bolder, GNJ Tytgat, RPJ Oude Elferink (2000) Zonal down-regulation and redistribution of the multidrug resistance protein 2 during bile duct ligation in rat liver. Hepatology 31: CC Paulusma, PJ Bosma, GJR Zaman, CTM Bakker, M Otter, GL Scheffer, RJ Scheper, P Borst, RPJ Oude Elferink (1996) Congenital jaundice in rats with a mutation in a multidrug resistanceassociated protein gene. Science 271: behoort belangrijk is voor de vorming van transportblaasjes, een proces dat essentieel is voor eiwit, lipide, en voedingsstoffen transport in de cel. Geen gemakkelijk onderzoek, maar wel uitdagend. Op naar de volgende enerverende 7 jaar! Geselecteerde publicaties: 1. Folmer DE, van der Mark VA, Ho-Mok KS, Oude Elferink RPJ, Paulusma CC (2009) Differential effects of progressive familial intrahepatic cholestasis type 1 and benign recurrent intrahepatic cholestasis type 1 mutations on canalicular localization of ATP8B1. Hepatology 50(5): Paulusma CC, Folmer DE, Ho-Mok KS, de Waart DR, Hilarius P, Verhoeven AJ, Oude Elferink RPJ (2008) ATP8B1 requires an accessory protein for endoplasmic reticulum exit and plasma membrane lipid flippase activity. Hepatology 47: 268. Figuur: Zeer schematische weergave van 2 hepatocyten die een canaliculair lumen (geel) omsluiten. Weergegeven zijn enkele ATP-afhankelijke transporteiwitten in het canaliculaire membraan die belangrijk zijn voor galvorming. Aan de linkerzijde de eiwitnamen met substraten tussen haken. De pijlen geven de richting van substraattransport aan. Aan de rechterzijde de (cholestatische) leverziekten/syndromen die veroorzaakt worden als gevolg van deficiëntie van betreffende activiteit. PFIC, progressieve familiaire intrahepatische cholestase; BRIC, benigne recurrente intrahepatische cholestase; ICP, zwangerschapscholestase (intrahepatic cholestasis of pregnancy). Sectie Klinische Hepatologie coördinatoren: - Dr. R.J. de Knegt, Rotterdam - Dr. L.C. Baak, Amsterdam In de schijnwerpers: Wendingen in Leiden Kersverse Leidse hoogleraar Maag-darm-leverziekten Bart van Hoek Laat in de middag ontmoeten we de kersverse nieuwe Leidse hoogleraar Bart van Hoek. Hij staat inmiddels geduldig te wachten, want we zijn iets later dan het ingecalculeerde Leidse kwartiertje. De MDL-afdeling lijkt intussen uitgestorven. Zijn werkkamer, die hij deelt met dr. Coenraad, is overzichtelijk. Aan de muur een paar foto s van een hard roeiende vrouw en een reproductie van El Lissitski ( Wendingen ). Onder het genot van een prima kopje koffie uit de automaat steken we van wal. Hoe is het nu in Leiden? We hebben een lastige tijd achter de rug. Op gegeven moment waren alleen Roeland Veenendaal en ik nog over als stafleden. Het was een beetje een gok om te blijven, maar het is goed afgelopen. Nu zijn we met 8 stafleden. We hebben drie speerpunten, te weten IBD, erfelijke darmtumoren en hepatologie/ levertransplantatie. Met de hele staf doen we dienst voor de MDL, met vier stafleden verrichten we de leverdiensten. Er zijn overigens op dit moment maar twee MDL-artsen met een leverprofiel. Daarnaast hebben we zelf twee nurse practitioners voor de levertransplantatie opgeleid, en dat werkt erg goed. Er staan forse bezuinigingen voor de deur. In het hele LUMC moeten 600 mensen weg. Ik heb echter goede hoop dat we de dans enigszins ontspringen, aangezien we de laatste tijd al veel veranderingen hebben doorgevoerd. Het Leidse wereldje bevalt me overigens goed. Vergeleken met Maastricht heeft het een veel academischer milieu. Wij geven meer gespecialiseerde zorg, in Maastricht deed men veel klinische basiszorg. Wel is onze organisatie nogal stro- 7
8 perig. Daar kan nog wel winst gehaald worden. We proberen een goede communicatie en samenwerking te hebben met de klinieken in de omgeving, te weten het Diakonessenhuis Leiden en het Rijnland Ziekenhuis in Leiderdorp. De opleiding doen we samen met het Haga Ziekenhuis in Den Haag. Verder houden we, naast specialisten nascholing, regelmatig bijeenkomsten voor de huisartsen in de buurt. En dan nu hoogleraar Sinds 1 december 2009 ben ik benoemd tot hoogleraar Maag-darmleverziekten in het bijzonder de Hepatologie. Het belangrijkste is dat ik mijn werk kan blijven doen, zoals ik dat gewend was. Het is een mix van scopiëren, (poli)kliniek en research/onderwijs. Als levertransplantatiecentrum geven we de assistenten veel hepatologische bagage mee en verzorgen we ook het aandachtsgebied hepatologie in de MDL-opleiding. Ik scopieer nog steeds alles, maar de nadruk ligt op varices en ERCP s. Voor de research hebben we een trialbureau en twee levertrial nurses. We hebben vier promovendi bij de leverziekten rondlopen. We participeren en initiëren fase II en III studies voor HCV. Met een fase I studie hebben we achter het net gevist, die is naar Amsterdam gegaan. Verder spelen we een rol in het landelijke cohort voor autoimmuun hepatitis. Andere wetenschappelijke ambities betreffen de levertransplantatie. Helaas hebben we in Nederland een fors donortekort. Ook het niet bezwaar systeem zal het aanbod van levers niet verhogen. Vandaar dat we in Leiden in 2001 van start zijn gegaan met de zogenaamde non-heart-beating procedures. Dat lijkt goed te gaan. Wel zien we wat meer galwegproblemen achteraf. In Leiden doen we ook auxiliaire levertransplantaties bij acuut leverfalen en metabole stoornissen, een erfenis van Onno Terpstra. In samenwerking met de afdeling Chirurgie vergelijken we de uitkomsten met de gebruikelijke orthotope procedures. Verder richten we ons op het verbeteren van de preservatie van de donor-levers. Ook doen we onderzoek naar de innate immunity, want deze speelt een grote rol bij infectiegevoeligheid post transplantatie. Met dertig transplantaties per jaar doen we het goed, kwalitatief zitten we boven het Europese niveau. De leverpoli en kliniek hebben we beter georganiseerd, zodat we ook weer bij zijn met de brieven. Tevens hebben we CV Bart van Hoek juni Geboren te Voorbrug gymnasium B Thorbecke Lyceum, Arnhem Studie geneeskunde Groningen Specialisatie Interne geneeskunde Groningen (prof. dr. E. Mandema, prof. dr. W. Reitsma) 1989 Proefschrift Clinical monitoring of autoimmune chronic active hepatitis (prof. dr. C.H. Gips, prof. dr. T.H. The, dr. A.J.K. Grond, Dr. C.G.M. Kallenberg) Fellow Surgery research en Advanced Clinical hepatology, Mayo Clinic, Rochester, USA Specialisatie Gastroenterologie, Maastricht (prof. dr. R. Stockbrugger) heden Staflid afdeling MDL LUMC Leiden december benoeming tot hoogleraar MDL in het bijzonder Hepatologie, LUMC Leiden Gehuwd met Beryl A. Flikweert, 2 kinderen een zorgpad HCC op de poli geopend. Dit maakt de wachttijden kort en onze zorg laagdrempeliger en patiëntvriendelijker. Wat kan je vertellen over je buitenlandse werkervaring? Na mijn promotie in Groningen wilde ik graag een tijdje naar het buitenland. Uiteindelijk heb ik gekozen voor de Mayo Clinics. Ten eerste, omdat daar veel bekendheid was met mijn promotieonderwerp, autoimmuun hepatitis. Ten tweede, omdat via Ruud Krom een extra ingang aanwezig was naar de transplantatieafdeling. Ik ben er twee jaar gebleven, eerst een jaar research, daarna een jaar klinische hepatologie. Tijdens mijn Groningse jaren had ik het Amerikaanse Artsexamen afgelegd, dus ik kon in de Mayo ook klinisch actief zijn. Door die twee jaar is mijn blik verruimd, je maakte kennis met een andere cultuur. Alles was mogelijk, van basaal onderzoek tot toegepast klinisch onderzoek. Nadeel vond ik wel de defensieve geneeskunde en de grote mate van bureaucratie. Ik denk dat je kunt zeggen dat de Amerikanen een groter doorzettingsvermogen hebben dan de Europeanen, maar dat ze in Europa creatiever zijn. Ik heb er veel geleerd, zelfs van mijn teleurstellingen. Zo heb ik in mijn eerste jaar veel tijd besteed aan de isolatie van intrahepatische galgangcellen. Dat lukte niet goed. Ik ben toen naar Pittsburgh gegaan om te kijken hoe ze dat daar deden. Bleken ze daar, zonder het zelf te beseffen, extra hepatische galgangcellen te hebben geïsoleerd. Uiteindelijk is het niet tot een publicatie gekomen en zijn we net ingehaald door Birmingham, waar de celisolatie wel was gelukt. Ik heb daarna o.a. nog aan een chronische rejectie gewerkt, wat toen een groot probleem was. Na twee jaar ben ik teruggegaan. Ik geniet van het culturele leven in Europa en ik houd van Nederland, want mijn familie en vrienden zitten hier. Overigens heb ik veel contacten overgehouden aan mijn Amerikaanse tijd. En nu privé Ik ben sinds 1979 samen met mijn vrouw Beryl. Ze heeft Spaans en kunstgeschiedenis gestudeerd. Momenteel werkt ze als freelance, eerst bij een cultureel organisatiebureau en nu in de Lakenhal. Daar begeleidt ze verschillende kunstprojecten en verzorgt ze rondleidingen voor klassen. Daarnaast is ze een hartstochtelijk roeister. Zelf ben ik daar ook weer mee begonnen. We hebben een zoon van 18 in de examenklas van het VWO en een dochter van 19 die in het eerste jaar zit van haar studie Psychobiologie aan de UVA. Ik wist ook niet dat dat bestond, maar ben erg blij met haar keuze. Ik waardeer het doorzettingsvermogen en enthousiasme van mijn kinderen enorm. Ik heb altijd geprobeerd om rond uur thuis te zijn, zodat we gezamenlijk konden eten. Ik vind het leuk om een boek te lezen en piano te spelen, al komt dat er soms te weinig van. Ook gaan we graag naar een concert. 8
9 Samenwerking in de toekomst In Leiden is de afdeling Infectieziekten altijd zeer sterk geweest. Vanuit de levertransplantatie werken we veel samen. Natuurlijk hebben we ook veel discussie over het antibiotica beleid. Verder is er overleg over de virale hepatitis. We hebben in het LUMC de afspraak dat de mono-infecties HBV en HCV voornamelijk door de MDL afdeling worden behandeld. Tenslotte gaat het hier om een orgaanziekte. Bij complicaties komen de patiënten anders toch bij de MDL-arts terecht. Bovendien is het onderdeel van onze opleiding. De hele discussie over een zogenaamd hepatitis centrum wachten we rustig af. Kwaliteit staat voorop. Onze afdeling heeft nu vier hoogleraren. (Daan Hommes, Hans Vasen, Sander van Deventer en ik). Vroeger had Leiden er maar een. Ik denk niet dat we elkaar de tent zullen uitvechten. We kunnen veel van elkaar leren. De input vanuit het AMC met betrekking tot IBD en colorectaal carcinoom is goed geïntegreerd in de afdeling. Verder hoop ik op een samenwerking tussen de leverziekten en de translationele gastro-enterologie. De reorganisatie van de afdeling was spannend. Maar we hebben nieuwe impulsen gekregen en het laboratorium is weer actief. Het wordt tijd om afscheid te nemen. Het is 19.oo uur geweest en er moet gegeten worden. We lopen nog even over de afdeling. Er is veel veranderd. Te oordelen aan de appelgroene stoeltjes in de koffieruimte heeft een binnenhuisarchitect zich mogen uitleven. In Leiden is hard tegen de stroom in geroeid. Er zijn wendingen ten goede gekomen. Zelden hebben we meer toepasselijke wanddecoraties in een werkkamer gezien. Belangrijke publicaties: - Mazzaferro V, Llovet JM, Miceli R, Bhoori S, Schiavo M, Mariani L, Camerini T,Roayaie S, Schwartz ME, Grazi GL, Adam R, Neuhaus P, Salizzoni M, Bruix J, Forner A, De Carlis L, Cillo U, Burroughs AK, Troisi R, Rossi M, Gerunda GE, Lerut J, Belghiti J, Boin I, Gugenheim J, Rochling F, Van Hoek B, Majno P; on behalf of the Metroticket Investigator Study Group. Predicting survival after liver transplantation in patients with hepatocellular carcinoma beyond the Milan criteria: a retrospective, exploratory analysis. Lancet Oncol. 2009; 10(1): ten Hove WR, de Rooij BJF, van Hoek B, Kuyvenhoven JPh, Meijer MJW, van den Berg M, van der Reijden JJ, Verduyn W, Dubbeld J, Hommes DW, Lamers CBHW, Verspaget HW. MMP-2 and MMP-9 serum levels change but their gene promoter polymorphisms are not associated with late phase I/R injury or rejection after orthotopic liver transplantation. The Open Transplantation Journal, 2008, 2, Ringers J, Dubbeld J, Baranski AG, Coenraad M, Sarton E, Schaapherder AF, van Hoek B. Reuse of auxiliary liver grafts in second recipients with chronic liver disease. Am J Transplant 2007;7: Bouwman LH, Roos A, Terpstra OT, de Knijff P, van Hoek B, Verspaget HW, Berger SP, Daha MR, Frolich M, van der Slik AR, Doxiadis II, Roep BO, Schaapherder AF. Mannose binding lectin gene polymorphisms confer a major risk for severe infections after liver transplantation. Gastroenterology 2005;129: Hepatology Alert: De glazen bol bij chronische hepatitis C: van matglas naar kristal? Met peginterferon alfa/ribavirine behaalt slechts 60% van de chronische hepatitis C patiënten een blijvende virologische respons (sustained virological respons SVR). 1,2 Diverse factoren zijn geassocieerd met een blijvende klaring van het virus, maar voor de individuele patiënt is voorafgaand aan de therapie nog onvoldoende duidelijk wie er wel en wie er niet een SVR gaat behalen. Vanwege de bijwerkingen en lange behandelingsduur, zou een adequate voorspelling van non-respons vele ongemakken en kosten kunnen besparen. In potentiële responders kan het bijdragen aan de therapietrouw. Het virale genotype is momenteel de belangrijkste voorspeller voor SVR. In de voornaamste peginterferon en ribavirine studies werd 41-52% van de genotype 1 patiënten, en 76%-84% van de genotype 2/3 patiënten succesvol behandeld. 1,2 Hoewel met name de virale daling tijdens de behandeling belangrijk is voor de kans op genezing, heeft de virale lading bij aanvang ook voorspellende waarde. Naast deze virale markers zijn er nog vele andere factoren die een rol spelen, waaronder de mate van leverfibrose en/of -steatose, de aanwezigheid van insuline resistentie en de hoogte van het gamma glutamyltransferase (ggt) en ferritine. Ongunstige demografische factoren zijn een hogere BMI en leeftijd, waarbij vooral patiënten jonger dan jaar in het voordeel zijn. 3 De etniciteit is een andere belangrijke patiëntgebonden factor van invloed op de genezingskans. Vooral het negroïde ras is met SVR percentages van 19-28% duidelijk in het nadeel ten opzichte van de 39-52% in niet-negroïde patiënten. 4 Patiënten met een Zuid-Amerikaanse afkomst zitten hier tussen, met een succespercentage van 34%. 5 Aziaten klaren het virus juist vaker dan Kaukasische patiënten; respectievelijk 65% versus 45% van de genotypen 1, 2 en 3 infecties behaalt een SVR. 6 Met de recent gepubliceerde resultaten van een genoombrede associatiestudie (genome-wide association GWA) lijkt het raciale verschil gedeeltelijk verklaard. In het toonaangevende tijdschrift Nature beschreven de onderzoekers namelijk een enkel nucleotide polymorfisme, gelegen nabij het voor Interferon-λ-3 coderende IL28B gen, met grote voorspellende waarde voor de uitkomst van de behandeling. 7 Homozygotie voor het Cytosine (C) allel geeft bijna 80% kans op SVR in vergelijking met 38% in heterozygote CT en 26% in homozygote TT patiënten. Opmerkelijk is dat de frequentie van het C-allel toeneemt in de rassen met betere resultaten op antivirale therapie, waarbij zelfs negroïde patiënten met het gunstige CC-genotype vaker genezen dan nietnegroïde patiënten met het ongunstige TT-genotype. De voorspellende waarde van dit specifieke polymorfisme bleek groter dan van de virale lading, mate van leverschade en etniciteit. Eveneens interessant is dat ditzelfde CC-genotype ook gepaard gaat met een gunstiger natuurlijk beloop van de infectie, aangezien deze patiënten het virus vaker spontaan klaren. 8 Hierna vonden twee andere onafhankelijk GWA-studies nog andere aan SVR geassocieerde polymorfismen in en rond het IL28B gen, waarbij eveneens belangrijke relaties met betrekking tot nonrespons op peginterferon en ribavirine worden beschreven. 9 Echter, zolang er maar één behandeling bestaat voor chronische hepatitis C blijft het nut van nieuwe positief voorspellende factoren enigszins beperkt. In de afweging om antivirale therapie te starten zijn markers met hoge positief voorspellende waarde (PVW) namelijk voor de individuele patiënt maar zelden van doorslaggevend belang. De waarde van een hoge PVW zal toenemen indien de registratie van nieuwe antivirale middelen tot diverse behandelingsstrategieën leidt. Naast het bijwerkingenprofiel, zal dan immers ook de individuele kans op genezing 9
10 per behandeling aan de basis van de therapiekeuze staan. Een belangrijk gevolg voor de huidige behandeling kan verkorting van de therapieduur zijn, zoals de virale parameters hebben laten zien.2,10 Echter de praktische implementatie van dergelijke consequenties zal lang duren door de noodzakelijke prospectieve validatie. De consequenties van factoren met een hoge negatief voorspellende waarde (NVW), waaraan eveneens een grote klinische behoefte bestaat, zouden sneller doorgevoerd kunnen worden. Noemenswaardig is dan ook dat een complexe analyse van het virale genotype diverse specifieke covariërende netwerken van aminozuren gevonden heeft, welke voor 100% gepaard gaan met nonrespons op de standaard therapie.11 Dit zijn veelbelovende resultaten, mede doordat de netwerken in meer dan 95% van de nonresponders en helemaal niet in responders aanwezig waren. Uiteraard zal validatie in een tweede cohort afgewacht moeten worden, voordat deze tijdrovende en dure techniek tot een klinisch bruikbare test kan worden ontwikkeld. Denkbaar is dat uitgebreide genetische analyses de voorspelling van de virologische respons nog verder kunnen optimaliseren en hopelijk houdt hun voorspellende waarde ook stand wanneer de directe antivirale middelen aan de huidige behandeling worden toegevoegd. Omdat de nieuwe genetische markers eveneens aanknopingspunten lijken te bieden voor het verbeteren van de antivirale behandeling, zijn ze in de toekomst mogelijk zelfs overbodig. Echter de aandacht voor de predictie van respons zal pas verdwijnen wanneer genezing dankzij adequate antivirale therapie gegarandeerd is. Verkorte Productinformatie NAAM VAN HET GENEESMIDDEL: PegIntron 50, 80, 100, 120 of 150 microgram, poeder en oplosmiddel voor oplossing voor injectie in voorgevulde pen. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING: Elke voorgevulde pen met PegIntron 50, 80, 100, 120 of 150 microgram bevat een voldoende hoeveelheid peginterferon-alfa-2b zoals gemeten op proteïnebasis in een poeder voor oplossing voor injectie, en de overeenkomstige hoeveelheid oplosmiddel om 50, 80, 100, 120 of 150 microgram in 0,5 ml peginterferon-alfa-2b te leveren wanneer opgelost zoals aanbevolen. Het actieve bestanddeel is een covalent conjugaat van recombinant interferon-alfa-2b met monomethoxy-polyethyleenglycol. De sterkte van dit product mag niet vergeleken worden met die van een andere gepegyleerde of niet-gepegyleerde proteïne van dezelfde therapeutische klasse (zie rubriek 5.1*). geproduceerd door rdna-technologie in E.coli cellen die drager zijn van een genetisch gemodificeerde plasmidehybride die een interferon-alfa-2b-gen afkomstig van menselijke leukocyten bevat. Hulpstoffen: Poeder voor oplossing voor injectie: watervrij dinatriumfosfaat, natriumdiwaterstoffosfaat dihydraat, sucrose, Polysorbaat 80. Oplosmiddel voor parenteraal gebruik: water voor injecties. PegIntron bevat 40 mg sucrose per 0,5 ml. Leverbaar volume van de pen = 0,5 ml. FARMACEUTISCHE VORM: Poeder en oplosmiddel voor oplossing voor injectie in voorgevulde pen. Wit poeder. Helder en kleurloos oplosmiddel. THERAPEUTISCHE INDICATIES: PegIntron is geïndiceerd voor de behandeling van volwassen patiënten met chronische hepatitis C die verhoogde transaminasenconcentraties hebben zonder leverdecompensatie en die positief zijn voor serum HCV-RNA of serum anti-hcv, met inbegrip van niet eerder behandelde patiënten met een co-infectie met klinisch stabiel HIV (zie rubriek 4.4*). Voor deze indicatie wordt PegIntron het beste gebruikt in combinatie met ribavirine. Deze combinatie is geïndiceerd bij niet eerder behandelde patiënten, met inbegrip van patiënten met een co-infectie met klinisch stabiel HIV en bij patiënten die niet hebben gereageerd op eerdere behandeling met interferon-alfa (gepegyleerd of niet-gepegyleerd) en combinatietherapie met ribavirine of monotherapie met interferon-alfa (zie rubriek 5.1*). Monotherapie met interferon, inclusief PegIntron, is met name geïndiceerd in geval van intolerantie of contraindicatie voor ribavirine. Zie ook de samenvatting van de productkenmerken van ribavirine wanneer PegIntron in combinatie met ribavirine gebruikt wordt. CONTRA-INDICATIES: -Overgevoeligheid voor het werkzaam bestanddeel, voor interferonen of voor één van de hulpstoffen; -Een voorgeschiedenis van een ernstige, reeds bestaande hartziekte, met inbegrip van instabiele of ongecontroleerde hartziekte, tijdens de zes voorafgaande maanden (zie rubriek 4.4*); -Ernstige verzwakkende medische toestand; -Auto-immune hepatitis of een voorgeschiedenis van een auto-immuunziekte; -Ernstige leverstoornissen of een gedecompenseerde levercirrose; -Reeds bestaande schildklieraandoening tenzij deze aandoening onder controle kan worden gehouden met een klassieke behandeling; -Epilepsie en/of stoornissen van het centraal zenuwstelsel (CZS); -Het starten van de behandeling met PegIntron is gecontraïndiceerd bij patiënten die gelijktijdig met HCV/HIV besmet zijn, en cirrose en een Child-Pugh score van 6 hebben. Combinatietherapie met ribavirine: Zie eveneens ribavirine Samenvatting van de Productkenmerken (SPC) indien PegIntron moet toegediend worden in combinatie met ribavirine bij patiënten met chronische hepatitis C. BELANGRIJKSTE WAARSCHUWINGEN: Psychiatrische effecten en centraal zenuwstelsel (CZS): Ernstige effecten op het CZS, in het bijzonder depressie, zelfmoordgedachten en zelfmoordpoging werden bij sommige patiënten waargenomen gedurende de therapie met PegIntron, en zelfs na stopzetting van de behandeling voornamelijk tijdens de follow-up periode van 6 maanden. Andere effecten op het CZS waaronder agressief gedrag (soms gericht op anderen), bipolaire stoornissen, manie, verwardheid en wijzigingen van de mentale toestand werden waargenomen met alfa-interferonen. Meer significante stupor en coma, waaronder gevallen van encefalopathie, werden waargenomen bij sommige patiënten, gewoonlijk ouderen, die behandeld werden met hogere doses voor oncologische indicaties. Zeer zelden kwamen epileptische aanvallen voor bij hoge doses interferon-alfa. Recente behandelingsrichtlijnen moeten geraadpleegd worden om na te gaan of leverbiopsie noodzakelijk is vóór het begin van de behandeling. Acute overgevoeligheid: Acute overgevoeligheidsreacties (bijvoorbeeld urticaria, angio-oedeem, bronchoconstrictie, anafylaxis) werden zelden vastgesteld tijdens een therapie met interferon-alfa-2b. Cardiovasculair systeem: Zoals met interferon-alfa-2b, moeten patiënten met een voorgeschiedenis van decompensatio cordis, myocardinfarct en/of vroegere of huidige hartritmestoornissen, die een therapie met PegIntron krijgen toegediend, nauwlettend gevolgd worden. Bij patiënten met reeds bestaande hartstoornissen is het raadzaam om voor en tijdens de behandeling een elektrocardiogram te maken. Cardiale (vooral supraventriculaire) hartritmestoornissen reageren gewoonlijk op de klassieke therapie maar kunnen een onderbreking van de therapie met PegIntron vereisen. Leverfunctie: Zoals voor alle interferonen geldt, moet ook de behandeling met PegIntron onderbroken worden bij patiënten die een verlenging van de stollingsparameters ontwikkelen, wat kan wijzen op leverdecompensatie. Koorts: Hoewel koorts geassocieerd kan zijn met de griepachtige verschijnselen die vaak worden vastgesteld tijdens de therapie met interferon, moeten andere oorzaken van aanhoudende koorts uitgesloten worden. Hydratatie: Patiënten die een therapie met PegIntron krijgen moeten adequaat gehydrateerd worden aangezien sommige patiënten die met alfa-interferonen behandeld werden hypotensie, gerelateerd aan vochtdepletie, ontwikkelden. Longafwijkingen: Longinfiltraten, pneumonitis en pneumonie, met soms fatale afloop, werden zelden waargenomen bij patiënten behandeld met interferon-alfa. Auto-immuunziekten: De ontwikkeling van auto-antilichamen en auto-immuunziekten werd gemeld tijdens de behandeling met alfa-interferonen. Patiënten met een aanleg voor het ontwikkelen van auto-immuunziekten kunnen een verhoogd risico lopen. Gevallen van het syndroom van Vogt-Koyanagi-Harada (VKH) zijn gemeld bij patiënten met chronische hepatitis C die werden behandeld met interferon. Dit syndroom is een granulomateuze inflammatoire ziekte die de ogen, het gehoorsysteem, het hersenvlies en de huid aantast. Als het VKH-syndroom wordt vermoed, moet antivirale therapie worden gestopt en corticosteroïdentherapie worden besproken (zie rubriek 4.8*). Oculaire afwijkingen: Oftalmologische aandoeningen, inclusief retinale bloedingen, wattenachtige vlekken op de retina en obstructie van de retinale arterie of ader werden in zeldzame gevallen gerapporteerd na behandeling met alfa-interferonen. Schildklierafwijkingen: Zelden ontwikkelden de patiënten die voor chronische hepatitis C met interferon-alfa behandeld werden schildklierafwijkingen, hetzij hypo- of hyperthyroïdie. Metabolische stoornissen: Hypertriglyceridemie en verergering van hypertriglyceridemie, soms ernstig, is waargenomen. HCV/HIV Co-infectie. Mitochondriale toxiciteit en lactaatacidose: Patiënten die gelijktijdig met HCV/HIV besmet zijn en een hoog-actieve antiretrovirale therapie (HAART) krijgen, kunnen een verhoogd risico lopen om lactaatacidose te ontwikkelen. Leverdecompensatie bij patiënten die gelijktijdig met HCV/HIV besmet zijn, en een gevorderde cirrose hebben: Patiënten die gelijktijdig met HCV/HIV besmet zijn, een gevorderde cirrose hebben, en HAART krijgen, kunnen een verhoogd risico lopen op leverdecompensatie en de dood. Toevoeging van alfa-interferonen alleen of in combinatie met ribavirine kan het risico bij deze deelgroep verhogen. Andere baselinefactoren bij patiënten die gelijktijdig met HCV/HIV besmet zijn, die kunnen worden geassocieerd met een hoger risico op leverdecompensatie, zijn onder andere behandeling met didanosine en verhoogde serumconcentratie van bilirubine. Hematologische afwijkingen bij patiënten die gelijktijdig met HCV/HIV besmet zijn: Patiënten die gelijktijdig met HCV/HIV besmet zijn, en die met peginterferon-alfa-2b/ribavirine behandeld worden, en HAART krijgen, kunnen een verhoogd risico lopen om hematologische afwijkingen (als neutropenie, trombocytopenie en anemie) te ontwikkelen in vergelijking met patiënten die alleen met HCV besmet zijn. Patiënten die behandeld worden met de combinatietherapie van PegIntron en ribavirine samen met zidovudine, lopen een verhoogd risico om anemie te ontwikkelen en daarom wordt gelijktijdig gebruik van deze combinatie en zidovudine niet aanbevolen (zie rubriek 4.5*). Patiënten met lage CD4tellingen: Bij patiënten die gelijktijdig met HCV/HIV besmet zijn, zijn beperkte gegevens over werkzaamheid en veiligheid (N = 25) beschikbaar bij patiënten met CD4-tellingen van minder dan 200 cellen/µl. Dentale en periodontale stoornissen: Dentale en periodontale stoornissen, die kunnen leiden tot tandverlies, werden gemeld bij patiënten die de combinatietherapie met PegIntron en ribavirine kregen. Bovendien kon een droge mond een schadelijk effect hebben op tanden en slijmvliezen van de mond tijdens langetermijnbehandeling met de combinatie van PegIntron en ribavirine. Bovendien is het mogelijk dat sommige patiënten moeten braken. Ontvangers van een orgaantransplantaat: De veiligheid en werkzaamheid van PegIntron alleen of in combinatie met ribavirine voor de behandeling van hepatitis C werden niet bestudeerd bij personen die een lever of een ander orgaan getransplanteerd kregen. Andere: Aangezien gemeld is dat interferon-alfa reeds bestaande psoriarisaandoeningen en sarcoïdose verergerde, wordt het gebruik van PegIntron bij patiënten met psoriasis of sarcoïdose alleen aangeraden als het potentiële voordeel opweegt tegen het potentiële risico. Laboratoriumbepalingen: De standaard hematologiebepalingen, het routinebloedonderzoek en een test van de schildklierfunctie moeten bij alle patiënten uitgevoerd worden vóór de therapie met PegIntron. Belangrijke informatie over enkele bestanddelen van PegIntron: Dit geneesmiddel bevat minder dan 1 mmol natrium (23 mg) per 0,7 ml, d.w.z. dat het in wezen natriumvrij is. Patiënten met zeldzame erfelijke aandoeningen zoals fructose-intolerantie, glucose-galactose malabsorptie of sucraseisomaltase insufficiëntie dienen dit geneesmiddel niet te gebruiken. BIJWERKINGEN: De meest voorkomende aan de behandeling gerelateerde bijwerkingen die gemeld werden tijdens klinische onderzoeken met PegIntron in combinatie met ribavirine, waargenomen bij meer dan de helft van de onderzoeksdeelnemers, waren hoofdpijn, vermoeidheid en reactie op de injectieplaats. Andere belangrijke bijwerkingen die gemeld werden bij meer dan 25% van de patiënten waren onder andere myalgie, koorts, asthenie, alopecia, nausea, anorexie, gewichtsverlies, depressie, prikkelbaarheid en slapeloosheid. De meest gemelde bijwerkingen waren hoofdzakelijk mild tot matig-ernstig en waren gemakkelijk te behandelen zonder dat aanpassen van de dosis of stopzetten van de therapie vereist was. Vermoeidheid, alopecia, pruritus, nausea, anorexie, gewichtsverlies, prikkelbaarheid en slapeloosheid komen opvallend minder snel voor bij patiënten die met PegIntron monotherapie werden behandeld in vergelijking met patiënten die met combinatietherapie werden behandeld. Bijwerkingen die gemeld werden tijdens klinische onderzoeken of post-marketing surveillance bij patiënten in de groep met interferon-alfa-2b, inclusief PegIntron monotherapie of PegIntron + ribavirine: Zeer vaak ( 1/10) virale infectie, gewichtsverlies, depressie, prikkelbaarheid, slapeloosheid, angst, verminderde concentratie, emotionele labiliteit, hoofdpijn, droge mond, dyspnoe, faryngitis, hoesten, braken, nausea, abdominale pijn, diarree, anorexie, alopecia, pruritus, droge huid, rash, myalgie, atralgie, pijn in spieren en skelet, ontsteking op de injectieplaats, reactie op de injectieplaats, duizeligheid, vermoeidheid, rigor, koorts, griepachtige symptomen en asthenie. Deze bijwerkingen kwamen vaak voor ( 1/100 tot < 1/10) tijdens klinische onderzoeken bij patiënten die behandeld werden met PegIntron monotherapie. Vaak ( 1/100 tot < 1/10): schimmelinfectie, bacteriële infectie, herpes simplex, otitis media, anemie, leukopenie, trombocytopenie, lymfadenopathie, hypothyroïdie, hyperthyroïdie, hypocalciëmie, hyperurikemie, dorst, aggressief gedrag, gedragsstoornis, agitatie, nervositeit, slaperigheid, slaapstoornis, abnormaal dromen, verminderd libido, apathie, verhoogde eetlust, verwarring, tremor, ataxie, neuralgie, vertigo, paresthesie, hypo-esthesie, hyperesthesie, hypertonie, migraine, toegenomen transpiratie, conjunctivitis, troebel zicht, traanklierafwijking, oogpijn, gehoorstoornis/gehoorverlies, tinnitus, palpitatie, tachycardie, hypotensie, hypertensie, syncope, flush, sinusitis, bronchitis, dysfonie, epistaxis, rhinitis, ademhalingsstoornis, nasale congestie, rinorroe, droge hoest, dyspepsie, gastro-esofageale reflux, stomatitis, ulceratieve stomatitis, bloedend tandvlees, dunne ontlasting, constipatie, flatulentie, hemorroïden, gingivitis, glossitis, dehydratie, smaakverandering, hepatomegalie, hyperbilirubinemie, psoriasis, fotosensibiliteitsreactie, maculo-papuleuze rash, dermatitis, oedeem van het aangezicht of perifeer oedeem, erythemateuze rash, eczeem, acne, furunculose, erytheem, urticaria, afwijkende haartextuur, nagelafwijking, artritis, frequent urineren, abnormale urine, amenorroe, impotentie, pijn in de borst, menorragie, menstruatiestoornissen, aandoeningen van het ovarium, vaginale aandoeningen, seksuele disfunctie (niet gespecifieerd), prostatitis, pijn op de borst, pijn in het rechterboven-kwadrant, malaise en pijn op de injectieplaats. Soms ( 1/1.000 tot < 1/100): poging tot zelfmoord, zelfmoordgedachten. Zie de volledige SPC voor bijwerkingen die zelden of zeer zelden werden gemeld of waarvan de frequentie niet bekend is. Patiënten die gelijktijdig met HCV/HIV besmet zijn: Voor patiënten die gelijktijdig met HCV/HIV besmet zijn en PegIntron in combinatie met ribavirine krijgen, waren andere bijwerkingen (die niet gemeld werden bij mono-geïnfecteerde patiënten) die gemeld werden in de studies met een frequentie van > 5%: orale candidiase (14%), verworven lipodystrofie (13%), verlaagde CD4-lymfocyten (8%), verminderde eetlust (8%), verhoogde gamma-glutamyltransferase (9%), rugpijn (5%), verhoogde bloedamylase (6%), verhoogd melkzuur in het bloed (5%), cytolytische hepatitis (6%), verhoogde lipase (6%) en pijn in de ledematen (6%). Mitochondriale toxiciteit: Mitochondriale toxiciteit en lactaatacidose zijn gemeld bij HIV-positieve patiënten die een NRTI-behandeling kregen in combinatie met ribavirine voor een gelijktijdige infectie met HCV (zie rubriek 4.4*). Laboratoriumwaarden voor patiënten die gelijktijdig met HCV/HIV besmet zijn: Hoewel hematologische toxiciteit als neutropenie, trombocytopenie en anemie vaker voorkwamen bij patiënten die gelijktijdig met HCV/HIV besmet zijn, kon het merendeel onder controle gehouden worden door dosisaanpassing en vereiste het zelden vroegtijdige stopzetting van de behandeling (zie rubriek 4.4*). Hematologische afwijkingen werden vaker gemeld bij patiënten die PegIntron in combinatie met ribavirine kregen in vergelijking met patiënten die interferon-alfa-2b in combinatie met ribavirine kregen. In Studie 1 (zie rubriek 5.1*) werd een daling in de absolute neutrofielentelling onder 500 cellen/mm3 waargenomen bij 4% (8/194) van de patiënten, en werd een daling in bloedplaatjes onder /mm3 waargenomen bij 4% (8/194) van de patiënten die PegIntron in combinatie met ribavirine kregen. Anemie (hemoglobine < 9,4 g/dl) werd gemeld bij 12% (23/194) van de patiënten die behandeld werden met PegIntron in combinatie met ribavirine. Daling in CD4-lymfocyten: Behandeling met PegIntron in combinatie met ribavirine werd geassocieerd met dalingen in het absolute aantal CD4+-cellen binnen de eerste 4 weken zonder een vermindering in het percentage CD4+-cellen. De daling in het aantal CD4+-cellen was reversibel bij dosisvermindering of stopzetten van de behandeling. Het gebruik van PegIntron in combinatie met ribavirine had geen merkbaar negatief effect op de controle van HIV-viremie tijdens de behandeling of de follow-up. Beperkte veiligheidsdata (N = 25) zijn beschikbaar bij gecoïnfecteerde patiënten met aantal CD4+-cellen < 200/µl (zie rubriek 4.4*). FARMACOTHERAPEUTISCHE GROEP: Immunostimulerende stoffen, cytokines en immunomodulerende stoffen, interferonen, peginterferonalfa-2b, ATC-code: L03AB10. AFLEVERINGSWIJZE: Receptplichtig. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN: SP Europe, Stallestraat 73, B-1180 Brussel, België. NUMMERS VAN DE VERGUNNING VOOR HET IN HANDEL BRENGEN: EU/1/00/131/ (PegIntron Pen). DATUM: 5 december Schering-Plough BV, Houten, , medicalinfo.nl@spcorp.com *Voor volledige productinformatie verwijzen wij naar de huidig goedgekeurde Samenvatting van de Productkenmerken. Adriaan J.P. van der Meer, Robert J. de Knegt, Erasmus MC, Rotterdam Referenties: 1 M. P. Manns, J. G. McHutchison, S. C. Gordon et al., Lancet 358 (9286), 958 (2001); S. J. Hadziyannis, H. Sette, Jr., T. R. Morgan et al., Annals of internal medicine 140 (5), 346 (2004). 2 M. W. Fried, M. L. Shiffman, K. R. Reddy et al., The New England journal of medicine 347 (13), 975 (2002). 3 A. Kau, J. Vermehren, and C. Sarrazin, Journal of hepatology 49 (4), 634 (2008). 4 A. J. Muir, J. D. Bornstein, and P. G. Killenberg, The New England journal of medicine 350 (22), 2265 (2004); H. S. Conjeevaram, M. W. Fried, L. J. Jeffers et al., Gastroen-terology 131 (2), 470 (2006); J. G. McHutchison, E. J. Lawitz, M. L. Shiffman et al., The New England journal of medicine 361 (6), 580 (2009). 5 M. Rodriguez-Torres, L. J. Jeffers, M. Y. Sheikh et al., The New England journal of medicine 360 (3), 257 (2009). 6 M. J. Hepburn, L. M. Hepburn, N. S. Cantu et al., The American journal of medicine 117 (3), 163 (2004); S. Missiha, J. Heathcote, T. Arenovich et al., The American journal of gastroenterology 102 (10), 2181 (2007). 7 D. Ge, J. Fellay, A. J. Thompson et al., Nature 461 (7262), 399 (2009). 8 D. L. Thomas, C. L. Thio, M. P. Martin et al., Nature 461 (7265), 798 (2009). 9 V. Suppiah, M. Moldovan, G. Ahlenstiel et al., Nature genetics 41 (10), 1100 (2009); Y. Tanaka, N. Nishida, M. Sugiyama et al., Nature genetics 41 (10), 1105 (2009). 10 J. de Bruijne, E. H. Buster, H. C. Gelderblom et al., The Netherlands journal of medicine 66 (7), 311 (2008). 11 R. Aurora, M. J. Donlin, N. A. Cannon et al., The Journal of clinical investigation 119 (1), 225 (2009). 10 VIREAD ABBREVIATED PRESCRIBING INFORMATION Presentation: Viread film-coated tablet containing 245mg of tenofovir (as fumarate), equivalent to 300mg of tenofovir fumarate, orviread 136mg ofabbreviated tenofovir. Indications: For the treatment of chronic hepatitis B (CHB), in adults with compensated liver disease, with evidence of active PRESCRIBING INFORMATION viral replication,viread persistently elevated serum alanine245mg aminotransferase (ALT) levels histological evidence of active and/orfumarate, fibrosis. Presentation: film-coated tablet containing of tenofovir (asand fumarate), equivalent to 300mg of inflammation tenofovir Inorcombination with other antiretroviral products for treatment Infected adults 18 years liver of age. Dosage Administration: 136mg of tenofovir. Indications: Formedicinal the treatment of chronic hepatitisofbhiv-1 (CHB), in adults with over compensated disease, with&evidence of active Adults: One tabletpersistently (245mg) once daily taken food.aminotransferase Children and adolescents: notand recommended. Elderly: Insufficient data are available which viral replication, elevated serumwith alanine (ALT) levels histological evidence of active inflammation and/oronfibrosis. toinmake dose recommendations for patients over the age of for 65 treatment years caution should be exercised. Not18recommended patients&with severe renal combination with other antiretroviral medicinal products of HIV-1 Infected adults over years of age. indosage Administration: impairment (creatinine clearance (CrCl) <30ml/min). No dose modification necessary in patients with mild to moderate liver disease. Optimal Adults: One tablet (245mg) once daily taken with food. Children and adolescents: not recommended. Elderly: Insufficient data are available on which duration treatment is unknown.forcontraindications: Known to tenofovir, tenofovirnot fumarate, or any ofwith thesevere excipients. to make of dose recommendations patients over the age of 65 hypersensitivity years caution should be exercised. recommended in patients renal Warnings Precautions: Renal: Renal failure andno impairment, elevated creatinine, proximal tubulopathy (including impairmentand (creatinine clearance (CrCl) <30ml/min). dose modification necessary hypophosphataemia in patients with mild and to moderate liver disease. Optimal Fanconi have been reported with the use of tenofovir fumarate in clinicaltenofovir practice. It is recommended CrClofisthe calculated in durationsyndrome) of treatment is unknown. Contraindications: Known hypersensitivity to tenofovir, fumarate, that or any excipients. all patients prior to therapy initiation and renal function monitored every 4 weeks for the first year and every 3 months thereafter. In patients at risk Warnings and Precautions: Renal: Renal failure and impairment, elevated creatinine, hypophosphataemia and proximal tubulopathy (including offanconi renal impairment, including previously experienced events while receiving dipivoxil, consideration should bein syndrome) have beenpatients reportedwho withhave the use of tenofovir renal fumarate in clinical practice. Itadefovir is recommended that CrCl is calculated given to more frequent monitoring of renal function. There are limited data4on the safety of tenofovir fumarateininpatients patientsatwith all patients prior to therapy initiation and renal function monitored every weeks for theand firstefficacy year and every 3 months thereafter. risk impaired renal function. Tenofovir should only be used inrenal these patients if the potential benefitsdipivoxil, outweighconsideration the risks. Forshould patients of renal impairment, including patients whofumarate have previously experienced events while receiving adefovir be with < 50ml/min, dosing interval be adjusted follows: moderate renal and impairment ml/min) fumarate 1 tablet every 48 hours. givencrcl to more frequentthe monitoring of renalshould function. There areaslimited data on the safety efficacy(crcl of tenofovir in patients with Severe renal impairment (CrCl < 30 ml/min) use of tenofovir fumarate is not recommended. Refer to SPC for full monitoring and dose impaired renal function. Tenofovir fumarate should only be used in these patients if the potential benefits outweigh the risks. For patients adjustment HIV Co-infection: HIV antibody be renal offered to all HBV-infected initiating tenofovir with CrCl < recommendations. 50ml/min, the dosing interval should be adjusted as testing follows:should moderate impairment (CrCl 30-49patients ml/min) before 1 tablet every 48 hours. fumarate therapy. Due< to risk ofuse development HIV resistance, fumarate should bemonitoring used as part an Severe renal impairment (CrCl 30the ml/min) of tenofovir of fumaratetenofovir is not recommended. Refer to SPC only for full andofdose appropriate combination regimen in HIV/HBV co-infected must tenofovir hasinitiating not beentenofovir proven adjustment antiretroviral recommendations. HIV Co-infection: HIV antibody testingpatients. should Patients be offered to be all advised HBV-infected patients before to prevent the risk of transmission HBV to others through sexual contact or contamination withfumarate blood and appropriate must fumarate therapy. Due oftohiv the orrisk of development of HIV resistance, tenofovir should only beprecautions used as part of be an used. Exacerbations of hepatitis Flares on treatment: Spontaneous exacerbations in CHB are relatively common. Patients with cirrhosis may be at appropriate antiretroviral combination regimen in HIV/HBV co-infected patients. Patients must be advised tenofovir has not been proven higher risk for exacerbationsofand monitored closely. However it also should noted that increase inprecautions ALT can bemust part of to prevent thehepatic risk of transmission HIVtherefore or HBV toshould othersbe through sexual contact or contamination withbe blood and appropriate be HBV duringoftherapy tenofovir. Flares after treatmentexacerbations discontinuation: exacerbations of hepatitis havewith alsocirrhosis been reported used.clearance Exacerbations hepatitiswith Flares on treatment: Spontaneous in Acute CHB are relatively common. Patients may be inat patients whoforhave discontinued hepatitis B therapy.should Hepatic function should behowever monitored at repeated withincrease both clinical higher risk hepatic exacerbations and therefore be monitored closely. it also should beintervals noted that in ALTand canlaboratory be part of follow-up for at least months with aftertenofovir. discontinuation therapy. Treatment discontinuation is not recommended in patients withbeen advanced liverin HBV clearance during6 therapy Flares of after treatment discontinuation: Acute exacerbations of hepatitis have also reported disease cirrhosis, since post-treatment of hepatitis mayshould lead tobehepatic decompensation. Co-infection C orlaboratory D: There patientsorwho have discontinued hepatitisexacerbations B therapy. Hepatic function monitored at repeated intervals with with bothhepatitis clinical and are no dataforonattheleast efficacy of tenofovir patients co-infected with hepatitis C ordiscontinuation D virus. Hepatic of tenofovir in patients follow-up 6 months after in discontinuation of therapy. Treatment is decompensation: not recommendedthe in safety patients with advanced liver with decompensated liver disease is being exacerbations studied. At present the safety thistopatient population has not been thoroughly Other: disease or cirrhosis, since post-treatment of hepatitis mayinlead hepatic decompensation. Co-infection withevaluated. hepatitis C or D:Lactic There acidosis andon lipodystrophy to SPC for recommendations regarding bone mineral density. are no data the efficacy ofrefer tenofovir in patients co-infected with hepatitismonitoring. C or D virus.decrease Hepatic decompensation: The Triple safetynucleoside/nucleotide of tenofovir in patients therapy. Mitochondrialliver dysfunction. Reactivation Syndrome. Osteonecrosis. in antiretroviral experienced patients harbouring with decompensated disease isimmune being studied. At present the safety in this patientavoid population has not been thoroughly evaluated. Other: K65R Lactic mutation.interactions: Low potential CYP450 mediated interactions withmonitoring. other medicinal products. nottriple be administered with other acidosis and lipodystrophy refer to for SPC for recommendations regarding Decrease boneviread mineralshould density. nucleoside/nucleotide medicinal products containing tenofovir fumarate Syndrome. or adefovir dipivoxil, nephrotoxic or medicinal products patients that reduce renal function therapy. Mitochondrial dysfunction. Immune Reactivation Osteonecrosis. Avoid agents in antiretroviral experienced harbouring K65R ormutation.interactions: compete for active tubular secretion. function if tenofovirwith fumarateproducts. administered with tacrolimus. Co-administration with Low potential formonitor CYP450renal mediated interactions other medicinal Viread should not be administered with other didanosine is not recommended as it may result in afumarate 40-60%or increase systemic nephrotoxic exposure to agents didanosine which may increase risk ofrenal didanosinemedicinal products containing tenofovir adefovirindipivoxil, or medicinal products thatthe reduce function related adverse events. Co-administration with 400 mg daily didanosine has been associated with significant decreases in CD4 cell counts. A or compete for active tubular secretion. Monitor renal function if tenofovir fumarate administered with tacrolimus. Co-administration with reduced dose of 250 mg didanosine administered tenofovir fumarate has been associated withmay reports of high virological didanosine is not recommended as it may result in awith 40-60% increase in systemic exposure to didanosine which increase therates risk ofofdidanosinefailure. with lopinavir/ritonavir; 30%mg increase in tenofovir has AUC.Co-administration withsignificant atazanavir/ritonavir relatedco-administration adverse events. Co-administration with 400 daily didanosine been associated with decreases decreased in CD4 cellatazanavir counts. A concentrations, increased exposureadministered to tenofovir. with Higher tenofovir concentrations tenofovirwith associated events including reduced dose ofbut250 mg didanosine tenofovir fumaratecould has potentiate been associated reports ofadverse high rates of virological renal disorders. Food haswith beenlopinavir/ritonavir; shown to enhance bioavailability of Viread. Refer to SPC for drug details fordecreased protease atazanavir inhibitors, failure. Co-administration 30%theincrease in tenofovir AUC.Co-administration with interaction atazanavir/ritonavir NRTIs, NNRTIs.but Useincreased in pregnancy andtolactation: limited clinical data on could exposed pregnancies. Risk/benefit mustevents be considered concentrations, exposure tenofovir. There Higheristenofovir concentrations potentiate tenofovir associatedratio adverse including before use in pregnancy. Avoid Side the effects: Very commonly reported adverse events hypophosphataemia, renal disorders. Food has beenbreast-feeding. shown to enhance bioavailability of Viread. Refer to SPC for drug ( 1/10): interaction details for proteasedizziness, inhibitors, diarrhoea, vomiting, nausea. Commonly reported adverse events ( 1/100, <1/10): headache, abdominal pain, abdominal ALT NRTIs, NNRTIs. Use in pregnancy and lactation: There is limited clinical dataflatulence, on exposed pregnancies. Risk/benefit ratio mustdistension, be considered increase, fatigue. Rarely reported adverse eventsside ( 1/10,000, lactic acidosis, increased transaminases, rash, renal failure, before use in pregnancy. Avoid breast-feeding. effects:<1/1,000): Very commonly reportedpancreatitis, adverse events ( 1/10): hypophosphataemia, dizziness, acute renal vomiting, failure, proximal Fanconi events syndrome, increased creatinine. rarely reported adverse (<1/10,000): acute diarrhoea, nausea.tubulopathy Commonly including reported adverse ( 1/100, <1/10): flatulence,very headache, abdominal pain, events abdominal distension, ALT tubular necrosis, dyspnoea, hepatitis, asthenia. Adverse Events of unknown frequency: Nephritis (including acute interstitial nephritis), nephrogenic increase, fatigue. Rarely reported adverse events ( 1/10,000, <1/1,000): lactic acidosis, pancreatitis, increased transaminases, rash, renal failure, diabetes insipidus, osteomalacia (both associated with proximal renal tubulopathy). In patients with generally risk factors, acute renal failure,myopathy, proximal tubulopathy including Fanconi syndrome, increased creatinine. Very rarely reported adverseacknowledged events (<1/10,000): acute advanced HIV disease or long-term exposure to combination antiretroviral therapy (CART),Nephritis cases of(including osteonecrosis been reported. tubular necrosis, dyspnoea, hepatitis, asthenia. Adverse Events of unknown frequency: acutehave interstitial nephritis),inflammatory nephrogenic reaction asymptomatic or residual opportunistic infections may in patients with severe In immunodeficiency at the acknowledged time of initiationrisk of factors, CART. diabetestoinsipidus, myopathy, osteomalacia (both associated with arise proximal renal tubulopathy). patients with generally CART has been associated with metabolic abnormalities suchantiretroviral as hypertriglyceridaemia, hypercholesterolaemia, insulin hyperglycaemia, advanced HIV disease or long-term exposure to combination therapy (CART), cases of osteonecrosis haveresistance, been reported. Inflammatory hyperlactataemia and lipodystrophy. patients withinfections CHB, exacerbations hepatitiswith during treatment may arise. Refer SPCoffor full information reaction to asymptomatic or residualinopportunistic may arise inofpatients severe immunodeficiency at thetotime initiation of CART. on adverse events. Overdosage: If overdose occurs, monitor forhypertriglyceridaemia, evidence of toxicity. Apply standard supportiveinsulin treatment if necessary. Tenofovir CART has been associated with metabolic abnormalities such as hypercholesterolaemia, resistance, hyperglycaemia, can be removed byand haemodialysis. Pharmaceutical No special precautions for storage or may handling. Package hyperlactataemia lipodystrophy. In patients withprecautions: CHB, exacerbations of hepatitis during treatment arise.legal ReferCategory: to SPC forpom. full information Quantities: Bottle ofoverdosage: 30 film coated tablets. occurs, Marketing Authorisation available from the on adverse events. If overdose monitor for evidencenumbers: of toxicity. EU/1/01/200/001Further Apply standard supportiveinformation treatment ifisnecessary. Tenofovir marketing authorisation holder: Gilead Sciences International Ltd, Granta Park, Abington, Cambridge CB21 6GT. Telephone: can be removed by haemodialysis. Pharmaceutical Precautions: No special precautions for storage or handling. Legal Category: POM. Package ukmedinfo@gilead.com SUMMARY OFAuthorisation PRODUCT CHARACTERISTICS BEFORE PRESCRIBING IN Quantities: Bottle of 30CONSULT film coatedthe tablets. Marketing numbers: EU/1/01/200/001Further information isparticularly available from the RELATION TO SIDE EFFECTS, PRECAUTIONS AND CONTRAINDICATIONS.Viread is Cambridge a registeredcb21 trademark Date of API01223 preparation: marketing authorisation holder: Gilead Sciences International Ltd, Granta Park, Abington, 6GT. Telephone: March /UKM/08-03/SM/19 ukmedinfo@gilead.com CONSULT THE SUMMARY OF PRODUCT CHARACTERISTICS BEFORE PRESCRIBING PARTICULARLY IN RELATION TO SIDE EFFECTS, PRECAUTIONS AND CONTRAINDICATIONS.Viread is a registered trademark Date of API preparation: March /UKM/08-03/SM/19 GIVD901 bijsluiter A6 ZW.indd 1 2/17/09 1:16:34 PM GIVD901 bijsluiter A6 ZW.indd 1 2/17/09 1:16:34 PM
11 Lever Casus De tweede aflevering aflevering van de nieuwe rubriek; Lever Casus. Doel van deze rubriek is om vooral de jonge maar ook de meer ervaren (klinisch) hepatologen kennis te laten maken met bijzondere en zeldzame lever casuïstiek. Een ieder die een interessante casus heeft en die in de toekomst in deze rubriek Lever Casus zou willen presenteren, is van harte uitgenodigd. Neem dan contact op met Partiële biliaire diversie als behandeling van PFIC type 1 en PFIC type 2 Janneke M. Stapelbroek Roderick H.J. Houwen Nog altijd is de behandeling van intrahepatische cholestase een grote uitdaging omdat de meeste van deze ziektebeelden niet of nauwelijks reageren op de huidige medicamenteuze therapieën. Voor een belangrijk deel van deze patiënten biedt een partiële biliaire diversie echter uitkomst. Het gunstige effect van deze ingreep is beschreven bij diverse vormen van intrahepatische cholestase, zoals PFIC type 1 en 2, en het syndroom van Alagille (1-3). Middels deze casus willen we het gunstige effect van biliaire drainage bij progressieve familiaire intrahepatische cholestase type 1 (PFIC type 1) nog eens onder de aandacht brengen. Het betreft een jongetje van een half jaar oud. Hij was a term geboren met een geboortegewicht van 4054 gram (+ 1SD). Behoudens een lichte astma bij vader zijn ouders en een ouder broertje gezond. Ouders zijn niet consanguin. Vanaf de leeftijd van 4 maanden had de patiënt heftige jeuk. Daarnaast was er sprake van een afbuigende groeicurve. Bij lichamelijk onderzoek werd een alerte, wat humeurige zuigeling gezien met een bleek vale kleur. Over zijn huid enkele excoriaties. Zijn lever was 3 cm palpabel onder de ribbenboog. Lengte 66 cm (-1 SD), gewicht 6430 gram (-2 SD). Laboratorium onderzoek toonde een geringe cholestase, met verhoogde galzouten in het serum en licht afwijkende transaminases met een normaal GGT. Bilirubine totaal 33 µmol/l (3-21), bilirubine direct 20 µmol/l (0-5), GGT 15 U/L (0-45), ASAT 108 U/L (0-51), ALAT 83 U/L (0-45), albumine 35.6 g/l ( ), galzouten 72 µmol/l (0-12), PTT 25.4 sec (13.5), APTT 75 sec (35) (normaalwaardes tussen haakjes). De combinatie van verhoogde serum transaminases en galzouten met een normaal GGT en jeuk is zeer suggestief voor een familiaire intrahepatische cholestase, m.n. voor PFIC type 1 of 2. In afwachting van de uitslag van genetische diagnostiek werd gestart met rifampicine, wat de 6α-hydroxylatie van galzuren verhoogd en dus de wateroplosbaarheid en daarmee de uitscheiding in de urine. In eerste instantie was dit effectief, verdween de jeuk en normaliseerden de serum galzoutwaarden (figuur tijdstip 1). Echter, zoals voor meer patiënten met intrahepatische cholestase was de werkzaamheid van de medicamenteuze behandeling maar van beperkte duur (figuur tijdstip 2). Middels genetisch onderzoek was de diagnose progressieve familiaire intrahepatische cholestase (PFIC) type 1 intussen gesteld. De prognose van deze aandoening wordt aanzienlijk verbeterd door het aanleggen van een cholecystojejunocutaneostoma, een zogenaamde partiële biliaire diversie (PBD). Na deze procedure worden ongeveer 80% van de galzouten door het stoma aan de buitenwereld afgegeven, en zijn niet meer beschikbaar voor reabsorptie in het terminale ileum. Bij % van de patiënten met PFIC type 1 of 2 verbetert deze behandeling de cholestase en, indien op tijd gestart, kan het progressie naar een terminaal leverfalen aanzienlijk vertragen en mogelijk zelfs voorkomen (3). Met een snel progressieve cholestase en een definitieve diagnose van PFIC type 1 werd bij deze patiënt dan ook besloten tot het aanleggen van een PBD. Hiermee normaliseerden de serum waarden van transaminases en galzouten en verdween de jeuk (figuur tijdstip 3). Op een korte terugval na, wat bleek te berusten op een disfunctionerend stoma (figuur tijdstip 4) gaat het tot op heden erg goed met patiënt en blijven de serumgalzouten stabiel rond een waarde van 50 µmol/l (figuur tijdstip 5). PFIC type 1 wordt veroorzaakt door mutaties in het ATP8B1 gen wat codeert voor het ATP8B1 eiwit (ook wel bekend als het FIC1 eiwit) (4,5). ATP8B1 is een transmembraan eiwit en wordt gevonden in de apicale membraan van epitheliale cellen zoals de hepatocyt, de enterocyt en de haarcellen in het binnenoor (6-8). Op dit moment wordt gedacht dat ATP8B1 functioneert als een fosfolipide translocase en zo bijdraagt aan een asymmetrische verdeling van fosfolipiden over de celmembraan, wat essentieel is voor tal van intracellulaire processen en de stabiliteit van de membraan zelf. In de lever leidt dit tot disfunctioneren van het galzouttransport in de hepatocyt met accumulatie van toxische galzouten; in het binnenoor kan dit leiden tot degeneratie van de haarcellen (8,9). Een klinisch moeilijk van PFIC type 1 te onderscheiden ziektebeeld is PFIC type 2, wat wordt veroorzaakt door mutaties in ABCB11 dat codeert voor de belangrijkste galzout transporter in de lever: ABCB11 (ook wel bekend als BSEP). In tegenstelling tot ATP8B1 komt ABCB11 alleen tot expressie in de canaliculaire membraan van de hepatocyt (10,11). Figuur: Serum concentratie galzouten (µmol/l). ➊ Het eerste effect van rifampicine is gunstig, ➋ echter de werkzaamheid is van beperkte duur. ➌ Na het aanleggen van een partiële biliaire drainage (PBD) normaliseren de serumwaarden van galzouten opnieuw. ➍ Ondanks een klein rebound effect bij een disfunctionerende drain, ➎ blijven de galzoutwaarden tot nu toe stabiel. 11
12 Omdat iedere patiënt telt I BEAT HEP C met de bewezen effectiviteit van PegIntron 1 Nu ook geregistreerd voor patiënten met HIV co-infectie herbehandeling van non-responders/relapsers* Actuele informatie over hepatitis op ieder gewenst moment met Zorg op maat voor uw hepatitis patiënt met Snel meer zekerheid voor uw hepatitis patiënt met Walmolen 1, 3994 DL Houten Medical Information: of medicalinfo.nl@spcorp.com * op eerdere behandeling met (peg)interferon + ribavirine Productinformatie elders in dit blad 2009-NL-76
13 Op dit moment is er geen effectieve medicamenteuze behandeling voor PFIC type 1 of 2. PBD kan, zoals hierboven beschreven, de prognose van de leverproblematiek in een belangrijke mate verbeteren, maar meestal is een levertransplantatie uiteindelijk toch onvermijdelijk. Echter, in de nabije toekomst kan het gebruik van nucleaire receptoren betrokken bij de galproductie wellicht als target voor farmaceutische interventie gebruikt worden. Deze ontwikkeling en het gebruik van chaperonnes, die de expressie van gemuteerde transporters kunnen induceren, of mutatie specifieke therapie zijn veelbelovend voor de behandeling van intrahepatische cholestase (3). Zo n behandeling is voor sommige patiënten met een specifieke mutatie in ATP8B1 misschien niet eens heel ver weg (12). Referenties (1 ) Whitington PF, Whitington GL. Partial external diversion of bile for the treatment of intractable pruritus associated with intrahepatic cholestasis. Gastroenterology 1988;95: (2) Arnell H, Bergdahl S, Papadogiannakis N, Nemeth A, Fischer B. Preoperative observations and short-term outcome after partial external biliary diversion in 13 patients with progressive familial intrahepatic cholestasis. J Pediatr Surg 2008;43: (3) Stapelbroek JM, van Erpecum KJ, Klomp LW, Houwen RH. Liver disease associated with canalicular transport defects: Current and future therapies. J Hepatol 2009 [Epub ahead of print] (4) Bull LN, van Eijk MJ, Pawlikowska L, DeYoung JA, Juijn JA, Liao M, et al. A gene encoding a P-type ATPase mutated in two forms of hereditary cholestasis. Nat Genet 1998;18: (5) Klomp LW, Vargas JC, van Mil SW, Pawlikowska L, Strautnieks SS, van Eijk MJ, et al. Characterization of mutations in ATP8B1 associated with hereditary cholestasis. Hepatology 2004;40:27-38 (6) Eppens EF, van Mil SW, De Vree JM, Kok KS, Juijn JA, Oude Elferink RP, et al. FIC1, the protein affected in two forms of hereditary cholestasis, is localized in the cholangiocyte and the canalicular membrane of the hepatocyte. J Hepatol 2001;35: (7) van Mil SW, van Oort MM, van den Berg IE, Berger R, Houwen RH, Klomp LW. Fic1 is expressed at the apical membranes of different epithelial cells in the digestive tract and is induced in the small intestine during postnatal development of mice. Pediatr Res 2004;56: (8) Stapelbroek JM, Peters TA, van Beurden DH, Curfs JH, Joosten A, Beynon AJ, et al. ATP8B1 is essential for maintaining normal hearing. Proc Natl Acad Sci U S A 2009;106: (9) Paulusma CG, Groen A, Kunne C, Ho-Mok KS, Spijkerboer AL, Rudi de WD, et al. Atp8b1 deficiency in mice reduces resistance of the canalicular membrane to hydrophobic bile salts and impairs bile salt transport. Hepatology 2006:44: (10) Strautnieks SS, Bull LN, Knisely AS, Kocoshis SA, Dahl N, Arnell H, et al. A gene encoding a liver-specific ABC transporter is mutated in progressive familial intrahepatic cholestasis. Nat Genet 1998;20: (11) Strautnieks SS, Byrne JA, Pawlikowska L, Cebecauerova D, Rayner A, Dutton L, et al. Severe bile salt export pump deficiency: 82 different ABCB11 mutations in 109 families. Gastroenterology 2008;14: (12) van der Velden LM, Stapelbroek JM, Krieger E, van den Berghe PV, Berger R, Verhulst PM. Folding defects in P-type ATP 8B1 associated with hereditary cholestasis are ameliorated by 4-phenylbutyrate. Hepatology 2010;51: References: 1. Baraclude (entecavir). Summary of Product Characteristics. February Tenney DJ et al. Longterm monitoring shows hepatitis B virus resistance to entecavir in nucleoside-naïve patients is rare through 5 years of therapy. Hepatology. Vol In press. Published Online 4 Feb Lok AS-F, McMahon BJ. AASLD practice guidelines chronic hepatitis B. Hepatology. 2007; 45: Locarnini S, Omata M. Molecular virology of hepatitis B virus and the development of antiviral drug resistance. Liver International. 2006; 26: Verkorte productinformatie Baraclude Samenstelling: Baraclude filmomhulde tabletten bevatten 0,5 mg of 1,0 entecavir (als monohydraat). Indicaties: Baraclude is geïndiceerd voor de behandeling van chronische hepatitis B virusinfectie (HBV) bij volwassen patiënten met gecompenseerde leverziekte en tekenen van actieve virale replicatie, aanhoudend verhoogde serum-alanineaminotransferase (ALT)-spiegels en histologische tekenen van actieve ontsteking en/of fibrose. Deze indicatie is gebaseerd op klinisch onderzoek bij HBeAg-positieve en HBeAgnegatieve patiënten, nucleoside-naïeve patiënten en patiënten met lamivudine-refractaire hepatitis B. Contra-indicaties: Overgevoeligheid voor het werkzame bestanddeel of voor één van de hulpstoffen. Waarschuwingen en voorzorgsmaatregelen: Aanpassing van de dosering wordt aanbevolen voor patiënten met nierfunctiestoornissen. Tijdens en na het staken van de behandeling dient men bedacht te zijn op mogelijk ernstige exacerbaties van hepatitis. Het verdient aanbeveling om de leverfunctie tijdens de behandeling zorgvuldig te controleren. Bij patiënten met gedecompenseerde cirrose zijn vaker ernstige leverbijwerkingen waargenomen dan bij patiënten met een gecompenseerde leverfunctie. Voorvallen van lactaatacidose (in afwezigheid van hypoxemie), soms fataal, gewoonlijk samengaand met ernstige hepatomegalie en hepatische steatose, zijn gemeld bij het gebruik van nucleosideanalogen. Met name bij lamivudine-refractaire patiënten dient de virologische response in verband met resistentie gecontroleerd te worden. Entecavir dient niet gebruikt te worden bij patiënten met hiv/hbv co-infectie die geen HAART krijgen. Entecavir is niet onderzocht als behandeling tegen hiv en wordt daarvoor afgeraden. De nierfunctie van patiënten die na een levertransplantatie cyclosporine of tacrolimus gebruiken, moet voor en tijdens de behandeling met entecavir zorgvuldig worden geëvalueerd. Bijwerkingen: slapeloosheid, hoofdpijn, duizeligheid, slaperigheid, braken, diarree, misselijkheid, huiduitslag, dyspepsie, vermoeidheid, afwijkende laboratoriumwaarden, anafylactische reacties, alopecia. Dosering: Bij nucleoside-naïeve patiënten is de aanbevolen dosis 0,5 mg eenmaal daags met of zonder voedsel. Bij lamivudine-refractaire patiënten (met tekenen van viremie tijdens de behandeling met lamivudine of de aanwezigheid van lamivudine resistentie [LVDr] mutaties) is de aanbevolen dosis 1 mg eenmaal daags op een lege maag (meer dan twee uur vóór of meer dan twee uur na een maaltijd). Aanpassing van de dosis wordt aanbevolen voor patiënten met een creatinineklaring van minder dan 50 ml/min, inclusief patiënten die hemodialyse of continue ambulante peritoneaaldialyse (CAPD) ondergaan. Afleverstatus: UR. Vergoeding en prijzen: Volledige vergoeding; voor prijzen zie Z-index. Voor volledige productinformatie, zie Samenvatting van de Productkenmerken. Bristol-Myers Squibb B.V., Woerden, aug Verkorte samenvatting van van de de productkenmerken van Pegasys van Pegasys Samenstelling: Pegasys bevat bevat peginterferon peginterferon alfa-2a, alfa-2a, gevormd gevormd door conjugatie door conjugatie van PEG-reagens van PEG-reagens (molecuulmassa 40 KD) aan 40 interferon KD) aan alfa-2a. interferon Pegasys alfa-2a. is beschikbaar Pegasys is beschikbaar in voorgevulde in wegwerpspuit voorgevulde wegwerpspuit met gebruiksklare met (molecuulmassa gebruiksklare oplossing voor oplossing injectie met voor 180 injectie of 135 μg met peginterferon 180 of 135 alfa-2a μg peginterferon per 0,5 ml. Indicatie: alfa-2a per 1. 0,5 Chronische ml. Indicatie: hepatitis 1. C Chronische (CHC) bij volwassen hepatitis C patiënten (CHC) bij volwassen die positief patiënten zijn voor die HCV-RNA positief zijn in voor het HCV-RNA serum, inclusief het serum, patiënten inclusief met patiënten gecompenseerde met gecompenseerde cirrose en/of cirrose co-infectie en/of met co-infectie klinisch stabiele met klinisch HIV. De stabiele optimale HIV. behandeling De optimale is behandeling combinatie is in met combinatie ribavirine. met Deze ribavirine. combinatie Deze is geïndiceerd combinatie bij is naïeve geïndiceerd patiënten bij naïeve en patiënten patiënten bij wie en eerdere patiënten behandeling bij wie eerdere met behandeling interferon alfa met (gepegyleerd interferon of alfa niet-gepegyleerd) (gepegyleerd of ontoereikend niet-gepegyleerd) was. 2. ontoereikend HBeAg-positieve was. of 2. -negatieve HBeAg-positieve chronische of -negatieve chronische hepatitis B (CHB) bij volwassen patiënten met gecompenseerde leverziekte en bewijs van hepatitis B (CHB) bij volwassen patiënten met gecompenseerde leverziekte en bewijs van virale replicatie, virale replicatie, verhoogt ALT en histologisch bevestigde leverontsteking en/of fibrose. Contra-indicaties: verhoogt ALT en histologisch bevestigde leverontsteking en/of fi brose. Contra-indicaties: Overgevoeligheid voor Overgevoeligheid voor alfa interferonen of een van de hulpstoffen, auto-immuun hepatitis, ernstige alfa interferonen of een van de hulpstoffen, auto-immuun hepatitis, ernstige leverdisfunctie of gedecompenseerde leverdisfunctie of gedecompenseerde levercirrose, neonaten en kinderen tot 3 jaar oud vanwege de hulpstof levercirrose, neonaten en kinderen tot 3 jaar oud vanwege de hulpstof benzylalcohol, ernstige al bestaande benzylalcohol, ernstige al bestaande hartaandoening in de anamnese en HIV-CHC patiënten met cirrose en een hartaandoening in de anamnese en HIV-CHC patiënten met cirrose en een Child-Pugh score 6. Dosering en Child-Pugh score 6. Dosering en wijze van toediening: De aanbevolen dosering Pegasys bedraagt 180 wijze van toediening: De aanbevolen dosering Pegasys bedraagt 180 μg eenmaal per week subcutaan μg eenmaal per week subcutaan toegediend in buik of dij. De therapieduur is o.a. afhankelijk van het genotype, basale toegediend viral in load buik of en dij. de De respons. therapieduur Belangrijkste is o.a. afhankelijk waarschuwingen: van het genotype, Ernstige basale viral effecten load op en het de respons. centrale zenuwstelsel, Belangrijkste voornamelijk waarschuwingen: depressie, Ernstige suïcide effecten gedachten op en het pogingen centrale tot zenuwstelsel, suïcide, zijn voornamelijk waargenomen depressie, bij enkele patiënten suïcidegedachten tijdens en en soms pogingen nog tot tot 6 maanden suïcide, na zijn Pegasys-behandeling. waargenomen bij enkele Pegasys-behandeling patiënten tijdens werd en in soms verband nog gebracht tot 6 maanden met anemie na Pegasys-behandeling. (in combinatie met ribavirine), Pegasys-behandeling trombocytopenie, werd leukopenie, in verband neutropenie gebracht met en lymfopenie. anemie (in Bij combinatie gebruik van met alfa ribavirine), interferonen trombocytopenie, zijn schildklierfunctie-afwijkingen leukopenie, neutropenie of verergering en lymfopenie. van schildklieraandoeningen Bij gebruik van alfa gemeld. interferonen Hypertensie, zijn schildklierfunctie-afwijkingen supraventriculaire aritmieën, of verergering decompensatio van schildklieraandoeningen cordis, pijn op de borst gemeld. en myocardinfarct Hypertensie, zijn supraventriculaire in verband aritmieën, gebracht decompensatio met alfa-interferontherapie. cordis, pijn op de Indien borst tijdens myocardinfarct behandeling zijn in aanwijzingen verband gebracht voor leverdecompensatie met alfa-interferontherapie. ontstaan, Indien alsmede tijdens indien behandeling bij CHC/HIV-patiënten aanwijzingen een voor Child-Pugh leverdecompensatie score van 7 ontstaan, wordt bereikt, alsmede dient indien Pegasys bij CHC/HIV- onmiddellijk patiënten gestaakt een Child-Pugh te worden. score Ernstige, van 7 acute wordt overgevoeligheidsreacties bereikt, dient Pegasys onmiddellijk zijn zelden waargenomen gestaakt te worden. tijdens Ernstige, behandeling acute met overgevoeligheidsreacties alfa interferonen. Ernstige zijn infecties zelden zijn waargenomen gemeld tijdens tijdens behandeling met alfa met interferonen. alfa Bij Pegasys Ernstige zijn infecties diabetes zijn gemeld mellitus, tijdens retinopathie, behandeling pulmonale met alfa symptomen, interferonen. cardiomyopathie, Bij Pegasys zijn vasculitis diabetes en mellitus, nierinsufficiëntie retinopathie, waargenomen. pulmonale Tevens symptomen, is exacerbatie cardiomyopathie, en provocatie vasculitis van psoriasis en nierinsuffi en sarcoïdose ciëntie waargenomen. Pegasys Tevens is mag exacerbatie alleen tijdens provocatie de zwangerschap van psoriasis gebruikt en sarcoïdose worden wanneer waargenomen. het mogelijke Pegasys voordeel mag het alleen mogelijke tijdens risico de zwangerschap voor de foetus gebruikt rechtvaardigt. worden Borstvoeding wanneer het mogelijke moet voorafgaand voordeel het aan mogelijke de behandeling risico voor worden gestopt. foetus rechtvaardigt. Bijwerkingen: Borstvoeding In studies bleek moet het voorafgaand veiligheidsprofiel aan de van behandeling Pegasys bij worden CHB gelijk gestopt. aan Bijwerkingen: dat bij CHC. Met In studies uitzondering bleek het van veiligheidsprofi pyrexie was el de van frequentie Pegasys bij van CHB de gelijk meerderheid aan dat bij van CHC. de Met bijwerkingen uitzondering opmerkelijk van pyrexie lager was bij de patiënten frequentie met van CHB de meerderheid dan bij patiënten van de met bijwerkingen CHC. Bij opmerkelijk patiënten met lager HIV-CHC bij patiënten co-infectie met CHB waren dan bij de patiënten klinische bijwerkingprofielen met CHC. Bij patiënten gemeld met voor HIV-CHC Pegasys, co-infectie alleen waren of in combinatie de klinische met bijwerkingprofi ribavirine, elen gelijk gemeld aan die voor bij patiënten Pegasys, met alleen CHC of in mono-infectie. combinatie met Zeer ribavirine, vaak ( 1/10) gelijk aan voorkomende die bij patiënten bijwerkingen met CHC mono-infectie. tijdens Pegasys Zeer monotherapie vaak ( 1/10) bij voorkomende CHB of CHC bijwerkingen of in combinatie tijdens Pegasys met ribavirine monotherapie i.h.g. van bij CHB CHC of zijn CHC anorexie, of in combinatie gewichtsafname, met ribavirine hoofdpijn, in het slapeloosheid, geval van CHC angst, zijn anorexie, prikkelbaarheid, gewichtsafname, depressie, hoofdpijn, duizeligheid, slapeloosheid, verminderde angst, concentratie, prikkelbaarheid, dyspnoe, depressie, hoesten, misselijkheid, duizeligheid, verminderde diarree, buikpijn, concentratie, alopecia, dyspnoe, pruritus, hoesten, dermatitis, misselijkheid, droge huid, diarree, myalgie, buikpijn, artralgie, alopecia, vermoeidheid, pruritus, koorts, rillingen, reacties op de injectieplaats, asthenie en pijn. Afleverstatus: U.R. Pegasys wordt volledig dermatitis, droge huid, myalgie, artralgie, vermoeidheid, koorts, rillingen, reacties op de injectieplaats, asthenie vergoed. Volledige productinformatie is beschikbaar bij Roche Nederland B.V., Postbus 44, 3440 en pijn. Afl everstatus: U.R. Volledige productinformatie is beschikbaar bij Roche Nederland B.V., AA WOERDEN. Telefoon: , (05/2009) Postbus 44, 3440 AA WOERDEN. Telefoon: , (05/2009) Baraclude is a registered trademark of Bristol-Myers Squibb Company and its affiliates Bristol-Myers Squibb. All rights reserved. January 2010 NLBC-K HQ09PM037(10) Roche Nederland B.V. Postbus 44, 3440 AA Woerden Tel , hepatitis vraagt om een krachtige aanpak NLBC-K0001_SPI Trim 92x126mm NLBC_K0001_SPI_92x120_V7.indd 1 2/4/ _bijsluiter 10:00 AM 90x132.indd :37:40 13
14 Lever van eigen bodem Weer een prima kwartaal voor de Nederlandse en Vlaamse Hepatologie! 18 papers voldeden dit kwartaal aan de geautomatiseerde PubMED zoekopdracht met deze eisen: Eerste dan wel laatste auteur van het betreffende paper is lid van de Nederlandse Vereniging voor Hepatologie. Het artikel heeft een duidelijke link met hepatologische onderwerpen Impact factor is > 4 Dank voor alle inzendingen van korte reclameboodschappen over de betreffende papers! Erg goed om te zien dat steeds meer auteurs gehoor geven aan ons verzoek. Op deze manier kunnen we de belangrijkste bevindingen van onze Nederlandse basaal en klinisch georiënteerde collega s op de voet volgen. Wij willen ons verontschuldigen wanneer onze zoekcriteria ontoereikend zijn en uw artikel wel aan bovengenoemde voorwaarden voldoet, maar onverhoopt niet door ons is geselecteerd. Graag horen wij dit van u zodat wij onze zoekcriteria kunnen aanscherpen. Dit speciaal met het oog op de Young Hepatologist prijzen die ieder voorjaar worden uitgereikt. De winnaars van deze prijzen worden gekozen op basis van de PubMed search die gebruikt wordt in deze rubriek. Saskia van Mil Klinisch onderzoek: Dendritic cells in chronic viral hepatitis B and C: victims or guardian angels? Woltman AM, Boonstra A, Janssen HL. Gut Jan;59(1): PMID: Dankzij hun centrale en sterk regulerende rol in afweerresponsen worden dendritische cellen (DC) vaak misbruikt door virussen om effectieve anti-virale immuniteit te voorkomen. Dit review geeft een gedetailleerd overzicht van de functie van DC in HBV en HCV infectie, de interactie tussen HBV/HCV en DC en de consequentie daarvan voor ontwikkeling van chronische virale hepatitis. Ook worden de mogelijkheden voor behandeling van chronische virale hepatitis gericht op DC modulatie besproken. Migration of allosensitizing donor myeloid dendritic cells into recipients after liver transplantation. Bosma BM, Metselaar HJ, Gerrits JH, van Besouw NM, Mancham S, Groothuismink ZM, Boor PP, van der Laan LJ, Tilanus HW, Kuipers EJ, Kwekkeboom J. Liver Transpl Jan; 16(1): PMID: Er is gesuggereerd dat myeloïde dendritische cellen (MDC) uit de getransplanteerde lever bijdragen aan acceptatie door de ontvanger. Wij hebben aangetoond dat direct na klinische levertransplantatie, maar niet na niertransplantatie, MDC uit het donor orgaan migreren in de circulatie van de ontvanger. MDC die loskomen uit de donor-lever stimuleren echter allogene T-cellen tot produktie van pro-inflammatoire cytokinen, en dragen daarom waarschijnlijk niet bij aan acceptatie, maar juist aan afstoting. Treatment of polycystic liver disease. van Keimpema L, Höckerstedt K. Br J Surg Dec; 96(12): PMID: Een groot deel van de patiënten met polycysteuze levers hebben geen klachten en behoeven dan ook geen behandeling. Echter, wanneer de lever zo groot wordt dat klachten ontstaan is er vaak vraag naar behandeling. De keuze van behandeling van polycysteuze levers hangt af van het aantal cysten, de grootte van de cysten en de ligging van de cysten. De verschillende behandelopties, aspiratie-sclerotherapie, laparoscopische fenestratie en levertransplantatie, worden beschreven. Tevens wordt aangegeven welke patiënten geschikt zijn voor een van de behandelmogelijkheden. Factors that predict response of patients with hepatitis B e antigen-positive chronic hepatitis B to peginterferon-alfa. Buster EH, Hansen BE, Lau GK, Piratvisuth T, Zeuzem S, Steyerberg EW, Janssen HL. Gastroenterology Dec;137(6): PMID: Behandeling met peginterferon geeft weliswaar de hoogste kans op blijvende respons in vergelijking met andere antivirale middelen, toch betreft dit altijd nog de minderheid van de behandelde patiënten. Het is daarom van belang de verwachte kans op respons op peginterferon vóór aanvang van behandeling te kunnen bepalen. Deze studie biedt een praktisch hulpmiddel om juist die patiënten met de hoogste kans op blijvende respons te kunnen identificeren. Early HBeAg loss during peginterferon alpha-2b therapy predicts HBsAg loss: results of a long-term follow-up study in chronic hepatitis B patients. Buster EH, Flink HJ, Simsek H, Heathcote EJ, Sharmila S, Kitis GE, 14
15 Gerken G, Buti M, de Vries RA, Verhey E, Hansen BE, Janssen HL. Am J Gastroenterol Oct;104(10): PMID: HBsAg verlies treedt op bij 11% van patiënten binnen 5 jaar na behandeling met peginterferon alpha-2b. Deze studie toont dat met name het tijdstip van HBeAg verlies de kans op HBsAg verlies op lange termijn voorspelt. Bij patiënten met HBeAg verlies binnen 32 weken behandeling is de kans op HBsAg verlies maar liefst 36%, terwijl HBsAg verlies nauwelijks voorkomt bij patiënten met HBsAg verlies na dit tijdstip (4%). Activation of the complement system in human nonalcoholic fatty liver disease. Rensen SS, Slaats Y, Driessen A, Peutz-Kootstra CJ, Nijhuis J, Steffensen R, Greve JW, Buurman WA. Hepatology Dec;50(6): PMID: Management of hemobilia and pancreatitis after liver biopsy: a key role for endoscopic retrograde cholangiopancreaticography. Hendriks MP, Wanten GJ, Drenth JP. Liver Transpl Nov;15(11): PMID: Hemobilie als complicatie van een leverbiopt is zeldzaam. In deze ingezonden brief beschrijven de auteurs een patiënt die zich vier dagen na echo begeleide leverbioptie hematemesis ontwikkelde die berustte op hemobilie. Door de aanwezigheid van stolsels in de galwegen ontstond galwegobstructie en pancreatitis. De auteurs verrichten een ERCP met plaatsing van een endoprothese. Hierdoor werd de galwegdoorgankelijkheid gezekerd en verdween de pancreatitis. Figuur: (A) ERCP met multipele ophelderingen in de galwegen passend bij stolsels. (B) Bloed komend uit de papil van vater passend bij hemobilie. Wij hebben voor het eerst aangetoond dat het complement systeem, een belangrijke component van het aangeboren afweersysteem, geactiveerd is bij mensen met niet-alcoholische vette leverziekte (NAFLD). Depositie van complement factoren rondom vervette hepatocyten was gecorreleerd met de klinische graad van de ziekte. Deze resultaten wijzen op een belangrijke rol van het complement systeem in de NAFLD pathogenese, te meer daar complement factoren betrokken zijn bij zowel lever fibrose als regeneratie. Liver disease associated with canalicular transport defects: Current and future therapies. Stapelbroek JM, van Erpecum KJ, Klomp LW, Houwen RH. J Hepatol Nov 21. PMID: Dit artikel geeft een korte beschrijving van de canaliculaire transport defecten. Op dit moment is voor deze leverziekten maar zelden effectieve medicamenteuze behandeling mogelijk. Operatief ingrijpen zoals partiële biliaire drainage (PBD) of een levertransplantatie is meestal de enige optie. Echter agentia die via nucleaire receptoren de galproductie kunnen verbeteren, chaperonnes die de expressie van de gemuteerde transporters kunnen induceren of mutatie specifieke therapie zijn veelbelovende nieuwe ontwikkelingen. Impaired fibrinolysis as a risk factor for Budd-Chiari syndrome. Hoekstra J, Guimaraes AH, Leebeek FW, Darwish Murad S, Malfliet JJ, Plessier A, Hernandez-Guerra M, Langlet P, Elias E, Trebicka J, Primignani M, Garcia-Pagan JC, Valla DC, Rijken DC, Janssen HL. Blood Nov 18. [Epub ahead of print] PMID: Bij veel patiënten met Budd-Chiari syndroom (BCS) kan inmiddels een onderliggende oorzaak voor trombose worden aangetoond. Er zijn echter nog steeds patiënten bij wie geen risicofactor kan worden gevonden. In deze case-control studie is gekeken naar de rol van veranderingen in het fibrinolytische syteem (hypofibrinolyse) als mogelijke protrombotische factor. Onze resultaten laten zien dat een verminderde fibrinolytische capaciteit een potentiële risicofactor is voor het ontstaan van trombose bij patiënten met BCS. Rapid HCV-RNA decline with once-daily TMC435: A Phase I study in healthy volunteers and hepatitis C patients. Reesink HW, Fanning GC, Abou Farha K, Weegink C, Van Vliet A, van t Klooster G, Lenz O, Aharchi F, Mariën K, Van Remoortere P, de Kock H, Broeckaert F, Meyvisch P, Van Beirendonck E, Simmen K, Verloes R. Gastroenterology Oct 20. [Epub ahead of print] PMID: TMC435 is een HCV NS3/4A protease remmer waarvan de veiligheid, verdraagzaamheid en farmaco-kinetiek onderzocht werd in een placebo gecontroleerde fase-1 studie bij 49 gezonde vrijwilligers in oplopende dosering tot 600 mg per dag; 6 chronische hepatitis C patiënten ontvingen open label 200 mg TMC435 een maal daags gedurende 5 dagen. TMC435 werd in beide groepen goed verdragen. HCV-RNA daalde 3,9 log10 IU/ml zonder dat virale doorbraak werd waargenomen. In de patiënten was de gemiddelde EC50 waarde 275 maal de in vitro replicon bepaling. TMC435 is een zeer krachtige NS3/4A protease remmer, met als groot voordeel de mogelijkheid van een maal daags dosering. New hope for a cure for chronic hepatitis C. Reesink HW, Weegink CJ. J Hepatol Oct;51(4): Epub 2009 Jul 21. PMID: Onlangs werden twee placebo gecontroleerde fase 2 studies gepubliceerd in het gezaghebbende medische tijdschrift New England Journal of Medicine (2009; 360: 1827 en 1839). De studies lieten zien dat nooit eerder behandelde chronische hepatitis C patiënten (genotype-1), die met de combinatie Telaprevir (een HCV specifieke protease remmer), Peg-interferon en ribavirine behandeld waren in 67-69% hun HCV infectie kwijt raakten, terwijl dit met standaard behandeling slechts in 41-46% geschiedde. 15
16 I sbn n UR 871 / Basaal onderzoek Folding defects in P-type ATP 8B1 associated with hereditary cholestasis are ameliorated by 4-phenylbutyrate. van der Velden LM, Stapelbroek JM, Krieger E, van den Berghe PV, Berger R, Verhulst PM, Holthuis JC, Houwen RH, Klomp LW, van de Graaf SF. Hepatology Jan;51(1): PMID: Mutaties in het ATP8B1 gen kunnen leiden tot een progressieve of recurrente vorm van cholestase. In deze studie tonen we aan dat 7 verschillende mutaties in het ATP8B1 gen leiden tot verstoorde vouwing van het ATP8B1 eiwit. De consequenties hiervan op eiwitexpressie en plasmamembraan lokalisatie kunnen gedeeltelijk verholpen worden met 4-fenylbutyraat voor de meest voorkomende mutaties in ATP8B1. Mogelijk kan 4-fenylbutyraat-behandeling de aanvallen van cholestase helpen voorkomen of beëindigen. Bile salt sequestration induces hepatic de novo lipogenesis through farnesoid X receptor- and liver X receptoralpha-controlled metabolic pathways in mice. Herrema H, Meissner M, van Dijk TH, Brufau G, Boverhof R, Oosterveer MH, Reijngoud DJ, Müller M, Stellaard F, Groen AK, Kuipers F. Hepatology. [Epub ahead of print] 23 Oct 2009 PMID: Galzoutbinders worden succesvol ingezet om hypercholesterolemie en hyperglycemie in patiënten met diabetes te verbeteren. Minder bekend zijn de effecten van galzoutbinders op het vet metabolisme. In dit werk laten we zien dat specifieke veranderingen in galzout synthese en -opname leiden tot verhoogde productie van vet in levers van diabetische muizen die behandeld zijn met de galzoutbinder colesevelam HCl. De resultaten benadrukken de belangrijke en multifactoriële rol van galzouten in regulatie van stofwisseling in de lever. Characterisation of the activated liver progenitor cell niche, potential involvement of Wnt and Notch signalling. Spee B, Carpino G, Schotanus BA, Katoonizadeh A, Vander Borght S, Gaudio E, Roskams T. Gut Nov 1. [Epub ahead of print] PMID: Lever progenitor cellen (LPCs) zijn een potentieel middel als curatieve therapie voor leverziekten. Hiervoor is een beter inzicht in de proliferatie en differentiatie signalen nodig. Dit artikel beschrijft de betrokkenheid van signaal paden in verscheidene leverziekten. De resultaten tonen dat Wnt geactiveerd is waar LPC proliferatie optreedt en Notch betrokken is bij biliaire differentiatie. Het activeren van LPCs in de patiënt kan leiden tot een nieuwe behandelmethode van leverziekten. Reduced expression of ATP7B affected by Wilson disease-causing mutations is rescued by pharmacological folding chaperones 4-phenylbutyrate and curcumin. van den Berghe PV, Stapelbroek JM, Krieger E, de Bie P, van de Graaf SF, de Groot RE, van Beurden E, Spijker E, Houwen RH, Berger R, Klomp LW. Hepatology Dec;50(6): PMID: Mutaties in ATP7B veroorzaken de ziekte van Wilson. Dit is een autosomaal recessieve koperstapelingsziekte in de lever doordat ATP7B geen koper meer kan transporteren. Deze mutaties leiden tot verminderde eiwitexpressie door misvouwing van het ATP7B eiwit. De eiwitvouwing kan worden gestimuleerd met curcumin en 4-phenylbutyraat, waardoor de eiwitexpressie en waarschijnlijk de kopertransportfunctie van ATP7B wordt verbeterd. Mogelijk biedt dit een nieuwe behandelingsmethode voor patiënten met de ziekte van Wilson. Mededelingen Inschrijving voorjaarsvergadering 2009 Het aanstaande voorjaarscongres van onze vereniging zal plaatsvinden op 18 en 19 maart a.s. in Congrescentrum NH Koningshof in Veldhoven. U vindt bij deze nieuwsbrief het programma en een inschrijvingskaart voor het congres waarmee u zich bovendien kunt opgeven voor het cursorisch onderwijs in maag-darm-leverziekten op woensdag 17 maart, dus voorafgaand aan het congres. Het thema is deze keer infecties. Het programma kunt u downloaden via Wilt u zich in verband met de accommodatie weer tijdig inschrijven? Agenda casuïstisch conferenties 2010 te Utrecht Deze door de Nederlandse Vereniging van Gastroenterologie georganiseerde conferenties zullen in 2010 plaatsvinden op 27 april, 7 september en 9 november. Deze geaccrediteerde bijeenkomsten worden gehouden in de Jaarbeurs in Utrecht (Beatrixgebouw) van tot uur (vanaf uur zullen de firma s AstraZeneca en Tramedico een oriëntaals buffet verzorgen). Wellicht kunt u deze bijeenkomsten vast in uw agenda noteren. U bent van harte uitgenodigd. Leerboek Leverziekten Veel NVH-leden zijn op dit moment Leverziekten al in bezit In de afgelopen van jaren is veel onderzoek het verricht prachtig binnen de hepatologie. Dit heeft geleid uitgevoerde leerboek tot revolutionaire veranderingen waardoor de diagnostiek van leverziekten aanzienlijk is verbeterd. Ook de progressie die is geboekt in de behandeling van leverziekten is enorm. Deze grote en recente vooruitgang op diagnostisch en therapeutisch gebied maakt de behoefte aan een goede, actuele leidraad voor de klinische praktijk noodzakelijk. Leverziekten. Ook In Leverziekten zijn de ontwikkelingen van de afgelopen jaren samengebracht. naast algemene hoofdstukken als anatomie, histologie, functies en onderzoeksmethoden worden diagnostiek en behandeling van alle veelvoorkomende leveraandoeningen beschreven, tevens van de meer zeldzame aandoeningen. In afzonderlijke het hoofdstukken bezit wordt aandacht komen besteed aan voeding leverziekten, van zwangerschap, het u kunt in levertransplantatie en operatierisico s bij leverziekten. Leverziekten biedt een overzicht van de volle breedte waarin het vak binnen het nederlandse taalgebied wordt uitgeoefend slaat een brug tussen enerzijds het basaal en klinisch leveronderzoek anderzijds het klinisch handelen. leerboek door inzenden van Leverziekten is samengesteld door vele specialisten uit nederland en Vlaanderen. Zij bieden hiermee studenten geneeskunde, assistenten opleiding en fellows een onmisbaar, rijk geïllustreerd overzichtwerk om wegwijs te raken de wereld van de leverziekten. Daarnaast helpt het maag-darm-leverartsen, internisten, huisartsen en andere medische professionals bij het oplossen van hepatologische problemen. inschrijfformulier dat is ingesloten bij deze nieuwsbrief. Het boek is op voorraad en wordt binnen 5 werkdagen na ontvangst van uw aanmelding toegestuurd. Voor inlichtingen belt u met het secretariaat in Haarlem, telefoonnummer O Bohn Stafleu van Loghum Er zijn op dit moment nog boeken in voorraad bij het secretariaat. Janssen / Drenth / Hoek (red.) Leverziekten O Bohn Stafleu van Loghum Leverziekten Onder redactie van Prof.dr. H.l.A. Janssen Prof.dr. J.P.H. Drenth Dr. b. van Hoek 16
17 Jong hepatologisch talent van 2009! Ook dit jaar zal de NVH weer 2 prijzen uitloven voor het beste artikel van de hand van een klinisch en basaal hepatoloog. Een goede wetenschappelijke publicatie is vaak een beloning van een lange weg van goed onderzoek en komt niet vanzelf. Vele maanden onderzoek, hard werken, en een beetje geluk komen er aan te pas om van dat ene manuscript een toppublicatie te maken. De NVH heeft als doelstelling dat het het wetenschappelijk werk dat door haar leden wordt verricht te bevorderen. Wij vinden het erg belangrijk dat goed Nederlands leveronderzoek haar weg vindt in de wetenschappelijke topbladen. Om deze inspanning speciaal te erkennen en belonen, hebben wij sinds vorig jaar 2 prijzen ingesteld: De klinische junior onderzoeker NVH prijs, bedoeld voor de beste klinisch-hepatologische publikatie, en de basale junior onderzoeker NVH prijs, bedoeld voor de beste basaal hepatologische publicatie. Voorwaarden om naar deze prijs mee te dingen 3-ledig: 1. het artikel beschrijft een hepatologisch onderwerp, 2. de eerste auteur is lid van de NVH, 3. de eerste auteur is nog niet gepromoveerd of minder dan 2 jaar post-doc op het moment van publicatie. In tegenstelling tot vorig jaar, zullen de winnaars gekozen worden op basis van de PubMed search die gebruikt wordt in de rubriek Lever van eigen bodem. Reden te meer om aan te geven wanneer uw artikel onverhoopt niet uit deze search is gekomen en u niet benaderd bent om een korte samenvatting voor deze rubriek in Lever te schrijven. Neem dan contact op met secretariaat@nvh.nl. De NVH junior onderzoekers prijs bestaat uit een certificaat en een geldbedrag van 500,-. De jury zal de papers beoordelen op: duidelijkheid van de vraagstelling, originaliteit, sterkte van de publicatie uitgedrukt in impactfactor, gebruikte methode, wetenschappelijke waarde, klinische impact / relevantie, klinisch of basaal, lay-out, opbouw en leesbaarheid. De prijzen zullen worden uitgereikt tijdens de voorjaarsvergadering van de NVH op 19 maart Informatie Gastrostart-subsidie Gastrostart kent één subsidievorm, nl. een startsubsidie met een maximumbedrag van 7.500,00. Deze subsidie is uitsluitend bedoeld voor beginnend en innoverend onderzoek op gastroenterologisch-hepatologisch gebied en alleen ten behoeve van leden (projectleider of hoofdaanvrager) van de NVGE, NVGIC of NVH. Het heeft geen zin om een aanvraag in te dienen indien het startelement niet aanwezig is. Aanvragers wordt gevraagd om specifiek behalve het innoverende karakter van het project, ook het risicodragende aspect (redenen waarom het onderzoek niet kansrijk is bij andere subsidiegevers) te becommentariëren. De subsidie is bedoeld om onderzoekers in de gelegenheid te stellen voorbereidend onderzoek te verrichten, c.q. technieken operationeel te maken, op grond waarvan een goed onderbouwd subsidieverzoek bij de MLDS of een andere subsidiegever, kan worden ingediend. Er worden geen subsidies toegekend voor het verrichten van onderzoek of volgen van stages in buitenland. Beoordeling geschiedt door de Gastrostart-commissie. Indien nodig worden externe deskundigen geraadpleegd. De aanvrager is verplicht binnen een jaar na toekenning van een eventuele subsidie schriftelijk verslag aan de Gastrostart-commissie uit te brengen over het resultaat c.q. het verloop van het onderzoek. De volgende subsidierondes zijn: 1 april 2010, 1 september 2010 en 1 januari 2011 Inlichtingen: Commissie Gastrostart, Mevr. M.J. van Gijtenbeek Postbus 657, 2003 RR Haarlem, telefoon (023) , fax (023) , secretariaat@nvge.nl Het aanvraagformulier voor Gastrostart subsidie kunt u downloaden via De aanvraag dient digitaal te worden ingezonden naar secretariaat@nvge.nl en daarnaast een getekende kopie per post aan het hierboven vermelde secretariaatsadres. NVGE-NVH reisstipendia De Nederlandse Vereniging voor Gastroenterologie stelt jaarlijks reisbeurzen ter beschikking aan leden van de NVGE en NVH. Aanvraagformulieren en voorwaarden kunnen worden gedownload via de site van de NVGE: Lidmaatschap Nederlandse Vereniging voor Hepatologie De contributie bedraagt 35,00 per jaar, aanmelding van nieuwe leden bij de secretaris, Dr. K.N. Faber, Postbus 657, 2003 RR Haarlem, fax (023) Uitvoerige informatie over de voordelen van het lidmaatschap vindt u op de website: www. hepatologie.org Het lidmaatschap wordt automatisch verlengd tenzij schriftelijk bericht van opzegging is ontvangen vóór 1 november van het lopende jaar. Voorwaarden sponsoring proefschriften door NVH De Nederlandse Vereniging voor Hepatologie levert, onder bepaalde voorwaarden, een bijdrage van 500,- aan de drukkosten van proefschriften. De maatregel is bedoeld om AIO s/oio s (of onderzoekers met een vergelijkbaar salaris) te ondersteunen. Zie voor voorwaarden en aanvraagformulier: org. U vindt op onze website ook samenvattingen van eerder verschenen (en gesponsorde) proefschriften van NVH-leden. Nieuws DLW 2010 Begin febuari heeft u per post inmiddels het volledige programma van de DLW 2010, inclusief inschrijvingskaart ontvangen. Zoals u wellicht weet van vorig jaar vindt tijdens de DLW ook de al langer bestaande cursus klinische hepatologie plaats. Deze cursus dient door AIOS MDL eenmaal verplicht gevolgd te worden tijdens het MDL-deel van de opleiding (jaar drie t/m zes). De cursus vindt dit jaar plaats van 9 t/m 11 juni a.s. te Amsterdam. Als NVH-lid kunt u deelnemen aan de DLW / cursus voor een gereduceerd bedrag. Bij de Cursus Klinische Hepatologie hoort ook het gebruikelijke cursusboek met bijdragen van alle sprekers aan de cursus. Van de cursus van 2009 hebben wij overigens nog exemplaren beschikbaar. NVH-leden kunnen dit kosteloos aanvragen via secretariaat@nvh.nl. Informatie over de DLW via 17
18 NIEUW voor de behandeling van volwassenen met gecompenseerde chronische hepatitis B Eén lever. Eén leven. Eénmaal daags één tablet VIREAD. Uitgebreide productinformatie verkrijgbaar bij GILEAD Telefoon: gileadnl@gilead.com
19 Proefschriftsamenvatting Samenvatting proefschrift Esther M.E. van Straten Metabolic programming of lipid metabolism: Effects of prenatal pharmacological and nutritional interference Promotiedatum: 2 december 2009 Rijksuniversiteit Groningen Promotores: Prof. dr. F. Kuipers Prof. dr. H.J. Verkade Uit epidemiologisch en proefdieronderzoek blijkt dat een suboptimale voeding van de moeder tijdens de zwangerschap de kans kan vergroten dat haar kinderen op latere leeftijd hart- en vaatziekten en type II diabetes ontwikkelen. Dit verband tussen prenatale voeding en ontwikkeling van ziekten op latere leeftijd wordt ook wel metabole programmering genoemd. In dit proefschrift worden verschillende muismodellen gebruikt waarin metabole programmering met betrekking tot het hepatische cholesterol- en vetmetabolisme beschreven wordt. Een belangrijke regulator van het cholesterol- en vetmetabolisme is de Lever X Receptor (LXR). Specifieke activering van LXR door middel van toediening van een farmacologische agonist veroorzaakt een verhoging van het (goede) plasma HDL cholesterol, maar heeft ook een negatieve bijwerking, namelijk vetstapeling (steatose) in de lever. Studies beschreven in dit proefschrift laten zien dat LXR in de foetale lever geactiveerd kan worden door orale toediening van een farmacologische LXR activator aan de moeder. Bovendien blijkt uit onze experimenten dat het ontwikkelen van hepatische steatose in de foetale lever slechts marginaal het vetmetabolisme tijdens jongvolwassenheid beïnvloedt. Daarnaast werd een welbekend model gebruikt om metabole programmering in nakomelingen te realiseren. Tijdens de zwangerschap werd een eiwitarm dieet gegeven aan zwangere muizen. Het eiwitarme dieet leidde tot een verandering in de foetale DNA methyleringsstatus en veroorzaakte in de foetale lever sterke effecten op de expressie van genen die betrokken zijn bij cholesteroltransport. Dit leidde echter niet tot verschillen in cholesteroltransport van moeder naar foetus. In volwassen nakomelingen zorgde het prenatale eiwitarme dieet ervoor dat het vet- en glucosemetabolisme van vrouwelijke nakomelingen meer leek op het mannelijke vet- en glucosemetabolisme. Deze bevindingen zouden kunnen impliceren dat de voedingsstatus van de moeder tijdens de zwangerschap geslachtsspecifieke effecten heeft op het metabolisme van haar kinderen. Proefschriftenservice Het is voor leden van de vereniging mogelijk om via het secretariaat recente proefschriften aan te vragen. Aan toekomstige promovendi wordt verzocht om een exemplaar van hun proefschrift toe te zenden aan het secretariaat onder vermelding van correspondentie-adres, zodat aanvragen doorgestuurd kunnen worden naar de promovendus. Recente proefschriften: - 2 december 2009 Esther M.E. van Straten: Metabolic programming of lipid metabolism: Effects of prenatal pharmacological and nutritional interference - 21 oktober 2009 Maaike Oosterveer: Control of metabolic flux by nutrient sensors - 30 september 2009 Marijke Schreurs: Regulatory enzymes of mitochondrial β-oxidation as targets for treatment of the metabolic syndrome - 7 september 2009 Jannes Woudenberg: Novel aspects of peroxisome composition and function in the liver - 29 april 2009 Jaap Mulder: Towards treatment of cholestatic liver disease in children via interference with transcriptional regulation of hepatic transport systems - 28 april 2009 Peter V.E. van den Berghe: Posttranslational regulation of copper transporters - 24 april 2009 Astrid van der Velde: Novel insights in cholesterol excretion - 17 december 2008 Esmé Waanders: Insights in the molecular pathogenesis of polycystic liver disease: a view from different perspectives - 15 december 2008 Sandra Dunning: Resistance of activated stellate cells to cell death in liver fibrosis: mechanisms and targets for intervention - 8 december 2008 Carlijn Buis: Molecular and biochemical mechanisms of bile duct injury after liver transplantation Adres van het secretariaat van de Nederlandse Vereniging voor Hepatologie: Postbus 657, 2003 RR HAARLEM 19
20 Baraclude : Helps hold back resistance year after year January 2010 NLBC-K HQ09PM037(10) in nucleos(t)ide analogue (NA)-naïve patients up to Year 5 1,2 Please see prescribing information overleaf. Standing strong against resistance in NA-naïve patients NLBC_K0001_AD210x280_v2.indd 1 NLBC-K0001 Trim 210x280mm 2/4/10 9:50 AM Baraclude for NA-naïve chronic hepatitis B patients 2,3 Effective viral suppression and a high genetic barrier protects against resistance long-term 2,4 Undetectable viral load* achieved in 93% of a 5-year treatment** cohort of Baraclude-treated NA-naïve patients (n=108) 2 <1% virological breakthrough due to genotypic Baraclude resistance in NA-naïve patients from a treatment cohort up to Year 5 1 *HBV DNA measured using Roche COBAS Amplicor PCR assay (LLOQ=300 copies/ml). **Patients enrolling in the open-label rollover cohort Trial 901 for long-term efficacy analysis initially received a combination of Baraclude 1mg and lamivudine 100mg daily. Subsequently the protocol was amended for patients to receive monotherapy with Baraclude 1mg daily. The Baraclude-treated NA-naïve cohort consisted of 108 patients at Week 240, initially treated in Trials 022 (HBeAg-positive patients, n=103) and 027 (HBeAg-negative patients, n=5) who were subsequently enrolled in the open-label rollover cohort Trial 901. Virological breakthrough defined as 1 log 10 increase from nadir by PCR. Calculated as the cumulative probability through 240 weeks. All nucleoside-naïve patients with detectable HBV DNA ( 300 copies/ml) at Week 48, Week 96, Week 144, Week 192, Week 240 or end of treatment were monitored for resistance. Different dosing regimen after 96 weeks; for more information please refer to SPC. The Baraclude-treated NA-naïve resistance cohort consisted of 663, 278, 149, 120 and 108 patients at Week 48, , 192 and 240, respectively, initially treated in Trials 022 (HBeAg-positive patients) and 027 (HBeAg-negative patients) who were subsequently enrolled in the open-label rollover cohort Trial 901. January 2010 NLBC-K HQ09PM037(10) Please see prescribing information overleaf. Standing strong against resistance in NA-naïve patients
Bijlage : relevante rubrieken van de bijsluiter die werden herwerkt (de veranderingen in de tekst zijn onderlijnd)
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL PegIntron 50 microgram poeder en oplosmiddel voor oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL PegIntron 50 microgram poeder en oplosmiddel voor oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke
SAMENVATTING VAN DE PRODUCTKENMERKEN
 Samenvatting van de productkenmerken (SmPC) Pagina 1/32 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Rebetol 200 mg harde capsules 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke
Samenvatting van de productkenmerken (SmPC) Pagina 1/32 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Rebetol 200 mg harde capsules 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke
VICTRELIS Boceprevir
 De gezondheidsautoriteiten van de EU hebben een aantal voorwaarden gekoppeld aan het in de handel brengen van het geneesmiddel VICTRELIS. Het verplichte plan voor risicobeperking in België, waarvan deze
De gezondheidsautoriteiten van de EU hebben een aantal voorwaarden gekoppeld aan het in de handel brengen van het geneesmiddel VICTRELIS. Het verplichte plan voor risicobeperking in België, waarvan deze
Uw behandeling met YERVOY (ipilimumab)
 Uw behandeling met YERVOY (ipilimumab) Patiëntenfolder YERVOY is onderworpen aan aanvullende monitoring. U wordt verzocht alle vermoedelijke bijwerkingen te melden. Dit educatieve materiaal is een verplichte
Uw behandeling met YERVOY (ipilimumab) Patiëntenfolder YERVOY is onderworpen aan aanvullende monitoring. U wordt verzocht alle vermoedelijke bijwerkingen te melden. Dit educatieve materiaal is een verplichte
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN. Medicinal product no longer authorised
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL Ribavirine BioPartners 200 mg filmomhulde tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke Ribavirine BioPartners
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL Ribavirine BioPartners 200 mg filmomhulde tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke Ribavirine BioPartners
hoofdstuk 3 hoofdstuk 4 hoofdstuk 5
 Samenvatting Samenvatting De lever heeft een aantal belangrijke functies, waaronder het produceren van gal en het verwerken en afbreken van schadelijke verbindingen. Zij bestaat uit verschillende soorten
Samenvatting Samenvatting De lever heeft een aantal belangrijke functies, waaronder het produceren van gal en het verwerken en afbreken van schadelijke verbindingen. Zij bestaat uit verschillende soorten
KEYTRUDA (pembrolizumab)
 Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab) voor patiënten KEYTRUDA (pembrolizumab) Patiënteninformatiefolder Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab)
Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab) voor patiënten KEYTRUDA (pembrolizumab) Patiënteninformatiefolder Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab)
Verkorte SKP - MOVICOL Vloeibaar Sinaasappelsmaak - Juni 2013
 Verkorte SKP - MOVICOL Vloeibaar Sinaasappelsmaak - Juni 2013 Naam van het geneesmiddel: MOVICOL Vloeibaar Sinaasappelsmaak, concentraat voor drank Kwalitatieve en kwantitatieve samenstelling: Elke 25
Verkorte SKP - MOVICOL Vloeibaar Sinaasappelsmaak - Juni 2013 Naam van het geneesmiddel: MOVICOL Vloeibaar Sinaasappelsmaak, concentraat voor drank Kwalitatieve en kwantitatieve samenstelling: Elke 25
I N H O U D Bestuurszaken Basaal onderzoek Klinisch onderzoek Mededelingen Nieuws Congresagenda
 Nieuwsbulletin van de Nederlandse Vereniging voor Hepatologie I N H O U D Bestuurszaken Basaal onderzoek Klinisch onderzoek Mededelingen Nieuws Congresagenda Jaargang 33, nr.2 Mei 2009 C o l o f o n C
Nieuwsbulletin van de Nederlandse Vereniging voor Hepatologie I N H O U D Bestuurszaken Basaal onderzoek Klinisch onderzoek Mededelingen Nieuws Congresagenda Jaargang 33, nr.2 Mei 2009 C o l o f o n C
Zwangerschap bij chronische ontstekingsziekten van de darm
 Zwangerschap bij chronische ontstekingsziekten van de darm Inleiding Zwanger worden als je een chronische ontstekingsziekte van de darm (IBD = inflammatory Bowel disease) hebt zoals de ziekte van Crohn
Zwangerschap bij chronische ontstekingsziekten van de darm Inleiding Zwanger worden als je een chronische ontstekingsziekte van de darm (IBD = inflammatory Bowel disease) hebt zoals de ziekte van Crohn
Behandeling van Hepatitis C
 Behandeling van Hepatitis C MDL-centrum IJsselland Ziekenhuis www.mdlcentrum.nl Inleiding Uw behandelend arts heeft bij u Hepatitis C geconstateerd. De MDL-verpleegkundige gaat u begeleiden bij het behandelen
Behandeling van Hepatitis C MDL-centrum IJsselland Ziekenhuis www.mdlcentrum.nl Inleiding Uw behandelend arts heeft bij u Hepatitis C geconstateerd. De MDL-verpleegkundige gaat u begeleiden bij het behandelen
 Samenvatting Samenvatting Bij patiënten die met antikanker geneesmiddelen worden behandeld wordt een grote interindividuele variabiliteit gezien in de antitumor werking en de bijwerkingen. Naast klinische
Samenvatting Samenvatting Bij patiënten die met antikanker geneesmiddelen worden behandeld wordt een grote interindividuele variabiliteit gezien in de antitumor werking en de bijwerkingen. Naast klinische
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Patiëntenfolder
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
Elke tablet bevat: 20 mg esomeprazol als esomeprazol magnesium(amorf) Hulpstoffen gekend effect: Elke tablet bevat ook maximaal 27,45 mg sucrose.
 NAAM VAN HET GENEESMIDDEL Esomeprazole Apotex 20 mg maagsapresistente tabletten Esomeprazole Apotex 40 mg maagsapresistente tabletten KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke tablet bevat: 20 mg
NAAM VAN HET GENEESMIDDEL Esomeprazole Apotex 20 mg maagsapresistente tabletten Esomeprazole Apotex 40 mg maagsapresistente tabletten KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke tablet bevat: 20 mg
Gerenvooieerde versie CALCIPOTRIOL 50 MICROGRAM/G ZALF PCH zalf
 1.3.1 : Productinformatie Bladzijde : 1 1. NAAM VAN HET GENEESMIDDEL Calcipotriol 50 microgram/g PCH,. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Zalf: calcipotriol 50 microgram per gram. Hulpstoffen:
1.3.1 : Productinformatie Bladzijde : 1 1. NAAM VAN HET GENEESMIDDEL Calcipotriol 50 microgram/g PCH,. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Zalf: calcipotriol 50 microgram per gram. Hulpstoffen:
Toolbox-meeting Het gevaar van naalden (van junks) in de liftput
 Toolbox-meeting Het gevaar van naalden (van junks) in de liftput Inleiding Monteurs van vooral de service en reparatie&renovatie lopen een kans geïnfecteerd te raken met een virus, tengevolge van het (per
Toolbox-meeting Het gevaar van naalden (van junks) in de liftput Inleiding Monteurs van vooral de service en reparatie&renovatie lopen een kans geïnfecteerd te raken met een virus, tengevolge van het (per
MAPROTILINE HCl 25-50 - 75 PCH tabletten. MODULE I : ALGEMENE GEGEVENS Datum : 29 februari 2008 1.3.3 : Bijsluiter Bladzijde : 1
 1.3.3 : Bijsluiter Bladzijde : 1 Pharmachemie B.V. Swensweg 5 Postbus 552 2003 RN Haarlem INFORMATIE VOOR DE PATIËNT SAMENSTELLING Per tablet: respectievelijk 25 mg, 50 mg en 75 mg maprotilinehydrochloride.
1.3.3 : Bijsluiter Bladzijde : 1 Pharmachemie B.V. Swensweg 5 Postbus 552 2003 RN Haarlem INFORMATIE VOOR DE PATIËNT SAMENSTELLING Per tablet: respectievelijk 25 mg, 50 mg en 75 mg maprotilinehydrochloride.
ESSENTIELE GEGEVENS. Voor de volledige lijst van hulpstoffen, zie rubriek Lijst van hulpstoffen van de SKP.
 ESSENTIELE GEGEVENS 1. NAAM VAN HET GENEESMIDDEL Onglyza 2,5 mg, filmomhulde tabletten Onglyza 5 mg, filmomhulde tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Onglyza 2,5 mg: iedere tablet bevat
ESSENTIELE GEGEVENS 1. NAAM VAN HET GENEESMIDDEL Onglyza 2,5 mg, filmomhulde tabletten Onglyza 5 mg, filmomhulde tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Onglyza 2,5 mg: iedere tablet bevat
KEYTRUDA (pembrolizumab)
 Risicominimalisatiemateriaal betreffende Keytruda (pembrolizumab) voor patiënten KEYTRUDA (pembrolizumab) Patiënteninformatiefolder Risicominimalisatiemateriaal betreffende Keytruda (pembrolizumab) voor
Risicominimalisatiemateriaal betreffende Keytruda (pembrolizumab) voor patiënten KEYTRUDA (pembrolizumab) Patiënteninformatiefolder Risicominimalisatiemateriaal betreffende Keytruda (pembrolizumab) voor
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL Pegasys 135 microgram oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke injectieflacon van 1 ml oplossing
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL Pegasys 135 microgram oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke injectieflacon van 1 ml oplossing
UW NIEUWE COPD BEHANDELING
 Patiëntenkaart UW NIEUWE COPD BEHANDELING Lees ook aandachtig de bijsluiter voordat u met dit geneesmiddel begint. q Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe
Patiëntenkaart UW NIEUWE COPD BEHANDELING Lees ook aandachtig de bijsluiter voordat u met dit geneesmiddel begint. q Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe
PARONAL I.E. PARONAL I.E.
 P2-1/5 BIJSLUITERTEKST Lees de hele bijsluiter aandachtig door alvorens dit geneesmiddel te gebruiken. Bewaar deze bijsluiter, misschien heeft u hem nog een keer nodig. Raadpleeg uw arts of apotheker,
P2-1/5 BIJSLUITERTEKST Lees de hele bijsluiter aandachtig door alvorens dit geneesmiddel te gebruiken. Bewaar deze bijsluiter, misschien heeft u hem nog een keer nodig. Raadpleeg uw arts of apotheker,
Mission Statement. Ad 2a) Er zal naar verwachting een veel grotere opkomst zijn tijdens de gezamenlijke sessies op beide vergaderdagen.
 Mission Statement Voorstel voor samenwerking van de sectie Experimentele Gastroenterologie (SEG) van de NVGE en de sectie Basale Hepatologie (SBH) van de NVH I. De voorgestelde samenwerking heeft tot doel
Mission Statement Voorstel voor samenwerking van de sectie Experimentele Gastroenterologie (SEG) van de NVGE en de sectie Basale Hepatologie (SBH) van de NVH I. De voorgestelde samenwerking heeft tot doel
STANDPUNTEN ANAKINRA (VOORLOPIGE BEHANDELRICHTLIJN) Oktober 2002
 NVR map Anakinra 12-03-2003 09:36 Pagina 1 STANDPUNTEN ANAKINRA (VOORLOPIGE BEHANDELRICHTLIJN) Oktober 2002 NVR map Anakinra 12-03-2003 09:36 Pagina 2 De door de gepubliceerde richtlijnen en standpunten
NVR map Anakinra 12-03-2003 09:36 Pagina 1 STANDPUNTEN ANAKINRA (VOORLOPIGE BEHANDELRICHTLIJN) Oktober 2002 NVR map Anakinra 12-03-2003 09:36 Pagina 2 De door de gepubliceerde richtlijnen en standpunten
BIJSLUITER: INFORMATIE VOOR GEBRUIKERS. FERCAYL 100mg/2ml Oplossing voor injectie / infusie. Ijzer (element) in de vorm van ijzer dextraan complex
 BIJSLUITER: INFORMATIE VOOR GEBRUIKERS FERCAYL 100mg/2ml Oplossing voor injectie / infusie Ijzer (element) in de vorm van ijzer dextraan complex Lees goed de hele bijsluiter voordat u dit geneesmiddel
BIJSLUITER: INFORMATIE VOOR GEBRUIKERS FERCAYL 100mg/2ml Oplossing voor injectie / infusie Ijzer (element) in de vorm van ijzer dextraan complex Lees goed de hele bijsluiter voordat u dit geneesmiddel
 PUBLICATIONS Langers P, Cremers SCLM, den Hartigh J, Veenendaal RA, ten Hove WR, Ringers J, Lamers CBHW, van Hoek B. Switching monitoring of emulsified cyclosporine from trough level to 2-hour level in
PUBLICATIONS Langers P, Cremers SCLM, den Hartigh J, Veenendaal RA, ten Hove WR, Ringers J, Lamers CBHW, van Hoek B. Switching monitoring of emulsified cyclosporine from trough level to 2-hour level in
NRLP-12 Gerelateerde Terugkerende Koorts
 www.printo.it/pediatric-rheumatology/be_fm/intro NRLP-12 Gerelateerde Terugkerende Koorts Versie 2016 1. WAT IS NRLP-12 GERELATEERDE TERUGKERENDE KOORTS 1.1 Wat is het? NRLP-12 gerelateerde terugkerende
www.printo.it/pediatric-rheumatology/be_fm/intro NRLP-12 Gerelateerde Terugkerende Koorts Versie 2016 1. WAT IS NRLP-12 GERELATEERDE TERUGKERENDE KOORTS 1.1 Wat is het? NRLP-12 gerelateerde terugkerende
HEPATITIS B. J.W. den Ouden-Muller internist Rotterdam
 HEPATITIS B J.W. den Ouden-Muller internist Rotterdam Wat is Hepatitis B? Hepatitis B is een ontsteking van de lever veroorzaakt door het hepatitis B virus (HBV) en is een van de meest voorkomende infectieziekten
HEPATITIS B J.W. den Ouden-Muller internist Rotterdam Wat is Hepatitis B? Hepatitis B is een ontsteking van de lever veroorzaakt door het hepatitis B virus (HBV) en is een van de meest voorkomende infectieziekten
Hepatitis C, een update. Vincent Rijckborst, Maag-Darm-Leverarts Milan J. Sonneveld, AIOS Maag-Darm-Leverziekten
 Hepatitis C, een update Vincent Rijckborst, Maag-Darm-Leverarts Milan J. Sonneveld, AIOS Maag-Darm-Leverziekten Disclosures spreker (potentiële) belangenverstrengeling Voor bijeenkomst mogelijk relevante
Hepatitis C, een update Vincent Rijckborst, Maag-Darm-Leverarts Milan J. Sonneveld, AIOS Maag-Darm-Leverziekten Disclosures spreker (potentiële) belangenverstrengeling Voor bijeenkomst mogelijk relevante
Nederlandse samenvatting. (summary in Dutch)
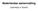 (summary in Dutch) Type 2 diabetes is een chronische ziekte, waarvan het voorkomen wereldwijd fors toeneemt. De ziekte wordt gekarakteriseerd door chronisch verhoogde glucose spiegels, wat op den duur
(summary in Dutch) Type 2 diabetes is een chronische ziekte, waarvan het voorkomen wereldwijd fors toeneemt. De ziekte wordt gekarakteriseerd door chronisch verhoogde glucose spiegels, wat op den duur
Voorlichtingsmateriaal betreffende sebelipase alfa voor de zorgverlener. Belangrijke veiligheidsinformatie
 Voorlichtingsmateriaal betreffende sebelipase alfa voor de zorgverlener Belangrijke veiligheidsinformatie Risico minimalisatie materiaal betreffende sebelipase alfa voor zorgverleners - versie 2-03/2018
Voorlichtingsmateriaal betreffende sebelipase alfa voor de zorgverlener Belangrijke veiligheidsinformatie Risico minimalisatie materiaal betreffende sebelipase alfa voor zorgverleners - versie 2-03/2018
IntronA 18 miljoen IE oplossing voor injectie in multi-dosis pen SAMENVATTING VAN DE PRODUCTKENMERKEN
 Samenvatting van de productkenmerken (SmPC) Pagina 1/27 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL IntronA 18 miljoen IE oplossing voor injectie in multi-dosis 2. KWALITATIEVE EN
Samenvatting van de productkenmerken (SmPC) Pagina 1/27 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL IntronA 18 miljoen IE oplossing voor injectie in multi-dosis 2. KWALITATIEVE EN
Bijsluiter: informatie voor de patiënt. Removab 10 microgram concentraat voor oplossing voor infusie catumaxomab
 Bijsluiter: informatie voor de patiënt Removab 10 microgram concentraat voor oplossing voor infusie catumaxomab Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
Bijsluiter: informatie voor de patiënt Removab 10 microgram concentraat voor oplossing voor infusie catumaxomab Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
Ustekinumab. (Stelara) Dermatologie
 Ustekinumab (Stelara) Dermatologie Inhoudsopgave Inleiding 4 1. Hoe werkt Ustekinumab (Stelara) 4 2. Wat moet u weten voordat u Ustekinumab (Stelara) gebruikt 5 Gebruik Ustekinumab (Stelara) niet 5 Wees
Ustekinumab (Stelara) Dermatologie Inhoudsopgave Inleiding 4 1. Hoe werkt Ustekinumab (Stelara) 4 2. Wat moet u weten voordat u Ustekinumab (Stelara) gebruikt 5 Gebruik Ustekinumab (Stelara) niet 5 Wees
BELANGRIJKE VEILIGHEIDSINFORMATIE
 Aanbevelingen Neem de volledige medische voorgeschiedenis van de patiënt in overweging, inclusief enig eerder of gelijktijdig gebruikte biological BELANGRIJKE VEILIGHEIDSINFORMATIE Er is geen ervaring
Aanbevelingen Neem de volledige medische voorgeschiedenis van de patiënt in overweging, inclusief enig eerder of gelijktijdig gebruikte biological BELANGRIJKE VEILIGHEIDSINFORMATIE Er is geen ervaring
Downloaded from UvA-DARE, the institutional repository of the University of Amsterdam (UvA)
 Downloaded from UvA-DARE, the institutional repository of the University of Amsterdam (UvA) http://hdl.handle.net/11245/2.63195 File ID Filename Version uvapub:63195 Chapter 9: Samenvatting final SOURCE
Downloaded from UvA-DARE, the institutional repository of the University of Amsterdam (UvA) http://hdl.handle.net/11245/2.63195 File ID Filename Version uvapub:63195 Chapter 9: Samenvatting final SOURCE
Nederlandse samenvatting
 Nederlandse samenvatting Nederlandse samenvatting Samenvatting Levertransplantatie is de aangewezen behandeling voor patiënten met eindstadium leverfalen. Het succespercentage van een transplantatie is
Nederlandse samenvatting Nederlandse samenvatting Samenvatting Levertransplantatie is de aangewezen behandeling voor patiënten met eindstadium leverfalen. Het succespercentage van een transplantatie is
YERVOY. (ipilimumab) Concentraat voor oplossing voor infusie Dit geneesmiddel is onderworpen aan aanvullende monitoring.
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
BIJLAGE III WIJZIGINGSVOORSTELLENEN VOOR DE SAMENVATTING VAN DE PRODUCTKENMERKEN EN DE BIJSLUITER
 BIJLAGE III WIJZIGINGSVOORSTELLENEN VOOR DE SAMENVATTING VAN DE PRODUCTKENMERKEN EN DE BIJSLUITER 1 WIJZIGINGVOORSTELLEN AAN TE BRENGEN IN DE RELEVANTE RUBRIEKEN VAN DE SAMENVATTING VAN DE PRODUCTKENMERKEN
BIJLAGE III WIJZIGINGSVOORSTELLENEN VOOR DE SAMENVATTING VAN DE PRODUCTKENMERKEN EN DE BIJSLUITER 1 WIJZIGINGVOORSTELLEN AAN TE BRENGEN IN DE RELEVANTE RUBRIEKEN VAN DE SAMENVATTING VAN DE PRODUCTKENMERKEN
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL Ribavirine BioPartners 200 mg filmomhulde tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke Ribavirine BioPartners
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL Ribavirine BioPartners 200 mg filmomhulde tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke Ribavirine BioPartners
VALDOXAN. (agomelatine) Informatie voor beroepsbeoefenaren in de gezondheidszorg: Aanbevelingen met betrekking tot:
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Valdoxan 25 mg. Het verplicht plan voor risicobeperking in België, waarvan deze
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Valdoxan 25 mg. Het verplicht plan voor risicobeperking in België, waarvan deze
Risico minimalisatie materiaal betreffende Aripiprazol Sandoz (aripiprazol)
 Risico minimalisatie materiaal betreffende Aripiprazol Sandoz (aripiprazol) Dit risico materiaal is beoordeeld door het College ter Beoordeling van Geneesmiddelen (CBG) en beschrijft aanbevelingen voor
Risico minimalisatie materiaal betreffende Aripiprazol Sandoz (aripiprazol) Dit risico materiaal is beoordeeld door het College ter Beoordeling van Geneesmiddelen (CBG) en beschrijft aanbevelingen voor
1.3.1.3 Package leaflet 1.3.1.3-1
 1.3.1.3 Package leaflet 1.3.1.3-1 Patiëntenbijsluiter PARACETAMOL/VITAMINE C 500/50 MG DRANK BIJ VERKOUDHEID, poeder voor drank Lees deze bijsluiter zorgvuldig door, want deze bevat belangrijke informatie
1.3.1.3 Package leaflet 1.3.1.3-1 Patiëntenbijsluiter PARACETAMOL/VITAMINE C 500/50 MG DRANK BIJ VERKOUDHEID, poeder voor drank Lees deze bijsluiter zorgvuldig door, want deze bevat belangrijke informatie
Biotransformatie en toxiciteit van
 Biotransformatie en toxiciteit van paracetamol 062 1 Biotransformatie en toxiciteit van paracetamol Inleiding Paracetamol is het farmacologisch actieve bestanddeel van een groot aantal vrij en op recept
Biotransformatie en toxiciteit van paracetamol 062 1 Biotransformatie en toxiciteit van paracetamol Inleiding Paracetamol is het farmacologisch actieve bestanddeel van een groot aantal vrij en op recept
Postdatum. Geachte Dokter,
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Quetiapine Krka 50 mg / 200 mg / 300 mg/400 mg tabletten met verlengde afgifte.
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Quetiapine Krka 50 mg / 200 mg / 300 mg/400 mg tabletten met verlengde afgifte.
www.virology-education.nl
 HEPATITIS MASTERCLASS UTRECHT 2016-2017 MEETING PROSPECTUS www.virology-education.nl INHOUD Introductie... 3 Meeting beschrijving... 4 Achtergrond... 4 Leerdoelen... 4 Opzet... 4 Doelgroep... 4 Voorzitters...
HEPATITIS MASTERCLASS UTRECHT 2016-2017 MEETING PROSPECTUS www.virology-education.nl INHOUD Introductie... 3 Meeting beschrijving... 4 Achtergrond... 4 Leerdoelen... 4 Opzet... 4 Doelgroep... 4 Voorzitters...
Mijn kind heeft diarree
 Mijn kind heeft diarree Beste ouders, Uw kind heeft diarree. In deze brochure vindt u een antwoord op de meeste vragen en ook praktische tips, opdat dit tijdelijk ongemak u geen onnodige hoofdbrekens zou
Mijn kind heeft diarree Beste ouders, Uw kind heeft diarree. In deze brochure vindt u een antwoord op de meeste vragen en ook praktische tips, opdat dit tijdelijk ongemak u geen onnodige hoofdbrekens zou
WAARVOOR WORDT HET GEBRUIKT?
 BIJSLUITER Lees de hele bijsluiter aandachtig door, omdat er voor u belangrijke informatie in staat. Dit geneesmiddel is zonder voorschrift verkrijgbaar. Desalniettemin dient u LORATADINE TEVA zorgvuldig
BIJSLUITER Lees de hele bijsluiter aandachtig door, omdat er voor u belangrijke informatie in staat. Dit geneesmiddel is zonder voorschrift verkrijgbaar. Desalniettemin dient u LORATADINE TEVA zorgvuldig
1.3.1.3 Package Leaflet 1.3.1.3-1
 1.3.1.3 Package Leaflet 1.3.1.3-1 Patiëntenbijsluiter ETOS PARACETAMOL/VITAMINE C 500/50 MG DRANK, poeder voor drank Lees deze bijsluiter zorgvuldig door, want deze bevat belangrijke informatie voor u.
1.3.1.3 Package Leaflet 1.3.1.3-1 Patiëntenbijsluiter ETOS PARACETAMOL/VITAMINE C 500/50 MG DRANK, poeder voor drank Lees deze bijsluiter zorgvuldig door, want deze bevat belangrijke informatie voor u.
Het syndroom van Klinefelter: Screening en opvolging van metabole afwijkingen. David Unuane Endocrinologie Klinefelter Kliniek
 Het syndroom van Klinefelter: Screening en opvolging van metabole afwijkingen David Unuane Endocrinologie Klinefelter Kliniek Achtergrond Het Klinefelter syndroom(ks): Genetisch kenmerk extra X-chromosoom:
Het syndroom van Klinefelter: Screening en opvolging van metabole afwijkingen David Unuane Endocrinologie Klinefelter Kliniek Achtergrond Het Klinefelter syndroom(ks): Genetisch kenmerk extra X-chromosoom:
Periodieke Koorts met Afteuze Faryngitis en Adenitis (PFAPA)
 www.printo.it/pediatric-rheumatology/be_fm/intro Periodieke Koorts met Afteuze Faryngitis en Adenitis (PFAPA) Versie 2016 1. WAT IS PFAPA 1.1 Wat is het? PFAPA staat voor Periodic Fever Adenitis Pharyngitis
www.printo.it/pediatric-rheumatology/be_fm/intro Periodieke Koorts met Afteuze Faryngitis en Adenitis (PFAPA) Versie 2016 1. WAT IS PFAPA 1.1 Wat is het? PFAPA staat voor Periodic Fever Adenitis Pharyngitis
De ziekte van Alzheimer. Diagnose
 De ziekte van Alzheimer Bij dementie is er sprake van een globale achteruitgang van de cognitieve functies, zoals het geheugen of de taalfuncties. Deze achteruitgang leidt tot functionele beperkingen in
De ziekte van Alzheimer Bij dementie is er sprake van een globale achteruitgang van de cognitieve functies, zoals het geheugen of de taalfuncties. Deze achteruitgang leidt tot functionele beperkingen in
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKERS. Removab 10 microgram concentraat voor oplossing voor infusie catumaxomab
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKERS Removab 10 microgram concentraat voor oplossing voor infusie catumaxomab Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken - Bewaar deze bijsluiter.
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKERS Removab 10 microgram concentraat voor oplossing voor infusie catumaxomab Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken - Bewaar deze bijsluiter.
Doorbraak in onderzoek naar ME
 Doorbraak in onderzoek naar ME Gezaghebbende Amerikaanse overheidsinstanties hebben opnieuw bij MEpatiënten een virus aangetroffen. Al eerder berichtte EenVandaag over de ontdekking van het XMRV-virus
Doorbraak in onderzoek naar ME Gezaghebbende Amerikaanse overheidsinstanties hebben opnieuw bij MEpatiënten een virus aangetroffen. Al eerder berichtte EenVandaag over de ontdekking van het XMRV-virus
Bijlage III. Aanpassingen aan relevante rubrieken van de samenvatting van de productkenmerken en bijsluiters
 Bijlage III Aanpassingen aan relevante rubrieken van de samenvatting van de productkenmerken en bijsluiters Opmerking: Het kan zijn dat de aanpassingen aan de samenvatting van de productkenmerken en bijsluiters
Bijlage III Aanpassingen aan relevante rubrieken van de samenvatting van de productkenmerken en bijsluiters Opmerking: Het kan zijn dat de aanpassingen aan de samenvatting van de productkenmerken en bijsluiters
HUIDIGE BEHANDELING VAN CHRONISCHE HEPATITIS-B-VIRUSINFECTIE VOLGENS DE RICHTLIJNEN
 HUIDIGE BEHANDELING VAN CHRONISCHE HEPATITIS-B-VIRUSINFECTIE VOLGENS DE RICHTLIJNEN Nederlandse richtlijn? (2008 en 2012) AASLD richtlijn? (2009) EASL richtlijn? (2012) Met dank aan Erik Buster en de overige
HUIDIGE BEHANDELING VAN CHRONISCHE HEPATITIS-B-VIRUSINFECTIE VOLGENS DE RICHTLIJNEN Nederlandse richtlijn? (2008 en 2012) AASLD richtlijn? (2009) EASL richtlijn? (2012) Met dank aan Erik Buster en de overige
RMA gewijzigde versie 10/2017 KEYTRUDA. (pembrolizumab) Dit geneesmiddel is onderworpen aan aanvullende monitoring. Patiëntenwaarschuwingskaart
 RMA gewijzigde versie 10/2017 KEYTRUDA (pembrolizumab) Dit geneesmiddel is onderworpen aan aanvullende monitoring. Patiëntenwaarschuwingskaart Bewaar deze kaart altijd bij u en laat deze kaart zien aan
RMA gewijzigde versie 10/2017 KEYTRUDA (pembrolizumab) Dit geneesmiddel is onderworpen aan aanvullende monitoring. Patiëntenwaarschuwingskaart Bewaar deze kaart altijd bij u en laat deze kaart zien aan
Wat u zou moeten weten over Rixathon
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Rixathon. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Rixathon. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING. Actief bestanddeel: Gezuiverd capsulair Vi polyoside van Salmonella typhi (stam Ty2): 25 microgram
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL TYPHIM Vi, 25 microgram/dosis, oplossing voor injectie Polyoside buiktyfusvaccin 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Eén dosis
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL TYPHIM Vi, 25 microgram/dosis, oplossing voor injectie Polyoside buiktyfusvaccin 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Eén dosis
Patiënteninformatie over ernstige primaire IGF-1-deficiëntie en hoe Increlex daarbij kan helpen
 Ipsen Endocrinologie Increlex (injectie met mecasermine [rdna-herkomst]) Patiënteninformatie over ernstige primaire IGF-1-deficiëntie en hoe Increlex daarbij kan helpen Voorlichtingsfolder zoals beschreven
Ipsen Endocrinologie Increlex (injectie met mecasermine [rdna-herkomst]) Patiënteninformatie over ernstige primaire IGF-1-deficiëntie en hoe Increlex daarbij kan helpen Voorlichtingsfolder zoals beschreven
infuusbehandeling met remicade
 patiënteninformatie infuusbehandeling met remicade U heeft in overleg met uw arts besloten tot een infuusbehandeling met Remicade. In deze folder geven wij informatie over dit geneesmiddel, wat de bijwerkingen
patiënteninformatie infuusbehandeling met remicade U heeft in overleg met uw arts besloten tot een infuusbehandeling met Remicade. In deze folder geven wij informatie over dit geneesmiddel, wat de bijwerkingen
Voor langdurige behandeling: bewijs van cardiale valvulopathie als vastgesteld door middel van echocardiografie voorafgaand aan de behandeling.
 RUBRIEKEN VAN DE SAMENVATTING VAN DE PRODUCTKENMERKEN VOOR CABERGOLINE BEVATTENDE PRODUCTEN 4.2 Dosering en wijze van toediening Beperking van de maximumdosis tot 3 mg/dag 4.3 Contra-indicaties Voor langdurige
RUBRIEKEN VAN DE SAMENVATTING VAN DE PRODUCTKENMERKEN VOOR CABERGOLINE BEVATTENDE PRODUCTEN 4.2 Dosering en wijze van toediening Beperking van de maximumdosis tot 3 mg/dag 4.3 Contra-indicaties Voor langdurige
Nederlandse Samenvatting
 Nederlandse Samenvatting Het aantal mensen met een gestoorde nierfunctie is de afgelopen decennia sterk toegenomen. Dit betekent dat er steeds meer mensen moeten dialyseren of een niertransplantatie moeten
Nederlandse Samenvatting Het aantal mensen met een gestoorde nierfunctie is de afgelopen decennia sterk toegenomen. Dit betekent dat er steeds meer mensen moeten dialyseren of een niertransplantatie moeten
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL 135 microgram oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING peginterferon alfa-2a * 135 microgram
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL 135 microgram oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING peginterferon alfa-2a * 135 microgram
1. NAAM VAN HET GENEESMIDDEL. SORBITOL DELALANDE 5 g poeder voor drank. SORBITOL DELALANDE Menthe 5 g poeder voor drank.
 1. NAAM VAN HET GENEESMIDDEL SORBITOL DELALANDE 5 g poeder voor drank. SORBITOL DELALANDE Menthe 5 g poeder voor drank. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Sorbitol 5 g per zakje. Voor de volledige
1. NAAM VAN HET GENEESMIDDEL SORBITOL DELALANDE 5 g poeder voor drank. SORBITOL DELALANDE Menthe 5 g poeder voor drank. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Sorbitol 5 g per zakje. Voor de volledige
infuusbehandeling met remicade
 patiënteninformatie infuusbehandeling met remicade U heeft in overleg met uw arts besloten tot een infuusbehandeling met het geneesmiddel Remicade. In deze folder geven wij informatie over dit geneesmiddel,
patiënteninformatie infuusbehandeling met remicade U heeft in overleg met uw arts besloten tot een infuusbehandeling met het geneesmiddel Remicade. In deze folder geven wij informatie over dit geneesmiddel,
als u duidelijke tekens van de ziekte van Parkinson of andere bewegingsstoornissen vertoont.
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER SIBELIUM 10 mg tabletten flunarizine Lees de hele bijsluiter zorgvuldig door voordat u start met het gebruik van dit geneesmiddel. - Bewaar deze bijsluiter.
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER SIBELIUM 10 mg tabletten flunarizine Lees de hele bijsluiter zorgvuldig door voordat u start met het gebruik van dit geneesmiddel. - Bewaar deze bijsluiter.
(MSD Belgium BVBA/SPRL)
 Farmaceutisch bedrijf (MSD Belgium BVBA/SPRL) 1. NAAM VAN HET GENEESMIDDEL PegIntron 150 microgram poeder en oplosmiddel voor oplossing voor injectie in voorgevulde pen 2. KWALITATIEVE EN KWANTITATIEVE
Farmaceutisch bedrijf (MSD Belgium BVBA/SPRL) 1. NAAM VAN HET GENEESMIDDEL PegIntron 150 microgram poeder en oplosmiddel voor oplossing voor injectie in voorgevulde pen 2. KWALITATIEVE EN KWANTITATIEVE
Juveniele Spondylartropathie/Enthesitis Gerelateerde Artritis (SPA-ERA)
 www.printo.it/pediatric-rheumatology/be_fm/intro Juveniele Spondylartropathie/Enthesitis Gerelateerde Artritis (SPA-ERA) Versie 2016 1. WAT IS JUVENIELE SPONDYLARTROPATHIE/ENTHESITIS GERELATEERDE ARTRITIS
www.printo.it/pediatric-rheumatology/be_fm/intro Juveniele Spondylartropathie/Enthesitis Gerelateerde Artritis (SPA-ERA) Versie 2016 1. WAT IS JUVENIELE SPONDYLARTROPATHIE/ENTHESITIS GERELATEERDE ARTRITIS
Icterus na tropenbezoek. Sophie Willemse Maag-Darm-Leverarts Academisch Medisch Centrum
 Icterus na tropenbezoek Sophie Willemse Maag-Darm-Leverarts Academisch Medisch Centrum Casus 1 Man, 51 jaar Voorgeschiedenis Niertransplantatie prednison, cellcept en tacrolimus M. Bechterew etanercept
Icterus na tropenbezoek Sophie Willemse Maag-Darm-Leverarts Academisch Medisch Centrum Casus 1 Man, 51 jaar Voorgeschiedenis Niertransplantatie prednison, cellcept en tacrolimus M. Bechterew etanercept
SAMENVATTING VAN DE PRODUCTKENMERKEN
 Samenvatting van de productkenmerken (SmPC) Pagina 1/39 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL PegIntron 100 microgram poeder en oplosmiddel voor oplossing 2. KWALITATIEVE EN
Samenvatting van de productkenmerken (SmPC) Pagina 1/39 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL PegIntron 100 microgram poeder en oplosmiddel voor oplossing 2. KWALITATIEVE EN
HET PARTNER-ONDERZOEK
 Deelnemersinformatie en geïnformeerde voor de HIV-positieve partner HET PARTNER-ONDERZOEK Het PARTNER-onderzoek is een onderzoek naar stellen, waarbij: (i) de ene partner HIV-positief is en de ander HIV-negatief;
Deelnemersinformatie en geïnformeerde voor de HIV-positieve partner HET PARTNER-ONDERZOEK Het PARTNER-onderzoek is een onderzoek naar stellen, waarbij: (i) de ene partner HIV-positief is en de ander HIV-negatief;
REPOSIT (Melanoom) / melanoom
 REPOSIT (Melanoom) / melanoom Onderzoek voor patiënten met een uitgezaaid melanoom die behandeld worden met het combinatiemiddel vemurafenib en cobimetinib. Onderzocht wordt of met behulp van beeldvorming
REPOSIT (Melanoom) / melanoom Onderzoek voor patiënten met een uitgezaaid melanoom die behandeld worden met het combinatiemiddel vemurafenib en cobimetinib. Onderzocht wordt of met behulp van beeldvorming
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER SPASMINE FORTE, 120 MG, CAPSULES, HARD ALVERINE CITRAAT
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER SPASMINE FORTE, 120 MG, CAPSULES, HARD ALVERINE CITRAAT Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat innemen want er staat belangrijke informatie
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER SPASMINE FORTE, 120 MG, CAPSULES, HARD ALVERINE CITRAAT Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat innemen want er staat belangrijke informatie
Apotheek Haagse Ziekenhuizen. SPC Individuele Bereidingen. Clobazam 2 mg, capsule
 1. Naam van het geneesmiddel Clobazam 1 mg, capsule Clobazam 1,5 mg, capsule Clobazam 2,5 mg, capsule 2. Kwalitatieve en kwantitatieve samenstelling Bevat per capsule resp. 1, 1,5, 2 of 2,5 mg clobazam
1. Naam van het geneesmiddel Clobazam 1 mg, capsule Clobazam 1,5 mg, capsule Clobazam 2,5 mg, capsule 2. Kwalitatieve en kwantitatieve samenstelling Bevat per capsule resp. 1, 1,5, 2 of 2,5 mg clobazam
dagziekenhuis inwendige geneeskunde Zoledroninezuur
 dagziekenhuis inwendige geneeskunde Zoledroninezuur Inhoud Zoledroninezuur 3 Voorbereiding 3 Rijvaardigheid en gebruik van machines 3 Gebruik bij ouderen 4 Uitzonderingen bij gebruik 4 Combinatie met andere
dagziekenhuis inwendige geneeskunde Zoledroninezuur Inhoud Zoledroninezuur 3 Voorbereiding 3 Rijvaardigheid en gebruik van machines 3 Gebruik bij ouderen 4 Uitzonderingen bij gebruik 4 Combinatie met andere
Adalimumab (Hyrimoz ) bij IBD
 Adalimumab (Hyrimoz ) bij IBD Uw behandelende arts en/of IBD verpleegkundige heeft met u gesproken over het gebruik van Adalimumab (Hyrimoz ). In deze folder krijgt u informatie over de werking en het
Adalimumab (Hyrimoz ) bij IBD Uw behandelende arts en/of IBD verpleegkundige heeft met u gesproken over het gebruik van Adalimumab (Hyrimoz ). In deze folder krijgt u informatie over de werking en het
a a a a a a a a a a a a a a a a a a a a a a a a a a a
 a a a a a a a a a a a a a a a a a a a a a a a a a a a EXPERIMENTELE LABORATORIA BASAAL ONDERZOEK LEVERTRANSPLANTATIE Basaal onderzoek Levertransplantatie (Senior onderzoeker Luc van der Laan) Achtergrond:
a a a a a a a a a a a a a a a a a a a a a a a a a a a EXPERIMENTELE LABORATORIA BASAAL ONDERZOEK LEVERTRANSPLANTATIE Basaal onderzoek Levertransplantatie (Senior onderzoeker Luc van der Laan) Achtergrond:
Het hepatitis B -virus is heel besmettelijk en wordt overgedragen door seksueel contact, door bloed-op-bloed contact of bij de geboorte.
 Hepatitis B CWZ is één van de door de NVMDL erkende hepatitis behandelcentra in Nederland. Op de polikliniek Maag-, darm- en leverziekte (MDL) werken meerdere MDL-artsen en een verpleegkundige specialist
Hepatitis B CWZ is één van de door de NVMDL erkende hepatitis behandelcentra in Nederland. Op de polikliniek Maag-, darm- en leverziekte (MDL) werken meerdere MDL-artsen en een verpleegkundige specialist
Servier Benelux S.A. PROTELOS. (strontiumranelaat) GIDS EN CHECKLIST VOOR DE ARTS
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Protelos 2 g. Het verplicht plan voor risicobeperking in België, waarvan deze
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Protelos 2 g. Het verplicht plan voor risicobeperking in België, waarvan deze
Juveniele spondylartropathie/enthesitis gerelateerde artritis (SpA-ERA)
 www.printo.it/pediatric-rheumatology/nl/intro Juveniele spondylartropathie/enthesitis gerelateerde artritis (SpA-ERA) Versie 2016 1. WAT IS JUVENIELE SPONDYLARTROPATHIE/ENTHESITIS GERELATEERDE ARTRITIS
www.printo.it/pediatric-rheumatology/nl/intro Juveniele spondylartropathie/enthesitis gerelateerde artritis (SpA-ERA) Versie 2016 1. WAT IS JUVENIELE SPONDYLARTROPATHIE/ENTHESITIS GERELATEERDE ARTRITIS
ETOS AMYLMETACRESOL PLUS DICHLOORBENZYLALCOHOL HONING & CITROEN zuigtabletten
 1.3.1 : Productinformatie Bladzijde: 1 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke zuigtablet bevat: Amylmetacresol 0,60 mg 2,
1.3.1 : Productinformatie Bladzijde: 1 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke zuigtablet bevat: Amylmetacresol 0,60 mg 2,
Periodieke Koorts Met Afteuze Faryngitis En Adenitis (PFAPA)
 www.printo.it/pediatric-rheumatology/nl/intro Periodieke Koorts Met Afteuze Faryngitis En Adenitis (PFAPA) Versie 2016 1. WAT IS PFAPA 1.1 Wat is het? PFAPA staat voor Periodic Fever Adenitis Pharyngitis
www.printo.it/pediatric-rheumatology/nl/intro Periodieke Koorts Met Afteuze Faryngitis En Adenitis (PFAPA) Versie 2016 1. WAT IS PFAPA 1.1 Wat is het? PFAPA staat voor Periodic Fever Adenitis Pharyngitis
Nederlandse Samenvatting
 249 Migraine is een ernstige en veelvoorkomende hoofdpijnaandoening met grote impact op het leven van patiënten en hun familieleden. Een migraineaanval wordt gekenmerkt door matige tot ernstige hoofdpijn,
249 Migraine is een ernstige en veelvoorkomende hoofdpijnaandoening met grote impact op het leven van patiënten en hun familieleden. Een migraineaanval wordt gekenmerkt door matige tot ernstige hoofdpijn,
Chapter 9 Samenvatting
 Samenvatting Marcel D. Posthumus SAMENVATTING Reumatoïde artritis (RA) is een aandoening die voorkomt bij 0,5-1% van de bevolking en die gekenmerkt wordt door een chronische ontsteking van meerdere gewrichten
Samenvatting Marcel D. Posthumus SAMENVATTING Reumatoïde artritis (RA) is een aandoening die voorkomt bij 0,5-1% van de bevolking en die gekenmerkt wordt door een chronische ontsteking van meerdere gewrichten
Inhoudsopgave Inleiding Voor wie is deze brochure? 1. Hepatitis 2. Behandeling medicijnen Alternatieve aanvullende behandelingen
 Inhoudsopgave Inleiding 1 Voor wie is deze brochure? 1 1. Hepatitis B 1 1.1 Wanneer behandelen 1 1.2 Wanneer niet behandelen 2 1.3 Zwangerschap en behandeling 3 2. Behandeling en medicijnen 4 2.1 PEG-interferon
Inhoudsopgave Inleiding 1 Voor wie is deze brochure? 1 1. Hepatitis B 1 1.1 Wanneer behandelen 1 1.2 Wanneer niet behandelen 2 1.3 Zwangerschap en behandeling 3 2. Behandeling en medicijnen 4 2.1 PEG-interferon
Package Leaflet / 1 van 5
 1.3.1.3 Package Leaflet 1.3.1.3 / 1 van 5 Bijsluiter: informatie voor de gebruiker Hydroxocobalamine HCl CF 0,5 mg/ml, oplossing voor injectie hydroxocobalamine Lees goed de hele bijsluiter voordat u dit
1.3.1.3 Package Leaflet 1.3.1.3 / 1 van 5 Bijsluiter: informatie voor de gebruiker Hydroxocobalamine HCl CF 0,5 mg/ml, oplossing voor injectie hydroxocobalamine Lees goed de hele bijsluiter voordat u dit
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL PegIntron 50 microgram poeder en oplosmiddel voor oplossing voor injectie PegIntron 80 microgram poeder en oplosmiddel voor
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL PegIntron 50 microgram poeder en oplosmiddel voor oplossing voor injectie PegIntron 80 microgram poeder en oplosmiddel voor
Acknowledgement. Acknowledgement
 Acknowledgement Acknowledgement This study is part of TREND (Trauma RElated Neuronal Dysfunction), a Dutch Consortium that integrates research on epidemiology, assessment technology, pharmacotherapeutics,
Acknowledgement Acknowledgement This study is part of TREND (Trauma RElated Neuronal Dysfunction), a Dutch Consortium that integrates research on epidemiology, assessment technology, pharmacotherapeutics,
Welke patiënten zijn geschikt voor MTX?
 Methotrexaat (MTX) Wat is methotrexaat (MTX) MTX is een geneesmiddel dat wordt gebruikt voor de behandeling bij ernstige psoriasis. Aanvankelijk werd het gebruikt bij de behandeling van kanker. Bij toeval
Methotrexaat (MTX) Wat is methotrexaat (MTX) MTX is een geneesmiddel dat wordt gebruikt voor de behandeling bij ernstige psoriasis. Aanvankelijk werd het gebruikt bij de behandeling van kanker. Bij toeval
Azathioprine (Imuran) bij de ziekte van Crohn, colitis ulcerosa en auto-immuun hepatitis
 Azathioprine (Imuran) bij de ziekte van Crohn, colitis ulcerosa en auto-immuun hepatitis Uw behandelend arts heeft met u gesproken over het gebruik van Azathioprine (Imuran). In deze folder krijgt u informatie
Azathioprine (Imuran) bij de ziekte van Crohn, colitis ulcerosa en auto-immuun hepatitis Uw behandelend arts heeft met u gesproken over het gebruik van Azathioprine (Imuran). In deze folder krijgt u informatie
 www.printo.it/pediatric-rheumatology/be_fm/intro Majeed Versie 2016 1. WAT IS MAJEED 1.1 Wat is het? Het Majeed syndroom is een zeldzame genetische aandoening. Kinderen met dit syndroom lijden aan chronische
www.printo.it/pediatric-rheumatology/be_fm/intro Majeed Versie 2016 1. WAT IS MAJEED 1.1 Wat is het? Het Majeed syndroom is een zeldzame genetische aandoening. Kinderen met dit syndroom lijden aan chronische
Nederlandse samenvatting
 Nederlandse samenvatting GENETISCHE EN RADIOLOGISCHE MARKERS VOOR DE PROGNOSE EN DIAGNOSE VAN MULTIPLE SCLEROSE Multiple Sclerose (MS) is een aandoening van het centrale zenuwstelsel (hersenen en ruggenmerg)
Nederlandse samenvatting GENETISCHE EN RADIOLOGISCHE MARKERS VOOR DE PROGNOSE EN DIAGNOSE VAN MULTIPLE SCLEROSE Multiple Sclerose (MS) is een aandoening van het centrale zenuwstelsel (hersenen en ruggenmerg)
Hoe gaat het in z n werk daar? Wat is er anders dan een gewone poli?
 INTERVIEW d.d. 28 december 2009 Coeliakiepoli Op het interview-wenslijstje van Nynke en Zara staat Dr. Luisa Mearin. Zij is kinderarts MDL in het LUMC te Leiden en heeft als eerste met haar collega s in
INTERVIEW d.d. 28 december 2009 Coeliakiepoli Op het interview-wenslijstje van Nynke en Zara staat Dr. Luisa Mearin. Zij is kinderarts MDL in het LUMC te Leiden en heeft als eerste met haar collega s in
BIJSLUITER. Inhoud van deze bijsluiter :
 BIJSLUITER Lees deze bijsluiter helemaal door alvorens dit geneesmiddel te nemen. Hij bevat belangrijke informatie voor uw behandeling Voor alle andere vragen of twijfels kunt u terecht bij uw arts of
BIJSLUITER Lees deze bijsluiter helemaal door alvorens dit geneesmiddel te nemen. Hij bevat belangrijke informatie voor uw behandeling Voor alle andere vragen of twijfels kunt u terecht bij uw arts of
YERVOY. (ipilimumab) Concentraat voor oplossing voor infusie. Patiëntenbrochure. met patiëntenwaarschuwingskaart
 Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel YERVOY, om voor een goed gebruik ervan te zorgen en om de ongewenste effecten ervan te beperken, zijn er bepaalde
Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel YERVOY, om voor een goed gebruik ervan te zorgen en om de ongewenste effecten ervan te beperken, zijn er bepaalde
BIJSLUITER. MELOXIDYL 0,5 mg/ml suspensie voor oraal gebruik voor katten
 BIJSLUITER MELOXIDYL 0,5 mg/ml suspensie voor oraal gebruik voor katten 1. NAAM EN HET ADRES VAN DE HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EN VAN DE FABRIKANT VERANTWOORDELIJK VOOR DE VRIJGIFTE,
BIJSLUITER MELOXIDYL 0,5 mg/ml suspensie voor oraal gebruik voor katten 1. NAAM EN HET ADRES VAN DE HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EN VAN DE FABRIKANT VERANTWOORDELIJK VOOR DE VRIJGIFTE,
Behandeling van Hepatitis C
 Behandeling van Hepatitis C Maatschap Maag-, Darm- en Leverziekten IJsselland Ziekenhuis www.mdlcentrum.nl Inleiding Uw behandelend arts heeft bij u Hepatitis C geconstateerd. De MDL-verpleegkundige gaat
Behandeling van Hepatitis C Maatschap Maag-, Darm- en Leverziekten IJsselland Ziekenhuis www.mdlcentrum.nl Inleiding Uw behandelend arts heeft bij u Hepatitis C geconstateerd. De MDL-verpleegkundige gaat
Lonsurf trifluridine/tipiracil
 Lonsurf trifluridine/tipiracil Product Informatie Fiche T +32(0)89 32 50 50 F +32(0)89 32 79 00 info@zol.be Campus Sint-Jan Schiepse bos 6 B 3600 Genk Campus Sint-Barbara Bessemerstraat 478 B 3620 Lanaken
Lonsurf trifluridine/tipiracil Product Informatie Fiche T +32(0)89 32 50 50 F +32(0)89 32 79 00 info@zol.be Campus Sint-Jan Schiepse bos 6 B 3600 Genk Campus Sint-Barbara Bessemerstraat 478 B 3620 Lanaken
