Let op: elke juist beantwoorde vraag levert punten op; elke onjuist beantwoorde aftrek. Per vraag is dat (punten/aftrek); blanco = 0 punten.
|
|
|
- Dirk Lambrechts
- 7 jaren geleden
- Aantal bezoeken:
Transcriptie
1 SPM _09; - Opdracht/deeltoets I Datum: 26 februari 2009, Tijd: Deze deeltoets bestaat uit 10 meerkeuzevragen en 2 open vragen. U begint met een saldo van 30 punten. U mag gebruiken schrijfmateriaal, een rekenmachine en aangehecht formuleblad. LEVER DIT VEL IN Naam:... Studienummer:... Meerkeuze vragen (30 punten) Let op: elke juist beantwoorde vraag levert punten op; elke onjuist beantwoorde aftrek. Per vraag is dat (punten/aftrek); blanco = 0 punten. 1. Welke stof is niet een fossiele energiebron? (1.5/0.5) 0 bruinkool 0 steenkool houtskool 0 blanco 2. De eerste hoofdwet van de Thermodynamica luidt: (3/1) 0 de entropie van het Universum neemt altijd toe de energie van het Universum is constant 0 massa kan niet worden vernietigd noch gecreëerd 0 blanco 3. We maken onderscheid tussen open en gesloten systemen. (3/1) 0 open systemen hebben een systeemgrens, gesloten systemen niet 0 in open systemen vindt altijd accumulatie plaats, in gesloten systemen niet open systemen staan in verbinding met hun omgeving, gesloten systemen niet 0 blanco 4. In wereldenergiestatistieken wordt de voorraadpositie van ruwe aardolie (en andere energiebronnen) gekarakteriseerd met het kental (1.5/0.5) 0 R [ExaJoules] 0 P/R [dimensieloos] R/P [jaar] 0 blanco 5. In een mengsel van 50 gew.% water (H 2 O) en 50% alcohol (C 2 H 5 OH) (3/1) is het mol% alcohol kleiner dan het mol% water 0 is het mol% alcohol gelijk aan het mol% water 0 is het mol% alcohol groter dan het mol% water 0 blanco Toelichting: het molgewicht van water (H 2 O) is 18 [g/mol], het molgewicht van alcohol (C 2 H 5 OH) is 46 [g/mol]. In 100 gram mengsel zit dus 100 [g] * 0.50 /18 [g/mol] = 2.8 [mol] water, en 100 [g]* 0.5/46 [g/mol] = 1.1 mol alcohol. Het molpercentage water is dus 100* 2.8/( ) = 72%, het molpercentage alcohol is slechts 28%.
2 6. Als de verbrandingstemperatuur in een elektriciteitscentrale 500 graden Celsius bedraagt en de buiten temperatuur is slechts 15 graden, dan is het maximale rendement van deze centrale (3/1) 0 niet te bepalen ongeveer 63 % 0 ongeveer 97 % 0 blanco Toelichting: het maximale rendement van een thermische centrale wordt gegeven door het Carnot-rendement, η Carnot =1-(T c /T h ). = 1 (273+15)/( ) = 63% ZIE OOK OMMEZIJDE voor MEERKEUZEVRAGEN In een consumententest naar kookplaten (elektrisch, gas, butagas, keramisch, wok etc.) wordt in een standaardtheeketel een liter water gekookt. Men begint telkens bij standaardcondities. De tijd die het duurt tot het fluitje klinkt is (1.5/0.5) 0 altijd hetzelfde een eerste indicatie voor het vermogen [kw] van de kookplaat 0 een eerste indicatie voor het rendement [%] van de kookplaat 0 blanco De grootste diamant ter wereld, de Cullinan, is 530 karaat. Diamant bestaat uit zuiver koolstof, een karaat is 200 milligram. 8. Hoeveel mol is een karaat? (3/1) blanco Toelichting: een karaat is 200 milligram. Het molgewicht van koolstof C is 12 [g/mol]. Dus één karaat is 200 * 10-3 /12 = [g] 9. Hoeveel CO 2 zou ontstaan bij verbranding van de Cullinan? (4.5/1.5) gram 389 gram gram 0 blanco Toelichting: de Cullinan is 530 karaat of 530 [karaat] * 0.2 [g/karaat] = 106 [g] Ze bestaat uit zuiver koolstof, dus verbrandingsreactie is C + O 2 CO 2 Het molgewicht van C is 12 [g/mol], dat van CO 2 is 44 [g/mol]. Er onstaat dus 106 [g] * 44/12 = 389 gram CO 2 bij verbranding van de Cullinan. 10. Gegeven volgende data: (4.5 punten, geen aftrek) 2H 2 + O 2 2H 2 O ΔH= -482[kJ/mol] (reactie 1) CH 4 + 2O 2 CO 2 + 2H 2 O ΔH= -810[kJ/mol] (reactie 2) Wat is dan de ΔH voor de reactie? CH 4 + O 2 2H 2 + CO 2 (reactie 3) De ΔH is gelijk aan [kj/mol] Toelichting: met de Wet van Hess kunnen we dit berekenen als volgt. We construeren een pad uit reactie 1 en 2 (beschikbare gegevens!) om op reactie 3 uit te komen (overall). Dit kunnen we doen, omdat ΔH een toestandsgrootheid is (Wet van Hess). Als we eerst reactie 2 uitvoeren, en vervolgens reactie 1 in omgekeerde richting, dan is de overall reactie gelijk aan reactie 3. De enthalpieverandering ΔH van reactie 3 is dus gelijk aan de enthalpie van reactie 2 + enthalpie van omgekeerde reactie 1 = = -382 [kj/mol]
3 Open vragen Vraagstuk 11: Elektriciteit (30 punten) Het rendement van elektriciteitscentrales gestookt met fossiele energiedragers is in Nederland ongeveer 50%. Het intern elektriciteitsverbruik van Nederland is ongeveer 800 PJ, waarvan eenderde wordt opgewekt met steenkool (rendement 45%), eenderde met aardgas (rendement 55%) en eenderde met warmte/kracht centrales op aardgas (elektrisch rendement 30%, thermisch rendement 80%). a. Teken een systeemdiagram van de Nederlandse elektriciteitsopwekking waarmee u tevens de onderstaande vragen kunt beantwoorden Steenkool Steenkool centrale Elektricitiet Restwarmte (warm water) Carbondioxide Koelwater Zuurstof Aardgas Aardgas centrale Elektricitiet Restwarmte (warm water) Carbondioxide Koelwater Zuurstof Aardgas WKK centrale Elektricitiet Restwarmte (warm water) Carbondioxide Koelwater Zuurstof b. Als de LHV van steenkool 28 MJ/Kg is en die van aardgas 50 MJ/kg is, hoeveel steenkool respectievelijk aardgas wordt dan verstookt per jaar om deze hoeveelheid elektriciteit op te wekken? Voor elke centrale kunnen we met behulp van het omzettingsrendement (brandstof elektriciteit) de jaarlijks benodigde hoeveelheid brandstof berekenen als we weten hoeveel elektriciteit jaarlijks wordt geproduceerd. Jaarlijks wordt per centrale (1/3*800)=267 PJ opgewekt. - Steenkool LHV = 28 MJ/kg Omzettingsrendement η=45%(1 e hoofdwet) De hoeveelheid steenkool is: 267*10^15 [J]/(0,45*28*10^6[J/kg]) = 2,12*10^10 kg = 2,12*10^7 ton = 21 Mton steenkool per jaar - Aardgas LHV = 50 MJ/kg Er zijn 2 typen centrales die aardgas stoken 1) Omzettingsrendement aardgas centrale = 55% 2) Omzettingsrendement WKK centrale naar elektriciteit = 30%
4 Hoeveelheid aardgas centrale is: 267*10^9/(0,55*50) Hoeveelheid aardgas WKK is: 267*10^9/(0,3*50) Totaal wordt dus jaarlijks verstookt 2,75*10^10 kg = 2,75*10^7 ton = 27,5 Mton aardgas per jaar c. Als de CO 2 belasting 25 euro per ton uitgestoten CO 2 bedraagt, hoeveel belasting kan Minister Bos dan jaarlijks tegemoet zien? 1) Uitstoot CO 2 door steenkool De verhoudingsformule van steenkool is CH De molverhouding CO 2 per CH is 1:1 De verhouding [g/mol] CO 2 per CH is: 44/13 De hoeveel CO 2 uitgestoten door de steenkool centrales is dus: 21[Mton]*44/13 = 71,1 Mton per jaar 2) Uitstoot CO 2 door aardgas De verhoudingsformule van aardgas, methaan is CH 4 De molverhouding CO 2 per CH 4 is: 1:1 De verhouding [g/mol] CO 2 per CH 4 is: 44/16 De hoeveelheid CO 2 uitgestoten door aardgas centrales + WKK's: 27,5[Mton]*44/16 = 75,6 Mton per jaar 3) De ontvangen hoeveelheid belasting De totale hoeveelheid CO 2 uitgestoten is 146,7 Mton per jaar De belasting per jaar is dus: 146,7*10^6*25 = 3,7*10^9 euro per jaar Nota Bene: omdat de totale CO 2 uitstoot van Nederland ongeveer 220 Miljoen Ton op jaarbasis is lijkt dit getal aan de hoge kant. De werkelijke jaarlijkse elektriciteitsproductie in Nederland is ongeveer 100 miljard kilowattuur (kwh) ( 1 kwh = 3.6 MJ, dus de werkelijke elektriciteitsproductie is 100*10^9 * 3.6*10^6 = 360 * 10^15 = 360 PJ. Omdat de verdeling wel ongeveer klopt, is een betere schatting van de CO 2 uitstoot 147 MTA * 360/800 = 66 MTA. De bijbehorende belastingopbrengst zou zijn 66 MTA * 25 Euro/ton = 1.65 miljard Euro per jaar. d. Stel dat alle geproduceerde warmte geleverd wordt aan woningen via een warmtenet, en dat het gemiddelde warmtegebruik per woning [50 GJ/jaar] bedraagt, hoeveel woningen zijn dan aangesloten op dat warmtenet? o De rest warmte van grootschalige elektriciteitscentrales wordt weg gekoeld; alleen de warmte geproduceerd uit WKK s is te gebruiken voor een warmtenet o 1/3 van de elektriciteit komt uit WKK s o Dat is 267 PJ o Het totale rendement van de WKK is 80%. De verhouding elektriciteit (kracht) warmte (W) = 30:50 (100% input, 30% elektriciteit, 50% warmte, 20% verlies) o We nemen aan dat alle geproduceerde warmte van WKK centrales naar het warmtenet gaat.
5 o en dat de WKK produceert precies op de momenten dat er warmte wordt gevraagd o van de 267 PJ gaat 50% naar warmte net, dus 133,5 PJ per jaar o 133,5*10^6 (GJ/jaar)/50 (GJ/jaar/woning) = 26,7*10^5 woningen kunnen dan aangesloten zijn op het warmtenet e. In Nederland is de gemiddelde zonne-instraling 900 [W/m 2 ] gedurende 12 uur per etmaal. Stel dat PV-systemen met een rendement van 15% de elektriciteitsopwekking zullen vervangen. Hoeveel ruimte is dan nodig? - een m^2 levert per jaar: 900*60*60*12*365*0,15 = 21,3*10^9 Joules per jaar - de totale oppervlakte nodig hiervoor is: 800*10^15/21,3*10^9 = 37,5*10^6 m^2. Dat staat gelijk aan 37,5 km^2 Vraagstuk 12. Bioethanol (30 punten) Regels uit Brussel schrijven voor dat benzine vanaf 2005 voor 2 procent (vol.).uit biobrandstoffen moet bestaan, in 2010 is dat percentage op 5,75.. In benzine uit olieraffinaderijen kan bio-ethanol worden bijgemengd. Alle moderne benzine-auto s zijn geschikt om op benzine/ethanol mengsels van genoemde samenstellingen te rijden. Het omzettingsrendement van de motor blijft daarbij gelijk. In Nederland rijden +/- 4 miljoen benzineauto s die gemiddeld km/jaar rijden. a) maak een eerste-orde schatting van de hoeveelheid bio-ethanol die voor de Nederlandse benzinemarkt moet worden geproduceerd in 2005 respectievelijk 2010 volgens de Brusselse richtlijnen. - in totaal wordt er 4*10^6*17*10^3 = 68*10^9 km gereden per jaar - de hoeveelheid benzine nodig om deze afstand af te leggen is: 68*10^9/15[km/liter] = 4,53*10^9 [liter] - voor de 2005 richtlijn is de hoeveelheid bio-ethanol nodig: 4,53*10^9*0,02[vol.%!] = 90*10^6 [liter/jaar] = 90 miljoen [liter/jaar] - voor de 2010 richtlijn is de hoeveelheid bio-ethanol nodig: 4,53*10^9*0,0575 = 260*10^6 liter = 260 miljoen [liter/jaar] In Nederland zijn de laatste jaren een aantal bio-ethanol fabrieken gebouwd om aan de verwachte vraag te kunnen voldoen door Zoals bekend kunnen in water opgeloste suikers en zetmeel met behulp van micro-organismen gefermenteerd worden tot alcoholhoudende dranken zoals wijn en bier. Bij een alcohol-percentage > 15 vol.% sterven de micro-organismen die de fermentatie uitvoeren echter af. In een bio-ethanol fabriek wordt de fermentatie op industriële schaal uitgevoerd met dezelfde micro-organismen. Zo n fabriek bevat dan ook altijd een grote destillatie eenheid om uiteindelijk 99% zuivere bio-ethanol te verkrijgen. Druivesuiker en zetmeel, met de verhoudings formule C 6 H 12 O 6 reageren tijdens de fermentatie tot slechts (bio)-ethanol en CO 2. b) Schrijf de (kloppende) reactievergelijking uit voor de fermentatie van druivesuiker. C 6 H 12 O 6 2 CO C 2 H 6 O c) Bereken de reactie-enthalpie onder meer met behulp van de gegevens uit de onderstaande tabel - reactie enthalpie [kj/mol] = H producten - H reactanten
6 - 2*H(CO 2 ) + 2*H(C 2 H 6 O) H(C 6 H 12 O 6 ) [kj/mol] - De verbrandingsenthalpie van CO 2 = 0 (definitie! LHV) - H(C 2 H 6 O) = 27 [MJ/kg] - H(C 6 H 12 O 6 ) = 37.5 [MJ/kg - Uit 1 kg druivesuiker ontstaat 2*46[g/mol]/180[g/mol]=92/ Dus de reactie-enthalpie is 2*0 + (92/180) * = 23.7 [kj/mol] d) teken een principeschema voor een industriële alcoholfabriek die ton industriële alcohol (99 vol%) per jaar produceert uit suiker/zetmeel (melasse) dat voor 50gew.% uit biomassa bestaat, voor 50% uit water. e) Stel dat de melasse per binnenvaart tankers met een laadvermogen van 1500 ton wordt aangevoerd. Hoeveel tankers zijn dan jaarlijks nodig? - 1 mol ethanol is: 46g - 1 mol suiker is: 180 g - De stoechiometrische verhouding suiker en ethanol in de reactie is: 1:2 dus per mol ethanol is 0,5 mol suiker voor nodig. - De massaverhouding tussen een mol suiker en een mol ethanol is: 46:180 1:4 - De hoeveelheid ton ethanol geproduceerd is; *0.99 = ton - De hoeveelheid suiker nodig voor deze productie is: *4*0,5 = ton - De hoeveelheid tankers nodig is: /1.500 = 132 tankers per jaar f) Komt bij het proces netto warmte vrij denkt u? Leg uit waarom (niet)? De reactie enthalpie is negatief, dus komt er netto energie vrij. Deze energie is in de vorm van warmte, dus komt er netto warmte vrij in het proces. Als deze warmte van voldoende temperatuur is, dan kan ze wellicht gebruikt worden voor de scheiding van ethanol en water, door destillatie. In dat geval komt restwarmte vrij uit de destillatie, in het andere geval van de reactor. Gegevens van een aantal stoffen Stof Verhoudingsformule Verbrandingsenthalpie Dichtheid (20 o C) Methanol CH 4 O (CH 3 OH) 21 [MJ/kg]
7 Ethanol* C 2 H 6 O (C 2 H 5 OH) 27 [MJ/kg] Koolhydraten* C 6 H 12 O [MJ/kg] Benzine C 8 H [MJ/kg] 0.75 *dat zijn onder meer suiker, zetmeel enz.
8 Formuleblad en Periodiek systeem Energie: E kin = ½ m v 2 [J] Q = C p m T [J] W max = Q h (T h T c ) / T h Q c = Q h W max = Q h T c / T h 132.E = Avogadro: Straling: N = 6, [moleculen/mol] c λ piek = Tpiek [m] S = k T 4 (k = 5,67 * 10-8 [W/m 2 ]) E = h f = h c/λ [J] h = [Js] c = 3, [m/s] Heisenberg: Ideaal gas: ()xmv p V = n R T (R = 0,0821 [atm L K-1]) (L = liter) R = [J/(K*mol)] Zuurgraad: ph = -log[h + ] A 8A 1 2 H He A 3A 4A 5A 6A 7A Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Ge Sb Te I Xe (98) Cs Ba La Hf Ta W Re Os Ir Pt Au Hg Tl Sn Bi Po At Rn (209) (210) (222) Fr Ra Ac Unq Unp Unh Uns Uno Une Uun Uuu Uub (223) 226 (227) Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu (145) Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr (231) (237) (244) (243) (247) (247) (251) (252) (257) (258) (259) (260)
9
Tentamen TB142-E 20 mei uur
 TB142-E Tentamen 20 mei 2014 Tentamen TB142-E 20 mei 2014 9-10 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan dit tentamen).
TB142-E Tentamen 20 mei 2014 Tentamen TB142-E 20 mei 2014 9-10 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan dit tentamen).
Deel 2. Basiskennis chemie
 Deel 2. Basiskennis chemie Achteraan vind je een periodiek systeem van de elementen. Gebruik dit waar nodig. Vraag 21 Koolstofmonoxide (C) kan gesynthetiseerd worden door stoom met methaan (CH4 ) te laten
Deel 2. Basiskennis chemie Achteraan vind je een periodiek systeem van de elementen. Gebruik dit waar nodig. Vraag 21 Koolstofmonoxide (C) kan gesynthetiseerd worden door stoom met methaan (CH4 ) te laten
Algemene en Technische Scheikunde
 Algemene en Technische Scheikunde Naam en voornaam: Examennummer: Reeks: Theorie: Oefeningen: Totaal: 1A 2A 3B 4B 5B 6B 7B 8B 1B 2B 3A 4A 5A 6A 7A 8A 1 1 H 1.008 2 He 4.003 2 3 Li 6.941 4 Be 9.012 5 B
Algemene en Technische Scheikunde Naam en voornaam: Examennummer: Reeks: Theorie: Oefeningen: Totaal: 1A 2A 3B 4B 5B 6B 7B 8B 1B 2B 3A 4A 5A 6A 7A 8A 1 1 H 1.008 2 He 4.003 2 3 Li 6.941 4 Be 9.012 5 B
Hertentamen TB142-E 3 juli uur
 TB142-E Hertentamen 3 juli 2014 Hertentamen TB142-E 3 juli 2014 11-12 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan dit
TB142-E Hertentamen 3 juli 2014 Hertentamen TB142-E 3 juli 2014 11-12 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan dit
Uitwerking Tentamen TB142-E 20 mei uur
 TB142-E Tentamen 20 mei 2014 Uitwerking Tentamen TB142-E 20 mei 2014 9-10 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan
TB142-E Tentamen 20 mei 2014 Uitwerking Tentamen TB142-E 20 mei 2014 9-10 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan
Tentamen spm April uur
 spm1520 Tentamen 20 April 2012 Tentamen spm1520 20 April 2012 14-17 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan dit tentamen).
spm1520 Tentamen 20 April 2012 Tentamen spm1520 20 April 2012 14-17 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan dit tentamen).
gelijk aan het aantal protonen in de kern. hebben allemaal hetzelfde aantal protonen in de kern.
 1 Atoombouw 1.1 Atoomnummer en massagetal Er bestaan vele miljoenen verschillende stoffen, die allemaal zijn opgebouwd uit ongeveer 100 verschillende atomen. Deze atomen zijn zelf ook weer opgebouwd uit
1 Atoombouw 1.1 Atoomnummer en massagetal Er bestaan vele miljoenen verschillende stoffen, die allemaal zijn opgebouwd uit ongeveer 100 verschillende atomen. Deze atomen zijn zelf ook weer opgebouwd uit
Uitwerking Hertentamen TB142-E 3 juli uur
 TB142-E Hertentamen 3 juli 2014 Uitwerking Hertentamen TB142-E 3 juli 2014 11-12 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan
TB142-E Hertentamen 3 juli 2014 Uitwerking Hertentamen TB142-E 3 juli 2014 11-12 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan
spm _09; - Opdracht/Deeltoets II;
 spm1510-08_09; - Opdracht/Deeltoets II; LEVER DIT VEL IN 20 maart 2009, 9.45-12.45 uur Naam:... Studienummer:... Deze deeltoets bestaat uit 13 meerkeuzevragen en 3 open vragen. U mag uitsluitend gebruiken:
spm1510-08_09; - Opdracht/Deeltoets II; LEVER DIT VEL IN 20 maart 2009, 9.45-12.45 uur Naam:... Studienummer:... Deze deeltoets bestaat uit 13 meerkeuzevragen en 3 open vragen. U mag uitsluitend gebruiken:
MEERKEUZEVRAGEN. spm1520 Uitwerking tentamen 20 April 2012
 spm1520 Uitwerking tentamen 20 April 2012 MEERKEUZEVRAGEN 1. (1 punt) Het Wereldgebruik aan aardolie is de afgelopen jaren ongeveer A. 86 miljoen TOE B. 86 miljoen vaten per dag C. 86 miljard vaten per
spm1520 Uitwerking tentamen 20 April 2012 MEERKEUZEVRAGEN 1. (1 punt) Het Wereldgebruik aan aardolie is de afgelopen jaren ongeveer A. 86 miljoen TOE B. 86 miljoen vaten per dag C. 86 miljard vaten per
Spm1520 Werkcollege 1. dr.ir. Emile J.L. Chappin kamer a
 Spm1520 Werkcollege 1 dr.ir. Emile J.L. Chappin kamer a.3.300 e.j.l.chappin@tudelft.nl Spm1520 De werkcolleges Wat werkt? Bestudeer aan de hand van de sheets en aantekeningen uit college s Oefen de opgaven
Spm1520 Werkcollege 1 dr.ir. Emile J.L. Chappin kamer a.3.300 e.j.l.chappin@tudelft.nl Spm1520 De werkcolleges Wat werkt? Bestudeer aan de hand van de sheets en aantekeningen uit college s Oefen de opgaven
Elektrische auto stoot evenveel CO 2 uit als gewone auto
 Elektrische auto stoot evenveel CO 2 uit als gewone auto Bron 1: Elektrische auto s zijn duur en helpen vooralsnog niets. Zet liever in op zuinige auto s, zegt Guus Kroes. 1. De elektrische auto is in
Elektrische auto stoot evenveel CO 2 uit als gewone auto Bron 1: Elektrische auto s zijn duur en helpen vooralsnog niets. Zet liever in op zuinige auto s, zegt Guus Kroes. 1. De elektrische auto is in
KLASTOETS GRAAD 11. FISIESE WETENSKAPPE: CHEMIE Toets 4: Materie en materiale 1
 KLASTOETS GRAAD FISIESE WETENSKAPPE: CHEMIE Toets 4: Materie en materiale PUNTE: 45 TYD: uur INSTRUKSIES EN INLIGTING. Beantwoord AL die vrae. 2. Nieprogrammeerbare sakrekenaars mag gebruik word. 3. Toepaslike
KLASTOETS GRAAD FISIESE WETENSKAPPE: CHEMIE Toets 4: Materie en materiale PUNTE: 45 TYD: uur INSTRUKSIES EN INLIGTING. Beantwoord AL die vrae. 2. Nieprogrammeerbare sakrekenaars mag gebruik word. 3. Toepaslike
Tentamen spm april uur
 spm1520 Tentamen 17 april 2013 Tentamen spm1520 17 april 2013 14-17 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan dit tentamen).
spm1520 Tentamen 17 april 2013 Tentamen spm1520 17 april 2013 14-17 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan dit tentamen).
spm1510_06_07; - Deeltoets IV; Vrijdag 29 mei 2009, 13:45-15:45
 NAAM: - page 1 - STUD.NO.: spm1510_06_07; - Deeltoets IV; Vrijdag 29 mei 2009, 13:45-15:45 LEVER DIT VEL IN! LEVER DIT VEL IN! Deze deeltoets bestaat uit 13 meerkeuzevragen, 2 open vragen en een bonusvraag.
NAAM: - page 1 - STUD.NO.: spm1510_06_07; - Deeltoets IV; Vrijdag 29 mei 2009, 13:45-15:45 LEVER DIT VEL IN! LEVER DIT VEL IN! Deze deeltoets bestaat uit 13 meerkeuzevragen, 2 open vragen en een bonusvraag.
Tabellen. Thermodynamica voor ingenieurs, Tabellen 1
 abellen abel 1. De elementen (molaire massa s) abel 2. Soortelijke warmte c p (bij lage drukken 0 1 ) in.k abel 3. Soortelijke warmte c p an lucht abel 4. Van der Waals coëfficiënten* abel 5. Gemiddelde
abellen abel 1. De elementen (molaire massa s) abel 2. Soortelijke warmte c p (bij lage drukken 0 1 ) in.k abel 3. Soortelijke warmte c p an lucht abel 4. Van der Waals coëfficiënten* abel 5. Gemiddelde
Energie en Energiebalans. Dictaat hoofdstuk 5
 Energie en Energiebalans Dictaat hoofdstuk 5 Inleiding Energiebalansen = boekhouden met energie elementaire warmteleer; energieberekeningen rond eenvoudige systemen en chemische reacties Overzicht college
Energie en Energiebalans Dictaat hoofdstuk 5 Inleiding Energiebalansen = boekhouden met energie elementaire warmteleer; energieberekeningen rond eenvoudige systemen en chemische reacties Overzicht college
De verliezen van /in het systeem zijn ook het gevolg van energietransformaties!
 Centrale Verwarmingssysteem Uitwerking van de deelvragen 1 ) Wat zijn de Energietransformaties in het systeem? De Energietransformaties die optreden in het CV-systeem zijn a. Boven de brander c.q. in de
Centrale Verwarmingssysteem Uitwerking van de deelvragen 1 ) Wat zijn de Energietransformaties in het systeem? De Energietransformaties die optreden in het CV-systeem zijn a. Boven de brander c.q. in de
Tentamen ta januari :00-12:00 uur
 Tentamen ta3290 25 januari 2013 9:00-12:00 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine periodiek systeem (afgedrukt op volgende pagina). Het tentamen heeft betrekking op de
Tentamen ta3290 25 januari 2013 9:00-12:00 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine periodiek systeem (afgedrukt op volgende pagina). Het tentamen heeft betrekking op de
Deel 1. Basiskennis wiskunde met oplossingen
 IJkingstoets Basiskennis wiskunde juni Deel. Basiskennis wiskunde met oplossingen Vraag Een reservoir bevat x liter water. Men verbruikt % van dat water waarna men liter water toevoegt aan het reservoir.
IJkingstoets Basiskennis wiskunde juni Deel. Basiskennis wiskunde met oplossingen Vraag Een reservoir bevat x liter water. Men verbruikt % van dat water waarna men liter water toevoegt aan het reservoir.
Tb151-00; - Deeltoets I; - Uitwerking Donderdag 28 Maart, 2002, 13:45-15:45
 Tb151-00; - Deeltoets I; - Uitwerking Donderdag 28 Maart, 2002, 13:45-15:45 Vraagstuk 1 (20 punten) a) Aardolie, aardgas en steenkool b) De (wereld)voorraadpositie van deze (en andere) energiebronnen wordt
Tb151-00; - Deeltoets I; - Uitwerking Donderdag 28 Maart, 2002, 13:45-15:45 Vraagstuk 1 (20 punten) a) Aardolie, aardgas en steenkool b) De (wereld)voorraadpositie van deze (en andere) energiebronnen wordt
spm _09; - Opdracht/Deeltoets III;
 spm1510-08_09; - Opdracht/Deeltoets III; LEVER DIT VEL IN 10 mei 2009, 13.45-15.45 uur Naam:... Studienummer:... Deze deeltoets bestaat uit 13 meerkeuzevragen en 3 open vragen. U mag uitsluitend gebruiken:
spm1510-08_09; - Opdracht/Deeltoets III; LEVER DIT VEL IN 10 mei 2009, 13.45-15.45 uur Naam:... Studienummer:... Deze deeltoets bestaat uit 13 meerkeuzevragen en 3 open vragen. U mag uitsluitend gebruiken:
Opgave 1. n = m / M. e 500 mg soda (Na 2CO 3) = 0,00472 mol. Opgave 2. m = n x M
 Hoofdstuk 8 Rekenen met de mol bladzijde 1 Opgave 1 n = m / M a 64,0 g zuurstofgas (O 2) = 2,00 mol (want n = 64,0 / 32,0) enz b 10,0 g butaan (C 4H 10) = 0,172 mol c 1,00 g suiker (C 12H 22O 11) = 0,00292
Hoofdstuk 8 Rekenen met de mol bladzijde 1 Opgave 1 n = m / M a 64,0 g zuurstofgas (O 2) = 2,00 mol (want n = 64,0 / 32,0) enz b 10,0 g butaan (C 4H 10) = 0,172 mol c 1,00 g suiker (C 12H 22O 11) = 0,00292
TENTAMEN CHEMISCHE THERMODYNAMICA. Dinsdag 25 oktober 2011 13.15 15.15
 TENTAMEN CHEMISCHE THERMODYNAMICA Dinsdag 25 oktober 2011 13.15 15.15 Bij het tentamen mag gebruik worden gemaakt van BINAS en een (grafische) rekenmachine. Let op eenheden en significante cijfers. 1.
TENTAMEN CHEMISCHE THERMODYNAMICA Dinsdag 25 oktober 2011 13.15 15.15 Bij het tentamen mag gebruik worden gemaakt van BINAS en een (grafische) rekenmachine. Let op eenheden en significante cijfers. 1.
SCHEIKUNDE VWO 4 MOLBEREKENINGEN ANTW.
 OPGAVE 1 LEVEL 1 Uit de opgave haal je dat koper en zuurstof links van de pijl moeten staan en koper(ii)oxide rechts van de pijl. Daarna maak je de reactievergelijking kloppend. 2 Cu + O 2 à 2 CuO Filmpje
OPGAVE 1 LEVEL 1 Uit de opgave haal je dat koper en zuurstof links van de pijl moeten staan en koper(ii)oxide rechts van de pijl. Daarna maak je de reactievergelijking kloppend. 2 Cu + O 2 à 2 CuO Filmpje
Tentamen TB142Ea 2 juli uur
 TB142Ea Tentamen 2 juli 2014 Tentamen TB142Ea 2 juli 2014 9-11 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan dit tentamen).
TB142Ea Tentamen 2 juli 2014 Tentamen TB142Ea 2 juli 2014 9-11 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan dit tentamen).
5 Formules en reactievergelijkingen
 5 Formules en reactievergelijkingen Stoffen bestaan uit moleculen en moleculen uit atomen (5.1) Stoffen bestaan uit moleculen. Een zuivere stof bestaat uit één soort moleculen. Een molecuul is een groepje
5 Formules en reactievergelijkingen Stoffen bestaan uit moleculen en moleculen uit atomen (5.1) Stoffen bestaan uit moleculen. Een zuivere stof bestaat uit één soort moleculen. Een molecuul is een groepje
Rekenen aan reacties (de mol)
 Rekenen aan reacties (de mol) 1. Reactievergelijkingen oefenen: Scheikunde Deze opgaven zijn bedoeld voor diegenen die moeite hebben met rekenen aan reacties 1. Reactievergelijkingen http://www.nassau-sg.nl/scheikunde/tutorials/deeltjes/deeltjes.html
Rekenen aan reacties (de mol) 1. Reactievergelijkingen oefenen: Scheikunde Deze opgaven zijn bedoeld voor diegenen die moeite hebben met rekenen aan reacties 1. Reactievergelijkingen http://www.nassau-sg.nl/scheikunde/tutorials/deeltjes/deeltjes.html
Oplossing oefeningen. Deel 1: Elektriciteit
 Oplossing oefeningen Afhankelijk van je oplossingsmethode en het al dan niet afronden van tussenresultaten, kun je een lichtjes verschillende uitkomst verkrijgen. Deel 1: Elektriciteit Hoofdstuk 1: Elektrische
Oplossing oefeningen Afhankelijk van je oplossingsmethode en het al dan niet afronden van tussenresultaten, kun je een lichtjes verschillende uitkomst verkrijgen. Deel 1: Elektriciteit Hoofdstuk 1: Elektrische
Inhoud LEERPLANDOELSTELLINGEN LEERINHOUDEN. De leerlingen kunnen
 Inhoud 1. Inleiding... 2 2. Het spectrum van waterstof en het atoommodel van Bohr... 5 3. Het atoommodel van BohrSommerfeld... 8 4. Elektronenconfiguratie... 10 5. Het periodiek systeem... 11 5.1. Historiek...
Inhoud 1. Inleiding... 2 2. Het spectrum van waterstof en het atoommodel van Bohr... 5 3. Het atoommodel van BohrSommerfeld... 8 4. Elektronenconfiguratie... 10 5. Het periodiek systeem... 11 5.1. Historiek...
Afsluitende les. Leerlingenhandleiding. Alternatieve brandstoffen
 Afsluitende les Leerlingenhandleiding Alternatieve brandstoffen Inleiding Deze chemie-verdiepingsmodule over alternatieve brandstoffen sluit aan op het Reizende DNA-lab Racen met wc-papier. Doel Het Reizende
Afsluitende les Leerlingenhandleiding Alternatieve brandstoffen Inleiding Deze chemie-verdiepingsmodule over alternatieve brandstoffen sluit aan op het Reizende DNA-lab Racen met wc-papier. Doel Het Reizende
woensdag 14 december 2011 16:06:43 Midden-Europese standaardtijd
 INLEIDING Geef de reactievergelijking van de ontleding van aluminiumoxide. 2 Al 2 O 3 4 Al + 3 O 2 Massaverhouding tussen Al en O 2 1,00 : 0,889 Hoeveel ton Al 2 O 3 is er nodig om 1,50 ton O 2 te produceren?
INLEIDING Geef de reactievergelijking van de ontleding van aluminiumoxide. 2 Al 2 O 3 4 Al + 3 O 2 Massaverhouding tussen Al en O 2 1,00 : 0,889 Hoeveel ton Al 2 O 3 is er nodig om 1,50 ton O 2 te produceren?
Curie Hoofdstuk 6 HAVO 4
 Rekenen aan reacties Curie Hoofdstuk 6 HAVO 4 6.1 Rekenen met de mol 6.2 Rekenen met massa s 6.3 Concentratie 6.4 SPA en Stappenplan 6.1 Rekenen met de mol Eenheden en grootheden 1d dozijn potloden 12
Rekenen aan reacties Curie Hoofdstuk 6 HAVO 4 6.1 Rekenen met de mol 6.2 Rekenen met massa s 6.3 Concentratie 6.4 SPA en Stappenplan 6.1 Rekenen met de mol Eenheden en grootheden 1d dozijn potloden 12
Tentamen spm april uur
 spm1520 Tentamen 15 April 2010 Tentamen spm1520 15 april 2010 14-17 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan dit tentamen).
spm1520 Tentamen 15 April 2010 Tentamen spm1520 15 april 2010 14-17 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan dit tentamen).
Samenvatting Scheikunde Hoofdstuk 3
 Samenvatting Scheikunde Hoofdstuk 3 Samenvatting door K. 1467 woorden 5 maart 2016 5,5 2 keer beoordeeld Vak Scheikunde Scheikunde Samenvatting H3 3V 3.1 Energie Fossiele brandstoffen -> nu nog er afhankelijk
Samenvatting Scheikunde Hoofdstuk 3 Samenvatting door K. 1467 woorden 5 maart 2016 5,5 2 keer beoordeeld Vak Scheikunde Scheikunde Samenvatting H3 3V 3.1 Energie Fossiele brandstoffen -> nu nog er afhankelijk
Samenvatting NaSk 1 Hoofdstuk 5
 Samenvatting NaSk 1 Hoofdstuk 5 Samenvatting door R. 956 woorden 12 oktober 2015 7,4 4 keer beoordeeld Vak NaSk 1 Paragraaf 1 De belangrijkste energiebronnen in huis zijn elektriciteit en aardgas. De meeste
Samenvatting NaSk 1 Hoofdstuk 5 Samenvatting door R. 956 woorden 12 oktober 2015 7,4 4 keer beoordeeld Vak NaSk 1 Paragraaf 1 De belangrijkste energiebronnen in huis zijn elektriciteit en aardgas. De meeste
SCHEIKUNDEOLYMPIADE 2017
 SCHEIKUNDEOLYMPIADE 2017 CORRECTIEMODEL VOORRONDE 2 af te nemen in de periode van 20 tot en met 24 maart 2017 Deze voorronde bestaat uit 20 meerkeuzevragen verdeeld over 7 onderwerpen en 3 opgaven met
SCHEIKUNDEOLYMPIADE 2017 CORRECTIEMODEL VOORRONDE 2 af te nemen in de periode van 20 tot en met 24 maart 2017 Deze voorronde bestaat uit 20 meerkeuzevragen verdeeld over 7 onderwerpen en 3 opgaven met
1 Algemene begrippen. THERMOCHEMIE p. 1
 TERMOCEMIE p. 1 1 Algemene begrippen De chemische thermodynamica bestudeert de energieveranderingen en energieuitwisselingen bij chemische processen. Ook het voorspellen van het al of niet spontaan verloop
TERMOCEMIE p. 1 1 Algemene begrippen De chemische thermodynamica bestudeert de energieveranderingen en energieuitwisselingen bij chemische processen. Ook het voorspellen van het al of niet spontaan verloop
Thermische Centrales voor Elektriciteit
 Thermische Centrales voor Elektriciteit College spm1520 5 maart 2013 Dr.ir. Gerard P.J. Dijkema Universitair Hoofddocent Energie en Industrie Faculty of Technology, Policy and Management Industry and Energy
Thermische Centrales voor Elektriciteit College spm1520 5 maart 2013 Dr.ir. Gerard P.J. Dijkema Universitair Hoofddocent Energie en Industrie Faculty of Technology, Policy and Management Industry and Energy
Leerlingenhandleiding
 Leerlingenhandleiding Afsluitende module Alternatieve Brandstoffen - Chemie verdieping - Ontwikkeld door dr. T. Klop en ir. J.F. Jacobs Op alle lesmaterialen is de Creative Commons Naamsvermelding-Niet-commercieel-Gelijk
Leerlingenhandleiding Afsluitende module Alternatieve Brandstoffen - Chemie verdieping - Ontwikkeld door dr. T. Klop en ir. J.F. Jacobs Op alle lesmaterialen is de Creative Commons Naamsvermelding-Niet-commercieel-Gelijk
Inhoud LEERPLANDOELSTELLINGEN LEERINHOUDEN. De leerlingen kunnen
 Inhoud Hoofdstuk1: Atoombouw... 1. Inleiding.... Het spectrum van waterstof en het atoommodel van Bohr... 5 3. Het atoommodel van BohrSommerfeld.... 9 4. Elektronenconfiguratie... 1 5. Het periodiek systeem...
Inhoud Hoofdstuk1: Atoombouw... 1. Inleiding.... Het spectrum van waterstof en het atoommodel van Bohr... 5 3. Het atoommodel van BohrSommerfeld.... 9 4. Elektronenconfiguratie... 1 5. Het periodiek systeem...
Oefen opgaven rekenen 4 HAVO bladzijde 1
 Oefen opgaven rekenen 4 HAVO bladzijde 1 Opgave 1 uitrekenen en afronden Bij +/- rond je af op het kleinste aantal DECIMALEN, bij x/ rond je af op het kleinste aantal SIGNIFICANTE CIJFERS. Bij gecombineerde
Oefen opgaven rekenen 4 HAVO bladzijde 1 Opgave 1 uitrekenen en afronden Bij +/- rond je af op het kleinste aantal DECIMALEN, bij x/ rond je af op het kleinste aantal SIGNIFICANTE CIJFERS. Bij gecombineerde
Uitwerking Tentamen spm april uur
 spm1520 Tentamen 17 april 2013 Uitwerking Tentamen spm1520 17 april 2013 14-17 uur Aanwijzingen: U mocht gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan
spm1520 Tentamen 17 april 2013 Uitwerking Tentamen spm1520 17 april 2013 14-17 uur Aanwijzingen: U mocht gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan
T2: Verbranden en Ontleden, De snelheid van een reactie en Verbindingen en elementen
 T2: Verbranden en Ontleden, De snelheid van een reactie en Verbindingen en elementen 2008 Voorbeeld toets dinsdag 29 februari 60 minuten NASK 2, 2(3) VMBO-TGK, DEEL B. H5: VERBRANDEN EN ONTLEDEN 3(4) VMBO-TGK,
T2: Verbranden en Ontleden, De snelheid van een reactie en Verbindingen en elementen 2008 Voorbeeld toets dinsdag 29 februari 60 minuten NASK 2, 2(3) VMBO-TGK, DEEL B. H5: VERBRANDEN EN ONTLEDEN 3(4) VMBO-TGK,
Module 2 Chemische berekeningen Antwoorden
 2 Meten is weten 1 Nee, want bijvoorbeeld 0,0010 kg is net zo nauwkeurig als 1,0 gram. 2 De minst betrouwbare meting is de volumemeting. Deze variabele bepaald het aantal significante cijfers. 3 IJs: 1,5
2 Meten is weten 1 Nee, want bijvoorbeeld 0,0010 kg is net zo nauwkeurig als 1,0 gram. 2 De minst betrouwbare meting is de volumemeting. Deze variabele bepaald het aantal significante cijfers. 3 IJs: 1,5
Samenvatting Scheikunde H3 Reacties
 Samenvatting Scheikunde H3 Reacties Samenvatting door L. 710 woorden 7 december 2016 6,8 24 keer beoordeeld Vak Methode Scheikunde Chemie overal Scheikunde Hoofdstuk 3: Reacties 3.2 Kenmerken van een chemische
Samenvatting Scheikunde H3 Reacties Samenvatting door L. 710 woorden 7 december 2016 6,8 24 keer beoordeeld Vak Methode Scheikunde Chemie overal Scheikunde Hoofdstuk 3: Reacties 3.2 Kenmerken van een chemische
Natuurlijk heb je nu nog géén massa s berekend. Maar dat kan altijd later nog. En dan kun je mooi kiezen, van welke stoffen je de massa wil berekenen.
 Hoofdstuk 17: Rekenen in molverhoudingen 17.1 Rekenen aan reacties: een terugblik én een alternatief In hoofdstuk 11 hebben we gerekend aan reacties. Het achterliggende idee was vaak, dat je bij een reactie
Hoofdstuk 17: Rekenen in molverhoudingen 17.1 Rekenen aan reacties: een terugblik én een alternatief In hoofdstuk 11 hebben we gerekend aan reacties. Het achterliggende idee was vaak, dat je bij een reactie
THEORIE UIT EXPERIMENTEN TABELLEN SCIENCE / NATUURKUNDE / SCHEIKUNDE
 THEORIE UIT EXPERIMENTEN ONDERBOUW TABELLEN SCIENCE / NATUURKUNDE / SCHEIKUNDE TABEL 1 DICHTHEID (bij 25 C) gram per cm 3 = g cm -3 aardgas 0,00076 alcohol 0,8 aluminium 2,7 broom 3,1 butagas 0,0024 eikenhout
THEORIE UIT EXPERIMENTEN ONDERBOUW TABELLEN SCIENCE / NATUURKUNDE / SCHEIKUNDE TABEL 1 DICHTHEID (bij 25 C) gram per cm 3 = g cm -3 aardgas 0,00076 alcohol 0,8 aluminium 2,7 broom 3,1 butagas 0,0024 eikenhout
Eindexamen scheikunde havo 2006-II
 4 Beoordelingsmodel Element 115 1 Calcium heeft atoomnummer 20 en americium heeft atoomnummer 95. Dus samen hebben ze 115 protonen. calcium heeft atoomnummer 20 en americium heeft atoomnummer 95 1 2 Een
4 Beoordelingsmodel Element 115 1 Calcium heeft atoomnummer 20 en americium heeft atoomnummer 95. Dus samen hebben ze 115 protonen. calcium heeft atoomnummer 20 en americium heeft atoomnummer 95 1 2 Een
E85 rijdende flexifuel auto uitstoot ten gevolge van de aanwezigheid van benzine in de brandstof.
 Energielabel auto Personenwagens moeten voorzien zijn van een zogenaamd energielabel. Deze maatregel is ingesteld om de consument de mogelijkheid te geven om op eenvoudige wijze het energieverbruik van
Energielabel auto Personenwagens moeten voorzien zijn van een zogenaamd energielabel. Deze maatregel is ingesteld om de consument de mogelijkheid te geven om op eenvoudige wijze het energieverbruik van
Aardolie is een zwart, stroperig mengsel van heel veel stoffen, wat door middel van een bepaalde scheidingsmethode in zeven fracties gescheiden wordt.
 Meerkeuzevragen Naast koolstofdioxide en waterdamp komen bij verbranding van steenkool nog flinke hoeveelheden schadelijke stoffen vrij. Dit komt doordat steenkool ook zwavel- en stikstofatomen bevat,
Meerkeuzevragen Naast koolstofdioxide en waterdamp komen bij verbranding van steenkool nog flinke hoeveelheden schadelijke stoffen vrij. Dit komt doordat steenkool ook zwavel- en stikstofatomen bevat,
Tentamen spm April uur
 spm1520 Tentamen 7 April 2011 Tentamen spm1520 7 April 2011 14-17 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan dit tentamen).
spm1520 Tentamen 7 April 2011 Tentamen spm1520 7 April 2011 14-17 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan dit tentamen).
Deel 2. Basiskennis wiskunde
 IJkingstoets Basiskennis wiskunde juli 5 Deel. Basiskennis wiskunde Vraag 7 De vijf punten in de onderstaande druk-volume-grafiek stellen vijf verschillende toestanden voor van e e n mol van een ideaal
IJkingstoets Basiskennis wiskunde juli 5 Deel. Basiskennis wiskunde Vraag 7 De vijf punten in de onderstaande druk-volume-grafiek stellen vijf verschillende toestanden voor van e e n mol van een ideaal
In deze eindtoets willen we met jullie samenvatten waar we het in het afgelopen kwartiel over gehad hebben:
 Eindtoets 3DEX1: Fysica van nieuwe energie 21-1- 2014 van 9:00-12:00 Roger Jaspers & Adriana Creatore In deze eindtoets willen we met jullie samenvatten waar we het in het afgelopen kwartiel over gehad
Eindtoets 3DEX1: Fysica van nieuwe energie 21-1- 2014 van 9:00-12:00 Roger Jaspers & Adriana Creatore In deze eindtoets willen we met jullie samenvatten waar we het in het afgelopen kwartiel over gehad
natuurlijke radioactiviteit Sytze Brandenburg sb/radsaf2003_2/1
 natuurlijke radioactiviteit Sytze Brandenburg sb/radsaf2003_2/1 primordiale radionucliden nucliden gevormd in sterren voor ontstaan zonnestelsel leeftijd heelal 15 x 10 9 jaar leeftijd zonnestelsel 4.5
natuurlijke radioactiviteit Sytze Brandenburg sb/radsaf2003_2/1 primordiale radionucliden nucliden gevormd in sterren voor ontstaan zonnestelsel leeftijd heelal 15 x 10 9 jaar leeftijd zonnestelsel 4.5
Thermische Centrales voor Elektriciteit College TB142Ea, 12 mei 2014
 Thermische Centrales voor Elektriciteit College TB142Ea, 12 mei 2014 Dr.ir. Gerard P.J. Dijkema E.On kolencentrales, Maasvlakte, Rotterdam. G.P.J. Dijkema 5 mei 2014 Faculty of Technology, Policy and Management
Thermische Centrales voor Elektriciteit College TB142Ea, 12 mei 2014 Dr.ir. Gerard P.J. Dijkema E.On kolencentrales, Maasvlakte, Rotterdam. G.P.J. Dijkema 5 mei 2014 Faculty of Technology, Policy and Management
Thermodynamica. Daniël Slenders Faculteit Ingenieurswetenschappen Katholieke Universiteit Leuven
 Thermodynamica Daniël Slenders Faculteit Ingenieurswetenschappen Katholieke Universiteit Leuven Academiejaar 2009-2010 Inhoudsopgave Eerste hoofdwet - deel 1 3 Oefening 1.1......................................
Thermodynamica Daniël Slenders Faculteit Ingenieurswetenschappen Katholieke Universiteit Leuven Academiejaar 2009-2010 Inhoudsopgave Eerste hoofdwet - deel 1 3 Oefening 1.1......................................
Toets T1 Algemene en Anorganische Chemie. 02 oktober 2013
 Toets T1 Algemene en Anorganische Chemie 02 oktober 2013 Naam: Studentnummer Universiteit Leiden: Dit is de enige originele versie van jouw tentamen. Het bevat dit voorblad, enkele pagina s met informatie
Toets T1 Algemene en Anorganische Chemie 02 oktober 2013 Naam: Studentnummer Universiteit Leiden: Dit is de enige originele versie van jouw tentamen. Het bevat dit voorblad, enkele pagina s met informatie
Eindtoets 3DEX0: Fysica van nieuwe energie 30-1- 2013 van 9:00-12:00
 Eindtoets 3DEX0: Fysica van nieuwe energie 30-1- 2013 van 9:00-12:00 Roger Jaspers & Adriana Creatore In deze eindtoets willen we met jullie samenvatten waar we het in het afgelopen kwartiel over gehad
Eindtoets 3DEX0: Fysica van nieuwe energie 30-1- 2013 van 9:00-12:00 Roger Jaspers & Adriana Creatore In deze eindtoets willen we met jullie samenvatten waar we het in het afgelopen kwartiel over gehad
a. Beschrijf deze reactie met een vergelijking. In het artikel is sprake van terugwinning van zwavel in zuivere vorm.
 PEARL GTL Oliemaatschappijen zoals Shell willen aan de nog steeds stijgende vraag naar benzine en diesel kunnen blijven voldoen én ze willen de eindige olievoorraad zoveel mogelijk beschikbaar houden als
PEARL GTL Oliemaatschappijen zoals Shell willen aan de nog steeds stijgende vraag naar benzine en diesel kunnen blijven voldoen én ze willen de eindige olievoorraad zoveel mogelijk beschikbaar houden als
Cursus Chemie 5-1. Hoofdstuk 5: KWANTITATIEVE ASPECTEN VAN CHEMISCHE REACTIES 1. BELANGRIJKE BEGRIPPEN. 1.1. Relatieve Atoommassa (A r)
 Cursus Chemie 5-1 Hoofdstuk 5: KWANTITATIEVE ASPECTEN VAN CHEMISCHE REACTIES 1. BELANGRIJKE BEGRIPPEN 1.1. Relatieve Atoommassa (A r) A r = een onbenoemd getal dat de verhouding weergeeft van de atoommassa
Cursus Chemie 5-1 Hoofdstuk 5: KWANTITATIEVE ASPECTEN VAN CHEMISCHE REACTIES 1. BELANGRIJKE BEGRIPPEN 1.1. Relatieve Atoommassa (A r) A r = een onbenoemd getal dat de verhouding weergeeft van de atoommassa
3. De globale aanpak voor wat betreft controle op radioactieve bronnen
 Verslag aan de Koning Sire, 1. Inleiding Sinds eind jaren 90, begin 2000 buigen de internationale instanties (IAEA, Euratom...) zich over de beveiliging en veiligheid van radioactieve bronnen. De Europese
Verslag aan de Koning Sire, 1. Inleiding Sinds eind jaren 90, begin 2000 buigen de internationale instanties (IAEA, Euratom...) zich over de beveiliging en veiligheid van radioactieve bronnen. De Europese
1 ENERGIE Inleiding Het omzetten van energie Fossiele brandstoffen Duurzame energiebronnen
 1 ENERGIE... 2 1.1. Inleiding... 2 1.2. Het omzetten van energie... 2 1.3. Fossiele brandstoffen... 5 1.4. Duurzame energiebronnen... 7 1.5. Kernenergie... 9 1.6. Energie besparen... 10 1.7. Energieverbruik
1 ENERGIE... 2 1.1. Inleiding... 2 1.2. Het omzetten van energie... 2 1.3. Fossiele brandstoffen... 5 1.4. Duurzame energiebronnen... 7 1.5. Kernenergie... 9 1.6. Energie besparen... 10 1.7. Energieverbruik
TENTAMEN. Van Quantum tot Materie
 TENTMEN Van Quantum tot Materie Prof. Dr. C. Gooijer en Prof. Dr. R. Griessen Vrijdag 22 december 2006 12.00-14.45 Q105/ M143/ C121 Dit schriftelijk tentamen bestaat uit 5 opdrachten. Naast de titel van
TENTMEN Van Quantum tot Materie Prof. Dr. C. Gooijer en Prof. Dr. R. Griessen Vrijdag 22 december 2006 12.00-14.45 Q105/ M143/ C121 Dit schriftelijk tentamen bestaat uit 5 opdrachten. Naast de titel van
Oefenvragen Hoofdstuk 4 Chemische reacties antwoorden
 Oefenvragen Hoofdstuk 4 Chemische reacties antwoorden Vraag 1 Geef juiste uitspraken over een chemische reactie. Kies uit: stofeigenschappen reactieproducten beginstoffen. I. Bij een chemische reactie
Oefenvragen Hoofdstuk 4 Chemische reacties antwoorden Vraag 1 Geef juiste uitspraken over een chemische reactie. Kies uit: stofeigenschappen reactieproducten beginstoffen. I. Bij een chemische reactie
Uitwerkingen. T2: Verbranden en Ontleden, De snelheid van een reactie en Verbindingen en elementen
 Uitwerkingen T2: Verbranden en Ontleden, De snelheid van een reactie en Verbindingen en elementen 2008 Voorbeeld toets dinsdag 29 februari 60 minuten NASK 2, 2(3) VMBO-TGK, DEEL B. H5: VERBRANDEN EN ONTLEDEN
Uitwerkingen T2: Verbranden en Ontleden, De snelheid van een reactie en Verbindingen en elementen 2008 Voorbeeld toets dinsdag 29 februari 60 minuten NASK 2, 2(3) VMBO-TGK, DEEL B. H5: VERBRANDEN EN ONTLEDEN
TOETS CTD voor 1 ste jaars MST (4051CHTHEY) 1 maart uur Docenten: L. de Smet, B. Dam
 TOETS CTD voor 1 ste jaars MST (4051CHTHEY) 1 maart 2016 13.30-15.00 uur Docenten: L. de Smet, B. Dam Dit tentamen bestaat uit 30 multiple-choice vragen Hiermee zijn in totaal 20 punten te verdienen Voor
TOETS CTD voor 1 ste jaars MST (4051CHTHEY) 1 maart 2016 13.30-15.00 uur Docenten: L. de Smet, B. Dam Dit tentamen bestaat uit 30 multiple-choice vragen Hiermee zijn in totaal 20 punten te verdienen Voor
1) Stoffen, moleculen en atomen
 Herhaling leerstof klas 3 1) Stoffen, moleculen en atomen Scheikundigen houden zich bezig met stoffen. Betekenissen van stof zijn onder andere: - Het materiaal waar kleding van gemaakt is; - Fijne vuildeeltjes;
Herhaling leerstof klas 3 1) Stoffen, moleculen en atomen Scheikundigen houden zich bezig met stoffen. Betekenissen van stof zijn onder andere: - Het materiaal waar kleding van gemaakt is; - Fijne vuildeeltjes;
TOETS CTD voor 1 ste jaars MST (4051CHTHEY) 7 maart uur Docenten: T. Savenije, B. Dam
 TOETS CTD voor 1 ste jaars MST (4051CHTHEY) 7 maart 2017 13.30-15.00 uur Docenten: T. Savenije, B. Dam Dit tentamen bestaat uit 30 multiple-choice vragen Hiermee zijn in totaal 20 punten te verdienen Voor
TOETS CTD voor 1 ste jaars MST (4051CHTHEY) 7 maart 2017 13.30-15.00 uur Docenten: T. Savenije, B. Dam Dit tentamen bestaat uit 30 multiple-choice vragen Hiermee zijn in totaal 20 punten te verdienen Voor
Rekenen aan reacties 2. Deze les. Zelfstudieopdrachten. Zelfstudieopdrachten voor volgende week. Zelfstudieopdrachten voor deze week 18-4-2016
 Rekenen aan reacties 2 Scheikunde Niveau 4 Jaar 1 Periode 3 Week 4 Deze les Rekenen aan reactievergelijkingen Samenvatting Vragen Huiswerk voor volgende week Bestuderen Lezen voor deze week Bestuderen
Rekenen aan reacties 2 Scheikunde Niveau 4 Jaar 1 Periode 3 Week 4 Deze les Rekenen aan reactievergelijkingen Samenvatting Vragen Huiswerk voor volgende week Bestuderen Lezen voor deze week Bestuderen
3. Welke van onderstaande formules geeft een zout aan? A. Al 2O 3 B. P 2O 3 C. C 2H 6 D. NH 3
 Toelatingsexamens en Ondersteunend Onderwijs VOORBLAD EXAMENOPGAVEN Toetsdatum: n.v.t. Vak: Scheikunde voorbeeldexamen 2015 Tijdsduur: 2 uur en 30 minuten De volgende hulpmiddelen zijn toegestaan bij het
Toelatingsexamens en Ondersteunend Onderwijs VOORBLAD EXAMENOPGAVEN Toetsdatum: n.v.t. Vak: Scheikunde voorbeeldexamen 2015 Tijdsduur: 2 uur en 30 minuten De volgende hulpmiddelen zijn toegestaan bij het
SEPTEMBERCURSUS CHEMIE HOOFDSTUK 3: STOICHIOMETRIE
 SEPTEMBERCURSUS CHEMIE HOOFDSTUK 3: STOICHIOMETRIE 1 OVERZICHT 1. Basisgrootheden en eenheden 2. Berekening van het aantal mol 3. Berekening in niet-normale omstandigheden 4. Oplossingen 5. Berekeningen
SEPTEMBERCURSUS CHEMIE HOOFDSTUK 3: STOICHIOMETRIE 1 OVERZICHT 1. Basisgrootheden en eenheden 2. Berekening van het aantal mol 3. Berekening in niet-normale omstandigheden 4. Oplossingen 5. Berekeningen
Bepaling toezichtvorm gemeente Stein
 Bepaling toezichtvorm 2008-2011 gemeente Stein F i n a n c i e e l v e r d i e p i n g s o n d e r z o e k P r o v i n c i e L i m b u r g, juni 2 0 0 8 V e r d i e p i n g s o n d e r z o e k S t e i
Bepaling toezichtvorm 2008-2011 gemeente Stein F i n a n c i e e l v e r d i e p i n g s o n d e r z o e k P r o v i n c i e L i m b u r g, juni 2 0 0 8 V e r d i e p i n g s o n d e r z o e k S t e i
3.1 Energie. 3.2 Kenmerken chemische reactie
 3.1 Energie Wat is energie? Energie voorziening Fossiele brandstof verbranden Co2 komt vrij slecht voor het broeikaseffect Windmolen park Zonnepanelen Energie is iets wat nodig is voor een verbrandingsreactie
3.1 Energie Wat is energie? Energie voorziening Fossiele brandstof verbranden Co2 komt vrij slecht voor het broeikaseffect Windmolen park Zonnepanelen Energie is iets wat nodig is voor een verbrandingsreactie
Eindexamen natuurkunde 1 havo 2005-II
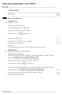 4 Beoordelingsmodel Opgave Marathonloper uitkomst: 0% Wuit Voor het rendement geldt: 00%, Ein waarin Wuit 0,0 kj(/s) en Ein,50 kj(/s). 0,0 0 Hieruit volgt dat 00% 0%., 50 0 Wuit gebruik van 00% Ein inzicht
4 Beoordelingsmodel Opgave Marathonloper uitkomst: 0% Wuit Voor het rendement geldt: 00%, Ein waarin Wuit 0,0 kj(/s) en Ein,50 kj(/s). 0,0 0 Hieruit volgt dat 00% 0%., 50 0 Wuit gebruik van 00% Ein inzicht
Tentamen spm juli uur
 spm1530 Tentamen 1 juli 2011 Tentamen spm1530 1 juli 2011 14-17 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan dit tentamen).
spm1530 Tentamen 1 juli 2011 Tentamen spm1530 1 juli 2011 14-17 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine formuleblad en periodiek systeem (afgedrukt achteraan dit tentamen).
5-1 Moleculen en atomen
 5-1 Moleculen en atomen Vraag 1. Uit hoeveel soorten moleculen bestaat een zuivere stof? Vraag 2. Wat is een molecuul? Vraag 3. Wat is een atoom? Vraag 4. Van welke heb je er het meeste: moleculen of atomen?
5-1 Moleculen en atomen Vraag 1. Uit hoeveel soorten moleculen bestaat een zuivere stof? Vraag 2. Wat is een molecuul? Vraag 3. Wat is een atoom? Vraag 4. Van welke heb je er het meeste: moleculen of atomen?
Chemisch rekenen, zo doe je dat!
 1 Chemisch rekenen, zo doe je dat! GOE Opmerkingen vooraf: 1. Belangrijke schrijfwijzen: 100 = 10 2 ; 1000 = 10 3, enz. 0,1 = 1/10 = 10-1 ; 0,001 = 1/1000 = 10-3 ; 0,000.000.1 = 10-7, enz. gram/kg = gram
1 Chemisch rekenen, zo doe je dat! GOE Opmerkingen vooraf: 1. Belangrijke schrijfwijzen: 100 = 10 2 ; 1000 = 10 3, enz. 0,1 = 1/10 = 10-1 ; 0,001 = 1/1000 = 10-3 ; 0,000.000.1 = 10-7, enz. gram/kg = gram
Hoofdstuk 3. en energieomzetting
 Energie Hoofdstuk 3 Energie en energieomzetting Grootheid Energie; eenheid Joule afkorting volledig wetenschappelijke notatie 1 J 1 Joule 1 Joule 1 J 1 KJ 1 KiloJoule 10 3 Joule 1000 J 1 MJ 1 MegaJoule
Energie Hoofdstuk 3 Energie en energieomzetting Grootheid Energie; eenheid Joule afkorting volledig wetenschappelijke notatie 1 J 1 Joule 1 Joule 1 J 1 KJ 1 KiloJoule 10 3 Joule 1000 J 1 MJ 1 MegaJoule
Spm1510-'08-'09; - Tentamen; 30 juni 2009, 14:00 17:00 uur
 -- 1 -- Spm1510-'08-'09; - Tentamen; 30 juni 2009, 14:00 17:00 uur Dit tentamen bestaat uit 13 meerkeuzevragen, 5 open vragen en een bonusvraag. De beschikbare tijd is 3 uur. U mag uitsluitend gebruiken:
-- 1 -- Spm1510-'08-'09; - Tentamen; 30 juni 2009, 14:00 17:00 uur Dit tentamen bestaat uit 13 meerkeuzevragen, 5 open vragen en een bonusvraag. De beschikbare tijd is 3 uur. U mag uitsluitend gebruiken:
NATIONALE SCHEIKUNDEOLYMPIADE
 NATIONALE SCHEIKUNDEOLYMPIADE CORRECTIEMODEL VOORRONDE 1 af te nemen in de periode van woensdag 30 januari 2013 tot en met woensdag 6 februari 2013 Deze voorronde bestaat uit 22 meerkeuzevragen verdeeld
NATIONALE SCHEIKUNDEOLYMPIADE CORRECTIEMODEL VOORRONDE 1 af te nemen in de periode van woensdag 30 januari 2013 tot en met woensdag 6 februari 2013 Deze voorronde bestaat uit 22 meerkeuzevragen verdeeld
Stand van zaken Stadswarmte in Utrecht
 Stand van zaken Stadswarmte in Utrecht Stan de Ranitz Jaarbijeenkomst Warmtenetwerk 12 mei 2016 Inhoud presentatie 1. Stadswarmte Utrecht 2. Het equivalent opwek rendement (EOR) in Utrecht 3. Verdere verduurzaming
Stand van zaken Stadswarmte in Utrecht Stan de Ranitz Jaarbijeenkomst Warmtenetwerk 12 mei 2016 Inhoud presentatie 1. Stadswarmte Utrecht 2. Het equivalent opwek rendement (EOR) in Utrecht 3. Verdere verduurzaming
h+i Bij de grenzen met Duitsland en België zijn nog mogelijkheden voor blue energie bij de mondingen van resp. de Eems en de Schelde.
 Antwoorden door T. 1507 woorden 13 juni 2016 6,8 7 keer beoordeeld Vak NaSk De zee als zonnepaneel? Behalve het versterkte broeikaseffect is ook de luchtvervuiling voor de inwoners van dichtbevolkte gebieden
Antwoorden door T. 1507 woorden 13 juni 2016 6,8 7 keer beoordeeld Vak NaSk De zee als zonnepaneel? Behalve het versterkte broeikaseffect is ook de luchtvervuiling voor de inwoners van dichtbevolkte gebieden
ZUIVERE STOF één stof, gekenmerkt door welbepaalde fysische constanten zoals kooktemperatuur, massadichtheid,.
 PARATE KENNIS CHEMIE 4 e JAAR SCHEMA ZUIVERE STOF één stof, gekenmerkt door welbepaalde fysische constanten zoals kooktemperatuur, massadichtheid,. MENGSEL bestaat uit meerdere zuivere stoffen, de kooktemperatuur,
PARATE KENNIS CHEMIE 4 e JAAR SCHEMA ZUIVERE STOF één stof, gekenmerkt door welbepaalde fysische constanten zoals kooktemperatuur, massadichtheid,. MENGSEL bestaat uit meerdere zuivere stoffen, de kooktemperatuur,
Biomassa: brood of brandstof?
 RUG3 Biomassa: brood of brandstof? Centrum voor Energie en Milieukunde dr ir Sanderine Nonhebel Dia 1 RUG3 To set the date: * >Insert >Date and Time * At Fixed: fill the date in format mm-dd-yy * >Apply
RUG3 Biomassa: brood of brandstof? Centrum voor Energie en Milieukunde dr ir Sanderine Nonhebel Dia 1 RUG3 To set the date: * >Insert >Date and Time * At Fixed: fill the date in format mm-dd-yy * >Apply
SCHEIKUNDEOLYMPIADE 2018
 SCHEIKUNDEOLYMPIADE 08 CORRECTIEMODEL VOORRONDE af te nemen in de periode van 9 tot en met maart 08 Deze voorronde bestaat uit 0 meerkeuzevragen verdeeld over 7 onderwerpen en opgaven met in totaal 6 open
SCHEIKUNDEOLYMPIADE 08 CORRECTIEMODEL VOORRONDE af te nemen in de periode van 9 tot en met maart 08 Deze voorronde bestaat uit 0 meerkeuzevragen verdeeld over 7 onderwerpen en opgaven met in totaal 6 open
Tentamen Anorganische Chemie I
 Tentamen Anorganische Chemie I 29-3-2006 et tentamen bestaat uit vijf onderdelen (A,, C, D en E). De eerste tien vragen zijn meerkeuze vragen, het is hierbij voldoende om het nummer van de vraag en het
Tentamen Anorganische Chemie I 29-3-2006 et tentamen bestaat uit vijf onderdelen (A,, C, D en E). De eerste tien vragen zijn meerkeuze vragen, het is hierbij voldoende om het nummer van de vraag en het
Tentamen ta januari uur
 Tentamen ta3290 22 januari 2010 9-12 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine periodiek systeem (afgedrukt achteraan dit tentamen). Het tentamen heeft betrekking op het
Tentamen ta3290 22 januari 2010 9-12 uur Aanwijzingen: U mag gebruik maken van: schrijfmateriaal rekenmachine periodiek systeem (afgedrukt achteraan dit tentamen). Het tentamen heeft betrekking op het
Ken en begrijp je energiegebruik Leer om te gaan met de begrippen en eenheden
 Ken en begrijp je energiegebruik Leer om te gaan met de begrippen en eenheden Rekenen met Energie Vragen en antwoorden over energie en besparingen voor VVE 010 22 juni 2017 Frans Debets www.debetsbv.nl
Ken en begrijp je energiegebruik Leer om te gaan met de begrippen en eenheden Rekenen met Energie Vragen en antwoorden over energie en besparingen voor VVE 010 22 juni 2017 Frans Debets www.debetsbv.nl
Tentamen: Energie, duurzaamheid en de rol van kernenergie
 Tentamen: Energie, duurzaamheid en de rol van kernenergie Docenten: J. F. J. van den Brand en R. Aaij Telefoon: 0620 539 484 Datum: 28 mei 2013 Zaal: WN-M143 Tijd: 08:45-11.30 uur Maak elke opgave op een
Tentamen: Energie, duurzaamheid en de rol van kernenergie Docenten: J. F. J. van den Brand en R. Aaij Telefoon: 0620 539 484 Datum: 28 mei 2013 Zaal: WN-M143 Tijd: 08:45-11.30 uur Maak elke opgave op een
Energiesysteemanalyse Thermische Centrales College TB142Ea, 19 mei 2014
 Energiesysteemanalyse Thermische Centrales College TB142Ea, 19 mei 2014 Dr.ir. Gerard P.J. Dijkema E.On kolencentrales, Maasvlakte, Rotterdam. G.P.J. Dijkema 5 mei 2014 Faculty of Technology, Policy and
Energiesysteemanalyse Thermische Centrales College TB142Ea, 19 mei 2014 Dr.ir. Gerard P.J. Dijkema E.On kolencentrales, Maasvlakte, Rotterdam. G.P.J. Dijkema 5 mei 2014 Faculty of Technology, Policy and
INTRODUCTIECURSUS BOUWCHEMIE HOOFDSTUK 1: INLEIDING MOLECULEN EN ATOMEN
 INTRODUCTIECURSUS BOUWCHEMIE HOOFDSTUK 1: INLEIDING MOLECULEN EN ATOMEN 1 OVERZICHT 1. Zuivere stof, moleculen en atomen 1. Moleculeformules 2. Elementen 3. Atoomtheorie 4. Atoommassa 5. Moleculemassa
INTRODUCTIECURSUS BOUWCHEMIE HOOFDSTUK 1: INLEIDING MOLECULEN EN ATOMEN 1 OVERZICHT 1. Zuivere stof, moleculen en atomen 1. Moleculeformules 2. Elementen 3. Atoomtheorie 4. Atoommassa 5. Moleculemassa
Presenta/e door Jan de Kraker - 5 mei 2014. Energie in Beweging
 Presenta/e door Jan de Kraker - 5 mei 2014 Energie in Beweging Wat is Well to Wheel Met Well to Wheel wordt het totale rendement van brandstoffen voor wegtransport uitgedrukt Well to Wheel maakt duidelijk
Presenta/e door Jan de Kraker - 5 mei 2014 Energie in Beweging Wat is Well to Wheel Met Well to Wheel wordt het totale rendement van brandstoffen voor wegtransport uitgedrukt Well to Wheel maakt duidelijk
Fysische Chemie Oefeningenles 1 Energie en Thermochemie. Eén mol He bevindt zich bij 298 K en standaarddruk (1 bar). Achtereenvolgens wordt:
 Fysische Chemie Oefeningenles 1 Energie en Thermochemie 1 Vraag 1 Eén mol He bevindt zich bij 298 K en standaarddruk (1 bar). Achtereenvolgens wordt: Bij constante T het volume reversibel verdubbeld. Het
Fysische Chemie Oefeningenles 1 Energie en Thermochemie 1 Vraag 1 Eén mol He bevindt zich bij 298 K en standaarddruk (1 bar). Achtereenvolgens wordt: Bij constante T het volume reversibel verdubbeld. Het
Paragraaf 1: Fossiele brandstoffen
 Scheikunde Hoofdstuk 2 Samenvatting Paragraaf 1: Fossiele brandstoffen Fossiele brandstof Koolwaterstof Onvolledige verbranding Broeikaseffect Brandstof ontstaan door het afsterven van levende organismen,
Scheikunde Hoofdstuk 2 Samenvatting Paragraaf 1: Fossiele brandstoffen Fossiele brandstof Koolwaterstof Onvolledige verbranding Broeikaseffect Brandstof ontstaan door het afsterven van levende organismen,
Eindexamen vwo scheikunde pilot I
 Duurzame productie van waterstof uit afvalwater 1 maximumscore 4 C 6 H 12 O 6 + 4 H 2 O 4 H 2 + 2 CH 3 COO + 2 HCO 3 + 4 H + molverhouding CH 3 COO : HCO 3 = 1 : 1 en C balans juist 1 coëfficiënt voor
Duurzame productie van waterstof uit afvalwater 1 maximumscore 4 C 6 H 12 O 6 + 4 H 2 O 4 H 2 + 2 CH 3 COO + 2 HCO 3 + 4 H + molverhouding CH 3 COO : HCO 3 = 1 : 1 en C balans juist 1 coëfficiënt voor
Toestandsgrootheden en energieconversie
 Toestandsgrootheden en energieconversie Dr.ir. Gerard P.J. Dijkema Faculty of Technology, Policy and Management Industry and Energy Group PO Box 5015, 2600 GA Delft, The Netherlands Eemscentrale, Eemshaven,
Toestandsgrootheden en energieconversie Dr.ir. Gerard P.J. Dijkema Faculty of Technology, Policy and Management Industry and Energy Group PO Box 5015, 2600 GA Delft, The Netherlands Eemscentrale, Eemshaven,
Les Biomassa. Werkblad
 LESSENSERIE ENERGIETRANSITIE Les Biomassa Werkblad Les Biomassa Werkblad Niet windenergie, niet zonne-energie maar biomassa is de belangrijkste bron van hernieuwbare energie in Nederland. Meer dan 50%
LESSENSERIE ENERGIETRANSITIE Les Biomassa Werkblad Les Biomassa Werkblad Niet windenergie, niet zonne-energie maar biomassa is de belangrijkste bron van hernieuwbare energie in Nederland. Meer dan 50%
Hoofdstuk 3. en energieomzetting
 Hoofdstuk 3 Energie en energieomzetting branders luchttoevoer brandstoftoevoer koelwater condensator stoomturbine generator transformator regelkamer stoom water ketel branders 1 Energiesoort Omschrijving
Hoofdstuk 3 Energie en energieomzetting branders luchttoevoer brandstoftoevoer koelwater condensator stoomturbine generator transformator regelkamer stoom water ketel branders 1 Energiesoort Omschrijving
VWO 1995 Scheikunde tijdvak 1. Het antwoord 2-methyl-1,2-propadiol of methyl-1,2-propadiol mag goed worden gerekend.
 2 3 1 notie dat het evenwicht bij hogere ph naar rechts is verschoven/afgelopen 1 (de oplossing is dan oranjegeel) dus: Mo ionen veroorzaken de oranjegele kleur 3 4 2 bij verwarmen verschuift het evenwicht
2 3 1 notie dat het evenwicht bij hogere ph naar rechts is verschoven/afgelopen 1 (de oplossing is dan oranjegeel) dus: Mo ionen veroorzaken de oranjegele kleur 3 4 2 bij verwarmen verschuift het evenwicht
