Implanon 68 mg Implantaat Subcutaan gebruik. Implanon 68 mg Implantaat Subcutaan gebruik. Implanon 68 mg Implantaat Subcutaan gebruik
|
|
|
- Esmée Boender
- 7 jaren geleden
- Aantal bezoeken:
Transcriptie
1 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG EN HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1
2 Lidstaat EU/EEA Houder van de vergunning voor het in de handel brengen Aanvrager Fantasienaam Sterkte Farmaceutische vorm Toedieningsweg Oostenrijk N.V. Organon Kloosterstraat AB, Oss België N.V. Organon Kloosterstraat 6 Tsjechië N.V. Organon Kloosterstraat 6 Denemarken N.V. Organon Kloosterstraat 6 Finland N.V. Organon Kloosterstraat 6 Frankrijk Organon SA Immeuble Optima 10, rue Godefroy Puteaux Cedex, Frankrijk Duitsland Essex Pharma GmbH Thomas-Dehler-Straße Munich Duitsland Hongarije N.V. Organon Kloosterstraat 6 Implanon - Implantat 68 mg Implantaat Subcutaan gebruik 2
3 Lidstaat EU/EEA Houder van de vergunning voor het in de handel brengen Aanvrager Fantasienaam Sterkte Farmaceutische vorm Toedieningsweg IJsland N.V. Organon Kloosterstraat 6 Ierland Organon Ireland Ltd. Drynam Road Swords Co. Dublin Ierland Italië N.V. Organon Kloosterstraat 6 Luxemburg N.V. Organon Kloosterstraat 6 Malta Organon Laboratories Ltd Cambridge Science Park Milton Road Cambridge CB4 0FL Verenigd Koninkrijk N.V. Organon Kloosterstraat 6 Noorwegen N.V. Organon Kloosterstraat 6 Portugal Organon Portuguesa Produtos Químicos e Farmacêuticos, Lda Av. José Malhoa, 16B - 2 Implanon 68 mg implant 68 mg Implantaat Subcutaan gebruik Implanon 68 mg 68 mg Implantaat Subcutaan gebruik 3
4 Lidstaat EU/EEA Houder van de vergunning voor het in de handel brengen Aanvrager Fantasienaam Sterkte Farmaceutische vorm Toedieningsweg Lisboa Portugal Slowakije N.V. Organon Kloosterstraat 6 Spanje Organon Española, S.A. Ctra. de Hospitalet, Cityparc Ronda de Dalt Edificio Amsterdam Cornellá de Llobregat, Barcelona Spanje Zweden N.V. Organon Verenigd Koninkrijk Organon Laboratories Ltd Cambridge Science Park Milton Road Cambridge CB4 0FL Verenigd Koninkrijk 4
5 BIJLAGE II WETENSCHAPPELIJKE CONCLUSIES 5
6 WETENSCHAPPELIJKE CONCLUSIES SAMENVATTING VAN DE WETENSCHAPPELIJKE BEOORDELING VAN IMPLANON Implanon is een langwerkend anticonceptivum dat bestaat uit een niet-biologisch afbreekbaar implantaat waaruit alleen een progestageen afgegeven wordt en dat direct onder de huid wordt ingebracht. De aangegeven gebruiksperiode bedraagt 3 jaar. Het implantaat is een 4 cm lang staafje met een diameter van 2 mm en bevat 68 mg etonogestrel (ENG) in een EVA-matrix (ethyleenvinylacetaat-copolymeer). Kort na het inbrengen geeft het Implanon-implantaat μg ENG per dag af; deze dosis is aan het begin van het tweede jaar afgenomen tot ongeveer 40 μg/dag en aan het eind van het derde jaar tot ongeveer μg/dag. De anticonceptieve werking van Implanon wordt voornamelijk bereikt door ovulatieremming. Implanon werd in de EU goedgekeurd tijdens een wederzijdse-erkenningsprocedure met als rapporterende lidstaat en is sinds 1998 op de markt met als indicatie anticonceptie. De eerste Europese verlenging van de handelsvergunning van Implanon vond plaats in Tot juli 2008 zijn er wereldwijd totaal 5 miljoen Implanon-implantaten verkocht. In 2007 werd een tweede Europese verlenging van de handelsvergunning in gang gezet, waarbij de meerderheid van de EU-lidstaten van mening was dat het baten-risicoprofiel nog steeds positief is en de aanbeveling van de rapporterende lidstaat voor een verlenging voor 5 jaar ondersteunde. Een van de betrokken lidstaten bracht echter een aantal bedenkingen in en vond de tweede verlenging niet aanvaardbaar. De zaak werd verwezen naar de coördinatiegroep voor wederzijdse erkenning en decentrale procedures (CMD(h)) en de rapporterende lidstaat voerde een beoordeling uit. Omdat er op dag 60 geen overeenstemming was bereikt werd de procedure verwezen naar het CHMP. Het CHMP onderzocht het dossier en de beschikbare gegevens, waarbij de door de opponerende lidstaat ingebrachte punten werden meegenomen. Het CHMP was van mening dat problemen met inbrengen, migratie en verwijdering (bekend onder de afkorting IRRE s, insertion and removal related events ) weinig en zelfs steeds minder vaak voorkomen. Het is bijzonder belangrijk, en het zou vanzelfsprekend moeten zijn, dat iedereen die de implantaten inbrengt of verwijdert, goed geinstrueerd wordt en op de hoogte is van de procedures. Als het implantaat op onjuiste wijze wordt ingebracht, kan dat leiden tot problemen bij het verwijderen ervan. Het CHMP is van mening dat de implantatie eenvoudig is en dat de IRRE s voorkomen of verminderd kunnen worden als men zich houdt aan de nieuwe instructies en de trainingsmaterialen goed bestudeert. De vergunninghouder werd verzocht om de resultaten van het Amerikaanse AMP ( active monitoring program ) voor IRRE s te rapporteren. Omdat dit AMP geen gegevens oplevert over de nieuwe applicator (Implanon NXT), werd de vergunninghouder ook gevraagd om de introductie en resultaten van de nieuwe applicator nauwlettend te volgen in het kader van het risicobeheersplan. Het CHMP was het ermee eens dat er sprake is van onderrapportage, maar vond dat er geen signalen waren voor een verhoogde kans op borstkanker. Het verschil tussen de waargenomen en het verwachte aantal gevallen is aanzienlijk en kan niet worden verklaard door onderrapportage alleen. De mogelijkheid van een verhoogd risico wordt niet ondersteund door deze postmarketing-gegevens. Bovendien is de mate van onderrapportage waarschijnlijk lager bij Implanon dan bij spontane rapportage van bijwerkingen in het algemeen; daarom vindt het CHMP niet dat spontane rapportages van borstkanker bij Implanon-gebruiksters nieuwe signalen zijn voor deze bijwerking. De informatie hierover die al vermeld wordt in rubriek 4.4 van de samenvatting van de productkenmerken, wordt voldoende geacht. De vergunninghouder heeft de beschikbare onderzoeksgegevens verzameld; in het algemeen zijn er weinig gegevens over het verband tussen anticonceptiemiddelen met alleen een progestageen en borstkanker en de beschikbare gegevens betreffen meestal het gebruik van injecteerbaar DMPA (medroxyprogesteronacetaat-depot). De meeste gegevens betreffen dus injecteerbare progestageenalleen anticonceptiva; er zijn slechts weinig gegevens over andere anticonceptiva met alleen een progestageen en helemaal geen voor Implanon. Men is het er over eens dat de beschikbare gegevens beperkingen hebben; er is een gebrek aan gegevens over het verband met de progestageen-alleen-pil (POP), de statistische kracht om risicoverbanden in subgroepen te onderzoeken is gering en er zijn geen zinvolle onderzoeksgegevens over de effecten van implantaten. Van enige relevantie zijn de gegevens uit de interim-analyse van de lopende case-controlstudie met het progestageenafgevende 6
7 spiraaltje (IUD) Mirena (verslag ICPE conferentie 2008). Hoewel Mirena zeer lage doses levonorgestrel afgeeft, kunnen de gegevens ook relevant zijn voor implantaten omdat Mirena een continue en langdurige systemische blootstelling aan progestageen bij jonge vrouwen veroorzaakt. Uit de interim-analyse komen geen gegevens die de onderzoekshypothese van een verhoogde kans op borstkanker kunnen ondersteunen. De onderzoeksgegevens zijn gecorrigeerd voor de leeftijd van de studiepopulatie, zodat die vergeleken kan worden met de gebruikerspopulatie van Implanon. Daarom zijn de eindresultaten van het onderzoek relevant voor Implanon. Na beoordeling van deze gegevens was het CHMP van mening dat er op dit moment geen duidelijke aanwijzingen zijn voor een verband tussen blootstelling aan Implanon en een verhoogde kans op borstkanker bij jonge vrouwen. Men vond de eindresultaten van de Mirena-studie relevant; zij kunnen een bijdrage leveren bij het onderzoek naar de veiligheid van Implanon. De rapportage uit het Amerikaanse AMP ( active monitoring program ) over verwijdering van Implanon bij borstkankerpatiënten kan waardevolle informatie bevatten over patiëntenseries die naar verwachting relatief volledig zullen zijn. De Mirena-studie en verslagen uit het Amerikaanse AMP moeten toegevoegd worden aan het bijgewerkte risicobeheersplan. Het CHMP is van mening dat een nieuw epidemiologisch onderzoek naar borstkanker bij Implanon-gebruiksters op dit moment niet gerechtvaardigd is. Volgens het CHMP kunnen bij alle anticonceptiemethoden met alleen progestageen onregelmatige bloedingen verwacht worden, vooral bij ovulatieremmende methoden. Dit algemeen bekende feit is soms een reden om met deze anticonceptiemethode te stoppen. Hoewel het bloedingspatroon vaak onvoorspelbaar is, rapporteren vele vrouwen een vermindering van de frequentie van bloedingsperioden en van het totale aantal dagen met bloedverlies ten opzichte van hun normale menstruatiepatroon. Bijna alle vrouwen hebben een vermindering van het totale bloedverlies, zelfs vrouwen met een toename van het aantal bloedingsdagen. Veel vrouwen zijn daarom tevreden met het bloedingspatroon, hoewel de onvoorspelbaarheid voor sommigen een probleem blijft. Het CHMP is van mening dat veranderingen in het bloedingspatroon niet beschouwd mogen worden als een probleem voor de gezondheid omdat het patroon normaliseert als Implanon gestaakt wordt en er geen gezondheidsrisico s voor de vrouw uit voortkomen. Uit ervaring blijkt dat zorgvuldige voorlichting en advies voorafgaand aan de implantatie, evenals ondersteuning en het gebruik van een bloedingsdagboek tijdens het gebruik, belangrijk zijn voor de acceptatie en compliance op lange termijn. De verwijdering van Implanon wegens onregelmatig bloedverlies mag niet beschouwd worden als een ernstige complicatie, omdat de chirurgische ingreep voor het verwijderen van Implanon minimaal is: na een oppervlakkige huidincisie van slechts 0,5-1 cm kan het implantaat verwijderd worden. Het voorstel van de vergunninghouder voor aanvulling van de informatie over bloedingen in rubriek 4.8 met de nieuwe Amerikaanse gegevens en verbetering van het voorlichtingsmateriaal over het bloedingspatroon werd goedgekeurd. Het CHMP was van mening dat in de EU schriftelijke informatie en toestemming ( informed consent ) in verband wordt gebracht met geneesmiddelen die een ernstig risico met zich brengen en dat de invoering van een informatie- en toestemmingsprocedure voor Implanon, een van de meest gebruikte anticonceptiemethoden, niet gerechtvaardigd is; het zou geheel ten onrechte kunnen duiden op de aanwezigheid van een gezondheidsrisico. Het belangrijkste voordeel van alle anticonceptiemethoden is de werkzaamheid. Volgens het CHMP is Implanon bijzonder goed werkzaam en zijn er geen aanwijzingen voor een verminderde werkzaamheid tijdens het derde gebruiksjaar of bij vrouwen met overgewicht. Ook vond het CHMP de huidige tekst van de samenvatting van de productkenmerken over werkzaamheid en gewicht zinvol en correct. Er zijn geen anticonceptiemethoden die aan alle eisen voldoen en daarom is er een breed scala van methoden ontwikkeld om voor iedere vrouw een methode te kunnen vinden die voldoet aan haar behoeften van dat moment. Het grote voordeel van implantaten is de afwezigheid van complianceproblemen of maagdarmstoornissen die een negatief effect hebben op de anticonceptieve werkzaamheid. Een nadeel vormen de onregelmatige bloedingen die voorkomen bij alle continue progestageen-alleen methoden die de ovulatie remmen. Het CHMP was ten slotte van mening dat de anticonceptieve werkzaamheid van Implanon beter is dan die van andere hormonale anticonceptiva en dat de Pearl Index van Implanon duidelijk lager is dan die van andere systemische hormonale anticonceptiva en zeker lager dan die van gecombineerde orale anticonceptiva, vooral ook omdat die 7
8 vaak vergeten worden en meer maagdarmstoornissen met zich brengen. Samenvattend vindt het CHMP Implanon een effectieve anticonceptiemethode met een positieve baten-risicoverhouding die geen duidelijke veiligheidsproblemen met zich brengt. De aanvullende gegevens uit het Amerikaanse AMP zijn welkom, vooral de gegevens over de werkzaamheid bij vrouwen met ernstig overgewicht. Na beoordeling van alle bij de aanvraag ingediende gegevens was het CHMP van mening dat er verder gewerkt moet worden aan vermindering van de risico s met als doel een veilig en effectief gebruik van dit farmaceutische product. Het risicobeheersplan wordt binnen 3 maanden ingediend bij de rapporterende lidstaat en zal alle punten bevatten die genoemd worden in de voorwaarden voor vernieuwing van de vergunning voor het in de handel brengen. REDENEN VOOR HET ADVIES Samenvattend vindt het CHMP Implanon een effectieve anticonceptiemethode met een positieve baten-risicoverhouding die geen duidelijke veiligheidsproblemen met zich brengt. Het CHMP stemde in met het volgende voorstel voor voorwaarden voor de vernieuwing van de handelsvergunning dat reeds eerder was ingediend door de rapporterende lidstaat: De nieuwe handelsvergunning wordt toegekend voor 5 jaar, onder de volgende voorwaarden: De vergunninghouder gaat door met de 12-maandelijkse rapportage van mogelijke bijwerkingen (PSUR s of Periodic Safety Update Reports ). De vergunninghouder gaat de komende 5 jaar door met de 6-maandelijkse rapportage over alle onbedoelde zwangerschappen en problemen met het inbrengen en verwijderen van de implantaten (IRRE s). Bij de 6-maandelijkse IRRE-rapportage voegt de vergunninghouder de meest recente resultaten van het lopende AMP ( active monitoring program ) in de VS. In 2009 doet de vergunninghouder een aanvraag voor een type II-wijziging voor de introductie van het nieuwe Implanon (Implanon NXT). Een voorstel voor een risicobeheersplan voor Implanon NXT zal deel uitmaken van deze wijziging. De vergunninghouder verbetert het voorlichtings- en adviesmateriaal voor artsen en verpleegkundigen en de gebruiksters over de bloedingspatronen die tijdens het gebruik van Implanon op kunnen treden. Dit materiaal kan worden aangeboden aan vrouwen die overwegen om Implanon als anticonceptiemethode te gaan gebruiken. Relevante onderdelen van de bovengenoemde activiteiten worden beschreven in een voorstel voor een risicobeheersplan dat de vergunninghouder binnen drie maanden zal indienen. Bovendien moeten in het ontwerpplan de volgende punten worden opgenomen: In het AMP wordt bij vroegtijdige verwijdering van het implantaat (met inbegrip van zwangerschap) gevraagd naar het lichaamsgewicht. Aanvulling van de informatie over het bloedingspatroon in rubriek 4.8 van de samenvatting van de productkenmerken en bijsluiter zoals voorgesteld in het etiketteringsontwerp van de vergunninghouder. Overwegende dat - de lange gebruiksduur en de afwezigheid van compliance-problemen een duidelijk voordeel van de methode zijn, - correct inbrengen van het implantaat eenvoudig is en IRRE s voorkomen of verminderd kunnen worden als men zich houdt aan de nieuwe instructies en de trainingsmaterialen goed bestudeert, - er geen signalen geïdentificeerd zijn voor een toename van de kans op borstkanker, - onregelmatigheden in het bloedingspatroon niet beschouwd kunnen worden als een gezondheidsprobleem, 8
9 - Implanon bewezen heeft dat het een effectieve anticonceptiemethode is, ook bij vrouwen met overgewicht, ondanks een lage dosering, adviseert het CHMP verlenging van de vergunning voor het in de handel brengen van Implanon, waarvoor de samenvatting van de productkenmerken, etikettering en bijsluiter zijn weergegeven in bijlage III. 9
10 BIJLAGE III SAMENVATTING VAN DE PRODUCTKENMERKEN, ETIKETTERING EN BIJSLUITER 10
11 De geldige Samenvatting van de productkenmerken, etikettering en bijsluiter zijn de finale versies verkregen tijdens de Coördinatie groep procedure. 11
12 BIJLAGE IV VOORWAARDEN VOOR DE VERLENGING VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN 12
13 De nationale bevoegde instanties, gecoördineerd door de rapporterende lidstaat, zullen ervoor zorgen dat de volgende voorwaarden door de houders van de vergunning voor het in de handel brengen worden vervuld: De nieuwe handelsvergunning wordt toegekend voor 5 jaar, onder de volgende voorwaarden: De vergunninghouder gaat door met de 12-maandelijkse rapportage van mogelijke bijwerkingen (PSUR s of Periodic Safety Update Reports ). De vergunninghouder gaat de komende 5 jaar door met de 6-maandelijkse rapportage over alle onbedoelde zwangerschappen en problemen met het inbrengen en verwijderen van de implantaten (IRRE s). Bij de 6-maandelijkse IRRE-rapportage voegt de vergunninghouder de meest recente resultaten van het lopende AMP ( active monitoring program ) in de VS. In 2009 doet de vergunninghouder een aanvraag voor een type II-wijziging voor de introductie van het nieuwe Implanon (Implanon NXT). Een voorstel voor een risicobeheersplan voor Implanon NXT zal deel uitmaken van deze wijziging. De vergunninghouder verbetert het voorlichtings- en adviesmateriaal voor artsen en verpleegkundigen en de gebruiksters over de bloedingspatronen die tijdens het gebruik van Implanon op kunnen treden. Dit materiaal kan worden aangeboden aan vrouwen die overwegen om Implanon als anticonceptiemethode te gaan gebruiken. Relevante onderdelen van de bovengenoemde activiteiten worden beschreven in een voorstel voor een risicobeheersplan dat de vergunninghouder binnen drie maanden zal indienen. Bovendien moeten in het ontwerpplan de volgende punten worden opgenomen: In het AMP wordt bij vroegtijdige verwijdering van het implantaat (met inbegrip van zwangerschap) gevraagd naar het lichaamsgewicht. Aanvulling van de informatie over het bloedingspatroon in rubriek 4.8 van de samenvatting van de productkenmerken en bijsluiter zoals voorgesteld in het etiketteringsontwerp van de vergunninghouder. 13
Houder van de vergunning voor het in de handel brengen. Fantasienaam Sterkte Farmaceutische vorm Toedieningsweg
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1 Lidstaat Oostenrijk België Cyprus
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1 Lidstaat Oostenrijk België Cyprus
BIJLAGE I. EMEA/CVMP/495339/2007-NL november 2007 1/10
 BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN DE GENEESMIDDELEN, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER/AANVRAGER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EMEA/CVMP/495339/2007-NL november
BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN DE GENEESMIDDELEN, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER/AANVRAGER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EMEA/CVMP/495339/2007-NL november
NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
 BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN 1/7 Aanvrager of houder van de vergunning voor
BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN 1/7 Aanvrager of houder van de vergunning voor
Wetenschappelijke conclusies
 Bijlage II Wetenschappelijke conclusies en redenen voor het positieve advies voor de handelsvergunning mits aan de voorwaarden wordt voldaan, en voor de wijziging van de samenvatting van de productkenmerken
Bijlage II Wetenschappelijke conclusies en redenen voor het positieve advies voor de handelsvergunning mits aan de voorwaarden wordt voldaan, en voor de wijziging van de samenvatting van de productkenmerken
NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
 BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN 1/7 Aanvrager of houder van de vergunning voor
BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN 1/7 Aanvrager of houder van de vergunning voor
NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORT, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
 BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORT, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN 1/7 Aanvrager of houder van de vergunning voor het
BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORT, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN 1/7 Aanvrager of houder van de vergunning voor het
Lidstaat Houder van de vergunning voor het in de handel brengen Fantasienaam Sterkte Farmaceutische vorm Toedieningswijze SIMVASTATIN BMM PHARMA
 BIJLAGE I LIJST VAN DE NAMEN, FARMACEUTISCHE VORMEN, STERKTES VAN DE GENEESMIDDELEN, TOEDIENINGSWIJZE EN HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1 Lidstaat Houder van de
BIJLAGE I LIJST VAN DE NAMEN, FARMACEUTISCHE VORMEN, STERKTES VAN DE GENEESMIDDELEN, TOEDIENINGSWIJZE EN HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1 Lidstaat Houder van de
Aanvrager (Fantasie) Naam Sterkte Farmaceutische vorm. Actocalcio D3 35 mg mg/880 IU. Acrelcombi 35 mg mg/880 IU
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORMEN, STERKTEN VAN HET GENEESMIDDELEN, TOEDIENINGSWEG, AANVRAGERS, HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1 Lidstaat EU/EER Houder
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORMEN, STERKTEN VAN HET GENEESMIDDELEN, TOEDIENINGSWEG, AANVRAGERS, HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1 Lidstaat EU/EER Houder
Vantas 50 mg Implantaat Subcutaan 50 mg Ireland Ltd North Wall Quay, Dublin, Ierland Duitsland Valera
 BIJLAGE I LIJST MET DE NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, AANVRAGER EN VERGUNNINGHOUDER VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN Lidstaat Houder van de vergunning
BIJLAGE I LIJST MET DE NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, AANVRAGER EN VERGUNNINGHOUDER VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN Lidstaat Houder van de vergunning
NAAM, FARMACEUTISCHE VORM, STERKTE VAN DE GENEESMIDDELEN, DIERSOORTEN, TOEDIENINGSWEGEN, EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
 BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN DE GENEESMIDDELEN, DIERSOORTEN, TOEDIENINGSWEGEN, EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EMEA/CVMP/166766/2006-NL mei 2006 1/7 Lidstaat
BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN DE GENEESMIDDELEN, DIERSOORTEN, TOEDIENINGSWEGEN, EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EMEA/CVMP/166766/2006-NL mei 2006 1/7 Lidstaat
Leflunomid Actavis 20 mg Filmtabletten LEFLUNOMID ACTAVIS 20 MG. Leflunomide Actavis 100 mg, filmomhulde
 Bijlage I Lijst met namen, farmaceutische vorm, sterkte van het geneesmiddel, toedieningsweg en houder van de vergunning voor het in de handel brengen in de lidstaten 1 Lidstaat EU/EEA Houder van de vergunning
Bijlage I Lijst met namen, farmaceutische vorm, sterkte van het geneesmiddel, toedieningsweg en houder van de vergunning voor het in de handel brengen in de lidstaten 1 Lidstaat EU/EEA Houder van de vergunning
IMPLANON NXT informatiebrochure voor patiënten
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel IMPLANON NXT. Het verplicht plan voor risicobeperking in België, waarvan deze
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel IMPLANON NXT. Het verplicht plan voor risicobeperking in België, waarvan deze
Farmaceutische vorm. Amoxicillin 40 mg Clavulanic acid 10 mg. Clavulanic acid 10 mg. Clavulanic acid 10 mg. Clavulanic acid 10 mg
 Bijlage I Lijst met nam, farmaceutische vorm, sterkte van het geesmiddel voor diergeeskundig gebruik, diersoort, toediingsweg, aanvrager/houder van de handelsvergunning in de lidstat 1/11 Lidstaat EU/EER
Bijlage I Lijst met nam, farmaceutische vorm, sterkte van het geesmiddel voor diergeeskundig gebruik, diersoort, toediingsweg, aanvrager/houder van de handelsvergunning in de lidstat 1/11 Lidstaat EU/EER
Arimidex 1 mg Filmomhulde tabletten Oraal. Arimidex 1 mg Filmomhulde tabletten Oraal. Arimidex 1 mg Filmomhulde tabletten Oraal
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, HOUDER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN Lidstaat Houder van de vergunning
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, HOUDER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN Lidstaat Houder van de vergunning
Lipophoral Tablets 150mg. Mediator 150 mg Tablet Oraal gebruik. Benfluorex Qualimed. Mediator 150mg Tablet Oraal gebruik
 BIJLAGE I LIJST MET FANTASIENAMEN, FARMACEUTISCHE VORMEN, STERKTE VAN DE GENEESMIDDELEN, TOEDIENINGSWEG EN HOUDERS VAN EEN VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN (EER) 1 Lidstaat Cyprus
BIJLAGE I LIJST MET FANTASIENAMEN, FARMACEUTISCHE VORMEN, STERKTE VAN DE GENEESMIDDELEN, TOEDIENINGSWEG EN HOUDERS VAN EEN VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN (EER) 1 Lidstaat Cyprus
IMPLANON NXT informatiebrochure voor patiënten
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel IMPLANON NXT. Het verplicht plan voor risicobeperking in België, waarvan deze
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel IMPLANON NXT. Het verplicht plan voor risicobeperking in België, waarvan deze
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, AANVRAGERS IN DE LIDSTATEN
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, AANVRAGERS IN DE LIDSTATEN 1 AT - Oostenrijk Flutiform 50 Mikrogramm/5 Mikrogramm pro Sprühstoß Druckgasinhalation
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, AANVRAGERS IN DE LIDSTATEN 1 AT - Oostenrijk Flutiform 50 Mikrogramm/5 Mikrogramm pro Sprühstoß Druckgasinhalation
Bijlage I. Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen
 Bijlage I Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen 1 Wetenschappelijke conclusies Rekening houdend met het beoordelingsrapport
Bijlage I Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen 1 Wetenschappelijke conclusies Rekening houdend met het beoordelingsrapport
INFORMATIE IMPLANON NXT. 3 jaar onbezorgde anticonceptie. 3 jaar onbezorgde anticonceptie
 INFORMATIE IMPLANON NXT Inhoud Introductie 3 Eigenschappen 4 Werking 6 Inbrengen 8 Het juiste startmoment 10 Menstruatie 13 Betrouwbaarheid 14 Bijwerkingen 15 Veilig vrijen 15 Combinatie met andere geneesmiddelen
INFORMATIE IMPLANON NXT Inhoud Introductie 3 Eigenschappen 4 Werking 6 Inbrengen 8 Het juiste startmoment 10 Menstruatie 13 Betrouwbaarheid 14 Bijwerkingen 15 Veilig vrijen 15 Combinatie met andere geneesmiddelen
Naam Sterkte Farmaceutische vorm Wijze van toediening. Lidstaat EU/EER Houder van de vergunning voor het in de handel brengen
 BIJLAGE I LIJST VAN DE NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, WIJZE VAN TOEDIENING, HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1 Lidstaat EU/EER Houder van
BIJLAGE I LIJST VAN DE NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, WIJZE VAN TOEDIENING, HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1 Lidstaat EU/EER Houder van
Bijlage I. Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen
 Bijlage I Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen 1 Wetenschappelijke conclusies Rekening houdend met het beoordelingsrapport
Bijlage I Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen 1 Wetenschappelijke conclusies Rekening houdend met het beoordelingsrapport
Drie jaar niet meer aan mijn anticonceptie denken.
 I N F O R M A T I E Drie jaar niet meer aan mijn anticonceptie denken. 3 jaar onbezorgde anticonceptie Inhoud Introductie Introductie............................................ 3 Eigenschappen........................................
I N F O R M A T I E Drie jaar niet meer aan mijn anticonceptie denken. 3 jaar onbezorgde anticonceptie Inhoud Introductie Introductie............................................ 3 Eigenschappen........................................
INFORMATIE IMPLANON NXT. 3 jaar onbezorgde anticonceptie. 3 jaar onbezorgde anticonceptie
 INFORMATIE IMPLANON NXT Inhoud Introductie 3 Eigenschappen 4 Werking 6 Inbrengen 8 Het juiste startmoment 10 Menstruatie 13 Betrouwbaarheid 14 Introductie Je hebt gekozen voor IMPLANON NXT. Dit is een
INFORMATIE IMPLANON NXT Inhoud Introductie 3 Eigenschappen 4 Werking 6 Inbrengen 8 Het juiste startmoment 10 Menstruatie 13 Betrouwbaarheid 14 Introductie Je hebt gekozen voor IMPLANON NXT. Dit is een
Fantasienaam Sterkte Farmaceutische vorm. Tavanic 250 mg Filmtabletten. Tavanic 500 mg Filmtabletten. Tavanic Infusionsflasche
 Bijlage I Lijst met namen, farmaceutische en, sterkten van de geneesmiddelen, toedieningswegen, houders van de in de lidstaten 1 Oostenrijk Oostenrijk Oostenrijk België België België Bulgarije Bulgarije
Bijlage I Lijst met namen, farmaceutische en, sterkten van de geneesmiddelen, toedieningswegen, houders van de in de lidstaten 1 Oostenrijk Oostenrijk Oostenrijk België België België Bulgarije Bulgarije
Wetenschappelijke conclusies en redenen voor de conclusies
 Bijlage IV Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunningen voor het in de handel brengen, en nadere uitleg over het onderscheid in de aanbeveling van het
Bijlage IV Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunningen voor het in de handel brengen, en nadere uitleg over het onderscheid in de aanbeveling van het
NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
 BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN 1/7 Lidstaat Aanvrager of houder van de vergunning
BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN 1/7 Lidstaat Aanvrager of houder van de vergunning
Lidstaat Houder van de vergunning voor het in de handel brengen Fantasienaam Sterkte Farmaceutische vorm Toedieningsweg
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN CHMP/309507/2007 1/6 EMEA 2007 Lidstaat
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN CHMP/309507/2007 1/6 EMEA 2007 Lidstaat
Aanvrager Naam Sterkte Farmaceutische vorm. Lansoprazol TEVA 15 mg Kapseln Lansoprazol TEVA 30 mg Kapseln
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORMEN, STERKTEN VAN DE GENEESMIDDELLEN, TOEDIENINGSWEGEN, AANVRAGERS, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN Lidstaat Houder
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORMEN, STERKTEN VAN DE GENEESMIDDELLEN, TOEDIENINGSWEGEN, AANVRAGERS, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN Lidstaat Houder
Bijlage IV. Wetenschappelijke conclusies en redenen voor de wijziging in de voorwaarden van de vergunningen voor het in de handel brengen
 Bijlage IV Wetenschappelijke conclusies en redenen voor de wijziging in de voorwaarden van de vergunningen voor het in de handel brengen 28 Wetenschappelijke conclusies Algehele samenvatting van de wetenschappelijke
Bijlage IV Wetenschappelijke conclusies en redenen voor de wijziging in de voorwaarden van de vergunningen voor het in de handel brengen 28 Wetenschappelijke conclusies Algehele samenvatting van de wetenschappelijke
Bijlage I. Lijst van nationaal goedgekeurde geneesmiddelen en vergunningaanvragen
 Bijlage I Lijst van nationaal goedgekeurde geneesmiddelen en vergunningaanvragen 1 Bijlage IA: Geneesmiddelen aanbevolen voor handhaving en aanvragen van vergunningen voor het in de handel brengen waarvoor
Bijlage I Lijst van nationaal goedgekeurde geneesmiddelen en vergunningaanvragen 1 Bijlage IA: Geneesmiddelen aanbevolen voor handhaving en aanvragen van vergunningen voor het in de handel brengen waarvoor
LIJST MET NAMEN, FARMACEUTISCHE VORMEN, STERKTEN, DIERSOORTEN, TOEDIENINGSWEGEN, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN / AANVRAGERS
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORMEN, STERKTEN, DIERSOORTEN, TOEDIENINGSWEGEN, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN / AANVRAGERS 1/9 Lidstaat/nummer van de vergunning voor
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORMEN, STERKTEN, DIERSOORTEN, TOEDIENINGSWEGEN, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN / AANVRAGERS 1/9 Lidstaat/nummer van de vergunning voor
Bijlage I. Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen
 Bijlage I Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen 1 Wetenschappelijke conclusies Rekening houdend met het beoordelingsrapport
Bijlage I Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen 1 Wetenschappelijke conclusies Rekening houdend met het beoordelingsrapport
LIJST MET NAMEN, FARMACEUTISCHE VORM, DIERSOORTEN, TOEDIENINGSWEG EN HOUDERS VAN DE VERGUNNINGEN VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, DIERSOORTEN, TOEDIENINGSWEG EN HOUDERS VAN DE VERGUNNINGEN VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN EMEA/CVMP/269630/2006-NL juli 2006 1/7 Lidstaat
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, DIERSOORTEN, TOEDIENINGSWEG EN HOUDERS VAN DE VERGUNNINGEN VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN EMEA/CVMP/269630/2006-NL juli 2006 1/7 Lidstaat
Aanvrager Fantasienaam Sterkte Farmaceutische vorm. Loratadine. Vitabalans 10 mg tablety. Loratadine. Vitabalans. Vitabalans 10 mg tabletes
 Biljage I Lijst met namen, farmaceutische vorm, sterkte van het geneesmiddel, toedieningsweg, aanvrager en houder van de vergunning voor het in de handel brengen in de lidstaten 1 Lidstaat (EU/EER) Houder
Biljage I Lijst met namen, farmaceutische vorm, sterkte van het geneesmiddel, toedieningsweg, aanvrager en houder van de vergunning voor het in de handel brengen in de lidstaten 1 Lidstaat (EU/EER) Houder
Fantasienaam Sterkte Farmaceutische vorm. Sandimmun 50 mg/ml Concentraat voor oplossing voor infusie 50 mg/ml
 BIJLAGE I LIJST VAN DE NAMEN, FARMACEUTISCHE VORMEN, STERKTES VAN DE GENEESMIDDELEN, TOEDIENINGSWEG, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1 Oostenrijk België Tsjechië
BIJLAGE I LIJST VAN DE NAMEN, FARMACEUTISCHE VORMEN, STERKTES VAN DE GENEESMIDDELEN, TOEDIENINGSWEG, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1 Oostenrijk België Tsjechië
Bijlage II. Wetenschappelijke conclusies en redenen voor het positieve advies, opgesteld door het Europees Geneesmiddelenbureau
 Bijlage II Wetenschappelijke conclusies en redenen voor het positieve advies, opgesteld door het Europees Geneesmiddelenbureau 6 Wetenschappelijke conclusies Algehele samenvatting van de wetenschappelijke
Bijlage II Wetenschappelijke conclusies en redenen voor het positieve advies, opgesteld door het Europees Geneesmiddelenbureau 6 Wetenschappelijke conclusies Algehele samenvatting van de wetenschappelijke
Fantasienaam Sterkte Farmaceutisch e vorm
 Bijlage I Lijst met namen, farmaceutische vorm, sterkte van het geneesmiddel voor diergeneeskundig gebruik, diersoorten, houders van de vergunning voor het in de handel brengen in de lidstaten 1/10 Lidstaat
Bijlage I Lijst met namen, farmaceutische vorm, sterkte van het geneesmiddel voor diergeneeskundig gebruik, diersoorten, houders van de vergunning voor het in de handel brengen in de lidstaten 1/10 Lidstaat
Bijlage III. Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiters
 Bijlage III Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiters NB: Deze Samenvatting van de productkenmerken, Etikettering
Bijlage III Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiters NB: Deze Samenvatting van de productkenmerken, Etikettering
Bijlage I. Lijst met namen, farmaceutische vorm, sterkten van de geneesmiddelen, toedieningsweg, aanvrager in de lidstaten
 Bijlage I Lijst met namen, farmaceutische vorm, sterkten van de geneesmiddelen, toedieningsweg, aanvrager in de lidstaten 1 Lidstaat EU/EEA Aanvrager (Fantasie)naam Sterkte Farmaceutische vorm Toedieningsweg
Bijlage I Lijst met namen, farmaceutische vorm, sterkten van de geneesmiddelen, toedieningsweg, aanvrager in de lidstaten 1 Lidstaat EU/EEA Aanvrager (Fantasie)naam Sterkte Farmaceutische vorm Toedieningsweg
Voorstel voor een BESLUIT VAN DE RAAD. ter bepaling van de samenstelling van het Economisch en Sociaal Comité
 EUROPESE COMMISSIE Brussel, 11.6.2014 COM(2014) 227 final 2014/0129 (NLE) Voorstel voor een BESLUIT VAN DE RAAD ter bepaling van de samenstelling van het Economisch en Sociaal Comité NL NL TOELICHTING
EUROPESE COMMISSIE Brussel, 11.6.2014 COM(2014) 227 final 2014/0129 (NLE) Voorstel voor een BESLUIT VAN DE RAAD ter bepaling van de samenstelling van het Economisch en Sociaal Comité NL NL TOELICHTING
de heer Jordi AYET PUIGARNAU, directeur, namens de secretarisgeneraal van de Europese Commissie
 Raad van de Europese Unie Brussel, 23 mei 2017 (OR. en) 9601/17 ADD 4 JAI 537 ASIM 57 CO EUR-PREP 27 BEGELEIDENDE NOTA van: ingekomen: 17 mei 2017 aan: de heer Jordi AYET PUIGARNAU, directeur, namens de
Raad van de Europese Unie Brussel, 23 mei 2017 (OR. en) 9601/17 ADD 4 JAI 537 ASIM 57 CO EUR-PREP 27 BEGELEIDENDE NOTA van: ingekomen: 17 mei 2017 aan: de heer Jordi AYET PUIGARNAU, directeur, namens de
Raad van de Europese Unie Brussel, 18 mei 2017 (OR. en)
 Raad van de Europese Unie Brussel, 18 mei 2017 (OR. en) 9438/17 ADD 1 MAP 12 BEGELEIDENDE NOTA van: ingekomen: 17 mei 2017 aan: de heer Jordi AYET PUIGARNAU, directeur, namens de secretaris-generaal van
Raad van de Europese Unie Brussel, 18 mei 2017 (OR. en) 9438/17 ADD 1 MAP 12 BEGELEIDENDE NOTA van: ingekomen: 17 mei 2017 aan: de heer Jordi AYET PUIGARNAU, directeur, namens de secretaris-generaal van
Tarieven Europa: staffel 1
 Tarieven Europa: staffel 1 Wanneer u op basis van uw daadwerkelijkaantal zendingen boven de 49 zendingen per jaar uitkomt, dan kunt u ons contacteren voor verbeterde tarieven. Wij passen uw prijzen dan
Tarieven Europa: staffel 1 Wanneer u op basis van uw daadwerkelijkaantal zendingen boven de 49 zendingen per jaar uitkomt, dan kunt u ons contacteren voor verbeterde tarieven. Wij passen uw prijzen dan
Algehele samenvatting van de wetenschappelijke beoordeling van nimesulidebevattende geneesmiddelen voor systemisch gebruik (zie bijlage I)
 Bijlage II Wetenschappelijke conclusies en redenen voor de wijzigingen van de samenvatting van de productkenmerken en de bijsluiter, opgesteld door het EMA 42 Wetenschappelijke conclusies Algehele samenvatting
Bijlage II Wetenschappelijke conclusies en redenen voor de wijzigingen van de samenvatting van de productkenmerken en de bijsluiter, opgesteld door het EMA 42 Wetenschappelijke conclusies Algehele samenvatting
Annex I. Lijst van namen, farmaceutische vorm, sterkten van het geneesmiddel, toedieningsweg en aanvrager in de Member States.
 Annex I Lijst van namen, farmaceutische vorm, sterkten van het geneesmiddel, toedieningsweg en aanvrager in de Member States. Lidstaat EU/EEA Aanvrager (Fantasienaam ) Naam Sterkte Farmaceutische vorm
Annex I Lijst van namen, farmaceutische vorm, sterkten van het geneesmiddel, toedieningsweg en aanvrager in de Member States. Lidstaat EU/EEA Aanvrager (Fantasienaam ) Naam Sterkte Farmaceutische vorm
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Claritine, tabletten 10 mg. loratadine
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Claritine, tabletten 10 mg loratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor u. Gebruik
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Claritine, tabletten 10 mg loratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor u. Gebruik
Wetenschappelijke conclusies
 BIJLAGE II WETENSCHAPPELIJKE CONCLUSIES EN REDENEN VOOR DE WIJZIGING VAN DE SAMENVATTING VAN DE PRODUCTKENMERKEN, DE ETIKETTERING EN DE BIJSLUITER, OPGESTELD DOOR HET EUROPEES GENEESMIDDELENBUREAU 14 Wetenschappelijke
BIJLAGE II WETENSCHAPPELIJKE CONCLUSIES EN REDENEN VOOR DE WIJZIGING VAN DE SAMENVATTING VAN DE PRODUCTKENMERKEN, DE ETIKETTERING EN DE BIJSLUITER, OPGESTELD DOOR HET EUROPEES GENEESMIDDELENBUREAU 14 Wetenschappelijke
ANNEX BIJLAGE. bij VERSLAG VAN DE COMMISSIE AAN HET EUROPEES PARLEMENT EN DE RAAD
 EUROPESE COMMISSIE Brussel, 21.9.2018 COM(2018) 651 final ANNEX BIJLAGE bij VERSLAG VAN DE COMMISSIE AAN HET EUROPEES PARLEMENT EN DE RAAD over de werking van Richtlijn 2011/24/EU betreffende de toepassing
EUROPESE COMMISSIE Brussel, 21.9.2018 COM(2018) 651 final ANNEX BIJLAGE bij VERSLAG VAN DE COMMISSIE AAN HET EUROPEES PARLEMENT EN DE RAAD over de werking van Richtlijn 2011/24/EU betreffende de toepassing
Bijsluiter: informatie voor de gebruiker. Bridion 100 mg/ml oplossing voor injectie sugammadex
 Bijsluiter: informatie voor de gebruiker Bridion 100 mg/ml oplossing voor injectie sugammadex Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke informatie
Bijsluiter: informatie voor de gebruiker Bridion 100 mg/ml oplossing voor injectie sugammadex Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke informatie
Volume: 0-49 zendingen per jaar Europa 0 2 kg 2-10 kg kg kg
 Wanneer u op basis van uw daadwerkelijkaantal zendingen boven de 49 zendingen per jaar uitkomt, dan kunt u ons contacteren voor verbeterde tarieven. Wij passen uw prijzen dan direct aan. Volume: 0-49 zendingen
Wanneer u op basis van uw daadwerkelijkaantal zendingen boven de 49 zendingen per jaar uitkomt, dan kunt u ons contacteren voor verbeterde tarieven. Wij passen uw prijzen dan direct aan. Volume: 0-49 zendingen
Informatie voor beroepsbeoefenaren in de gezondheidszorg. Brochure Zwangerschapspreventie Programma (ZPP)
 Imnovid (pomalidomide) Informatie voor beroepsbeoefenaren in de gezondheidszorg Brochure Zwangerschapspreventie Programma (ZPP) Inleiding De additionele risico minimalisatie materialen voor Imnovid (pomalidomide),
Imnovid (pomalidomide) Informatie voor beroepsbeoefenaren in de gezondheidszorg Brochure Zwangerschapspreventie Programma (ZPP) Inleiding De additionele risico minimalisatie materialen voor Imnovid (pomalidomide),
0,5 mg - Tabletten. 1mg - Tabletten. 2 mg - Tabletten. 3 mg - Tabletten. 4 mg - Tabletten. Risperidon Risperdal 0,5 mg - Filmtabletten
 BIJLAGE I LIJST VAN DE NAMEN, FARMACEUTISCHE VORMEN, STERKTE VAN DE GENEESMIDDELEN, TOEDIENINGSWEG, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1 Lidstaat Registratiehouder
BIJLAGE I LIJST VAN DE NAMEN, FARMACEUTISCHE VORMEN, STERKTE VAN DE GENEESMIDDELEN, TOEDIENINGSWEG, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1 Lidstaat Registratiehouder
Claritine 10mg tabletten. loratadine
 CLARITINE Bijsluiter: informatie voor de gebruiker Claritine 10mg tabletten loratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor
CLARITINE Bijsluiter: informatie voor de gebruiker Claritine 10mg tabletten loratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor
(Fantasie)naam Sterkte Farmaceutische vorm. VASOBRAL, comprimé sécable. VASOBRAL, solution buvable en flacon. 0,10 g/1 g per 100 ml
 Bijlage I Lijst met namen, farmaceutische vorm, sterkten van de geneesmiddelen, toedieningswegen, aanvrager(s), houder(s) van de vergunning voor het in de handel brengen in de lidstaten 1 Lidstaat (EU/EER)
Bijlage I Lijst met namen, farmaceutische vorm, sterkten van de geneesmiddelen, toedieningswegen, aanvrager(s), houder(s) van de vergunning voor het in de handel brengen in de lidstaten 1 Lidstaat (EU/EER)
BIJSLUITER: INFORMATIE VOOR DE PATIËNT
 BIJSLUITER: INFORMATIE VOOR DE PATIËNT Tiorfix 100 mg harde capsules Racecadotril Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat innemen want er staat belangrijke informatie in voor u. Gebruik
BIJSLUITER: INFORMATIE VOOR DE PATIËNT Tiorfix 100 mg harde capsules Racecadotril Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat innemen want er staat belangrijke informatie in voor u. Gebruik
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Claritine, tabletten 10 mg. loratadine
 Bijsluiter Pagina 1/5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Claritine, tabletten 10 mg loratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
Bijsluiter Pagina 1/5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Claritine, tabletten 10 mg loratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
Raad van de Europese Unie Brussel, 9 november 2017 (OR. en)
 Raad van de Europese Unie Brussel, 9 november 2017 (OR. en) Interinstitutioneel dossier: 2017/0274 (E) 13588/17 ACP 119 FIN 647 PTOM 20 WETGEVINGSBESLUITEN EN ANDERE INSTRUMENTEN Betreft: BESLUIT VAN DE
Raad van de Europese Unie Brussel, 9 november 2017 (OR. en) Interinstitutioneel dossier: 2017/0274 (E) 13588/17 ACP 119 FIN 647 PTOM 20 WETGEVINGSBESLUITEN EN ANDERE INSTRUMENTEN Betreft: BESLUIT VAN DE
Arbeidsmarkt allochtonen
 Streekpact 2013-2018 Cijferanalyse Publicatiedatum: 30 september 2013 Contactpersoon: Kim Nevelsteen Arbeidsmarkt allochtonen Samenvatting 1.176 werkzoekende allochtone Kempenaren (2012) vaak man meestal
Streekpact 2013-2018 Cijferanalyse Publicatiedatum: 30 september 2013 Contactpersoon: Kim Nevelsteen Arbeidsmarkt allochtonen Samenvatting 1.176 werkzoekende allochtone Kempenaren (2012) vaak man meestal
Direct Healthcare Professional Communication
 Direct Healthcare Professional Communication Belangrijke informatie over Arixtra (natriumfondaparinux) voorgevulde spuiten - een defect aan de naaldbeschermkap Geachte zorgverlener, In overleg met het
Direct Healthcare Professional Communication Belangrijke informatie over Arixtra (natriumfondaparinux) voorgevulde spuiten - een defect aan de naaldbeschermkap Geachte zorgverlener, In overleg met het
Voorstel voor een BESLUIT VAN DE RAAD. ter bepaling van de samenstelling van het Comité van de Regio's
 EUROPESE COMMISSIE Brussel, 11.6.2014 COM(2014) 226 final 2014/0128 (NLE) Voorstel voor een BESLUIT VAN DE RAAD ter bepaling van de samenstelling van het Comité van de Regio's NL NL TOELICHTING 1. ACHTERGROND
EUROPESE COMMISSIE Brussel, 11.6.2014 COM(2014) 226 final 2014/0128 (NLE) Voorstel voor een BESLUIT VAN DE RAAD ter bepaling van de samenstelling van het Comité van de Regio's NL NL TOELICHTING 1. ACHTERGROND
Waarom was het onderzoek nodig?
 INPULSIS -ON: De veiligheid op lange termijn van nintedanib bij patiënten met idiopathische pulmonale fibrose (IPF) Dit is een samenvatting van een klinisch onderzoek bij patiënten met IPF. Het is geschreven
INPULSIS -ON: De veiligheid op lange termijn van nintedanib bij patiënten met idiopathische pulmonale fibrose (IPF) Dit is een samenvatting van een klinisch onderzoek bij patiënten met IPF. Het is geschreven
Tarieven Europa: staffel 1
 Tarieven Europa: staffel 1 Wanneer u op basis van uw daadwerkelijkaantal zendingen boven de 49 zendingen per jaar uitkomt, dan kunt u ons contacteren voor verbeterde tarieven. Wij passen uw prijzen dan
Tarieven Europa: staffel 1 Wanneer u op basis van uw daadwerkelijkaantal zendingen boven de 49 zendingen per jaar uitkomt, dan kunt u ons contacteren voor verbeterde tarieven. Wij passen uw prijzen dan
BIJSLUITER: INFORMATIE VOOR GEBRUIKERS. Molaxole, poeder voor drank. Macrogol 3350 Natriumchloride Natriumwaterstofcarbonaat Kaliumchloride
 BIJSLUITER: INFORMATIE VOOR GEBRUIKERS Molaxole, poeder voor drank Macrogol 3350 Natriumchloride Natriumwaterstofcarbonaat Kaliumchloride Lees goed de hele bijsluiter, want deze bevat belangrijke informatie.
BIJSLUITER: INFORMATIE VOOR GEBRUIKERS Molaxole, poeder voor drank Macrogol 3350 Natriumchloride Natriumwaterstofcarbonaat Kaliumchloride Lees goed de hele bijsluiter, want deze bevat belangrijke informatie.
Bijlage B4. Eerste treden op de arbeidsmarkt. Freek Bucx
 Bijlage B4 Eerste treden op de arbeidsmarkt Freek Bucx Inhoud Tabel B4.1... 3 Tabel B4.2... 4 Tabel B4.3... 5 Tabel B4.4... 6 Tabel B4.5... 7 Tabel B4.6... 8 Bijlage B4 Eerste treden op de arbeidsmarkt
Bijlage B4 Eerste treden op de arbeidsmarkt Freek Bucx Inhoud Tabel B4.1... 3 Tabel B4.2... 4 Tabel B4.3... 5 Tabel B4.4... 6 Tabel B4.5... 7 Tabel B4.6... 8 Bijlage B4 Eerste treden op de arbeidsmarkt
Vragen en antwoorden over het burgerinitiatief
 Vragen en antwoorden over het burgerinitiatief EU-burgers kunnen de EU binnenkort vragen nieuwe wetgeving in te voeren indien zij daarvoor een miljoen handtekeningen kunnen verzamelen. Dit nieuwe instrument
Vragen en antwoorden over het burgerinitiatief EU-burgers kunnen de EU binnenkort vragen nieuwe wetgeving in te voeren indien zij daarvoor een miljoen handtekeningen kunnen verzamelen. Dit nieuwe instrument
Aanvrager (Fantasie)naam Sterkte Farmaceutische vorm. Vertimen 8 mg Tabletten. Vertimen 16 mg Tabletten. Vertisan 16 mg Таблетка
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM(EN), STERKTE(N) VAN HET (DE) GENEESMIDDEL(LEN), TOEDIENINGSWEG(EN), AANVRAGER(S), HOUDER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM(EN), STERKTE(N) VAN HET (DE) GENEESMIDDEL(LEN), TOEDIENINGSWEG(EN), AANVRAGER(S), HOUDER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN
Bijlage IV. Wetenschappelijke conclusies
 Bijlage IV Wetenschappelijke conclusies Wetenschappelijke conclusies Natriumglucose-cotransporter-2-remmers (SGLT2-remmers) worden gebruikt in combinatie met een dieet en lichaamsbeweging bij patiënten
Bijlage IV Wetenschappelijke conclusies Wetenschappelijke conclusies Natriumglucose-cotransporter-2-remmers (SGLT2-remmers) worden gebruikt in combinatie met een dieet en lichaamsbeweging bij patiënten
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Effezel 1 mg/g + 25 mg/g, gel Adapaleen/Benzoylperoxide
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Effezel 1 mg/g + 25 mg/g, gel Adapaleen/Benzoylperoxide Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Effezel 1 mg/g + 25 mg/g, gel Adapaleen/Benzoylperoxide Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
EUROPESE UNIE HET EUROPEES PARLEMENT PE-CONS 3659/1/01 REV 1
 EUROPESE UNIE HET EUROPEES PARLEMENT DE RAAD Brussel, 27 mei 2002 2001/0138 (COD) LEX 311 PE-CONS 3659/1/01 REV 1 TRANS 181 PECOS 199 CODEC 1126 VERORDENING (EG) Nr. /2002 VAN HET EUROPEES PARLEMENT EN
EUROPESE UNIE HET EUROPEES PARLEMENT DE RAAD Brussel, 27 mei 2002 2001/0138 (COD) LEX 311 PE-CONS 3659/1/01 REV 1 TRANS 181 PECOS 199 CODEC 1126 VERORDENING (EG) Nr. /2002 VAN HET EUROPEES PARLEMENT EN
BIJSLUITER: INFORMATIE VOOR DE PATIËNT. Aprokam 50 mg poeder voor oplossing voor injectie. Cefuroxim
 BIJSLUITER: INFORMATIE VOOR DE PATIËNT Aprokam 50 mg poeder voor oplossing voor injectie Cefuroxim Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
BIJSLUITER: INFORMATIE VOOR DE PATIËNT Aprokam 50 mg poeder voor oplossing voor injectie Cefuroxim Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
Bijlage I. Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen
 Bijlage I Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen 1 Wetenschappelijke conclusies Rekening houdend met het beoordelingsrapport
Bijlage I Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen 1 Wetenschappelijke conclusies Rekening houdend met het beoordelingsrapport
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER VIGAMOX 5 mg/ml oogdruppels, oplossing Moxifloxacine (als hydrochloride)
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER VIGAMOX 5 mg/ml oogdruppels, oplossing Moxifloxacine (als hydrochloride) Lees de hele bijsluiter zorgvuldig door voordat u start met het gebruik van dit geneesmiddel.
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER VIGAMOX 5 mg/ml oogdruppels, oplossing Moxifloxacine (als hydrochloride) Lees de hele bijsluiter zorgvuldig door voordat u start met het gebruik van dit geneesmiddel.
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Claritine, stroop 1 mg/ml. loratadine
 Bijsluiter Pagina 1/5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Claritine, stroop 1 mg/ml loratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
Bijsluiter Pagina 1/5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Claritine, stroop 1 mg/ml loratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
Wat zijn feiten en cijfers rond geneesmiddelenonderzoek?
 Deze kaart geeft een overzicht van beschikbare feiten en geneesmiddelenonderzoek. De kaart is tot stand gekomen op basis van literatuuronderzoek, interviews en denksessies met deskundigen. Met dank aan
Deze kaart geeft een overzicht van beschikbare feiten en geneesmiddelenonderzoek. De kaart is tot stand gekomen op basis van literatuuronderzoek, interviews en denksessies met deskundigen. Met dank aan
Antwoorden Aardrijkskunde Antwoorden Discovery par. 1
 Antwoorden Aardrijkskunde Antwoorden Discovery par. 1 Antwoorden door een scholier 1209 woorden 24 februari 2013 4,8 4 keer beoordeeld Vak Methode Aardrijkskunde Terra Discovery 1: Noord- Europa IJsland
Antwoorden Aardrijkskunde Antwoorden Discovery par. 1 Antwoorden door een scholier 1209 woorden 24 februari 2013 4,8 4 keer beoordeeld Vak Methode Aardrijkskunde Terra Discovery 1: Noord- Europa IJsland
~ :-.~? 'J~ ~ Vlaamse Regering. DE VLAAMSE MINISTER VAN WEL2;IJN, VOLKSGEZONDHEID EN GEZI1ir
 I 'J~ ~ ~ :-.~? Vlaamse Regering DE VLAAMSE MINISTER VAN WEL2;IJN, VOLKSGEZONDHEID EN GEZI1ir Omzendbrief betreffende de toepassing van de Vlaamse zorgverzekering voor Belgisch sociaal verzekerden met:
I 'J~ ~ ~ :-.~? Vlaamse Regering DE VLAAMSE MINISTER VAN WEL2;IJN, VOLKSGEZONDHEID EN GEZI1ir Omzendbrief betreffende de toepassing van de Vlaamse zorgverzekering voor Belgisch sociaal verzekerden met:
Europese feestdagen 2017
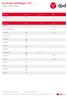 Januari - Februari - Maart Bestemming Januari Februari Maart Nederland (NL) 01-01 Bestemming Januari Februari Maart België (BE) 01-01 Bosnie en Herzegovina (BA) 01-03 Bulgarije (BG) 01-01 03-03 Denemarken
Januari - Februari - Maart Bestemming Januari Februari Maart Nederland (NL) 01-01 Bestemming Januari Februari Maart België (BE) 01-01 Bosnie en Herzegovina (BA) 01-03 Bulgarije (BG) 01-01 03-03 Denemarken
Europese feestdagen 2019
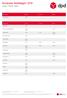 Januari - Februari - Maart Bestemming Januari Februari Maart Nederland (NL) 01-01 Bestemming Januari Februari Maart België (BE) 01-01 Bosnie en Herzegovina (BA) 01-01 02-01 01-03 Bulgarije (BG) 01-01 01-02
Januari - Februari - Maart Bestemming Januari Februari Maart Nederland (NL) 01-01 Bestemming Januari Februari Maart België (BE) 01-01 Bosnie en Herzegovina (BA) 01-01 02-01 01-03 Bulgarije (BG) 01-01 01-02
Europese feestdagen 2018
 Januari - Februari - Maart Bestemming Januari Februari Maart Nederland (NL) 01-01 Bestemming Januari Februari Maart België (BE) 01-01 Bosnie en Herzegovina (BA) 01-01 02-01 01-03 Bulgarije (BG) 01-01 03-03
Januari - Februari - Maart Bestemming Januari Februari Maart Nederland (NL) 01-01 Bestemming Januari Februari Maart België (BE) 01-01 Bosnie en Herzegovina (BA) 01-01 02-01 01-03 Bulgarije (BG) 01-01 03-03
Bijlage II. Wetenschappelijke conclusies
 Bijlage II Wetenschappelijke conclusies 8 Wetenschappelijke conclusies Solu-Medrol 40 mg poeder en oplosmiddel voor oplossing voor injectie (hierna Solu-Medrol ) bevat methylprednisolon en, als hulpstof,
Bijlage II Wetenschappelijke conclusies 8 Wetenschappelijke conclusies Solu-Medrol 40 mg poeder en oplosmiddel voor oplossing voor injectie (hierna Solu-Medrol ) bevat methylprednisolon en, als hulpstof,
Bijlage B4. Werken aan de start. Freek Bucx
 Bijlage B4 Werken aan de start Freek Bucx Inhoud Tabel B4.1... 3 Tabel B4.2... 5 Tabel B4.3... 6 Tabel B4.4... 7 Tabel B4.5... 8 Tabel B4.6... 9 Tabel B4.7... 10 Tabel B4.8... 11 Tabel B4.9... 12 Tabel
Bijlage B4 Werken aan de start Freek Bucx Inhoud Tabel B4.1... 3 Tabel B4.2... 5 Tabel B4.3... 6 Tabel B4.4... 7 Tabel B4.5... 8 Tabel B4.6... 9 Tabel B4.7... 10 Tabel B4.8... 11 Tabel B4.9... 12 Tabel
1. 31958 Q 1101: EAEC Raad: De Statuten van het Voorzieningsagentschap van Euratom (PB 27 van 6.12.1958, blz. 534), gewijzigd bij:
 9. ENERGIE 1. 31958 Q 1101: EAEC Raad: De Statuten van het Voorzieningsagentschap van Euratom (PB 27 van 6.12.1958, blz. 534), gewijzigd bij: 31973 D 0045: Besluit 73/45/Euratom van de Raad van 8 maart
9. ENERGIE 1. 31958 Q 1101: EAEC Raad: De Statuten van het Voorzieningsagentschap van Euratom (PB 27 van 6.12.1958, blz. 534), gewijzigd bij: 31973 D 0045: Besluit 73/45/Euratom van de Raad van 8 maart
Raad van de Europese Unie Brussel, 29 oktober 2014 (OR. en)
 Raad van de Europese Unie Brussel, 29 oktober 2014 (OR. en) Interinstitutioneel dossier: 2014/0298 (E) 14563/14 ACP 166 FIN 764 PTOM 51 WETGEVINGSBESLUITEN EN ANDERE INSTRUMENTEN Betreft: Besluit van de
Raad van de Europese Unie Brussel, 29 oktober 2014 (OR. en) Interinstitutioneel dossier: 2014/0298 (E) 14563/14 ACP 166 FIN 764 PTOM 51 WETGEVINGSBESLUITEN EN ANDERE INSTRUMENTEN Betreft: Besluit van de
11562/08 CS/lg DG H 1 A
 RAAD VA DE EUROPESE U IE Brussel, 22 juli 2008 (OR. en) 11562/08 Interinstitutioneel dossier: 2008/0074 (C S) VISA 239 COMIX 554 WETGEVI GSBESLUITE E A DERE I STRUME TE Betreft: VERORDENING VAN DE RAAD
RAAD VA DE EUROPESE U IE Brussel, 22 juli 2008 (OR. en) 11562/08 Interinstitutioneel dossier: 2008/0074 (C S) VISA 239 COMIX 554 WETGEVI GSBESLUITE E A DERE I STRUME TE Betreft: VERORDENING VAN DE RAAD
BIJLAGE II VERGUNNINGHOUDER VERANTWOORDELIJK VOOR IMPORT EN VRIJGIFTE, VOORWAARDEN OF BEPERKINGEN TEN AANZIEN VAN DE LEVERING EN HET GEBRUIK
 BIJLAGE II VERGUNNINGHOUDER VERANTWOORDELIJK VOOR IMPORT EN VRIJGIFTE, VOORWAARDEN OF BEPERKINGEN TEN AANZIEN VAN DE LEVERING EN HET GEBRUIK 1 A. HOUDER VAN DE VERGUNNING VOOR DE VERVAARDIGING Fabrikant
BIJLAGE II VERGUNNINGHOUDER VERANTWOORDELIJK VOOR IMPORT EN VRIJGIFTE, VOORWAARDEN OF BEPERKINGEN TEN AANZIEN VAN DE LEVERING EN HET GEBRUIK 1 A. HOUDER VAN DE VERGUNNING VOOR DE VERVAARDIGING Fabrikant
Bijlage II. Wetenschappelijke conclusies en redenen voor de weigering, opgesteld door het Europees Geneesmiddelenbureau
 Bijlage II Wetenschappelijke conclusies en redenen voor de weigering, opgesteld door het Europees Geneesmiddelenbureau 5 Wetenschappelijke conclusies Samenvatting van de wetenschappelijke beoordeling van
Bijlage II Wetenschappelijke conclusies en redenen voor de weigering, opgesteld door het Europees Geneesmiddelenbureau 5 Wetenschappelijke conclusies Samenvatting van de wetenschappelijke beoordeling van
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Fluomizin 10 mg tabletten voor vaginaal gebruik Dequaliniumchloride
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Fluomizin 10 mg tabletten voor vaginaal gebruik Dequaliniumchloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Fluomizin 10 mg tabletten voor vaginaal gebruik Dequaliniumchloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
Bijlage II. Wetenschappelijke conclusies
 Bijlage II Wetenschappelijke conclusies 198 Wetenschappelijke conclusies Naar aanleiding van de beoordeling van een in januari 2012 gestarte werkverdeling voor het PSUR (periodic safety update report,
Bijlage II Wetenschappelijke conclusies 198 Wetenschappelijke conclusies Naar aanleiding van de beoordeling van een in januari 2012 gestarte werkverdeling voor het PSUR (periodic safety update report,
VERSLAG VAN DE COMMISSIE AAN HET EUROPEES PARLEMENT, DE RAAD, HET EUROPEES ECONOMISCH EN SOCIAAL COMITÉ EN HET COMITÉ VAN DE REGIO'S
 EUROPESE COMMISSIE Brussel, 17.6.2011 COM(2011) 352 definitief VERSLAG VAN DE COMMISSIE AAN HET EUROPEES PARLEMENT, DE RAAD, HET EUROPEES ECONOMISCH EN SOCIAAL COMITÉ EN HET COMITÉ VAN DE REGIO'S Tweede
EUROPESE COMMISSIE Brussel, 17.6.2011 COM(2011) 352 definitief VERSLAG VAN DE COMMISSIE AAN HET EUROPEES PARLEMENT, DE RAAD, HET EUROPEES ECONOMISCH EN SOCIAAL COMITÉ EN HET COMITÉ VAN DE REGIO'S Tweede
BIJLAGE. Wetenschappelijke aspecten
 BIJLAGE Wetenschappelijke aspecten 3 BIJLAGE Wetenschappelijke aspecten A) INLEIDING Sparfloxacine is een antibioticum van de chinolonengroep dat is geïndiceerd voor de behandeling van: - in gemeenschapsverband
BIJLAGE Wetenschappelijke aspecten 3 BIJLAGE Wetenschappelijke aspecten A) INLEIDING Sparfloxacine is een antibioticum van de chinolonengroep dat is geïndiceerd voor de behandeling van: - in gemeenschapsverband
(1) Risico op acute pancreatitis Er zijn meldingen geweest van acute pancreatitis na de behandeling met carbimazol/thiamazol.
 GEADRESSEERDE ADRES POSTCODE WOONPLAATS 31 januari 2019 Belangrijke risico-informatie: Geneesmiddelen die carbimazol of thiamazol (synoniem: methimazol) bevatten: (1) risico op acute pancreatitis en (2)
GEADRESSEERDE ADRES POSTCODE WOONPLAATS 31 januari 2019 Belangrijke risico-informatie: Geneesmiddelen die carbimazol of thiamazol (synoniem: methimazol) bevatten: (1) risico op acute pancreatitis en (2)
Tabel 1: Economische indicatoren (1)
 Tabel 1: Economische indicatoren (1) Grootte van de Openheid van de Netto internationale Saldo op de lopende rekening (% economie (in economie (Export + BBP per hoofd, nominaal (EUR) BBP per hoofd, nominaal,
Tabel 1: Economische indicatoren (1) Grootte van de Openheid van de Netto internationale Saldo op de lopende rekening (% economie (in economie (Export + BBP per hoofd, nominaal (EUR) BBP per hoofd, nominaal,
Methylprednisolonwaterstofsuccinaat
 Bijlage I Lijst met namen, farmaceutische vormen, sterkten van de diergeneesmiddelen, diersoorten, toedieningswegen en aanvrager/houder van de vergunning voor het in de handel brengen in de lidstaten 1/7
Bijlage I Lijst met namen, farmaceutische vormen, sterkten van de diergeneesmiddelen, diersoorten, toedieningswegen en aanvrager/houder van de vergunning voor het in de handel brengen in de lidstaten 1/7
1. WAT IS ORGALUTRAN EN WAARVOOR WORDT HET GEBRUIKT?
 In deze bijsluiter komen de volgende onderdelen aan bod: 1. Wat is Orgalutran en waarvoor wordt het gebruikt? 2. Wat u moet weten voordat u Orgalutran gebruikt 3. Hoe wordt Orgalutran gebruikt? 4. Mogelijke
In deze bijsluiter komen de volgende onderdelen aan bod: 1. Wat is Orgalutran en waarvoor wordt het gebruikt? 2. Wat u moet weten voordat u Orgalutran gebruikt 3. Hoe wordt Orgalutran gebruikt? 4. Mogelijke
PGI 2. Europese Raad Brussel, 19 juni 2018 (OR. en) EUCO 7/1/18 REV 1
 Europese Raad Brussel, 19 juni 2018 (OR. en) Interinstitutionele dossiers: 2017/0900 (E) 2013/0900 (E) EUCO 7/1/18 REV 1 INST 92 POLGEN 23 CO EUR 8 RECHTSHANDELINGEN Betreft: BESLUIT VAN DE EUROPESE RAAD
Europese Raad Brussel, 19 juni 2018 (OR. en) Interinstitutionele dossiers: 2017/0900 (E) 2013/0900 (E) EUCO 7/1/18 REV 1 INST 92 POLGEN 23 CO EUR 8 RECHTSHANDELINGEN Betreft: BESLUIT VAN DE EUROPESE RAAD
BIJSLUITER: INFORMATIE VOOR GEBRUIKERS. Molaxole, poeder voor drank. Macrogol 3350 Natriumchloride Natriumwaterstofcarbonaat Kaliumchloride
 BIJSLUITER: INFORMATIE VOOR GEBRUIKERS Molaxole, poeder voor drank Macrogol 3350 Natriumchloride Natriumwaterstofcarbonaat Kaliumchloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
BIJSLUITER: INFORMATIE VOOR GEBRUIKERS Molaxole, poeder voor drank Macrogol 3350 Natriumchloride Natriumwaterstofcarbonaat Kaliumchloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
Publicatieblad van de Europese Unie L 331/13
 5.11.2004 Publicatieblad van de Europese Unie L 331/13 VERORDENING (EG) Nr. 1925/2004 VAN DE COMMISSIE van 29 oktober 2004 tot vaststelling van nadere uitvoeringsvoorschriften voor enkele bepalingen van
5.11.2004 Publicatieblad van de Europese Unie L 331/13 VERORDENING (EG) Nr. 1925/2004 VAN DE COMMISSIE van 29 oktober 2004 tot vaststelling van nadere uitvoeringsvoorschriften voor enkele bepalingen van
Bijsluiter: informatie voor de gebruiker. Cyklokapron, oplossing voor injectie 100 mg/ml. Tranexaminezuur
 Bijsluiter: informatie voor de gebruiker Cyklokapron, oplossing voor injectie 100 mg/ml. Tranexaminezuur Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke
Bijsluiter: informatie voor de gebruiker Cyklokapron, oplossing voor injectie 100 mg/ml. Tranexaminezuur Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke
VERSLAG VAN DE COMMISSIE
 EUROPESE COMMISSIE Brussel, 23.9.2016 COM(2016) 618 final VERSLAG VAN DE COMMISSIE Verslag met het oog op de berekening van de toegewezen hoeveelheid van de Unie, alsook het verslag met het oog op de berekening
EUROPESE COMMISSIE Brussel, 23.9.2016 COM(2016) 618 final VERSLAG VAN DE COMMISSIE Verslag met het oog op de berekening van de toegewezen hoeveelheid van de Unie, alsook het verslag met het oog op de berekening
