Handleiding voor gezondheidszorgbeoefenaars
|
|
|
- Helena Vos
- 8 jaren geleden
- Aantal bezoeken:
Transcriptie
1 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel LEMTRADA. Het verplichte plan voor risicobeperking in België, waarvan deze informatie deel uitmaakt, is een maatregel genomen om een veilig en doeltreffend gebruik van LEMTRADA te waarborgen (RMA gewijzigde versie 07/2015). Dit geneesmiddel is onderworpen aan aanvullende monitoring Handleiding voor gezondheidszorgbeoefenaars Dit materiaal bevat niet alle informatie. Voor de volledige informatie: Lees aandachtig de SPK (in bijlage) vooraleer Lemtrada voor te schrijven en/of te gebruiken. De volledige en geactualiseerde tekst van deze SPK is beschikbaar op de website rubriek bijsluiters
2 Doel van dit materiaal (RMA of risicobeperkende activiteiten): Deze informatie maakt deel uit van het Belgische risicobeheerplan dat informatiemateriaal ter beschikking stelt aan gezondheidszorgbeoefenaars (en patiënten). Deze bijkomende risicobeperkende activiteiten hebben als doel een veilig en doeltreffend gebruik van Lemtrada te waarborgen en moeten volgende belangrijke onderdelen bevatten: > Samenvatting van de productkenmerken > Een handleiding voor gezondheidszorgbeoefenaars > Een checklist voor de voorschrijvers > Een handleiding voor patiënten > Een patiëntenkaart De handleiding voor gezondheidszorgbeoefenaars moet de volgende belangrijke boodschappen bevatten: 1. Een beschrijving van de risico s die met het gebruik van LEMTRADA gepaard gaan, namelijk: > Immuun Trombocytopenische Purpura (ITP) > Nefropathieën, waaronder de antiglomerulaire-basaalmembraan (anti-gbm)-ziekte > Schildklieraandoeningen 2. Aanbevelingen over hoe deze risico s te verminderen aan de hand van aangepaste raadgevingen aan, opvolging en management van de patiënt 3. Een rubriek Veel gestelde vragen De checklist voor de voorschrijvers moet de volgende belangrijke boodschappen bevatten: 1. Lijst van testen die dienen uitgevoerd te worden bij de initiële screening van de patiënt 2. Vaccinatieschema welke ten laatste 6 weken voor aanvang van de behandeling volbracht moet zijn 3. Toedienen van premedicatie, nazicht van de algemene gezondheidstoestand, uitsluiten van zwangerschap en nazicht van anticonceptie juist voor aanvang van de behandeling 4. Biologische monitoring gedurende de behandeling en gedurende 4 jaar na de laatste behandeling 5. Een specifieke verwijzing dat de patiënt werd geïnformeerd over en het risico begrijpt op ernstige auto-immuunaandoeningen, infecties en kwaadaardige aandoeningen, en de maatregelen om deze risico s te minimaliseren 2
3 De handleiding voor patiënten moet de volgende sleutelboodschappen bevatten: 1. Een beschrijving van de risico s die met het gebruik van LEMTRADA gepaard gaan, namelijk: > Immuun Trombocytopenische Purpura (ITP) > Nefropathieën, waaronder de antiglomerulaire-basaalmembraan (anti-gbm)-ziekte > Schildklieraandoeningen > Ernstige Infecties 2. Een beschrijving van tekens en symptomen van risico s op auto-immuunaandoeningen 3. Een beschrijving van de beste manier om te reageren wanneer dergelijke tekens en symptomen zich voordoen (bijv. Waar kan u uw artsen bereiken ) 4. Aanbevelingen voor de planning van het opvolgingsschema De patiëntenkaart moet de volgende belangrijke boodschappen bevatten: 1. Een waarschuwingsboodschap voor de gezondheidszorgbeoefenaars die de patiënt om het even wanneer behandelen, inclusief in spoed -omstandigheden, waarin staat dat de patiënt met LEMTRADA werd behandeld 2. Dat een behandeling met LEMTRADA het risico kan verhogen op: > Immuun Trombocytopenische Purpura (ITP) > Nefropathieën, waaronder de antiglomerulaire-basaalmembraan (anti-gbm)-ziekte > Schildklieraandoeningen > Ernstige Infecties 3. Contactgegevens van de voorschrijver van LEMTRADA 3
4 Inhoudsopgave 1> Introductie LEMTRADA 05 2> Wat zijn de vertraagd optredende bijwerkingen bij het gebruik van LEMTRADA? 07 3> Samenvatting van de aanbevolen patiëntenopvolging 11 4> Management van patiënten behandeld met LEMTRADA 12 5> Aanvullende informatie 13 6> Veel gestelde vragen 14 4
5 1> Introductie LEMTRADA LEMTRADA is geïndiceerd voor gebruik bij volwassen patiënten met actieve relapsingremitting multiple sclerose (RRMS), vastgesteld door klinische testen of beeldvormende technieken. LEMTRADA is een monoklonaal antilichaam dat intraveneus wordt toegediend. Het bindt zich aan CD52, een antigen dat in hoge mate aanwezig is op het oppervlak van T-lymfocyten (CD3+), B-lymfocyten (CD19+) en in mindere mate op het oppervlak van NK-cellen (natural killercellen), monocyten en macrofagen. Het mechanisme waarmee LEMTRADA therapeutische invloeden uitoefent bij MS is nog niet geheel opgehelderd. Echter, onderzoeksresultaten wijzen op immunomodulerende effecten via depletie en repopulatie van lymfocyten, waaronder: > Veranderingen in aantal en eigenschappen van sommige sub-sets van lymfocyten na de behandeling. > Een relatieve toename van regulatoire T-cellen. > Een relatieve toename van geheugen T- en B-lymfocyten. > Voorbijgaande effecten op componenten van aangeboren immuniteit (d.w.z. neutrofielen, macrofagen, NK-cellen). Het therapeutisch effect kan mogelijks toegeschreven worden aan de vermindering van het aantal circulerende B- en T-cellen door behandeling met LEMTRADA en de daarop volgende hernieuwde aanmaak en samenstelling (repopulatie). Het gebruik van alemtuzumab is in verband gebracht met het risico op ernstige infectie en auto-immuun aandoeningen. Auto-immuun aandoeningen kunnen vele jaren na de behandeling optreden en kunnen ernstig of levensbedreigend zijn. LEMTRADA moet voorgeschreven en begeleid worden door een neuroloog met ervaring in de behandeling van patiënten met MS. Teneinde de potentiële risico s en bijwerkingen van LEMTRADA tot een minimum te beperken, moeten voorschrijvers en patiënten zich houden aan een 48-maanden follow-up na de laatste infusie van LEMTRADA. Het is belangrijk dat patiënten begrijpen dat ze moeten doorgaan met de controles, ook al voelen ze zich goed en is hun MS onder controle. Wanneer u een partnerschap aangaat met uw patiënt en uw medisch team en daarbij zorgvuldig overloopt hoe het educatief materiaal voor de patiënten te gebruiken, zal dit patiënten helpen om: > De periodieke onderzoeken te blijven ondergaan. > Symptomen en klachten vroegtijdig te herkennen en te melden. > Wanneer nodig snel de juiste behandeling te krijgen. 5
6 Zie voor meer bijzonderheden de rubriek in deze handleiding met de titel Management van patiënten behandeld met LEMTRADA. Om een beter begrip te krijgen van de duur van de effecten van de behandeling en de lengte van de vereiste follow-up, kan u de onderstaande schema s raadplegen, met als titel Overzicht van de de behandeling met LEMTRADA en Overzicht van de follow-up bij behandeling met LEMTRADA. Overzicht van de follow-up bij behandeling met LEMTRADA Start bloed- en urineonderzoek vóór de behandeling en ga hiermee door tot 4 jaar na de laatste infusie Behandelingskuur 1 Behandelingskuur 2 Behandeling van 5 dagen Behandeling van 3 dagen Jaar 1 Jaar 2 Jaar 3 Jaar 4 Jaar 5 OPMERKING Voor NOTE de For meeste most patiënten patients, 2 werken courses 2 kuren work for gedurende 2 years or 2 jaar longer. of langer. BEHANDELING CONTROLE Overzicht van de behandeling met LEMTRADA Pathologie Activiteit Tijdstip Immuun Trombocytopenische Purpura (ITP) Volledig bloedbeeld met plaatjestelling Vóór aanvang van de behandeling met LEMTRADA Maandelijks tot 48 maanden na de laatste infusie Nefropathieën, waaronder de antiglomerulairebasaalmembraan (anti- GBM)-ziekte Serumcreatinine Microscopische urineanalyse Vóór aanvang van de behandeling met LEMTRADA Maandelijks tot 48 maanden na de laatste infusie Schildklieraandoeningen Schildklierfunctieonderzoek (zoals TSH) Vóór aanvang van de behandeling met LEMTRADA Elke 3 maanden tot 48 maanden na de laatste infusie 6
7 2> Wat zijn de vertraagd optredende bijwerkingen bij het gebruik van LEMTRADA? Auto-immuunaandoeningen Het gebruik van alemtuzumab gaat gepaard met het risico op auto-immuunaandoeningen, zoals: > Immuun Trombocytopenische Purpura (ITP) > Schildklieraandoeningen > Nefropathieën, waaronder de antiglomerulaire-basaalmembraan (anti-gbm)-ziekte Deze bijwerkingen kunnen ernstig zijn, tot morbiditeit en/of mortaliteit leiden en vele jaren na de behandeling optreden. Vroegtijdige ontdekking kan de prognose bij patiënten die deze bijwerkingen krijgen, verbeteren. Het is belangrijk om de labwaarden nauwkeurig te controleren en alert te zijn voor klachten en symptomen. Lees de volgende rubrieken aandachtig door om een beter inzicht in deze risico s te krijgen. Immuun Trombocytopenische Purpura (ITP) Immuun trombocytopenische purpura is een auto-immuun aandoening die gewoonlijk gepaard gaat met antistoffen tegen bloedplaatjes. Depletie van bloedplaatjes vermindert het stollingsvermogen van het bloed. Symptomen van ITP kunnen onder andere zijn: gemakkelijk blauwe plekken krijgen, petechiën, spontane mucocutane bloeding (bijv. epistaxis, haemoptysis), zwaardere dan normaal of onregelmatige menstruatie. Deze klinische symptomen van ITP kunnen optreden voordat er zich een ernstige bloeding ontwikkelt. Het doel van de maatregelen voor risicovermindering die in dit document beschreven staan, is om potentiële gevallen van ITP zo vroeg mogelijk te ontdekken en te behandelen. ITP kan een ernstige aandoening zijn met morbiditeit en mortaliteit als gevolg en kan enkele jaren na de toediening optreden. In klinische onderzoeken werden de patiënten regelmatig gecontroleerd en geïnformeerd over de tekenen en symptomen van ITP om vroege opsporing van deze ziekte mogelijk te maken. Doordat ze deze aanbevelingen volgden, konden patiënten met ITP tijdig gediagnosticeerd en behandeld worden. In de meeste gevallen reageerden de patiënten op eerstelijns medische behandeling. Het is belangrijk dat alle patiënten op de volgende wijze gecontroleerd worden op ITP: > Er moet een volledig bloedbeeld met plaatjestelling verkregen worden vóór aanvang van de behandeling en daarna met maandelijkse intervallen tot 48 maanden na de laatste infusie. > Controleer de patiënt op klinische symptomen van ITP. 7
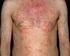
8 > Adviseer de patiënt over het belang van naleving van de maandelijkse controle en de noodzaak om tot 48 maanden na de laatste infusie hiermee door te gaan. > Leer de patiënt symptomen van ITP te herkennen en benadruk dat hij/zij er alert voor moet blijven. > Als ITP vermoed wordt, moet de juiste medische hulp snel op gang komen, waaronder onmiddellijke doorverwijzing naar een specialist. Ernstige of wijdverspreide bloeding is levensbedreigend en vereist onmiddellijke zorg. Zie de rubriek Patiënten die behandeld worden met LEMTRADA voor belangrijke informatie over de veiligheid van het product. Het potentiële risico verbonden aan de behandeling met LEMTRADA na het optreden van ITP is onbekend. Voorbeelden van blauwe plekken en petechiën ten gevolge van ITP Opmerking : Deze foto s zijn enkel een richtlijn om voorbeelden van blauwe plekken en petechiën ten gevolge van ITP te laten zien. De patiënt kan minder erge blauwe plekken of petechiën hebben dan op deze foto s, en toch ITP hebben. Dit is een voorbeeld van een been met petechiën. Petechiën zijn kleine, rode, roze of paarse, onder de huid verspreide vlekjes. Ze lijken op speldenprikken. Petechiën kunnen overal op het lichaam van de patiënt optreden, niet alleen op de benen. Dit is een voorbeeld van snel of te veel blauwe plekken krijgen. Deze blauwe plekken komen niet alleen op de armen voor, maar kunnen overal op het lichaam voorkomen. Dit is een voorbeeld van purpura onder de tong. Dit kan overal in de mond optreden - onder de tong op het gehemelte, aan de binnenzijde van de wang, op de tong of op het tandvlees. 8
9 Nefropathieën, waaronder de anti-gbm- ziekte Nefropathie, met name antiglomerulaire-basaalmembraan (anti-gbm)-ziekte, is in klinisch onderzoek zelden gemeld na behandeling met LEMTRADA bij patiënten met multipele sclerose en is over het algemeen binnen 39 maanden na de laatste toediening van LEMTRADA opgetreden. De klinische verschijnselen van een nefropathie, met name antiglomerulaire basaalmembraan (anti-gbm)-ziekte kunnen onder meer verhoging van het serumcreatinine, hematurie en/of proteïnurie omvatten. Hoewel geen alveolaire bloeding werd waargenomen in klinische onderzoeken, kan een alveolaire bloeding zich manifesteren als haemoptysis gerelateerd aan de antiglomerulaire-basaalmembraan (anti-gbm)-ziekte. Omdat het mogelijk is dat patiënten geen symptomen ondervinden, is het belangrijk dat er periodieke laboratoriumonderzoeken worden uitgevoerd. > De serumcreatininegehalten moeten bepaald worden vóór aanvang van de behandeling en daarna met maandelijkse intervallen tot 48 maanden na de laatste infusie. > Een microscopische urineanalyse moet uitgevoerd worden vóór aanvang van de behandeling en daarna met maandelijkse intervallen tot 48 maanden na de laatste infusie. Na deze periode zullen deze analyses worden uitgevoerd indien er klinische aanwijzingen zijn voor nefropathie, met name de antiglomerulaire-basaalmembraan (anti-gbm)-ziekte. > Bij klinisch significante wijzigingen ten opzichte van de uitgangswaarde van serumcreatinine, onverklaarde hematurie en/of proteïnurie, moet meer diepgaand onderzoek uitgevoerd worden om een nefropathie op te sporen, en moet onmiddellijk een specialist geraadpleegd worden. > Vroegtijdige opsporing en behandeling van nefropathieën, met name antiglomerulairebasaal membraan (anti-gbm)-ziekte, kunnen de prognose van een nefropathie verbeteren. > Gelieve bij vrouwen het urineonderzoek buiten de menstruatieperiode plannen om een vals positief resultaat te voorkomen. > Directe verwijzing naar een specialist voor verdere beoordeling van patiënten in geval van verdenking van een nefropathie, met name antiglomerulaire-basaalmembraan (anti-gbm)-ziekte, is ten zeerste aanbevolen. De anti-gbm-ziekte is levensbedreigend als deze niet behandeld wordt, en daarom moet onmiddellijke zorg verleend worden aan de patiënt. Als patiënten niet meteen behandeld worden, kunnen ze snel nierfalen ontwikkelen waarvoor dialyse en/of een transplantatie nodig is. Ook kan dit leiden tot een dodelijke afloop. 9
10 Schildklierafwijkingen Bij klinisch onderzoek zijn er auto-immuunschildklieraandoeningen gemeld, waaronder hyperthyroïdie en hypothyroïdie. Schildklieraandoeningen kwamen in klinisch onderzoek vaak voor; de meeste waren licht tot matig ernstig en traden op tot en met 48 maanden na de eerste blootstelling aan LEMTRADA. De meeste schildklieraandoeningen werden behandeld met conventionele medische therapie; enkele patiënten moesten geopereerd worden. > De schildklierfunctie moet onderzocht worden, aan de hand van bijvoorbeeld het gehalte van het schildklierstimulerend hormoon (TSH), en vóór aanvang van de behandeling en daarna elke 3 maanden gedurende 48 maanden na de laatste infusie. Na deze periode dient de schildklierfunctie onderzocht te worden indien er klinische aanwijzingen zijn voor het niet goed functioneren van de schildklier. > Verder moet u alert zijn voor klachten en symptomen van schildklieraandoeningen. > Een schildklieraandoening brengt speciale risico s met zich mee bij vrouwen die zwanger worden. Een onbehandelde schildklierfunctiestoornis kan schade toebrengen aan het ongeboren en pasgeboren kind. Extra voorzichtigheid is geboden bij zwangere vrouwen met de ziekte van Basedow (ook wel ziekte van Graves genoemd), omdat antistoffen tegen de schildklierstimulerende hormoonreceptor van de moeder overdragen kunnen worden aan een foetus in ontwikkeling en voorbijgaande neonatale ziekte van Basedow kunnen veroorzaken. De behandelende specialist verantwoordelijk voor de begeleiding van de zwangerschap moet op de hoogte zijn van het verhoogde risico op schildklierafwijkingen ten gevolge van de behandeling met LEMTRADA en van de noodzaak deze adequaat te behandelen. 10
11 3> Samenvatting van de aanbevolen patiëntenopvolging Zie de onderstaande tabel voor een overzicht van de aanbevolen opvolgtijdstippen. Ook ontvangt u een pakket met voorgedrukte checklists voor elk van uw patiënten aan wie u LEMTRADA voorschrijft. Zorg vooral dat u vóór aanvang van de behandeling met LEMTRADA het gedeelte Contra-indicaties van de bijgevoegde SPK leest. Pathologie Activiteit Tijdstip Immuun Trombocytopenische Purpura (ITP) Volledig bloedbeeld met plaatjestelling Vóór aanvang van de behandeling met LEMTRADA Maandelijks tot 48 maanden na de laatste infusie Nefropathieën, waaronder de antiglomerulairebasaalmembraan (anti-gbm)-ziekte Serumcreatinine Microscopische urineanalyse Vóór aanvang van de behandeling met LEMTRADA Maandelijks tot 48 maanden na de laatste infusie Schildklieraandoeningen Schildklierfunctieonderzoek (zoals TSH) Vóór aanvang van de behandeling met LEMTRADA Elke 3 maanden tot 48 maanden na de laatste infusie 11
12 4> Management van patiënten behandeld met LEMTRADA > Het is uiterst belangrijk dat uw patiënt begrijpt dat hij/zij verplicht is om periodieke onderzoeken te laten uitvoeren (gedurende 48 maanden na de laatste infusie), ook al heeft hij/zij geen symptomen en is zijn/haar MS goed onder controle. > U dient samen met uw patiënt zijn/haar periodieke opvolging te plannen en te beheren. > Patiënten die deze periodieke opvolging niet naleven hebben mogelijk nog meer advies nodig, waarbij u de risico s van het niet uitvoeren van de geplande onderzoeken benadrukt. > U dient hun onderzoeksresultaten te controleren en alert te blijven voor de symptomen van bijwerkingen. > Neem de handleiding voor patiënten en de bijsluiter van LEMTRADA samen met uw patiënt door. Vóór aanvang van de behandeling moeten patiënten geïnformeerd worden over de voordelen en de risico s. Herinner de patiënt eraan om alert te blijven voor symptomen van auto-immuun aandoeningen en om medische hulp te zoeken in geval van twijfel. > Moedig de patiënt aan om de patiëntenkaart altijd bij zich te hebben. Deze kaart moeten ze altijd tonen aan alle gezondheidszorgbeoefenaars die hen behandelen voor welke reden dan ook, of in geval van een medische noodsituatie. > Specialisten en de benodigde middelen moeten beschikbaar zijn om een tijdige diagnose en behandeling van de meest voorkomende bijwerkingen, in het bijzonder autoimmuunaandoeningen en infecties, mogelijk te maken. 12
13 5> Aanvullende informatie Vaccinaties > Het is aan te raden dat patiënten alle - volgens de nationale richtlijnen - vereiste vaccinaties gekregen hebben waarbij de laatste vaccinatie minstens 6 weken voor aanvang van de behandeling met LEMTRADA heeft plaatsgevonden. > Aangezien de veiligheid van immunisering met levend afgezwakte vaccins na behandeling met LEMTRADA niet bestudeerd is, mogen deze niet worden toegediend aan patiënten die onlangs een behandelingskuur met LEMTRADA hebben ontvangen. > Vóór behandeling met LEMTRADA dient u de VZV (Varicella Zoster Virus)-vaccinatie van patiënten die negatief zijn voor antistoffen te overwegen. Vruchtbaarheid, anticonceptie, zwangerschap en borstvoeding > Vrouwen die zwanger kunnen worden, moeten voor effectieve anticonceptie zorgen tijdens de behandeling met LEMTRADA en gedurende 4 maanden na de behandeling met LEMTRADA. > Er bestaan geen adequate en goed gecontroleerde onderzoeken van LEMTRADA bij zwangere vrouwen. LEMTRADA mag bij zwangerschap alleen toegediend worden als het potentiële voordeel het potentiële risico voor de foetus rechtvaardigt. > Schildklieraandoeningen vormen een bijzonder risico voor zwangere vrouwen (zie rubriek 2, Schildklieraandoeningen). Bij moeders met de ziekte van Basedow (ook wel ziekte van Graves genoemd), kunnen er antistoffen tegen de schildklierstimulerende hormoonreceptor van de moeder overgedragen worden aan een foetus in ontwikkeling, en deze kunnen voorbijgaande neonatale ziekte van Basedow veroorzaken. > Het is niet bekend of alemtuzumab in de moedermelk wordt uitgescheiden. Risico voor pasgeborenen/zuigelingen kan niet worden uitgesloten. Borstvoeding moet daarom worden gestaakt tijdens behandeling met LEMTRADA en gedurende 4 maanden na de laatste infusie van elke behandelingskuur. Desalniettemin kunnen de voordelen van overgedragen immuniteit via moedermelk bij de pasgeborenen/zuigelingen opwegen tegen de risico s van mogelijke blootstelling aan LEMTRADA. > Er bestaan geen adequate klinische veiligheidsgegevens over het effect van LEMTRADA op de vruchtbaarheid. In een substudie bij 13 mannelijke patiënten die werden behandeld met alemtuzumab (behandeld met 12 mg of 24 mg) is geen aanwijzing gevonden voor aspermie, azoöspermie, significant verlaagde spermatelling, mobiliteitsstoornissen of een toename van het aantal morfologische afwijkingen van de spermatozoïden. Het is gekend dat Glycoproteïne CD52 voorkomt in de reproductieve weefsels van mensen en knaagdieren. Alhoewel gegevens uit dieronderzoek wijzen op effecten op de vruchtbaarheid van gehumaniseerde muizen (zie rubriek 5.3 van de SPK), is er, op basis van de beschikbare gegevens, niets bekend over een potentiële impact op de vruchtbaarheid van mensen gedurende de periode van blootstelling. 13
14 6> Veel gestelde vragen (FAQ s) Overweeg het volgende voordat u LEMTRADA voorschrijft: Welke laboratoriumonderzoeken moeten er plaatsvinden voor aanvang van de behandeling met LEMTRADA? De onderzoeken die moeten plaatsvinden, zijn: > Volledig bloedbeeld met plaatjestelling > Creatininewaarde > Microscopisch urineonderzoek > Schildklieronderzoek met het testen van de TSH-waarde Meer informatie vindt u in rubriek 3, Samenvatting van de aanbevolen patiëntenopvolging. Kan ik LEMTRADA voorschrijven aan patiënten die andere behandelingen voor MS ontvangen? LEMTRADA werd niet tegelijk, of na een behandeling, met antineoplastische of immunosuppressieve middelen toegediend voor de behandeling van MS. Net als met andere immunomodulerende therapieën moet er rekening gehouden worden met eventuele gecombineerde invloeden op het immuunsysteem van de patiënt wanneer de toediening van LEMTRADA overwogen wordt. Gelijktijdig gebruik van LEMTRADA met welke van deze therapieën ook, kan het risico op immuunsuppressie vergroten. Moet ik tijdens en na de behandeling met LEMTRADA doorgaan met de laboratoriumonderzoeken? Hoelang? Ja. De onderzoeken moeten doorgaan gedurende 48 maanden na de laatste infusie. Verdere gegevens over welke onderzoeken er moeten plaatsvinden, wanneer en hoelang, kunt u vinden in rubriek 3, Samenvatting van de aanbevolen patiëntenopvolging. Wat gebeurt er als mijn patiënt een infectie heeft wanneer ik met een behandelingskuur met LEMTRADA wil beginnen? U moet overwegen om de aanvang van de toediening van LEMTRADA aan patiënten met actieve infectie uit te stellen tot de infectie volledig onder controle is. 14
15 Behandeling Hoe wordt LEMTRADA toegediend en hoelang duurt de infusie? LEMTRADA wordt in twee jaarlijkse kuren via intraveneuze infusie toegediend. De eerste kuur bestaat uit een dagelijkse infusie over een periode van 5 opeenvolgende dagen. De tweede kuur wordt 12 maanden later toegediend en bestaat uit een dagelijkse infusie over een periode van 3 opeenvolgende dagen. Indien een infusie gerelateerde reactie optreedt, dient u, indien nodig, de gepaste symptomatische behandeling te geven. Als de infusie niet goed getolereerd wordt, kan de snelheid van de infusie worden verlaagd. Als er ernstige infusiereacties optreden, moet onmiddellijke stopzetting van de intraveneuze infusie overwogen worden. Tijdens klinische onderzoeken waren anafylactische of ernstige reacties die stopzetting van de behandeling vereisten, zeer zeldzaam. Artsen moeten zich bewust zijn van de cardiale voorgeschiedenis van de patiënt omdat infuus gerelateerde reacties, cardiale symptomen zoals tachycardie kunnen omvatten. Er moeten middelen beschikbaar zijn voor adequate behandeling van milde of ernstige overgevoeligheidsreacties. Bestaan er profylactische middelen die genomen kunnen worden? Patiënten moeten voorafgaand aan de behandeling met LEMTRADA corticosteroïden toegediend krijgen (1000 mg methylprednisolon of een equivalent daarvan) gedurende de eerste 3 dagen van elke behandelingskuur. Verder kan ook behandeling vooraf met antihistaminica en/of antipyretica vóór de toediening van LEMTRADA overwogen worden. Orale profylaxe tegen herpesinfectie moet worden gegeven vanaf de eerste dag van elke behandelingskuur en moet ten minste gedurende één maand na behandeling met LEMTRADA worden voortgezet. In klinische onderzoeken kregen patiënten tweemaal per dag 200 mg aciclovir of equivalent toegediend. Monitoring van bijwerkingen Wat zijn de klachten en symptomen van ITP? Symptomen van ITP kunnen onder andere (maar zijn niet beperkt tot) de volgende zijn: gemakkelijk blauwe plekken krijgen, petechiën, spontane mucocutane bloeding (bijv. epistaxis, haemoptysis), zware of onregelmatige menstruatie. Deze klinische symptomen van ITP kunnen optreden voordat er zich een ernstige bloeding ontwikkelt. Lage aantallen bloedplaatjes of klinisch significante veranderingen ten opzichte van de uitgangswaarden bij aanvang van de behandeling, zoals bepaald door het bloedbeeld met bloedplaatjes geven eveneens ITP aan. 15
16 Voorbeelden van blauwe plekken en petechiën ten gevolge van ITP Opmerking : Deze foto s zijn enkel een richtlijn om voorbeelden van blauwe plekken en petechiën ten gevolge van ITP te laten zien. De patiënt kan minder erge blauwe plekken of petechiën hebben dan op deze foto s, en toch ITP hebben. Dit is een voorbeeld van een been met petechiën. Petechiën zijn kleine, rode, roze of paarse, onder de huid verspreide vlekjes. Ze lijken op speldenprikken. Petechiën kunnen overal op het lichaam van de patiënt optreden, niet alleen op de benen. Dit is een voorbeeld van snel of te veel blauwe plekken krijgen. Deze blauwe plekken komen niet alleen op de armen voor, maar kunnen overal op het lichaam voorkomen. Dit is een voorbeeld van purpura onder de tong. Dit kan overal in de mond optreden - onder de tong op het gehemelte, aan de binnenzijde van de wang, op de tong of op het tandvlees. Hoe moet ik een patiënt behandelen bij wie er vermoedens zijn van ITP? Het is belangrijk alle patiënten op tekenen van ITP op te volgen teneinde dit tijdig te kunnen diagnosticeren en te behandelen. Daarom moet een volledig bloedbeeld met plaatjestelling worden verkregen vóór aanvang van de behandeling en daarna met maandelijkse intervallen tot 48 maanden na de laatste infusie. Bij een vermoeden van ITP moet onmiddellijk een volledig bloedbeeld met plaatjestelling worden uitgevoerd. Als het optreden van ITP wordt bevestigd, moet onmiddellijk een passende medische behandeling worden ingesteld, met inbegrip van de onmiddellijke raadpleging van een specialist. Een ernstige of uitgebreide bloeding is levensbedreigend en vereist onmiddellijke zorg. 16
17 Welke symptomen kunnen mogelijk duiden op nefropathie, met name de antiglomerulairebasaalmembraan (anti-gbm)-ziekte? Manifestaties van nefropathie kunnen verhoging van het serumcreatinine, hematurie en/of proteïnurie zijn. Hoewel geen alveolaire bloeding is waargenomen in klinische onderzoeken, kan een alveolaire bloeding zich manifesteren als haemoptysis gerelateerd aan antiglomerulaire-basaalmembraan (anti-gbm)-ziekte. Omdat het mogelijk is dat sommige patiënten geen symptomen ondervinden, is het belangrijk dat de periodieke labonderzoeken (serumcreatinine, en microscopisch urineonderzoek) worden uitgevoerd. Hoe moet ik een patiënt behandelen bij wie een nefropathie, met name de antiglomerulaire-basaalmembraan (anti-gbm)-ziekte, wordt vermoed? Het observeren van klinisch significante afwijkingen van de uitgangswaarde van serum creatinine, onverklaarbare hematurie, en/of proteïnurie, moet aanleiding geven tot verder nefrologisch onderzoek met onmiddellijke verwijzing naar een specialist. Vroegtijdige opsporing en behandeling van nefropathieën, met name de antiglomerulairebasaalmembraan (anti-gbm)-ziekte, kunnen de prognose van nefropathie verbeteren. Gelden er speciale overwegingen bij de behandeling van patiënten die een infectie ontwikkeld hebben? Er gelden geen speciale overwegingen. Het advies is om infecties met standaard therapieën te behandelen. Advies bij zwangerschap en anticonceptie Moeten vrouwelijke patiënten anticonceptie gebruiken? Als ze zwanger willen worden, hoelang moeten ze dan wachten na een behandelingskuur met LEMTRADA? De alfa-halfwaardetijd bedroeg ongeveer 4-5 dagen en was vergelijkbaar tussen kuren, resulterend in lage of niet te detecteren serumconcentraties binnen ongeveer 30 dagen na elke behandelingskuur. Daarom moeten vrouwen die zwanger kunnen worden voor effectieve anticonceptie zorgen tijdens de behandeling met LEMTRADA en gedurende 4 maanden na elke behandelingskuur met LEMTRADA. 17
18 Zal LEMTRADA de toekomstige vruchtbaarheid van mannen of vrouwen aantasten? Er bestaan geen adequate klinische veiligheidsgegevens over het effect van LEMTRADA op de vruchtbaarheid. In een substudie bij 13 mannelijke patiënten die werden behandeld met alemtuzumab (behandeld met 12 mg of 24 mg) werd geen aanwijzing gevonden voor aspermie, azoöspermie, verlengde verlaagde spermatelling, mobiliteitsstoornissen of een toename van het aantal morfologische afwijkingen van de spermatozoïden. Het is gekend dat glycoproteïne CD52 voorkomt in de reproductieve weefsels van mensen en knaagdieren. Alhoewel gegevens uit dieronderzoek wijzen op effecten op de vruchtbaarheid van gehumaniseerde muizen, op basis van de beschikbare gegevens is niets bekend over een potentiële impact op de vruchtbaarheid van mensen gedurende de periode van blootstelling. Mag een patiënt die borstvoeding geeft een behandelingskuur met LEMTRADA ontvangen? Het is niet bekend of alemtuzumab in de moedermelk wordt uitgescheiden. Risico voor pasgeborenen/zuigelingen kan niet worden uitgesloten. Borstvoeding moet daarom worden gestaakt tijdens behandeling met LEMTRADA en gedurende 4 maanden na de laatste infusie van elke behandelingskuur. Desalniettemin kunnen de voordelen van overgedragen immuniteit via moedermelk bij de pasgeborenen/zuigelingen opwegen tegen de risico s van mogelijke blootstelling aan LEMTRADA. In welke mate diet er rekening gehouden te worden met vaccinaties bij overweging van behandeling met LEMTRADA? Aangezien de veiligheid van immunisering met levend vaccin na behandeling met LEMTRADA niet bestudeerd is, mogen deze niet worden toegediend aan patiënten die onlangs met LEMTRADA behandeld werden. Het is aan te raden dat patiënten alle - volgens de nationale richtlijnen - vereiste vaccinaties gekregen hebben waarbij de laatste minstens 6 weken voor aanvang van de behandeling met LEMTRADA heeft plaatsgevonden. Vóór behandeling met LEMTRADA dient u een VZV (Varicella Zoster Virus)-vaccinatie van patiënten die negatief zijn voor antistoffen te overwegen. 18
19 Melden van bijwerkingen De gezondheidszorgbeoefenaars worden verzocht bijwerkingen van Lemtrada te melden aan het Belgisch Centrum voor Geneesmiddelenbewaking voor geneesmiddelen voor humaan gebruik (BCGH) van het FAGG. Het melden kan online gebeuren via www. gelefiche.be of via de papieren gele fiche beschikbaar via het Gecommentarieerd Geneesmiddelenrepertorium en drie maal per jaar via de Folia Pharmacotherapeutica. De gele fiche kanworden opgestuurd naar het adres FAGG - BCGB - Eurostation II Victor Hortaplein 40/ Brussel, per fax op het nummer 02/ of per naar: adversedrugreactions@afmps.be Bijwerkingen kunnen ook gemeld worden aan de afdeling Geneesmiddelenbewaking van Sanofi Belgium - Tel (24/24 uur) -pharmacovigilance.belgium@sanofi.com. Als u meerdere exemplaren wenst van een of meer van de RMA-documenten, neem dan contact op met de Medische Informatiedienst van Sanofi België op het algemene telefoonnummer
20
Handleiding voor zorgprofessionals. Gebruik van LEMTRADA (alemtuzumab) bij patiënten met actieve relapsing remitting multiple sclerose (RRMS)
 Handleiding voor zorgprofessionals Gebruik van LEMTRADA (alemtuzumab) bij patiënten met actieve relapsing remitting multiple sclerose (RRMS) Inhoudsopgave 1> LEMTRADA 03 2> Mogelijke risico s bij het gebruik
Handleiding voor zorgprofessionals Gebruik van LEMTRADA (alemtuzumab) bij patiënten met actieve relapsing remitting multiple sclerose (RRMS) Inhoudsopgave 1> LEMTRADA 03 2> Mogelijke risico s bij het gebruik
Handleiding voor gezondheidszorgbeoefenaars
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel LEMTRADA. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel LEMTRADA. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
Handleiding voor patiënten. Belangrijke informatie voor patiënten die beginnen aan een behandeling met LEMTRADA
 Handleiding voor patiënten Belangrijke informatie voor patiënten die beginnen aan een behandeling met LEMTRADA Inhoudsopgave 1> Wat is LEMTRADA en hoe werkt het? 03 2> Bijwerkingen 04 3> Planning van uw
Handleiding voor patiënten Belangrijke informatie voor patiënten die beginnen aan een behandeling met LEMTRADA Inhoudsopgave 1> Wat is LEMTRADA en hoe werkt het? 03 2> Bijwerkingen 04 3> Planning van uw
Handleiding voor patiënten
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel LEMTRADA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel LEMTRADA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Handleiding voor zorgprofessionals. Gebruik van LEMTRADA (alemtuzumab) bij patiënten met actieve relapsing remitting multiple sclerose (RRMS)
 Handleiding voor zorgprofessionals Gebruik van LEMTRADA (alemtuzumab) bij patiënten met actieve relapsing remitting multiple sclerose (RRMS) Inhoudsopgave 1> LEMTRADA 03 2> Mogelijke risico s bij het gebruik
Handleiding voor zorgprofessionals Gebruik van LEMTRADA (alemtuzumab) bij patiënten met actieve relapsing remitting multiple sclerose (RRMS) Inhoudsopgave 1> LEMTRADA 03 2> Mogelijke risico s bij het gebruik
Gelieve de patiëntenwaarschuwingskaart van Entyvio in te vullen en te overhandigen aan elke patiënt.
 Deze informatie maakt deel uit van het Belgische en Luxemburgse risicobeheerplan, dat informatiemateriaal beschikbaar stelt aan gezondheidszorgbeoefenaars (en patiënten). Deze bijkomende risicobeperkende
Deze informatie maakt deel uit van het Belgische en Luxemburgse risicobeheerplan, dat informatiemateriaal beschikbaar stelt aan gezondheidszorgbeoefenaars (en patiënten). Deze bijkomende risicobeperkende
VALDOXAN. (agomelatine) Informatie voor beroepsbeoefenaren in de gezondheidszorg: Aanbevelingen met betrekking tot:
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Valdoxan 25 mg. Het verplicht plan voor risicobeperking in België, waarvan deze
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Valdoxan 25 mg. Het verplicht plan voor risicobeperking in België, waarvan deze
Handleiding voor de patiënt
 Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel Lemtrada, om voor een goed gebruik ervan te zorgen en om de ongewenste effecten ervan te beperken, zijn er bepaalde
Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel Lemtrada, om voor een goed gebruik ervan te zorgen en om de ongewenste effecten ervan te beperken, zijn er bepaalde
Servier Benelux S.A. PROTELOS. (strontiumranelaat) GIDS EN CHECKLIST VOOR DE ARTS
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Protelos 2 g. Het verplicht plan voor risicobeperking in België, waarvan deze
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Protelos 2 g. Het verplicht plan voor risicobeperking in België, waarvan deze
VISTABEL (botulinum toxine type A) Educatieve brochure voor artsen. 50 Allerganeenheden Poeder voor oplossing voor injectie
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VISTABEL. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VISTABEL. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
GIDS VOOR DE VOORSCHRIJVER
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel Cerdelga. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel Cerdelga. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Educatief materiaal. EFIENT (Prasugrel) Dit geneesmiddel is onderworpen aan aanvullende monitoring.
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel EFIENT. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel EFIENT. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Dit geneesmiddel is onderworpen aan aanvullende monitoring.
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Erivedge. Het verplicht plan voor risicobeperking in België, waar deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Erivedge. Het verplicht plan voor risicobeperking in België, waar deze informatie
BOTOX (botulinum toxine type A) Educatieve brochure voor artsen. 100 Allerganeenheden Poeder voor oplossing voor injectie
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel BOTOX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel BOTOX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
VICTRELIS Boceprevir
 De gezondheidsautoriteiten van de EU hebben een aantal voorwaarden gekoppeld aan het in de handel brengen van het geneesmiddel VICTRELIS. Het verplichte plan voor risicobeperking in België, waarvan deze
De gezondheidsautoriteiten van de EU hebben een aantal voorwaarden gekoppeld aan het in de handel brengen van het geneesmiddel VICTRELIS. Het verplichte plan voor risicobeperking in België, waarvan deze
RISICO MINIMALISATIE MATERIAAL BETREFFENDE FLIXABI (INFLIXIMAB) VOOR VOORSCHRIJVERS
 Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke
Vectibix (panitumumab) Educatief materiaal voor de arts
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Vectibix. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Vectibix. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
MAVENCLAD (Cladribine)
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel MAVENCLAD. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel MAVENCLAD. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Mysimba 8 mg/90 mg tabletten met verlengde afgifte. (naltrexonhydrochloride en bupropionhydrochloride)
 1 De Europese gezondheidsautoriteiten hebben bepaaide voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Mysimba 8 mg/90 mg tabletten met verlengde afgifte. Het verplichte plan voor
1 De Europese gezondheidsautoriteiten hebben bepaaide voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Mysimba 8 mg/90 mg tabletten met verlengde afgifte. Het verplichte plan voor
YERVOY. (ipilimumab) Concentraat voor oplossing voor infusie Dit geneesmiddel is onderworpen aan aanvullende monitoring.
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
VALDOXAN (agomelatine) Informatie voor beroepsbeoefenaren in de gezondheidszorg. Aanbevelingen met betrekking tot:
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Valdoxan 25 mg. Het verplicht plan voor risicobeperking in België, waarvan deze
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Valdoxan 25 mg. Het verplicht plan voor risicobeperking in België, waarvan deze
CAPRELSA (vandetanib)
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CAPRELSA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CAPRELSA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Risico minimalisatie materialen betreffende Inflectra (infliximab) voor de voorschrijvers
 Inflectra (infliximab) Dit geneesmiddel is onderworpen aan aanvullende monitoring Risico minimalisatie materialen betreffende Inflectra (infliximab) voor de voorschrijvers De risico minimalisatie materialen
Inflectra (infliximab) Dit geneesmiddel is onderworpen aan aanvullende monitoring Risico minimalisatie materialen betreffende Inflectra (infliximab) voor de voorschrijvers De risico minimalisatie materialen
Rechtstreekse mededeling aan de Gezondheidszorgbeoefenaars
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
MYCOFENOLAATHOUDENDE GENEESMIDDELEN Informatiegids voor de gezondheidszorgbeoefenaars TERATOGEEN RISICO
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van geneesmiddelen die mycofenolaat bevatten. Het verplicht plan voor risicobeperking in België, waarvan
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van geneesmiddelen die mycofenolaat bevatten. Het verplicht plan voor risicobeperking in België, waarvan
Olumiant (baricitinib) filmomhulde tabletten Dit geneesmiddel is onderworpen aan aanvullende monitoring
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Olumiant. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Olumiant. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Informatiefiche voor artsen voor een veilig en doeltreffend gebruik van het geneesmiddel
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
RECONSTITUTIE, DOSERING EN TOEDIENING
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VELCADE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VELCADE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
BELANGRIJKE VEILIGHEIDSINFORMATIE
 Aanbevelingen Neem de volledige medische voorgeschiedenis van de patiënt in overweging, inclusief enig eerder of gelijktijdig gebruikte biological BELANGRIJKE VEILIGHEIDSINFORMATIE Er is geen ervaring
Aanbevelingen Neem de volledige medische voorgeschiedenis van de patiënt in overweging, inclusief enig eerder of gelijktijdig gebruikte biological BELANGRIJKE VEILIGHEIDSINFORMATIE Er is geen ervaring
Selectie en training van patiënten voor thuistoediening van Nplate
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Dit verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Dit verplicht plan voor risicobeperking in België, waarvan deze informatie
MAVENCLAD (Cladribine)
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel MAVENCLAD. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel MAVENCLAD. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Rechtstreekse melding aan de gezondheidszorgbeoefenaars
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
VOOR ALLE GENEESMIDDELEN DIE ORALE RETINOÏDEN BEVATTEN (ACITRETINE, ALITRETINOÏNE OF ISOTRETINOÏNE)
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van geneesmiddelen die orale retinoïden bevatten. Het verplicht plan voor risicobeperking in België,
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van geneesmiddelen die orale retinoïden bevatten. Het verplicht plan voor risicobeperking in België,
Artsenbrochure. bij de behandeling van patiënten met jichtartritis met Ilaris
 Artsenbrochure bij de behandeling van patiënten met jichtartritis met Ilaris Risico minimalisatie materiaal betreffende Ilaris (canakinumab) voor artsen De risico minimalisatie materialen voor Ilaris (canakinumab),
Artsenbrochure bij de behandeling van patiënten met jichtartritis met Ilaris Risico minimalisatie materiaal betreffende Ilaris (canakinumab) voor artsen De risico minimalisatie materialen voor Ilaris (canakinumab),
Postdatum. Geachte Dokter,
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Quetiapine Krka 50 mg / 200 mg / 300 mg/400 mg tabletten met verlengde afgifte.
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Quetiapine Krka 50 mg / 200 mg / 300 mg/400 mg tabletten met verlengde afgifte.
REMICADE (Infliximab) Informatiebrochure voor gezondheidsmedewerkers
 De gezondheidsautoriteiten van de EU hebben een aantal voorwaarden gekoppeld aan het in de handel brengen van het geneesmiddel REMICADE. Het verplichte plan voor risicobeperking in België, waarvan deze
De gezondheidsautoriteiten van de EU hebben een aantal voorwaarden gekoppeld aan het in de handel brengen van het geneesmiddel REMICADE. Het verplichte plan voor risicobeperking in België, waarvan deze
INFORMATIEBROCHURE VOOR BEROEPSBEOEFENAARS IN DE GEZONDHEIDSZORG
 De gezondheidsinstanties van de Europese Unie hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel OPSUMIT. Het verplicht plan voor risicobeperking in België, waarvan deze
De gezondheidsinstanties van de Europese Unie hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel OPSUMIT. Het verplicht plan voor risicobeperking in België, waarvan deze
LEIDRAAD VOOR BEROEPSBEOEFENAREN IN DE GEZONDHEIDSZORG
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel KANUMA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel KANUMA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
BIJLAGE VOORWAARDEN OF BEPERKINGEN MET BETREKKING TOT HET VEILIG EN DOELTREFFEND GEBRUIK VAN HET GENEESMIDDEL TE IMPLEMENTEREN DOOR DE LIDSTATEN
 BIJLAGE VOORWAARDEN OF BEPERKINGEN MET BETREKKING TOT HET VEILIG EN DOELTREFFEND GEBRUIK VAN HET GENEESMIDDEL TE IMPLEMENTEREN DOOR DE LIDSTATEN VOORWAARDEN OF BEPERKINGEN MET BETREKKING TOT HET VEILIG
BIJLAGE VOORWAARDEN OF BEPERKINGEN MET BETREKKING TOT HET VEILIG EN DOELTREFFEND GEBRUIK VAN HET GENEESMIDDEL TE IMPLEMENTEREN DOOR DE LIDSTATEN VOORWAARDEN OF BEPERKINGEN MET BETREKKING TOT HET VEILIG
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Belangrijke informatie voor beroepsbeoefenaren
 De gezondheidsautoriteiten van de Europese Unie hebben het in de handel brengen van het geneesmiddel Kadcyla verbonden aan bepaalde voorwaarden. Het verplichte farmacovigilantieplan ter minimalisatie van
De gezondheidsautoriteiten van de Europese Unie hebben het in de handel brengen van het geneesmiddel Kadcyla verbonden aan bepaalde voorwaarden. Het verplichte farmacovigilantieplan ter minimalisatie van
Handleiding voor zorgverleners
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel Toujeo. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel Toujeo. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Artsenbrochure. bij de behandeling van patiënten met Cryopyrin-Associated Periodic Syndromes (CAPS) met Ilaris
 Artsenbrochure bij de behandeling van patiënten met Cryopyrin-Associated Periodic Syndromes (CAPS) met Ilaris Risico minimalisatie materiaal betreffende Ilaris (canakinumab) voor artsen De risico minimalisatie
Artsenbrochure bij de behandeling van patiënten met Cryopyrin-Associated Periodic Syndromes (CAPS) met Ilaris Risico minimalisatie materiaal betreffende Ilaris (canakinumab) voor artsen De risico minimalisatie
Capecitabine Accord moet permanent worden stopgezet bij patiënten die een ernstige huidreactie hebben gehad tijdens de behandeling.
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Brochure voor de professionele zorgverleners
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Mitoxantrone Sandoz. Het verplicht plan voor risicobeperking in België, waarvan
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Mitoxantrone Sandoz. Het verplicht plan voor risicobeperking in België, waarvan
FLOLAN INFORMATIEGIDS VOOR PATIENTEN - FLOLAN
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
STRIMVELIS (autologe CD34 + -cellen getransduceerd om ADA tot expressie te brengen)
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel STRIMVELIS. Het verplichte plan voor risicobeperking in België, waarvan deze
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel STRIMVELIS. Het verplichte plan voor risicobeperking in België, waarvan deze
Mycofenolaat Mofetil (MMF CellCept ) bij reumatische aandoeningen
 Mycofenolaat Mofetil (MMF CellCept ) bij reumatische aandoeningen Uw behandelend arts heeft aangegeven u met het geneesmiddel mycofenolaat mofetil te willen gaan behandelen. Deze folder geeft informatie
Mycofenolaat Mofetil (MMF CellCept ) bij reumatische aandoeningen Uw behandelend arts heeft aangegeven u met het geneesmiddel mycofenolaat mofetil te willen gaan behandelen. Deze folder geeft informatie
Kyleena (19,5 mg levonorgestrel) afleveringsysteem voor intra-uterien gebruik
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Kyleena. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Kyleena. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Patiëntenfolder
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
NRLP-12 Gerelateerde Terugkerende Koorts
 www.printo.it/pediatric-rheumatology/be_fm/intro NRLP-12 Gerelateerde Terugkerende Koorts Versie 2016 1. WAT IS NRLP-12 GERELATEERDE TERUGKERENDE KOORTS 1.1 Wat is het? NRLP-12 gerelateerde terugkerende
www.printo.it/pediatric-rheumatology/be_fm/intro NRLP-12 Gerelateerde Terugkerende Koorts Versie 2016 1. WAT IS NRLP-12 GERELATEERDE TERUGKERENDE KOORTS 1.1 Wat is het? NRLP-12 gerelateerde terugkerende
isotretinoïne 10 mg en 20 mg zachte capsules Zwangerschapspreventie programma
 isotretinoïne 10 mg en 20 mg zachte capsules Zwangerschapspreventie programma Richtlijnen voor apothekers bij het afleveren van isotretinoïne De risico minimalisatie materialen voor isotretinoïne zijn
isotretinoïne 10 mg en 20 mg zachte capsules Zwangerschapspreventie programma Richtlijnen voor apothekers bij het afleveren van isotretinoïne De risico minimalisatie materialen voor isotretinoïne zijn
Bijgevoegd vindt u de risico minimalisatie materialen.
 Begeleidende brief voor HCP Betreft: Risico minimalisatie materialen betreffende, infliximab voor voorschrijvers Geachte Heer / Mevrouw, REMSIMA (Infliximab) 100 mg poeder voor concentraat voor oplossing
Begeleidende brief voor HCP Betreft: Risico minimalisatie materialen betreffende, infliximab voor voorschrijvers Geachte Heer / Mevrouw, REMSIMA (Infliximab) 100 mg poeder voor concentraat voor oplossing
Checklist voor voorschrijvers
 De Nederlandse en Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Jext. Het verplicht plan voor risicobeperking in Nederland en
De Nederlandse en Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Jext. Het verplicht plan voor risicobeperking in Nederland en
Imnovid (pomalidomide) Directe berichtgeving aan gezondheidszorgbeoefenaars
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Imnovid. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Imnovid. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Belangrijke informatie voor zorgverleners over de nieuwe formulering van FLOLAN
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Dosisgids bestemd voor de arts voor de behandeling van Reumatoïde Artritis (RA) met RoACTEMRA
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel RoACTEMRA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel RoACTEMRA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Informatie verspreid onder het gezag van het federaal agentschap voor geneesmiddelen en gezondheidsproducten
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Directe communicatie aan gezondheidszorgbeoefenaars over de associatie van Sprycel (dasatinib) met Pulmonaire Arteriële Hypertensie (PAH)
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Informatieboekje voor patiënten Wat u moet weten
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VOLIBRIS. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VOLIBRIS. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Educatieve PrEP-brochure voor voorschrijvers 1
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Emtricitabine/Tenofovirdisoproxil Mylan 200 mg/245 mg filmomhulde tabletten.
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Emtricitabine/Tenofovirdisoproxil Mylan 200 mg/245 mg filmomhulde tabletten.
isotretinoïne 10 mg en 20 mg zachte capsules Preventie van zwangerschap & blootstelling van de foetus
 isotretinoïne 10 mg en 20 mg zachte capsules Preventie van zwangerschap & blootstelling van de foetus Richtlijnen voor apothekers bij het afleveren van Isotretinoïne Inleiding Isotretinoïne bevat de actieve
isotretinoïne 10 mg en 20 mg zachte capsules Preventie van zwangerschap & blootstelling van de foetus Richtlijnen voor apothekers bij het afleveren van Isotretinoïne Inleiding Isotretinoïne bevat de actieve
Brochure voor Artsen
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel Arava. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel Arava. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
ACTYNOX 50%/50% v/v Distikstofoxide (N 2 O) en Zuurstof (O 2 ) Medicinaal gas, samengeperst
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ACTYNOX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ACTYNOX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Dosisgids bestemd voor de arts voor de behandeling van Reumatoïde Artritis (RA) met RoACTEMRA
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel RoACTEMRA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel RoACTEMRA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Onderwerp: Ernstige huidreacties geassocieerd met Capecitabine (Xeloda )
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
CINRYZE (C1-REMMER [HUMAAN])
![CINRYZE (C1-REMMER [HUMAAN]) CINRYZE (C1-REMMER [HUMAAN])](/thumbs/66/54698885.jpg) De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CINRYZE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel CINRYZE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Patiënteninformatiebrochure
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel KEYTRUDA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel KEYTRUDA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Om het risico op PML te verminderen wordt aanbevolen om de volgende acties te ondernemen:
 Datum: 20 november 2015 Betreft: belangrijke risico-informatie: nieuwe maatregelen voor het minimaliseren van het risico op PML bij gebruik van Tecfidera (dimethylfumaraat) verbeterde regels voor monitoren
Datum: 20 november 2015 Betreft: belangrijke risico-informatie: nieuwe maatregelen voor het minimaliseren van het risico op PML bij gebruik van Tecfidera (dimethylfumaraat) verbeterde regels voor monitoren
VOORLICHTINGSBROCHURE VOOR DE GEZONDHEIDSZORGBEOEFENAAR
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ACCUSOL 35. Het verplicht plan voor risicobeperking in België, waarvan deze
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel ACCUSOL 35. Het verplicht plan voor risicobeperking in België, waarvan deze
Familiaire Mediterrane Koorts
 www.printo.it/pediatric-rheumatology/nl/intro Familiaire Mediterrane Koorts Versie 2016 2. DIAGNOSE EN BEHANDELING 2.1 Hoe wordt het gediagnosticeerd? Over het algemeen wordt de volgende aanpak gehanteerd:
www.printo.it/pediatric-rheumatology/nl/intro Familiaire Mediterrane Koorts Versie 2016 2. DIAGNOSE EN BEHANDELING 2.1 Hoe wordt het gediagnosticeerd? Over het algemeen wordt de volgende aanpak gehanteerd:
FORMULIER VOOR START VAN DE BEHANDELING MET TYSABRI
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van TYSABRI. Het verplichte plan voor risicobeperking in België, waarvan deze informatie deel uitmaakt,
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van TYSABRI. Het verplichte plan voor risicobeperking in België, waarvan deze informatie deel uitmaakt,
RISICO MINIMALISATIE MATERIAAL BETREFFENDE BARICITINIB VOOR DE VOORSCHRIJVER, APOTHEKER EN VERPLEEGKUNDIGE
 RISICO MINIMALISATIE MATERIAAL BETREFFENDE BARICITINIB VOOR DE VOORSCHRIJVER, APOTHEKER EN VERPLEEGKUNDIGE De risico minimalisatie materialen voor baricitinib zijn beoordeeld door het College ter Beoordeling
RISICO MINIMALISATIE MATERIAAL BETREFFENDE BARICITINIB VOOR DE VOORSCHRIJVER, APOTHEKER EN VERPLEEGKUNDIGE De risico minimalisatie materialen voor baricitinib zijn beoordeeld door het College ter Beoordeling
INFLECTRA (infliximab) RISICO MINIMALISATIE MATERIALEN BETREFFENDE INFLECTRA (INFLIXIMAB) VOOR DE VOORSCHRIJVERS. Biologics
 INFLECTRA (infliximab) Dit geneesmiddel is onderworpen aan aanvullende monitoring RISICO MINIMALISATIE MATERIALEN BETREFFENDE INFLECTRA (INFLIXIMAB) VOOR DE VOORSCHRIJVERS De risico minimalisatie materialen
INFLECTRA (infliximab) Dit geneesmiddel is onderworpen aan aanvullende monitoring RISICO MINIMALISATIE MATERIALEN BETREFFENDE INFLECTRA (INFLIXIMAB) VOOR DE VOORSCHRIJVERS De risico minimalisatie materialen
Hemlibra (emicizumab) Subcutane injectie Dit geneesmiddel is onderworpen aan aanvullende monitoring. Informatiebrochure voor de patiënt/verzorger
 Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel Hemlibra, om voor een goed gebruik ervan te zorgen en om de ongewenste effecten ervan te beperken, zijn er bepaalde
Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel Hemlibra, om voor een goed gebruik ervan te zorgen en om de ongewenste effecten ervan te beperken, zijn er bepaalde
Deficiëntie van de IL-1-Receptorantagonist (DIRA)
 www.printo.it/pediatric-rheumatology/be_fm/intro Deficiëntie van de IL-1-Receptorantagonist (DIRA) Versie 2016 1. WAT IS DIRA 1.1 Wat is het? Deficiëntie van de IL-1-receptorantagonist (DIRA) is een zeldzame
www.printo.it/pediatric-rheumatology/be_fm/intro Deficiëntie van de IL-1-Receptorantagonist (DIRA) Versie 2016 1. WAT IS DIRA 1.1 Wat is het? Deficiëntie van de IL-1-receptorantagonist (DIRA) is een zeldzame
Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab) voor voorschrijvende artsen. KEYTRUDA (pembrolizumab)
 Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab) voor voorschrijvende artsen KEYTRUDA (pembrolizumab) 1 Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab) voor voorschrijvende
Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab) voor voorschrijvende artsen KEYTRUDA (pembrolizumab) 1 Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab) voor voorschrijvende
Behandeling met ustekinumab. Risico minimalisatie materiaal: Veiligheidsinformatie betreffende ustekinumab voor patiënten
 Behandeling met ustekinumab Risico minimalisatie materiaal: Veiligheidsinformatie betreffende ustekinumab voor patiënten Belangrijke informatie Deze materialen beschrijven aanbevelingen om belangrijke
Behandeling met ustekinumab Risico minimalisatie materiaal: Veiligheidsinformatie betreffende ustekinumab voor patiënten Belangrijke informatie Deze materialen beschrijven aanbevelingen om belangrijke
Bijlage III. Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiters
 Bijlage III Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiters NB: Deze Samenvatting van de productkenmerken, Etikettering
Bijlage III Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiters NB: Deze Samenvatting van de productkenmerken, Etikettering
Infliximab (Remicade ) bij reumatische aandoeningen
 Infliximab (Remicade ) bij reumatische aandoeningen Uw behandelend arts heeft aangegeven u met het geneesmiddel infliximab te willen gaan behandelen. Deze folder geeft informatie over dit geneesmiddel.
Infliximab (Remicade ) bij reumatische aandoeningen Uw behandelend arts heeft aangegeven u met het geneesmiddel infliximab te willen gaan behandelen. Deze folder geeft informatie over dit geneesmiddel.
RISICO MINIMALISATIE MATERIAAL BETREFFENDE BARICITINIB VOOR DE VOORSCHRIJVER, APOTHEKER EN VERPLEEGKUNDIGE
 RISICO MINIMALISATIE MATERIAAL BETREFFENDE BARICITINIB VOOR DE VOORSCHRIJVER, APOTHEKER EN VERPLEEGKUNDIGE De risico minimalisatie materialen voor baricitinib zijn beoordeeld door het College ter Beoordeling
RISICO MINIMALISATIE MATERIAAL BETREFFENDE BARICITINIB VOOR DE VOORSCHRIJVER, APOTHEKER EN VERPLEEGKUNDIGE De risico minimalisatie materialen voor baricitinib zijn beoordeeld door het College ter Beoordeling
Informatiebrochure voor laboratoriumpersoneel
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel hemlibra. Het verplicht plan voor risicobeperking in België en het Groothertogdom
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel hemlibra. Het verplicht plan voor risicobeperking in België en het Groothertogdom
Dit geneesmiddel is onderworpen aan aanvullende monitoring
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Alofisel. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Alofisel. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Azathioprine (Imuran ) bij dermatologische aandoeningen
 Azathioprine (Imuran ) bij dermatologische aandoeningen Uw behandelend arts heeft aangegeven u met het geneesmiddel azathioprine te willen gaan behandelen. Deze folder geeft informatie over dit geneesmiddel.
Azathioprine (Imuran ) bij dermatologische aandoeningen Uw behandelend arts heeft aangegeven u met het geneesmiddel azathioprine te willen gaan behandelen. Deze folder geeft informatie over dit geneesmiddel.
INFORMATIE VOOR DE VOORSCHRIJVER
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Tracleer. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Tracleer. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Wat u moet weten over MabThera
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel MabThera. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel MabThera. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Abatacept (Orencia ) Behandeling tweedelijns antireumatica
 Abatacept (Orencia ) Behandeling tweedelijns antireumatica Abatacept (Orencia ) is een antireumatisch geneesmiddel dat er voor zorgt dat de ontsteking en de pijn in uw gewrichten afneemt. Het zorgt er
Abatacept (Orencia ) Behandeling tweedelijns antireumatica Abatacept (Orencia ) is een antireumatisch geneesmiddel dat er voor zorgt dat de ontsteking en de pijn in uw gewrichten afneemt. Het zorgt er
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de
Informatie verstrekt onder het gezag van het fagg. Rechtstreekse mededeling aan de gezondheidszorgbeoefenaars
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Rituximab (MabThera ) Voorgeschreven door de reumatoloog
 Rituximab (MabThera ) Voorgeschreven door de reumatoloog Albert Schweitzer ziekenhuis juli 2013 pavo 0908 Inleiding De reumatoloog heeft met u besproken dat u rituximab gaat gebruiken. In deze folder leest
Rituximab (MabThera ) Voorgeschreven door de reumatoloog Albert Schweitzer ziekenhuis juli 2013 pavo 0908 Inleiding De reumatoloog heeft met u besproken dat u rituximab gaat gebruiken. In deze folder leest
Informatie over onderhoudsmedicatie voor (zeer) actieve Multiple Sclerose
 Multiple Sclerose Centrum Noord Nederland Informatie over onderhoudsmedicatie voor (zeer) actieve Multiple Sclerose Patiënteninformatie 1905 Informatie over onderhoudsmedicatie voor (zeer) actieve Multiple
Multiple Sclerose Centrum Noord Nederland Informatie over onderhoudsmedicatie voor (zeer) actieve Multiple Sclerose Patiënteninformatie 1905 Informatie over onderhoudsmedicatie voor (zeer) actieve Multiple
Dit geneesmiddel is onderworpen aan aanvullende monitoring.
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Erivedge. Het verplicht plan voor risicobeperking in België, waar deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Erivedge. Het verplicht plan voor risicobeperking in België, waar deze informatie
Informatie verstrekt onder het gezag van het Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
NEBIDO (TESTOSTERONUNDECANOAAT) 1000 mg/4 ml oplossing voor injectie GIDS VOOR DE VOORSCHRIJVER
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nebido. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nebido. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Gids voor gezondheidszorgbeoefenaars
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Lariam. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Lariam. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
RECONSTITUTIE, DOSERING EN TOEDIENING
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VELCADE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VELCADE. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Bijsluiter: informatie voor de patiënt
 Bijsluiter: informatie voor de patiënt Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. U kunt hieraan bijdragen door melding
Bijsluiter: informatie voor de patiënt Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. U kunt hieraan bijdragen door melding
Wat u zou moeten weten over Rixathon
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Rixathon. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Rixathon. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
NLRP-12 Gerelateerde Terugkerende Koorts
 www.printo.it/pediatric-rheumatology/nl/intro NLRP-12 Gerelateerde Terugkerende Koorts Versie 2016 1. WAT IS NLRP12 GERELATEERDE TERUGKERENDE KOORTS 1.1 Wat is het? NLRP12 gerelateerde terugkerende koorts
www.printo.it/pediatric-rheumatology/nl/intro NLRP-12 Gerelateerde Terugkerende Koorts Versie 2016 1. WAT IS NLRP12 GERELATEERDE TERUGKERENDE KOORTS 1.1 Wat is het? NLRP12 gerelateerde terugkerende koorts
Azathioprine (Imuran ) bij dermatologische aandoeningen
 Azathioprine (Imuran ) bij dermatologische aandoeningen Uw behandelend arts heeft aangegeven u met het geneesmiddel azathioprine te willen gaan behandelen. Deze folder geeft informatie over dit geneesmiddel.
Azathioprine (Imuran ) bij dermatologische aandoeningen Uw behandelend arts heeft aangegeven u met het geneesmiddel azathioprine te willen gaan behandelen. Deze folder geeft informatie over dit geneesmiddel.
