vorm Orale suspensie toltrazuril/ml toltrazuril/ml toltrazuril/ml toltrazuril/ml toltrazuril/ml toltrazuril/ml toltrazuril/ml
|
|
|
- Daniël Martens
- 5 jaren geleden
- Aantal bezoeken:
Transcriptie
1 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET DIERGENEESMIDDEL, DIERSOORT, TOEDIENINGSWEG, AANVRAGER/HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1/11
2 Lidstaat Oostenrijk Aanvrager/ Houder van de vergunning voor het in de handel brengen Fantasienaam CEVAZURIL /ml, Suspension zum Eingeben für Ferkel Farmaceutische vorm Sterkte Diersoort Frequentie van toediening en toedieningsweg België Bulgarije Cyprus CEVAZURIL /ml, orale suspensie voor biggen СЕВАЗУРИЛ 50 мг/мл, суспензия за перорално прилагане при прасета CEVAZURIL /ml, πόσιµο εναιώρηµα για χοιρίδια Tsjechische Republiek Denemarken Estland Bristol UK CEVAZURIL /ml, Perorální suspense pro selata Cevazuril 50mg/ml, oral suspension til spædgrise CEVAZURIL /ml, Suukaudne suspension jaoks põrsad 2/11
3 Lidstaat Frankrijk Duitsland Griekenland Hongarije Ierland Italië Letland Aanvrager/ Houder van de vergunning voor het in de handel brengen Fantasienaam CEVAZURIL /ml, suspension buvable pour porcelets 1 CEVAZURIL /ml, Suspension zum Eingeben für Ferkel CEVAZURIL /ml, πόσιµο εναιώρηµα για χοιρίδια CEVAZURIL /ml, belsőleges szuszpenzió malacoknak CEVAZURIL /ml, oral suspension for piglets CEVAZURIL /ml, sospensione orale per suinetti CEVAZURIL /ml, Suspensija iekšķīgai lietošanai dēļ sivēni Farmaceutische vorm Sterkte Diersoort Frequentie van toediening en toedieningsweg 1 Vergunning voor het in de handel brengen is verleend 3/11
4 Lidstaat Litouwen Luxemburg Malta Nederland Polen Portugal Roemenië Aanvrager/ Houder van de vergunning voor het in de handel brengen Fantasienaam CEVAZURIL /ml, Geriamoji suspensija dèl paršeliai CEVAZURIL /ml, suspension buvable pour porcelets 2 CEVAZURIL /ml Suspensjoni orali għal ħnienes CEVAZURIL /ml, orale suspensie voor biggen CEVAZURIL /ml, zawiesina doustna dla prosiąt CEVAZURIL /ml, suspensão oral para leitões CEVAZURIL /ml, Suspensie orală pentru purceii Farmaceutische vorm Sterkte Diersoort Frequentie van toediening en toedieningsweg. 2 Vergunning voor het in de handel brengen is verleend 4/11
5 Lidstaat Slowakije Spanje Verenigd Koninkrijk Aanvrager/ Houder van de vergunning voor het in de handel brengen Fantasienaam CEVAZURIL /ml, Perorálna suspenzia pre prasiatka CEVAZURIL /ml, Suspensión Oral para lechones CEVAZURIL /ml, oral suspension for piglets Farmaceutische vorm Sterkte Diersoort Frequentie van toediening en toedieningsweg... 5/11
6 BIJLAGE II WETENSCHAPPELIJKE CONCLUSIES 6/11
7 ALGEHELE SAMENVATTING VAN DE WETENSCHAPPELIJKE BEOORDELING VAN CEVAZURIL /ml orale suspensie voor biggen 1. Inleiding CEVAZURIL /ml orale suspensie voor biggen is een suspensie voor orale toediening die als werkzame stof bevat. Het geneesmiddel is geïndiceerd voor de preventie van klinische verschijnselen van coccidiose bij pasgeboren biggen op bedrijven met een bevestigde ziektegeschiedenis van door Isospora suis veroorzaakte coccidiose. De aanbevolen dosis is een enkele orale dosis van 20 mg 0,4 ml orale suspensie per kg lichaamsgewicht, op levensdag 3-5. Het middel is een genericum van Baycox 5% orale oplossing. Tijdens de gedecentraliseerde procedure bestond er tussen de lidstaten verschil van inzicht over de vraag of de gegevens die voor fase II van de beoordeling van de milieurisico s zijn overgelegd wel adequaat waren. De aanvrager overlegde aanvankelijk alleen een fase I-beoordeling van de milieurisico s van het middel, waaruit bleek dat de PEC bodem ruimschoots onder de 100 µg/kg lag. Omdat enkele betrokken lidstaten bedenkingen uitten over de persistentie van de belangrijkste metaboliet van toltrazuril, toltrazurilsulfon, was de aanvrager verplicht een fase II-beoordeling in te dienen. In antwoord op de vragen die in de gedecentraliseerde procedure werden gesteld, verwees de aanvrager naar de conclusies waartoe het CVMP tijdens de overeenkomstig artikel 35 van Richtlijn 2001/82/EG uitgevoerde verwijzingsprocedure was gekomen, en wel voor toltrazuril bevattende diergeneesmiddelen bedoeld voor gebruik bij pluimveesoorten en wat betreft de beoordeling van de milieurisico s. Hij voerde aan dat: de PEC bodem bij varkens duidelijk lager is dan bij pluimvee; de fok- en productiemethoden bij pluimvee en varkens vergelijkbaar zijn; het metabolisme van toltrazuril bij pluimvee en varkens als kwalitatief vergelijkbaar wordt beschouwd. Daarom was de aanvrager van mening dat de conclusies van de CVMP-verwijzing voor pluimvee konden worden geëxtrapoleerd naar biggen. Dit antwoord werd door de rapporterende lidstaat geaccepteerd, maar door enkele betrokken lidstaten afgewezen op grond van het feit dat verwijzing naar eindpuntwaarden van een gepubliceerde samenvatting van een beoordeling niet voldoende was als vervanging voor gegevens van een milieurisicobeoordeling. Gezien het verschil van inzicht werd de kwestie naar het CVMP verwezen. 2. Evaluatie van de milieurisicobeoordeling 2.1 Beoordeling van de overgelegde fase II-gegevens De door de aanvrager uitgevoerde fase II-beoordeling was gebaseerd op: de conclusies uit de verwijzingsprocedure overeenkomstig artikel 35 van Richtlijn 2001/82/EG met betrekking tot toltrazuril bevattende diergeneesmiddelen bedoeld voor gebruik bij pluimveesoorten en wat betreft de beoordeling van de milieurisico s; de argumentatie dat de voorspelde milieuconcentratie (Predicted Environmental Concentration - PEC) als gevolg van het gebruik van het middel bij varkens lager is dan de PEC als gevolg van het gebruik bij pluimvee. De overgelegde informatie bevat geen details over de opzet, uitvoering, analyse en resultaten van het onderzoek die een volledige en onafhankelijke beoordeling mogelijk maken, en laat daarom geen ruimte 7/11
8 voor een fase II-beoordeling overeenkomstig de wettelijke vereisten en relevante van kracht zijnde richtsnoeren 3. Bovendien zijn de scenario s voor varkens- en pluimveemest niet noodzakelijkerwijs vergelijkbaar, omdat de fokomstandigheden, toepassing en agrarische gebruiken voor de verwerking van mest vaak sterk verschillen. Erkend wordt dat de belangrijkste metaboliet voor deze verbinding bij varkens waarschijnlijk dezelfde is als bij pluimvee en dat in de berekeningen in fase I van de milieurisicobeoordeling bij de berekening van de milieublootstelling 100% van de dosis wordt meegenomen (totaalresidubenadering). Een mogelijk verschil in metabolisme is daarom van weinig praktische betekenis bij de fase I-berekening van de PEC-waarde. Samenvattend concludeert het CVMP dat de door de aanvrager overgelegde informatie met betrekking tot de fase II-beoordeling onvoldoende is en dat daarom geen vergunning voor het in de handel brengen zou moeten worden verleend als voor het middel een fase II-beoordeling vereist is. 2.1 Evaluatie van fase I en overwegingen over de noodzaak van een fase II-beoordeling Naast de vraag of de verstrekte gegevens voldoende waren voor een fase II-beoordeling (zie boven), heeft het Comité de bij de aanvraag overgelegde fase I-beoordeling opnieuw bekeken om tot een advies te komen over het verlenen of weigeren van de vergunning voor het in de handel brengen van het middel overeenkomstig artikel 36 van Richtlijn 2001/82/EG. Het Comité bestudeerde fase I van de milieurisicobeoordeling van de aanvrager voor Cevazuril /kg voor oraal gebruik bij biggen om na te gaan of voor de beoordeling van de milieurisico s van het middel fase I zou volstaan, of dat ook fase II vereist zou zijn. De uitkomst van fase I was dat de PEC bodem voor biggen 12 µg/kg is, wat beduidend lager is dan de drempelwaarde van 100 µg/kg voor een fase IIbeoordeling. Voor de milieurisicobeoordeling zou fase I daarom volstaan, tenzij er bijzondere punten van zorg waren die een verzoek om een fase II-beoordeling, zoals voorzien in de VICH-richtsnoer GL 6, zouden rechtvaardigen. De VICH-richtsnoer GL 6 bepaalt het volgende: Voor bepaalde diergeneesmiddelen waarvoor de beoordeling anders met fase I zou kunnen eindigen, kan extra milieu-informatie vereist zijn om bijzondere punten van zorg met betrekking tot hun werking en gebruik aan de orde te stellen. Dergelijke situaties zullen naar verwachting eerder uitzondering dan regel zijn en er dient enig bewijsmateriaal ter ondersteuning van het punt van zorg voorhanden te zijn." Uit bewijsmateriaal uit het publieke domein blijkt dat de belangrijkste metaboliet en het belangrijkste afbraakproduct in de bodem van toltrazuril (toltrazurilsulfon) persistent, fytotoxisch en mobiel is en kan uitspoelen naar het grondwater. Daarom kan in principe bij wijze van uitzondering om een fase II worden verzocht. Het CVMP heeft eerder echter geconcludeerd dat toltrazuril en toltrazurilsulfon geen onaanvaardbaar risico opleveren bij milieuconcentraties die hoger zijn dan de voorspelde concentraties bij normaal gebruik van Cevazuril /ml orale suspensie voor biggen. Het huidige bewijsmateriaal is daarom onvoldoende om het overwicht van een bijzonder punt van zorg aan te tonen en een fase IIbeoordeling nodig te maken. Het CVMP is daarom tot de conclusie gekomen dat de milieurisicobeoordeling van het middel met fase I kan eindigen. 3 CVMP/VICH GL6: Environmental impact assessment (EIAS) for veterinary medicinal products - Phase I (CVMP/VICH/592/98-FINAL), CVMP/VICH GL38: Environmental impact assessments for veterinary medicinal products (VMPs) - Phase II (CVMP/VICH/790/03-FINAL) and Environmental Impact Assessment for Veterinary Medicinal Products in support of the VICH guidelines GL6 and GL38 (EMEA/CVMP/ERA/418282/2005- Rev.1) 8/11
9 REDENEN VOOR DE AANBEVELING TOT VERLENING VAN EEN VERGUNNING VOOR HET IN DE HANDEL BRENGEN Het CVMP concludeert dat de door de aanvrager overgelegde informatie geen ruimte laat voor een fase IIbeoordeling overeenkomstig de wettelijke vereisten en van kracht zijnde richtsnoeren. De beoordeling van de milieurisico s van het middel overeenkomstig de VICH-richtsnoer GL 6 (Environmental Impact Assessment for veterinary medicinal products- Phase I, CVMP/VICH/592/98- Final) heeft uitgewezen dat de PEC bodem voor biggen 12 µg/kg bedraagt, wat beduidend lager is dan de drempelwaarde van 100 µg/kg voor een fase II-beoordeling. Het CVMP is van mening dat er op basis van de huidige informatie geen wetenschappelijke gronden zijn om een fase II-beoordeling te vereisen en dat de milieurisicobeoordeling van het middel daarom kan eindigen met fase I. Na bestudering van alle schriftelijk overgelegde en in de mondelinge toelichting verstrekte gegevens en na overleg met de Werkgroep Beoordeling Milieurisico s heeft het CVMP geconcludeerd dat de tijdens de gedecentraliseerde procedure aangevoerde bezwaren geen beletsel mogen zijn voor de verlening van een vergunning voor het in de handel brengen. Daarom beveelt het CVMP aan een vergunning te verlenen voor het in de handel brengen van CEVAZURIL /ml orale suspensie voor biggen, waarvoor de samenvatting van de productkenmerken, etikettering en bijsluiter in bijlage III van het CVMP-advies worden uiteengezet. 9/11
10 BIJLAGE III: SAMENVATTING VAN DE PRODUCTKENMERKEN, ETIKETTERING EN BIJSLUITER 10/11
11 De geldige samenvatting van de productkenmerken, de etikettering en de bijsluiter zijn de definitieve versies die tijdens de procedure van de Coördinatiegroep zijn overeengekomen. 11/11
Bijlage I Lijst met namen, farmaceutische vorm, sterkte van het diergeneesmiddel, diersoorten, toedieningsweg, aanvrager in de lidstaten
 Bijlage I Lijst met namen, farmaceutische vorm, sterkte van het diergeneesmiddel, diersoorten, toedieningsweg, aanvrager in de lidstaten 1/10 Lidstaat Aanvrager Naam Werkzaam bestanddeel Sterkte Farmaceutische
Bijlage I Lijst met namen, farmaceutische vorm, sterkte van het diergeneesmiddel, diersoorten, toedieningsweg, aanvrager in de lidstaten 1/10 Lidstaat Aanvrager Naam Werkzaam bestanddeel Sterkte Farmaceutische
NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
 BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN 1/7 Aanvrager of houder van de vergunning voor
BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN 1/7 Aanvrager of houder van de vergunning voor
BIJLAGE I. EMEA/CVMP/495339/2007-NL november 2007 1/10
 BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN DE GENEESMIDDELEN, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER/AANVRAGER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EMEA/CVMP/495339/2007-NL november
BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN DE GENEESMIDDELEN, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER/AANVRAGER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EMEA/CVMP/495339/2007-NL november
NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORT, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
 BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORT, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN 1/7 Aanvrager of houder van de vergunning voor het
BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORT, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN 1/7 Aanvrager of houder van de vergunning voor het
NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
 BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN 1/7 Aanvrager of houder van de vergunning voor
BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN 1/7 Aanvrager of houder van de vergunning voor
Annex I. Lijst met naam, farmaceutische vorm, sterkte van het diergeneesmiddel, diersoort, toediening, aanvrager in de lidstaat.
 Annex I Lijst met naam, farmaceutische vorm, sterkte van het diergeneesmiddel, diersoort, toediening, aanvrager in de lidstaat. 1 Lid EU/EEA Aanvrager Naam INN Farmaceutische vorm Sterkte Diersoort Toedieningsweg
Annex I Lijst met naam, farmaceutische vorm, sterkte van het diergeneesmiddel, diersoort, toediening, aanvrager in de lidstaat. 1 Lid EU/EEA Aanvrager Naam INN Farmaceutische vorm Sterkte Diersoort Toedieningsweg
Volume: 0-49 zendingen per jaar Europa 0 2 kg 2-10 kg kg kg
 Wanneer u op basis van uw daadwerkelijkaantal zendingen boven de 49 zendingen per jaar uitkomt, dan kunt u ons contacteren voor verbeterde tarieven. Wij passen uw prijzen dan direct aan. Volume: 0-49 zendingen
Wanneer u op basis van uw daadwerkelijkaantal zendingen boven de 49 zendingen per jaar uitkomt, dan kunt u ons contacteren voor verbeterde tarieven. Wij passen uw prijzen dan direct aan. Volume: 0-49 zendingen
Houder van de vergunning voor het in de handel brengen. Fantasienaam Sterkte Farmaceutische vorm Toedieningsweg
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1 Lidstaat Oostenrijk België Cyprus
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1 Lidstaat Oostenrijk België Cyprus
Suspensie voor injectie. florfenicol. injectie. injectie. injectie. injectie. injectie. injectie
 Bijlage I Lijst met de naam, farmaceutische vorm, sterkte van het geneesmiddel voor diergeneeskundig, diersoorten, toedieningsweg en aanvrager in de lidstaten 1 Lidstaat EU/EER Aanvrager Naam INN Farmaceutische
Bijlage I Lijst met de naam, farmaceutische vorm, sterkte van het geneesmiddel voor diergeneeskundig, diersoorten, toedieningsweg en aanvrager in de lidstaten 1 Lidstaat EU/EER Aanvrager Naam INN Farmaceutische
Tarieven Europa: staffel 1
 Tarieven Europa: staffel 1 Wanneer u op basis van uw daadwerkelijkaantal zendingen boven de 49 zendingen per jaar uitkomt, dan kunt u ons contacteren voor verbeterde tarieven. Wij passen uw prijzen dan
Tarieven Europa: staffel 1 Wanneer u op basis van uw daadwerkelijkaantal zendingen boven de 49 zendingen per jaar uitkomt, dan kunt u ons contacteren voor verbeterde tarieven. Wij passen uw prijzen dan
1. 31958 Q 1101: EAEC Raad: De Statuten van het Voorzieningsagentschap van Euratom (PB 27 van 6.12.1958, blz. 534), gewijzigd bij:
 9. ENERGIE 1. 31958 Q 1101: EAEC Raad: De Statuten van het Voorzieningsagentschap van Euratom (PB 27 van 6.12.1958, blz. 534), gewijzigd bij: 31973 D 0045: Besluit 73/45/Euratom van de Raad van 8 maart
9. ENERGIE 1. 31958 Q 1101: EAEC Raad: De Statuten van het Voorzieningsagentschap van Euratom (PB 27 van 6.12.1958, blz. 534), gewijzigd bij: 31973 D 0045: Besluit 73/45/Euratom van de Raad van 8 maart
LIJST MET NAMEN, FARMACEUTISCHE VORMEN, STERKTEN, DIERSOORTEN, TOEDIENINGSWEGEN, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN / AANVRAGERS
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORMEN, STERKTEN, DIERSOORTEN, TOEDIENINGSWEGEN, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN / AANVRAGERS 1/9 Lidstaat/nummer van de vergunning voor
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORMEN, STERKTEN, DIERSOORTEN, TOEDIENINGSWEGEN, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN / AANVRAGERS 1/9 Lidstaat/nummer van de vergunning voor
Aanvrager Fantasienaam Sterkte Farmaceutische vorm. Loratadine. Vitabalans 10 mg tablety. Loratadine. Vitabalans. Vitabalans 10 mg tabletes
 Biljage I Lijst met namen, farmaceutische vorm, sterkte van het geneesmiddel, toedieningsweg, aanvrager en houder van de vergunning voor het in de handel brengen in de lidstaten 1 Lidstaat (EU/EER) Houder
Biljage I Lijst met namen, farmaceutische vorm, sterkte van het geneesmiddel, toedieningsweg, aanvrager en houder van de vergunning voor het in de handel brengen in de lidstaten 1 Lidstaat (EU/EER) Houder
NAAM, FARMACEUTISCHE VORM, STERKTE VAN DE GENEESMIDDELEN, DIERSOORTEN, TOEDIENINGSWEGEN, EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
 BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN DE GENEESMIDDELEN, DIERSOORTEN, TOEDIENINGSWEGEN, EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EMEA/CVMP/166766/2006-NL mei 2006 1/7 Lidstaat
BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN DE GENEESMIDDELEN, DIERSOORTEN, TOEDIENINGSWEGEN, EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EMEA/CVMP/166766/2006-NL mei 2006 1/7 Lidstaat
Tarieven Europa: staffel 1
 Tarieven Europa: staffel 1 Wanneer u op basis van uw daadwerkelijkaantal zendingen boven de 49 zendingen per jaar uitkomt, dan kunt u ons contacteren voor verbeterde tarieven. Wij passen uw prijzen dan
Tarieven Europa: staffel 1 Wanneer u op basis van uw daadwerkelijkaantal zendingen boven de 49 zendingen per jaar uitkomt, dan kunt u ons contacteren voor verbeterde tarieven. Wij passen uw prijzen dan
Fantasienaam Sterkte Farmaceutisch e vorm
 Bijlage I Lijst met namen, farmaceutische vorm, sterkte van het geneesmiddel voor diergeneeskundig gebruik, diersoorten, houders van de vergunning voor het in de handel brengen in de lidstaten 1/10 Lidstaat
Bijlage I Lijst met namen, farmaceutische vorm, sterkte van het geneesmiddel voor diergeneeskundig gebruik, diersoorten, houders van de vergunning voor het in de handel brengen in de lidstaten 1/10 Lidstaat
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, AANVRAGERS IN DE LIDSTATEN
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, AANVRAGERS IN DE LIDSTATEN 1 AT - Oostenrijk Flutiform 50 Mikrogramm/5 Mikrogramm pro Sprühstoß Druckgasinhalation
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, AANVRAGERS IN DE LIDSTATEN 1 AT - Oostenrijk Flutiform 50 Mikrogramm/5 Mikrogramm pro Sprühstoß Druckgasinhalation
LIJST MET NAMEN, FARMACEUTISCHE VORM, DIERSOORTEN, TOEDIENINGSWEG EN HOUDERS VAN DE VERGUNNINGEN VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, DIERSOORTEN, TOEDIENINGSWEG EN HOUDERS VAN DE VERGUNNINGEN VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN EMEA/CVMP/269630/2006-NL juli 2006 1/7 Lidstaat
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, DIERSOORTEN, TOEDIENINGSWEG EN HOUDERS VAN DE VERGUNNINGEN VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN EMEA/CVMP/269630/2006-NL juli 2006 1/7 Lidstaat
Lijst met namen, farmaceutische vorm, sterkte van het diergeneesmiddel, doeldieren, toedieningsweg, houder van de vergunning in de lidstaten.
 Bijlage I Lijst met namen, farmaceutische vorm, sterkte van het diergeneesmiddel, doeldieren, toedieningsweg, houder van de vergunning in de lidstaten. 1/11 Lidstaat EU/EEA Houder van de vergunning Naam
Bijlage I Lijst met namen, farmaceutische vorm, sterkte van het diergeneesmiddel, doeldieren, toedieningsweg, houder van de vergunning in de lidstaten. 1/11 Lidstaat EU/EEA Houder van de vergunning Naam
BIJLAGE I. EMEA/CVMP/345752/2008-NL 16 juli /14
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN DE GENEESMIDDELEN VOOR DIERGENEESKUNDIG GEBRUIK, DIERSOORTEN, TOEDIENINGSWEG(EN), HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN DE GENEESMIDDELEN VOOR DIERGENEESKUNDIG GEBRUIK, DIERSOORTEN, TOEDIENINGSWEG(EN), HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN
Amoxicillin 200 mg Clavulanic acid 50 mg Prednisolone 10 mg. Amoxicillin 200 mg Clavulanic acid 50 mg Prednisolone 10 mg
 Bijlage I Lijst met namen, farmaceutische vormen, sterkten van het diergeneesmiddel, diersoorten, toedieningsweg, wachttijden, aanvrager, houder van de vergunning voor het in de handel brengen in de lidstaten
Bijlage I Lijst met namen, farmaceutische vormen, sterkten van het diergeneesmiddel, diersoorten, toedieningsweg, wachttijden, aanvrager, houder van de vergunning voor het in de handel brengen in de lidstaten
ANNEX BIJLAGE. bij VERSLAG VAN DE COMMISSIE AAN HET EUROPEES PARLEMENT EN DE RAAD
 EUROPESE COMMISSIE Brussel, 21.9.2018 COM(2018) 651 final ANNEX BIJLAGE bij VERSLAG VAN DE COMMISSIE AAN HET EUROPEES PARLEMENT EN DE RAAD over de werking van Richtlijn 2011/24/EU betreffende de toepassing
EUROPESE COMMISSIE Brussel, 21.9.2018 COM(2018) 651 final ANNEX BIJLAGE bij VERSLAG VAN DE COMMISSIE AAN HET EUROPEES PARLEMENT EN DE RAAD over de werking van Richtlijn 2011/24/EU betreffende de toepassing
NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
 BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN 1/7 Lidstaat Aanvrager of houder van de vergunning
BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN 1/7 Lidstaat Aanvrager of houder van de vergunning
EUROPESE UNIE HET EUROPEES PARLEMENT PE-CONS 3659/1/01 REV 1
 EUROPESE UNIE HET EUROPEES PARLEMENT DE RAAD Brussel, 27 mei 2002 2001/0138 (COD) LEX 311 PE-CONS 3659/1/01 REV 1 TRANS 181 PECOS 199 CODEC 1126 VERORDENING (EG) Nr. /2002 VAN HET EUROPEES PARLEMENT EN
EUROPESE UNIE HET EUROPEES PARLEMENT DE RAAD Brussel, 27 mei 2002 2001/0138 (COD) LEX 311 PE-CONS 3659/1/01 REV 1 TRANS 181 PECOS 199 CODEC 1126 VERORDENING (EG) Nr. /2002 VAN HET EUROPEES PARLEMENT EN
Farmaceutische vorm. Amoxicillin 40 mg Clavulanic acid 10 mg. Clavulanic acid 10 mg. Clavulanic acid 10 mg. Clavulanic acid 10 mg
 Bijlage I Lijst met nam, farmaceutische vorm, sterkte van het geesmiddel voor diergeeskundig gebruik, diersoort, toediingsweg, aanvrager/houder van de handelsvergunning in de lidstat 1/11 Lidstaat EU/EER
Bijlage I Lijst met nam, farmaceutische vorm, sterkte van het geesmiddel voor diergeeskundig gebruik, diersoort, toediingsweg, aanvrager/houder van de handelsvergunning in de lidstat 1/11 Lidstaat EU/EER
TRACTATENBLAD VAN HET
 34 (2007) Nr. 7 TRACTATENBLAD VAN HET KONINKRIJK DER NEDERLANDEN JAARGANG 2015 Nr. 4 A. TITEL Verdrag van Lissabon tot wijziging van het Verdrag betreffende de Europese Unie en het Verdrag tot oprichting
34 (2007) Nr. 7 TRACTATENBLAD VAN HET KONINKRIJK DER NEDERLANDEN JAARGANG 2015 Nr. 4 A. TITEL Verdrag van Lissabon tot wijziging van het Verdrag betreffende de Europese Unie en het Verdrag tot oprichting
Methylprednisolonwaterstofsuccinaat
 Bijlage I Lijst met namen, farmaceutische vormen, sterkten van de diergeneesmiddelen, diersoorten, toedieningswegen en aanvrager/houder van de vergunning voor het in de handel brengen in de lidstaten 1/7
Bijlage I Lijst met namen, farmaceutische vormen, sterkten van de diergeneesmiddelen, diersoorten, toedieningswegen en aanvrager/houder van de vergunning voor het in de handel brengen in de lidstaten 1/7
Voorstel voor een BESLUIT VAN DE RAAD. ter bepaling van de samenstelling van het Economisch en Sociaal Comité
 EUROPESE COMMISSIE Brussel, 11.6.2014 COM(2014) 227 final 2014/0129 (NLE) Voorstel voor een BESLUIT VAN DE RAAD ter bepaling van de samenstelling van het Economisch en Sociaal Comité NL NL TOELICHTING
EUROPESE COMMISSIE Brussel, 11.6.2014 COM(2014) 227 final 2014/0129 (NLE) Voorstel voor een BESLUIT VAN DE RAAD ter bepaling van de samenstelling van het Economisch en Sociaal Comité NL NL TOELICHTING
VERSLAG VAN DE COMMISSIE AAN HET EUROPEES PARLEMENT, DE RAAD, HET EUROPEES ECONOMISCH EN SOCIAAL COMITÉ EN HET COMITÉ VAN DE REGIO'S
 EUROPESE COMMISSIE Brussel, 17.6.2011 COM(2011) 352 definitief VERSLAG VAN DE COMMISSIE AAN HET EUROPEES PARLEMENT, DE RAAD, HET EUROPEES ECONOMISCH EN SOCIAAL COMITÉ EN HET COMITÉ VAN DE REGIO'S Tweede
EUROPESE COMMISSIE Brussel, 17.6.2011 COM(2011) 352 definitief VERSLAG VAN DE COMMISSIE AAN HET EUROPEES PARLEMENT, DE RAAD, HET EUROPEES ECONOMISCH EN SOCIAAL COMITÉ EN HET COMITÉ VAN DE REGIO'S Tweede
Aanvrager (Fantasie) Naam Sterkte Farmaceutische vorm. Actocalcio D3 35 mg mg/880 IU. Acrelcombi 35 mg mg/880 IU
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORMEN, STERKTEN VAN HET GENEESMIDDELEN, TOEDIENINGSWEG, AANVRAGERS, HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1 Lidstaat EU/EER Houder
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORMEN, STERKTEN VAN HET GENEESMIDDELEN, TOEDIENINGSWEG, AANVRAGERS, HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1 Lidstaat EU/EER Houder
Annex I. Lijst van namen, farmaceutische vorm, sterkten van het geneesmiddel, toedieningsweg en aanvrager in de Member States.
 Annex I Lijst van namen, farmaceutische vorm, sterkten van het geneesmiddel, toedieningsweg en aanvrager in de Member States. Lidstaat EU/EEA Aanvrager (Fantasienaam ) Naam Sterkte Farmaceutische vorm
Annex I Lijst van namen, farmaceutische vorm, sterkten van het geneesmiddel, toedieningsweg en aanvrager in de Member States. Lidstaat EU/EEA Aanvrager (Fantasienaam ) Naam Sterkte Farmaceutische vorm
doxycycline hyclate doxycycline hyclate doxycycline hyclate doxycycline hyclate doxycycline hyclate doxycycline hyclate doxycycline hyclate
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTEN VAN HET GENEESMIDDEL VOOR DIERGENEESKUNDIG GEBRUIK, DIERSOORTEN, TOEDIENINGSWEG, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTAAT
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTEN VAN HET GENEESMIDDEL VOOR DIERGENEESKUNDIG GEBRUIK, DIERSOORTEN, TOEDIENINGSWEG, HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTAAT
Bijlage I. Lijst van nationaal goedgekeurde geneesmiddelen en vergunningaanvragen
 Bijlage I Lijst van nationaal goedgekeurde geneesmiddelen en vergunningaanvragen 1 Bijlage IA: Geneesmiddelen aanbevolen voor handhaving en aanvragen van vergunningen voor het in de handel brengen waarvoor
Bijlage I Lijst van nationaal goedgekeurde geneesmiddelen en vergunningaanvragen 1 Bijlage IA: Geneesmiddelen aanbevolen voor handhaving en aanvragen van vergunningen voor het in de handel brengen waarvoor
***I STANDPUNT VAN HET EUROPEES PARLEMENT
 Europees Parlement 2014-2019 Geconsolideerd wetgevingsdocument 13.6.2017 EP-PE_TC1-COD(2016)0186 ***I STANDPUNT VAN HET EUROPEES PARLEMENT in eerste lezing vastgesteld op 13 juni 2017 met het oog op de
Europees Parlement 2014-2019 Geconsolideerd wetgevingsdocument 13.6.2017 EP-PE_TC1-COD(2016)0186 ***I STANDPUNT VAN HET EUROPEES PARLEMENT in eerste lezing vastgesteld op 13 juni 2017 met het oog op de
de heer Jordi AYET PUIGARNAU, directeur, namens de secretarisgeneraal van de Europese Commissie
 Raad van de Europese Unie Brussel, 23 mei 2017 (OR. en) 9601/17 ADD 4 JAI 537 ASIM 57 CO EUR-PREP 27 BEGELEIDENDE NOTA van: ingekomen: 17 mei 2017 aan: de heer Jordi AYET PUIGARNAU, directeur, namens de
Raad van de Europese Unie Brussel, 23 mei 2017 (OR. en) 9601/17 ADD 4 JAI 537 ASIM 57 CO EUR-PREP 27 BEGELEIDENDE NOTA van: ingekomen: 17 mei 2017 aan: de heer Jordi AYET PUIGARNAU, directeur, namens de
MEDEDELING VAN DE COMMISSIE
 EUROPESE COMMISSIE Brussel, XXX [ ](2013) XXX draft MEDEDELING VAN DE COMMISSIE Uitvoering van artikel 260 van het Verdrag betreffende de werking van de Europese Unie Aanpassing van de gegevens die worden
EUROPESE COMMISSIE Brussel, XXX [ ](2013) XXX draft MEDEDELING VAN DE COMMISSIE Uitvoering van artikel 260 van het Verdrag betreffende de werking van de Europese Unie Aanpassing van de gegevens die worden
I. VERZOEK OM INFORMATIE betreffende de transnationale terbeschikkingstelling van werknemers met het oog op het verrichten van diensten
 FORMULIER VOOR (FACULTATIEF) GEBRUIK DOOR DE OVERHEIDSINSTANTIE DIE OM INFORMATIE VERZOEKT I. VERZOEK OM INFORMATIE betreffende de transnationale terbeschikkingstelling van werknemers met het oog op het
FORMULIER VOOR (FACULTATIEF) GEBRUIK DOOR DE OVERHEIDSINSTANTIE DIE OM INFORMATIE VERZOEKT I. VERZOEK OM INFORMATIE betreffende de transnationale terbeschikkingstelling van werknemers met het oog op het
EUROPESE UNIE HET EUROPEES PARLEMENT
 EUROPESE UNIE HET EUROPEES PARLEMENT DE RAAD Brussel, 20 juni 2017 (OR. en) 2016/0186 (COD) PE-CONS 25/17 CULT 69 AELE 49 EEE 27 CODEC 867 WETGEVINGSBESLUITEN EN ANDERE INSTRUMENTEN Betreft: BESLUIT VAN
EUROPESE UNIE HET EUROPEES PARLEMENT DE RAAD Brussel, 20 juni 2017 (OR. en) 2016/0186 (COD) PE-CONS 25/17 CULT 69 AELE 49 EEE 27 CODEC 867 WETGEVINGSBESLUITEN EN ANDERE INSTRUMENTEN Betreft: BESLUIT VAN
Europese feestdagen 2017
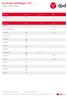 Januari - Februari - Maart Bestemming Januari Februari Maart Nederland (NL) 01-01 Bestemming Januari Februari Maart België (BE) 01-01 Bosnie en Herzegovina (BA) 01-03 Bulgarije (BG) 01-01 03-03 Denemarken
Januari - Februari - Maart Bestemming Januari Februari Maart Nederland (NL) 01-01 Bestemming Januari Februari Maart België (BE) 01-01 Bosnie en Herzegovina (BA) 01-03 Bulgarije (BG) 01-01 03-03 Denemarken
Europese feestdagen 2019
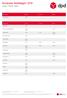 Januari - Februari - Maart Bestemming Januari Februari Maart Nederland (NL) 01-01 Bestemming Januari Februari Maart België (BE) 01-01 Bosnie en Herzegovina (BA) 01-01 02-01 01-03 Bulgarije (BG) 01-01 01-02
Januari - Februari - Maart Bestemming Januari Februari Maart Nederland (NL) 01-01 Bestemming Januari Februari Maart België (BE) 01-01 Bosnie en Herzegovina (BA) 01-01 02-01 01-03 Bulgarije (BG) 01-01 01-02
BIJLAGE I. Blz. 1 van 5
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET DIERGENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEG(EN), HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN Blz. 1 van 5 Lidstaat
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET DIERGENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEG(EN), HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN Blz. 1 van 5 Lidstaat
Europese feestdagen 2018
 Januari - Februari - Maart Bestemming Januari Februari Maart Nederland (NL) 01-01 Bestemming Januari Februari Maart België (BE) 01-01 Bosnie en Herzegovina (BA) 01-01 02-01 01-03 Bulgarije (BG) 01-01 03-03
Januari - Februari - Maart Bestemming Januari Februari Maart Nederland (NL) 01-01 Bestemming Januari Februari Maart België (BE) 01-01 Bosnie en Herzegovina (BA) 01-01 02-01 01-03 Bulgarije (BG) 01-01 03-03
Voorstel voor een BESLUIT VAN DE RAAD. ter bepaling van de samenstelling van het Comité van de Regio's
 EUROPESE COMMISSIE Brussel, 11.6.2014 COM(2014) 226 final 2014/0128 (NLE) Voorstel voor een BESLUIT VAN DE RAAD ter bepaling van de samenstelling van het Comité van de Regio's NL NL TOELICHTING 1. ACHTERGROND
EUROPESE COMMISSIE Brussel, 11.6.2014 COM(2014) 226 final 2014/0128 (NLE) Voorstel voor een BESLUIT VAN DE RAAD ter bepaling van de samenstelling van het Comité van de Regio's NL NL TOELICHTING 1. ACHTERGROND
Raad van de Europese Unie Brussel, 18 mei 2017 (OR. en)
 Raad van de Europese Unie Brussel, 18 mei 2017 (OR. en) 9438/17 ADD 1 MAP 12 BEGELEIDENDE NOTA van: ingekomen: 17 mei 2017 aan: de heer Jordi AYET PUIGARNAU, directeur, namens de secretaris-generaal van
Raad van de Europese Unie Brussel, 18 mei 2017 (OR. en) 9438/17 ADD 1 MAP 12 BEGELEIDENDE NOTA van: ingekomen: 17 mei 2017 aan: de heer Jordi AYET PUIGARNAU, directeur, namens de secretaris-generaal van
SAMENVATTING VAN DE PRODUCTKENMERKEN
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET DIERGENEESMIDDEL 50 mg/ml, orale suspensie voor biggen en kalveren. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Per ml: Werkzaam bestanddeel: Toltrazuril...50,0
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET DIERGENEESMIDDEL 50 mg/ml, orale suspensie voor biggen en kalveren. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Per ml: Werkzaam bestanddeel: Toltrazuril...50,0
Bijlage B4. Werken aan de start. Freek Bucx
 Bijlage B4 Werken aan de start Freek Bucx Inhoud Tabel B4.1... 3 Tabel B4.2... 5 Tabel B4.3... 6 Tabel B4.4... 7 Tabel B4.5... 8 Tabel B4.6... 9 Tabel B4.7... 10 Tabel B4.8... 11 Tabel B4.9... 12 Tabel
Bijlage B4 Werken aan de start Freek Bucx Inhoud Tabel B4.1... 3 Tabel B4.2... 5 Tabel B4.3... 6 Tabel B4.4... 7 Tabel B4.5... 8 Tabel B4.6... 9 Tabel B4.7... 10 Tabel B4.8... 11 Tabel B4.9... 12 Tabel
Algehele samenvatting van de wetenschappelijke beoordeling van nimesulidebevattende geneesmiddelen voor systemisch gebruik (zie bijlage I)
 Bijlage II Wetenschappelijke conclusies en redenen voor de wijzigingen van de samenvatting van de productkenmerken en de bijsluiter, opgesteld door het EMA 42 Wetenschappelijke conclusies Algehele samenvatting
Bijlage II Wetenschappelijke conclusies en redenen voor de wijzigingen van de samenvatting van de productkenmerken en de bijsluiter, opgesteld door het EMA 42 Wetenschappelijke conclusies Algehele samenvatting
Wetenschappelijke conclusies
 Bijlage II Wetenschappelijke conclusies en redenen voor het positieve advies voor de handelsvergunning mits aan de voorwaarden wordt voldaan, en voor de wijziging van de samenvatting van de productkenmerken
Bijlage II Wetenschappelijke conclusies en redenen voor het positieve advies voor de handelsvergunning mits aan de voorwaarden wordt voldaan, en voor de wijziging van de samenvatting van de productkenmerken
Bijlage B4. Eerste treden op de arbeidsmarkt. Freek Bucx
 Bijlage B4 Eerste treden op de arbeidsmarkt Freek Bucx Inhoud Tabel B4.1... 3 Tabel B4.2... 4 Tabel B4.3... 5 Tabel B4.4... 6 Tabel B4.5... 7 Tabel B4.6... 8 Bijlage B4 Eerste treden op de arbeidsmarkt
Bijlage B4 Eerste treden op de arbeidsmarkt Freek Bucx Inhoud Tabel B4.1... 3 Tabel B4.2... 4 Tabel B4.3... 5 Tabel B4.4... 6 Tabel B4.5... 7 Tabel B4.6... 8 Bijlage B4 Eerste treden op de arbeidsmarkt
Aanvrager (Fantasie)naam Sterkte Farmaceutische vorm. Vertimen 8 mg Tabletten. Vertimen 16 mg Tabletten. Vertisan 16 mg Таблетка
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM(EN), STERKTE(N) VAN HET (DE) GENEESMIDDEL(LEN), TOEDIENINGSWEG(EN), AANVRAGER(S), HOUDER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM(EN), STERKTE(N) VAN HET (DE) GENEESMIDDEL(LEN), TOEDIENINGSWEG(EN), AANVRAGER(S), HOUDER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN
Lidstaat Houder van de vergunning voor het in de handel brengen Fantasienaam Sterkte Farmaceutische vorm Toedieningswijze SIMVASTATIN BMM PHARMA
 BIJLAGE I LIJST VAN DE NAMEN, FARMACEUTISCHE VORMEN, STERKTES VAN DE GENEESMIDDELEN, TOEDIENINGSWIJZE EN HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1 Lidstaat Houder van de
BIJLAGE I LIJST VAN DE NAMEN, FARMACEUTISCHE VORMEN, STERKTES VAN DE GENEESMIDDELEN, TOEDIENINGSWIJZE EN HOUDERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN 1 Lidstaat Houder van de
14072/14 roe/lep/hh DG C 1
 Raad van de Europese Unie Brussel, 13 oktober 2014 (OR. en) Interinstitutioneel dossier: 2014/0292 (E) 14072/14 ACP 154 FIN 727 PTOM 45 WETGEVINGSBESLUITEN EN ANDERE INSTRUMENTEN Betreft: Besluit van de
Raad van de Europese Unie Brussel, 13 oktober 2014 (OR. en) Interinstitutioneel dossier: 2014/0292 (E) 14072/14 ACP 154 FIN 727 PTOM 45 WETGEVINGSBESLUITEN EN ANDERE INSTRUMENTEN Betreft: Besluit van de
21.10.2015 A8-0249/139. Door de Commissie voorgestelde tekst
 21.10.2015 A8-0249/139 139 Jens Rohde e.a. Artikel 4 lid 1 1. De lidstaten beperken op zijn minst hun jaarlijkse antropogene emissies van zwaveldioxide (SO2), stikstofoxiden (NOx), vluchtige organische
21.10.2015 A8-0249/139 139 Jens Rohde e.a. Artikel 4 lid 1 1. De lidstaten beperken op zijn minst hun jaarlijkse antropogene emissies van zwaveldioxide (SO2), stikstofoxiden (NOx), vluchtige organische
Sterkte Diersoorten Frequentie van toediening en toedieningsweg
 Bijlage I Lijst met namen, farmaceutische vorm, sterkte van het diergeneesmiddel, diersoorten, toedieningsweg(en), houder van de vergunning voor het in de handel brengen in de lidstaten 1/7 Lidstaat Aanvrager
Bijlage I Lijst met namen, farmaceutische vorm, sterkte van het diergeneesmiddel, diersoorten, toedieningsweg(en), houder van de vergunning voor het in de handel brengen in de lidstaten 1/7 Lidstaat Aanvrager
Zuivelproductie per land 2015 Dairy production by country
 Zuivelproductie per land 2015 Melkaanvoer en productie EU-28 2015 Milk deliveries and production EU-28 index: 2014=100 EU-28 jan feb mrt apr mei jun jul aug sep okt nov dec cumulatief index Melkaanvoer
Zuivelproductie per land 2015 Melkaanvoer en productie EU-28 2015 Milk deliveries and production EU-28 index: 2014=100 EU-28 jan feb mrt apr mei jun jul aug sep okt nov dec cumulatief index Melkaanvoer
BIJLAGE. bij VERSLAG VAN DE COMMISSIE AAN HET EUROPEES PARLEMENT, DE RAAD, HET EUROPEES ECONOMISCH EN SOCIAAL COMITÉ EN HET COMITÉ VAN DE REGIO'S
 EUROPESE COMMISSIE Brussel, 9.2.28 COM(28) 86 final ANNEXES to 3 BIJLAGE bij VERSLAG VAN DE COMMISSIE AAN HET EUROPEES PARLEMENT, DE RAAD, HET EUROPEES ECONOMISCH EN SOCIAAL COMITÉ EN HET COMITÉ VAN DE
EUROPESE COMMISSIE Brussel, 9.2.28 COM(28) 86 final ANNEXES to 3 BIJLAGE bij VERSLAG VAN DE COMMISSIE AAN HET EUROPEES PARLEMENT, DE RAAD, HET EUROPEES ECONOMISCH EN SOCIAAL COMITÉ EN HET COMITÉ VAN DE
SAMENVATTING VAN DE PRODUCTKENMERKEN. TOLRACOL 50 mg/ml suspensie voor oraal gebruik voor varkens, runderen en schapen
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET DIERGENEESMIDDEL TOLRACOL 50 mg/ml suspensie voor oraal gebruik voor varkens, runderen en schapen 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET DIERGENEESMIDDEL TOLRACOL 50 mg/ml suspensie voor oraal gebruik voor varkens, runderen en schapen 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml
TRACTATENBLAD VAN HET
 66 (1991) Nr. 6 TRACTATENBLAD VAN HET KONINKRIJK DER NEDERLANDEN JAARGANG 2014 Nr. 39 A. TITEL Overeenkomst betreffende samenwerking en een douane-unie tussen de Europese Gemeenschap en haar lidstaten,
66 (1991) Nr. 6 TRACTATENBLAD VAN HET KONINKRIJK DER NEDERLANDEN JAARGANG 2014 Nr. 39 A. TITEL Overeenkomst betreffende samenwerking en een douane-unie tussen de Europese Gemeenschap en haar lidstaten,
Bijlage VMBO-GL en TL
 Bijlage VMBO-GL en TL 2015 tijdvak 2 economie CSE GL en TL GT-0233-a-15-2-b Zelfstandig of niet informatiebron 1 Cijfers Kamer van Koophandel over 2013 Starters 113.823 Bedrijfsbeëindigingen 136.640 informatiebron
Bijlage VMBO-GL en TL 2015 tijdvak 2 economie CSE GL en TL GT-0233-a-15-2-b Zelfstandig of niet informatiebron 1 Cijfers Kamer van Koophandel over 2013 Starters 113.823 Bedrijfsbeëindigingen 136.640 informatiebron
BIJLAGE. bij het. Voorstel voor een besluit van de Raad
 EUROPESE COMMISSIE Brussel, 18.2.2016 COM(2016) 70 final ANNEX 1 BIJLAGE bij het Voorstel voor een besluit van de Raad betreffende de ondertekening, namens de Europese Unie en haar lidstaten, van het protocol
EUROPESE COMMISSIE Brussel, 18.2.2016 COM(2016) 70 final ANNEX 1 BIJLAGE bij het Voorstel voor een besluit van de Raad betreffende de ondertekening, namens de Europese Unie en haar lidstaten, van het protocol
TRACTATENBLAD VAN HET
 36 (2010) Nr. 2 TRACTATENBLAD VAN HET KONINKRIJK DER NEDERLANDEN JAARGANG 2015 Nr. 24 A. TITEL Overeenkomst tussen de Europese Unie en haar lidstaten, enerzijds, en Georgië, anderzijds, betreffende een
36 (2010) Nr. 2 TRACTATENBLAD VAN HET KONINKRIJK DER NEDERLANDEN JAARGANG 2015 Nr. 24 A. TITEL Overeenkomst tussen de Europese Unie en haar lidstaten, enerzijds, en Georgië, anderzijds, betreffende een
UITVOERINGSBESLUIT VAN DE COMMISSIE. van
 EUROPESE COMMISSIE Brussel, 29.4.2014 C(2014) 2737 final UITVOERINGSBESLUIT VAN DE COMMISSIE van 29.4.2014 tot vaststelling van de lijst van bewijsstukken die door visumaanvragers moeten worden overgelegd
EUROPESE COMMISSIE Brussel, 29.4.2014 C(2014) 2737 final UITVOERINGSBESLUIT VAN DE COMMISSIE van 29.4.2014 tot vaststelling van de lijst van bewijsstukken die door visumaanvragers moeten worden overgelegd
UITVOERINGSBESLUIT VAN DE COMMISSIE
 13.12.2013 Publicatieblad van de Europese Unie L 334/37 UITVOERINGSBESLUIT VAN DE COMMISSIE van 11 december 2013 tot wijziging van Besluit 2012/226/EU betreffende de tweede reeks gemeenschappelijke veiligheidsdoelen
13.12.2013 Publicatieblad van de Europese Unie L 334/37 UITVOERINGSBESLUIT VAN DE COMMISSIE van 11 december 2013 tot wijziging van Besluit 2012/226/EU betreffende de tweede reeks gemeenschappelijke veiligheidsdoelen
Raad van de Europese Unie Brussel, 29 oktober 2014 (OR. en)
 Raad van de Europese Unie Brussel, 29 oktober 2014 (OR. en) Interinstitutioneel dossier: 2014/0298 (E) 14563/14 ACP 166 FIN 764 PTOM 51 WETGEVINGSBESLUITEN EN ANDERE INSTRUMENTEN Betreft: Besluit van de
Raad van de Europese Unie Brussel, 29 oktober 2014 (OR. en) Interinstitutioneel dossier: 2014/0298 (E) 14563/14 ACP 166 FIN 764 PTOM 51 WETGEVINGSBESLUITEN EN ANDERE INSTRUMENTEN Betreft: Besluit van de
PGI 2. Europese Raad Brussel, 19 juni 2018 (OR. en) EUCO 7/1/18 REV 1
 Europese Raad Brussel, 19 juni 2018 (OR. en) Interinstitutionele dossiers: 2017/0900 (E) 2013/0900 (E) EUCO 7/1/18 REV 1 INST 92 POLGEN 23 CO EUR 8 RECHTSHANDELINGEN Betreft: BESLUIT VAN DE EUROPESE RAAD
Europese Raad Brussel, 19 juni 2018 (OR. en) Interinstitutionele dossiers: 2017/0900 (E) 2013/0900 (E) EUCO 7/1/18 REV 1 INST 92 POLGEN 23 CO EUR 8 RECHTSHANDELINGEN Betreft: BESLUIT VAN DE EUROPESE RAAD
Leflunomid Actavis 20 mg Filmtabletten LEFLUNOMID ACTAVIS 20 MG. Leflunomide Actavis 100 mg, filmomhulde
 Bijlage I Lijst met namen, farmaceutische vorm, sterkte van het geneesmiddel, toedieningsweg en houder van de vergunning voor het in de handel brengen in de lidstaten 1 Lidstaat EU/EEA Houder van de vergunning
Bijlage I Lijst met namen, farmaceutische vorm, sterkte van het geneesmiddel, toedieningsweg en houder van de vergunning voor het in de handel brengen in de lidstaten 1 Lidstaat EU/EEA Houder van de vergunning
Arbeidsmarkt allochtonen
 Streekpact 2013-2018 Cijferanalyse Publicatiedatum: 30 september 2013 Contactpersoon: Kim Nevelsteen Arbeidsmarkt allochtonen Samenvatting 1.176 werkzoekende allochtone Kempenaren (2012) vaak man meestal
Streekpact 2013-2018 Cijferanalyse Publicatiedatum: 30 september 2013 Contactpersoon: Kim Nevelsteen Arbeidsmarkt allochtonen Samenvatting 1.176 werkzoekende allochtone Kempenaren (2012) vaak man meestal
Bijlage I Lijst met namen, farmaceutische vormen, concentraties van de diergeneesmiddelen, doeldieren, toedieningsweg, aanvrager in de Lidstaten
 Bijlage I Lijst met namen, farmaceutische vormen, concentraties van de diergeneesmiddelen, doeldieren, toedieningsweg, aanvrager in de Lidstaten 1/13 EU/EEA Lidstaat Aanvrager Naam INN Concentra tie Farmaceutische
Bijlage I Lijst met namen, farmaceutische vormen, concentraties van de diergeneesmiddelen, doeldieren, toedieningsweg, aanvrager in de Lidstaten 1/13 EU/EEA Lidstaat Aanvrager Naam INN Concentra tie Farmaceutische
Levend infectieuzebursitisvirus,
 BIJLAGE I DE NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET DIERGENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEG, AANBEVOLEN DOSIS, WACHTTIJD, AANVRAGER/HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN
BIJLAGE I DE NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET DIERGENEESMIDDEL, DIERSOORTEN, TOEDIENINGSWEG, AANBEVOLEN DOSIS, WACHTTIJD, AANVRAGER/HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN IN
DE HERSCHIKTE EOR RICHTLIJN
 DE HERSCHIKTE EOR RICHTLIJN EOR reglementering : drie wettelijke documenten de richtlijnen 1994/45 en 2009/38 de omzetting in nationale wetgeving uw akkoord 2 2009/38? akkoorden getekend na 5.06.2011 ongewijzigde
DE HERSCHIKTE EOR RICHTLIJN EOR reglementering : drie wettelijke documenten de richtlijnen 1994/45 en 2009/38 de omzetting in nationale wetgeving uw akkoord 2 2009/38? akkoorden getekend na 5.06.2011 ongewijzigde
Additioneel reglement 1. Slotbepalingen (art. 8-9) Bijlage I - Lijst bedoeld in artikel 2, eerste alinea
 Additioneel reglement 1 Samenvatting Hoofdstuk I - Van de rogatoire commissies (art. 1-3)...000 Hoofdstuk II - Van de toelating om kosteloos te procederen (art. 4-5)...000 Hoofdstuk III - Van aangifte
Additioneel reglement 1 Samenvatting Hoofdstuk I - Van de rogatoire commissies (art. 1-3)...000 Hoofdstuk II - Van de toelating om kosteloos te procederen (art. 4-5)...000 Hoofdstuk III - Van aangifte
Vantas 50 mg Implantaat Subcutaan 50 mg Ireland Ltd North Wall Quay, Dublin, Ierland Duitsland Valera
 BIJLAGE I LIJST MET DE NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, AANVRAGER EN VERGUNNINGHOUDER VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN Lidstaat Houder van de vergunning
BIJLAGE I LIJST MET DE NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, AANVRAGER EN VERGUNNINGHOUDER VOOR HET IN DE HANDEL BRENGEN IN DE LIDSTATEN Lidstaat Houder van de vergunning
Herziening NEC-richtlijn. LNE Afdeling Lucht, Hinder, Risicobeheer, Milieu & Gezondheid
 Herziening NEC-richtlijn LNE Afdeling Lucht, Hinder, Risicobeheer, Milieu & Gezondheid Inhoud presentatie Huidige NEC-richtlijn Herziening NEC-richtlijn: motivatie Inhoud herziene NEC-richtlijn: Overzicht
Herziening NEC-richtlijn LNE Afdeling Lucht, Hinder, Risicobeheer, Milieu & Gezondheid Inhoud presentatie Huidige NEC-richtlijn Herziening NEC-richtlijn: motivatie Inhoud herziene NEC-richtlijn: Overzicht
BIJLAGE PROTOCOL. bij het. voorstel voor een besluit van de Raad
 EUROPESE COMMISSIE Brussel, 26.2.2016 COM(2016) 91 final ANNEX 1 BIJLAGE PROTOCOL bij het voorstel voor een besluit van de Raad betreffende de sluiting, namens de Europese Unie en haar lidstaten, van het
EUROPESE COMMISSIE Brussel, 26.2.2016 COM(2016) 91 final ANNEX 1 BIJLAGE PROTOCOL bij het voorstel voor een besluit van de Raad betreffende de sluiting, namens de Europese Unie en haar lidstaten, van het
TRACTATENBLAD VAN HET. JAARGANG 2009 Nr. 199
 67 (1999) Nr. 9 TRACTATENBLAD VAN HET KONINKRIJK DER NEDERLANDEN JAARGANG 2009 Nr. 199 A. TITEL Overeenkomst tussen de Europese Gemeenschap en haar lidstaten, enerzijds, en de Zwitserse Bondsstaat, anderzijds,
67 (1999) Nr. 9 TRACTATENBLAD VAN HET KONINKRIJK DER NEDERLANDEN JAARGANG 2009 Nr. 199 A. TITEL Overeenkomst tussen de Europese Gemeenschap en haar lidstaten, enerzijds, en de Zwitserse Bondsstaat, anderzijds,
HET KONINKRIJK BELGIË, DE REPUBLIEK BULGARIJE, DE TSJECHISCHE REPUBLIEK, HET KONINKRIJK DENEMARKEN, DE BONDSREPUBLIEK DUITSLAND, DE REPUBLIEK ESTLAND,
 PROTOCOL TOT WIJZIGING VAN HET AAN HET VERDRAG BETREFFENDE DE EUROPESE UNIE, HET VERDRAG BETREFFENDE DE WERKING VAN DE EUROPESE UNIE EN HET VERDRAG TOT OPRICHTING VAN DE EUROPESE GEMEENSCHAP VOOR ATOOMENERGIE
PROTOCOL TOT WIJZIGING VAN HET AAN HET VERDRAG BETREFFENDE DE EUROPESE UNIE, HET VERDRAG BETREFFENDE DE WERKING VAN DE EUROPESE UNIE EN HET VERDRAG TOT OPRICHTING VAN DE EUROPESE GEMEENSCHAP VOOR ATOOMENERGIE
Product Maximumformaat Maximumgewicht
 Pakketten moeten bij Fietskoeriers.nl voldoen aan de volgende specificaties. Product Maximumformaat Maximumgewicht Pakket 60x60x40 cm 10 kg Brievenbuspakket 28x26,5x3,2 cm 2 kg Pakket XL 180x100x50 cm*
Pakketten moeten bij Fietskoeriers.nl voldoen aan de volgende specificaties. Product Maximumformaat Maximumgewicht Pakket 60x60x40 cm 10 kg Brievenbuspakket 28x26,5x3,2 cm 2 kg Pakket XL 180x100x50 cm*
TRACTATENBLAD VAN HET KONINKRIJK DER NEDERLANDEN. JAARGANG 2015 Nr. 70
 13 (2013) Nr. 2 TRACTATENBLAD VAN HET KONINKRIJK DER NEDERLANDEN JAARGANG 2015 Nr. 70 A. TITEL Euro-mediterrane luchtvaartovereenkomst tussen de Europese Unie en haar lidstaten, enerzijds, en de regering
13 (2013) Nr. 2 TRACTATENBLAD VAN HET KONINKRIJK DER NEDERLANDEN JAARGANG 2015 Nr. 70 A. TITEL Euro-mediterrane luchtvaartovereenkomst tussen de Europese Unie en haar lidstaten, enerzijds, en de regering
SLOTAKTE. AF/EEE/XPA/nl 1
 SLOTAKTE AF/EEE/XPA/nl 1 De gevolmachtigden van: DE EUROPESE GEMEENSCHAP, hierna "de Gemeenschap" te noemen, en van HET KONINKRIJK BELGIË, HET KONINKRIJK DENEMARKEN, DE BONDSREPUBLIEK DUITSLAND, DE HELLEENSE
SLOTAKTE AF/EEE/XPA/nl 1 De gevolmachtigden van: DE EUROPESE GEMEENSCHAP, hierna "de Gemeenschap" te noemen, en van HET KONINKRIJK BELGIË, HET KONINKRIJK DENEMARKEN, DE BONDSREPUBLIEK DUITSLAND, DE HELLEENSE
BESLUIT VAN DE COMMISSIE
 27.4.2012 Publicatieblad van de Europese Unie L 115/27 BESLUIT VAN DE COMMISSIE van 23 april 2012 betreffende de tweede reeks gemeenschappelijke veiligheidsdoelen voor het spoorwegsysteem (Kennisgeving
27.4.2012 Publicatieblad van de Europese Unie L 115/27 BESLUIT VAN DE COMMISSIE van 23 april 2012 betreffende de tweede reeks gemeenschappelijke veiligheidsdoelen voor het spoorwegsysteem (Kennisgeving
Thema 2 Om ons heen. Samenvatting. Meander Samenvatting groep 7. Landschappen. Klimaten. Samenwerking. de regering. Onder de loep.
 Meander Samenvatting groep 7 Thema 2 Om ons heen Samenvatting Landschappen Landschappen in Europa zijn heel verschillend. Nederland is een heel vlak land. Frankrijk is een land met heuvels en bergen. Zweden
Meander Samenvatting groep 7 Thema 2 Om ons heen Samenvatting Landschappen Landschappen in Europa zijn heel verschillend. Nederland is een heel vlak land. Frankrijk is een land met heuvels en bergen. Zweden
"Culturele Hoofdstad van Europa" voor het tijdvak 2005 tot 2019 ***I
 P5_TA(2004)0361 "Culturele Hoofdstad van Europa" voor het tijdvak 2005 tot 2019 ***I Wetgevingsresolutie van het Europees Parlement over het voorstel voor een besluit van het Europees Parlement en de Raad
P5_TA(2004)0361 "Culturele Hoofdstad van Europa" voor het tijdvak 2005 tot 2019 ***I Wetgevingsresolutie van het Europees Parlement over het voorstel voor een besluit van het Europees Parlement en de Raad
RAAD VAN DE EUROPESE UNIE. Brussel, 26 november 2003 (27.11) (OR. fr) 15314/03 Interinstitutioneel dossier: 2003/0274 (COD) CULT 66 CODEC 1678
 RAAD VAN DE EUROPESE UNIE Brussel, 26 november 2003 (27.11) (OR. fr) 15314/03 Interinstitutioneel dossier: 2003/0274 (COD) CULT 66 CODEC 1678 VOORSTEL van: de Europese Commissie d.d.: 18 november 2003
RAAD VAN DE EUROPESE UNIE Brussel, 26 november 2003 (27.11) (OR. fr) 15314/03 Interinstitutioneel dossier: 2003/0274 (COD) CULT 66 CODEC 1678 VOORSTEL van: de Europese Commissie d.d.: 18 november 2003
Samenstelling van het Europees Parlement met het oog op de verkiezingen van 2014
 P7_TA(2013)0082 Samenstelling van het Europees Parlement met het oog op de verkiezingen van 2014 Resolutie van het Europees Parlement van 13 maart 2013 over de samenstelling van het Europees Parlement
P7_TA(2013)0082 Samenstelling van het Europees Parlement met het oog op de verkiezingen van 2014 Resolutie van het Europees Parlement van 13 maart 2013 over de samenstelling van het Europees Parlement
Berekening zorgtoeslag 2013
 Toeslagen Belastingdienst Berekening zorgtoeslag 2013 ib 998 - ib*7pl Berekening zorgtoeslag 2013 De zorgtoeslag is een bijdrage in de kosten van de zorgverzekering. Of en hoeveel zorgtoeslag uw klant
Toeslagen Belastingdienst Berekening zorgtoeslag 2013 ib 998 - ib*7pl Berekening zorgtoeslag 2013 De zorgtoeslag is een bijdrage in de kosten van de zorgverzekering. Of en hoeveel zorgtoeslag uw klant
Toeslagen Belastingdienst. Berekening zorgtoeslag 2018
 Toeslagen Belastingdienst Berekening zorgtoeslag 2018 De zorgtoeslag is een bijdrage in de kosten van de zorgverzekering. Of en hoeveel zorgtoeslag uw klant krijgt, hangt af van: de standaardpremie de
Toeslagen Belastingdienst Berekening zorgtoeslag 2018 De zorgtoeslag is een bijdrage in de kosten van de zorgverzekering. Of en hoeveel zorgtoeslag uw klant krijgt, hangt af van: de standaardpremie de
Docentenvel opdracht 18 (De grote klimaat- en Europa- quiz)
 Docentenvel opdracht 18 (De grote klimaat- en Europa- quiz) Lees ter voorbereiding de volgende teksten en bekijk de vragen en antwoorden van de quiz. De juiste antwoorden zijn vetgedrukt. Wat wil en doet
Docentenvel opdracht 18 (De grote klimaat- en Europa- quiz) Lees ter voorbereiding de volgende teksten en bekijk de vragen en antwoorden van de quiz. De juiste antwoorden zijn vetgedrukt. Wat wil en doet
DE STAATSSECRETARIS VAN ECONOMISCHE ZAKEN, In overeenstemming met de MINISTER VAN VOLKSGEZONDHEID, WELZIJN EN SPORT,
 BD/2015/REG NL 114467/zaak 450281 DE STAATSSECRETARIS VAN ECONOMISCHE ZAKEN, In overeenstemming met de MINISTER VAN VOLKSGEZONDHEID, WELZIJN EN SPORT, Gezien het verzoek van Krka d.d., Novo mesto te Novo
BD/2015/REG NL 114467/zaak 450281 DE STAATSSECRETARIS VAN ECONOMISCHE ZAKEN, In overeenstemming met de MINISTER VAN VOLKSGEZONDHEID, WELZIJN EN SPORT, Gezien het verzoek van Krka d.d., Novo mesto te Novo
Dit document vormt slechts een documentatiehulpmiddel en verschijnt buiten de verantwoordelijkheid van de instellingen
 2012D0226 NL 13.12.2013 001.001 1 Dit document vormt slechts een documentatiehulpmiddel en verschijnt buiten de verantwoordelijkheid van de instellingen B BESLUIT VAN DE COMMISSIE van 23 april 2012 betreffende
2012D0226 NL 13.12.2013 001.001 1 Dit document vormt slechts een documentatiehulpmiddel en verschijnt buiten de verantwoordelijkheid van de instellingen B BESLUIT VAN DE COMMISSIE van 23 april 2012 betreffende
DE STAATSSECRETARIS VAN ECONOMISCHE ZAKEN, In overeenstemming met de MINISTER VAN VOLKSGEZONDHEID, WELZIJN EN SPORT,
 BD/2017/REG NL 110949/zaak 528717 DE STAATSSECRETARIS VAN ECONOMISCHE ZAKEN, In overeenstemming met de MINISTER VAN VOLKSGEZONDHEID, WELZIJN EN SPORT, Gezien het verzoek van LAVET Pharmaceuticals Ltd te
BD/2017/REG NL 110949/zaak 528717 DE STAATSSECRETARIS VAN ECONOMISCHE ZAKEN, In overeenstemming met de MINISTER VAN VOLKSGEZONDHEID, WELZIJN EN SPORT, Gezien het verzoek van LAVET Pharmaceuticals Ltd te
Gezondheid: uw Europese ziekteverzekeringskaart altijd mee op vakantie?
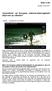 MEMO/11/406 Brussel, 16 juni 2011 Gezondheid: uw Europese ziekteverzekeringskaart altijd mee op vakantie? Vakantie verwacht het onverwachte. Gaat u binnenkort op reis in de EU of naar IJsland, Liechtenstein,
MEMO/11/406 Brussel, 16 juni 2011 Gezondheid: uw Europese ziekteverzekeringskaart altijd mee op vakantie? Vakantie verwacht het onverwachte. Gaat u binnenkort op reis in de EU of naar IJsland, Liechtenstein,
COMMISSIE VAN DE EUROPESE GEMEENSCHAPPEN. Voorstel voor een BESCHIKKING VAN DE RAAD
 COMMISSIE VAN DE EUROPESE GEMEENSCHAPPEN Brussel, 16.5.2007 COM(2007) 256 definitief 2007/0090 (CNS) Voorstel voor een BESCHIKKING VAN DE RAAD overeenkomstig artikel 122, lid 2, van het Verdrag betreffende
COMMISSIE VAN DE EUROPESE GEMEENSCHAPPEN Brussel, 16.5.2007 COM(2007) 256 definitief 2007/0090 (CNS) Voorstel voor een BESCHIKKING VAN DE RAAD overeenkomstig artikel 122, lid 2, van het Verdrag betreffende
Instructie aanvraag verblijfsvergunning voor deelname EVS
 Instructie aanvraag verblijfsvergunning voor deelname EVS Wanneer gebruiken? Deze instructie is alleen van nut indien u een aanvraag wilt indienen voor een jongere die langer dan 3 maanden in Nederland
Instructie aanvraag verblijfsvergunning voor deelname EVS Wanneer gebruiken? Deze instructie is alleen van nut indien u een aanvraag wilt indienen voor een jongere die langer dan 3 maanden in Nederland
BIJLAGE. bij. Voorstel voor een Besluit van de Raad
 EUROPESE COMMISSIE Brussel, 3.8.2017 COM(2017) 412 final ANNEX 1 BIJLAGE bij Voorstel voor een Besluit van de Raad betreffende de ondertekening, namens de Europese Unie en haar lidstaten, en de voorlopige
EUROPESE COMMISSIE Brussel, 3.8.2017 COM(2017) 412 final ANNEX 1 BIJLAGE bij Voorstel voor een Besluit van de Raad betreffende de ondertekening, namens de Europese Unie en haar lidstaten, en de voorlopige
Sabine Heijning. het Notarieel Bureau. voor vragen:
 Sabine Heijning het Notarieel Bureau www.hetnb.nl voor vragen: ipr@hetnb.nl De Verordening in de tijd Nalatenschap opengevallen vóór of na 17 augustus 2015 Wanneer oud ipr toepassen? Welk ipr? Wat valt
Sabine Heijning het Notarieel Bureau www.hetnb.nl voor vragen: ipr@hetnb.nl De Verordening in de tijd Nalatenschap opengevallen vóór of na 17 augustus 2015 Wanneer oud ipr toepassen? Welk ipr? Wat valt
Tweede Kamer der Staten-Generaal
 Tweede Kamer der Staten-Generaal 2 Vergaderjaar 2015 2016 21 501-07 Raad voor Economische en Financiële Zaken Nr. 1317 BRIEF VAN DE MINISTER VAN FINANCIËN Aan de Voorzitter van de Tweede Kamer der Staten-Generaal
Tweede Kamer der Staten-Generaal 2 Vergaderjaar 2015 2016 21 501-07 Raad voor Economische en Financiële Zaken Nr. 1317 BRIEF VAN DE MINISTER VAN FINANCIËN Aan de Voorzitter van de Tweede Kamer der Staten-Generaal
UITVOERINGSBESLUIT VAN DE COMMISSIE. van
 EUROPESE COMMISSIE Brussel, 6.6.2016 C(2016) 3347 final UITVOERINGSBESLUIT VAN DE COMMISSIE van 6.6.2016 tot vaststelling van de lijst van bewijsstukken die visumaanvragers moeten verstrekken in Iran,
EUROPESE COMMISSIE Brussel, 6.6.2016 C(2016) 3347 final UITVOERINGSBESLUIT VAN DE COMMISSIE van 6.6.2016 tot vaststelling van de lijst van bewijsstukken die visumaanvragers moeten verstrekken in Iran,
2.2. EUROPESE UNIE Droogte remt groei melkaanvoer af. Melkaanvoer per lidstaat (kalenderjaren) (1.000 ton) % 18/17
 2.2. EUROPESE UNIE 2.2.1. Droogte remt groei melkaanvoer af Melkaanvoer per lidstaat (kalenderjaren) (1.000 ton) 2005 2015 2017 2018 % 18/17 België 3 022 3 988 4 025 4 190 4,1 Denemarken 4 451 5 278 5
2.2. EUROPESE UNIE 2.2.1. Droogte remt groei melkaanvoer af Melkaanvoer per lidstaat (kalenderjaren) (1.000 ton) 2005 2015 2017 2018 % 18/17 België 3 022 3 988 4 025 4 190 4,1 Denemarken 4 451 5 278 5
RAAD VAN DE EUROPESE UNIE. Brussel, 3 november 2004 (05.11) (OR. en) 14028/04 EUROPOL 50 JAI 409
 RAAD VAN DE EUROPESE UNIE Brussel, 3 november 2004 (05.11) (OR. en) 14028/04 EUROPOL 50 JAI 409 NOTA van: de Franse, de Duitse, de Italiaanse, de Spaanse en de Britse delegatie aan: het Comité van artikel
RAAD VAN DE EUROPESE UNIE Brussel, 3 november 2004 (05.11) (OR. en) 14028/04 EUROPOL 50 JAI 409 NOTA van: de Franse, de Duitse, de Italiaanse, de Spaanse en de Britse delegatie aan: het Comité van artikel
Tariefplan: Kruidvat Mobiel voor 1 juli Nationaal
 Tariefplan: Kruidvat Mobiel voor 1 juli 2013 Je kan niet meer naar dit tariefplan overstappen. Nationaal Bellen in Nederland Prijs in Euro Duur * Vaste net Kruidvat Mobiel 0,05 Per minuut mobiel van andere
Tariefplan: Kruidvat Mobiel voor 1 juli 2013 Je kan niet meer naar dit tariefplan overstappen. Nationaal Bellen in Nederland Prijs in Euro Duur * Vaste net Kruidvat Mobiel 0,05 Per minuut mobiel van andere
