Bijlage II. Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning voor het in de handel brengen
|
|
|
- Casper Aerts
- 7 jaren geleden
- Aantal bezoeken:
Transcriptie
1 Bijlage II Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning voor het in de handel brengen 7
2 Wetenschappelijke conclusies Algehele samenvatting van de wetenschappelijke beoordeling van Nasonex en verwante namen (zie bijlage I) De werkzame stof van Nasonex, mometasonfuroaatmonohydraat, is een synthetische, 17- heterocyclische corticosteroïde met een ontstekingsremmende werking. Nasonex-neusspray 50 mcg is een handpompverstuiver voor toediening van afgemeten doses neusspray die een waterige suspensie van mometasonfuroaatmonohydraat bevat overeenkomend met 0,05% gewichtsprocent mometasonfuroaat, in een waterig medium dat glycerine, microkristallijne cellulose en natriumcarboxymethylcellulose, natriumcitraat, citroenzuur, benzalkoniumchloride en polysorbaat 80 bevat. Nasonex wordt in de volgende EU-lidstaten in de handel gebracht: België, Bulgarije, Denemarken, Duitsland, Estland, Finland, Frankrijk, Griekenland, Hongarije, Ierland, Italië, Letland, Litouwen, Luxemburg, Malta, Nederland, Oostenrijk, Polen, Portugal, Roemenië, Slovenië, Slowakije, Spanje, Tsjechië, het Verenigd Koninkrijk en Zweden, alsook in IJsland en Noorwegen. Nasonex is momenteel niet geregistreerd in Cyprus. Het werd in 16 Europese landen goedgekeurd via de nationale procedure en in 13 lidstaten via de procedure van wederzijdse erkenning, met het Verenigd Koninkrijk als rapporterende lidstaat. Vanwege de verschillende beslissingen die de lidstaten op nationaal niveau hebben genomen met betrekking tot de goedkeuring van Nasonex en verwante namen, kondigde de Europese Commissie bij het Europees Geneesmiddelenbureau een officiële verwijzing overeenkomstig artikel 30 van Richtlijn 2001/83/EG aan om de verschillen tussen de goedgekeurde SPC s voor het bovengenoemde product weg te nemen en zo de SPC's in de hele EU te harmoniseren. Samenvatting van de productkenmerken (SPC) De houder van de vergunning voor het in de handel brengen heeft de huidige, via de procedure van wederzijdse erkenning goedgekeurde productinformatie die wordt ondersteund door de beschikbare werkzaamheids- en veiligheidsgegevens, voorgesteld als basis voor de geharmoniseerde productinformatie. Rubriek 4.1 Therapeutische indicaties Behandeling van de symptomen van rinitis Seizoensgebonden allergische rinitis Er werden zes onderzoeken uitgevoerd om de werkzaamheid van mometasonfuroaat aan te tonen bij patiënten met seizoensgebonden allergische rinitis gerandomiseerd naar behandeling met mometasonfuroaat, placebo of een actief controlemiddel. Van de zes onderzoeken werden er vier samengevoegd en het patiëntendagboek wees op een daling van 33% ten opzichte van de baseline tijdens de eerste twee weken van de behandeling met mometasonfuroaat, tegenover 15% bij patiënten die met placebo werden behandeld. De gemiddelde scores voor beoordelingen van de totale nasale symptomen door artsen wezen op grotere dalingen voor mometasonfuroaat tijdens alle bezoeken (variërend van 36% tot 62%) ten opzichte van placebo (22% tot 48%). Chronische rinitis Op basis van de negen onderzoeken in het oorspronkelijke programma voor chronische rinitis werd de indicatie voor chronische rinitis door de landen die de procedure van wederzijdse erkenning hanteerden in 1997 goedgekeurd en door de andere betrokken lidstaten in 1997 en Vervolgens werd onderzoek Q97-921, dat specifiek werd uitgevoerd bij proefpersonen met 8
3 chronische niet-allergische rinitis (PNAR), afgerond met een positieve uitkomst, waarna in mei 2000 in Zweden een indicatie voor PNAR werd goedgekeurd. Deze onderzoeken ondersteunen de voorgestelde indicatie voor de symptomatische behandeling van (seizoensgebonden allergische en chronische) rinitis bij volwassenen. Pediatrische patiënten De vergunninghouder heeft informatie ingediend over het pediatrische programma en de onderzoeksresultaten (werkzaamheid en veiligheid). De totale respons in termen van verbetering ten opzichte van de baseline in de subgroep van drie tot vijf jaar bleek vergelijkbaar te zijn met die in de subgroep van zes tot elf jaar. De werkzaamheid in de leeftijdsgroep van drie tot vijf jaar wordt dus ondersteund en er wordt vanuit farmacologisch oogpunt geen verschil verwacht tussen de werkzaamheid bij een kind van drie jaar en die bij een kind van zes jaar. Het gebruik van mometasonfuroaat bij chronische rinitis bij kinderen ouder dan drie jaar zoals voorgesteld door de vergunninghouder werd door het CHMP aanvaardbaar geacht. Profylaxe van seizoensgebonden allergische rinitis Er werd verwezen naar twee gerandomiseerde, multicentrische onderzoeken uit het dossier inzake de procedure van wederzijdse erkenning waarbij mometasonfuroaat werd toegediend aan patiënten met een voorgeschiedenis van seizoensgebonden allergische rinitis. De ingediende onderzoeken worden geacht de profylaxe van seizoensgebonden allergische rinitis niet te ondersteunen, aangezien de voor deze indicatie ingediende gegevens met betrekking tot het geschikte tijdstip van aanvang van de behandeling niet overtuigend waren, gelet op het feit dat een vroeg begin van de behandeling niet vergeleken werd met een aanvang van de behandeling op het moment dat de eerste symptomen optreden. Mometasonfuroaat heeft een snel intredende werking bij patiënten met allergische symptomen en het waargenomen effect na profylactische behandeling (zoals dat is beschreven in de onderzoeken) kon dus in verband gebracht worden met een behandeleffect zoals dat in de algemene indicatie voor rinitis is opgenomen. De indicatie voor de profylaxe van seizoensgebonden allergische rinitis werd derhalve niet door het CHMP aanvaard. In plaats hiervan werd er tekst opgenomen in rubriek 4.2 van de SPC om te verduidelijken dat de behandeling bij patiënten met een voorgeschiedenis van matige tot ernstige symptomen van seizoensgebonden allergische rinitis mogelijk enkele dagen voor het verwachte begin van het allergieseizoen dient te worden ingesteld. Neuspolypose Er werden twee gerandomiseerde, placebogecontroleerde, dubbelblinde, multicentrische behandelingsproeven met parallelle groepen met een looptijd van vier maanden waarin de werkzaamheid en veiligheid werden onderzocht, en een observationeel vervolgonderzoek waarin niet werd behandeld, besproken ter ondersteuning van de indicatie voor de behandeling van neuspolypose, waarbij twee doses mometasonfuroaat ten opzichte van placebo (200 µg eenmaal daags en tweemaal daag) werden onderzocht bij in totaal 664 proefpersonen, van wie er 441 werden behandeld met mometasonfuroaat. De indicatie voor de behandeling van neuspolypose werd door het CHMP aanvaard. De vergunninghouder heeft ervoor gekozen de indicatie voor de preventie van neuspoliepen na een functionele endoscopische sinusoperatie (FESS), die alleen in Zweden is goedgekeurd, niet in de voorgestelde geharmoniseerde SPC op te nemen. Behandeling van acute sinusitis Uit twee onderzoeken waarin sinusitis werd onderzocht alsook uit de resultaten en analyse van een aanvullend onderzoek (A2-3852) dat werd uitgevoerd om de klinische relevantie van het waargenomen behandeleffect te beoordelen, bleek dat de klinische relevantie van de in deze onderzoeken gegenereerde gegevens met betrekking tot de voorgestelde indicatie niet was 9
4 vastgesteld. De indicatie voor de behandeling van acute sinusitis werd derhalve niet door het CHMP aanvaard. Rubriek 4.2 Dosering en wijze van toediening Op basis van 19 fase II- en fase III-onderzoeken waarin mometasonfuroaat werd toegediend aan jongeren tot 18 jaar en volwassenen, werd een totale dosis van 200 µg eenmaal daags gekozen als klinische standaarddosering voor jongeren tot 18 jaar en volwassenen, waarbij dosistitratie tot een maximale dagelijkse dosis van 400 µg mogelijk was. De aanvangsdosis voor rinitis en neuspoliepen is 100 µg eenmaal daags in elk neusgat (totale dagelijkse dosering 200 µg). In geval van onvoldoende respons werd verhoging van de dosis tot 100 µg tweemaal daags in elk neusgat (totale dagelijkse dosis 400 µg) voorgesteld, zoals in de meeste lidstaten. Bij patiënten met een voorgeschiedenis van matige tot ernstige symptomen van seizoensgebonden allergische rinitis wordt erop gewezen dat de behandeling met mometasonfuroaat mogelijk enkele dagen voor het verwachte begin van het pollenseizoen dient te worden ingesteld. Pediatrische patiënten De veiligheid en werkzaamheid van Nasonex-neusspray zijn niet aangetoond bij: - kinderen jonger dan 3 jaar met seizoensgebonden allergische rinitis en chronische allergische rinitis; - kinderen en jongeren tot 18 jaar met neuspolypose. De tekst in rubriek 4.2 is herzien en in overeenstemming gebracht met de QRD-eisen. Rubriek 4.3 Contra-indicaties Bekende overgevoeligheid voor de werkzame stof, mometasonfuroaat, of voor een van de hulpstoffen is voorgesteld overeenkomstig het huidige richtsnoer voor de samenvatting van productkenmerken. Mometasonfuroaat is gecontra-indiceerd bij onbehandelde gelokaliseerde infectie zoals herpes simplex, waarbij neusslijmvliezen betrokken zijn, en ook voor patiënten die recent een neusoperatie of -trauma hebben ondergaan, totdat genezing heeft plaatsgevonden, vanwege het remmende effect van corticosteroïden op de wondgenezing. Rubriek 4.4 Bijzondere waarschuwingen en voorzorgen bij gebruik De inhoud van deze rubriek is niet gewijzigd ten opzichte van wat in de meeste landen is goedgekeurd, hoewel de formulering in sommige gevallen is gewijzigd om harmonisatie te bereiken. Er wordt melding gemaakt van de immunosuppressieve effecten van corticosteroïden en het risico van blootstelling van patiënten aan bepaalde infecties (zoals waterpokken en mazelen) en van het belang een arts te raadplegen indien van een dergelijke blootstelling sprake is. Het gebruik van mometasonfuroaat wordt niet aanbevolen in geval van neusseptumperforatie (de informatie over gemelde gevallen van neusseptumperforatie wordt vermeld in rubriek 4.8). De hogere incidentie van epitaxis die in klinische onderzoeken werd waargenomen, wordt ook vermeld in deze rubriek alsook in rubriek 4.8. Bovendien is in deze rubriek een waarschuwing opgenomen over de aanwezigheid van de hulpstof benzalkoniumchloride, die neusirritatie kan veroorzaken. Er is een rubriek opgenomen over de systemische effecten van corticosteroïden en er zijn meldingen van verhoogde intraoculaire druk na het gebruik van intranasale corticosteroïden 10
5 opgenomen. De noodzaak van gelijktijdig gebruik van een passende aanvullende behandeling voor verlichting van niet-nasale symptomen, met name oculaire symptomen, wordt ook benadrukt. Er wordt ook geadviseerd om bij langdurige behandeling met nasale corticosteroïden het effect op de groei bij pediatrische patiënten regelmatig te controleren. Rubriek 4.5 Interacties met andere geneesmiddelen en andere vormen van interactie Er wordt verwezen naar een klinisch interactieonderzoek dat werd uitgevoerd met loratadine en waarbij geen interacties gemeld werden. Er is een kruisverwijzing naar rubriek 4.4 toegevoegd voor gebruik in combinatie met systemische corticosteroïden. Rubriek 4.6 Vruchtbaarheid, zwangerschap en borstvoeding De door de vergunninghouder voorgestelde formulering onder de kopjes Zwangerschap en Borstvoeding werd door het CHMP aanvaardbaar geacht. De rubriek Vruchtbaarheid werd zodanig gewijzigd dat alleen de relevante conclusies van nietklinische toxiciteitsonderzoeken genoemd worden, overeenkomstig het huidige richtsnoer voor de samenvatting van productkenmerken. Rubriek 4.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen De opmerking dat er geen effecten op de rijvaardigheid en op het vermogen om machines te bedienen bekend zijn, werd door het CHMP aanvaardbaar geacht. Rubriek 4.8 Bijwerkingen Rubriek 4.8 werd overeenkomstig het voorstel van het CHMP geherstructureerd om de leesbaarheid te bevorderen en aan het QRD-model en het SPC-richtsnoer te voldoen. De bijwerkingen werden onafhankelijk van de indicatie gepresenteerd, waarbij alle gegevens (samengevoegd) in tabelvorm werden weergegeven. Rubriek 4.9 Overdosering Er wordt vermeld dat het onwaarschijnlijk is dat bij overdosering naast observatie behandeling nodig is aangezien de systemische biologische beschikbaarheid van mometasonfuroaat <1% is. Inhalatie of orale toediening van zeer hoge doses corticosteroïden kan echter leiden tot onderdrukking van de functie van de HPA-as. Rubriek 5.1 Farmacodynamische eigenschappen Deze rubriek van de voorgestelde SPC bevat informatie over het werkingsmechanisme van mometasonfuroaat en de farmacodynamische effecten ervan bij patiënten met seizoensgebonden allergische rinitis. Het Europees Geneesmiddelenbureau heeft besloten af te zien van de verplichting om de resultaten in te dienen van onderzoek met Nasonex-neusspray en verwante namen in alle subgroepen van pediatrische patiënten met seizoensgebonden en chronische allergische rinitis (zie rubriek 4.2 voor informatie over pediatrisch gebruik). Rubriek 5.2 Farmacokinetische eigenschappen De door de vergunninghouder voorgestelde informatie in deze rubriek van de SPC werd vermeld onder de kopjes absorptie, distributie, biotransformatie en eliminatie, en werd door het CHMP aanvaardbaar geacht behoudens de aanbevolen wijzigingen. 11
6 Rubriek 5.3 Gegevens uit het preklinisch veiligheidsonderzoek De glucocorticoïde-gerelateerde effecten van mometasonfuroaat die in dieronderzoeken werden waargenomen, worden in deze rubriek beschreven. Mometasonfuroaat vertoont geen androgene, anti-androgene, oestrogene of anti-oestrogene activiteit. Er werden geen toxicologische effecten aangetoond die specifiek zijn voor de blootstelling aan mometasonfuroaat. Bijsluiter De veranderingen in de SPC waarmee het CHMP instemde, werden ook weergegeven in de bijsluiter, voor zover ze relevant waren voor de gebruiker. De verkregen resultaten van de gebruikerstests in wijziging UK/H/0196/001/II/032 die moest worden ingediend ten behoeve van de verlenging in verband met de procedure van wederzijdse erkenning en die in januari 2009 werd goedgekeurd, werden door het CHMP aanvaardbaar geacht. Nasonex is een neuspreparaat voor topisch gebruik en bevat benzalkoniumchloride. Aangezien de hoeveelheid benzalkoniumchloride 0,02 mg per afgifte hoger is dan de drempelwaarde van 10 microgram per toegediende dosis, is de opmerking dat Nasonex benzalkoniumchloride bevat, dat neusirritatie kan veroorzaken, in de bijsluiter opgenomen overeenkomstig het richtsnoer voor hulpstoffen op het etiket en in de bijsluiter (2003). Redenen voor de wijziging van de voorwaarden verbonden aan de vergunning(en) voor het in de handel brengen Overwegende dat het CHMP de verwijzing krachtens artikel 30 van Richtlijn 2001/83/EG in acht heeft genomen; het CHMP de vastgestelde verschillen voor Nasonex en verwante namen met betrekking tot de rubrieken therapeutische indicaties, dosering en wijze van toediening alsook de resterende rubrieken van de SPC's in overweging heeft genomen; het CHMP de door de vergunninghouder ingediende gegevens van de bestaande klinische en niet-klinische onderzoeken en de door de vergunninghouder gemelde ervaringen na het in de handel brengen van Nasonex en verwante namen, waarmee de voorgestelde harmonisatie van de productinformatie wordt gerechtvaardigd, heeft beoordeeld; het CHMP instemde met de harmonisatie van de samenvatting van de productkenmerken, de etikettering en de bijsluiter die door de vergunninghouder werd voorgesteld en besproken; adviseert het CHMP de wijziging van de voorwaarden verbonden aan de vergunningen voor het in de handel brengen waarvoor de samenvatting van de productkenmerken, de etikettering en de bijsluiter zijn weergegeven in bijlage III voor Nasonex en verwante namen (zie bijlage I). 12
Bijlage II. Wetenschappelijke conclusies
 Bijlage II Wetenschappelijke conclusies 14 Wetenschappelijke conclusies Haldol, dat de werkzame stof haloperidol bevat, is een antipsychoticum dat behoort tot de butyrofenonengroep. Het is een krachtige
Bijlage II Wetenschappelijke conclusies 14 Wetenschappelijke conclusies Haldol, dat de werkzame stof haloperidol bevat, is een antipsychoticum dat behoort tot de butyrofenonengroep. Het is een krachtige
Wetenschappelijke conclusies
 BIJLAGE II WETENSCHAPPELIJKE CONCLUSIES EN REDENEN VOOR DE WIJZIGING VAN DE SAMENVATTING VAN DE PRODUCTKENMERKEN, DE ETIKETTERING EN DE BIJSLUITER, OPGESTELD DOOR HET EUROPEES GENEESMIDDELENBUREAU 14 Wetenschappelijke
BIJLAGE II WETENSCHAPPELIJKE CONCLUSIES EN REDENEN VOOR DE WIJZIGING VAN DE SAMENVATTING VAN DE PRODUCTKENMERKEN, DE ETIKETTERING EN DE BIJSLUITER, OPGESTELD DOOR HET EUROPEES GENEESMIDDELENBUREAU 14 Wetenschappelijke
Beclometason Sandoz Nevel 50, neusspray suspensie 50 microgram/dosis
 Sandoz B.V. Page 1/5 1. NAAM VAN HET GENEESMIDDEL Beclometason Sandoz Nevel 50, neusspray suspensie 50 microgram/dosis 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Beclometason Sandoz Nevel 50 levert
Sandoz B.V. Page 1/5 1. NAAM VAN HET GENEESMIDDEL Beclometason Sandoz Nevel 50, neusspray suspensie 50 microgram/dosis 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Beclometason Sandoz Nevel 50 levert
SAMENVATTING VAN DE PRODUCTKENMERKEN
 1. NAAM VAN HET GENEESMIDDEL Sedistress 100 harde capsules. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Iedere capsule bevat 100 mg zuiver droog extract van de bovengrondse delen van Passiflora incarnata
1. NAAM VAN HET GENEESMIDDEL Sedistress 100 harde capsules. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Iedere capsule bevat 100 mg zuiver droog extract van de bovengrondse delen van Passiflora incarnata
Dit geneesmiddel is een traditioneel kruidengeneesmiddel. De toepassing is uitsluitend gebaseerd op het langdurige gebruik.
 SEDISTRESS 1. NAAM VAN HET GENEESMIDDEL Sedistress 200 omhulde tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke omhulde tablet bevat 200 mg droogextract van de bovengrondse delen van passiebloem
SEDISTRESS 1. NAAM VAN HET GENEESMIDDEL Sedistress 200 omhulde tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke omhulde tablet bevat 200 mg droogextract van de bovengrondse delen van passiebloem
Volume: 0-49 zendingen per jaar Europa 0 2 kg 2-10 kg kg kg
 Wanneer u op basis van uw daadwerkelijkaantal zendingen boven de 49 zendingen per jaar uitkomt, dan kunt u ons contacteren voor verbeterde tarieven. Wij passen uw prijzen dan direct aan. Volume: 0-49 zendingen
Wanneer u op basis van uw daadwerkelijkaantal zendingen boven de 49 zendingen per jaar uitkomt, dan kunt u ons contacteren voor verbeterde tarieven. Wij passen uw prijzen dan direct aan. Volume: 0-49 zendingen
VITAMINE C TEVA 250 MG VITAMINE C TEVA 100 MG. VITAMINE C TEVA 500 MG tabletten
 1.3.1 : Productinformatie Bladzijde : 1 1. NAAM VAN HET GENEESMIDDEL Vitamine C Teva 50 mg, Vitamine C Teva 100 mg, Vitamine C Teva 250 mg, Vitamine C Teva 500 mg, 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
1.3.1 : Productinformatie Bladzijde : 1 1. NAAM VAN HET GENEESMIDDEL Vitamine C Teva 50 mg, Vitamine C Teva 100 mg, Vitamine C Teva 250 mg, Vitamine C Teva 500 mg, 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
ETOS AMYLMETACRESOL PLUS DICHLOORBENZYLALCOHOL HONING & CITROEN zuigtabletten
 1.3.1 : Productinformatie Bladzijde: 1 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke zuigtablet bevat: Amylmetacresol 0,60 mg 2,
1.3.1 : Productinformatie Bladzijde: 1 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke zuigtablet bevat: Amylmetacresol 0,60 mg 2,
ANNEX III WIJZIGINGEN IN DE SAMENVATTINGEN VAN DE PRODUCTKENMERKEN EN DE BIJSLUITER
 ANNEX III WIJZIGINGEN IN DE SAMENVATTINGEN VAN DE PRODUCTKENMERKEN EN DE BIJSLUITER Deze aanpassingen aan de SPC en bijsluiter zijn valide op het moment van de beschikking van de commissie. Na de beschikking
ANNEX III WIJZIGINGEN IN DE SAMENVATTINGEN VAN DE PRODUCTKENMERKEN EN DE BIJSLUITER Deze aanpassingen aan de SPC en bijsluiter zijn valide op het moment van de beschikking van de commissie. Na de beschikking
Mometasonfuroaat Dermapharm 50 microgram / verstuiving, neusspray, suspensie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Mometasonfuroaat Dermapharm 50 microgram / verstuiving, neusspray, suspensie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke verstuiving
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Mometasonfuroaat Dermapharm 50 microgram / verstuiving, neusspray, suspensie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke verstuiving
Thymoseptine is een traditioneel geneesmiddel op basis van planten; het gebruik bij deze specifieke indicatie is uitsluitend gebaseerd op traditie.
 Thymoseptine 1. NAAM VAN HET GENEESMIDDEL Thymoseptine siroop 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 5 ml siroop bevat 750 mg vloeibaar extract (1:1) van Thymus vulgaris L., herba (tijm). Oplosmiddel
Thymoseptine 1. NAAM VAN HET GENEESMIDDEL Thymoseptine siroop 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 5 ml siroop bevat 750 mg vloeibaar extract (1:1) van Thymus vulgaris L., herba (tijm). Oplosmiddel
Tarieven Europa: staffel 1
 Tarieven Europa: staffel 1 Wanneer u op basis van uw daadwerkelijkaantal zendingen boven de 49 zendingen per jaar uitkomt, dan kunt u ons contacteren voor verbeterde tarieven. Wij passen uw prijzen dan
Tarieven Europa: staffel 1 Wanneer u op basis van uw daadwerkelijkaantal zendingen boven de 49 zendingen per jaar uitkomt, dan kunt u ons contacteren voor verbeterde tarieven. Wij passen uw prijzen dan
SAMENVATTING VAN DE PRODUCTKENMERKEN
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL trianal vitis caps harde capsules 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke harde capsule bevat 300 mg Vitis vinifera L., folium
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL trianal vitis caps harde capsules 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke harde capsule bevat 300 mg Vitis vinifera L., folium
Wetenschappelijke conclusies
 Bijlage II Wetenschappelijke conclusies en redenen voor het positieve advies voor de handelsvergunning mits aan de voorwaarden wordt voldaan, en voor de wijziging van de samenvatting van de productkenmerken
Bijlage II Wetenschappelijke conclusies en redenen voor het positieve advies voor de handelsvergunning mits aan de voorwaarden wordt voldaan, en voor de wijziging van de samenvatting van de productkenmerken
Summary of the Product Characteristics
 1.3.1.1 Summary of the Product Characteristics 1.3.1.1-1 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Bevat dinatriumcromoglicaat overeenkomend
1.3.1.1 Summary of the Product Characteristics 1.3.1.1-1 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Bevat dinatriumcromoglicaat overeenkomend
Samenvatting van de Productkenmerken (SmPC) Pagina 1/9 SAMENVATTING VAN DE PRODUCTKENMERKEN
 Samenvatting van de Productkenmerken (SmPC) Pagina 1/9 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Nasonex 50 microgram/verstuiving, neusspray, suspensie 2. KWALITATIEVE EN KWANTITATIEVE
Samenvatting van de Productkenmerken (SmPC) Pagina 1/9 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Nasonex 50 microgram/verstuiving, neusspray, suspensie 2. KWALITATIEVE EN KWANTITATIEVE
Samenvatting van de Productkenmerken (SmPC) Pagina 1/9 SAMENVATTING VAN DE PRODUCTKENMERKEN
 Samenvatting van de Productkenmerken (SmPC) Pagina 1/9 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Nasonex 50 microgram/verstuiving, neusspray, suspensie 2. KWALITATIEVE EN KWANTITATIEVE
Samenvatting van de Productkenmerken (SmPC) Pagina 1/9 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Nasonex 50 microgram/verstuiving, neusspray, suspensie 2. KWALITATIEVE EN KWANTITATIEVE
SAMENVATTING VAN DE PRODUCTKENMERKEN. Kruidvat Amylmetacresol Plus Dichloorbenzylalcohol honing & citroen zuigtabletten
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Kruidvat Amylmetacresol Plus Dichloorbenzylalcohol honing & citroen zuigtabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke zuigtablet
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Kruidvat Amylmetacresol Plus Dichloorbenzylalcohol honing & citroen zuigtabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke zuigtablet
Hulpstof met bekend effect: Opticrom, oogdruppels bevat benzalkoniumchloride. Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1 NAAM VAN HET GENEESMIDDEL Opticrom, oogdruppels, oplossing 20 mg/ml Opticrom Unit Dose, oogdruppels, oplossing 20 mg/ml 2 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
SAMENVATTING VAN DE PRODUCTKENMERKEN 1 NAAM VAN HET GENEESMIDDEL Opticrom, oogdruppels, oplossing 20 mg/ml Opticrom Unit Dose, oogdruppels, oplossing 20 mg/ml 2 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Ferrum-Homaccord; Druppels voor oraal gebruik, oplossing 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 100 g oplossing bevat:
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Ferrum-Homaccord; Druppels voor oraal gebruik, oplossing 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 100 g oplossing bevat:
SAMENVATTING VAN DE PRODUCTKENMERKEN
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL Pulmocap Thymus, stroop 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml stroop (overeenkomend met 1,1 g) bevat 110 mg (0,11 ml) vloeibaar
SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL Pulmocap Thymus, stroop 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml stroop (overeenkomend met 1,1 g) bevat 110 mg (0,11 ml) vloeibaar
SAMENVATTING VAN DE PRODUCTKENMERKEN. NORGALAX, 0,12 g / 10 g, gel voor rectaal gebruik. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL NORGALAX, 0,12 g / 10 g, gel voor rectaal gebruik. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Actief bestanddeel: Natriumdocusaat 0,12
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL NORGALAX, 0,12 g / 10 g, gel voor rectaal gebruik. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Actief bestanddeel: Natriumdocusaat 0,12
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Hepeel; Tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 tablet (301,5 mg) bevat: Colocynthis D6 90 mg Veratrum album
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Hepeel; Tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 tablet (301,5 mg) bevat: Colocynthis D6 90 mg Veratrum album
LAXEERSTROOP TEVA 667 mg/ml, stroop. MODULE I : ALGEMENE GEGEVENS Datum : 9 februari : Productinformatie Bladzijde : 1
 1.3.1 : Productinformatie Bladzijde : 1 1. NAAM VAN HET GENEESMIDDEL Laxeerstroop Teva. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Laxeerstroop Teva is een waterige oplossing van 667 mg lactulose per
1.3.1 : Productinformatie Bladzijde : 1 1. NAAM VAN HET GENEESMIDDEL Laxeerstroop Teva. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Laxeerstroop Teva is een waterige oplossing van 667 mg lactulose per
Version 7.3.1, 03/2010 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 Version 7.3.1, 03/2010 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL Norit 200, capsules 200 mg, hard 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING De capsule bevat 200
Version 7.3.1, 03/2010 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL Norit 200, capsules 200 mg, hard 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING De capsule bevat 200
SAMENVATTING VAN DE PRODUCTKENMERKEN. Elke verstuiving bevat mometasonfuroaatmonohydraat, overeenkomend met 50 microgram mometasonfuroaat watervrij.
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Mometasone EG 50 microgram/verstuiving, neusspray, suspensie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke verstuiving bevat mometasonfuroaatmonohydraat,
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Mometasone EG 50 microgram/verstuiving, neusspray, suspensie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke verstuiving bevat mometasonfuroaatmonohydraat,
Bevat dinatriumcromoglicaat overeenkomend met 20 mg natriumcromoglicaat per ml.
 1. NAAM VAN HET GENEESMIDDEL Natriumcromoglicaat oogdruppels 20 mg/ml, oogdruppels, oplossing 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Bevat dinatriumcromoglicaat overeenkomend met 20 mg natriumcromoglicaat
1. NAAM VAN HET GENEESMIDDEL Natriumcromoglicaat oogdruppels 20 mg/ml, oogdruppels, oplossing 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Bevat dinatriumcromoglicaat overeenkomend met 20 mg natriumcromoglicaat
SAMENVATTING VAN DE PRODUCTKENMERKEN
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL BRONCHO-VAXOM Kinderen, capsules, hard BRONCHO-VAXOM Volwassenen, capsules, hard 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING BRONCHO-VAXOM
SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL BRONCHO-VAXOM Kinderen, capsules, hard BRONCHO-VAXOM Volwassenen, capsules, hard 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING BRONCHO-VAXOM
Aanvrager Fantasienaam Sterkte Farmaceutische vorm. Loratadine. Vitabalans 10 mg tablety. Loratadine. Vitabalans. Vitabalans 10 mg tabletes
 Biljage I Lijst met namen, farmaceutische vorm, sterkte van het geneesmiddel, toedieningsweg, aanvrager en houder van de vergunning voor het in de handel brengen in de lidstaten 1 Lidstaat (EU/EER) Houder
Biljage I Lijst met namen, farmaceutische vorm, sterkte van het geneesmiddel, toedieningsweg, aanvrager en houder van de vergunning voor het in de handel brengen in de lidstaten 1 Lidstaat (EU/EER) Houder
Version 3.1, 06/2015 SAMENVATTING VAN DE PRODUCTKENMERKEN
 Version 3.1, 06/2015 SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL PYRIDOXINE LABAZ 250 mg tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Pyridoxine hydrochloride (vitamine
Version 3.1, 06/2015 SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL PYRIDOXINE LABAZ 250 mg tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Pyridoxine hydrochloride (vitamine
BIJLAGE I. EMEA/CVMP/495339/2007-NL november 2007 1/10
 BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN DE GENEESMIDDELEN, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER/AANVRAGER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EMEA/CVMP/495339/2007-NL november
BIJLAGE I NAAM, FARMACEUTISCHE VORM, STERKTE VAN DE GENEESMIDDELEN, DIERSOORTEN, TOEDIENINGSWEGEN EN HOUDER/AANVRAGER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EMEA/CVMP/495339/2007-NL november
Bijlage II. Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden verbonden aan de vergunning voor het in de handel brengen
 Bijlage II Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden verbonden aan de vergunning voor het in de handel brengen 7 Wetenschappelijke conclusies Algehele samenvatting van
Bijlage II Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden verbonden aan de vergunning voor het in de handel brengen 7 Wetenschappelijke conclusies Algehele samenvatting van
SAMENVATTING VAN DE PRODUCTKENMERKEN. BRONCHOSTOP Duo Hoestpastilles tijm- en heemstwortelextract
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET MEDISCH PRODUCT BRONCHOSTOP Duo Hoestpastilles tijm- en heemstwortelextract 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 pastille bevat: 51,1 mg
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET MEDISCH PRODUCT BRONCHOSTOP Duo Hoestpastilles tijm- en heemstwortelextract 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 pastille bevat: 51,1 mg
SAMENVATTING VAN DE PRODUCTKENMERKEN. Mometasonfuroaat Glenmark 50 microgram / verstuiving, neusspray, suspensie
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Mometasonfuroaat Glenmark 50 microgram / verstuiving, neusspray, suspensie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke verstuiving
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Mometasonfuroaat Glenmark 50 microgram / verstuiving, neusspray, suspensie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke verstuiving
Algehele samenvatting van de wetenschappelijke beoordeling van nimesulidebevattende geneesmiddelen voor systemisch gebruik (zie bijlage I)
 Bijlage II Wetenschappelijke conclusies en redenen voor de wijzigingen van de samenvatting van de productkenmerken en de bijsluiter, opgesteld door het EMA 42 Wetenschappelijke conclusies Algehele samenvatting
Bijlage II Wetenschappelijke conclusies en redenen voor de wijzigingen van de samenvatting van de productkenmerken en de bijsluiter, opgesteld door het EMA 42 Wetenschappelijke conclusies Algehele samenvatting
Bijlage II. Wetenschappelijke conclusies
 Bijlage II Wetenschappelijke conclusies 8 Wetenschappelijke conclusies Amitriptyline is een bekend tricyclisch antidepressivum met een vastgesteld werkingsmechanisme en gebruik(brunton 2011).Amitriptyline
Bijlage II Wetenschappelijke conclusies 8 Wetenschappelijke conclusies Amitriptyline is een bekend tricyclisch antidepressivum met een vastgesteld werkingsmechanisme en gebruik(brunton 2011).Amitriptyline
BIJLAGE II WETENSCHAPPELIJKE CONCLUSIES
 BIJLAGE II WETENSCHAPPELIJKE CONCLUSIES 20 Wetenschappelijke conclusies Achtergrondinformatie Durogesic-pleisters voor transdermaal gebruik bevatten fentanyl, een krachtig synthetisch opioïde analgeticum
BIJLAGE II WETENSCHAPPELIJKE CONCLUSIES 20 Wetenschappelijke conclusies Achtergrondinformatie Durogesic-pleisters voor transdermaal gebruik bevatten fentanyl, een krachtig synthetisch opioïde analgeticum
Summary of product characteristics
 1 Summary of product characteristics 1 NAAM VAN HET GENEESMIDDEL Lamberts Valeriaan tabletten. 2 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Eén filmomhulde tablet bevat 300 mg droog extract van de wortel
1 Summary of product characteristics 1 NAAM VAN HET GENEESMIDDEL Lamberts Valeriaan tabletten. 2 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Eén filmomhulde tablet bevat 300 mg droog extract van de wortel
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER
 Sandoz B.V. Page 1/5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER suspensie 50 microgram/dosis beclometasondipropionaat Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat
Sandoz B.V. Page 1/5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER suspensie 50 microgram/dosis beclometasondipropionaat Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Nux vomica-homaccord; Druppels voor oraal gebruik, oplossing. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 100 g oplossing
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Nux vomica-homaccord; Druppels voor oraal gebruik, oplossing. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 100 g oplossing
SAMENVATTING VAN DE PRODUCTKENMERKEN. Water voor injecties B. Braun, oplosmiddel voor parenteraal gebruik 100% m/v
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Water voor injecties B. Braun, oplosmiddel voor parenteraal gebruik 100% m/v 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 100 ml oplossing
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Water voor injecties B. Braun, oplosmiddel voor parenteraal gebruik 100% m/v 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 100 ml oplossing
BECLOMETASON NEVEL APOTEX 50, NEUSSPRAY SUSPENSIE 50 MICROGRAM/DOSIS RVG 28086= Version 2016_06 Page 1 of 6
 Version 2016_06 Page 1 of 6 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER BECLOMETASON NEVEL APOTEX 50, NEUSSPRAY beclometasondipropionaat Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken,
Version 2016_06 Page 1 of 6 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER BECLOMETASON NEVEL APOTEX 50, NEUSSPRAY beclometasondipropionaat Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken,
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Oculo-Heel; Oogdruppels, oplossing 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Oculo-Heel bevat per monodosis van 0,45 ml
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Oculo-Heel; Oogdruppels, oplossing 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Oculo-Heel bevat per monodosis van 0,45 ml
1.3. PRODUCT INFORMATION
 1.3. PRODUCT INFORMATION 1.3.1. SPC, LABELLING AND PACKAGE LEAFLET 1.3.1.1. SUMMARY OF PRODUCT CHARACTERISTICS SAMENVATTING VAN DE PRODUCTKENMERKEN STODAL, stroop 1. NAAM VAN HET GENEESMIDDEL STODAL, stroop
1.3. PRODUCT INFORMATION 1.3.1. SPC, LABELLING AND PACKAGE LEAFLET 1.3.1.1. SUMMARY OF PRODUCT CHARACTERISTICS SAMENVATTING VAN DE PRODUCTKENMERKEN STODAL, stroop 1. NAAM VAN HET GENEESMIDDEL STODAL, stroop
THIAMINE HCL TEVA 25 MG THIAMINE HCL TEVA 50 MG THIAMINE HCL TEVA 100 MG tabletten
 1.3.1 : Productinformatie Blz. : 1 1. NAAM VAN HET GENEESMIDDEL Thiamine HCl Teva 25 mg,. Thiamine HCl Teva 50 mg, Thiamine HCl Teva 100 mg, 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Thiamine HCl
1.3.1 : Productinformatie Blz. : 1 1. NAAM VAN HET GENEESMIDDEL Thiamine HCl Teva 25 mg,. Thiamine HCl Teva 50 mg, Thiamine HCl Teva 100 mg, 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Thiamine HCl
Tarieven Europa: staffel 1
 Tarieven Europa: staffel 1 Wanneer u op basis van uw daadwerkelijkaantal zendingen boven de 49 zendingen per jaar uitkomt, dan kunt u ons contacteren voor verbeterde tarieven. Wij passen uw prijzen dan
Tarieven Europa: staffel 1 Wanneer u op basis van uw daadwerkelijkaantal zendingen boven de 49 zendingen per jaar uitkomt, dan kunt u ons contacteren voor verbeterde tarieven. Wij passen uw prijzen dan
SAMENVATTING VAN DE PRODUCTKENMERKEN
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1 / 6 1. NAAM VAN HET GENEESMIDDEL Pulmocap Hedera, stroop 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml siroop (overeenkomend met 1,1 g) bevat 5,4 mg extract
SAMENVATTING VAN DE PRODUCTKENMERKEN 1 / 6 1. NAAM VAN HET GENEESMIDDEL Pulmocap Hedera, stroop 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml siroop (overeenkomend met 1,1 g) bevat 5,4 mg extract
Bijlage II. Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden verbonden aan de vergunning voor het in de handel brengen
 Bijlage II Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden verbonden aan de vergunning voor het in de handel brengen 13 Wetenschappelijke conclusies Algehele samenvatting van
Bijlage II Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden verbonden aan de vergunning voor het in de handel brengen 13 Wetenschappelijke conclusies Algehele samenvatting van
Mometasonfuroaat (in de vorm van monohydraat), 50 microgram per verstuiving.
 Samenvatting van de productkenmerken 1. NAAM VAN HET GENEESMIDDEL Nasonex 50 microgram per verstuiving, neusspray, suspensie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Mometasonfuroaat (in de vorm
Samenvatting van de productkenmerken 1. NAAM VAN HET GENEESMIDDEL Nasonex 50 microgram per verstuiving, neusspray, suspensie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Mometasonfuroaat (in de vorm
MODULE ZURE OORDRUPPELS MET HYDROCORTISON DMB 1% FNA
 MODULE 1.3.1.1 APPLICATION FORM SUMMARY OF PRODUCT CHARACTERISTICS ZURE OORDRUPPELS MET HYDROCORTISON DMB 1% FNA Regulatory Affairs February 2017 Page 1 of 6 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM
MODULE 1.3.1.1 APPLICATION FORM SUMMARY OF PRODUCT CHARACTERISTICS ZURE OORDRUPPELS MET HYDROCORTISON DMB 1% FNA Regulatory Affairs February 2017 Page 1 of 6 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Vertigoheel; Tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 tablet (301,5 mg) bevat: Cocculus indicus D4 210 mg Conium
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Vertigoheel; Tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 tablet (301,5 mg) bevat: Cocculus indicus D4 210 mg Conium
van een arts, zelfs bij seizoensgebonden allergische conjunctivitis.
 1. NAAM VAN HET GENEESMIDDEL Allergodil oogdruppels 0,5 mg/ml, oogdruppels, oplossing. SAMENVATTING VAN DE PRODUCTKENMERKEN 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Azelastinehydrochloride 0,05%
1. NAAM VAN HET GENEESMIDDEL Allergodil oogdruppels 0,5 mg/ml, oogdruppels, oplossing. SAMENVATTING VAN DE PRODUCTKENMERKEN 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Azelastinehydrochloride 0,05%
MODULE ZURE OORDRUPPELS MET TRIAMCINOLONACETONIDE DMB 0,1% FNA
 MODULE 1.3.1.1 APPLICATION FORM SUMMARY OF PRODUCT CHARACTERISTICS ZURE OORDRUPPELS MET TRIAMCINOLONACETONIDE DMB 0,1% FNA Regulatory Affairs October 2016 Page 1 of 6 SAMENVATTING VAN DE PRODUCTKENMERKEN
MODULE 1.3.1.1 APPLICATION FORM SUMMARY OF PRODUCT CHARACTERISTICS ZURE OORDRUPPELS MET TRIAMCINOLONACETONIDE DMB 0,1% FNA Regulatory Affairs October 2016 Page 1 of 6 SAMENVATTING VAN DE PRODUCTKENMERKEN
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Neurexan; Tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 tablet (301,5 mg) bevat: Avena sativa D2 0,6 mg Coffea cruda
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Neurexan; Tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 tablet (301,5 mg) bevat: Avena sativa D2 0,6 mg Coffea cruda
Wetenschappelijke conclusies
 Bijlage II Wetenschappelijke conclusies en redenen voor de wijziging van de samenvatting van de productkenmerken, de etikettering en de bijsluiter, opgesteld door het Europees Geneesmiddelenbureau 23 Wetenschappelijke
Bijlage II Wetenschappelijke conclusies en redenen voor de wijziging van de samenvatting van de productkenmerken, de etikettering en de bijsluiter, opgesteld door het Europees Geneesmiddelenbureau 23 Wetenschappelijke
SAMENVATTING VAN DE PRODUCTKENMERKEN
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL Lactulose 680 mg/ml drank 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke ml drank bevat 0,68 g lactulose. Voor de volledige lijst
SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL Lactulose 680 mg/ml drank 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke ml drank bevat 0,68 g lactulose. Voor de volledige lijst
Bijlage B4. Eerste treden op de arbeidsmarkt. Freek Bucx
 Bijlage B4 Eerste treden op de arbeidsmarkt Freek Bucx Inhoud Tabel B4.1... 3 Tabel B4.2... 4 Tabel B4.3... 5 Tabel B4.4... 6 Tabel B4.5... 7 Tabel B4.6... 8 Bijlage B4 Eerste treden op de arbeidsmarkt
Bijlage B4 Eerste treden op de arbeidsmarkt Freek Bucx Inhoud Tabel B4.1... 3 Tabel B4.2... 4 Tabel B4.3... 5 Tabel B4.4... 6 Tabel B4.5... 7 Tabel B4.6... 8 Bijlage B4 Eerste treden op de arbeidsmarkt
CHLOORAMFENICOL 5 MG/ML TEVA oogdruppels. MODULE I : ALGEMENE GEGEVENS Datum : 1 juni : productinformatie Bladzijde : 1
 1.3.1 : productinformatie Bladzijde : 1 1. NAAM VAN HET GENEESMIDDEL Chlooramfenicol 5 mg/ml Teva,. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Chlooramfenicol 5 mg/ml Teva, bevat per ml waterige 5
1.3.1 : productinformatie Bladzijde : 1 1. NAAM VAN HET GENEESMIDDEL Chlooramfenicol 5 mg/ml Teva,. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Chlooramfenicol 5 mg/ml Teva, bevat per ml waterige 5
1. 31958 Q 1101: EAEC Raad: De Statuten van het Voorzieningsagentschap van Euratom (PB 27 van 6.12.1958, blz. 534), gewijzigd bij:
 9. ENERGIE 1. 31958 Q 1101: EAEC Raad: De Statuten van het Voorzieningsagentschap van Euratom (PB 27 van 6.12.1958, blz. 534), gewijzigd bij: 31973 D 0045: Besluit 73/45/Euratom van de Raad van 8 maart
9. ENERGIE 1. 31958 Q 1101: EAEC Raad: De Statuten van het Voorzieningsagentschap van Euratom (PB 27 van 6.12.1958, blz. 534), gewijzigd bij: 31973 D 0045: Besluit 73/45/Euratom van de Raad van 8 maart
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL Transipeg 5,9 g, poeder voor drank. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Dit product bevat per sachet van 6,9 gram.
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL Transipeg 5,9 g, poeder voor drank. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Dit product bevat per sachet van 6,9 gram.
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, AANVRAGERS IN DE LIDSTATEN
 BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, AANVRAGERS IN DE LIDSTATEN 1 AT - Oostenrijk Flutiform 50 Mikrogramm/5 Mikrogramm pro Sprühstoß Druckgasinhalation
BIJLAGE I LIJST MET NAMEN, FARMACEUTISCHE VORM, STERKTE VAN HET GENEESMIDDEL, TOEDIENINGSWEG, AANVRAGERS IN DE LIDSTATEN 1 AT - Oostenrijk Flutiform 50 Mikrogramm/5 Mikrogramm pro Sprühstoß Druckgasinhalation
ANNEX BIJLAGE. bij VERSLAG VAN DE COMMISSIE AAN HET EUROPEES PARLEMENT EN DE RAAD
 EUROPESE COMMISSIE Brussel, 21.9.2018 COM(2018) 651 final ANNEX BIJLAGE bij VERSLAG VAN DE COMMISSIE AAN HET EUROPEES PARLEMENT EN DE RAAD over de werking van Richtlijn 2011/24/EU betreffende de toepassing
EUROPESE COMMISSIE Brussel, 21.9.2018 COM(2018) 651 final ANNEX BIJLAGE bij VERSLAG VAN DE COMMISSIE AAN HET EUROPEES PARLEMENT EN DE RAAD over de werking van Richtlijn 2011/24/EU betreffende de toepassing
SAMENVATTING VAN DE PRODUCTKENMERKEN. Mometasonfuroaat Cipla 50 microgram/verstuiving neusspray, suspensie
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Mometasonfuroaat Cipla 50 microgram/verstuiving neusspray, suspensie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke verstuiving (100
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Mometasonfuroaat Cipla 50 microgram/verstuiving neusspray, suspensie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke verstuiving (100
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Oteel; Oordruppels, oplossing. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 monodosis van 0,45 ml (= 0,45 g) bevat: Arnica
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Oteel; Oordruppels, oplossing. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 monodosis van 0,45 ml (= 0,45 g) bevat: Arnica
Bijlage II. Wetenschappelijke conclusies
 Bijlage II Wetenschappelijke conclusies 8 Wetenschappelijke conclusies Solu-Medrol 40 mg poeder en oplosmiddel voor oplossing voor injectie (hierna Solu-Medrol ) bevat methylprednisolon en, als hulpstof,
Bijlage II Wetenschappelijke conclusies 8 Wetenschappelijke conclusies Solu-Medrol 40 mg poeder en oplosmiddel voor oplossing voor injectie (hierna Solu-Medrol ) bevat methylprednisolon en, als hulpstof,
Bijlage I. Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen
 Bijlage I Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen 1 Wetenschappelijke conclusies Rekening houdend met het beoordelingsrapport
Bijlage I Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen 1 Wetenschappelijke conclusies Rekening houdend met het beoordelingsrapport
SAMENVATTING VAN DE PRODUCTKENMERKEN
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL BIFITERAL siroop 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 100 ml Bifiteral siroop bevatten 66,7 g lactulose galactose lactose epilactose
SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL BIFITERAL siroop 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 100 ml Bifiteral siroop bevatten 66,7 g lactulose galactose lactose epilactose
MEDEDELING VAN DE COMMISSIE
 EUROPESE COMMISSIE Brussel, XXX [ ](2013) XXX draft MEDEDELING VAN DE COMMISSIE Uitvoering van artikel 260 van het Verdrag betreffende de werking van de Europese Unie Aanpassing van de gegevens die worden
EUROPESE COMMISSIE Brussel, XXX [ ](2013) XXX draft MEDEDELING VAN DE COMMISSIE Uitvoering van artikel 260 van het Verdrag betreffende de werking van de Europese Unie Aanpassing van de gegevens die worden
1. NAAM VAN HET GENEESMIDDEL
 1. NAAM VAN HET GENEESMIDDEL ERAZABAN 100 mg/g crème 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke gram crème bevat 100 mg docosanol. Hulpstof: 50 mg propyleenglycol/gram crème. Voor een volledige
1. NAAM VAN HET GENEESMIDDEL ERAZABAN 100 mg/g crème 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke gram crème bevat 100 mg docosanol. Hulpstof: 50 mg propyleenglycol/gram crème. Voor een volledige
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER
 Sandoz B.V. Page 1/5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER suspensie 50 microgram/dosis beclometasondipropionaat Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat
Sandoz B.V. Page 1/5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER suspensie 50 microgram/dosis beclometasondipropionaat Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat
Bijlage B4. Werken aan de start. Freek Bucx
 Bijlage B4 Werken aan de start Freek Bucx Inhoud Tabel B4.1... 3 Tabel B4.2... 5 Tabel B4.3... 6 Tabel B4.4... 7 Tabel B4.5... 8 Tabel B4.6... 9 Tabel B4.7... 10 Tabel B4.8... 11 Tabel B4.9... 12 Tabel
Bijlage B4 Werken aan de start Freek Bucx Inhoud Tabel B4.1... 3 Tabel B4.2... 5 Tabel B4.3... 6 Tabel B4.4... 7 Tabel B4.5... 8 Tabel B4.6... 9 Tabel B4.7... 10 Tabel B4.8... 11 Tabel B4.9... 12 Tabel
SAMENVATTING VAN DE PRODUCTKENMERKEN
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Priciasol 1 mg/ml neusspray, oplossing Priciasol 1 mg/ml neusdruppels, oplossing Priciasol 0,5 mg/ml neusdruppels, oplossing kinderen 2.
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Priciasol 1 mg/ml neusspray, oplossing Priciasol 1 mg/ml neusdruppels, oplossing Priciasol 0,5 mg/ml neusdruppels, oplossing kinderen 2.
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Glucomed 625 mg tabletten. Glucosamine
 BIJSLUITER BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Glucomed 625 mg tabletten Glucosamine Lees de hele bijsluiter zorgvuldig door, want deze bevat belangrijke informatie voor u. Dit geneesmiddel kan zonder
BIJSLUITER BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Glucomed 625 mg tabletten Glucosamine Lees de hele bijsluiter zorgvuldig door, want deze bevat belangrijke informatie voor u. Dit geneesmiddel kan zonder
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Traumeel; Gel 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 100 g gel bevat: Arnica montana radix D3 1,50 g Calendula officinalis
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Traumeel; Gel 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 100 g gel bevat: Arnica montana radix D3 1,50 g Calendula officinalis
SAMENVATTING VAN DE PRODUCT KENMERKEN
 SAMENVATTING VAN DE PRODUCT KENMERKEN 20141114 Pagina 1 van 6 1. NAAM VAN HET GENEESMIDDEL GAVISCON ADVANCE Muntsmaak Unidose suspensie voor oraal gebruik 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
SAMENVATTING VAN DE PRODUCT KENMERKEN 20141114 Pagina 1 van 6 1. NAAM VAN HET GENEESMIDDEL GAVISCON ADVANCE Muntsmaak Unidose suspensie voor oraal gebruik 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
SAMENVATTING VAN DE PRODUCTKENMERKEN
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL PROTAGENS 2%, oogdruppels, oplossing 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml oplossing bevat 20 mg povidon (polyvinylpyrrolidon).
SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL PROTAGENS 2%, oogdruppels, oplossing 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml oplossing bevat 20 mg povidon (polyvinylpyrrolidon).
2 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING. Voor de volledige lijst van hulpstoffen, zie rubriek 6.1
 Sandoz Business use only Page 1 of 11 1 NAAM VAN HET GENEESMIDDEL Mometasone Sandoz 50 microgram/dosis neusspray, suspensie 2 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Telkens als de pomp wordt geactiveerd,
Sandoz Business use only Page 1 of 11 1 NAAM VAN HET GENEESMIDDEL Mometasone Sandoz 50 microgram/dosis neusspray, suspensie 2 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Telkens als de pomp wordt geactiveerd,
SAMENVATTING VAN DE PRODUCTKENMERKEN. Water voor Injecties B. Braun, oplosmiddel voor parenteraal gebruik
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Water voor Injecties B. Braun, oplosmiddel voor parenteraal gebruik 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1000 ml oplosmiddel
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Water voor Injecties B. Braun, oplosmiddel voor parenteraal gebruik 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1000 ml oplosmiddel
SAMENVATTING VAN DE PRODUCTKENMERKEN
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Allergodil 1,5 mg/ml neusspray, oplossing 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Oplossing met 1,5 mg/ml azelastinehydrochloride.
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Allergodil 1,5 mg/ml neusspray, oplossing 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Oplossing met 1,5 mg/ml azelastinehydrochloride.
Bijlage III. Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiters
 Bijlage III Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiters NB: Deze Samenvatting van de productkenmerken, Etikettering
Bijlage III Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiters NB: Deze Samenvatting van de productkenmerken, Etikettering
Strepsils Original bij beginnende keelpijn, zuigtabletten. Strepsils Citroen & Honing bij beginnende keelpijn, zuigtabletten
 1. NAAM VAN HET GENEESMIDDEL Strepsils Original bij beginnende keelpijn, zuigtabletten Strepsils Citroen & Honing bij beginnende keelpijn, zuigtabletten Strepsils Sinaasappel & Vitamine C bij beginnende
1. NAAM VAN HET GENEESMIDDEL Strepsils Original bij beginnende keelpijn, zuigtabletten Strepsils Citroen & Honing bij beginnende keelpijn, zuigtabletten Strepsils Sinaasappel & Vitamine C bij beginnende
SAMENVATTING VAN DE PRODUCTKENMERKEN. Xylometazoline EG bevat 1 mg xylometazolinehydrochloride per ml.
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Xylometazoline EG 100 mg/100 ml neusspray, oplossing 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Xylometazoline EG bevat 1 mg xylometazolinehydrochloride
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Xylometazoline EG 100 mg/100 ml neusspray, oplossing 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Xylometazoline EG bevat 1 mg xylometazolinehydrochloride
SAMENVATTING VAN DE PRODUCTKENMERKEN (Ref )
 SAMENVATTING VAN DE PRODUCTKENMERKEN (Ref. 14.03.2014) 1 1. NAAM VAN HET GENEESMIDDEL Antistax Forte filmomhulde tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Een filmomhulde tablet bevat 360
SAMENVATTING VAN DE PRODUCTKENMERKEN (Ref. 14.03.2014) 1 1. NAAM VAN HET GENEESMIDDEL Antistax Forte filmomhulde tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Een filmomhulde tablet bevat 360
OPTICROM OPTICROM (MELISANA) XIV B 3 e. Naam van het geneesmiddel: OPTICROM 2 % oogdruppels, oplossing Natrium cromoglicaat
 OPTICROM OPTICROM (MELISANA) XIV B 3 e Naam van het geneesmiddel: OPTICROM 2 % oogdruppels, oplossing Natrium cromoglicaat Kwalitatieve en kwantitatieve samenstelling: Natrium cromoglicaat 20 mg per ml.
OPTICROM OPTICROM (MELISANA) XIV B 3 e Naam van het geneesmiddel: OPTICROM 2 % oogdruppels, oplossing Natrium cromoglicaat Kwalitatieve en kwantitatieve samenstelling: Natrium cromoglicaat 20 mg per ml.
SUMMARY OF PRODUCT CHARACTERISTICS
 SUMMARY OF PRODUCT CHARACTERISTICS 1 1. NAAM VAN HET GENEESMIDDEL Dormiplant Mono 500 mg, filmomhulde tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 filmomhulde tablet bevat 500 mg extract
SUMMARY OF PRODUCT CHARACTERISTICS 1 1. NAAM VAN HET GENEESMIDDEL Dormiplant Mono 500 mg, filmomhulde tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 filmomhulde tablet bevat 500 mg extract
1 sachet à 5 gram bevat 3,25 gram psylliumvezels (fijngemalen en gegranuleerde vezels van de Plantago ovata).
 Sandoz B.V. Page 1/5 1. NAAM VAN HET GENEESMIDDEL 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 sachet à 5 gram bevat 3,25 gram psylliumvezels (fijngemalen en gegranuleerde vezels van de Plantago ovata).
Sandoz B.V. Page 1/5 1. NAAM VAN HET GENEESMIDDEL 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 sachet à 5 gram bevat 3,25 gram psylliumvezels (fijngemalen en gegranuleerde vezels van de Plantago ovata).
Samenvatting van de Productkenmerken
 Samenvatting van de Productkenmerken 1. NAAM VAN HET GENEESMIDDEL XT Luis 4% g/g oplossing voor cutaan gebruik 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Dimeticon 4% g/g Voor een volledige lijst van
Samenvatting van de Productkenmerken 1. NAAM VAN HET GENEESMIDDEL XT Luis 4% g/g oplossing voor cutaan gebruik 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Dimeticon 4% g/g Voor een volledige lijst van
Gerenvooieerde versie FLUTICASONPROPIONAAT TEVA 50 MICROGRAM neusspray
 1.3.1 : Productinformatie Bladzijde : 1 1. NAAM VAN HET GENEESMIDDEL Fluticasonpropionaat Teva 50 microgram, 50 microgram/dosis. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke 100 microliter spray
1.3.1 : Productinformatie Bladzijde : 1 1. NAAM VAN HET GENEESMIDDEL Fluticasonpropionaat Teva 50 microgram, 50 microgram/dosis. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke 100 microliter spray
Wijzigingen in de Samenvatting van de Productkenmerken en Bijsluiter, voorgesteld door het Europees Geneesmiddelenbureau
 BIJLAGE II Wijzigingen in de Samenvatting van de Productkenmerken en Bijsluiter, voorgesteld door het Europees Geneesmiddelenbureau Deze Samenvatting van de Productkenmerken en Bijsluiter zijn het resultaat
BIJLAGE II Wijzigingen in de Samenvatting van de Productkenmerken en Bijsluiter, voorgesteld door het Europees Geneesmiddelenbureau Deze Samenvatting van de Productkenmerken en Bijsluiter zijn het resultaat
27 Mai (5) VSM Belgium bvba Rodizen, SPC-NL SAMENVATTING VAN DE PRODUCTKENMERKEN
 1(5) SAMENVATTING VAN DE PRODUCTKENMERKEN Rodizen filmomhulde tabletten 1. NAAM VAN HET GENEESMIDDEL Rodizen,, filmomhulde tabletten Actief bestanddeel: Rhodiola rosea wortelextract 2. KWALITATIEVE EN
1(5) SAMENVATTING VAN DE PRODUCTKENMERKEN Rodizen filmomhulde tabletten 1. NAAM VAN HET GENEESMIDDEL Rodizen,, filmomhulde tabletten Actief bestanddeel: Rhodiola rosea wortelextract 2. KWALITATIEVE EN
Europese feestdagen 2017
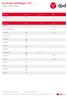 Januari - Februari - Maart Bestemming Januari Februari Maart Nederland (NL) 01-01 Bestemming Januari Februari Maart België (BE) 01-01 Bosnie en Herzegovina (BA) 01-03 Bulgarije (BG) 01-01 03-03 Denemarken
Januari - Februari - Maart Bestemming Januari Februari Maart Nederland (NL) 01-01 Bestemming Januari Februari Maart België (BE) 01-01 Bosnie en Herzegovina (BA) 01-03 Bulgarije (BG) 01-01 03-03 Denemarken
SEDISTRESS SLEEP 1. NAAM VAN HET GENEESMIDDEL 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 3. FARMACEUTISCHE VORM 4. KLINISCHE GEGEVENS
 SEDISTRESS SLEEP 1. NAAM VAN HET GENEESMIDDEL Sedistress Sleep filmomhulde tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke tablet bevat 500 mg droogextract van Valeriana officinalis L., radix
SEDISTRESS SLEEP 1. NAAM VAN HET GENEESMIDDEL Sedistress Sleep filmomhulde tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke tablet bevat 500 mg droogextract van Valeriana officinalis L., radix
BECLOMETASON NEVEL TEVA 50 microgram/dosis neusspray. Beclometason nevel Teva 50 microgram/dosis, neusspray.
 1.3.1 : Productinformatie Bladzijde : 1 1. NAAM VAN HET GENEESMIDDEL Beclometason nevel Teva 50 microgram/dosis,. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Beclometason nevel Teva 50 bevat 50 microgram
1.3.1 : Productinformatie Bladzijde : 1 1. NAAM VAN HET GENEESMIDDEL Beclometason nevel Teva 50 microgram/dosis,. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Beclometason nevel Teva 50 bevat 50 microgram
Europese feestdagen 2019
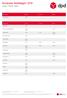 Januari - Februari - Maart Bestemming Januari Februari Maart Nederland (NL) 01-01 Bestemming Januari Februari Maart België (BE) 01-01 Bosnie en Herzegovina (BA) 01-01 02-01 01-03 Bulgarije (BG) 01-01 01-02
Januari - Februari - Maart Bestemming Januari Februari Maart Nederland (NL) 01-01 Bestemming Januari Februari Maart België (BE) 01-01 Bosnie en Herzegovina (BA) 01-01 02-01 01-03 Bulgarije (BG) 01-01 01-02
SAMENVATTING VAN DE PRODUCTKENMERKEN
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Mucorhinyl 0,5 mg/ml. Mucorhinyl 1 mg/ml. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Mucorhinyl 0,5 mg/ml: bevat 0,5 mg xylometazolinehydrochloride
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Mucorhinyl 0,5 mg/ml. Mucorhinyl 1 mg/ml. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Mucorhinyl 0,5 mg/ml: bevat 0,5 mg xylometazolinehydrochloride
SAMENVATTING VAN DE PRODUCTKENMERKEN 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL GAVISCON anijs, suspensie GAVISCON pepermunt, suspensie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Natriumalginaat 500 mg/10 ml Natriumbicarbonaat
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL GAVISCON anijs, suspensie GAVISCON pepermunt, suspensie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Natriumalginaat 500 mg/10 ml Natriumbicarbonaat
Licht blauwe, ronde, biconvexe omhulde tablet. Diameter van de tablet ongeveer 12,4 mm, hoogte van de tablet ongeveer 7,5 mm.
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Valeriamed Night, omhulde tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke filmomhulde tablet bevat 441,35 mg extract (als
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Valeriamed Night, omhulde tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke filmomhulde tablet bevat 441,35 mg extract (als
Healthypharm B.V., Etten-Leur, The Netherlands XT Luis 4% g/g, oplossing voor cutaan gebruik RVG Dimeticon
 1.3.1.1 Summary of product characteristics 1.3.1.1-1 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL XT Luis 4% g/g oplossing voor cutaan gebruik 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
1.3.1.1 Summary of product characteristics 1.3.1.1-1 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL XT Luis 4% g/g oplossing voor cutaan gebruik 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
