Risicominimalisatiemateriaal betreffende avelumab voor voorschrijvers, ziekenhuisapothekers
|
|
|
- Jasper Vedder
- 6 jaren geleden
- Aantal bezoeken:
Transcriptie
1 Avelumab 20 mg/ml concentraat voor oplossing voor infusie Risicominimalisatiemateriaal betreffende avelumab voor voorschrijvers, ziekenhuisapothekers en verpleegkundigen Versie 1.6, juli 2017
2 Introductie De risicominimalisatiematerialen voor avelumab zijn beoordeeld door het College ter Beoordeling van Geneesmiddelen (CBG). Deze materialen beschrijven aanbevelingen om belangrijke risico s van het geneesmiddel te beperken of te voorkomen. Samenvatting Inhoud Samenvatting 2 Hoe moet ik deze brochure gebruiken? 4 Voorafgaand aan de behandeling 5 Infuusgerelateerde reacties: Voorafgaand aan de eerste 4 infusies van avelumab moeten patiënten premedicatie krijgen met een antihistaminicum en met paracetamol. Belangrijke immuungerelateerde bijwerkingen: pneumonitis, hepatitis, colitis, hypo- en hyperthyreoïdie, bijnierinsufficiëntie en type 1 diabetes mellitus, nefritis, nierdisfunctie. myocarditis, myositis, hypopituïtarisme, uveïtis en Guillain-Barrésyndroom. De frequentie van immuungerelateerde bijwerkingen worden gemeld in rubriek 4.8 van de Samenvatting van de productkenmerken voor avelumab. Bij patiënten bij wie immuungerelateerde bijwerkingen niet onder controle kunnen worden gebracht met het gebruik van corticosteroïden, kan toediening van andere systemische immunosuppressiva worden overwogen. Bijwerkingen 6 Wat is de Informatiebrochure voor de patiënt? 11 Waar kan ik aanvullende informatie krijgen? 12 Melding van vermoedelijke bijwerkingen 12 Voor vermoedelijke immuungerelateerde bijwerkingen dient een adequate evaluatie plaats te vinden om de etiologie te bevestigen of andere oorzaken uit te sluiten. Op basis van de ernst van de bijwerking moet avelumab worden onderbroken en moeten corticosteroïden worden toegediend. Als corticosteroïden worden gebruikt om een bijwerking te behandelen, moet bij verbetering het gebruik worden afgebouwd over een periode van ten minste 1 maand. 2 Lees, voordat u avelumab voorschrijft, de bijgaande Samenvatting van de productkenmerken Lees, voordat u avelumab voorschrijft, de bijgaande Samenvatting van de productkenmerken 3
3 Hoe moet ik deze brochure gebruiken? Lees de Samenvatting van de productkenmerken voor avelumab en deze voorlichtingsbrochure goed door voordat u het middel voorschrijft. Hierin leest u hoe avelumab wordt gebruikt. Dat helpt u om: mogelijke bijwerkingen te begrijpen; bijwerkingen goed te behandelen; Voorafgaand aan de behandeling Premedicatie Voorafgaand aan de eerste 4 infusies van avelumab moeten patiënten premedicatie krijgen met een antihistaminicum en met paracetamol. Als de vierde infusie voltooid is zonder infusiegerelateerde reactie, kan premedicatie voor volgende doses worden toegediend volgens het oordeel van de arts. de Informatiebrochure voor de patiënt en de Patiëntenwaarschuwingskaart met patiënten te gebruiken; ervoor te zorgen dat bijwerkingen adequaat en op de juiste wijze worden gemeld. 4 Lees, voordat u avelumab voorschrijft, de bijgaande Samenvatting van de productkenmerken Lees, voordat u avelumab voorschrijft, de bijgaande Samenvatting van de productkenmerken 5
4 Bijwerkingen Welke bijwerkingen kunnen worden veroorzaakt door een behandeling met avelumab? Hoe moet ik monitoren op immuungerelateerde bijwerkingen bij patiënten die avelumab krijgen en hoe moet ik deze bijwerkingen behandelen? Ernstige bijwerkingen waren immuungerelateerde bijwerkingen en infusiegerelateerde reacties. De volgende belangrijke immuungerelateerde bijwerkingen zijn gemeld bij patiënten die met avelumab werden behandeld: Immuungerelateerde pneumonitis Immuungerelateerde hepatitis Immuungerelateerde colitis Immuungerelateerde endocrinopathieën - Schildklierstoornissen - Bijnierinsufficiëntie - Type 1 diabetes mellitus Immuungerelateerde nefritis en nierdisfunctie Andere immuungerelateerde bijwerkingen, waaronder myocarditis, myositis, hypopituïtarisme, uveïtis en Guillain-Barrésyndroom. De meeste immuungerelateerde bijwerkingen met avelumab waren omkeerbaar en waren onder controle met tijdelijke of definitieve stopzetting van avelumab, toediening van corticosteroïden en/of ondersteunende zorg. Voor vermoedelijke immuungerelateerde bijwerkingen dient een adequate evaluatie plaats te vinden om de etiologie te bevestigen of andere oorzaken uit te sluiten. Op basis van de ernst van de bijwerking moet avelumab worden onderbroken en moeten corticosteroïden worden toegediend. Als corticosteroïden worden gebruikt om een bijwerking te behandelen, moet bij verbetering het gebruik worden afgebouwd over een periode van ten minste 1 maand. Bij patiënten bij wie immuungerelateerde bijwerkingen niet onder controle kunnen worden gebracht met het gebruik van corticosteroïden, kan toediening van andere systemische immunosuppressiva worden overwogen. 6 Lees, voordat u avelumab voorschrijft, de bijgaande Samenvatting van de productkenmerken Lees, voordat u avelumab voorschrijft, de bijgaande Samenvatting van de productkenmerken 7
5 / behandelen Immuungerelateerde pneumonitis Patiënten moeten worden gemonitord op klachten en verschijnselen van immuungerelateerde pneumonitis en andere oorzaken dan immuungerelateerde pneumonitis moeten worden uitgesloten. Vermoeden van pneumonitis moet worden bevestigd met radiografische beeldvorming. Corticosteroïden moeten worden toegediend voor voorvallen van graad 2 (initiële dosis van 1 tot 2 mg/kg/dag prednison of equivalent middel, waarna de corticosteroïden moeten worden afgebouwd). Avelumab moet worden onderbroken voor immuungerelateerde pneumonitis van graad 2 tot die verdwenen is, en moet definitief worden stopgezet voor immuungerelateerde pneumonitis van graad 3, graad 4 of recidief van graad 2. Immuungerelateerde hepatitis Patiënten moeten worden gemonitord op veranderingen in leverfunctie en verschijnselen van immuungerelateerde hepatitis, en andere oorzaken dan immuungerelateerde hepatitis moeten worden uitgesloten. Corticosteroïden moeten worden toegediend voor voorvallen van graad 2 (initiële dosis van 1 tot 2 mg/kg/dag prednison of equivalent middel, waarna de corticosteroïden moeten worden afgebouwd). Avelumab moet worden onderbroken voor immuungerelateerde hepatitis van graad 2 tot die verdwenen is, en moet definitief worden stopgezet voor immuungerelateerde hepatitis van graad 3 of graad 4. Immuungerelateerde colitis Patiënten moeten worden gemonitord op klachten en verschijnselen van immuungerelateerde colitis, en andere oorzaken dan immuungerelateerde colitis moeten worden uitgesloten. Corticosteroïden moeten worden toegediend voor voorvallen van graad 2 (initiële dosis van 1 tot 2 mg/kg/dag prednison of equivalent middel, waarna de corticosteroïden moeten worden afgebouwd zodra de verschijnselen verbeteren of verdwijnen). Avelumab moet worden onderbroken voor immuungerelateerde colitis van graad 2 of graad 3 tot die verdwenen is, en moet definitief worden stopgezet voor immuungerelateerde colitis van graad 4 of recidief van graad 3. Immuungerelateerde endocrinopathieën Patiënten moeten worden gemonitord op klinische klachten en verschijnselen van endocrinopathieën. Avelumab moet worden onderbroken voor endocrinopathieën van graad 3 of graad 4 tot ze verdwenen zijn. Schildklierstoornissen (hypothyreoïdie/hyperthyreoïdie) Patiënten moeten worden gemonitord op veranderingen in schildklierfunctie (bij aanvang van de behandeling, regelmatig tijdens de behandeling en indien aangewezen op basis van klinische evaluatie) alsook op klinische klachten en verschijnselen van schildklierstoornissen. Zo nodig moet hypothyreoïdie worden behandeld met substitutietherapie en hyperthyreoïdie met een antischildkliergeneesmiddel. Avelumab moet worden onderbroken voor schildklierstoornissen van graad 3 of graad 4. Bijnierinsufficiëntie Tijdens en na behandeling moeten patiënten worden gemonitord op klachten en verschijnselen van bijnierinsufficiëntie. Corticosteroïden moeten worden toegediend (1 tot 2 mg/kg/dag prednison intraveneus of oraal equivalent) voor bijnierinsufficiëntie van graad 3, waarna moet worden afgebouwd tot een dosis van 10 mg/dag is bereikt. Type 1 diabetes mellitus Patiënten moeten worden gemonitord op hyperglykemie of andere klachten en verschijnselen van diabetes. Behandeling met insuline moet worden ingesteld voor type 1 diabetes mellitus. Behandeling met insuline moet worden ingesteld voor type 1 diabetes mellitus. Bij patiënten met hyperglykemie van graad 3 moet avelumab worden onderbroken en moeten antihyperglykemische middelen worden toegediend. Behandeling met avelumab moet worden hervat wanneer het metabolisme onder controle is met substitutietherapie met insuline. 8 Lees, voordat u avelumab voorschrijft, de bijgaande Samenvatting van de productkenmerken Lees, voordat u avelumab voorschrijft, de bijgaande Samenvatting van de productkenmerken 9
6 Immuungerelateerde nefritis en nierdisfunctie Vóór en regelmatig tijdens de behandeling moeten patiënten worden gemonitord op verhoogde serumcreatininewaarden. Corticosteroïden (initiële dosis van 1 tot 2 mg/kg/dag prednison of equivalent middel, waarna de corticosteroïden moeten worden afgebouwd) moeten worden toegediend voor nefritis van graad 2. Avelumab moet worden onderbroken voor nefritis van graad 2 of graad 3 tot die is hersteld tot graad 1, en moet definitief worden stopgezet voor nefritis van graad 4. Andere immuungerelateerde bijwerkingen Andere klinisch belangrijke, immuungerelateerde bijwerkingen zijn gemeld bij minder dan 1% van de patiënten: myocarditis, waaronder gevallen met fatale afloop, myositis, hypopituïtarisme, uveïtis en Guillain-Barrésyndroom. Voor vermoeden van immuungerelateerde bijwerkingen moet een geschikte evaluatie plaatsvinden om de etiologie te bevestigen of om andere oorzaken uit te sluiten. Op basis van de ernst van de bijwerking moet avelumab worden onderbroken en moeten corticosteroïden worden toegediend. Avelumab moet worden hervat wanneer de immuungerelateerde bijwerking opnieuw graad 1 of lager wordt na het afbouwen van de corticosteroïden. Avelumab moet definitief worden stopgezet voor een immuungerelateerde bijwerking van graad 3 die opnieuw optreedt en voor een immuungerelateerde bijwerking van graad 4. Wat is de Informatiebrochure voor de patiënt? Belangrijke informatie over de behandeling met avelumab wordt benadrukt in een Informatiebrochure voor de patiënt. U kunt de brochure als gids gebruiken om een discussie met de patiënt over de behandeling op gang te brengen. Patiënten kunnen deze zo nodig zelf nalezen om hun behandelingsregime beter te begrijpen. Naast een overzicht van de behandeling bevat de Informatiebrochure voor de patiënt ook informatie over wat de patiënt moet doen wanneer deze een bijwerking krijgt (dat wil zeggen een immuungerelateerde bijwerking of een infusiegerelateerde reactie). In elke brochure is een Patiëntenwaarschuwingskaart opgenomen, die patiënten te allen tijde bij zich moeten dragen en bij alle medische bezoeken moeten laten zien aan andere beroepsbeoefenaren in de gezondheidszorg dan degene die avelumab heeft voorgeschreven. Instrueer de patiënt om alle relevante gedeelten van de kaart in te vullen, inclusief alle contactinformatie voor de voorschrijver, patiënt, en iedere hulpverlener die een rol speelt bij het helpen van de patiënt. Deze kaart kan in het bijzonder nuttig zijn bij bezoeken aan centra voor spoedeisende hulp, waar de patiënt mogelijk niet bekend is. Neem even de tijd om ervoor te zorgen dat patiënten begrijpen hoe zij de Patiëntenwaarschuwingskaart moeten gebruiken. Zie erop toe dat deze een samenvatting bevat over de behandeling en wat de aangewezen behandeling van bijwerkingen is. Benadruk bij de patiënt hoe belangrijk het is dat de kaart wordt ingevuld en dat de patiënt deze altijd bij zich heeft tijdens de behandeling. Het allerbelangrijkste is dat patiënten eraan moeten worden herinnerd dat zij, als zij een bijwerking krijgen, onmiddellijk medische hulp moeten inroepen en snel een behandeling moeten ondergaan. Infusiegerelateerde reacties Patiënten moeten worden gemonitord op klachten en verschijnselen van infusiegerelateerde reacties, waaronder pyrexie, koude rillingen, blozen, hypotensie, dyspneu, piepende ademhaling, rugpijn, buikpijn en urticaria. Voor infusiegerelateerde reacties van graad 3 of graad 4 moet de infusie worden gestaakt en moet avelumab definitief worden stopgezet. Voor infusiegerelateerde reacties van graad 1 moet de infusiesnelheid van de huidige infusie worden vertraagd met 50%. Voor patiënten met infusiegerelateerde reacties van graad 2 moet de infusie tijdelijk worden gestaakt tot de reacties van graad 1 of verdwenen zijn, waarna de infusie wordt hervat met een 50% lagere infusiesnelheid. In geval van recidief van een infusiegerelateerde reactie van graad 1 of graad 2 kan de patiënt avelumab blijven krijgen onder nauwlettend toezicht, na de aangewezen aanpassing van de infusiesnelheid en premedicatie met paracetamol en een antihistaminicum. 10 Lees, voordat u avelumab voorschrijft, de bijgaande Samenvatting van de productkenmerken Lees, voordat u avelumab voorschrijft, de bijgaande Samenvatting van de productkenmerken 11
7 Waar kan ik aanvullende informatie krijgen? U kunt extra materiaal opvragen via medical.info.nl@merckgroup.com onder vermelding van armm avelumab. Aanvullende informatie betreffende avelumab is beschikbaar in de Samenvatting van productkenmerken (SmPC) en bijsluiter op Melding van vermoedelijke bijwerkingen Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Voor het snel onderkennen van bijwerkingen blijven spontane meldingen van groot belang. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden. In Nederland kunt u vermoede bijwerkingen melden bij Nationaal Bijwerkingen Centrum Lareb. U kunt daarvoor gebruik maken van het meldingsformulier dat u op internet kunt vinden ( of in het Farmacotherapeutisch Kompas. Bijwerkingen kunnen ook altijd gemeld worden bij de houder van de handelsvergunning van het product. De naam en contactgegevens van de vergunninghouder staat vermeld op de verpakking en in de bijsluiter. Bijwerkingen moeten ook worden gemeld bij Merck B.V. door te bellen naar telefoonnummer: Lees, voordat u avelumab voorschrijft, de bijgaande Samenvatting van de productkenmerken
8 Avelumab 20 mg/ml concentraat voor oplossing voor infusie Risicominimalisatiemateriaal betreffende avelumab voor patiënten Versie 1.6, juli 2017
9 Introductie Deze materialen beschrijven aanbevelingen om belangrijke risico s van het geneesmiddel te beperken of te voorkomen en zijn beoordeeld door het College ter Beoordeling van Geneesmiddelen (CBG). Samenvatting: Bij ten minste de eerste 4 behandelingen krijgt u paracetamol en een antihistaminicum voordat u avelumab krijgt, om mogelijke bijwerkingen in verband met de infusie te helpen voorkomen. Inleiding Uw arts heeft avelumab voorgeschreven om uw kanker te behandelen. Zie de bijsluiter om te lezen wat avelumab is en waarvoor het wordt gebruikt. Deze brochure dient als gids voor uw behandeling, inclusief wat u kunt verwachten terwijl u dit geneesmiddel gebruikt. In deze brochure worden enkele van de bijwerkingen uitgelegd die kunnen optreden terwijl u een behandeling met avelumab ondergaat en hoe u hierop kunt controleren. U leest ook waarom het belangrijk is eventuele verschijnselen onmiddellijk bij uw arts te melden. Avelumab kan ernstige bijwerkingen veroorzaken die onmiddellijk moeten worden behandeld. Zoek dringende medische hulp als u ergens in uw lichaam een ontsteking heeft of als u een van de klachten of verschijnselen heeft, of als ze verergeren, zoals beschreven op pagina 5 & 6. Plak Patiëntenwaarschuwingskaart hier Stempel arts 2 3
10 Informatie over avelumab Avelumab is een geneesmiddel dat wordt gebruikt om bepaalde vormen van kanker te behandelen. Voordat u met avelumab begint Gebruikt u naast avelumab nog andere geneesmiddelen, heeft u dat kort geleden gedaan of bestaat de mogelijkheid dat u in de nabije toekomst andere geneesmiddelen gaat gebruiken? Vertel dat dan uw arts. Zorg ervoor dat uw arts het weet als u: een autoimmuunziekte heeft (een aandoening waarbij het lichaam zijn eigen cellen aanvalt); een infectie met het humaan immunodeficiëntievirus (HIV) of verworven immunodeficiëntiesyndroom (AIDS) heeft; ooit een chronische virusinfectie van de lever gehad heeft, inclusief hepatitis B (HBV) of hepatitis C (HCV); Wat u moet weten over uw behandeling Hoe krijgt u avelumab toegediend? Avelumab wordt aan u toegediend in een ziekenhuis of kliniek onder het toezicht van een ervaren arts. Uw arts geeft u om de 2 weken avelumab als een infusie (een druppelinfuus) in een ader (intraveneus) over een periode van 1 uur. Uw arts zal bepalen hoeveel behandelingen u nodig heeft. Zie de bijsluiter voor de aanbevolen dosering van avelumab. geneesmiddelen krijgt om uw immuunsysteem te onderdrukken; een orgaantransplantatie heeft ondergaan; nog andere geneesmiddelen gebruikt of dat kort geleden heeft gedaan; zwanger bent, denkt zwanger te zijn of zwanger wilt worden; een vrouw bent die zwanger kan worden. U moet effectieve anticonceptie gebruiken tijdens uw behandeling met avelumab en gedurende ten minste 1 maand na uw laatste dosis; borstvoeding geeft of van plan bent dit te doen. Geef geen borstvoeding tijdens uw behandeling met avelumab en gedurende ten minste 1 maand na uw laatste dosis. Voordat u avelumab toegediend krijgt Bij ten minste de eerste 4 behandelingen krijgt u paracetamol en een antihistaminicum voordat u avelumab krijgt, om mogelijke bijwerkingen in verband met de infusie te helpen voorkomen. Afhankelijk van hoe uw lichaam op de behandeling reageert, is het mogelijk dat uw arts beslist om u deze geneesmiddelen te blijven geven voorafgaand aan al uw behandelingen met avelumab. Het is voor u zeer belangrijk dat u al uw afspraken voor toediening van avelumab nakomt. Als u een afspraak heeft gemist, vraag dan uw arts wanneer uw volgende dosis moet worden gepland. Avelumab kan ernstige bijwerkingen veroorzaken die onmiddellijk moeten worden behandeld Mogelijke bijwerkingen Zoals elk geneesmiddel kan ook dit geneesmiddel bijwerkingen hebben, al krijgt niet iedereen daarmee te maken. Avelumab heeft een werking op uw immuunsysteem en kan een ontsteking veroorzaken in delen van uw lichaam. Een ontsteking kan ernstige schade veroorzaken aan uw lichaam; sommige aandoeningen met een ontsteking kunnen tot Bijwerkingen Infusiereacties Longproblemen (ontsteking van de longen) Leverproblemen (ontsteking van de lever) Darmproblemen (ontsteking van de darmen) Klachten en verschijnselen de dood leiden en moeten worden behandeld of vereisen stopzetting van avelumab. Zoek direct medische hulp als u één van deze verschijnselen krijgt of als deze verergeren. Deze kunnen zich tot weken of maanden na uw laatste dosis voordoen. Probeer niet uzelf te behandelen met andere geneesmiddelen: Kortademigheid of piepende ademhaling Koude rillingen of beven Huiduitslag met bultjes of kwaddels Blozen Lage bloeddruk (duizeligheid, vermoeidheid, misselijkheid) Koorts Rugpijn Buikpijn Ademhalingsproblemen Hoesten Gele verkleuring van uw huid (geelzucht) en het wit van uw ogen Ernstige misselijkheid of braken Pijn rechtsboven in de buik Sufheid Donkere urine (de kleur van thee) Gemakkelijker een bloeding of blauwe plek krijgen dan normaal Minder hongergevoel dan gebruikelijk Vermoeidheid Afwijkende leverfunctiewaarden Diarree (dunne stoelgang) Vaker ontlasting hebben dan gebruikelijk is Bloed in uw stoelgang of donkere, teerachtige, kleverige stoelgang Ernstige pijn of gevoeligheid van de buik (abdomen) 4 5
11 Bijwerkingen Problemen met de hormoonklieren (vooral schildklier, hypofyse, bijnieren) Klachten en verschijnselen Extreme vermoeidheid Snelle hartslag Meer zweten Veranderingen in stemming of gedrag, zoals prikkelbaarheid of vergeetachtigheid Gevoel van koude Zeer lage bloeddruk (flauwvallen, duizeligheid, vermoeidheid, misselijkheid) Gewichtsverandering Hoofdpijn Wat moet u doen als er verschijnselen optreden als u van huis bent? Het is belangrijk dat u altijd contact opneemt met uw arts als zich verschijnselen voordoen. Zorg ervoor dat u altijd uw Patiëntenwaarschuwingskaart met de contactgegevens van uw arts bij u heeft, zodat hij of zij bereikt kan worden in geval van nood. De Patiëntenwaarschuwingskaart bevat belangrijke informatie over uw verschijnselen, die onmiddellijk moet worden gemeld aan de arts of verpleegkundige die u behandelt als u van huis bent. Deze kaart waarschuwt andere artsen ook dat u wordt behandeld met avelumab. Type 1 diabetes, inclusief meer zuur in het bloed dat wordt veroorzaakt door diabetes (diabetische ketoacidose) Nierproblemen (ontsteking van de nieren) Problemen in andere organen Groter honger- of dorstgevoel dan gebruikelijk is Vaker moeten plassen Gewichtsverlies Gevoel van vermoeidheid Afwijkende nierfunctietestwaarden Minder plassen dan gebruikelijk is Bloed in uw urine Zwelling in uw enkels Spierpijn of spierzwakte Ademhalingsproblemen Duizeligheid of flauwvallen Koorts Pijn en beklemd gevoel op de borst Griepachtige verschijnselen Letten op bijwerkingen Het is belangrijk dat u zich bewust bent van verschijnselen Als u klachten of verschijnselen opmerkt tijdens uw behandeling met avelumab, moet u onmiddellijk contact opnemen met uw arts. Bijwerkingen kunnen zich nog tot weken of maanden na uw laatste dosis avelumab voordoen. Bepaalde geneesmiddelen, zoals corticosteroïden, kunnen worden gebruikt om ernstigere complicaties te voorkomen en uw verschijnselen te verminderen. Uw arts kan uw behandeling uitstellen of volledig stoppen als uw bijwerkingen te ernstig zijn. Mis geen afspraak voor de behandeling met avelumab Als u uw behandeling stopt of onderbreekt, is het mogelijk dat het effect van het geneesmiddel stopt. Stop de behandeling met avelumab niet, tenzij u dit met uw arts heeft besproken. Kom al uw afspraken zo goed mogelijk na en plan een nieuwe afspraak in zodra u er een mist. Neem onmiddellijk contact op met uw arts als u last krijgt van bijwerkingen. Dat geldt ook voor bijwerkingen die niet in deze brochure zijn vermeld. Neem contact op met uw arts indien u vragen heeft over avelumab of over hoe dit middel werkt. Draag uw Patiëntenwaarschuwingskaart altijd bij u. Avelumab is een soort therapie die het immuunsysteem van uw lichaam helpt uw kanker te bestrijden. Dit soort therapie kan soms bijwerkingen met zich meebrengen. Avelumab kan sommige bijwerkingen hebben die ernstig kunnen zijn. Neem onmiddellijk contact op met uw arts als u bijwerkingen krijgt. Praat met uw arts indien u vragen heeft over avelumab of over hoe dit middel werkt. 6 7
12 Waar kunt u aanvullende informatie vinden? Voor meer informatie kunt u de bijsluiter van avelumab raadplegen op of Merck B.V. Medical Information bellen op Het melden van bijwerkingen Krijgt u last van bijwerkingen, neem dan contact op met uw arts, apotheker of verpleegkundige. Dit geldt ook voor mogelijke bijwerkingen die niet in de bijsluiter staan. Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. U kunt hieraan bijdragen door elke bijwerking die u ondervindt te melden. In Nederland kunt u vermoede bijwerkingen melden bij Nationaal Bijwerkingen Centrum Lareb. U kunt daarvoor gebruik maken van het meldingsformulier dat u op internet kunt vinden ( Bijwerkingen kunnen ook altijd gemeld worden bij de houder van de handelsvergunning van het product. De naam en contactgegevens van de vergunninghouder staat vermeld op de verpakking en in de bijsluiter. 8
13 BELANGRIJKE CONTACTINFORMATIE Avelumab 20 mg/ml concentraat voor oplossing voor infusie Naam specialist Telefoonnummer buiten werktijden Mijn naam Contactpersoon noodgeval (naam) PATIËNTEN- WAARSCHUWINGSKAART Telefoonnummer BELANGRIJKE INFORMATIE VOOR BEROEPSBEOEFENAREN IN DE GEZONDHEIDSZORG Mijn telefoonnummer Contactpersoon noodgeval (telefoonnummer) Deze waarschuwingskaart beschrijft aanbevelingen om belangrijke risico s van het geneesmiddel te beperken of te voorkomen en zijn beoordeeld door het College ter Beoordeling van Geneesmiddelen (CBG). Deze patiënt wordt behandeld met avelumab. Dit middel kan infusiegerelateerde reacties en immuungerelateerde bijwerkingen veroorzaken in de longen, lever, darmen, hormoonklieren, nieren en andere organen. Een vroege diagnose en passende behandeling zijn essentieel om eventuele gevolgen van immuungerelateerde bijwerkingen tot een minimum te beperken. Voor vermoedelijke immuungerelateerde bijwerkingen dient een adequate evaluatie plaats te vinden om de etiologie te bevestigen of andere oorzaken uit te sluiten. Op basis van de ernst van de bijwerking moet avelumab worden onderbroken en moeten corticosteroïden worden toegediend. Als corticosteroïden worden gebruikt om een bijwerking te behandelen, moet bij verbetering het gebruik worden afgebouwd over een periode van ten minste 1 maand. Bij patiënten bij wie immuungerelateerde bijwerkingen niet onder controle kunnen worden gebracht met het gebruik van corticosteroïden, kan toediening van andere systemische immunosuppressiva worden overwogen. Specifieke richtlijnen voor het behandelen van immuungerelateerde bijwerkingen zijn beschikbaar in de Samenvatting van de productkenmerken van avelumab. Beoordeel patiënten op klachten en verschijnselen van pneumonitis, hepatitis, colitis, endocrinopathieën, waaronder schildklierstoornissen (hypothyreoïdie/ Raadpleeg de Samenvatting van de productkenmerken voor avelumab via of bel hyperthyreoïdie), bijnierinsufficiëntie, type 1 diabetes mellitus, nefritis en nierdisfunctie, en andere immuungerelateerde bijwerkingen die zijn gemeld bij patiënten die avelumab krijgen: myocarditis, waaronder gevallen met fatale afloop, myositis, hypopituïtarisme, uveïtis en Guillain-Barrésyndroom. Merck Medical Information op telefoonnummer: voor meer informatie. Versie 1.6, juli 2017
14 AVELUMAB KAN ERNSTIGE BIJWERKINGEN VEROORZAKEN Infusiereacties: Darmen: Type 1 diabetes: Neem onmiddellijk contact op met uw specialist indien u één van de hieronder vermelde klachten of verschijnselen ontwikkelt. Het is mogelijk dat uw arts u andere geneesmiddelen geeft om ernstigere complicaties te voorkomen en uw verschijnselen te verminderen. BELANGRIJK Probeer bijwerkingen niet zelf te diagnosticeren of te behandelen. Draag deze Patiëntenwaarschuwingskaart altijd bij u, in het bijzonder wanneer u op reis bent, telkens wanneer u de Spoedeisende hulp bezoekt, of wanneer u een andere arts, verpleegkundige of apotheker moet bezoeken. Zorg ervoor dat u iedere beroepsbeoefenaar in de gezondheidszorg die u bezoekt, laat weten dat u wordt behandeld met avelumab en laat hem of haar deze kaart zien. Het is mogelijk dat uw arts de volgende dosis avelumab uitstelt of uw behandeling helemaal stopzet. Voor aanvullende informatie raadpleegt u de bijsluiter of belt u Merck Medical Information op Krijgt u last van bijwerkingen, neem dan contact op met uw arts, apotheker of verpleegkundige. Dit geldt ook voor mogelijke bijwerkingen die niet in de bijsluiter staan. U kunt bijwerkingen ook rechtstreeks melden via het Nederlands Bijwerkingen Centrum Lareb, website Door bijwerkingen te melden, kunt u ons helpen meer informatie te verkrijgen over de veiligheid van dit geneesmiddel. Kortademigheid of piepende ademhaling Koude rillingen of beven Huiduitslag met bultjes of kwaddels Blozen Lage bloeddruk (duizeligheid, vermoeidheid, misselijkheid) Koorts Rugpijn Buikpijn Longen: Ademhalingsproblemen Hoesten Lever: Gele verkleuring van uw huid (geelzucht) en het wit van uw ogen Ernstige misselijkheid of braken Pijn rechtsboven in de buik (abdomen) Sufheid Donkere urine (de kleur van thee) Gemakkelijker een bloeding of blauwe plek krijgen dan normaal Minder hongergevoel dan gebruikelijk Vermoeidheid Afwijkende leverfunctiewaarden Diarree (dunne stoelgang) Vaker ontlasting hebben dan gebruikelijk is Bloed in uw stoelgang of donkere, teerachtige, kleverige stoelgang Ernstige pijn of gevoeligheid van de buik (abdomen) Hormoonklieren: Extreme vermoeidheid Snelle hartslag Meer zweten Veranderingen in stemming of gedrag, zoals prikkelbaarheid of vergeetachtigheid Gevoel van koude Zeer lage bloeddruk (flauwvallen, duizeligheid, vermoeidheid, misselijkheid) Gewichtsverandering Hoofdpijn Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. U kunt hieraan bijdragen door elke bijwerking die u ondervindt te melden. In Nederland kunt u vermoede bijwerkingen melden bij Nationaal Bijwerkingen Centrum Lareb. Groter honger- of dorstgevoel dan gebruikelijk is Vaker moeten plassen Gewichtsverlies Gevoel van vermoeidheid Nieren: Afwijkende nierfunctiewaarden Minder plassen dan gebruikelijk is Bloed in uw urine Zwelling in uw enkels Andere organen: Spierpijn of spierzwakte Ademhalingsproblemen Duizeligheid of flauwvallen Koorts Pijn en beklemd gevoel op de borst Griepachtige symptomen U kunt daarvoor gebruik maken van het meldingsformulier dat u op internet kunt vinden ( Bijwerkingen kunnen ook altijd gemeld worden bij de houder van de handelsvergunning van het product. De naam en contactgegevens van de vergunninghouder staat vermeld op de verpakking en in de bijsluiter.
Dit geneesmiddel is onderworpen aan aanvullende monitoring
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Bavencio. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Bavencio. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
KEYTRUDA (pembrolizumab)
 Risicominimalisatiemateriaal betreffende Keytruda (pembrolizumab) voor patiënten KEYTRUDA (pembrolizumab) Patiënteninformatiefolder Risicominimalisatiemateriaal betreffende Keytruda (pembrolizumab) voor
Risicominimalisatiemateriaal betreffende Keytruda (pembrolizumab) voor patiënten KEYTRUDA (pembrolizumab) Patiënteninformatiefolder Risicominimalisatiemateriaal betreffende Keytruda (pembrolizumab) voor
KEYTRUDA (pembrolizumab)
 Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab) voor patiënten KEYTRUDA (pembrolizumab) Patiënteninformatiefolder Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab)
Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab) voor patiënten KEYTRUDA (pembrolizumab) Patiënteninformatiefolder Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab)
Risicominimalisatiemateriaal betreffende pembrolizumab voor patiënten PEMBROLIZUMAB. Patiënteninformatiefolder
 Risicominimalisatiemateriaal betreffende pembrolizumab voor patiënten PEMBROLIZUMAB Patiënteninformatiefolder Risicominimalisatiemateriaal betreffende pembrolizumab voor patiënten PEMBROLIZUMAB Patiënteninformatiefolder
Risicominimalisatiemateriaal betreffende pembrolizumab voor patiënten PEMBROLIZUMAB Patiënteninformatiefolder Risicominimalisatiemateriaal betreffende pembrolizumab voor patiënten PEMBROLIZUMAB Patiënteninformatiefolder
RMA gewijzigde versie 10/2017 KEYTRUDA. (pembrolizumab) Dit geneesmiddel is onderworpen aan aanvullende monitoring. Patiëntenwaarschuwingskaart
 RMA gewijzigde versie 10/2017 KEYTRUDA (pembrolizumab) Dit geneesmiddel is onderworpen aan aanvullende monitoring. Patiëntenwaarschuwingskaart Bewaar deze kaart altijd bij u en laat deze kaart zien aan
RMA gewijzigde versie 10/2017 KEYTRUDA (pembrolizumab) Dit geneesmiddel is onderworpen aan aanvullende monitoring. Patiëntenwaarschuwingskaart Bewaar deze kaart altijd bij u en laat deze kaart zien aan
Belangrijke informatie over pembrolizumab voor patiënten PEMBROLIZUMAB. Patiënteninformatiefolder
 Belangrijke informatie over pembrolizumab voor patiënten PEMBROLIZUMAB Patiënteninformatiefolder Belangrijke informatie over pembrolizumab voor patiënten PEMBROLIZUMAB Patiënteninformatiefolder Uw arts
Belangrijke informatie over pembrolizumab voor patiënten PEMBROLIZUMAB Patiënteninformatiefolder Belangrijke informatie over pembrolizumab voor patiënten PEMBROLIZUMAB Patiënteninformatiefolder Uw arts
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Patiënteninformatiebrochure
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel KEYTRUDA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel KEYTRUDA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
BELANGRIJKE VEILIGHEIDSINFORMATIE OM HET RISICO OP IMMUUNGERELATEERDE BIJWERKINGEN TOT EEN MINIMUM TE BEPERKEN
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Bavencio. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Bavencio. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Bijsluiter: informatie voor de patiënt. Bavencio 20 mg/ml concentraat voor oplossing voor infusie avelumab
 Bijsluiter: informatie voor de patiënt Bavencio 20 mg/ml concentraat voor oplossing voor infusie avelumab Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie
Bijsluiter: informatie voor de patiënt Bavencio 20 mg/ml concentraat voor oplossing voor infusie avelumab Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie
Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab) voor de voorschrijver, apotheker en verpleegkundige. KEYTRUDA (pembrolizumab)
 Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab) voor de voorschrijver, apotheker en verpleegkundige. KEYTRUDA (pembrolizumab) 1 Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab)
Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab) voor de voorschrijver, apotheker en verpleegkundige. KEYTRUDA (pembrolizumab) 1 Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab)
Uw behandeling met YERVOY (ipilimumab)
 Uw behandeling met YERVOY (ipilimumab) Patiëntenfolder YERVOY is onderworpen aan aanvullende monitoring. U wordt verzocht alle vermoedelijke bijwerkingen te melden. Dit educatieve materiaal is een verplichte
Uw behandeling met YERVOY (ipilimumab) Patiëntenfolder YERVOY is onderworpen aan aanvullende monitoring. U wordt verzocht alle vermoedelijke bijwerkingen te melden. Dit educatieve materiaal is een verplichte
YERVOY. (ipilimumab) Concentraat voor oplossing voor infusie Dit geneesmiddel is onderworpen aan aanvullende monitoring.
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
YERVOY. (ipilimumab) Concentraat voor oplossing voor infusie. Patiëntenbrochure. met patiëntenwaarschuwingskaart
 Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel YERVOY, om voor een goed gebruik ervan te zorgen en om de ongewenste effecten ervan te beperken, zijn er bepaalde
Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel YERVOY, om voor een goed gebruik ervan te zorgen en om de ongewenste effecten ervan te beperken, zijn er bepaalde
Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab) voor voorschrijvende artsen. KEYTRUDA (pembrolizumab)
 Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab) voor voorschrijvende artsen KEYTRUDA (pembrolizumab) 1 Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab) voor voorschrijvende
Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab) voor voorschrijvende artsen KEYTRUDA (pembrolizumab) 1 Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab) voor voorschrijvende
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Patiënteninformatiebrochure
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel KEYTRUDA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel KEYTRUDA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Patiëntenfolder
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel YERVOY. Het verplichte plan voor risicobeperking in België, waarvan deze informatie
Risicominimalisatiemateriaal over de risico s van pembrolizumab voor de voorschrijver, apotheker en verpleegkundige PEMBROLIZUMAB
 Risicominimalisatiemateriaal over de risico s van pembrolizumab voor de voorschrijver, apotheker en verpleegkundige PEMBROLIZUMAB 1 Risicominimalisatiemateriaal over de risico s van pembrolizumab voor
Risicominimalisatiemateriaal over de risico s van pembrolizumab voor de voorschrijver, apotheker en verpleegkundige PEMBROLIZUMAB 1 Risicominimalisatiemateriaal over de risico s van pembrolizumab voor
RISICO MINIMALISATIE MATERIAAL BETREFFENDE BARICITINIB VOOR DE VOORSCHRIJVER, APOTHEKER EN VERPLEEGKUNDIGE
 RISICO MINIMALISATIE MATERIAAL BETREFFENDE BARICITINIB VOOR DE VOORSCHRIJVER, APOTHEKER EN VERPLEEGKUNDIGE De risico minimalisatie materialen voor baricitinib zijn beoordeeld door het College ter Beoordeling
RISICO MINIMALISATIE MATERIAAL BETREFFENDE BARICITINIB VOOR DE VOORSCHRIJVER, APOTHEKER EN VERPLEEGKUNDIGE De risico minimalisatie materialen voor baricitinib zijn beoordeeld door het College ter Beoordeling
RISICO MINIMALISATIE MATERIAAL BETREFFENDE BARICITINIB VOOR DE VOORSCHRIJVER, APOTHEKER EN VERPLEEGKUNDIGE
 RISICO MINIMALISATIE MATERIAAL BETREFFENDE BARICITINIB VOOR DE VOORSCHRIJVER, APOTHEKER EN VERPLEEGKUNDIGE De risico minimalisatie materialen voor baricitinib zijn beoordeeld door het College ter Beoordeling
RISICO MINIMALISATIE MATERIAAL BETREFFENDE BARICITINIB VOOR DE VOORSCHRIJVER, APOTHEKER EN VERPLEEGKUNDIGE De risico minimalisatie materialen voor baricitinib zijn beoordeeld door het College ter Beoordeling
Risicominimalisatiemateriaal betreffende pembrolizumab voor de voorschrijver, apotheker en verpleegkundige. PEMBROLIZUMAB
 Risicominimalisatiemateriaal betreffende pembrolizumab voor de voorschrijver, apotheker en verpleegkundige. PEMBROLIZUMAB 1 Risicominimalisatiemateriaal betreffende pembrolizumab voor de voorschrijver,
Risicominimalisatiemateriaal betreffende pembrolizumab voor de voorschrijver, apotheker en verpleegkundige. PEMBROLIZUMAB 1 Risicominimalisatiemateriaal betreffende pembrolizumab voor de voorschrijver,
Risico Minimalisatie Materiaal. betreffende tolcapon 100 mg en 200 mg tabletten. voor patiënten
 Risico Minimalisatie Materiaal betreffende tolcapon 100 mg en 200 mg tabletten voor patiënten Inleiding Dit dagboek beschrijft aanbevelingen om belangrijke risico s van het geneesmiddel te beperken of
Risico Minimalisatie Materiaal betreffende tolcapon 100 mg en 200 mg tabletten voor patiënten Inleiding Dit dagboek beschrijft aanbevelingen om belangrijke risico s van het geneesmiddel te beperken of
Behandeling met ustekinumab. Risico minimalisatie materiaal: Veiligheidsinformatie betreffende ustekinumab voor patiënten
 Behandeling met ustekinumab Risico minimalisatie materiaal: Veiligheidsinformatie betreffende ustekinumab voor patiënten Belangrijke informatie Deze materialen beschrijven aanbevelingen om belangrijke
Behandeling met ustekinumab Risico minimalisatie materiaal: Veiligheidsinformatie betreffende ustekinumab voor patiënten Belangrijke informatie Deze materialen beschrijven aanbevelingen om belangrijke
Voorlichtingsmateriaal betreffende sebelipase alfa voor de zorgverlener. Belangrijke veiligheidsinformatie
 Voorlichtingsmateriaal betreffende sebelipase alfa voor de zorgverlener Belangrijke veiligheidsinformatie Risico minimalisatie materiaal betreffende sebelipase alfa voor zorgverleners - versie 2-03/2018
Voorlichtingsmateriaal betreffende sebelipase alfa voor de zorgverlener Belangrijke veiligheidsinformatie Risico minimalisatie materiaal betreffende sebelipase alfa voor zorgverleners - versie 2-03/2018
Voorlichtingsbrochure voor patiënten
 tolvaptan Voorlichtingsbrochure voor patiënten Additioneel risicominimalisatie-materiaal betreffende tolvaptan voor patiënten Samenvatting van risico s en risicobeperkende maatregelen. Het gebruik van
tolvaptan Voorlichtingsbrochure voor patiënten Additioneel risicominimalisatie-materiaal betreffende tolvaptan voor patiënten Samenvatting van risico s en risicobeperkende maatregelen. Het gebruik van
Risicominimalisatiemateriaal betreffende pembrolizumab voor de voorschrijver, apotheker en verpleegkundige. PEMBROLIZUMAB
 Risicominimalisatiemateriaal betreffende pembrolizumab voor de voorschrijver, apotheker en verpleegkundige. PEMBROLIZUMAB 1 Risicominimalisatiemateriaal betreffende pembrolizumab voor de voorschrijver,
Risicominimalisatiemateriaal betreffende pembrolizumab voor de voorschrijver, apotheker en verpleegkundige. PEMBROLIZUMAB 1 Risicominimalisatiemateriaal betreffende pembrolizumab voor de voorschrijver,
Risicominimalisatiemateriaal voor patiënten die worden behandeld met rituximab
 Risicominimalisatiemateriaal voor patiënten die worden behandeld met rituximab Dit materiaal beschrijft aanbevelingen om belangrijke risico s van het geneesmiddel te beperken of te voorkomen en zijn beoordeeld
Risicominimalisatiemateriaal voor patiënten die worden behandeld met rituximab Dit materiaal beschrijft aanbevelingen om belangrijke risico s van het geneesmiddel te beperken of te voorkomen en zijn beoordeeld
RISICO MINIMALISATIE MATERIAAL BETREFFENDE FLIXABI (INFLIXIMAB) VOOR VOORSCHRIJVERS
 Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke
Risicominimalisatiemateriaal over de risico s van pembrolizumab voor de voorschrijver, apotheker en verpleegkundige PEMBROLIZUMAB
 Risicominimalisatiemateriaal over de risico s van pembrolizumab voor de voorschrijver, apotheker en verpleegkundige PEMBROLIZUMAB 1 Risicominimalisatiemateriaal over de risico s van pembrolizumab voor
Risicominimalisatiemateriaal over de risico s van pembrolizumab voor de voorschrijver, apotheker en verpleegkundige PEMBROLIZUMAB 1 Risicominimalisatiemateriaal over de risico s van pembrolizumab voor
Behandeling met Entyvio (vedolizumab)
 Praat met uw arts als u graag meer informatie wilt over de behandeling met. Behandeling met (vedolizumab) Meer informatie Deze brochure is een aanvulling op de bijsluiter. We hopen dat de meeste vragen
Praat met uw arts als u graag meer informatie wilt over de behandeling met. Behandeling met (vedolizumab) Meer informatie Deze brochure is een aanvulling op de bijsluiter. We hopen dat de meeste vragen
Patiënteninformatie. Pembrolizumab (Keytruda )
 Patiënteninformatie Pembrolizumab (Keytruda ) Inhoud Inhoud... 2 Inleiding... 3 Wat u moet weten over uw behandeling Pembrolizumab... 3 Wat is de samenstelling van deze therapie?... 3 Waar wordt de therapie
Patiënteninformatie Pembrolizumab (Keytruda ) Inhoud Inhoud... 2 Inleiding... 3 Wat u moet weten over uw behandeling Pembrolizumab... 3 Wat is de samenstelling van deze therapie?... 3 Waar wordt de therapie
Risico minimalisatie materialen betreffende Inflectra (infliximab) voor de voorschrijvers
 Inflectra (infliximab) Dit geneesmiddel is onderworpen aan aanvullende monitoring Risico minimalisatie materialen betreffende Inflectra (infliximab) voor de voorschrijvers De risico minimalisatie materialen
Inflectra (infliximab) Dit geneesmiddel is onderworpen aan aanvullende monitoring Risico minimalisatie materialen betreffende Inflectra (infliximab) voor de voorschrijvers De risico minimalisatie materialen
Risicominimalisatie-materiaal voor patiënten die worden behandeld met rituximab
 Risicominimalisatie-materiaal voor patiënten die worden behandeld met rituximab Let op bij gebruik van rituximab. Rituximab is het werkzaam bestanddeel in het medicijn. Uw medicijn kan ook een andere (merk)naam
Risicominimalisatie-materiaal voor patiënten die worden behandeld met rituximab Let op bij gebruik van rituximab. Rituximab is het werkzaam bestanddeel in het medicijn. Uw medicijn kan ook een andere (merk)naam
Samenvatting van risico s en acties om deze te voorkomen of verminderen:
 T.a.v. Adresregel 1 Adresregel 2 Risico minimalisatie materialen betreffende: BOTOX, botulinum toxine type A, voor artsen en patiënten. Geachte Heer / Mevrouw In overleg met het College ter Beoordeling
T.a.v. Adresregel 1 Adresregel 2 Risico minimalisatie materialen betreffende: BOTOX, botulinum toxine type A, voor artsen en patiënten. Geachte Heer / Mevrouw In overleg met het College ter Beoordeling
Patiënten brochure betreffende XALKORI (crizotinib) voor patiënten die XALKORI voorgeschreven hebben gekregen.
 Patiënten brochure betreffende XALKORI (crizotinib) voor patiënten die XALKORI voorgeschreven hebben gekregen. XALK 030 januari 2017 Opgesteld in september 2016 678059_XalkoriPatBroch_newer.indd 1 26-01-17
Patiënten brochure betreffende XALKORI (crizotinib) voor patiënten die XALKORI voorgeschreven hebben gekregen. XALK 030 januari 2017 Opgesteld in september 2016 678059_XalkoriPatBroch_newer.indd 1 26-01-17
Risicominimalisatiemateriaal betreffende Valdoxan (agomelatine) voor zorgverleners:
 Risicominimalisatiemateriaal betreffende Valdoxan (agomelatine) voor zorgverleners: hernieuwde aandacht t.b.v. aanbevelingen voor monitoring van de leverfunctie Valdoxan en het risico op levertoxiciteit
Risicominimalisatiemateriaal betreffende Valdoxan (agomelatine) voor zorgverleners: hernieuwde aandacht t.b.v. aanbevelingen voor monitoring van de leverfunctie Valdoxan en het risico op levertoxiciteit
KEYTRUDA. Brochure voor beroepsbeoefenaren met veelgestelde vragen (FAQ) (pembrolizumab)
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel KEYTRUDA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel KEYTRUDA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Voorlichtingsmateriaal betreffende Kanuma (sebelipase alfa) voor de zorgverlener. Belangrijke veiligheidsinformatie
 Voorlichtingsmateriaal betreffende Kanuma (sebelipase alfa) voor de zorgverlener Belangrijke veiligheidsinformatie Risico minimalisatie materiaal KANUMA - versie 05/2016 De risico minimalisatie materialen
Voorlichtingsmateriaal betreffende Kanuma (sebelipase alfa) voor de zorgverlener Belangrijke veiligheidsinformatie Risico minimalisatie materiaal KANUMA - versie 05/2016 De risico minimalisatie materialen
Ustekinumab. (Stelara) Dermatologie
 Ustekinumab (Stelara) Dermatologie Inhoudsopgave Inleiding 4 1. Hoe werkt Ustekinumab (Stelara) 4 2. Wat moet u weten voordat u Ustekinumab (Stelara) gebruikt 5 Gebruik Ustekinumab (Stelara) niet 5 Wees
Ustekinumab (Stelara) Dermatologie Inhoudsopgave Inleiding 4 1. Hoe werkt Ustekinumab (Stelara) 4 2. Wat moet u weten voordat u Ustekinumab (Stelara) gebruikt 5 Gebruik Ustekinumab (Stelara) niet 5 Wees
Patiënteninformatie over ernstige primaire IGF-1-deficiëntie en hoe Increlex daarbij kan helpen
 Ipsen Endocrinologie Increlex (injectie met mecasermine [rdna-herkomst]) Patiënteninformatie over ernstige primaire IGF-1-deficiëntie en hoe Increlex daarbij kan helpen Voorlichtingsfolder zoals beschreven
Ipsen Endocrinologie Increlex (injectie met mecasermine [rdna-herkomst]) Patiënteninformatie over ernstige primaire IGF-1-deficiëntie en hoe Increlex daarbij kan helpen Voorlichtingsfolder zoals beschreven
Informatieve brochure voor refractaire gmg-patiënten
 BELANGRIJKE VEILIGHEIDSINFORMATIE 1 Ten gevolge van het werkingsmechanisme verhoogt het gebruik van SOLIRIS de vatbaarheid van de patiënt voor meningokokkeninfecties (Neisseria meningitidis). Derhalve
BELANGRIJKE VEILIGHEIDSINFORMATIE 1 Ten gevolge van het werkingsmechanisme verhoogt het gebruik van SOLIRIS de vatbaarheid van de patiënt voor meningokokkeninfecties (Neisseria meningitidis). Derhalve
Risico minimalisatie materiaal betreffende Aripiprazol Sandoz (aripiprazol)
 Risico minimalisatie materiaal betreffende Aripiprazol Sandoz (aripiprazol) Dit risico materiaal is beoordeeld door het College ter Beoordeling van Geneesmiddelen (CBG) en beschrijft aanbevelingen voor
Risico minimalisatie materiaal betreffende Aripiprazol Sandoz (aripiprazol) Dit risico materiaal is beoordeeld door het College ter Beoordeling van Geneesmiddelen (CBG) en beschrijft aanbevelingen voor
Belangrijke veiligheidsinformatie over dapagliflozine alleen voor diabetes type 1
 Belangrijke veiligheidsinformatie over dapagliflozine alleen voor diabetes type 1 Let op bij het gebruik van dapagliflozine. Dapagliflozine is het werkzame bestanddeel in het medicijn. Uw medicijn kan
Belangrijke veiligheidsinformatie over dapagliflozine alleen voor diabetes type 1 Let op bij het gebruik van dapagliflozine. Dapagliflozine is het werkzame bestanddeel in het medicijn. Uw medicijn kan
Belangrijke aandachtspunten
 1.8.2 armm Rev.nr. 1711 Pag. 1 van Risicominimalisatiemateriaal voor voorschrijvers Brochure controle nierfunctie bij behandeling van volwassenen met chronische hepatitis B De risico minimalisatie materialen
1.8.2 armm Rev.nr. 1711 Pag. 1 van Risicominimalisatiemateriaal voor voorschrijvers Brochure controle nierfunctie bij behandeling van volwassenen met chronische hepatitis B De risico minimalisatie materialen
Bijsluiter: informatie voor de patiënt. Removab 10 microgram concentraat voor oplossing voor infusie catumaxomab
 Bijsluiter: informatie voor de patiënt Removab 10 microgram concentraat voor oplossing voor infusie catumaxomab Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
Bijsluiter: informatie voor de patiënt Removab 10 microgram concentraat voor oplossing voor infusie catumaxomab Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
Vedolizumab (Entyvio ) bij de ziekte van Crohn en colitis ulcerosa
 Vedolizumab (Entyvio ) bij de ziekte van Crohn en colitis ulcerosa Ziekenhuis Gelderse Vallei Uw behandelend arts heeft met u gesproken over het gebruik van Vedolizumab (Entyvio ). In deze folder krijgt
Vedolizumab (Entyvio ) bij de ziekte van Crohn en colitis ulcerosa Ziekenhuis Gelderse Vallei Uw behandelend arts heeft met u gesproken over het gebruik van Vedolizumab (Entyvio ). In deze folder krijgt
dagziekenhuis inwendige geneeskunde Zoledroninezuur
 dagziekenhuis inwendige geneeskunde Zoledroninezuur Inhoud Zoledroninezuur 3 Voorbereiding 3 Rijvaardigheid en gebruik van machines 3 Gebruik bij ouderen 4 Uitzonderingen bij gebruik 4 Combinatie met andere
dagziekenhuis inwendige geneeskunde Zoledroninezuur Inhoud Zoledroninezuur 3 Voorbereiding 3 Rijvaardigheid en gebruik van machines 3 Gebruik bij ouderen 4 Uitzonderingen bij gebruik 4 Combinatie met andere
BELANGRIJKE VEILIGHEIDSINFORMATIE
 Aanbevelingen Neem de volledige medische voorgeschiedenis van de patiënt in overweging, inclusief enig eerder of gelijktijdig gebruikte biological BELANGRIJKE VEILIGHEIDSINFORMATIE Er is geen ervaring
Aanbevelingen Neem de volledige medische voorgeschiedenis van de patiënt in overweging, inclusief enig eerder of gelijktijdig gebruikte biological BELANGRIJKE VEILIGHEIDSINFORMATIE Er is geen ervaring
JINARC (tolvaptan) Voorlichtingsbrochure voor patiënten. Dit geneesmiddel is onderworpen aan aanvullende monitoring.
 Om maximaal voordeel te halen uit de effecten van JINARC op uw gezondheid, het juiste gebruik ervan te verzekeren en de ongewenste effecten ervan te beperken, zijn er bepaalde maatregelen/voorzorgsmaatregelen
Om maximaal voordeel te halen uit de effecten van JINARC op uw gezondheid, het juiste gebruik ervan te verzekeren en de ongewenste effecten ervan te beperken, zijn er bepaalde maatregelen/voorzorgsmaatregelen
Risicominimalisatiemateriaal betreffende rituximab* voor zorgverleners
 Risicominimalisatiemateriaal betreffende rituximab* voor zorgverleners *voor niet-oncologische indicaties Dit risicominimalisatiemateriaal werd goedgekeurd door het College ter Beoordeling van Geneesmiddelen
Risicominimalisatiemateriaal betreffende rituximab* voor zorgverleners *voor niet-oncologische indicaties Dit risicominimalisatiemateriaal werd goedgekeurd door het College ter Beoordeling van Geneesmiddelen
Rituximab waarschuwingskaart
 Rituximab waarschuwingskaart voor patiënten met andere aandoeningen dan kanker Waarom heb ik deze kaart ontvangen? Dit geneesmiddel kan de kans op een infectie vergroten. Deze kaart bevat informatie over:
Rituximab waarschuwingskaart voor patiënten met andere aandoeningen dan kanker Waarom heb ik deze kaart ontvangen? Dit geneesmiddel kan de kans op een infectie vergroten. Deze kaart bevat informatie over:
Emtricitabine/Tenofovirdisoproxil Krka 200 mg/245 mg filmomhulde tabletten (emtricitabine/tenofovirdisoproxil)
 Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel Emtricitabine/Tenofovirdisoproxil Krka 200 mg/245 mg filmomhulde tabletten, om voor een goed gebruik ervan te zorgen
Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel Emtricitabine/Tenofovirdisoproxil Krka 200 mg/245 mg filmomhulde tabletten, om voor een goed gebruik ervan te zorgen
Wat u zou moeten weten over Rixathon
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Rixathon. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Rixathon. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKERS. Removab 10 microgram concentraat voor oplossing voor infusie catumaxomab
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKERS Removab 10 microgram concentraat voor oplossing voor infusie catumaxomab Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken - Bewaar deze bijsluiter.
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKERS Removab 10 microgram concentraat voor oplossing voor infusie catumaxomab Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken - Bewaar deze bijsluiter.
Bijsluiter: informatie voor de patiënt. Cardene IV, 1 mg/ml oplossing voor infusie. nicardipinehydrochloride
 BIJSLUITER Bijsluiter: informatie voor de patiënt Cardene IV, 1 mg/ml oplossing voor infusie nicardipinehydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat
BIJSLUITER Bijsluiter: informatie voor de patiënt Cardene IV, 1 mg/ml oplossing voor infusie nicardipinehydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat
INFLECTRA (infliximab) RISICO MINIMALISATIE MATERIALEN BETREFFENDE INFLECTRA (INFLIXIMAB) VOOR DE VOORSCHRIJVERS. Biologics
 INFLECTRA (infliximab) Dit geneesmiddel is onderworpen aan aanvullende monitoring RISICO MINIMALISATIE MATERIALEN BETREFFENDE INFLECTRA (INFLIXIMAB) VOOR DE VOORSCHRIJVERS De risico minimalisatie materialen
INFLECTRA (infliximab) Dit geneesmiddel is onderworpen aan aanvullende monitoring RISICO MINIMALISATIE MATERIALEN BETREFFENDE INFLECTRA (INFLIXIMAB) VOOR DE VOORSCHRIJVERS De risico minimalisatie materialen
Infliximab (Inflectra ) Bij de ziekte van Crohn of colitis ulcerosa
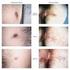 Infliximab (Inflectra ) Bij de ziekte van Crohn of colitis ulcerosa Ziekenhuis Gelderse Vallei Uw behandelend arts en/of verpleegkundige heeft met u gesproken over het gebruik van Infliximab (Inflectra
Infliximab (Inflectra ) Bij de ziekte van Crohn of colitis ulcerosa Ziekenhuis Gelderse Vallei Uw behandelend arts en/of verpleegkundige heeft met u gesproken over het gebruik van Infliximab (Inflectra
Prednison bij ziekte van Crohn en colitis ulcerosa Maag-Darm-Levercentrum
 Prednison bij ziekte van Crohn en colitis ulcerosa Maag-Darm-Levercentrum Beter voor elkaar Inleiding De maag-darm-leverarts (MDL-arts) heeft samen met u besloten om u te behandelen met Prednison. In deze
Prednison bij ziekte van Crohn en colitis ulcerosa Maag-Darm-Levercentrum Beter voor elkaar Inleiding De maag-darm-leverarts (MDL-arts) heeft samen met u besloten om u te behandelen met Prednison. In deze
Risico minimalisatie materiaal betreffende tenofovirdisoproxil voor voorschrijvers - Brochure controle nierfunctie bij behandeling van volwassenen
 Risico minimalisatie materiaal betreffende voor voorschrijvers - Brochure controle nierfunctie bij behandeling van volwassenen De risico minimalisatie materialen voor zijn beoordeeld door het College ter
Risico minimalisatie materiaal betreffende voor voorschrijvers - Brochure controle nierfunctie bij behandeling van volwassenen De risico minimalisatie materialen voor zijn beoordeeld door het College ter
Infliximab (Remicade )
 MDL Infliximab (Remicade ) bij de ziekte van Crohn en colitis ulcerosa Inhoudsopgave Algemeen...4 Werking...4 Voorzorgsmaatregelen...5 Gebruik...6 Bijwerkingen...7 Interactie met andere geneesmiddelen...8
MDL Infliximab (Remicade ) bij de ziekte van Crohn en colitis ulcerosa Inhoudsopgave Algemeen...4 Werking...4 Voorzorgsmaatregelen...5 Gebruik...6 Bijwerkingen...7 Interactie met andere geneesmiddelen...8
Praktische informatie over immunotherapie PATIËNTEN
 Praktische informatie over immunotherapie PATIËNTEN Mijn contactgegevens Mijn behandelende arts Tel. Ziekenhuis Tel. Over deze brochure In deze brochure vindt u informatie over immunotherapie bij kanker.
Praktische informatie over immunotherapie PATIËNTEN Mijn contactgegevens Mijn behandelende arts Tel. Ziekenhuis Tel. Over deze brochure In deze brochure vindt u informatie over immunotherapie bij kanker.
RISICO MINIMALISATIE MATERIAAL BETREFFENDE TENOFOVIRDISOPROXIL-BEVATTENDE PRODUCTEN VOOR VOORSCHRIJVERS.
 RISICO MINIMALISATIE MATERIAAL BETREFFENDE TENOFOVIRDISOPROXIL-BEVATTENDE PRODUCTEN VOOR VOORSCHRIJVERS. Brochure controle nierfunctie bij behandeling van volwassenen met HIV De risico minimalisatie materialen
RISICO MINIMALISATIE MATERIAAL BETREFFENDE TENOFOVIRDISOPROXIL-BEVATTENDE PRODUCTEN VOOR VOORSCHRIJVERS. Brochure controle nierfunctie bij behandeling van volwassenen met HIV De risico minimalisatie materialen
Patiënteninformatie over ernstige primaire IGF-1-deficiëntie en hoe Increlex daarbij kan helpen
 Ipsen Endocrinologie Increlex (injectie met mecasermine [rdna-herkomst]) Patiënteninformatie over ernstige primaire IGF-1-deficiëntie en hoe Increlex daarbij kan helpen Voorlichtingsfolder zoals beschreven
Ipsen Endocrinologie Increlex (injectie met mecasermine [rdna-herkomst]) Patiënteninformatie over ernstige primaire IGF-1-deficiëntie en hoe Increlex daarbij kan helpen Voorlichtingsfolder zoals beschreven
BIJSLUITER Atosiban Devrimed 6,75 mg/0,9 ml
 BIJSLUITER Atosiban Devrimed 6,75 mg/0,9 ml 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Atosiban Devrimed 6,75 mg/0,9 ml oplossing voor injectie Atosiban Lees goed de hele bijsluiter voordat u dit geneesmiddel
BIJSLUITER Atosiban Devrimed 6,75 mg/0,9 ml 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Atosiban Devrimed 6,75 mg/0,9 ml oplossing voor injectie Atosiban Lees goed de hele bijsluiter voordat u dit geneesmiddel
Risico minimalisatie materiaal betreffende testosteronundecanoaat voor beroepsbeoefenaren in de gezondheidszorg
 Risico minimalisatie materiaal betreffende testosteronundecanoaat voor beroepsbeoefenaren in de gezondheidszorg De risico minimalisatie materialen voor testosteronundecanoaat zijn beoordeeld door het College
Risico minimalisatie materiaal betreffende testosteronundecanoaat voor beroepsbeoefenaren in de gezondheidszorg De risico minimalisatie materialen voor testosteronundecanoaat zijn beoordeeld door het College
Handleiding voor patiënten. Belangrijke informatie voor patiënten die beginnen aan een behandeling met LEMTRADA
 Handleiding voor patiënten Belangrijke informatie voor patiënten die beginnen aan een behandeling met LEMTRADA Inhoudsopgave 1> Wat is LEMTRADA en hoe werkt het? 03 2> Bijwerkingen 04 3> Planning van uw
Handleiding voor patiënten Belangrijke informatie voor patiënten die beginnen aan een behandeling met LEMTRADA Inhoudsopgave 1> Wat is LEMTRADA en hoe werkt het? 03 2> Bijwerkingen 04 3> Planning van uw
Bijlage III. Wijzigingen in de relevante rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiter
 Bijlage III Wijzigingen in de relevante rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiter Opmerking: De relevante rubrieken van de Samenvatting van de productkenmerken en de bijsluiter
Bijlage III Wijzigingen in de relevante rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiter Opmerking: De relevante rubrieken van de Samenvatting van de productkenmerken en de bijsluiter
Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke informatie in voor u.
 BIJSLUITER: INFORMATIE VOOR GEBRUIKER Chromium [ 51 Cr] EDTA oplossing voor injectie 3,7 MBq/ml Chroom [ 51 Cr] edetaat Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er
BIJSLUITER: INFORMATIE VOOR GEBRUIKER Chromium [ 51 Cr] EDTA oplossing voor injectie 3,7 MBq/ml Chroom [ 51 Cr] edetaat Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er
Maag-, darm- en leverziekten
 Afdeling: Onderwerp: Maag-, darm- en leverziekten Prednison bij ziekte van Crohn en Colitis ulcerosa Inleiding De maag-darm-leverarts (MDL-arts) heeft samen met u besloten om u te behandelen met Prednison.
Afdeling: Onderwerp: Maag-, darm- en leverziekten Prednison bij ziekte van Crohn en Colitis ulcerosa Inleiding De maag-darm-leverarts (MDL-arts) heeft samen met u besloten om u te behandelen met Prednison.
Bijgevoegd vindt u de risico minimalisatie materialen.
 Begeleidende brief voor HCP Betreft: Risico minimalisatie materialen betreffende, infliximab voor voorschrijvers Geachte Heer / Mevrouw, REMSIMA (Infliximab) 100 mg poeder voor concentraat voor oplossing
Begeleidende brief voor HCP Betreft: Risico minimalisatie materialen betreffende, infliximab voor voorschrijvers Geachte Heer / Mevrouw, REMSIMA (Infliximab) 100 mg poeder voor concentraat voor oplossing
MEER INFORMATIE OVER UW NIEUWE ADRENALINE AUTO-INJECTOR
 INFORMATIE VOOR DE PATIËNT Adrenaline 150, 300, 500 µg MEER INFORMATIE OVER UW NIEUWE ADRENALINE AUTO-INJECTOR VOOR DE NOODBEHANDELING VAN ANAFYLAXIE DE RISICO MINIMALISATIE MATERIALEN VOOR EMERADE (ADRENALINE),
INFORMATIE VOOR DE PATIËNT Adrenaline 150, 300, 500 µg MEER INFORMATIE OVER UW NIEUWE ADRENALINE AUTO-INJECTOR VOOR DE NOODBEHANDELING VAN ANAFYLAXIE DE RISICO MINIMALISATIE MATERIALEN VOOR EMERADE (ADRENALINE),
Remicade. Interne geneeskunde
 Remicade Interne geneeskunde Uw behandelend arts of verpleegkundige heeft met u gesproken over het gebruik van Infliximab (Remicade ). In deze folder krijgt u informatie over de werking en het gebruik
Remicade Interne geneeskunde Uw behandelend arts of verpleegkundige heeft met u gesproken over het gebruik van Infliximab (Remicade ). In deze folder krijgt u informatie over de werking en het gebruik
Risicominimalisatie materiaal voor patiënten betreffende mycofenolaat-bevattende geneesmiddelen
 Risicominimalisatie materiaal voor patiënten betreffende mycofenolaat-bevattende geneesmiddelen Dit risicominimalisatie materiaal voor mycofenolaat-bevattende geneesmiddelen is beoordeeld door het College
Risicominimalisatie materiaal voor patiënten betreffende mycofenolaat-bevattende geneesmiddelen Dit risicominimalisatie materiaal voor mycofenolaat-bevattende geneesmiddelen is beoordeeld door het College
Risicominimalisatiemateriaal betreffende rituximab* voor zorgverleners
 Risicominimalisatiemateriaal betreffende rituximab* voor zorgverleners *voor niet-oncologische indicaties Dit risicominimalisatiemateriaal werd goedgekeurd door het College ter Beoordeling van Geneesmiddelen
Risicominimalisatiemateriaal betreffende rituximab* voor zorgverleners *voor niet-oncologische indicaties Dit risicominimalisatiemateriaal werd goedgekeurd door het College ter Beoordeling van Geneesmiddelen
Bijlage III. Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiters
 Bijlage III Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiters NB: Deze Samenvatting van de productkenmerken, Etikettering
Bijlage III Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiters NB: Deze Samenvatting van de productkenmerken, Etikettering
Darzalex (daratumumab) PATIËNTENBROCHURE
 PATIËNTENBROCHURE Darzalex (daratumumab) TOON DEZE FOLDER AAN UW HUISARTS, HUISAPOTHEKER EN THUISVERPLEEGKUNDIGE www.ziekenhuisgeel.be 2 Behandelschema Darzalex (daratumumab) is een doelgerichte therapie.
PATIËNTENBROCHURE Darzalex (daratumumab) TOON DEZE FOLDER AAN UW HUISARTS, HUISAPOTHEKER EN THUISVERPLEEGKUNDIGE www.ziekenhuisgeel.be 2 Behandelschema Darzalex (daratumumab) is een doelgerichte therapie.
Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke informatie in voor u.
 BIJSLUITER: INFORMATIE VOOR DE PATIËNT Ceretec 0,5 mg kit voor radiofarmaceutisch preparaat Exametazime Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke
BIJSLUITER: INFORMATIE VOOR DE PATIËNT Ceretec 0,5 mg kit voor radiofarmaceutisch preparaat Exametazime Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke
Patiënteninformatie. Behandeling met APD. Gebruik en bijwerkingen. 1234567890-terTER_
 Patiënteninformatie Behandeling met APD Gebruik en bijwerkingen 1234567890-terTER_ Behandeling met APD U heeft een afspraak in Tergooi voor een behandeling APD. Onze artsen en medewerkers doen er alles
Patiënteninformatie Behandeling met APD Gebruik en bijwerkingen 1234567890-terTER_ Behandeling met APD U heeft een afspraak in Tergooi voor een behandeling APD. Onze artsen en medewerkers doen er alles
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. fexofenadinehydrochloride
 Sandoz B.V. Page 1/5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Fexofenadine Sandoz 120 mg, filmomhulde tabletten fexofenadinehydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
Sandoz B.V. Page 1/5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Fexofenadine Sandoz 120 mg, filmomhulde tabletten fexofenadinehydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
Bijsluiter: informatie voor de patiënt. Neoclarityn 5 mg filmomhulde tabletten desloratadine
 Bijsluiter: informatie voor de patiënt Neoclarityn 5 mg filmomhulde tabletten desloratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in
Bijsluiter: informatie voor de patiënt Neoclarityn 5 mg filmomhulde tabletten desloratadine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in
Noscapine HCl Teva 1 mg/ml, stroop noscapine
 1.3.1 : Bijsluiter Bladzijde : 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Noscapine HCl Teva 1 mg/ml, noscapine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat belangrijke
1.3.1 : Bijsluiter Bladzijde : 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Noscapine HCl Teva 1 mg/ml, noscapine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat belangrijke
Bijsluiter: informatie voor de gebruiker. Replagal, 1 mg/ml, concentraat voor oplossing voor infusie Agalsidase alfa
 Bijsluiter: informatie voor de gebruiker Replagal, 1 mg/ml, concentraat voor oplossing voor infusie Agalsidase alfa Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat
Bijsluiter: informatie voor de gebruiker Replagal, 1 mg/ml, concentraat voor oplossing voor infusie Agalsidase alfa Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat
PATIENTENBIJSLUITER: informatie voor de gebruiker CosmoFer 50 mg/ml, oplossing voor injectie en infusie IJzer(III)
 PATIENTENBIJSLUITER: informatie voor de gebruiker CosmoFer 50 mg/ml, oplossing voor injectie en infusie IJzer(III) Lees de hele bijsluiter zorgvuldig door Bewaar deze bijsluiter, het kan nodig zijn om
PATIENTENBIJSLUITER: informatie voor de gebruiker CosmoFer 50 mg/ml, oplossing voor injectie en infusie IJzer(III) Lees de hele bijsluiter zorgvuldig door Bewaar deze bijsluiter, het kan nodig zijn om
Adalimumab (Humira) bij de ziekte van Crohn en colitis ulcerosa Maag-Darm-Levercentrum. Beter voor elkaar
 Adalimumab (Humira) bij de ziekte van Crohn en colitis ulcerosa Maag-Darm-Levercentrum Beter voor elkaar 2 Inleiding Uw behandelend arts heeft met u gesproken over het gebruik van Adalimumab (Humira).
Adalimumab (Humira) bij de ziekte van Crohn en colitis ulcerosa Maag-Darm-Levercentrum Beter voor elkaar 2 Inleiding Uw behandelend arts heeft met u gesproken over het gebruik van Adalimumab (Humira).
Remicade INFORMATIEBROCHURE VOOR DE PATIËNT
 Remicade INFORMATIEBROCHURE VOOR DE PATIËNT INHOUD 1. WERKING VAN REMICADE...4 2. AANDACHTSPUNTEN BIJ DEZE BEHANDELING...5 3. GEBRUIKT U NOG ANDERE GENEESMIDDELEN?...7 4. ZWANGERSCHAP, BORSTVOEDING EN
Remicade INFORMATIEBROCHURE VOOR DE PATIËNT INHOUD 1. WERKING VAN REMICADE...4 2. AANDACHTSPUNTEN BIJ DEZE BEHANDELING...5 3. GEBRUIKT U NOG ANDERE GENEESMIDDELEN?...7 4. ZWANGERSCHAP, BORSTVOEDING EN
Behandeling met infliximab Ter behandeling van de ziekte van Crohn en colitis ulcerosa
 Behandeling met infliximab Ter behandeling van de ziekte van Crohn en colitis ulcerosa Afdeling maag-darm-leverziekten Inleiding Uw arts heeft een behandeling met infliximab voorgesteld. Infliximab is
Behandeling met infliximab Ter behandeling van de ziekte van Crohn en colitis ulcerosa Afdeling maag-darm-leverziekten Inleiding Uw arts heeft een behandeling met infliximab voorgesteld. Infliximab is
Educatieve PrEP-brochure voor risicopersonen
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Emtricitabin/ Tenofovir Disoproxil Sandoz. Het verplicht plan voor risicobeperking
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Emtricitabin/ Tenofovir Disoproxil Sandoz. Het verplicht plan voor risicobeperking
Bijsluiter: informatie voor de gebruiker. Dacogen 50 mg poeder voor concentraat voor oplossing voor infusie decitabine
 Bijsluiter: informatie voor de gebruiker Dacogen 50 mg poeder voor concentraat voor oplossing voor infusie decitabine Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe
Bijsluiter: informatie voor de gebruiker Dacogen 50 mg poeder voor concentraat voor oplossing voor infusie decitabine Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe
Immunotherapie bij kanker. Informatie en praktische tips voor mantelzorgers
 Immunotherapie bij kanker Informatie en praktische tips voor mantelzorgers Inhoudsopgave 4 5 6 7 9 10 12 14 Het immuunsysteem Hoe werkt immunotherapie samen met het immuunsysteem bij de strijd tegen kanker?
Immunotherapie bij kanker Informatie en praktische tips voor mantelzorgers Inhoudsopgave 4 5 6 7 9 10 12 14 Het immuunsysteem Hoe werkt immunotherapie samen met het immuunsysteem bij de strijd tegen kanker?
Prednison / Prednisolon (corticosteroïden) bij Inflammatoire darmziekten (ziekte van Crohn, Colitis Ulcerosa)
 Prednison / Prednisolon (corticosteroïden) bij Inflammatoire darmziekten (ziekte van Crohn, Colitis Ulcerosa) Uw behandelend arts heeft met u gesproken over het gebruik van prednison/ prednisolon. In
Prednison / Prednisolon (corticosteroïden) bij Inflammatoire darmziekten (ziekte van Crohn, Colitis Ulcerosa) Uw behandelend arts heeft met u gesproken over het gebruik van prednison/ prednisolon. In
INFORMATIE VOOR DE PATIENT
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Increlex. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Increlex. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Abatacept (Orencia ) Behandeling tweedelijns antireumatica
 Abatacept (Orencia ) Behandeling tweedelijns antireumatica Abatacept (Orencia ) is een antireumatisch geneesmiddel dat er voor zorgt dat de ontsteking en de pijn in uw gewrichten afneemt. Het zorgt er
Abatacept (Orencia ) Behandeling tweedelijns antireumatica Abatacept (Orencia ) is een antireumatisch geneesmiddel dat er voor zorgt dat de ontsteking en de pijn in uw gewrichten afneemt. Het zorgt er
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Loperamide EG 2 mg capsules, hard. Loperamidehydrochloride
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Loperamide EG 2 mg capsules, hard Loperamidehydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat innemen want er staat belangrijke informatie
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Loperamide EG 2 mg capsules, hard Loperamidehydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat innemen want er staat belangrijke informatie
Patiënteninformatie. Behandeling met APD. Gebruik en bijwerkingen terTER_
 Patiënteninformatie Behandeling met APD Gebruik en bijwerkingen 1234567890-terTER_ Behandeling met APD U heeft een afspraak in Tergooi voor een behandeling APD. Onze artsen en medewerkers doen er alles
Patiënteninformatie Behandeling met APD Gebruik en bijwerkingen 1234567890-terTER_ Behandeling met APD U heeft een afspraak in Tergooi voor een behandeling APD. Onze artsen en medewerkers doen er alles
Educatieve PrEP-brochure voor risicopersonen
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Emtricitabine/ Tenofovirdisoproxil Mylan 200 mg/245 mg filmomhulde tabletten.
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Emtricitabine/ Tenofovirdisoproxil Mylan 200 mg/245 mg filmomhulde tabletten.
UW BEHANDEL- GIDS VOOR ADCETRIS
 AANBEVELINGEN VOOR PATIËNTEN UW BEHANDEL- GIDS VOOR ADCETRIS (Brentuximab vedotin) NY/ADC/19/0010 INHOUD 1 Inleiding....3 2 Wat is Adcetris?....4 3 Hoe werkt Adcetris?...5 4 Hoe wordt Adcetris toegediend?....6
AANBEVELINGEN VOOR PATIËNTEN UW BEHANDEL- GIDS VOOR ADCETRIS (Brentuximab vedotin) NY/ADC/19/0010 INHOUD 1 Inleiding....3 2 Wat is Adcetris?....4 3 Hoe werkt Adcetris?...5 4 Hoe wordt Adcetris toegediend?....6
Infliximab (Remicade) bij de ziekte van Crohn en colitis ulcerosa
 Infliximab (Remicade) bij de ziekte van Crohn en colitis ulcerosa Polikliniek Maag-Darm-Leverziekten Uw behandelend arts of IBD-verpleegkundige heeft met u gesproken over het gebruik van Infliximab (Remicade).
Infliximab (Remicade) bij de ziekte van Crohn en colitis ulcerosa Polikliniek Maag-Darm-Leverziekten Uw behandelend arts of IBD-verpleegkundige heeft met u gesproken over het gebruik van Infliximab (Remicade).
Patiënteninformatie. Een behandeling met Entyvio
 Patiënteninformatie Een behandeling met Entyvio Naam: Gewicht: kg Leeftijd:..jaar VOORONDERZOEKEN....... EERSTE INFUUS OP. 2 Waar moet u zijn? De behandeling gaat door in AZ Turnhout Campus Sint-Jozef
Patiënteninformatie Een behandeling met Entyvio Naam: Gewicht: kg Leeftijd:..jaar VOORONDERZOEKEN....... EERSTE INFUUS OP. 2 Waar moet u zijn? De behandeling gaat door in AZ Turnhout Campus Sint-Jozef
Inleiding. Wat is infliximab
 Infliximab-infuus Inleiding In overleg met uw maag-, darm-, leverarts (MDL-arts) gaat u starten met de behandeling infliximab. In deze folder vindt u informatie over infliximab, over de werking en de behandeling,
Infliximab-infuus Inleiding In overleg met uw maag-, darm-, leverarts (MDL-arts) gaat u starten met de behandeling infliximab. In deze folder vindt u informatie over infliximab, over de werking en de behandeling,
Lonsurf trifluridine/tipiracil
 Lonsurf trifluridine/tipiracil Product Informatie Fiche T +32(0)89 32 50 50 F +32(0)89 32 79 00 info@zol.be Campus Sint-Jan Schiepse bos 6 B 3600 Genk Campus Sint-Barbara Bessemerstraat 478 B 3620 Lanaken
Lonsurf trifluridine/tipiracil Product Informatie Fiche T +32(0)89 32 50 50 F +32(0)89 32 79 00 info@zol.be Campus Sint-Jan Schiepse bos 6 B 3600 Genk Campus Sint-Barbara Bessemerstraat 478 B 3620 Lanaken
