Samenvatting Scheikunde Basisstof examen
|
|
|
- Franciscus van der Berg
- 4 jaren geleden
- Aantal bezoeken:
Transcriptie
1 Samenvatting Scheikunde Basisstof examen Samenvatting door M woorden 28 juni ,8 7 keer beoordeeld Vak Methode Scheikunde Chemie overal Scheikunde samenvatting Zuivere stoffen en mengsels Gas >rijpen > vaste stof Vaste stof > smelten > vloeistof Vloeistof > verdampen > gas Gas > condenseren > vloeistof Vloeistof > stollen > vaste stof Vaste stof > sublimeren > gas Type mengsel Betekenis Kenmerken Oplossing Een mengsel van gas, vloeibare stof of Altijd helder en soms gekleurd een vaste stof in een vloeistof (water) Suspensie Vaste en vloeistof Altijd troebel en gekleurd Emulsie Twee vloeistoffen Altijd troebel Legering/alliage Metalen Betere eigenschappen dan afzonderlijke metalen Scheidingsmethode Principe berust op Type mengsel Extraheren Oplosbaarheid van stof Vaste stoffen Adsorberen Aanhechtingsvermogen Oplossing met bepaalde kleur Destilleren Kookpunt Vloeistoffen Filtreren Deeltjesgrootte Suspensie Centrifugeren Dichtheid Emulsie en suspensie Bezinken Dichtheid Emulsie Indampen Kookpunt Vaste stof in vloeistof Chromatografie Aanhechtingsvermogen en oplosbaarheid Verschillende mengsels Pagina 1 van 9
2 Elementen en verbindingen Één soort atoom: niet-ontleedbaar > elementen Twee of meer soorten atomen: ontleedbaar bijv. NH3 of CO2 Geladen atomen: ionen Positief ion: metaalionen Negatief ion: niet-metaalionen Ion van meerdere atomen: samengesteld ion Beginstoffen > reactieproducten Totale massa beginstof = totale massa reactieproduct Aantal elementen beginstof = aantal elementen reactieproduct Ontledingsreactie: reactie waarbij uit één stof meerdere stoffen ontstaan. Ontledingsreactie Thermolyse Elektrolyse Fotolyse Ontleding door Warmte Elektrische energie Licht reacties Verbrandingsreactie: brandbare stof met zuurstof Aanwezigheid zuurstof Aanwezigheid brandbare stof - Ontbrandingstemperatuur is goed Volledige verbranding: voldoende zuurstof = koolwaterstof > water en koolstofdioxide Onvolledige verbranding: onvoldoende zuurstof = koolwater > water en koolstofdioxide, roet en koolstofmono oxide. Exotherme reactie: energie komt vrij Endotherme reactie: energie is nodig. Reagens: stof die wordt gebruikt om andere stof aan te tonen Stof Reagens Waarneming Zuurstof Gloeiende houtspaander Gaat branden Waterstof Vlammetje Geluidseffect Water Wit kopersulfaat Wordt blauw Koolstofdioxide Helder kalkwater Wordt troebel Zwaveldioxide Geel broomoplossing Wordt kleurloos Pagina 2 van 9
3 zouten Zouten: sterke Ionbinding door +/- Zouten: bij kamertemperatuur vast en hoog smeltpunt. Hydratie: ionen worden gesplitst door oplossen in water. Je zet er (aq) achter. Neerslagreacties: 1. Ga na welke ionen aanwezig zijn na het samenvoegen van de oplossingen. Geef dit weer in een tabel 2. Ga met behulp van tabel 45A voor alle combinaties van ionen na of ze wel of niet oplosbaar zijn. Noteer dit in de tabel 3. Als minstens één combinatie een slecht oplosbaar zout vormt, ontstaat er een neerslag. Geef de reactievergelijking. Tribune- ionen: worden niet betrokken bij de reactie Toepassingen neerslag reacties: ionen uit oplossing verwijderen aanwezigheid van bepaalde ionen aantonen bepaald zout bereiden Atomen Atoom is altijd elektrisch neutraal ( evenveel protonen dan elektronen) Atoomnummer: aantal protonen massagetal: protonen en neutronen samen Neutronen = massagetal atoomnummer Bindingstypen en eigenschappen Soort stof Moleculaire stoffen Metalen Zouten Opgebouwd uit Uitsluitend niet-metaalatomen Metaalatomen Combinatie van metaalionen en niet-metaalionen Pagina 3 van 9
4 Soort binding Berust op aantrekkende kracht Komen voor bij Atoombinding/ covalente binding Positieve atoomresten en negatieve gemeenschappelijk elektronenpaar Moleculaire stoffen en zouten met samengestelde ionen Polaire atoombinding Positieve atoomresten en negatieve gemeenschappelijk elektronenpaar Moleculaire stoffen en zouten met samengestelde ionen waarbij het gemeenschappelijk elektronen paar iets verschoven is in de richting van het atoom dat het hardst trekt. Vanderwaalsbinding/ molecuulbinding Moleculen onderling in de vaste en vloeibare fase Moleculaire stoffen in de vaste en vloeibare fase Metaalbinding Positieve resten van metaalatomen en Metalen vrije elektronen Ionbinding Positieve en negatieve ionen Zouten Waterstofbrug Moleculen met N-H of H - O Moleculaire stoffen Soort stof Kookpunt Elektrische geleidbaarheid Sterkte binding Moleculaire stoffen Laag tot zeer laag Nooit Molecuulbinding: zwak Atoombinging: sterk Zouten Vrij hoog Alleen in vloeibare en Ionbinding: sterk opgeloste toestand Metalen Laag tot hoog Altijd Metaalbinding: matig tot sterk Reacties van koolstofverbindingen Additie: dubbele binding verdwijnen Kraken: grotere moleculen > kleiner alkeen en alkaan Verstering: een alchohol + alkaanzuur > ester + water Hydrolyse: ester + water > alkanol + alkaanzuur Polymerisatie: monomeren > polymeren dubbele binding verdwijnt Koolstofverbinding: Algemene formule: Binding tussen c atomen Achtervoegsel Alkanen(verzadigd) C n H 2n+2 C C -aan Alkenen(onverzadigd) C n H 2n C = C -een Pagina 4 van 9
5 Koolstofverbinding Algemene formule Karakteristieke groep Achtervoegsel Halogeenalkanolen C n H 2n+1 X X = F, Cl, Br, L Geen Alcohol: alkanol C n H 2n+1 OH -OH(hydroxylgroep) -ol Carbonzuren: Alkaanzuren C n H 2n+1 COOH -COOH ( carboxylgroep) -zuur Naamgeving van een koolstofverbinding: 1. Bepaal de stamnaam 1. Zoek langste keten van c-atoom 2. Zoek stamnaam: 1. Meth.. 2. Eth 3. Prop.. 3. Bepaal de karakterische groep 1. Zoek het achtervoegsel 2. Alkeen en alkaan Koolhydraten: C n (H 2 O) m Suikers, sachariden Door hydrolyse ontstaat glucose Vetten: Alcohol + alkaanzuur > vetten en oliën Alcohol: glycerol Alkaanzuur: vetzuur Hydrolyse van vetmoleculen: Vetmolecuul + h2o > glycerol + vetzuren Eiwitten Aminozuren Eiwitten zijn aminozuren aan elkaar gekoppeld door peptidebindingen Peptidebinding: -c-n- Eiwitmolecuul kun je ook weergeven met 3-lettersymbolen: Ala-gly-ala Hij moet in een structuur verbinding worden weergegeven. Toepassingen Reactievergelijkingen: beginstof>reactieproduct Reactievergelijkingen kun je weeergeven met behulp van: Molecuulformules Structuurformules Verhoudingsformules Ionen Rendement = werkelijke opbrengst/ theoretische opbrengt x100% Gebruik dezelfde eenheden Katalysator: Een stof die de reactie versnelt. Hij wordt wel gebruikt maar niet verbruikt. Reactiesnelheid en evenwichten Botsende deeltjes model De snelheid van een reactie is afhankelijk van het aantal effectieve botsingen dat per tijdseenheid plaatsvindt Pagina 5 van 9
6 Factoren Aangebrachte veranderingen Concentratie Vergroten concentratie van reagerende stof VerdelingsgraadVergroten oppervlak van reagerende stof Temperatuur Verhogen temperatuur Aantal botsingen Aantal effectieve botsingen Doordat er meer deeltjes zijn per De kans op het aantal volume eenheid, neemt de kans op effectieve botsingen het aantal botsingen toe. neemt toe Door vergroten van oppervlak > De kans op aantal aantal botsingen neemt toe effectieve botsingen neemt toe Door verhogen van temperatuur Kans op aantal hebben de deeltjes een grotere effectieve botsingen snelheid. Door die snelheid neem neemt toe door: de kans op botsingen toe en zijn - meer kans op de botsingen krachtiger effectieve botsingen - Botsingen die krachtiger zijn Reactiesnelheid neemt toe neemt toe neemt toe Evenwicht Bij een evenwichtstoestand geld: De snelheden van de heengaande en teruggaande reactie zijn gelijk Alle bij de evenwichtsreacties betrokken stoffen zijn in het reactiemengsel aanwezig De concentraties van de stoffen zijn gelijk, veranderen niet meer. Soort evenwicht Homogeen Heterogeen verdelingsevenwicht Omschrijving Alle stoffen verkeren in dezelfde fase Alle stoffen zijn in verschillende fase Een bijzondere vorm van heterogeen evenwicht. Het gaat daarbij om een stof die opgelost is in twee verschillende oplosmiddelen. De oplosmiddelen zijn iet onderling mengbaar. De opgeloste stof verdeelt zich dan over de twee oplosmiddelen Aflopende reactie Door het onttrekken van een sotf kan er geen teruggaande reactie plaats vinden. Door één van beide reacties onmogelijk te maken is een evenwichtstoestand niet meer mogelijk. Met een katalysator kun je een evenwichtsreactie niet aflopend maken. Rekenen aan reacties Massa Massa Omschrijving Te bepalen door Atoommassa Massa van atoom in u Opzoeken in talbel 40A of 99 Molecuulmassa Massa van molecuul in u Atoommassa s van de molecuulformules bij elkaar optellen Ionmassa Massa van een ion in u Massa van het bijbehorende atoom nemen. Massa ion is gelijk aan massa van atoom Pagina 6 van 9
7 Chemische hoeveelheid en molaire massa Chemische hoeveelheid: hoeveelheid stof in gram is even groot als massa van het deeltje in u Molaire massa: massa van een mol (gram per mol) Massa = chemische hoeveelheid x molaire massa m = n x M kmol = 10 3 mmol = 10-3 Symbool Grootheid Eenheid N Chemische hoeveelheid stof Mol M Molaire massa G mol-1 Gehalte Gebruik ook de eenheden mmol en kmol Gebruik dezelfde eenheden bij een reactie Begrip Omschrijving Eenheid Volume percentage Massapercentage Het percentage van een stof in een mengsel of oplossing op basis % van volume-eenheden Het percentage van een stof in een mengsel of oplossing op basis % van massa-eenheden Concentratie Het % van een atoom in een verbinding op basis van massaeenheden Het aantal gram opgeloste stof per liter oplossing G L -1 Het aantal mol opgeloste stof pet liter oplossing Mol L-1 Massa verhouding en molverhouding Overmaat: als je van een stof meer hebt dan nodig is. Er blijft een overmaat over. Blokkenschema Molaire massa: g mol -1 Volume: l Molariteit: mol L-1 Een chemisch proces vergroten Bulkproducten: producten die in grote hoeveelheden worden gemaakt Pagina 7 van 9
8 Blokschema Hoe werkt de chemische industrie Namen, formules en reacties van zuren en basen Sterkte en zwakke zuren Zuur: een deeltje dat H+-ionen kan afstaan PH is lager dan 7 Sterke zuren: zuren die in water volledig worden gesplitst Aflopende reactie: als alle moleculen H+ afstaan in water Zwakke zuren: zuren die in water niet helemaal worden gesplitst Evenwichtsreactie: niet alle moleculen splitsen zich Naam Formule Aantal h+ dat het zuur afstaat Waterstofchloride HCL 1 Sterk Zwavelzuur H 2 SO 4 2 Sterk Salpeterzuur HNO 3 1 Sterk Fosforzuur H 3 PO 4 3 Zwak Koolzuur H 2 CO 3 2 Zwak Azijnzuur CH 3 COOH 1 Sterk/zwak Sterke en zwakke basen Base: een deeltje dan H+ ionen kan opnemen Sterke base: als het alle H+ ionen opneemt Alle oxide-ionen nemen h+ op in water Zwakke base: neemt niet alle h+ deeltjes op in water Naam Formule Aantal H+ dat hij opneemt Sterk/zwak Oxide-ion O 2- `2 Sterk Hydroxide ion OH - 1 Sterk Carbonaation CO Zwak Ammoniak NH 3 1 Zwak Waterstofcarbonaation HCO 3-1 Zwak Ethanoaation CH 3 COO - 1 zwak Samenstelling van oplossingen Namen die eindigen op loog zijn basisch Formule stof Stof in water Naam oplossing Aanwezige deeltjes in oplossing HCL HCL > H + +CL - Zoutzuur zuur H+ en CL-(aq) NaOH NaOH> NA + + OH - Natronloog basisch NA+ en OH-(aq) KOH KOH > K + + Oh - Kaliloog basisch K+ en OH (aq) NH 3 NH 3 + H 2 O > NH OH - Ammonia basisch NH3 ( de rest is verwaarloosbaar klein Pagina 8 van 9
9 het effect van verdunnen op de ph Zuren en basische oplossingen worden verdund waardoor de ph naar 7 zal naderen, dit maakt niet uit of het een sterkte of een zwakke zuur of base is. Zuur-base reactie Als een zuur en een base bij elkaar worden gevoegd. Er vind een overdracht van h+ plaats Een zuur draagt die H+ af aan de base ph- berekeningen een zuurgraad of de ph wordt bepaald door de concentratie H+ ionen. ph= -log[h+] [H+] = 10 -ph mol L-1 Een basegraad of de poh wordt bepaald door de concentratie OH ionen poh = -log[oh-] en [OH-] = 10 -poh mol L-1 Bij een verband wordt het: poh +ph = 14 Om je antwoord te controleren: een zuur < 7, een base > 7 Neutralisatie: de ph wordt 7, neutraal. Er ontstaan H2O Reacties Redoxreactie: een reactie waarbij ovedracht plaatsvind tussen elektronen. Reductor: staat af Oxidator: neemt op Sterke oxidator staat boven Sterke reductor staat onderaan Elektrolyse: gedwongen reactie Tabel functies: 25 > atoomnummers en massagetallen 38A > formule van ph berekenen 40A > Lading van ionen, atoomnummers, massagetallen 45A > oplosbaarheid zouten 48 > oxidatoren en reductoren 49 > welke zuren en basen sterk zijn en welke zwak, rechterkolom: basen/ boven aan zwak 66B > formule van verbindingen 67A > structuurformules van de koolhydraten 67B > structuurformules van de vetzuren 98 > molaire massa s van veelgebruikte stoffen 99 > periodiek systeem Pagina 9 van 9
ßCalciumChloride oplossing
 Samenvatting door R. 1673 woorden 17 februari 2013 8 1 keer beoordeeld Vak Methode Scheikunde Pulsar chemie Additiereactie Bij een reactie tussen hexeen en broom springt de C=C binding open. Aan het molecuul
Samenvatting door R. 1673 woorden 17 februari 2013 8 1 keer beoordeeld Vak Methode Scheikunde Pulsar chemie Additiereactie Bij een reactie tussen hexeen en broom springt de C=C binding open. Aan het molecuul
Samenvatting Scheikunde Hoofdstuk 1 + 2
 Samenvatting Scheikunde Hoofdstuk 1 + 2 Samenvatting door K. 1077 woorden 22 maart 2016 6,1 9 keer beoordeeld Vak Scheikunde Impact 3 vwo Scheikunde hoofdstuk 1 + 2 Paragraaf 1: Stoffen bijv. Glas en hout,
Samenvatting Scheikunde Hoofdstuk 1 + 2 Samenvatting door K. 1077 woorden 22 maart 2016 6,1 9 keer beoordeeld Vak Scheikunde Impact 3 vwo Scheikunde hoofdstuk 1 + 2 Paragraaf 1: Stoffen bijv. Glas en hout,
Scheidingsmethoden methode principe voorbeeld. destilleren verschil in kookpunt wijn whiskey. filtreren verschil in deeltjesgrootte koffie
 1.2 Twee of meer atoomsoorten samen vormen een molecuul : bouwsteen die bestaat uit twee of meer atomen Atoom : bouwsteen van een molecuul Stoffen Zuivere stoffen Elementen: stoffen waarvan de bouwstenen
1.2 Twee of meer atoomsoorten samen vormen een molecuul : bouwsteen die bestaat uit twee of meer atomen Atoom : bouwsteen van een molecuul Stoffen Zuivere stoffen Elementen: stoffen waarvan de bouwstenen
1 De bouw van stoffen
 Inhoud 1 De bouw van stoffen 1 eigenschappen van stoffen 13 Mengsels en zuivere stoffen 13 D Oplossingen 15 Zuivere stoffen herkennen 15 Scheiding van mengsels 17 2 de opbouw van de materie 19 Moleculen
Inhoud 1 De bouw van stoffen 1 eigenschappen van stoffen 13 Mengsels en zuivere stoffen 13 D Oplossingen 15 Zuivere stoffen herkennen 15 Scheiding van mengsels 17 2 de opbouw van de materie 19 Moleculen
Samenvatting Scheikunde Hoofdstuk 1 en 2
 Samenvatting Scheikunde Hoofdstuk 1 en 2 Samenvatting door een scholier 918 woorden 13 januari 2005 6,3 193 keer beoordeeld Vak Methode Scheikunde Chemie overal Hoofdstuk 1 1.2: De bouw van een atoom.
Samenvatting Scheikunde Hoofdstuk 1 en 2 Samenvatting door een scholier 918 woorden 13 januari 2005 6,3 193 keer beoordeeld Vak Methode Scheikunde Chemie overal Hoofdstuk 1 1.2: De bouw van een atoom.
Samenvatting Scheikunde Hoofdstuk 1, 2, 4, 5, 6, 7, 9, 11, 12, 13
 Samenvatting Scheikunde Hoofdstuk 1, 2, 4, 5, 6, 7, 9, 11, 12, 13 Samenvatting door een scholier 3460 woorden 23 mei 2011 5,8 68 keer beoordeeld Vak Methode Scheikunde Pulsar chemie Samenvattingen van
Samenvatting Scheikunde Hoofdstuk 1, 2, 4, 5, 6, 7, 9, 11, 12, 13 Samenvatting door een scholier 3460 woorden 23 mei 2011 5,8 68 keer beoordeeld Vak Methode Scheikunde Pulsar chemie Samenvattingen van
9,3. Samenvatting door C woorden 21 mei keer beoordeeld. Scheikunde. Hoofdstuk 1: mengen scheiden en reageren
 Samenvatting door C. 2672 woorden 21 mei 2014 9,3 6 keer beoordeeld Vak Methode Scheikunde Curie Hoofdstuk 1: mengen scheiden en reageren Mengsel: bestaat uit verschillende stoffen. Zuivere stof: bestaat
Samenvatting door C. 2672 woorden 21 mei 2014 9,3 6 keer beoordeeld Vak Methode Scheikunde Curie Hoofdstuk 1: mengen scheiden en reageren Mengsel: bestaat uit verschillende stoffen. Zuivere stof: bestaat
Samenvatting Scheikunde Hoofdstuk 9, 10, 11 Zuren/Basen, Evenwichtsconstanten
 Samenvatting Scheikunde Hoofdstuk 9, 10, 11 Zuren/Basen, Evenwichtsconstanten Samenvatting door een scholier 1087 woorden 22 januari 2009 6 42 keer beoordeeld Vak Methode Scheikunde Pulsar chemie Scheikunde
Samenvatting Scheikunde Hoofdstuk 9, 10, 11 Zuren/Basen, Evenwichtsconstanten Samenvatting door een scholier 1087 woorden 22 januari 2009 6 42 keer beoordeeld Vak Methode Scheikunde Pulsar chemie Scheikunde
Eindexamen scheikunde havo 2001-I
 Eindexamen scheikunde havo -I 4 Antwoordmodel Nieuw element (in de tekst staat:) deze atomen zijn eerst ontdaan van een aantal elektronen dus de nikkeldeeltjes zijn positief geladen Indien in een overigens
Eindexamen scheikunde havo -I 4 Antwoordmodel Nieuw element (in de tekst staat:) deze atomen zijn eerst ontdaan van een aantal elektronen dus de nikkeldeeltjes zijn positief geladen Indien in een overigens
Overzicht van reactievergelijkingen Scheikunde
 verzicht van reactievergelijkingen Scheikunde Algemeen Verbranding Een verbranding is een reactie met zuurstof. ierbij ontstaan de oxiden van de elementen. Volledige verbranding Bij volledige verbranding
verzicht van reactievergelijkingen Scheikunde Algemeen Verbranding Een verbranding is een reactie met zuurstof. ierbij ontstaan de oxiden van de elementen. Volledige verbranding Bij volledige verbranding
vrijdag 15 juni 2012 15:26:05 Midden-Europese zomertijd H6 Zuren en basen 4havo voorjaar 2012
 H6 Zuren en basen 4havo voorjaar 2012 Toetsing in periode 4! 6 juni! DTM-T zuur/base t/m 6.6! Tabel 6.10,6.13,6.17 en ph-berekeningen (zoals in vragen 14,15,26 en 27)! Toetsweek einde periode! TW441 H1
H6 Zuren en basen 4havo voorjaar 2012 Toetsing in periode 4! 6 juni! DTM-T zuur/base t/m 6.6! Tabel 6.10,6.13,6.17 en ph-berekeningen (zoals in vragen 14,15,26 en 27)! Toetsweek einde periode! TW441 H1
Stoffen, structuur en bindingen
 Hoofdstuk 1: Stoffen, structuur en bindingen Scheikunde vwo 2011/2012 www.lyceo.nl Onderwerpen Scheikunde 2011 2012 Stoffen, structuur en binding Kenmerken van Reacties Zuren en base Redox Chemische technieken
Hoofdstuk 1: Stoffen, structuur en bindingen Scheikunde vwo 2011/2012 www.lyceo.nl Onderwerpen Scheikunde 2011 2012 Stoffen, structuur en binding Kenmerken van Reacties Zuren en base Redox Chemische technieken
Eindexamen scheikunde havo 2006-II
 4 Beoordelingsmodel Element 115 1 Calcium heeft atoomnummer 20 en americium heeft atoomnummer 95. Dus samen hebben ze 115 protonen. calcium heeft atoomnummer 20 en americium heeft atoomnummer 95 1 2 Een
4 Beoordelingsmodel Element 115 1 Calcium heeft atoomnummer 20 en americium heeft atoomnummer 95. Dus samen hebben ze 115 protonen. calcium heeft atoomnummer 20 en americium heeft atoomnummer 95 1 2 Een
Samenvatting Chemie Overal 3 havo
 Samenvatting Chemie Overal 3 havo Hoofdstuk 3: Reacties 3.1 Energie Energievoorziening Fossiele brandstoffen zijn nog steeds belangrijk voor onze energievoorziening. We zijn druk op zoek naar duurzame
Samenvatting Chemie Overal 3 havo Hoofdstuk 3: Reacties 3.1 Energie Energievoorziening Fossiele brandstoffen zijn nog steeds belangrijk voor onze energievoorziening. We zijn druk op zoek naar duurzame
Samenvatting Scheikunde Hoofdstuk 1 + 2
 Samenvatting Scheikunde Hoofdstuk 1 + 2 Samenvatting door A. 4666 woorden 27 oktober 2014 6,3 6 keer beoordeeld Vak Methode Scheikunde Chemie overal 1-2 Zuivere stof -Een soort moleculen -Element: een
Samenvatting Scheikunde Hoofdstuk 1 + 2 Samenvatting door A. 4666 woorden 27 oktober 2014 6,3 6 keer beoordeeld Vak Methode Scheikunde Chemie overal 1-2 Zuivere stof -Een soort moleculen -Element: een
Samenvatting Scheikunde Hfst. 6 Chemie en schoonmaken
 Samenvatting Scheikunde Hfst. 6 Chemie en sch Samenvatting door een scholier 2120 woorden 23 november 2010 4,5 9 keer beoordeeld Vak Scheikunde Natuurkunde hoofdstuk 6: Chemie en sch 6.1 Elementen Indelen
Samenvatting Scheikunde Hfst. 6 Chemie en sch Samenvatting door een scholier 2120 woorden 23 november 2010 4,5 9 keer beoordeeld Vak Scheikunde Natuurkunde hoofdstuk 6: Chemie en sch 6.1 Elementen Indelen
Hoofdstuk 6. De ph/zuurgraad is een getal waarin de hoeveelheid zuur of base wordt uitgedrukt. Dit getal ligt meestal tussen de 0 en 14.
 Samenvatting door W. 879 woorden 15 oktober 2012 5,8 52 keer beoordeeld Vak Methode Scheikunde Chemie overal Hoofdstuk 6 2 De PH van een oplossing De ph/zuurgraad is een getal waarin de hoeveelheid zuur
Samenvatting door W. 879 woorden 15 oktober 2012 5,8 52 keer beoordeeld Vak Methode Scheikunde Chemie overal Hoofdstuk 6 2 De PH van een oplossing De ph/zuurgraad is een getal waarin de hoeveelheid zuur
Samenvatting Pulsar Chemie (Scheikunde): boek 1
 Samenvatting Pulsar Chemie (Scheikunde): boek 1 Hoofdstuk 1: Zouten 1: Atoombouw Reactie: hergroepering van atomen van het beginmolecuul naar het eindmolecuul Elektron: negatief geladen deeltje, onderdeel
Samenvatting Pulsar Chemie (Scheikunde): boek 1 Hoofdstuk 1: Zouten 1: Atoombouw Reactie: hergroepering van atomen van het beginmolecuul naar het eindmolecuul Elektron: negatief geladen deeltje, onderdeel
Fosfor kan met waterstof reageren. d Geef de vergelijking van de reactie van fosfor met waterstof.
 1 Een oplossing van zwavelzuur en een oplossing van bariumhydroxide geladen beide elektriciteit. Wordt bij de zwavelzuuroplossing een oplossing van bariumhydroxide gedruppeld, dan neemt het elektrisch
1 Een oplossing van zwavelzuur en een oplossing van bariumhydroxide geladen beide elektriciteit. Wordt bij de zwavelzuuroplossing een oplossing van bariumhydroxide gedruppeld, dan neemt het elektrisch
Hoofdstuk 3: Zuren en basen
 Hoofdstuk 3: Zuren en basen Scheikunde VWO 2011/2012 www.lyceo.nl Onderwerpen Scheikunde 2011 2012 Stoffen, structuur en binding Kenmerken van Reacties Zuren en base Redox Chemische technieken Koolstofchemie
Hoofdstuk 3: Zuren en basen Scheikunde VWO 2011/2012 www.lyceo.nl Onderwerpen Scheikunde 2011 2012 Stoffen, structuur en binding Kenmerken van Reacties Zuren en base Redox Chemische technieken Koolstofchemie
Samenvatting Scheikunde Hoofdstuk 3
 Samenvatting Scheikunde Hoofdstuk 3 Samenvatting door K. 1467 woorden 5 maart 2016 5,5 2 keer beoordeeld Vak Scheikunde Scheikunde Samenvatting H3 3V 3.1 Energie Fossiele brandstoffen -> nu nog er afhankelijk
Samenvatting Scheikunde Hoofdstuk 3 Samenvatting door K. 1467 woorden 5 maart 2016 5,5 2 keer beoordeeld Vak Scheikunde Scheikunde Samenvatting H3 3V 3.1 Energie Fossiele brandstoffen -> nu nog er afhankelijk
1. Elementaire chemie en chemisch rekenen
 In onderstaande zelftest zijn de vragen gebundeld die als voorbeeldvragen zijn opgenomen in het bijhorend overzicht van de verwachte voorkennis chemie. 1. Elementaire chemie en chemisch rekenen 1.1 Grootheden
In onderstaande zelftest zijn de vragen gebundeld die als voorbeeldvragen zijn opgenomen in het bijhorend overzicht van de verwachte voorkennis chemie. 1. Elementaire chemie en chemisch rekenen 1.1 Grootheden
5 Water, het begrip ph
 5 Water, het begrip ph 5.1 Water Waterstofchloride is een sterk zuur, het reageert als volgt met water: HCI(g) + H 2 0(I) Cl (aq) + H 3 O + (aq) z b Hierbij reageert water als base. Ammoniak is een zwakke
5 Water, het begrip ph 5.1 Water Waterstofchloride is een sterk zuur, het reageert als volgt met water: HCI(g) + H 2 0(I) Cl (aq) + H 3 O + (aq) z b Hierbij reageert water als base. Ammoniak is een zwakke
OEFENTOETS Zuren en basen 5 VWO
 OEFENTOETS Zuren en basen 5 VWO Gesloten vragen 1. Carolien wil de zuurgraad van een oplossing onderzoeken met twee verschillende zuur-baseindicatoren en neemt hierbij het volgende waar: I de oplossing
OEFENTOETS Zuren en basen 5 VWO Gesloten vragen 1. Carolien wil de zuurgraad van een oplossing onderzoeken met twee verschillende zuur-baseindicatoren en neemt hierbij het volgende waar: I de oplossing
Het eindexamen bestaat uit het centraal examen en het schoolexamen.
 Examenprogramma scheikunde h.a.v.o. geldig vanaf 2009 Toelichting In het nieuwe programma wordt onderscheid gemaakt tussen stof die uisluitend op het schoolexamen kan worden gevraagd en stof die ook op
Examenprogramma scheikunde h.a.v.o. geldig vanaf 2009 Toelichting In het nieuwe programma wordt onderscheid gemaakt tussen stof die uisluitend op het schoolexamen kan worden gevraagd en stof die ook op
Eindexamen scheikunde havo 2007-II
 Beoordelingsmodel Kwik 1 maximumscore 2 aantal protonen: 160 aantal elektronen: 158 aantal protonen: 160 1 aantal elektronen: het gegeven aantal protonen verminderd met 2 1 2 maximumscore 2 g 2 Cl 2 Indien
Beoordelingsmodel Kwik 1 maximumscore 2 aantal protonen: 160 aantal elektronen: 158 aantal protonen: 160 1 aantal elektronen: het gegeven aantal protonen verminderd met 2 1 2 maximumscore 2 g 2 Cl 2 Indien
Samenvatting hoofdstuk 2
 temperatuur in o Scheikunde hemie op school Samenvatting hoofdstuk 2 De bouw van stoffen Samenvatting hoofdstuk 2 Er zijn verschillende eigenschappen waaraan je een stof kunt herkennen. We noemen deze
temperatuur in o Scheikunde hemie op school Samenvatting hoofdstuk 2 De bouw van stoffen Samenvatting hoofdstuk 2 Er zijn verschillende eigenschappen waaraan je een stof kunt herkennen. We noemen deze
SCHEIKUNDE. Hoofdstuk 9
 SCHEIKUNDE Hoofdstuk 9 Par. 1 Elke chemische reactie heeft een energie-effect. De chemische energie voor én na de reactie is niet gelijk. Als de reactie warmer wordt is de chemische energie omgezet in
SCHEIKUNDE Hoofdstuk 9 Par. 1 Elke chemische reactie heeft een energie-effect. De chemische energie voor én na de reactie is niet gelijk. Als de reactie warmer wordt is de chemische energie omgezet in
Je kunt de ph van een oplossing meten met een ph-meter, met universeelindicatorpapier of met behulp van zuur-base-indicatoren.
 Boekverslag door Merel 797 woorden 22 januari 2017 6.9 14 keer beoordeeld Vak Methode Scheikunde Chemie overal Zie de bijlage voor de grafiek en alle tabellen. H8 Zuren en en Basen Chemie Overal 8.2 De
Boekverslag door Merel 797 woorden 22 januari 2017 6.9 14 keer beoordeeld Vak Methode Scheikunde Chemie overal Zie de bijlage voor de grafiek en alle tabellen. H8 Zuren en en Basen Chemie Overal 8.2 De
Hoofdstuk 2: Kenmerken van reacties
 Hoofdstuk 2: Kenmerken van reacties Scheikunde VWO 2011/2012 www.lyceo.nl Onderwerpen Scheikunde 2011 20122012 Stoffen, structuur en binding Kenmerken van Reacties Zuren en base Redox Chemische technieken
Hoofdstuk 2: Kenmerken van reacties Scheikunde VWO 2011/2012 www.lyceo.nl Onderwerpen Scheikunde 2011 20122012 Stoffen, structuur en binding Kenmerken van Reacties Zuren en base Redox Chemische technieken
Samenvatting Scheikunde Hoofdstuk 1, 2, 3
 Samenvatting Scheikunde Hoofdstuk 1, 2, 3 4 Samenvatting door Syb 1176 woorden 4 keer beoordeeld 4 maart 2018 Vak Scheikunde Methode Chemie overal Scheikunde H1/H2/H3 Samenvatting PARAGRAAF 1.1 Een stof
Samenvatting Scheikunde Hoofdstuk 1, 2, 3 4 Samenvatting door Syb 1176 woorden 4 keer beoordeeld 4 maart 2018 Vak Scheikunde Methode Chemie overal Scheikunde H1/H2/H3 Samenvatting PARAGRAAF 1.1 Een stof
1. Elementaire chemie en chemisch rekenen
 In onderstaande zelftest zijn de vragen gebundeld die als voorbeeldvragen zijn opgenomen in het bijhorend overzicht van de verwachte voorkennis chemie. 1. Elementaire chemie en chemisch rekenen 1.1 Grootheden
In onderstaande zelftest zijn de vragen gebundeld die als voorbeeldvragen zijn opgenomen in het bijhorend overzicht van de verwachte voorkennis chemie. 1. Elementaire chemie en chemisch rekenen 1.1 Grootheden
EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN Dit examen bestaat voor iedere kandidaat uit 5 OPGAVEN
 MAVO-4 II EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN 1974 MAVO-4 Dinsdag 11 juni, 9.00 11.00 NATUUR-EN SCHEIKUNDE II (Scheikunde) OPEN VRAGEN Dit examen bestaat voor iedere kandidaat uit 5 OPGAVEN
MAVO-4 II EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN 1974 MAVO-4 Dinsdag 11 juni, 9.00 11.00 NATUUR-EN SCHEIKUNDE II (Scheikunde) OPEN VRAGEN Dit examen bestaat voor iedere kandidaat uit 5 OPGAVEN
Paragraaf 1: Fossiele brandstoffen
 Scheikunde Hoofdstuk 2 Samenvatting Paragraaf 1: Fossiele brandstoffen Fossiele brandstof Koolwaterstof Onvolledige verbranding Broeikaseffect Brandstof ontstaan door het afsterven van levende organismen,
Scheikunde Hoofdstuk 2 Samenvatting Paragraaf 1: Fossiele brandstoffen Fossiele brandstof Koolwaterstof Onvolledige verbranding Broeikaseffect Brandstof ontstaan door het afsterven van levende organismen,
Samenvatting Scheikunde H3 Door: Immanuel Bendahan
 Samenvatting Scheikunde H3 Door: Immanuel Bendahan Inhoudsopgave 1 Atoommodel... 1 Moleculen... 1 De ontwikkeling van het atoommodel... 1 Atoommodel van Bohr... 2 Indicatoren van atomen... 3 2 Periodiek
Samenvatting Scheikunde H3 Door: Immanuel Bendahan Inhoudsopgave 1 Atoommodel... 1 Moleculen... 1 De ontwikkeling van het atoommodel... 1 Atoommodel van Bohr... 2 Indicatoren van atomen... 3 2 Periodiek
1.3 Periodiek systeem: - Periode = horizontale rij van elementen - Groep = verticale kolom van elementen
 Hoofdstuk 1 1.2 Neutronen = massagetal atoomnummer Massagetal = Protonen + Neutronen Atoomnummer = protonen (positief geladen) = elektronen (negatief geladen) Atomaire massa- eenheden Isotopen Atoommassa
Hoofdstuk 1 1.2 Neutronen = massagetal atoomnummer Massagetal = Protonen + Neutronen Atoomnummer = protonen (positief geladen) = elektronen (negatief geladen) Atomaire massa- eenheden Isotopen Atoommassa
13 Evenwichten. Hoofdstuk 13 Evenwichten. 13.1 Omkeerbare reacties. 13.2 Dynamisch evenwicht
 13 Evenwichten 13.1 Omkeerbare reacties Hoofdstuk 13 Evenwichten Het is in de praktijk vrijwel onmogelijk om beide reacties tegelijk te laten verlopen. 7 a Roze + n H 2 O Blauw.n H 2 O 3 1 a Schrijf beide
13 Evenwichten 13.1 Omkeerbare reacties Hoofdstuk 13 Evenwichten Het is in de praktijk vrijwel onmogelijk om beide reacties tegelijk te laten verlopen. 7 a Roze + n H 2 O Blauw.n H 2 O 3 1 a Schrijf beide
8,1. Samenvatting door een scholier 2527 woorden 27 oktober keer beoordeeld. Scheikunde. Hoofdstuk 1
 Samenvatting door een scholier 2527 woorden 27 oktober 2014 8,1 129 keer beoordeeld Vak Methode Scheikunde Chemie overal Hoofdstuk 1 Paragraaf 2 Een zuivere stof is 1 stof met een unieke combinatie stofeigenschappen.
Samenvatting door een scholier 2527 woorden 27 oktober 2014 8,1 129 keer beoordeeld Vak Methode Scheikunde Chemie overal Hoofdstuk 1 Paragraaf 2 Een zuivere stof is 1 stof met een unieke combinatie stofeigenschappen.
Samenvatting Scheikunde Scheikunde Chemie overal H1 3 vwo
 Samenvatting Scheikunde Scheikunde Chemie overal H1 3 vwo Samenvatting door een scholier 1193 woorden 30 oktober 2012 5,8 23 keer beoordeeld Vak Methode Scheikunde Chemie overal Samenvatting Scheikunde
Samenvatting Scheikunde Scheikunde Chemie overal H1 3 vwo Samenvatting door een scholier 1193 woorden 30 oktober 2012 5,8 23 keer beoordeeld Vak Methode Scheikunde Chemie overal Samenvatting Scheikunde
Eindexamen scheikunde havo 2006-I
 4 Beoordelingsmodel Rood licht Maximumscore 1 1 edelgassen 2 Voorbeelden van een juist antwoord zijn: De (negatieve) elektronen bewegen zich richting elektrode A dus is elektrode A de positieve elektrode.
4 Beoordelingsmodel Rood licht Maximumscore 1 1 edelgassen 2 Voorbeelden van een juist antwoord zijn: De (negatieve) elektronen bewegen zich richting elektrode A dus is elektrode A de positieve elektrode.
5 VWO. H8 zuren en basen
 5 VWO H8 zuren en basen Inleiding Opdracht 1, 20 min in tweetallen Nakijken; eventueel vragen stellen 8.2 Zure, neutrale en basische oplossingen 8.2 Zure, neutrale en Indicator (tabel 52A) Zuurgraad 0-14?
5 VWO H8 zuren en basen Inleiding Opdracht 1, 20 min in tweetallen Nakijken; eventueel vragen stellen 8.2 Zure, neutrale en basische oplossingen 8.2 Zure, neutrale en Indicator (tabel 52A) Zuurgraad 0-14?
Eindexamen scheikunde havo 2003-II
 4 Antwoordmodel Superzwaar 1 Een juiste berekening leidt tot de uitkomst 50 (neutronen). opzoeken van het atoomnummer van krypton (36) 1 berekening van het aantal neutronen: 86 verminderd met het atoomnummer
4 Antwoordmodel Superzwaar 1 Een juiste berekening leidt tot de uitkomst 50 (neutronen). opzoeken van het atoomnummer van krypton (36) 1 berekening van het aantal neutronen: 86 verminderd met het atoomnummer
ZUREN EN BASEN. Samenvatting voor het HAVO. versie mei 2013
 ZUREN EN BASEN Samenvatting voor het HAVO versie mei 2013 INHOUDSOPGAVE 1. Vooraf 2. Algemeen 3. Zuren 4. Basen 5. Het waterevenwicht 6. Definities ph en poh 7. ph BEREKENINGEN 7.1. Algemeen 7.2. Water
ZUREN EN BASEN Samenvatting voor het HAVO versie mei 2013 INHOUDSOPGAVE 1. Vooraf 2. Algemeen 3. Zuren 4. Basen 5. Het waterevenwicht 6. Definities ph en poh 7. ph BEREKENINGEN 7.1. Algemeen 7.2. Water
1. Elementaire chemie en chemisch rekenen
 In onderstaande zelftest zijn de vragen gebundeld die als voorbeeldvragen zijn opgenomen in het bijhorend overzicht van de verwachte voorkennis chemie. 1. Elementaire chemie en chemisch rekenen 1.1 Grootheden
In onderstaande zelftest zijn de vragen gebundeld die als voorbeeldvragen zijn opgenomen in het bijhorend overzicht van de verwachte voorkennis chemie. 1. Elementaire chemie en chemisch rekenen 1.1 Grootheden
1.3 Periodiek systeem: - Periode = horizontale rij van elementen - Groep = verticale kolom van elementen
 Hoofdstuk 1 1.2 Neutronen = massagetal atoomnummer Massagetal = Protonen + Neutronen Atoomnummer = protonen (positief geladen) = elektronen (negatief geladen) Atomaire massa- eenheden 1,00 u = 1,66*10-27
Hoofdstuk 1 1.2 Neutronen = massagetal atoomnummer Massagetal = Protonen + Neutronen Atoomnummer = protonen (positief geladen) = elektronen (negatief geladen) Atomaire massa- eenheden 1,00 u = 1,66*10-27
Opgaven zuurgraad (ph) berekenen. ph = -log [H + ] poh = -log [OH - ] [H + ] = 10 -ph [OH - ] = 10 -poh. ph = 14 poh poh = 14 ph ph + poh = 14
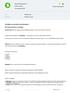
![Opgaven zuurgraad (ph) berekenen. ph = -log [H + ] poh = -log [OH - ] [H + ] = 10 -ph [OH - ] = 10 -poh. ph = 14 poh poh = 14 ph ph + poh = 14 Opgaven zuurgraad (ph) berekenen. ph = -log [H + ] poh = -log [OH - ] [H + ] = 10 -ph [OH - ] = 10 -poh. ph = 14 poh poh = 14 ph ph + poh = 14](/thumbs/82/85039734.jpg) Opgaven zuurgraad (ph) berekenen Met behulp van deze formules dien je berekeningen te kunnen uitvoeren. Deze hoef je niet uit je hoofd te leren, maar je moet ze wel kunnen toepassen. Bij een toets zullen
Opgaven zuurgraad (ph) berekenen Met behulp van deze formules dien je berekeningen te kunnen uitvoeren. Deze hoef je niet uit je hoofd te leren, maar je moet ze wel kunnen toepassen. Bij een toets zullen
ANTWOORDEN Herhaling zuren, basen en buffers
 ANTWOORDEN Herhaling zuren, basen en buffers 1) Wat geeft de onderstaande afbeelding weer? Je ziet deze deeltjes afgebeeld: het zwakke zuur HA (want veel deeltjes zijn niet geïoniseerd), de zwakke base
ANTWOORDEN Herhaling zuren, basen en buffers 1) Wat geeft de onderstaande afbeelding weer? Je ziet deze deeltjes afgebeeld: het zwakke zuur HA (want veel deeltjes zijn niet geïoniseerd), de zwakke base
Onderwerp: Onderzoek doen Kerndoel(en): 28 Leerdoel(en): - Onderzoek doen aan de hand van onderzoeksvragen - Uitkomsten van onderzoek presenteren.
 Vak: Scheikunde Leerjaar: Kerndoel(en): 28 De leerling leert vragen over onderwerpen uit het brede leergebied om te zetten in onderzoeksvragen, een dergelijk onderzoek over een natuurwetenschappelijk onderwerp
Vak: Scheikunde Leerjaar: Kerndoel(en): 28 De leerling leert vragen over onderwerpen uit het brede leergebied om te zetten in onderzoeksvragen, een dergelijk onderzoek over een natuurwetenschappelijk onderwerp
Module 2 Chemische berekeningen Antwoorden
 2 Meten is weten 1 Nee, want bijvoorbeeld 0,0010 kg is net zo nauwkeurig als 1,0 gram. 2 De minst betrouwbare meting is de volumemeting. Deze variabele bepaald het aantal significante cijfers. 3 IJs: 1,5
2 Meten is weten 1 Nee, want bijvoorbeeld 0,0010 kg is net zo nauwkeurig als 1,0 gram. 2 De minst betrouwbare meting is de volumemeting. Deze variabele bepaald het aantal significante cijfers. 3 IJs: 1,5
Chemie (ph) bij het inkuilen Scheikunde klas V41a en V41b door Erik Held
 Chemie (ph) bij het inkuilen Scheikunde klas V41a en V41b door Erik Held Inkuilproces Proces bij het inkuilen: In de kuil ondergaat het gewas een biochemisch proces onder invloed van micro-organismen Een
Chemie (ph) bij het inkuilen Scheikunde klas V41a en V41b door Erik Held Inkuilproces Proces bij het inkuilen: In de kuil ondergaat het gewas een biochemisch proces onder invloed van micro-organismen Een
Dit examen bestaat voor iedere kandidaat uit 20 vragen
 MAVO-4 II EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN 1982 MAVO-4 Woensdag 15 juni, 9.00 11.00 NATUUR-EN SCHEIKUNDE II (Scheikunde) MEERKEUZETOETS Dit examen bestaat voor iedere kandidaat uit 20
MAVO-4 II EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN 1982 MAVO-4 Woensdag 15 juni, 9.00 11.00 NATUUR-EN SCHEIKUNDE II (Scheikunde) MEERKEUZETOETS Dit examen bestaat voor iedere kandidaat uit 20
Vraag Antwoord Scores
 Ademtest 1 maximumscore 2 Voorbeelden van een juist antwoord zijn: Een ureummolecuul bevat NH 2 groepen / N-H bindingen, zodat er waterstbruggen (met watermoleculen) gevormd kunnen worden. (Dus ureum is
Ademtest 1 maximumscore 2 Voorbeelden van een juist antwoord zijn: Een ureummolecuul bevat NH 2 groepen / N-H bindingen, zodat er waterstbruggen (met watermoleculen) gevormd kunnen worden. (Dus ureum is
toelatingsexamen-geneeskunde.be Vraag 2 Wat is de ph van een zwakke base in een waterige oplossing met een concentratie van 0,1 M?
 Chemie juli 2009 Laatste wijziging: 31/07/09 Gebaseerd op vragen uit het examen. Vraag 1 Geef de structuurformule van nitriet. A. B. C. D. Vraag 2 Wat is de ph van een zwakke base in een waterige oplossing
Chemie juli 2009 Laatste wijziging: 31/07/09 Gebaseerd op vragen uit het examen. Vraag 1 Geef de structuurformule van nitriet. A. B. C. D. Vraag 2 Wat is de ph van een zwakke base in een waterige oplossing
Scheikunde leerjaar 2
 Scheikunde leerjaar 2 De verbranding van suiker. De ontleding van koper(i)jodide. Het vormen van vast ijzer(ii)sulfide. Verbranding van methaan. Bij de reactie van natrium met zwavel ontstaat natriumsulfide.
Scheikunde leerjaar 2 De verbranding van suiker. De ontleding van koper(i)jodide. Het vormen van vast ijzer(ii)sulfide. Verbranding van methaan. Bij de reactie van natrium met zwavel ontstaat natriumsulfide.
Eindexamen scheikunde havo 2011 - I
 Beoordelingsmodel Uraanerts 1 maximumscore 2 aantal protonen: 92 aantal elektronen: 88 aantal protonen: 92 1 aantal elektronen: aantal protonen verminderd met 4 1 2 maximumscore 2 Voorbeelden van een juist
Beoordelingsmodel Uraanerts 1 maximumscore 2 aantal protonen: 92 aantal elektronen: 88 aantal protonen: 92 1 aantal elektronen: aantal protonen verminderd met 4 1 2 maximumscore 2 Voorbeelden van een juist
Scheikunde Samenvatting H4+H5
 Scheikunde Samenvatting H4+H5 Hoofdstuk 4 4.2 Stoffen worden ingedeeld op grond van hun eigenschappen. Er zijn niet-ontleedbare stoffen en ontleedbare stoffen. De niet-ontleedbare stoffen zijn verdeeld
Scheikunde Samenvatting H4+H5 Hoofdstuk 4 4.2 Stoffen worden ingedeeld op grond van hun eigenschappen. Er zijn niet-ontleedbare stoffen en ontleedbare stoffen. De niet-ontleedbare stoffen zijn verdeeld
Samenvatting Scheikunde Hoofdstuk 1 t/m 4
 Samenvatting Scheikunde Hoofdstuk 1 t/m 4 Samenvatting door een scholier 2010 woorden 31 maart 2010 5,5 57 keer beoordeeld Vak Methode Scheikunde Chemie overal Scheikunde Hoofdstuk 1: De bouw van stoffen
Samenvatting Scheikunde Hoofdstuk 1 t/m 4 Samenvatting door een scholier 2010 woorden 31 maart 2010 5,5 57 keer beoordeeld Vak Methode Scheikunde Chemie overal Scheikunde Hoofdstuk 1: De bouw van stoffen
Samenvatting Scheikunde Hoofdstukken 8&9: zuren en basen
 Samenvatting Scheikunde Hoofdstukken 8&9: zuren en basen Samenvatting door een scholier 1810 woorden 4 december 2017 4,8 9 keer beoordeeld Vak Methode Scheikunde Chemie overal Scheikunde hoofdstuk 8 Zuren
Samenvatting Scheikunde Hoofdstukken 8&9: zuren en basen Samenvatting door een scholier 1810 woorden 4 december 2017 4,8 9 keer beoordeeld Vak Methode Scheikunde Chemie overal Scheikunde hoofdstuk 8 Zuren
UITWERKING TOELICHTING OP DE ANTWOORDEN VAN HET EXAMEN 2001-I EXAMEN: 2001-I
 UITWERKING TOELICHTING OP DE ANTWOORDEN VAN HET EXAMEN 2001-I VAK: NIVEAU: SCHEIKUNDE HAVO EXAMEN: 2001-I De uitgever heeft ernaar gestreefd de auteursrechten te regelen volgens de wettelijke bepalingen.
UITWERKING TOELICHTING OP DE ANTWOORDEN VAN HET EXAMEN 2001-I VAK: NIVEAU: SCHEIKUNDE HAVO EXAMEN: 2001-I De uitgever heeft ernaar gestreefd de auteursrechten te regelen volgens de wettelijke bepalingen.
Scheikunde hoofdstuk 8 en 9 VWO 5 SE 2 Hoofdstuk 8
 Scheikunde hoofdstuk 8 en 9 VWO 5 SE 2 Hoofdstuk 8 2 Een oplossing kan zuur, basisch of neutraal zijn. Om het verschil in zuurgraad in een getal te kunnen uitdrukken gebruik je de ph. Is de ph < 7 is de
Scheikunde hoofdstuk 8 en 9 VWO 5 SE 2 Hoofdstuk 8 2 Een oplossing kan zuur, basisch of neutraal zijn. Om het verschil in zuurgraad in een getal te kunnen uitdrukken gebruik je de ph. Is de ph < 7 is de
Zelfs zuiver water geleidt in zeer kleine mate elektrische stroom en dus wijst dit op de aanwezigheid van geladen deeltjes.
 Cursus Chemie 4-1 Hoofdstuk 4: CHEMISCH EVENWICHT 1. DE STERKTE VAN ZUREN EN BASEN Als HCl in water opgelost wordt dan bekomen we een oplossing die bijna geen enkele covalente HCl meer bevat. In de reactievergelijking
Cursus Chemie 4-1 Hoofdstuk 4: CHEMISCH EVENWICHT 1. DE STERKTE VAN ZUREN EN BASEN Als HCl in water opgelost wordt dan bekomen we een oplossing die bijna geen enkele covalente HCl meer bevat. In de reactievergelijking
EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN Dit examen bestaat voor iedere kandidaat uit 8 OPGAVEN
 MAVO-4 I EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN 1973 MAVO-4 Woensdag 9 mei, 9.00 11.00 NATUUR-EN SCHEIKUNDE II (Scheikunde) OPEN VRAGEN Dit examen bestaat voor iedere kandidaat uit 8 OPGAVEN
MAVO-4 I EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN 1973 MAVO-4 Woensdag 9 mei, 9.00 11.00 NATUUR-EN SCHEIKUNDE II (Scheikunde) OPEN VRAGEN Dit examen bestaat voor iedere kandidaat uit 8 OPGAVEN
Hoofdstuk 6: Zure en base oplossingen / ph
 Hoofdstuk 6: Zure en base oplossingen / ph 6.1 Herhaling: zure en basische oplossingen Arrhenius definieerde zuren als volgt: zuren zijn polaire covalente verbindingen die bij het oplossen in water H +
Hoofdstuk 6: Zure en base oplossingen / ph 6.1 Herhaling: zure en basische oplossingen Arrhenius definieerde zuren als volgt: zuren zijn polaire covalente verbindingen die bij het oplossen in water H +
Eindexamen scheikunde havo 2008-I
 Beoordelingsmodel Uraan 1 maximumscore 2 aantal protonen: 92 aantal neutronen: 146 aantal protonen: 92 1 aantal neutronen: 238 verminderen met het aantal protonen 1 2 maximumscore 2 UO 2 + 4 HF UF 4 +
Beoordelingsmodel Uraan 1 maximumscore 2 aantal protonen: 92 aantal neutronen: 146 aantal protonen: 92 1 aantal neutronen: 238 verminderen met het aantal protonen 1 2 maximumscore 2 UO 2 + 4 HF UF 4 +
Verbetering Chemie 1997 juli
 www. Verbetering Chemie 1997 juli Vraag 1 Reactievergelijking: Fe 2 O 3 + 2 Al Al 2 O 3 + 2 Fe Molaire massa s: Fe 2 O 3 : ( 2 x 55,9) + (3 x 16,0) = 159,8 g mol -1 Al: 27 g mol -1 Hoeveelheid stof: Fe
www. Verbetering Chemie 1997 juli Vraag 1 Reactievergelijking: Fe 2 O 3 + 2 Al Al 2 O 3 + 2 Fe Molaire massa s: Fe 2 O 3 : ( 2 x 55,9) + (3 x 16,0) = 159,8 g mol -1 Al: 27 g mol -1 Hoeveelheid stof: Fe
scheikunde oude stijl havo 2015-I
 Snelle auto's 1 maximumscore 2 Voorbeelden van een juist antwoord zijn: De molecuulformule C 7 H 12 voldoet niet aan de algemene formule voor alkanen: C n H 2n+2. Het mengsel bestaat dus niet uitsluitend
Snelle auto's 1 maximumscore 2 Voorbeelden van een juist antwoord zijn: De molecuulformule C 7 H 12 voldoet niet aan de algemene formule voor alkanen: C n H 2n+2. Het mengsel bestaat dus niet uitsluitend
3. Welke van onderstaande formules geeft een zout aan? A. Al 2O 3 B. P 2O 3 C. C 2H 6 D. NH 3
 Toelatingsexamens en Ondersteunend Onderwijs VOORBLAD EXAMENOPGAVEN Toetsdatum: n.v.t. Vak: Scheikunde voorbeeldexamen 2015 Tijdsduur: 2 uur en 30 minuten De volgende hulpmiddelen zijn toegestaan bij het
Toelatingsexamens en Ondersteunend Onderwijs VOORBLAD EXAMENOPGAVEN Toetsdatum: n.v.t. Vak: Scheikunde voorbeeldexamen 2015 Tijdsduur: 2 uur en 30 minuten De volgende hulpmiddelen zijn toegestaan bij het
Samenvatting Scheikunde Hoofdstuk 2 stoffen en reacties
 Samenvatting Scheikunde Hoofdstuk 2 stoffen en reacties Samenvatting door F. 1622 woorden 22 mei 2015 6,1 40 keer beoordeeld Vak Methode Scheikunde Nova Paragraaf 1 Gloeien, smelten en verdampen Als je
Samenvatting Scheikunde Hoofdstuk 2 stoffen en reacties Samenvatting door F. 1622 woorden 22 mei 2015 6,1 40 keer beoordeeld Vak Methode Scheikunde Nova Paragraaf 1 Gloeien, smelten en verdampen Als je
Eindexamen scheikunde havo I
 pgave (mono)stikstofmono-oxide Indien als antwoord stikstofoxide is gegeven 2 Een juiste verklaring leidt tot de uitkomst 7 (elektronen). elk atoom bevat 8 elektronen in totaal bevat het 2 - ion dus 2
pgave (mono)stikstofmono-oxide Indien als antwoord stikstofoxide is gegeven 2 Een juiste verklaring leidt tot de uitkomst 7 (elektronen). elk atoom bevat 8 elektronen in totaal bevat het 2 - ion dus 2
Eindexamen vwo scheikunde pilot I
 Duurzame productie van waterstof uit afvalwater 1 maximumscore 4 C 6 H 12 O 6 + 4 H 2 O 4 H 2 + 2 CH 3 COO + 2 HCO 3 + 4 H + molverhouding CH 3 COO : HCO 3 = 1 : 1 en C balans juist 1 coëfficiënt voor
Duurzame productie van waterstof uit afvalwater 1 maximumscore 4 C 6 H 12 O 6 + 4 H 2 O 4 H 2 + 2 CH 3 COO + 2 HCO 3 + 4 H + molverhouding CH 3 COO : HCO 3 = 1 : 1 en C balans juist 1 coëfficiënt voor
Antwoorden deel 1. Scheikunde Chemie overal
 Antwoorden deel 1 Scheikunde Chemie overal Huiswerk 2. a. Zuivere berglucht is scheikundig gezien geen zuivere stof omdat er in lucht verschillende moleculen zitten (zuurstof, stikstof enz.) b. Niet vervuild
Antwoorden deel 1 Scheikunde Chemie overal Huiswerk 2. a. Zuivere berglucht is scheikundig gezien geen zuivere stof omdat er in lucht verschillende moleculen zitten (zuurstof, stikstof enz.) b. Niet vervuild
5-1 Moleculen en atomen
 5-1 Moleculen en atomen Vraag 1. Uit hoeveel soorten moleculen bestaat een zuivere stof? Vraag 2. Wat is een molecuul? Vraag 3. Wat is een atoom? Vraag 4. Van welke heb je er het meeste: moleculen of atomen?
5-1 Moleculen en atomen Vraag 1. Uit hoeveel soorten moleculen bestaat een zuivere stof? Vraag 2. Wat is een molecuul? Vraag 3. Wat is een atoom? Vraag 4. Van welke heb je er het meeste: moleculen of atomen?
Eindexamen scheikunde havo 2005-I
 4 Beoordelingsmodel Zeewater 1 Sr 2+ juist symbool 1 juiste lading bij gegeven symbool 1 2 aantal protonen: 6 aantal neutronen: 8 juiste aantal protonen 1 aantal neutronen: 14 verminderen met het aantal
4 Beoordelingsmodel Zeewater 1 Sr 2+ juist symbool 1 juiste lading bij gegeven symbool 1 2 aantal protonen: 6 aantal neutronen: 8 juiste aantal protonen 1 aantal neutronen: 14 verminderen met het aantal
Eindexamen scheikunde havo II
 Opgave aantal protonen : 48 aantal elektronen : 46 aantal protonen: 48 aantal elektronen: aantal protonen minus 2 2 selenide ion : Se 2- cadmium(ii)selenide : dse selenide-ion: Se 2- formule cadmiumselenide
Opgave aantal protonen : 48 aantal elektronen : 46 aantal protonen: 48 aantal elektronen: aantal protonen minus 2 2 selenide ion : Se 2- cadmium(ii)selenide : dse selenide-ion: Se 2- formule cadmiumselenide
1) Stoffen, moleculen en atomen
 Herhaling leerstof klas 3 1) Stoffen, moleculen en atomen Scheikundigen houden zich bezig met stoffen. Betekenissen van stof zijn onder andere: - Het materiaal waar kleding van gemaakt is; - Fijne vuildeeltjes;
Herhaling leerstof klas 3 1) Stoffen, moleculen en atomen Scheikundigen houden zich bezig met stoffen. Betekenissen van stof zijn onder andere: - Het materiaal waar kleding van gemaakt is; - Fijne vuildeeltjes;
atomen die we nu kennen kunnen we tientallen miljoenen moleculen maken veel verschillende soorten stoffen.
 Samenvatting door F. 2194 woorden 15 november 2014 8 31 keer beoordeeld Vak Methode Scheikunde Chemie overal Zie bijlage voor grafieke en berekeningen! 1.2 zuivere stoffen en mengsels Zuivere stof: één
Samenvatting door F. 2194 woorden 15 november 2014 8 31 keer beoordeeld Vak Methode Scheikunde Chemie overal Zie bijlage voor grafieke en berekeningen! 1.2 zuivere stoffen en mengsels Zuivere stof: één
SCHEIKUNDEOLYMPIADE 2018
 SCHEIKUNDEOLYMPIADE 018 CORRECTIEMODEL VOORRONDE 1 af te nemen in de periode van 15 tot en met 7 januari 018 Deze voorronde bestaat uit 0 meerkeuzevragen verdeeld over 8 onderwerpen en opgaven met in totaal
SCHEIKUNDEOLYMPIADE 018 CORRECTIEMODEL VOORRONDE 1 af te nemen in de periode van 15 tot en met 7 januari 018 Deze voorronde bestaat uit 0 meerkeuzevragen verdeeld over 8 onderwerpen en opgaven met in totaal
ZUIVERE STOF één stof, gekenmerkt door welbepaalde fysische constanten zoals kooktemperatuur, massadichtheid,.
 PARATE KENNIS CHEMIE 4 e JAAR SCHEMA ZUIVERE STOF één stof, gekenmerkt door welbepaalde fysische constanten zoals kooktemperatuur, massadichtheid,. MENGSEL bestaat uit meerdere zuivere stoffen, de kooktemperatuur,
PARATE KENNIS CHEMIE 4 e JAAR SCHEMA ZUIVERE STOF één stof, gekenmerkt door welbepaalde fysische constanten zoals kooktemperatuur, massadichtheid,. MENGSEL bestaat uit meerdere zuivere stoffen, de kooktemperatuur,
Bindingen. Suiker Suiker heeft de molecuulformule C 12 H 22 O 11
 Bindingen Suiker Suiker heeft de molecuulformule C 12 H 22 O 11 1. Leg uit dat suiker een moleculaire stof is 2. Van suiker is de oplosbaarheid in water zeer hoog. Leg uit waarom suiker zo goed in water
Bindingen Suiker Suiker heeft de molecuulformule C 12 H 22 O 11 1. Leg uit dat suiker een moleculaire stof is 2. Van suiker is de oplosbaarheid in water zeer hoog. Leg uit waarom suiker zo goed in water
Oefenvraagstukken 5 HAVO Hoofdstuk 13 Antwoordmodel
 Oefenvraagstukken 5 AVO oofdstuk 13 Antwoordmodel Reactieomstandigheden 1 + 2 et zuur was in overmaat aanwezig dus de hoeveelheid O 2 is afhankelijk van de hoeveelheid ao 3. Alle drie gaan uit van dezelfde
Oefenvraagstukken 5 AVO oofdstuk 13 Antwoordmodel Reactieomstandigheden 1 + 2 et zuur was in overmaat aanwezig dus de hoeveelheid O 2 is afhankelijk van de hoeveelheid ao 3. Alle drie gaan uit van dezelfde
6,3. Samenvatting door N woorden 29 april keer beoordeeld. Scheikunde
 Samenvatting door N. 2779 woorden 29 april 2015 6,3 13 keer beoordeeld Vak Methode Scheikunde Chemie overal Zuivere stof: één stof met een unieke combinatie van stofeigenschappen. Bestaat uit dezelfde
Samenvatting door N. 2779 woorden 29 april 2015 6,3 13 keer beoordeeld Vak Methode Scheikunde Chemie overal Zuivere stof: één stof met een unieke combinatie van stofeigenschappen. Bestaat uit dezelfde
Dit examen bestaat voor iedere kandidaat uit 20 vragen
 MV0-3 EXMEN MELR LGEMEEN VOORTGEZET ONERWJS N 1982 MV0-3 onderdag 6 mei, 9.00-11.00 uur NTUUR- EN SHEKUNE (Scheikunde) MEERKEUZETOETS it examen bestaat voor iedere kandidaat uit 20 vragen ij het examen
MV0-3 EXMEN MELR LGEMEEN VOORTGEZET ONERWJS N 1982 MV0-3 onderdag 6 mei, 9.00-11.00 uur NTUUR- EN SHEKUNE (Scheikunde) MEERKEUZETOETS it examen bestaat voor iedere kandidaat uit 20 vragen ij het examen
Oefenopgaven CHEMISCHE INDUSTRIE
 Oefenopgaven CEMISCE INDUSTRIE havo OPGAVE 1 Een bereidingswijze van fosfor, P 4, kan men als volgt weergeven: Ca 3 (PO 4 ) 2 + SiO 2 + C P 4 + CO + CaSiO 3 01 Neem bovenstaande reactievergelijking over
Oefenopgaven CEMISCE INDUSTRIE havo OPGAVE 1 Een bereidingswijze van fosfor, P 4, kan men als volgt weergeven: Ca 3 (PO 4 ) 2 + SiO 2 + C P 4 + CO + CaSiO 3 01 Neem bovenstaande reactievergelijking over
scheikunde vwo 2017-II
 Kerosine uit zonlicht maximumscore 3 Een voorbeeld van een juiste berekening is: E = ( 2,42 0 5 ) + 0,5 ( 3,935 0 5 ) + 0,5 (,05 0 5 ) = +3,84 0 5 (J mol ). juiste verwerking van de vormingswarmten van
Kerosine uit zonlicht maximumscore 3 Een voorbeeld van een juiste berekening is: E = ( 2,42 0 5 ) + 0,5 ( 3,935 0 5 ) + 0,5 (,05 0 5 ) = +3,84 0 5 (J mol ). juiste verwerking van de vormingswarmten van
4. Van twee stoffen is hieronder de structuurformule weergegeven.
 MAVO Herexamen 1976 1. Beantwoord de volgende vragen over het element calcium. a. Hoeveel protonen bevat een atoom van dit element? Licht het antwoord toe. b. Hoe zijn de elektronen over de schillen verdeeld?
MAVO Herexamen 1976 1. Beantwoord de volgende vragen over het element calcium. a. Hoeveel protonen bevat een atoom van dit element? Licht het antwoord toe. b. Hoe zijn de elektronen over de schillen verdeeld?
7.1 Het deeltjesmodel
 Samenvatting door Mira 1711 woorden 24 juni 2017 10 3 keer beoordeeld Vak NaSk 7.1 Het deeltjesmodel Een model van een stof Elke stof heeft zijn eigen soort moleculen. Aangezien je niet kunt zien hoe een
Samenvatting door Mira 1711 woorden 24 juni 2017 10 3 keer beoordeeld Vak NaSk 7.1 Het deeltjesmodel Een model van een stof Elke stof heeft zijn eigen soort moleculen. Aangezien je niet kunt zien hoe een
Eindexamen scheikunde havo 2001-II
 Eindexamen scheikunde havo 00-II 4 Antwoordmodel Energievoorziening in de ruimte et (uiteenvallen van de Pu-38 atomen) levert energie dus het is een exotherm proces. er komt energie vrij aantal protonen:
Eindexamen scheikunde havo 00-II 4 Antwoordmodel Energievoorziening in de ruimte et (uiteenvallen van de Pu-38 atomen) levert energie dus het is een exotherm proces. er komt energie vrij aantal protonen:
Hoofdstuk 4. Chemische reacties. J.A.W. Faes (2019)
 Hoofdstuk 4 Chemische reacties J.A.W. Faes (2019) Hoofdstuk 4 Chemische reacties Paragrafen 4.1 Kenmerken van een reactie 4.2 Reactievergelijkingen 4.3 Rekenen aan reacties Practica Exp. 1 Waarnemen Exp.
Hoofdstuk 4 Chemische reacties J.A.W. Faes (2019) Hoofdstuk 4 Chemische reacties Paragrafen 4.1 Kenmerken van een reactie 4.2 Reactievergelijkingen 4.3 Rekenen aan reacties Practica Exp. 1 Waarnemen Exp.
Samenvatting Scheikunde H3 Reacties
 Samenvatting Scheikunde H3 Reacties Samenvatting door L. 710 woorden 7 december 2016 6,8 24 keer beoordeeld Vak Methode Scheikunde Chemie overal Scheikunde Hoofdstuk 3: Reacties 3.2 Kenmerken van een chemische
Samenvatting Scheikunde H3 Reacties Samenvatting door L. 710 woorden 7 december 2016 6,8 24 keer beoordeeld Vak Methode Scheikunde Chemie overal Scheikunde Hoofdstuk 3: Reacties 3.2 Kenmerken van een chemische
3.1 Energie. 3.2 Kenmerken chemische reactie
 3.1 Energie Wat is energie? Energie voorziening Fossiele brandstof verbranden Co2 komt vrij slecht voor het broeikaseffect Windmolen park Zonnepanelen Energie is iets wat nodig is voor een verbrandingsreactie
3.1 Energie Wat is energie? Energie voorziening Fossiele brandstof verbranden Co2 komt vrij slecht voor het broeikaseffect Windmolen park Zonnepanelen Energie is iets wat nodig is voor een verbrandingsreactie
SE voorbeeldtoets 5HAVO antwoordmodel
 SE voorbeeldtoets 5AV antwoordmodel Stikstof Zwaar stikstofgas bestaat uit stikstofmoleculen waarin uitsluitend stikstofatomen voorkomen met massagetal 15. 2p 1 oeveel protonen en hoeveel neutronen bevat
SE voorbeeldtoets 5AV antwoordmodel Stikstof Zwaar stikstofgas bestaat uit stikstofmoleculen waarin uitsluitend stikstofatomen voorkomen met massagetal 15. 2p 1 oeveel protonen en hoeveel neutronen bevat
Natuurlijk heb je nu nog géén massa s berekend. Maar dat kan altijd later nog. En dan kun je mooi kiezen, van welke stoffen je de massa wil berekenen.
 Hoofdstuk 17: Rekenen in molverhoudingen 17.1 Rekenen aan reacties: een terugblik én een alternatief In hoofdstuk 11 hebben we gerekend aan reacties. Het achterliggende idee was vaak, dat je bij een reactie
Hoofdstuk 17: Rekenen in molverhoudingen 17.1 Rekenen aan reacties: een terugblik én een alternatief In hoofdstuk 11 hebben we gerekend aan reacties. Het achterliggende idee was vaak, dat je bij een reactie
1. Elementaire chemie en chemisch rekenen
 In onderstaande zelftest zijn de vragen gebundeld die als voorbeeldvragen zijn opgenomen in het bijhorend overzicht van de verwachte voorkennis chemie 1. Elementaire chemie en chemisch rekenen 1.1 Grootheden
In onderstaande zelftest zijn de vragen gebundeld die als voorbeeldvragen zijn opgenomen in het bijhorend overzicht van de verwachte voorkennis chemie 1. Elementaire chemie en chemisch rekenen 1.1 Grootheden
Rekenen aan reacties (de mol)
 Rekenen aan reacties (de mol) 1. Reactievergelijkingen oefenen: Scheikunde Deze opgaven zijn bedoeld voor diegenen die moeite hebben met rekenen aan reacties 1. Reactievergelijkingen http://www.nassau-sg.nl/scheikunde/tutorials/deeltjes/deeltjes.html
Rekenen aan reacties (de mol) 1. Reactievergelijkingen oefenen: Scheikunde Deze opgaven zijn bedoeld voor diegenen die moeite hebben met rekenen aan reacties 1. Reactievergelijkingen http://www.nassau-sg.nl/scheikunde/tutorials/deeltjes/deeltjes.html
Scheikunde Chemie overal Week 1. Kelly van Helden
 Scheikunde Chemie overal Week 1 Kelly van Helden 1.1 Chemie om je heen Scheikunde is overal Scheiden of zuiveren van stoffen Veranderen van grondstoffen in bruikbare stoffen Drinkwater uit zeewater Poetsen
Scheikunde Chemie overal Week 1 Kelly van Helden 1.1 Chemie om je heen Scheikunde is overal Scheiden of zuiveren van stoffen Veranderen van grondstoffen in bruikbare stoffen Drinkwater uit zeewater Poetsen
Oefenopgaven ZUREN en BASEN havo
 Oefenopgaven ZUREN en BASEN havo OPGAVE 1 Men lost de volgende zouten op in water: (i) ammoniumnitraat (ii) kaliumsulfide (iii) natriumwaterstofsulfaat 01 Geef voor elk van deze zouten de oplosvergelijking.
Oefenopgaven ZUREN en BASEN havo OPGAVE 1 Men lost de volgende zouten op in water: (i) ammoniumnitraat (ii) kaliumsulfide (iii) natriumwaterstofsulfaat 01 Geef voor elk van deze zouten de oplosvergelijking.
Samenvatting Scheikunde H6 (Chemie)
 Samenvatting Scheikunde H6 (Chemie) Samenvatting door een scholier 892 woorden 18 maart 2004 5,1 73 keer beoordeeld Vak Scheikunde Scheikunde Hoofdstuk 6 Twee soorten bindingen bij moleculaire stoffen:
Samenvatting Scheikunde H6 (Chemie) Samenvatting door een scholier 892 woorden 18 maart 2004 5,1 73 keer beoordeeld Vak Scheikunde Scheikunde Hoofdstuk 6 Twee soorten bindingen bij moleculaire stoffen:
Extra oefenopgaven. Inleiding Scheikunde voor anesthesiemedewerkers en operatie-assistenten assistenten i.o. voorjaar 2008
 Extra oefenopgaven Inleiding Scheikunde voor anesthesiemedewerkers en operatie-assistenten assistenten i.o. voorjaar 2008 1. Geef van de volgende stoffen de chemische formule; geef ook aan tot welke categorie
Extra oefenopgaven Inleiding Scheikunde voor anesthesiemedewerkers en operatie-assistenten assistenten i.o. voorjaar 2008 1. Geef van de volgende stoffen de chemische formule; geef ook aan tot welke categorie
Wat zijn anorganische of minerale stoffen? In hoeveel stofklassen zijn de anorganische stoffen in te delen?
 Wat zijn anorganische of minerale stoffen? A. Deze stoffen komen hoofdzakelijk voor in de niet-levende natuur. In hoeveel stofklassen zijn de anorganische stoffen in te delen? B. 4 Welk van deze stofklassen
Wat zijn anorganische of minerale stoffen? A. Deze stoffen komen hoofdzakelijk voor in de niet-levende natuur. In hoeveel stofklassen zijn de anorganische stoffen in te delen? B. 4 Welk van deze stofklassen
