Bijlage III. Wijzigingen in de relevante rubrieken van de productinformatie
|
|
|
- Bert de clercq
- 5 jaren geleden
- Aantal bezoeken:
Transcriptie
1 Bijlage III Wijzigingen in de relevante rubrieken van de productinformatie Opmerking: Deze wijzigingen in de relevante rubrieken van de productinformatie zijn de uitkomst van de Referralprocedure. De productinformatie kan, indien nodig, vervolgens door de bevoegde instanties van de Lidstaat bijgewerkt worden, in samenspraak met de referentielidstaat (RMS), in overeenstemming met de procedures die zijn beschreven in hoofdstuk 4 van Titel III van Richtlijn 2001/83/EG. 52
2 Wijzigingen in de relevante rubrieken van de productinformatie De bestaande productinformatie moet worden aangepast (invoegen, vervangen of verwijderen van de tekst waar dit van toepassing is), om de overeengekomen tekst zoals hieronder weergegeven te reflecteren. Intraveneus gadoteerzuur, gadobutrol, gadoteridol magnetische resonantiebeeldvorming (MRI). De laagste dosis, die nog voldoende verhoging van het contrast geeft voor diagnostische doeleinden, moet worden gebruikt. De dosis moet worden berekend op basis van het lichaamsgewicht van de patiënt, en mag de in deze rubriek vermelde aanbevolen dosis per kilogram lichaamsgewicht niet overschrijden. Intra-articulair gadoteerzuur magnetische resonantiebeeldvorming (MRI). De laagste dosis, die nog voldoende verhoging van het contrast geeft voor diagnostische doeleinden, moet worden gebruikt. Intra-articulair gadopentetinezuur magnetische resonantiebeeldvorming (MRI) en wanneer een ander goedgekeurd product niet kan worden gebruikt. De laagste dosis, die nog voldoende verhoging van het contrast geeft voor diagnostische doeleinden, moet worden gebruikt. 53
3 Rubriek 4.4 Bijzondere waarschuwingen en voorzorgen bij gebruik Na intraveneuze toediening van <werkzame stofnaam (INN)> kan gadolinium achterblijven in de hersenen en in andere weefsels van het lichaam (botten, lever, nieren, huid), en kan een dosisafhankelijke toename in T1-gewogen signaalintensiteit geven in de hersenen, met name in de nucleus dentatus, globus pallidus en thalamus. Er zijn geen klinische gevolgen bekend. Retentie van gadolinium in de hersenen is niet gemeld bij intra-articulaire toediening van gadolinium. De mogelijke diagnostische voordelen van het gebruik van <werkzame stofnaam (INN)> bij patiënten bij wie scans moeten worden herhaald, moeten worden afgewogen tegen de kans op retentie van gadolinium in de hersenen en andere weefsels. 5.2 Farmacokinetische eigenschappen <Werkzame stofnaam (INN)> is een lineair gadolinium bevattend contrastmiddel (GdCA). Studies hebben aangetoond dat, na blootstelling aan intraveneus gegeven GdCA s bij aanzienlijk hogere doses dan bij intra-articulair gebruikte producten, gadolinium in het lichaam kan achterblijven in de hersenen en in andere weefsels en organen. Met de lineaire GdCA s kan dit een dosis-afhankelijke toename in T1-gewogen signaalintensiteit geven in de hersenen, met name in de nucleus dentatus, globus pallidus en thalamus. De toename in signaalintensiteit en niet-klinische gegevens duiden erop dat gadolinium vrijkomt uit lineaire GdCA s. Bijsluiter Rubriek 2: Wanneer mag dit middel niet worden toegediend of moet u er extra voorzichtig mee zijn? o Achterblijven van restant in het lichaam In <Productnaam> zit als werkzame stof een metaal, genaamd gadolinium. Uit studies is gebleken dat kleine hoeveelheden gadolinium in het lichaam kunnen achterblijven, waaronder in de hersenen. Dit is niet gezien wanneer er kleine hoeveelheden gadolinium met een injectie in het gewricht werden gegeven. Intraveneus gadoxetaat dinatrium <Productnaam> is geïndiceerd voor de detectie van focale leverlaesies en verschaft informatie over de aard van de laesies bij T1-gewogen magnetische resonantiebeeldvorming (MRI). magnetische resonantiebeeldvorming (MRI) en wanneer vertraagde fase beeldvorming vereist is. Dit geneesmiddel is uitsluitend voor diagnostisch gebruik met intraveneuze toediening. De laagste dosis, die nog voldoende verhoging van het contrast geeft voor diagnostische doeleinden, moet worden gebruikt. De dosis moet worden berekend op basis van het lichaamsgewicht van de 54
4 patiënt, en mag de in deze rubriek vermelde aanbevolen dosis per kilogram lichaamsgewicht niet overschrijden. Rubriek 4.4 Bijzondere waarschuwingen en voorzorgen bij gebruik Na toediening van <werkzame stofnaam (INN)> kan gadolinium achterblijven in de hersenen en in andere weefsels van het lichaam (botten, lever, nieren, huid), en kan een dosis-afhankelijke toename in T1-gewogen signaalintensiteit geven in de hersenen, met name in de nucleus dentatus, globus pallidus en thalamus. Er zijn geen klinische gevolgen bekend. De mogelijke diagnostische voordelen van het gebruik van <werkzame stofnaam (INN)> bij patiënten bij wie scans moeten worden herhaald, moeten worden afgewogen tegen de kans op retentie van gadolinium in de hersenen en andere weefsels. 5.2 Farmacokinetische eigenschappen <Werkzame stofnaam (INN)> is een lineair gadolinium bevattend contrastmiddel (GdCA). Studies hebben aangetoond dat, na blootstelling aan GdCA s, gadolinium in het lichaam kan achterblijven in de hersenen en in andere weefsels en organen. Met de lineaire GdCA s kan dit een dosis-afhankelijke toename in T1-gewogen signaalintensiteit geven in de hersenen, met name in de nucleus dentatus, globus pallidus en thalamus. De toename in signaalintensiteit en niet-klinische gegevens duiden erop dat gadolinium vrijkomt uit lineaire GdCA s. Bijsluiter Rubriek 2: Wanneer mag dit middel niet worden toegediend of moet u er extra voorzichtig mee zijn? o Achterblijven van restant in het lichaam In <Productnaam> zit als werkzame stof een metaal, genaamd gadolinium. Uit studies is gebleken dat kleine hoeveelheden gadolinium in het lichaam kunnen achterblijven, waaronder in de hersenen. Er zijn geen bijwerkingen gezien als gevolg van gadolinium dat in de hersenen is achtergebleven. Intraveneus gadobeenzuur (beperking van de indicatie alle referenties naar andere indicaties moeten uit de hele productinformatie worden verwijderd) Dit geneesmiddel is uitsluitend voor diagnostisch gebruik. <Productnaam> is een paramagnetische contrastvloeistof die wordt gebruikt voor magnetische resonantie tomografie (MRI) geïndiceerd voor: van de lever bij volwassenen en kinderen (ouder dan 2 jaar). MRI van de hersenen en het ruggenmerg in volwassenen en kinderen ouder dan 2 jaar waar het de detectie van laesies verbetert en het aanvullende diagnostische informatie kan geven op de informatie verkregen met een niet-versterkte MRI (zie sectie 5.1); MRI beeldvorming van het volledige lichaam in volwassen en kinderen (ouder dan 2 jaar) met inbegrip van hoofd en nek, de thoracale regio (met inbegrip van het hart en de vrouwelijke borsten), buik (pancreas en lever), buik (maag-darmkanaal), retroperitoneale ruimte (nier, bijnieren), bekken 55
5 (prostaat, blaas en uterus) en bewegingsapparaat waar het de identificatie van abnormale structuren of letsels vergemakkelijkt en helpt om normale van pathologische weefsels te onderscheiden (zie secties 4.2 en 5.1); Magnetische resonantie angiografie (MRA) voor de beoordeling van stenose, occlusies en collateralen bij volwassenen en kinderen (ouder dan 2 jaar); Specifieke toepassingen in het hart omvatten metingen van myocardiale perfusie onder farmacologische stresscondities en de diagnostiek van levensvatbaarheid ("vertraagde enhancement"). magnetische resonantiebeeldvorming (MRI) en wanneer vertraagde fase beeldvorming vereist is. Orgaan Hersenen en ruggenmerg Lever, nieren, urinewegen, bijnieren Magnetische resonantie angiografie Aanbevolen dosis 0,1 mmol/kg lichaamsgewicht (0,2 ml/kg van de 0,5 M oplossing) 0,05 mmol/kg lichaamsgewicht (0,1 ml/kg van de 0,5 M oplossing) 0,1 mmol/kg lichaamsgewicht (0,2 ml/kg van de 0,5 M oplossing) Hoofd en nek, thoracale regio (met inbegrip van het 0,1 mmol/kg lichaamsgewicht hart en de vrouwelijke borsten), buik (maagdarmkanaal (0,2 ml/kg van de 0,5 M oplossing) met inbegrip van de alvleesklier), bekken (prostaat, blaas en uterus) en bewegingsapparaat Hart MRI: Evaluatie van cardiale massa's of myocard levensvatbaarheid; Evaluatie van myocardiale perfusie 0,1 mmol/lichaamgewicht toegediend als één enkele bolus van 0,2 ml/kg van de 0,5 M oplossing Twee aparte injecties van 0,05 mmol/kg lichaamsgewicht (elk overeenstemmend met 0,1 ml/kg van de 0,5 M oplossing) gedurende rust en stress beeldvorming. De aanbevolen dosis <werkzame stof (INN)> bij volwassen patiënten en kinderen is 0,05 mmol/kg lichaamsgewicht (0,1 ml/kg van de 0,5 M oplossing). De laagste dosis, die nog voldoende verhoging van het contrast geeft voor diagnostische doeleinden, moet worden gebruikt. De dosis moet worden berekend op basis van het lichaamsgewicht van de patiënt, en mag de in deze rubriek vermelde aanbevolen dosis per kilogram lichaamsgewicht niet overschrijden. ( ) Post-contrast tomografische acquisitie: Lever Dynamische tomografie: Onmiddellijk na een bolus injectie. Vertraagde tomografie: Tussen de 40 en 120 minuten na de injectie, afhankelijk van de individuele tomografische behoefte. Hersenen en Tot 60 minuten na de toediening. ruggenmerg MRA Onmiddellijk na toediening, met scan vertraging die op basis van de testbolus of automatische bolus detectie techniek wordt berekend. Indien een automatische contrastdetectie puls-sequentie niet wordt gebruikt voor bolus 56
6 Borst Andere lichaamsdelen timing, dan dient een test bolus injectie < 2 ml van de oplossing gebruikt te worden om de geschikte scan vertraging te berekenen. Een T1-gewogen, gradiënt-echo sequentie met een tijdsresolutie van 2 minuten of minder moet bekomen worden voor de injectie van het contrastmiddel en meerdere malen herhaald worden gedurende een periode van 5 tot 8 minutes na een snelle intraveneuze bolusinjectie van het contrastmiddel. T1-gewogen sequenties worden verworven als ofwel dynamische of statische vertraagde weergaven. Speciale populaties Nierfunctiestoornis ( ) Indien gebruik van <Productnaam> niet kan worden vermeden, dient de dosis niet groter te zijn dan 0,1 mmol/kg lichaamsgewicht wanneer gebruikt voor MRI van de hersenen en ruggenmerg, MR angiografie, MRI van de borst of MRI van het volledige lichaam en niet groter dan 0,05 mmol/kg lichaamsgewicht wanneer gebruikt voor MRI van de lever, nieren, urinewegen of bijnieren. Niet meer dan één dosis mag worden gebruikt bij een scan tenzij voor MR cardiale perfusie beeldvorming waar twee afzonderlijke dosissen van 0,05 mmol/kg lichaamsgewicht tijdens een onderzoek kunnen worden toegediend. Wegens het ontbreken van informatie over herhaalde toedieningen dient <Productnaam> niet herhaald te worden toegediend, tenzij het interval tussen de injecties ten minste 7 dagen bedraagt. Rubriek 4.4 Bijzondere waarschuwingen en voorzorgen bij gebruik Na toediening van <werkzame stofnaam (INN)> kan gadolinium achterblijven in de hersenen en in andere weefsels van het lichaam (botten, lever, nieren, huid), en kan een dosis-afhankelijke toename in T1-gewogen signaalintensiteit gevenin de hersenen, met name in de nucleus dentatus, globus pallidus en thalamus. Er zijn geen klinische gevolgen bekend. De mogelijke diagnostische voordelen van het gebruik van <werkzame stofnaam (INN)> bij patiënten bij wie scans moeten worden herhaald, moeten worden afgewogen tegen de kans op retentie van gadolinium in de hersenen en andere weefsels. 5.2 Farmacokinetische eigenschappen <Werkzame stofnaam (INN)> is een lineair gadolinium bevattend contrastmiddel (GdCA). Studies hebben aangetoond dat, na blootstelling aan GdCA s, gadolinium in het lichaam kan achterblijven in de hersenen en in andere weefsels en organen. Met de lineaire GdCA s kan dit een dosis-afhankelijke toename in T1-gewogen signaalintensiteit gevenin de hersenen, met name in de nucleus dentatus, globus pallidus en thalamus. De toename in signaalintensiteit en niet-klinische gegevens duiden erop dat gadolinium vrijkomt uit lineaire GdCA s. Bijsluiter Rubriek 1 Wat is <Productnaam> en waarvoor wordt dit middel gebruikt? <Productnaam> is een speciale kleurstof (of contrastmiddel) die het zeldzame aardmetaal gadolinium bevat en die de afbeelding van de lever hersenen/ruggengraat, slagaders en andere lichaamsdelen verbetert wanneer een MRI-scan wordt gemaakt. Het helpt artsen om eventuele afwijkingen van uw lever hersonen/ruggengraat, slagaders of anderen delen van uw lichaam te herkennen. Dit geneesmiddel is uitsluitend voor diagnostisch gebruik. 57
7 <Productnaam> is goedgekeurd voor gebruik bij kinderen ouder dan twee jaar. Rubriek 2: Wanneer mag dit middel niet worden toegediend of moet u er extra voorzichtig mee zijn? o Achterblijven van restant in het lichaam In <Productnaam> zit als werkzame stof een metaal, genaamd gadolinium. Uit studies is gebleken dat kleine hoeveelheden gadolinium in het lichaam kunnen achterblijven, waaronder in de hersenen. Er zijn geen bijwerkingen gezien als gevolg van gadolinium dat in de hersenen is achtergebleven. Rubriek 3 Hoe wordt dit middel gebruikt? Voordat een MRI-scan wordt gemaakt, wordt <Productnaam> in een ader ingespoten, meestal in een ader van uw arm. De hoeveelheid (in milliliter) die wordt ingespoten, hangt af van het aantal kilo s dat u weegt. De aanbevolen dosis is: MRI scan van de hersenen/ruggengraat: 0,2 ml per kilogram lichaamgewicht. MRI scan van de slagaders: 0,2 ml per kilogram lichaamgewicht. MRI van de lever, nieren, urinewegen of bijnieren: 0,1 ml per kilogram lichaamgewicht. MRI van de borst, hart of andere lichaamsdelen: 0,2 ml per kilogram lichaamgewicht. In de informatie bestemd voor artsen en andere beroepsbeoefenaren in de gezondheidszorg: Post-contrast tomografische acquisitie: Lever Dynamische tomografie: Vertraagde tomografie: Onmiddellijk na een bolus injectie. Tussen de 40 en 120 minuten na de injectie, afhankelijk van de individuele tomografische behoefte. Hersenen en Tot 60 minuten na toediening. ruggenmerg MRA Borst Andere lichaamsdel en Onmiddellijk na toediening, met scan vertraging die op basis van de testbolus of automatische bolus detectie techniek wordt berekend. Indien een automatische contrastdetectie puls-sequentie niet wordt gebruikt voor bolus timing, dan dient een test bolus injectie <2 ml van de oplossing gebruikt te worden om de geschikte scan vertraging te berekenen. Een T1-gewogen, gradiënt-echo sequentie met een tijdsresolutie van 2 minuten of minder moet bekomen worden voor de injectie van het contrastmiddel en meerdere malen herhaald worden gedurende een periode van 5 tot 8 minutes na een snelle intraveneuze bolusinjectie van het contrastmiddel. T1-gewogen sequenties worden verworven als ofwel dynamische of statische vertraagde weergaven. Het wordt aanbevolen om vóór toediening van <Productnaam> alle patiënten te screenen op een nierfunctiestoornis door het uitvoeren van laboratoriumtesten. 58
8 Er zijn gevallen gemeld van Nefrogene Systemische Fibrose (NSF) die in verband zijn gebracht met het gebruik van sommige gadoliniumhoudende contrastmiddelen bij patiënten met een ernstige acute of chronische nierfunctiestoornis (GFR < 30 ml/min/1,73 m²). Patiënten die een levertransplantatie ondergaan, lopen een bijzonder risico aangezien de incidentie van acuut nierfalen verhoogd is bij deze patiënten. Aangezien er een mogelijkheid is dat NSF optreedt bij gebruik van <Productnaam>, dient het te worden vermeden bij patiënten met een ernstige nierfunctiestoornis en bij patiënten tijdens de perioperatieve levertransplantatieperiode tenzij de diagnostische informatie essentieel is en niet kan worden verkregen met niet-contrastversterkte MRI. Indien gebruik van <Productnaam> niet kan worden vermeden, dient de dosis niet groter te zijn dan 0,1 mmol/kg lichaamsgewicht wanneer gebruikt voor een MRI van de hersenen en ruggenmerg, MR angiografie, MRI van de borst of MRI van het volledige lichaam en niet groter dan 0,05 mmol/kg lichaamsgewicht wanneer gebruikt voor een MRI van de lever, nieren, urinewegen of bijnieren. Niet meer dan één dosis mag worden gebruikt bij een scan tenzij voor MR cardiale perfusie beeldvorming waar twee afzonderlijke dosissen van 0,05 mmol/kg lichaamsgewicht tijdens een onderzoek kunnen worden toegediend. Wegens het ontbreken van informatie over herhaalde toedieningen dient <Productnaam> niet herhaald te worden toegediend tenzij het interval tussen de injecties ten minste 7 dagen bedraagt. 59
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER MultiHance, oplossing voor injectie 529 mg/ml, 5 ml, 10 ml, 15 ml, 20 ml Gadobenaat-dimeglumine Lees de hele bijsluiter zorgvuldig door voordat u dit geneesmiddel
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER MultiHance, oplossing voor injectie 529 mg/ml, 5 ml, 10 ml, 15 ml, 20 ml Gadobenaat-dimeglumine Lees de hele bijsluiter zorgvuldig door voordat u dit geneesmiddel
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER MultiHance, oplossing voor injectie 529 mg/ml, 5 ml, 10 ml, 15 ml, 20 ml Gadobenaat-dimeglumine Lees de hele bijsluiter zorgvuldig door voordat u met het gebruik
BIJSLUITER: INFORMATIE VOOR DE GEBRUIK(ST)ER MultiHance, oplossing voor injectie 529 mg/ml, 5 ml, 10 ml, 15 ml, 20 ml Gadobenaat-dimeglumine Lees de hele bijsluiter zorgvuldig door voordat u met het gebruik
BIJSLUITER: INFORMATIE VOOR GEBRUIKER. MultiHance, 0,5 M oplossing voor injectie Gadobenaat-dimeglumine
 BIJSLUITER: INFORMATIE VOOR GEBRUIKER MultiHance, 0,5 M oplossing voor injectie Gadobenaat-dimeglumine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
BIJSLUITER: INFORMATIE VOOR GEBRUIKER MultiHance, 0,5 M oplossing voor injectie Gadobenaat-dimeglumine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER MultiHance, oplossing voor injectie 529 mg/ml, 5 ml, 10 ml, 15 ml, 20 ml Gadobenaat-dimeglumine Lees de hele bijsluiter zorgvuldig door voordat u dit geneesmiddel
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER MultiHance, oplossing voor injectie 529 mg/ml, 5 ml, 10 ml, 15 ml, 20 ml Gadobenaat-dimeglumine Lees de hele bijsluiter zorgvuldig door voordat u dit geneesmiddel
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. MultiHance 529 mg/ml oplossing voor injectie in een voorgevulde spuit Gadobenaatdimeglumine
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER MultiHance 529 mg/ml oplossing voor injectie in een voorgevulde spuit Gadobenaatdimeglumine Lees de hele bijsluiter zorgvuldig door voordat u dit geneesmiddal gaat
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER MultiHance 529 mg/ml oplossing voor injectie in een voorgevulde spuit Gadobenaatdimeglumine Lees de hele bijsluiter zorgvuldig door voordat u dit geneesmiddal gaat
Dotarem 0,5 mmol/ml Oplossing voor injectie in flacons. Gadoteerzuur
 BIJSLUITER: INFORMATIE VOOR DE PATIËNT Dotarem 0,5 mmol/ml Oplossing voor injectie in flacons Gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
BIJSLUITER: INFORMATIE VOOR DE PATIËNT Dotarem 0,5 mmol/ml Oplossing voor injectie in flacons Gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
Dotarem 0,5 mmol/ml Oplossing voor injectie in flacons. Gadoteerzuur
 BIJSLUITER: INFORMATIE VOOR DE PATIËNT Dotarem 0,5 mmol/ml Oplossing voor injectie in flacons Gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
BIJSLUITER: INFORMATIE VOOR DE PATIËNT Dotarem 0,5 mmol/ml Oplossing voor injectie in flacons Gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
SAMENVATTING VAN DE PRODUCTKENMERKEN
 1 SAMENVATTING VAN DE PRODUCTKENMERKEN MULTIHANCE SAMENVATTING VAN DE PRODUCTKENMERKEN 1 NAAM VAN HET GENEESMIDDEL MultiHance 529 mg/ml oplossing voor injectie in een voorgevulde spuit 2 KWALITATIEVE EN
1 SAMENVATTING VAN DE PRODUCTKENMERKEN MULTIHANCE SAMENVATTING VAN DE PRODUCTKENMERKEN 1 NAAM VAN HET GENEESMIDDEL MultiHance 529 mg/ml oplossing voor injectie in een voorgevulde spuit 2 KWALITATIEVE EN
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Gadoteerzuur Guerbet 0,5 mmol/ml. Oplossing voor injectie in voorgevulde spuit Gadoteerzuur
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Oplossing voor injectie in voorgevulde spuit Gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Oplossing voor injectie in voorgevulde spuit Gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER
 BIJSLUITER 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER MultiHance 529 mg/ml oplossing voor injectie in een voorgevulde spuit Gadobenaatdimeglumine Lees goed de hele bijsluiter voordat u dit geneesmiddel
BIJSLUITER 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER MultiHance 529 mg/ml oplossing voor injectie in een voorgevulde spuit Gadobenaatdimeglumine Lees goed de hele bijsluiter voordat u dit geneesmiddel
BIJSLUITER: INFORMATIE VOOR DE PATIËNT
 BIJSLUITER: INFORMATIE VOOR DE PATIËNT, gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt want er staat belangrijke informatie voor u in. Bewaar deze bijsluiter. Misschien heeft
BIJSLUITER: INFORMATIE VOOR DE PATIËNT, gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt want er staat belangrijke informatie voor u in. Bewaar deze bijsluiter. Misschien heeft
Gadoteerzuur Guerbet 0,5 mmol/ml (voor meervoudig gebruik)
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Gadoteerzuur Guerbet 0,5 mmol/ml Oplossing voor injectie in injectieflacons (voor meervoudig gebruik) Gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Gadoteerzuur Guerbet 0,5 mmol/ml Oplossing voor injectie in injectieflacons (voor meervoudig gebruik) Gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel
1. WAT IS DOTAREM EN WAARVOOR WORDT HET GEBRUIKT
 BIJSLUITER Lees de hele bijsluiter aandachtig door alvorens dit geneesmiddel te gebruiken. Bewaar deze bijsluiter. Misschien heeft u hem nog een keer nodig. Raadpleeg uw arts of apotheker als u aanvullende
BIJSLUITER Lees de hele bijsluiter aandachtig door alvorens dit geneesmiddel te gebruiken. Bewaar deze bijsluiter. Misschien heeft u hem nog een keer nodig. Raadpleeg uw arts of apotheker als u aanvullende
MULTIHANCE SAMENVATTING VAN DE PRODUCTKENMERKEN. MultiHance, oplossing voor injectie 529 mg/ml, 5 ml, 10 ml, 15 ml, 20 ml.
 MULTIHANCE SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL MultiHance, oplossing voor injectie 529 mg/ml, 5 ml, 10 ml, 15 ml, 20 ml. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke
MULTIHANCE SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL MultiHance, oplossing voor injectie 529 mg/ml, 5 ml, 10 ml, 15 ml, 20 ml. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKERS. ProHance 279,3 mg/ml, oplossing voor injectie. Gadoteridol
 Pagina 1 van 8 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKERS ProHance 279,3 mg/ml, oplossing voor injectie Gadoteridol Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
Pagina 1 van 8 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKERS ProHance 279,3 mg/ml, oplossing voor injectie Gadoteridol Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
Bijsluiter: informatie voor de patiënt. Gadovist 1,0 mmol/ml, oplossing voor injectie. Gadobutrol
 Gadovist vial bijsluiter Pagina 1 van 10 Bijsluiter: informatie voor de patiënt Gadovist 1,0 mmol/ml, oplossing voor injectie Gadobutrol Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
Gadovist vial bijsluiter Pagina 1 van 10 Bijsluiter: informatie voor de patiënt Gadovist 1,0 mmol/ml, oplossing voor injectie Gadobutrol Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
Bijsluiter: informatie voor de patiënt. Dotagraf 0,5 mmol/ml, oplossing voor injectie. gadoteerzuur
 Dotagraf 10/15/20 ml bijsluiter Pagina 1 van 8 Bijsluiter: informatie voor de patiënt Dotagraf 0,5 mmol/ml, oplossing voor injectie gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel
Dotagraf 10/15/20 ml bijsluiter Pagina 1 van 8 Bijsluiter: informatie voor de patiënt Dotagraf 0,5 mmol/ml, oplossing voor injectie gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel
Bijsluiter: informatie voor de gebruiker. Dotarem 0,5 mmol/ml, oplossing voor injectie. Gadoteerzuur
 Bijsluiter: informatie voor de gebruiker Dotarem 0,5 mmol/ml, oplossing voor injectie Gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
Bijsluiter: informatie voor de gebruiker Dotarem 0,5 mmol/ml, oplossing voor injectie Gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
BIJSLUITER: INFORMATIE VOOR GEBRUIKERS. ProHance, oplossing voor injectie 279,3 mg/ml = 0.5 molair Gadoteridol
 BIJSLUITER: INFORMATIE VOOR GEBRUIKERS ProHance, oplossing voor injectie 279,3 mg/ml = 0.5 molair Gadoteridol Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
BIJSLUITER: INFORMATIE VOOR GEBRUIKERS ProHance, oplossing voor injectie 279,3 mg/ml = 0.5 molair Gadoteridol Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
Bijsluiter: informatie voor de gebruiker. Primovist PFS 0,25 mmol/ml, oplossing voor injectie, voorgevulde spuit. dinatriumgadoxetaat
 1 van 9 Informatie voor de gebruiker Bijsluiter: informatie voor de gebruiker Primovist PFS 0,25 mmol/ml, oplossing voor injectie, voorgevulde spuit dinatriumgadoxetaat Lees goed de hele bijsluiter voordat
1 van 9 Informatie voor de gebruiker Bijsluiter: informatie voor de gebruiker Primovist PFS 0,25 mmol/ml, oplossing voor injectie, voorgevulde spuit dinatriumgadoxetaat Lees goed de hele bijsluiter voordat
Bijsluiter: informatie voor de patiënt. Gadovist 1,0 mmol/ml oplossing voor injectie in voorgevulde spuit/patroon. Gadobutrol
 Gadovist PFS/PFC bijsluiter Pagina 1 van 12 Bijsluiter: informatie voor de patiënt Gadovist 1,0 mmol/ml oplossing voor injectie in voorgevulde spuit/patroon Gadobutrol Lees goed de hele bijsluiter voordat
Gadovist PFS/PFC bijsluiter Pagina 1 van 12 Bijsluiter: informatie voor de patiënt Gadovist 1,0 mmol/ml oplossing voor injectie in voorgevulde spuit/patroon Gadobutrol Lees goed de hele bijsluiter voordat
PRAC-aanbevelingen met betrekking tot signalen voor bijwerking van de productinformatie
 22 januari 2015 EMA/PRAC/63314/2015 Risicobeoordelingscomité geneesmiddelenbewaking (PRAC) PRAC-aanbevelingen met betrekking tot signalen voor bijwerking van de productinformatie Goedgekeurd door het PRAC
22 januari 2015 EMA/PRAC/63314/2015 Risicobeoordelingscomité geneesmiddelenbewaking (PRAC) PRAC-aanbevelingen met betrekking tot signalen voor bijwerking van de productinformatie Goedgekeurd door het PRAC
Bijlage III. Wijzigingen in de relevante rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiter
 Bijlage III Wijzigingen in de relevante rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiter Opmerking: De relevante rubrieken van de Samenvatting van de productkenmerken en de bijsluiter
Bijlage III Wijzigingen in de relevante rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiter Opmerking: De relevante rubrieken van de Samenvatting van de productkenmerken en de bijsluiter
SAMENVATTING VAN DE PRODUCTKENMERKEN
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1 NAAM VAN HET GENEESMIDDEL Prohance, oplossing voor injectie 279,3 mg/ml = 0,5 molair 2 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Het werkzame bestanddeel van is
SAMENVATTING VAN DE PRODUCTKENMERKEN 1 NAAM VAN HET GENEESMIDDEL Prohance, oplossing voor injectie 279,3 mg/ml = 0,5 molair 2 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Het werkzame bestanddeel van is
Bijlage III. Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiter
 Bijlage III Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiter NB: Deze Samenvatting van de productkenmerken, Etikettering
Bijlage III Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiter NB: Deze Samenvatting van de productkenmerken, Etikettering
MULTIHANCE SAMENVATTING VAN DE PRODUCTKENMERKEN
 MULTIHANCE SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL MultiHance, 0.5 M oplossing voor injectie. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml oplossing voor injectie bevat:
MULTIHANCE SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL MultiHance, 0.5 M oplossing voor injectie. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml oplossing voor injectie bevat:
SAMENVATTING VAN DE PRODUCTKENMERKEN
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1 MULTIHANCE SAMENVATTING VAN DE PRODUCTKENMERKEN 1 NAAM VAN HET GENEESMIDDEL MultiHance 529 mg/ml oplossing voor injectie in een voorgevulde spuit 2 KWALITATIEVE EN
SAMENVATTING VAN DE PRODUCTKENMERKEN 1 MULTIHANCE SAMENVATTING VAN DE PRODUCTKENMERKEN 1 NAAM VAN HET GENEESMIDDEL MultiHance 529 mg/ml oplossing voor injectie in een voorgevulde spuit 2 KWALITATIEVE EN
MULTIHANCE SAMENVATTING VAN DE PRODUCTKENMERKEN. MultiHance, oplossing voor injectie 529 mg/ml, 5 ml, 10 ml, 15 ml, 20 ml.
 MULTIHANCE SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL MultiHance, oplossing voor injectie 529 mg/ml, 5 ml, 10 ml, 15 ml, 20 ml. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke
MULTIHANCE SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL MultiHance, oplossing voor injectie 529 mg/ml, 5 ml, 10 ml, 15 ml, 20 ml. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke
Bijlage III. Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiters
 Bijlage III Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiters NB: Deze Samenvatting van de productkenmerken, Etikettering
Bijlage III Wijzigingen die moeten worden aangebracht in de desbetreffende rubrieken van de Samenvatting van de Productkenmerken en de Bijsluiters NB: Deze Samenvatting van de productkenmerken, Etikettering
(1) Risico op acute pancreatitis Er zijn meldingen geweest van acute pancreatitis na de behandeling met carbimazol/thiamazol.
 GEADRESSEERDE ADRES POSTCODE WOONPLAATS 31 januari 2019 Belangrijke risico-informatie: Geneesmiddelen die carbimazol of thiamazol (synoniem: methimazol) bevatten: (1) risico op acute pancreatitis en (2)
GEADRESSEERDE ADRES POSTCODE WOONPLAATS 31 januari 2019 Belangrijke risico-informatie: Geneesmiddelen die carbimazol of thiamazol (synoniem: methimazol) bevatten: (1) risico op acute pancreatitis en (2)
Voor langdurige behandeling: bewijs van cardiale valvulopathie als vastgesteld door middel van echocardiografie voorafgaand aan de behandeling.
 RUBRIEKEN VAN DE SAMENVATTING VAN DE PRODUCTKENMERKEN VOOR CABERGOLINE BEVATTENDE PRODUCTEN 4.2 Dosering en wijze van toediening Beperking van de maximumdosis tot 3 mg/dag 4.3 Contra-indicaties Voor langdurige
RUBRIEKEN VAN DE SAMENVATTING VAN DE PRODUCTKENMERKEN VOOR CABERGOLINE BEVATTENDE PRODUCTEN 4.2 Dosering en wijze van toediening Beperking van de maximumdosis tot 3 mg/dag 4.3 Contra-indicaties Voor langdurige
Hulpstoffen met bekend effect: Dit geneesmiddel bevat minder dan 1 mmol natrium (23 mg) per dosis.
 Page 1 of 10 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL PROHANCE, 279,3 mg/ml, oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Gadoteridol 279,3 mg/ml (0,5
Page 1 of 10 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL PROHANCE, 279,3 mg/ml, oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Gadoteridol 279,3 mg/ml (0,5
Bijlage III. Wijzigingen in relevante rubrieken van de productinformatie
 Bijlage III Wijzigingen in relevante rubrieken van de productinformatie Opmerking: Deze wijzigingen in de relevante rubrieken van de samenvatting van de productkenmerken en de bijsluiter zijn het resultaat
Bijlage III Wijzigingen in relevante rubrieken van de productinformatie Opmerking: Deze wijzigingen in de relevante rubrieken van de samenvatting van de productkenmerken en de bijsluiter zijn het resultaat
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Dotarem 0,5 mmol/ml, oplossing voor injectie. Gadoteerzuur
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Dotarem 0,5 mmol/ml, oplossing voor injectie Gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Dotarem 0,5 mmol/ml, oplossing voor injectie Gadoteerzuur Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
Niet invasieve angiografie. Dr.H.Mertens
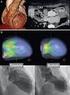 Niet invasieve angiografie. Dr.H.Mertens Morita S et al. Radiographics 2010;30:111-125 Man, 79j, linkszijdige hemiplegie en dysartrie. Man, 60j, malaise, intermittente diarree en rilkoorts. Wat is niet
Niet invasieve angiografie. Dr.H.Mertens Morita S et al. Radiographics 2010;30:111-125 Man, 79j, linkszijdige hemiplegie en dysartrie. Man, 60j, malaise, intermittente diarree en rilkoorts. Wat is niet
SAMENVATTING VAN DE PRODUCTKENMERKEN. Inspuitbaar Omniscan is een paramagnetisch, niet-ionisch contrastmiddel met de volgende fysischchemische
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1/9 1. NAAM VAN HET GENEESMIDDEL Omniscan 0,5 mmol/ml (equiv. 287 mg/ml) oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Gadodiamidum 287 mg
SAMENVATTING VAN DE PRODUCTKENMERKEN 1/9 1. NAAM VAN HET GENEESMIDDEL Omniscan 0,5 mmol/ml (equiv. 287 mg/ml) oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Gadodiamidum 287 mg
Bijlage III. NB: Deze Samenvatting van de productkenmerken, etikettering en bijsluiter zijn het resultaat van de referral procedure.
 Bijlage III Wijzigingen in relevante rubrieken van de Samenvatting van de productkenmerken en de Bijsluiter NB: Deze Samenvatting van de productkenmerken, etikettering en bijsluiter zijn het resultaat
Bijlage III Wijzigingen in relevante rubrieken van de Samenvatting van de productkenmerken en de Bijsluiter NB: Deze Samenvatting van de productkenmerken, etikettering en bijsluiter zijn het resultaat
De werkzame stof is gadoteerzuur. Het is aanwezig in de vorm van megluminegadoteraat (0,5 mmol megluminegadoteraat/ml).
 1. NAAM VAN HET GENEESMIDDEL Dotarem 0,5 mmol/ml, oplossing voor injectie. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING De werkzame stof is gadoteerzuur. Het is aanwezig in de vorm van megluminegadoteraat
1. NAAM VAN HET GENEESMIDDEL Dotarem 0,5 mmol/ml, oplossing voor injectie. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING De werkzame stof is gadoteerzuur. Het is aanwezig in de vorm van megluminegadoteraat
SAMENVATTING VAN DE PRODUCTKENMERKEN
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1 MULTIHANCE SAMENVATTING VAN DE PRODUCTKENMERKEN 1 NAAM VAN HET GENEESMIDDEL MultiHance 529 mg/ml oplossing voor injectie in een voorgevulde spuit 2 KWALITATIEVE EN
SAMENVATTING VAN DE PRODUCTKENMERKEN 1 MULTIHANCE SAMENVATTING VAN DE PRODUCTKENMERKEN 1 NAAM VAN HET GENEESMIDDEL MultiHance 529 mg/ml oplossing voor injectie in een voorgevulde spuit 2 KWALITATIEVE EN
BIJSLUITER: INFORMATIE VOOR DE PATIËNT. FLUORESCEINE 10% Faure oplossing voor injectie natriumfluoresceïne
 BIJSLUITER: INFORMATIE VOOR DE PATIËNT FLUORESCEINE 10% Faure oplossing voor injectie natriumfluoresceïne Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat belangrijke
BIJSLUITER: INFORMATIE VOOR DE PATIËNT FLUORESCEINE 10% Faure oplossing voor injectie natriumfluoresceïne Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat belangrijke
10 ml oplossing voor injectie bevat 2793,2 mg gadoteerzuur (als megluminezout), overeenkomend met
 Dotagraf 10/15/20 ml SmPC Pagina 1 van 9 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Dotagraf 0,5 mmol/ml, oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1
Dotagraf 10/15/20 ml SmPC Pagina 1 van 9 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Dotagraf 0,5 mmol/ml, oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1
Iedere ml bevat 0,25 mmol dinatriumgadoxetaat (dinatrium-gd-eob-dtpa), overeenkomend met 181,43 mg dinatriumgadoxetaat.
 Primovist PFS SmPC 1 van 11 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Primovist PFS 0,25 mmol/ml, oplossing voor injectie, voorgevulde spuit 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Primovist PFS SmPC 1 van 11 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Primovist PFS 0,25 mmol/ml, oplossing voor injectie, voorgevulde spuit 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
BIJSLUITER: INFORMATIE VOOR DE PATIËNT. Gadovist 1,0 mmol/ml oplossing voor injectie in voorgevulde spuit / patroon. Gadobutrol
 BIJSLUITER: INFORMATIE VOOR DE PATIËNT Gadovist 1,0 mmol/ml oplossing voor injectie in voorgevulde spuit / patroon Gadobutrol Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want
BIJSLUITER: INFORMATIE VOOR DE PATIËNT Gadovist 1,0 mmol/ml oplossing voor injectie in voorgevulde spuit / patroon Gadobutrol Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want
SAMENVATTING VAN DE PRODUCTKENMERKEN. Gadoteerzuur Guerbet 0,5 mmol/ml, oplossing voor injectie in voorgevulde spuit.
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL, oplossing voor injectie in voorgevulde spuit. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml oplossing voor injectie bevat 279,32
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL, oplossing voor injectie in voorgevulde spuit. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml oplossing voor injectie bevat 279,32
SAMENVATTING VAN DE PRODUCTKENMERKEN. DOTAREM 0,5 mmol/ml oplossing voor injectie in injectieflacons.
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL DOTAREM 0,5 mmol/ml. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml oplossing voor injectie bevat 279,32 mg gadoteerzuur (als megluminezout),
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL DOTAREM 0,5 mmol/ml. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml oplossing voor injectie bevat 279,32 mg gadoteerzuur (als megluminezout),
ANNEX III WIJZIGINGEN IN DE SAMENVATTINGEN VAN DE PRODUCTKENMERKEN EN DE BIJSLUITER
 ANNEX III WIJZIGINGEN IN DE SAMENVATTINGEN VAN DE PRODUCTKENMERKEN EN DE BIJSLUITER Deze aanpassingen aan de SPC en bijsluiter zijn valide op het moment van de beschikking van de commissie. Na de beschikking
ANNEX III WIJZIGINGEN IN DE SAMENVATTINGEN VAN DE PRODUCTKENMERKEN EN DE BIJSLUITER Deze aanpassingen aan de SPC en bijsluiter zijn valide op het moment van de beschikking van de commissie. Na de beschikking
SAMENVATTING VAN DE PRODUCTKENMERKEN. DOTAREM 0,5 mmol/ml oplossing voor injectie in injectieflacons.
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL DOTAREM 0,5 mmol/ml. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml oplossing voor injectie bevat 279,32 mg gadoteerzuur (als megluminezout),
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL DOTAREM 0,5 mmol/ml. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml oplossing voor injectie bevat 279,32 mg gadoteerzuur (als megluminezout),
10 ml oplossing voor injectie bevat 2793,2 mg gadoteerzuur (als megluminezout), overeenkomend met
 Dotagraf 10/15/20 ml SmPC Pagina 1 van 10 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Dotagraf 0,5 mmol/ml, oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Dotagraf 10/15/20 ml SmPC Pagina 1 van 10 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Dotagraf 0,5 mmol/ml, oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
METASTRON 37 MBq/ml oplossing voor injectie Strontium [ 89 Sr] chloride
![METASTRON 37 MBq/ml oplossing voor injectie Strontium [ 89 Sr] chloride METASTRON 37 MBq/ml oplossing voor injectie Strontium [ 89 Sr] chloride](/thumbs/39/18285193.jpg) BIJSLUITER: INFORMATIE VOOR DE PATIËNT METASTRON 37 MBq/ml oplossing voor injectie Strontium [ 89 Sr] chloride Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke
BIJSLUITER: INFORMATIE VOOR DE PATIËNT METASTRON 37 MBq/ml oplossing voor injectie Strontium [ 89 Sr] chloride Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke
Thiamini hydrochloridum 100 mg/ml, oplossing voor injectie thiaminehydrochloride
 1.3.1 : Bijsluiter Bladzijde : 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Thiamini hydrochloridum 100 mg/ml, thiaminehydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
1.3.1 : Bijsluiter Bladzijde : 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Thiamini hydrochloridum 100 mg/ml, thiaminehydrochloride Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken
SAMENVATTING VAN DE PRODUCTKENMERKEN. Gadoteerzuur Guerbet 0,5 mmol/ml, oplossing voor injectie in injectieflacons (voor meervoudig gebruik).
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Gadoteerzuur Guerbet 0,5 mmol/ml, (voor meervoudig gebruik). 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml oplossing voor injectie
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Gadoteerzuur Guerbet 0,5 mmol/ml, (voor meervoudig gebruik). 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml oplossing voor injectie
SAMENVATTING VAN DE PRODUCTKENMERKEN
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Indigokarmijn Serb 40 mg/5 ml, oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Indigotine (indigokarmijn)...40 mg
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Indigokarmijn Serb 40 mg/5 ml, oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Indigotine (indigokarmijn)...40 mg
BIJSLUITER Atosiban Devrimed 6,75 mg/0,9 ml
 BIJSLUITER Atosiban Devrimed 6,75 mg/0,9 ml 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Atosiban Devrimed 6,75 mg/0,9 ml oplossing voor injectie Atosiban Lees goed de hele bijsluiter voordat u dit geneesmiddel
BIJSLUITER Atosiban Devrimed 6,75 mg/0,9 ml 1 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Atosiban Devrimed 6,75 mg/0,9 ml oplossing voor injectie Atosiban Lees goed de hele bijsluiter voordat u dit geneesmiddel
Bijsluiter: informatie voor de patiënt. Dotagraf 0,5 mmol/ml (voor meervoudig gebruik) oplossing voor injectie. gadoteerzuur
 Dotagraf 60/100 ml bijsluiter Pagina 1 van 9 Bijsluiter: informatie voor de patiënt Dotagraf 0,5 mmol/ml (voor meervoudig gebruik) oplossing voor injectie gadoteerzuur Lees goed de hele bijsluiter voordat
Dotagraf 60/100 ml bijsluiter Pagina 1 van 9 Bijsluiter: informatie voor de patiënt Dotagraf 0,5 mmol/ml (voor meervoudig gebruik) oplossing voor injectie gadoteerzuur Lees goed de hele bijsluiter voordat
METASTRON 37 MBq/ml oplossing voor injectie Strontium [ 89 Sr] chloride
![METASTRON 37 MBq/ml oplossing voor injectie Strontium [ 89 Sr] chloride METASTRON 37 MBq/ml oplossing voor injectie Strontium [ 89 Sr] chloride](/thumbs/88/115148610.jpg) BIJSLUITER: INFORMATIE VOOR DE PATIËNT METASTRON 37 MBq/ml oplossing voor injectie Strontium [ 89 Sr] chloride Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke
BIJSLUITER: INFORMATIE VOOR DE PATIËNT METASTRON 37 MBq/ml oplossing voor injectie Strontium [ 89 Sr] chloride Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke
Bijlage III. Wijzigingen die zijn aangebracht aan relevante delen van de samenvatting van de productkenmerken en de bijsluiter
 Bijlage III Wijzigingen die zijn aangebracht aan relevante delen van de samenvatting van de productkenmerken en de bijsluiter Opmerking: Deze wijzigingen aan de relevante delen van de Samenvatting van
Bijlage III Wijzigingen die zijn aangebracht aan relevante delen van de samenvatting van de productkenmerken en de bijsluiter Opmerking: Deze wijzigingen aan de relevante delen van de Samenvatting van
SAMENVATTING VAN DE PRODUCTKENMERKEN. DOTAREM 0,5 mmol/ml (voor meervoudig gebruik) oplossing voor injectie in injectieflacons.
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1.NAAM VAN HET GENEESMIDDEL DOTAREM 0,5 mmol/ml (voor meervoudig gebruik) oplossing voor injectie in injectieflacons. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
SAMENVATTING VAN DE PRODUCTKENMERKEN 1.NAAM VAN HET GENEESMIDDEL DOTAREM 0,5 mmol/ml (voor meervoudig gebruik) oplossing voor injectie in injectieflacons. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. tranexaminezuur
 Sandoz B.V. Page 1/5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Tranexaminezuur Sandoz 100 mg/ml, oplossing voor tranexaminezuur Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want
Sandoz B.V. Page 1/5 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Tranexaminezuur Sandoz 100 mg/ml, oplossing voor tranexaminezuur Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want
Bijlage II. Wetenschappelijke conclusies
 Bijlage II Wetenschappelijke conclusies 30 Wetenschappelijke conclusies In overeenstemming met artikel 107k van Richtlijn 2001/83/EG bestudeerde het CHMP de aanbeveling van het PRAC die op 6 juli 2017
Bijlage II Wetenschappelijke conclusies 30 Wetenschappelijke conclusies In overeenstemming met artikel 107k van Richtlijn 2001/83/EG bestudeerde het CHMP de aanbeveling van het PRAC die op 6 juli 2017
Bijsluiter: informatie voor de patiënt. Edicis 2 mg kit voor radiofarmaceutisch preparaat Ethyleendicysteïne
 Bijsluiter: informatie voor de patiënt Edicis 2 mg kit voor radiofarmaceutisch preparaat Ethyleendicysteïne Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
Bijsluiter: informatie voor de patiënt Edicis 2 mg kit voor radiofarmaceutisch preparaat Ethyleendicysteïne Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
BIJLAGE III AMENDEMENTEN VAN RELEVANTE RUBRIEKEN VAN DE SAMENVATTING VAN DE PRODUCTKENMERKEN EN BIJSLUITERS
 BIJLAGE III AMENDEMENTEN VAN RELEVANTE RUBRIEKEN VAN DE SAMENVATTING VAN DE PRODUCTKENMERKEN EN BIJSLUITERS NB: De amendementen van de samenvatting van de productkenmerken en bijsluiters moeten hierna
BIJLAGE III AMENDEMENTEN VAN RELEVANTE RUBRIEKEN VAN DE SAMENVATTING VAN DE PRODUCTKENMERKEN EN BIJSLUITERS NB: De amendementen van de samenvatting van de productkenmerken en bijsluiters moeten hierna
Bijlage III. Amendementen in relevante rubrieken van de Samenvatting van de Productkenmerken
 Bijlage III Amendementen in relevante rubrieken van de Samenvatting van de Productkenmerken Opmerking: Deze amendementen in de relevante rubrieken van de Samenvatting van de Productkenmerken zijn het resultaat
Bijlage III Amendementen in relevante rubrieken van de Samenvatting van de Productkenmerken Opmerking: Deze amendementen in de relevante rubrieken van de Samenvatting van de Productkenmerken zijn het resultaat
SAMENVATTING VAN DE PRODUCTKENMERKEN. DOTAREM 0,5 mmol/ml oplossing voor injectie in voorgevulde spuit. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL DOTAREM 0,5 mmol/ml. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml oplossing voor injectie bevat 279,32 mg gadoteerzuur (als megluminezout),
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL DOTAREM 0,5 mmol/ml. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml oplossing voor injectie bevat 279,32 mg gadoteerzuur (als megluminezout),
Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke informatie in voor u.
 BIJSLUITER: INFORMATIE VOOR DE PATIËNT NANOCOLL 0,5 mg kit voor radiofarmaceutisch preparaat Humaan albumine nanocolloïd deeltjes Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend
BIJSLUITER: INFORMATIE VOOR DE PATIËNT NANOCOLL 0,5 mg kit voor radiofarmaceutisch preparaat Humaan albumine nanocolloïd deeltjes Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend
Annex I Wetenschappelijke conclusies en redenen voor wijziging van de voorwaarden verbonden aan de vergunningen voor het in de handel brengen
 Annex I Wetenschappelijke conclusies en redenen voor wijziging van de voorwaarden verbonden aan de vergunningen voor het in de handel brengen Wetenschappelijke conclusies Rekening houdend met het beoordelingsrapport
Annex I Wetenschappelijke conclusies en redenen voor wijziging van de voorwaarden verbonden aan de vergunningen voor het in de handel brengen Wetenschappelijke conclusies Rekening houdend met het beoordelingsrapport
HALDOL tabletten en drank
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
In overeenstemming met de MINISTER VAN VOLKSGEZONDHEID, WELZIJN EN SPORT,
 BD/2009/REG NL 3718/zaak 132285 In overeenstemming met de MINISTER VAN VOLKSGEZONDHEID, WELZIJN EN SPORT, Gezien het verzoek van Alfasan Nederland B.V. te WOERDEN d.d. 9 december 2009 tot wijziging van
BD/2009/REG NL 3718/zaak 132285 In overeenstemming met de MINISTER VAN VOLKSGEZONDHEID, WELZIJN EN SPORT, Gezien het verzoek van Alfasan Nederland B.V. te WOERDEN d.d. 9 december 2009 tot wijziging van
BIJSLUITER. MELOXIDYL 0,5 mg/ml suspensie voor oraal gebruik voor katten
 BIJSLUITER MELOXIDYL 0,5 mg/ml suspensie voor oraal gebruik voor katten 1. NAAM EN HET ADRES VAN DE HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EN VAN DE FABRIKANT VERANTWOORDELIJK VOOR DE VRIJGIFTE,
BIJSLUITER MELOXIDYL 0,5 mg/ml suspensie voor oraal gebruik voor katten 1. NAAM EN HET ADRES VAN DE HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EN VAN DE FABRIKANT VERANTWOORDELIJK VOOR DE VRIJGIFTE,
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1/5 1. NAAM VAN HET DIERGENEESMIDDEL 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Werkzame bestanddelen: Per 500 ml: 95,0 g calciumgluconaat 22,5 g calciumgluceptaat
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1/5 1. NAAM VAN HET DIERGENEESMIDDEL 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Werkzame bestanddelen: Per 500 ml: 95,0 g calciumgluconaat 22,5 g calciumgluceptaat
BIJSLUITER. Bijsluiter: informatie voor de gebruiker. GLUCOTRACE 185 MBq/ml, oplossing voor injectie Fludeoxyglucose ( 18 F)
 BIJSLUITER Bijsluiter: informatie voor de gebruiker GLUCOTRACE 185 MBq/ml, oplossing voor injectie Fludeoxyglucose ( 18 F) Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er
BIJSLUITER Bijsluiter: informatie voor de gebruiker GLUCOTRACE 185 MBq/ml, oplossing voor injectie Fludeoxyglucose ( 18 F) Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er
Hulpstoffen met bekend effect: Dit geneesmiddel bevat minder dan 1 mmol natrium (23 mg) per dosis.
 Page 1 of 9 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL PROHANCE, 279,3 mg/ml, oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Gadoteridol 279,3 mg/ml (0,5
Page 1 of 9 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL PROHANCE, 279,3 mg/ml, oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Gadoteridol 279,3 mg/ml (0,5
SAMENVATTING VAN DE PRODUCTKENMERKEN
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Clariscan 0,5 mmol/ml, oplossing voor injectie Clariscan 0,5 mmol/ml, oplossing voor injectie in voorgevulde spuit. 2. KWALITATIEVE EN
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Clariscan 0,5 mmol/ml, oplossing voor injectie Clariscan 0,5 mmol/ml, oplossing voor injectie in voorgevulde spuit. 2. KWALITATIEVE EN
RISICO MINIMALISATIE MATERIAAL BETREFFENDE TENOFOVIRDISOPROXIL-BEVATTENDE PRODUCTEN VOOR VOORSCHRIJVERS.
 RISICO MINIMALISATIE MATERIAAL BETREFFENDE TENOFOVIRDISOPROXIL-BEVATTENDE PRODUCTEN VOOR VOORSCHRIJVERS. Brochure controle nierfunctie bij behandeling van volwassenen met HIV De risico minimalisatie materialen
RISICO MINIMALISATIE MATERIAAL BETREFFENDE TENOFOVIRDISOPROXIL-BEVATTENDE PRODUCTEN VOOR VOORSCHRIJVERS. Brochure controle nierfunctie bij behandeling van volwassenen met HIV De risico minimalisatie materialen
Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke informatie in voor u.
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKERS BRIDATEC 40 mg kit voor radiofarmaceutisch preparaat mebrofenine Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKERS BRIDATEC 40 mg kit voor radiofarmaceutisch preparaat mebrofenine Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke
voor ouders Controleer deze lijst voor de n Motiveer uw kind voor het onderzoek.
 Speciale informatie voor ouders n Motiveer uw kind voor het onderzoek. Leg uit dat het noodzakelijk is om in het lichaam te kijken om de oorzaak te vinden waarom hij of zij zich niet goed voelt en vertel
Speciale informatie voor ouders n Motiveer uw kind voor het onderzoek. Leg uit dat het noodzakelijk is om in het lichaam te kijken om de oorzaak te vinden waarom hij of zij zich niet goed voelt en vertel
SAMENVATTING VAN DE PRODUCTKENMERKEN
 Gadovist PFS/PFC SmPC Pagina 1 van 13 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Gadovist 1,0 mmol/ml oplossing voor injectie in voorgevulde spuit/patroon 2. KWALITATIEVE EN KWANTITATIEVE
Gadovist PFS/PFC SmPC Pagina 1 van 13 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Gadovist 1,0 mmol/ml oplossing voor injectie in voorgevulde spuit/patroon 2. KWALITATIEVE EN KWANTITATIEVE
Risico minimalisatie materiaal betreffende tenofovirdisoproxil voor voorschrijvers - Brochure controle nierfunctie bij behandeling van volwassenen
 Risico minimalisatie materiaal betreffende voor voorschrijvers - Brochure controle nierfunctie bij behandeling van volwassenen De risico minimalisatie materialen voor zijn beoordeeld door het College ter
Risico minimalisatie materiaal betreffende voor voorschrijvers - Brochure controle nierfunctie bij behandeling van volwassenen De risico minimalisatie materialen voor zijn beoordeeld door het College ter
Bijsluiter: informatie voor de patiënt. Dopaview 222 MBq/ml oplossing voor injectie. Fluorodopa ( 18 F)
 Bijsluiter: informatie voor de patiënt Dopaview 222 MBq/ml oplossing voor injectie Fluorodopa ( 18 F) Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
Bijsluiter: informatie voor de patiënt Dopaview 222 MBq/ml oplossing voor injectie Fluorodopa ( 18 F) Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke informatie in voor u.
 BIJSLUITER: INFORMATIE VOOR GEBRUIKERS Sodium Chromate [ 51 Cr] Solution Ph. Eur. radiofarmaceutische uitgangsoplossing 37 MBq/ml natriumchromaat [ 51 Cr] Lees goed de hele bijsluiter voordat u dit geneesmiddel
BIJSLUITER: INFORMATIE VOOR GEBRUIKERS Sodium Chromate [ 51 Cr] Solution Ph. Eur. radiofarmaceutische uitgangsoplossing 37 MBq/ml natriumchromaat [ 51 Cr] Lees goed de hele bijsluiter voordat u dit geneesmiddel
Radiologie CT onderzoek maag CT onderzoek alvleesklier (pancreas)
 Radiologie CT onderzoek maag CT onderzoek alvleesklier (pancreas) CT onderzoek maag CT onderzoek alvleesklier (pancreas) U wordt vriendelijk verzocht deze folder in zijn geheel door te lezen. Deze folder
Radiologie CT onderzoek maag CT onderzoek alvleesklier (pancreas) CT onderzoek maag CT onderzoek alvleesklier (pancreas) U wordt vriendelijk verzocht deze folder in zijn geheel door te lezen. Deze folder
Bijlage I. Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen
 Bijlage I Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen 1 Wetenschappelijke conclusies Rekening houdend met het beoordelingsrapport
Bijlage I Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen 1 Wetenschappelijke conclusies Rekening houdend met het beoordelingsrapport
Bijsluiter: informatie voor de gebruiker. Glucose 5% B. Braun, oplossing voor infusie Glucose.monohydraat
 Bijsluiter: informatie voor de gebruiker Glucose 5% B. Braun, oplossing voor infusie Glucose.monohydraat Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat belangrijke
Bijsluiter: informatie voor de gebruiker Glucose 5% B. Braun, oplossing voor infusie Glucose.monohydraat Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken, want er staat belangrijke
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. Primovist 0,25 mmol/ml oplossing voor injectie, voorgevulde spuit. dinatriumgadoxetaat
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Primovist 0,25 mmol/ml oplossing voor injectie, voorgevulde spuit. dinatriumgadoxetaat Lees goed de hele bijsluiter voordat u dit geneesmiddel toegediend krijgt,
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER Primovist 0,25 mmol/ml oplossing voor injectie, voorgevulde spuit. dinatriumgadoxetaat Lees goed de hele bijsluiter voordat u dit geneesmiddel toegediend krijgt,
BIJSLUITER. Ketodolor 100 mg/ml oplossing voor injectie voor paarden, runderen en varkens
 BIJSLUITER Ketodolor 100 mg/ml oplossing voor injectie voor paarden, runderen en varkens 1. NAAM EN ADRES VAN DE HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EN DE FABRIKANT VERANTWOORDELIJK
BIJSLUITER Ketodolor 100 mg/ml oplossing voor injectie voor paarden, runderen en varkens 1. NAAM EN ADRES VAN DE HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EN DE FABRIKANT VERANTWOORDELIJK
Bijsluiter: informatie voor de gebruiker. Traxidot 100 mg/ml, oplossing voor injectie Tranexaminezuur
 Bijsluiter: informatie voor de gebruiker Traxidot 100 mg/ml, oplossing voor injectie Tranexaminezuur Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
Bijsluiter: informatie voor de gebruiker Traxidot 100 mg/ml, oplossing voor injectie Tranexaminezuur Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie
Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er staat belangrijke informatie in voor u.
 BIJSLUITER: INFORMATIE VOOR GEBRUIKER Chromium [ 51 Cr] EDTA oplossing voor injectie 3,7 MBq/ml Chroom [ 51 Cr] edetaat Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er
BIJSLUITER: INFORMATIE VOOR GEBRUIKER Chromium [ 51 Cr] EDTA oplossing voor injectie 3,7 MBq/ml Chroom [ 51 Cr] edetaat Lees goed de hele bijsluiter voordat u dit geneesmiddel krijgt toegediend want er
Belangrijke Veiligheidsinformatie over prasugrel
 Belangrijke Veiligheidsinformatie over prasugrel Prasugrel behoort tot de farmacotherapeutische groep van de bloedplaatjesaggregatieremmers (heparine niet meegerekend), een groep waaronder ook clopidogrel
Belangrijke Veiligheidsinformatie over prasugrel Prasugrel behoort tot de farmacotherapeutische groep van de bloedplaatjesaggregatieremmers (heparine niet meegerekend), een groep waaronder ook clopidogrel
Wijzigingen in de Samenvatting van de Productkenmerken en Bijsluiter, voorgesteld door het Europees Geneesmiddelenbureau
 BIJLAGE II Wijzigingen in de Samenvatting van de Productkenmerken en Bijsluiter, voorgesteld door het Europees Geneesmiddelenbureau Deze Samenvatting van de Productkenmerken en Bijsluiter zijn het resultaat
BIJLAGE II Wijzigingen in de Samenvatting van de Productkenmerken en Bijsluiter, voorgesteld door het Europees Geneesmiddelenbureau Deze Samenvatting van de Productkenmerken en Bijsluiter zijn het resultaat
Risico minimalisatie materiaal betreffende testosteronundecanoaat voor beroepsbeoefenaren in de gezondheidszorg
 Risico minimalisatie materiaal betreffende testosteronundecanoaat voor beroepsbeoefenaren in de gezondheidszorg De risico minimalisatie materialen voor testosteronundecanoaat zijn beoordeeld door het College
Risico minimalisatie materiaal betreffende testosteronundecanoaat voor beroepsbeoefenaren in de gezondheidszorg De risico minimalisatie materialen voor testosteronundecanoaat zijn beoordeeld door het College
De werkzame stof is gadoteerzuur. Het is aanwezig in de vorm van megluminegadoteraat (0,5 mmol megluminegadoteraat/ml).
 1. NAAM VAN HET GENEESMIDDEL Dotarem 0,5 mmol/ml, oplossing voor injectie. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING De werkzame stof is gadoteerzuur. Het is aanwezig in de vorm van megluminegadoteraat
1. NAAM VAN HET GENEESMIDDEL Dotarem 0,5 mmol/ml, oplossing voor injectie. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING De werkzame stof is gadoteerzuur. Het is aanwezig in de vorm van megluminegadoteraat
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN. Geneesmiddel niet langer geregistreerd
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL Ablavar 0,25 mmol/ml, oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml Ablavar oplossing voor injectie
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL Ablavar 0,25 mmol/ml, oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml Ablavar oplossing voor injectie
KEYTRUDA (pembrolizumab)
 Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab) voor patiënten KEYTRUDA (pembrolizumab) Patiënteninformatiefolder Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab)
Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab) voor patiënten KEYTRUDA (pembrolizumab) Patiënteninformatiefolder Risico minimalisatie materiaal betreffende Keytruda (pembrolizumab)
ANNEX III AANPASSINGEN VAN DE SAMENVATTING VAN PRODUCTKENMERKEN EN BIJSLUITER
 ANNEX III AANPASSINGEN VAN DE SAMENVATTING VAN PRODUCTKENMERKEN EN BIJSLUITER 25 RUBRIEKEN VAN DE SAMENVATTING VAN DE PRODUCTKENMERKEN VOOR BROMOCRIPTINE BEVATTENDE PRODUCTEN 4.2 Dosering en wijze van
ANNEX III AANPASSINGEN VAN DE SAMENVATTING VAN PRODUCTKENMERKEN EN BIJSLUITER 25 RUBRIEKEN VAN DE SAMENVATTING VAN DE PRODUCTKENMERKEN VOOR BROMOCRIPTINE BEVATTENDE PRODUCTEN 4.2 Dosering en wijze van
Gadovist 1,0 mmol/ml oplossing voor injectie in voorgevulde spuit / patroon
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Gadovist 1,0 mmol/ml oplossing voor injectie in voorgevulde spuit / patroon 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml oplossing
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Gadovist 1,0 mmol/ml oplossing voor injectie in voorgevulde spuit / patroon 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml oplossing
CT scan van de wervelzuil. Informatiebrochure
 CT scan van de wervelzuil Informatiebrochure 1 2 Geachte mevrouw, meneer Deze brochure is een uitgave van de dienst radiologie van het Sint- Andriesziekenhuis Tielt. Hiermee willen we u graag wat meer
CT scan van de wervelzuil Informatiebrochure 1 2 Geachte mevrouw, meneer Deze brochure is een uitgave van de dienst radiologie van het Sint- Andriesziekenhuis Tielt. Hiermee willen we u graag wat meer
Bijlage I. Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen
 Bijlage I Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen Wetenschappelijke conclusies Rekening houdend met het beoordelingsrapport
Bijlage I Wetenschappelijke conclusies en redenen voor de wijziging van de voorwaarden van de vergunning(en) voor het in de handel brengen Wetenschappelijke conclusies Rekening houdend met het beoordelingsrapport
Bijsluiter: informatie voor de gebruiker. Glypressin 0,1 mg/ml, oplossing voor injectie. Terlipressine
 Bijsluiter: informatie voor de gebruiker Glypressin 0,1 mg/ml, oplossing voor injectie Terlipressine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken. - Bewaar deze bijsluiter. Misschien
Bijsluiter: informatie voor de gebruiker Glypressin 0,1 mg/ml, oplossing voor injectie Terlipressine Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken. - Bewaar deze bijsluiter. Misschien
SAMENVATTING VAN DE PRODUCTKENMERKEN. 1 ml oplossing voor injectie bevat 279,32 mg gadoteerzuur (als megluminezout), wat overeenkomt met 0,5 mmol.
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Dotagraph 0,5 mmol/ml oplossing voor injectie (60 ml/100 ml) 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml oplossing voor injectie
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Dotagraph 0,5 mmol/ml oplossing voor injectie (60 ml/100 ml) 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 ml oplossing voor injectie
BIJSLUITER. Revertor 5 mg/ml Oplossing voor Injectie voor honden en katten
 BIJSLUITER Revertor 5 mg/ml Oplossing voor Injectie voor honden en katten 1. NAAM EN ADRES VAN DE HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EN DE FABRIKANT VERANTWOORDELIJK VOOR VRIJGIFTE,
BIJSLUITER Revertor 5 mg/ml Oplossing voor Injectie voor honden en katten 1. NAAM EN ADRES VAN DE HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN EN DE FABRIKANT VERANTWOORDELIJK VOOR VRIJGIFTE,
BIJSLUITER: INFORMATIE VOOR DE PATIËNT. OSTEOCIS 3 mg kit voor radiofarmaceutisch preparaat natriumoxidronaat
 BIJSLUITER: INFORMATIE VOOR DE PATIËNT OSTEOCIS 3 mg kit voor radiofarmaceutisch preparaat natriumoxidronaat Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
BIJSLUITER: INFORMATIE VOOR DE PATIËNT OSTEOCIS 3 mg kit voor radiofarmaceutisch preparaat natriumoxidronaat Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke
