HOVON 135 AML NL
|
|
|
- Camiel Adam
- 6 jaren geleden
- Aantal bezoeken:
Transcriptie
1 HOVON 135 AML NL Informatie voor de proefpersoon behorende bij het onderzoek: HOVON 135 AML: Een programma met gerandomiseerde fase II studie naar de verdraagbaarheid en werkzaamheid van het toevoegen van nieuwe geneesmiddelen aan 10 dagen decitabine bij patiënten van 66 jaar of ouder, niet fit voor intensieve chemotherapie, met onbehandelde acute myeloïde leukemie (AML) en hoog risico myelodysplastisch syndroom (MDS) Officiële titel: A randomized phase II multicenter study to assess the tolerability and efficacy of the addition of new drugs to 10-day decitabine in UNFIT (i.e. HCT-CI 3) AML and high risk myelodysplasia (MDS) (IPSS-R > 4.5) patients aged 66 years Inleiding Geachte heer, mevrouw, Wij vragen u vriendelijk om mee te doen aan het hierboven genoemde medisch-wetenschappelijk onderzoek. Dit onderzoek wordt uitgevoerd door de stichting HOVON (Hemato-Oncologie voor Volwassenen Nederland). Wij vragen u mee te doen aan dit onderzoek omdat u acute myeloïde leukemie (AML) of myelodysplasie (MDS) heeft. Het onderzoek zal in een groot aantal ziekenhuizen in Nederland en buiten Nederland worden uitgevoerd. In totaal zullen ten minste 140 patiënten meedoen. U beslist zelf of u wilt meedoen. Voordat u de beslissing neemt, is het belangrijk om meer te weten over het onderzoek. Lees deze informatiebrief rustig door. Bespreek het met partner, vrienden of familie. Lees ook de algemene brochure Medisch-wetenschappelijk onderzoek (bijlage 2). Daar staat veel algemene informatie over medisch-wetenschappelijk onderzoek in. Heeft u na het lezen van de informatie nog vragen? Dan kunt u terecht bij uw arts of de andere artsen die in bijlage 1 vermeld staan. 1. Wat is het doel van het onderzoek? Uit onderzoek is gebleken dat in uw beenmerg leukemiecellen aanwezig zijn, die de normale bloedaanmaak belemmeren. Afhankelijk van het aantal leukemiecellen dat in uw beenmerg is aangetroffen wordt er gesproken van acute myeloïde leukemie (AML) of van myelodysplasie (MDS) met een hoog risico. In de folder Acute leukemie van het KWF Kankerbestrijding (bijlage 3) kunt u hierover meer informatie vinden. De gebruikelijke behandeling bij AML en hoog risico MDS is intensieve chemotherapie (leukemiedodende geneesmiddelen). Bij patiënten, die vanwege bijkomende ziekten (zoals bijvoorbeeld hart/vaatziekten of longziekten), intensieve chemotherapie niet aan kunnen ( niet fit genoeg voor intensieve chemotherapie ), kan gekozen worden voor een mildere therapie. Deze leidt niet tot genezing, maar dient om de kwaliteit van leven zo lang mogelijk acceptabel te laten zijn. Voor deze groep patiënten is dit onderzoek ontwikkeld. Om niet fit genoeg voor intensieve chemotherapie te kunnen meten wordt de zogenaamde Sorror score gebruikt. Uit eerder onderzoek weten we dat patiënten met een Sorror score van 3 of hoger intensieve chemotherapie niet goed verdragen. U kunt deelnemen aan deze studie als u een Sorror score van 3 of hoger heeft of als u niet met intensieve chemotherapie behandeld wilt worden. Patiënteninformatie voor HOVON 135 AML Pagina 1 van 16
2 HOVON 135 AML NL Voor de behandeling van oudere AML patiënten die niet in aanmerking komen voor intensieve chemotherapie, zijn een aantal mogelijkheden beschikbaar. Eén van deze mogelijkheden is behandeling met het middel decitabine. is effectief tegen leukemie en heeft minder bijwerkingen dan intensieve chemotherapie., gegeven in kuren van 5 achtereenvolgende dagen is geregistreerd voor de behandeling van AML. Er is wetenschappelijk onderzoek dat suggereert dat decitabine gegeven in kuren van 10 achtereenvolgende dagen effectiever is en over het algemeen goed wordt verdragen. Deze behandeling is echter nog niet geregistreerd voor behandeling met AML. In dit wetenschappelijk onderzoek is de behandeling met 10-daagse kuren decitabine de standaardbehandeling, waarmee behandeling met 10-daagse decitabine in combinatie met een nieuw geneesmiddel wordt vergeleken. In deze informatiebrief wordt behandeling met 10-daagse decitabine kuren daarom ook de standaardbehandeling genoemd. Het doel van dit onderzoek is te onderzoeken of toevoeging van een nieuw geneesmiddel aan de standaardbehandeling uw ziekte beter onder controle brengt. Tevens wordt nagegaan of het nieuwe geneesmiddel bijwerkingen geeft. 2. Welke geneesmiddelen wordt onderzocht? In dit onderzoek kunnen tegelijkertijd een aantal nieuwe veelbelovende geneesmiddelen onderzocht worden. U kunt voor de standaardbehandeling in aanmerking komen of voor de standaardbehandeling aangevuld met één van die nieuwe geneesmiddelen. In bijlage 4 is de onderzoeksbehandeling in een schema weergegeven. Op dit moment wordt in uw centrum het volgende nieuwe geneesmiddel onderzocht: - ibrutinib Meer informatie over dit nieuwe geneesmiddel vindt u in de bijlage 5 van deze informatiebrief 3. Hoe wordt het onderzoek uitgevoerd? Indien u besluit om aan het onderzoek mee te doen, dan zal voor de start van de behandeling door loting worden bepaald of u de standaardbehandeling krijgt of de standaardbehandeling aangevuld met het nieuwe geneesmiddel. Uw onderzoeksarts heeft geen invloed op de loting. Zowel u als uw arts krijgt de uitslag van de loting te horen. De loting (ook wel randomisatie genoemd) is nodig om op onafhankelijke wijze de behandelingen met elkaar te kunnen vergelijken. De kans om voor een bepaalde behandeling in aanmerking te komen, is voor iedere behandelingsmogelijkheid even groot. Behandeling met decitabine (standaardbehandeling) Bij de eerste kuur zult u gedurende 10 dagen elke dag decitabine via een infuus in de arm krijgen toegediend. Deze toediening duurt ca. 1 uur. Als uw ziekte goed op de behandeling heeft gereageerd, dan zal de tweede kuur bestaan uit 5 dagen decitabine. Als uw ziekte nog onvoldoende op de behandeling heeft gereageerd, dan zal de tweede kuur wederom bestaan uit 10 dagen decitabine. Patiënteninformatie voor HOVON 135 AML Pagina 2 van 16
3 HOVON 135 AML NL Als uw ziekte na de tweede kuur goed op de behandeling heeft gereageerd, dan zal de derde kuur bestaan uit 5 dagen decitabine. Als uw ziekte nog onvoldoende op de behandeling heeft gereageerd, dan zal ook de derde kuur bestaan uit 10 dagen decitabine. Na 3 kuren zal de behandeling langdurig worden voortgezet in het 5 daagse schema totdat de ziekte terugkeert of verdere behandeling te zwaar wordt vanwege bijwerkingen. Om het effect van de behandeling te beoordelen zullen standaard beenmergonderzoeken worden gedaan na de 1e, 2e, en 3e kuur en 9 maanden na start van de behandeling. In principe vinden de eerste 3 kuren met decitabine om de 4 à 6 weken plaats. Vanaf kuur 4 vinden de kuren met decitabine om de 4 à 8 weken plaats. De duur van de periode tussen de kuren wordt vooral bepaald door het herstel van de bloedwaarden en uw conditie. Gewoonlijk zal de eerste kuur tijdens een opname van minimaal 10 dagen gegeven worden. Afhankelijk van hoe de ziekte reageert op de behandeling en de eventuele complicaties van de behandeling, kunnen de vervolgkuren zowel tijdens opname in het ziekenhuis of op de dagbehandeling worden gegeven. De behandeling met decitabine wordt gegeven zolang de ziekte voldoende onder controle is, de bijwerkingen acceptabel zijn en u baat hebt van de behandeling. Nieuw geneesmiddel (toegevoegd aan de standaardbehandeling) Bij het HOVON 135 onderzoek wordt continu de werkzaamheid en veiligheid van één of meerdere nieuwe geneesmiddelen bekeken. Informatie over de nieuwe geneesmiddelen die op dit moment in uw centrum worden onderzocht, staan beschreven in bijlage 5 van deze informatiebrief. Afhankelijk van de uitslag van de loting kan u voor behandeling met één van deze middelen in aanmerking komen. Omdat het nieuwe middel nog niet eerder aan de standaard behandeling voor AML en hoog risico MDS is toegevoegd, wordt in de eerste fase van het onderzoek de verdraagbaarheid en veilige dosering vastgesteld. Deze vastgestelde dosering wordt vervolgens voor de rest van het onderzoek gebruikt. 4. Wat wordt er van u verwacht? Tijdens het onderzoek vragen wij u de voorschriften van uw arts goed op te volgen. Het is voor uw veiligheid van belang, dat u zich niet zonder medeweten van uw arts ergens anders laat behandelen. U krijgt voor dit onderzoek onderzoeksmedicatie mee naar huis. Het is voor het onderzoek van belang dat u de eventuele niet geslikte medicatie en de lege verpakkingen mee terug brengt bij uw volgende bezoek aan het ziekenhuis. 5. Wat is meer of anders dan de reguliere behandeling(en) die u krijgt? Ongeacht de loting krijgen alle patiënten tijdens de eerste drie kuren dezelfde onderzoeken (met name bloedafnames en controles van het beenmerg). Echter bij patiënten die de standaardbehandeling krijgen met toevoeging van een nieuw geneesmiddel vinden soms extra beenmergpuncties plaats. Dit staat vermeld in de specifieke informatie over het nieuwe geneesmiddel (bijlage 5). Patiënteninformatie voor HOVON 135 AML Pagina 3 van 16
4 HOVON 135 AML NL Aanvullend onderzoek Tijdens enkele gebruikelijke beenmergpuncties (voor en tijdens de behandeling) willen we een beperkte hoeveelheid extra beenmerg opzuigen en extra bloed en speeksel afnemen. Voor het beenmerg is dit ongeveer 30 ml voor start van de behandeling en ongeveer 10 ml bij de punctie na 3 kuren en de punctie bij 9 maanden na start van de behandeling. Voor het bloed is dit 30 ml voor start van de behandeling en na de eerste kuur. Voor deze extra afnames hoeft u geen extra puncties te ondergaan. Om speeksel te verzamelen moet eenmalig in een potje worden gespuugd. Het extra lichaamsmateriaal is bedoeld voor aanvullend wetenschappelijk onderzoek waarbij er gekeken wordt naar kenmerken (DNA, RNA en eiwit) van de leukemie, metingen van restziekte (aanwezigheid van kleine hoeveelheden leukemiecellen) en andere wetenschappelijke vraagstellingen, die met AML of hoog risico MDS verband hebben. De resultaten van deze wetenschappelijke onderzoeken zullen pas later beschikbaar komen en zijn bedoeld voor het verbeteren van onze kennis over de behandeling van leukemie. Indien u de afname van extra beenmerg en bloed niet wilt, kunt u niet aan het HOVON 135 onderzoek deelnemen. Verder zult u tijdens de vervolgbehandelingen met decitabine regelmatig onderzocht worden. Hierbij wordt geïnformeerd naar uw klachten en wordt een algemeen lichamelijk onderzoek verricht. Ook wordt er regelmatig bloedonderzoek verricht, zoals gebruikelijk is bij de ziekte AML. In bijlage 6 vindt u in een schema weergegeven wat er tijdens elke fase in het onderzoek gebeurt. Mochten er in verband met het gebruik van een bepaald nieuw geneesmiddel nog extra onderzoeken nodig zijn, dan staat dit vermeld bij de specifieke informatie over het nieuwe geneesmiddel (bijlage 5). 6. Wat zijn de andere mogelijke behandelingen? Mocht u besluiten niet mee te doen dan zijn er een aantal behandelmogelijkheden beschikbaar, zoals alleen ondersteunende behandeling, behandeling met azacitidine of behandeling met decitabine volgens het 5 daagse schema. Uw behandelend arts zal u informeren over de mogelijke behandelingen informeren. 7. Welke bijwerkingen kunt u verwachten? Niet alle bekende bijwerkingen staan hier vermeld. Het is ook niet zo dat alle genoemde bijwerkingen met zekerheid bij elke patiënt zullen optreden. Daarnaast is het mogelijk dat er bijwerkingen optreden die nog niet bekend zijn. Wanneer u klachten krijgt, vragen wij u dit altijd aan uw arts te melden. Ook als u zelf denkt dat het geen bijwerking van het onderzoek is. Bij ernstige klachten moet u onmiddellijk contact opnemen met uw arts. Daarnaast zal tijdens uw bezoek op de polikliniek regelmatig gevraagd worden of u klachten heeft gehad en zo ja, in welke mate. Dit onderzoek kan de volgende bijwerkingen hebben: Bijwerkingen behandeling met 10 daagse kuren decitabine (standaardbehandeling) Bij de in deze studie gebruikte dosering decitabine is onderdrukking van de normale bloedaanmaak de meest voorkomende bijwerking. In tegenstelling tot intensieve chemotherapie heeft decitabine geen effect op weefsels met snelle celdeling, waardoor er in verhouding weinig bijwerkingen zijn en er nauwelijks of geen invloed is op uw haargroei. Patiënteninformatie voor HOVON 135 AML Pagina 4 van 16
5 HOVON 135 AML NL Hieronder staan bijwerkingen die ooit geregistreerd zijn voor decitabine: - Bij meer dan 10% van de patiënten: Zwelling van de enkels (perifeer oedeem), hoofdpijn, misselijkheid en braken, diarree, ontsteking van mond en lippen, constipatie (verstopping) en buikpijn, verminderde eetlust, hoesten, verlaagde bloedzouten, verlaagde bloedeiwitten en verhoogde bloedsuikerspiegel. - Bij 1 tot 10 % van de patiënten: Zweren van tong of lip, slapeloosheid, haaruitval, rode huid, verhoogde bloeddruk, onregelmatig hartritme, gewichtsverlies, verandering van lever- en nierfuncties, spierpijn (met name rug), gewrichtspijn en borstpijn. - Bij minder dan 1 % van de patiënten: Ernstige allergische reactie, septische shock (lage bloeddruk als gevolg van bloedinfectie), Sweet syndroom (syndroom met verhoogd aantal witte bloedcellen, rode huidplekken en koorts). Met betrekking tot bovenstaande dient opgemerkt te worden dat de genoemde maag- en darmklachten (misselijkheid, ontsteking van de mond, diarree) veel minder vaak en in minder ernstige vorm voorkomen bij decitabine dan bij intensieve chemotherapie het geval is. In de praktijk hebben patiënten die decitabine krijgen geen medicijnen tegen misselijkheid nodig. Nieuw geneesmiddel De reeds bekende bijwerkingen staan vermeld in de specifieke informatie over het nieuwe geneesmiddel (bijlage 5 van deze informatiebrief). Als er teveel bijwerkingen optreden bij de behandeling met decitabine + nieuw geneesmiddel, dan wordt de dosering van het middel verlaagd. Binnen het studie protocol zijn strikte regels gedefinieerd hoe hiermee omgegaan moet worden. Schade voor het (ongeboren) kind Hoewel dit voor de meeste patiënten niet meer aan de orde zal zijn, verstrekken wij toch de volgende informatie. Middelen die in dit onderzoek worden gebruikt kunnen schadelijk zijn voor het ongeboren kind. Vrouwen die zwanger zijn of borstvoeding geven mogen niet met deze middelen behandeld worden. Bent u een man? Dan mag u tijdens dit onderzoek geen kind verwekken. Uw arts zal met u de meest geschikte voorbehoedmiddelen bespreken. Wordt u of uw partner toch zwanger in de onderzoeksperiode? Neem direct contact op met uw arts. 8. Wat zijn de mogelijke voor- en nadelen van deelname aan dit onderzoek? Indien u meedoet aan dit onderzoek hopen we dat uw leukemie beter reageert op de behandeling door de toevoeging van een nieuw geneesmiddel, als u daarvoor heeft geloot. We kunnen u echter niet garanderen dat u baat heeft bij behandeling met een nieuw geneesmiddel. We weten ook niet welke van de verschillende nieuwe geneesmiddelen die onderzocht worden, beter wordt verdragen of welke de ziekte beter terugdringt. Dat zal dit onderzoek uit moeten wijzen. Door toevoeging van een nieuw geneesmiddel aan de behandeling is de kans op bijwerkingen groter. Dat kan een nadeel zijn. Hoewel het nieuwe geneesmiddel al eerder is toegepast en goed verdragen lijkt te worden, zijn mogelijk nog niet alle bijwerkingen bekend bij niet fitte patiënten met AML of hoog risico MDS die met decitabine behandeld worden. Ook kan het gebeuren dat ten gevolge van de bijwerkingen een tijdelijke ziekenhuisopname noodzakelijk is. Het onderzoek kan nuttige wetenschappelijke gegevens voor de toekomst opleveren, maar het valt niet te voorspellen of het nieuwe middel bij u werkzaam zal zijn. Patiënteninformatie voor HOVON 135 AML Pagina 5 van 16
6 HOVON 135 AML NL Wat gebeurt er als u niet wenst deel te nemen aan dit onderzoek? U beslist zelf of u meedoet aan het onderzoek. Deelname is vrijwillig. Als u besluit niet mee te doen, hoeft u verder niets te doen. U hoeft niets te tekenen. U hoeft ook niet te zeggen waarom u niet wilt meedoen. U krijgt dan de behandeling die u anders ook zou krijgen. Als u wel meedoet, kunt u zich altijd bedenken en toch stoppen, ook tijdens het onderzoek. Wat u ook besluit, het zal geen gevolgen hebben voor uw behandeling en uw verzorging. Als u tussentijds wilt stoppen, geef dit dan wel aan bij uw arts, zodat u het gebruik van de geneesmiddelen op een veilige manier kunt afbouwen of stoppen. Als u tussentijds stopt kan het voor de onderzoeker nuttig zijn om te weten of u zich terugtrekt omdat u het onderzoek te belastend vindt (bijvoorbeeld te veel bijwerkingen). Maar als u dat niet wilt, hoeft u niet te zeggen waarom u stopt. 10. Wat gebeurt er als het onderzoek is afgelopen? Het onderzoek is voor u afgelopen als u de onderzoeksbehandeling gehad heeft en als de daar op volgende controlevisites afgelopen zijn. In het kader van dit onderzoek zult u tot 5 jaar na het starten van de behandeling onder controle blijven. Het kan ook zijn dat uw arts uw behandeling eerder stopt, bijvoorbeeld omdat u te veel last heeft van bijwerkingen. Ook de stichting HOVON kan besluiten om het onderzoek te stoppen, omdat er nieuwe informatie bekend wordt over uw ziekte of de behandeling. 11. Bent u verzekerd wanneer u aan het onderzoek meedoet? Voor iedereen die meedoet aan dit onderzoek is een verzekering afgesloten. De verzekering dekt schade als gevolg van het onderzoek. Dit geldt voor schade die naar boven komt tijdens het onderzoek, of binnen vier jaar na het einde van het onderzoek. In bijlage 7 vindt u de verzekerde bedragen, de uitzonderingen en de adresgegevens van de verzekeraar. 12. Wordt u geïnformeerd als er tussentijds voor u relevante informatie over het onderzoek bekend wordt? Het onderzoek zal zo nauwkeurig mogelijk volgens plan verlopen. Maar de situatie kan veranderen. Bijvoorbeeld door de manier waarop u op de behandeling reageert, of door nieuwe informatie. Als dat zo is, bespreekt uw arts dat direct met u. U beslist dan zelf of u met het onderzoek wilt stoppen of doorgaan. Als uw veiligheid of welbevinden in gevaar is, stoppen we direct met het onderzoek. 13. Wat gebeurt er met uw gegevens en lichaamsmateriaal? Voor dit onderzoek is het nodig dat uw lichaamsmateriaal en uw medische en persoonsgegevens worden verzameld en gebruikt. Elke proefpersoon krijgt een code die op het lichaamsmateriaal en de gegevens komt te staan. Uw naam wordt weggelaten. Uw gegevens Al uw gegevens blijven vertrouwelijk. Alleen de onderzoeker en de medewerkers van het ziekenhuis die de onderzoeker helpen met de uitvoering van het onderzoek weten welke code u heeft. In sommige ziekenhuizen zullen medewerkers van het Integraal Kankercentrum Nederland (IKNL) inzage hebben in de code en uw gegevens, om de onderzoeker te helpen gegevens te verzamelen voor dit onderzoek. Wij geven uw gegevens door aan de opdrachtgever van het onderzoek, maar Patiënteninformatie voor HOVON 135 AML Pagina 6 van 16
7 HOVON 135 AML NL alleen met die code, nooit met uw naam. De sleutel voor de code blijft bij de onderzoeker in uw ziekenhuis. Ook in rapporten over het onderzoek wordt alleen die code gebruikt. Sommige mensen mogen uw medische en persoonsgegevens inzien. Dit is om te controleren of het onderzoek goed en betrouwbaar is. Algemene informatie hierover vindt u in de brochure Medischwetenschappelijk onderzoek. Mensen die uw gegevens kunnen inzien zijn het onderzoeksteam, een controleur die voor de opdrachtgever van het onderzoek werkt, en de Inspectie voor de Gezondheidszorg. Zij houden uw gegevens geheim. Als u de toestemmingsverklaring ondertekent, geeft u toestemming voor het verzamelen, bewaren en inzien van uw medische en persoonsgegevens. Uw medische gegevens zullen tot 5 na start van uw behandeling worden verzameld. Vervolgens worden alle gegevens met betrekking tot het onderzoek nog 15 jaar bewaard. Als u in een academisch ziekenhuis behandeld wordt, worden uw gegevens met betrekking tot het onderzoek gedurende 20 jaar bewaard. Uw lichaamsmateriaal Voor het bij dit onderzoek horende aanvullende laboratoriumonderzoek (zie ook paragraaf 5 van deze informatiebrief), wordt uw lichaamsmateriaal (bloed, beenmerg en speeksel) naar de hematologische laboratoria van het VUmc in Amsterdam en het Erasmus MC in Rotterdam gestuurd. Wij willen uw gegevens en overgebleven lichaamsmateriaal graag bewaren. Misschien kunnen we daar later extra onderzoek mee doen. Het gaat dan om onderzoek met als doel meer te leren over de ziekte die u heeft en om de diagnose en behandeling te kunnen verbeteren. Uw lichaamsmateriaal wordt 15 jaar bewaard. Op het toestemmingsformulier kunt u aangeven of u hiermee akkoord gaat. U kunt deze toestemming altijd weer intrekken. Uw opgeslagen lichaamsmateriaal wordt dan vernietigd. Als er al metingen in uw monsters zijn gedaan, worden de resultaten daarvan wel gebruikt. Er is een heel kleine kans dat bij later uitgevoerd onderzoek, met uw opgeslagen lichaamsmateriaal, medische informatie bekend wordt die belangrijk kan zijn voor u persoonlijk of uw familie. Bijvoorbeeld als ontdekt wordt dat u drager bent van een erfelijke ziekte. Als dit gebeurt, zal HOVON de onderzoeker in uw ziekenhuis informeren. Aan de hand van de code zal de onderzoeker uw persoonsgegevens herleiden en u hierover informeren. Als u dit niet wilt, kunt u dit aangeven op het toestemmingsformulier. 14. Wordt uw huisarts en/of behandelend specialist geïnformeerd bij deelname? Indien u een huisarts en/of behandelend specialist heeft, informeert uw arts hen schriftelijk dat u meedoet aan het onderzoek. Dit is voor uw eigen veiligheid. U geeft hiervoor toestemming op het toestemmingsformulier. Als u geen toestemming geeft, kunt u niet meedoen aan het onderzoek. 15. Zijn er extra kosten/is er een vergoeding wanneer u besluit aan dit onderzoek mee te doen? Aan deelname aan dit onderzoek zijn voor u geen extra kosten verbonden. Dat wil zeggen dat er geen extra kosten voor u of uw zorgverzekeraar zijn bovenop de kosten van de reguliere Patiënteninformatie voor HOVON 135 AML Pagina 7 van 16
8 HOVON 135 AML NL behandeling die u zou krijgen als u niet meedoet aan het onderzoek. Alleen de onderdelen van de behandeling in dit onderzoek die hetzelfde zijn als een reguliere behandeling worden bij uw zorgverzekering gedeclareerd, zoals dat anders ook zou gebeuren. U krijgt geen vergoeding voor deelname en reiskosten. 16. Welke medisch-ethische toetsingscommissie heeft dit onderzoek goedgekeurd? De medisch-ethische toetsingscommissie van het Universitair Medisch Centrum Groningen heeft dit onderzoek goedgekeurd. Meer informatie over de goedkeuring vindt u in de Algemene brochure. 17. Wilt u verder nog iets weten? Natuurlijk heeft u tijd nodig om erover na te denken of u aan dit onderzoek wilt meedoen. Ook zult u er waarschijnlijk met anderen over willen praten. Hiervoor krijgt u uiteraard de gelegenheid. Als het in uw belang is om binnen een bepaalde tijd met een behandeling te starten, zal uw arts u dat vertellen. Dit kan dan van invloed zijn op de bedenktijd die u heeft voor dit onderzoek. Mocht u verdere vragen hebben, dan kunt u die voorleggen aan uw arts of andere artsen in dit ziekenhuis. Als u voor of tijdens het onderzoek vragen heeft die u liever niet aan uw arts stelt, kunt u contact opnemen met een onafhankelijke arts, die zelf niet bij het onderzoek betrokken is. Als u niet tevreden bent over het onderzoek of de behandeling kunt u een klacht indienen. In bijlage 1 vindt u alle contactgegevens en kunt u vinden waar u een klacht kunt indienen. Als de resultaten van het hele onderzoek bekend zijn, wordt hierover een artikel geschreven en gepubliceerd via de patiëntenorganisatie Hematon (zie ook Ondertekening toestemmingsverklaring Als u besluit om aan het onderzoek mee te doen, vragen wij u het toestemmingsformulier te ondertekenen. Door ondertekening van deze toestemmingsverklaring stemt u in met deelname aan dit onderzoek. U kunt altijd nog beslissen om met deelname te stoppen. Uw arts zal het formulier eveneens ondertekenen en bevestigt daarmee dat u bent geïnformeerd over het onderzoek en dat u deze informatiebrief heeft ontvangen. *Bijlagen: 1. Contactgegevens 2. Brochure Medisch-wetenschappelijk onderzoek 3. Brochure AML van KWF Kankerbestrijding 4. Behandelschema 5. Specifieke informatie over ibrutinib 6. Overzicht van onderzoeken 7. Informatie over de verzekering 8. Toestemmingsverklaring Patiënteninformatie voor HOVON 135 AML Pagina 8 van 16
9 HOVON 135 AML Bijlage 1 NL Contactgegevens Meer informatie U kunt meer informatie over het onderzoek krijgen bij de onderzoeker: Dr. W.J.F.M. van der Velden Telefoonnummer: Onafhankelijk arts Als onafhankelijk arts kunt u raadplegen: Mw. dr. C.M.L. van Herpen, afdeling Medische Oncologie Telefoonnummer: Klachten Een klacht kunt u indienen bij de onafhankelijke klachtencommissie van het Radboudumc. De klachtencommissie is te bereiken op telefoonnummer Stichting HOVON Voor meer informatie over de stichting HOVON kunt u ook kijken op de website Patiënteninformatie voor HOVON 135 AML Pagina 9 van 16
10 HOVON 135 AML Bijlage 4 NL Behandelschema Kuur 1 Kuur 2 Kuur 3 Kuur 4 en volgende Standaard behandeling 10 dagen 5 of 10 dagen 5 of 10 dagen Tot verslechtering van de ziekte 5 dagen, iedere 4 tot 8 weken Loting Behandeling met nieuw medicijn Ibrutinib 3 dagen voorbehandeling Ibrutinib dag -2, -1 en dagen Ibrutinib vanaf dag 11 tot start volgende kuur 5 of 10 dagen Ibrutinib vanaf dag 6 of 11 tot start volgende kuur 5 of 10 dagen Ibrutinib vanaf dag 6 of 11 tot start volgende kuur Tot verslechtering van de ziekte 5 dagen, iedere 4 tot 8 weken Ibrutinib vanaf dag 6 tot start volgende kuur Behandeling met nieuw medicijn X 10 dagen Medicijn X 5 of 10 dagen Medicijn X 5 of 10 dagen Medicijn X Tot verslechtering van de ziekte 5 dagen, iedere 4 tot 8 weken Medicijn X Patiënteninformatie voor HOVON 135 AML Pagina 10 van 16
11 HOVON 135 AML Bijlage 5 NL Bijlage met specifieke informatie over ibrutinib Ibrutinib is een nieuw geneesmiddel dat in het HOVON 135 onderzoek onderzocht wordt. Ibrutinib is reeds beschikbaar voor de behandeling van andere bloedziekten zoals chronische lymfatische leukemie (CLL) en mantelcellymfoom. Ibrutinib blokkeert het eiwit Brutons tyrosinekinase (BTK) dat bepaalde kankers helpt te overleven en te groeien. Dit eiwit is in bepaalde cellen aanwezig en speelt een rol bij processen die de groei, verspreiding en overleving van deze cellen beïnvloeden. Wetenschappelijk onderzoek heeft laten zien dat het eiwit BTK ook een rol speelt bij AML. Gebleken is dat ibrutinib de groei van AML cellen kan remmen. Bij de HOVON 135 willen we onderzoeken of ibrutinib een positieve bijdrage levert aan de behandeling van patiënten met AML en hoog risico MDS. Doel van het onderzoek Het doel van het onderzoek is om vast te stellen wat de veilige dosering is van ibrutinib in combinatie met de 10-daagse kuren decitabine en wat de bijwerkingen van deze behandeling zijn. Daarnaast wordt de effectiviteit van de behandeling met 10-daagse kuren decitabine vergeleken met de behandeling met 10-daagse kuren decitabine gecombineerd met ibrutinib. Zoals beschreven in deze informatiebrief bestaat de behandeling met decitabine uit een onbepaald aantal kuren. Als u voor behandeling met ibrutinib hebt geloot, wordt ibrutinib 3 dagen voorafgaand aan de start van de behandeling met decitabine gegeven. Vervolgens wordt ibrutinib gegeven op alle dagen, behalve de dagen dat u decitabine krijgt. Ibrutinib wordt eenmaal daags oraal (via de mond) ingenomen in de vorm van capsules. De capsules ibrutinib moeten samen met een glas water worden ingenomen. U mag de capsules niet openen, breken of kauwen. Bijwerkingen van ibrutinib Bijwerkingen die ooit geregistreerd zijn voor ibrutinib: Bij meer dan 10% van de patiënten: lage bloedwaarden, koorts, koude rillingen, griepachtige klachten, blauwe plekken, puntbloedinkjes onder de huid, zweertjes in de mond, hoofdpijn, verstopping, misselijkheid, braken, diarree, rode huid, pijnlijke armen of benen, rugpijn of gewrichtspijn, spierkrampen, gezwollen handen of enkels of voeten. Bij 1 tot 10 % van de patiënten: bloed bij urine of ontlasting, snelle (onregelmatige) hartslag, toegenomen aantal witte bloedcellen, laag aantal witte bloedcellen met koorts, wazig zien, droge mond, infecties van urinewegen of huid, neusbloedingen, uitdroging, verhoogde urinezuurspiegel. Bij minder dan 1 % van de patiënten: sterke stijging van witte bloedcellen met klontering van cellen als gevolg. Niet alle bekende bijwerkingen staan hier vermeld. Het is ook niet zo dat alle genoemde bijwerkingen met zekerheid bij elke patiënt zullen optreden. Daarnaast is het mogelijk dat er Patiënteninformatie voor HOVON 135 AML Pagina 11 van 16
12 HOVON 135 AML Bijlage 5 NL bijwerkingen optreden die nog niet bekend zijn. Bij het optreden van onbegrepen klachten of verschijnselen is het belangrijk om te overleggen met uw behandelend arts. Interactie met andere geneesmiddelen of voedingsmiddelen Sommige voedingsmiddelen zoals grapefruit en bittere sinaasappelen, en sommige geneesmiddelen kunnen invloed hebben op de manier waarop uw lichaam ibrutinib verwerkt. Door deze interacties kan de hoeveelheid ibrutinib in uw lichaam hoger of lager zijn dan verwacht. Het kan ook zijn dat de inname van ibrutinib samen met uw gebruikelijke geneesmiddelen of supplementen, inclusief vitaminen, een invloed heeft op het effect van uw gebruikelijke geneesmiddelen of supplementen. Het is belangrijk op te merken dat ibrutinib niet in combinatie met anti-stollingsmedicatie en sommige antibiotica kan worden gegeven. Indien u anti-schimmelmedicatie nodig hebt dient de dosering van Ibrutinib te worden aangepast. Het is zeer belangrijk dat u sap van grapefruit en bittere sinaasappelen, supplementen zoals visolie en vitamine E preparaten en preparaten met St. Janskruid vermijdt en uw arts op de hoogte brengt van alle geneesmiddelen of supplementen die u tijdens het onderzoek gebruikt. Zorg dat u uw arts onmiddellijk elke bijwerking meldt om schade te voorkomen. Extra onderzoek en controle Patiënten die loten voor aanvullende behandeling met ibrutinib krijgen dit geneesmiddel 3 dagen voor de start van de eerste kuur decitabine. Deze voorbehandeling met ibrutinib wordt gedaan om het effect van alleen ibrutinib op de AML en hoog risico MDS cellen te onderzoeken. Daarom zal op de dag dat gestart wordt met de eerste kuur decitabine een extra beenmerg punctie met afname van 5 ml beenmerg en een extra bloedafname voor afname van 10 ml bloed uitgevoerd worden. De overige onderzoeken zijn zoals beschreven in deze informatiebrief. Patiënteninformatie voor HOVON 135 AML Pagina 12 van 16
13 HOVON 135 AML Bijlage 6 NL Overzicht van onderzoeken Bij start Na kuur 1, 2, 3 Tijdens kuur 4 en verder Medische voorgeschiedenis Check criteria voor deelname (inclusief Sorror score en geriatrische evaluatie) X X Afnemen toestemmingsverklaring X Controle bijwerkingen X X Lichamelijk onderzoek X Op indicatie Op indicatie Bloedafname voor controle X 1 Wekelijks tot herstel Iedere 4-8 weken, of bij terugkeer ziekte Afname extra bloed voor aanvullend onderzoek (geen extra punctie) Extra bij loting voor behandeling met ibrutinib: Afname extra bloed voor aanvullend onderzoek (wel extra punctie) Speeksel verzamelen X 1 X Op dag 10 van de 1 e kuur Op dag 1 van de 1 e kuur Afname beenmerg X 1 X Na 9 maanden of bij terugkeer ziekte Afname extra beenmerg voor aanvullend onderzoek (geen extra punctie) X 1 Na 3 kuren Na 9 maanden Extra bij loting voor behandeling met ibrutinib: Afname extra beenmerg voor aanvullend onderzoek (wel extra punctie) Op dag 1 van 1 e kuur Botbiopt Op indicatie Longfoto X Op indicatie Op indicatie ECG (hartfilmpje) X Op indicatie Onderzoek hartfunctie Op indicatie X 1 Bloed en beenmergonderzoek is reeds gedaan om de diagnose AML of MDS te stellen Indien bij diagnose nog geen extra bloed of beenmerg is afgenomen voor aanvullend onderzoek, zal dit nu voor start wel gebeuren. Patiënteninformatie voor HOVON 135 AML Pagina 13 van 16
14 HOVON 135 AML Bijlage 7 NL Informatie over de verzekering Voor iedereen die meedoet aan dit onderzoek, heeft HOVON een verzekering afgesloten. De verzekering dekt schade door deelname aan het onderzoek. Dit geldt voor schade tijdens het onderzoek of binnen vier jaar na het einde ervan. Schade moet u binnen die vier jaar aan de verzekeraar hebben gemeld. De verzekering dekt niet alle schade. Onderaan deze tekst staat in het kort welke schade niet wordt gedekt. Deze bepalingen staan in het Besluit verplichte verzekering bij medisch-wetenschappelijk onderzoek met mensen. Dit besluit staat op de website van de Centrale Commissie Mensgebonden Onderzoek (zie Bibliotheek en dan Wet- en regelgeving ). Bij schade kunt u direct contact leggen met de verzekeraar. De verzekeraar van het onderzoek is: Naam: HDI-Gerling Industrie Versicherung AG, Directie voor Nederland Adres: Postbus 925, 3000 AX ROTTERDAM Telefoonnummer: info@hdi-gerling.nl Onderzoek: HOVON 135 AML Contactpersoon: hr. M. Wijnsma, kantoor Amsterdam De verzekering biedt een dekking van per proefpersoon en voor het hele onderzoek. De verzekering dekt de volgende schade niet: schade door een risico waarover u in de schriftelijke informatie bent ingelicht. Dit geldt niet als het risico zich ernstiger voordoet dan was voorzien of als het risico heel onwaarschijnlijk was; schade aan uw gezondheid die ook zou zijn ontstaan als u niet aan het onderzoek had meegedaan; schade door het niet (volledig) opvolgen van aanwijzingen of instructies; schade aan uw nakomelingen, als gevolg van een negatief effect van het onderzoek op u of uw nakomelingen; schade door een bestaande behandelmethode bij onderzoek naar bestaande behandelmethoden. Patiënteninformatie voor HOVON 135 AML Pagina 14 van 16
15 HOVON 135 AML Bijlage 8 NL Toestemmingsverklaring Voor deelname aan het wetenschappelijk onderzoek: HOVON 135 AML : Een programma met gerandomiseerde fase II studies naar de verdraagbaarheid en werkzaamheid van het toevoegen van nieuwe geneesmiddelen aan 10 dagen decitabine bij patiënten van 66 jaar of ouder, niet fit voor intensieve chemotherapie, met onbehandelde acute myeloïde leukemie (AML) en hoog risico myelodysplastisch syndroom (MDS) Officiële titel: A randomized phase II multicenter study to assess the tolerability and efficacy of the addition of new drugs to 10-day decitabine in UNFIT (i.e. HCT-CI 3) AML and high risk myelodysplasia (MDS) (IPSS-R > 4.5) patients aged 66 years Ik heb de informatie voor de proefpersoon gelezen. Ik begrijp de informatie. Ik kon aanvullende vragen stellen. Mijn vragen zijn genoeg beantwoord. Ik had genoeg tijd om te beslissen of ik meedoe. Ik weet dat mijn deelname helemaal vrijwillig is. Ik kan op ieder moment beslissen om toch niet mee te doen, zonder dat ik daarvoor een reden hoef te geven. Ik geef toestemming om mijn huisarts te vertellen dat ik meedoe aan dit onderzoek. Ik geef toestemming om de specialist(en) die mij behandelt te vertellen dat ik meedoe aan dit onderzoek. Ik weet dat sommige mensen mijn gegevens kunnen inzien. Dit zijn de mensen die vermeld staan in de Algemene Brochure (bijlage 2) en deze informatiebrief. Ik geef toestemming om mijn gegevens te verwerken voor de doelen zoals die in de informatiebrief staan. Ik geef toestemming om mijn gegevens gedurende maximaal 15 jaar na afloop van het onderzoek te bewaren (20 jaar in een academisch ziekenhuis). Ik geef toestemming voor afname van extra beenmerg, bloed en speeksel ten behoeve van het bij dit onderzoek horende wetenschappelijk onderzoek. Ik ben bereid om mee te doen aan het onderzoek. Wilt u de volgende vragen beantwoorden (* Doorhalen wat niet van toepassing is): Ik geef WEL / GEEN* toestemming voor opslag van overgebleven lichaamsmateriaal voor maximaal 15 jaar na afloop van de studie voor de doelen zoals die in deze informatiebrief staan. Ik wil WEL / NIET* geïnformeerd worden als er bij later uitgevoerd onderzoek op mijn opgeslagen lichaamsmateriaal medische informatie bekend wordt die belangrijk kan zijn voor mij persoonlijk of mijn familie. Naam patiënt: Handtekening: Datum : / / Patiënteninformatie voor HOVON 135 AML Pagina 15 van 16
16 HOVON 135 AML Bijlage 8 NL Ik verklaar hierbij dat ik deze patiënt volledig heb geïnformeerd over het genoemde onderzoek. Als er tijdens het onderzoek informatie bekend wordt die de toestemming van de patiënt zou kunnen beïnvloeden, dan breng ik hem/haar daarvan tijdig op de hoogte. Naam onderzoeker (of diens vertegenwoordiger): Handtekening: Datum: / / Patiënteninformatie voor HOVON 135 AML Pagina 16 van 16
Officiële titel: Blinatumomab added to prephase and consolidation therapy in precursor B-acute lymphoblastic leukemia in adults. A phase II trial.
 HOVON 146 ALL NL61022.078.17 Informatie voor de proefpersoon behorende bij het onderzoek HOVON 146: Blinatumomab toegevoegd aan prefase en consolidatie behandeling van volwassenen met een precursor B-cel
HOVON 146 ALL NL61022.078.17 Informatie voor de proefpersoon behorende bij het onderzoek HOVON 146: Blinatumomab toegevoegd aan prefase en consolidatie behandeling van volwassenen met een precursor B-cel
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek PACER-onderzoek: Onderzoek naar de noodzaak van correctie van bloedplaatjestekort voor het plaatsen van een centraal veneuze
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek PACER-onderzoek: Onderzoek naar de noodzaak van correctie van bloedplaatjestekort voor het plaatsen van een centraal veneuze
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek. 16 jaar en ouder.
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek. 16 jaar en ouder. Allo-antistofvorming bij sikkelcelziekte na transfusie: Wat is de rol van ontsteking en erfelijke aanleg?
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek. 16 jaar en ouder. Allo-antistofvorming bij sikkelcelziekte na transfusie: Wat is de rol van ontsteking en erfelijke aanleg?
HOVON 132 AML/SAKK 30/13
 Patiënteninformatie ten behoeve van het verzamelen van beenmerg, bloed en speeksel voor wetenschappelijk onderzoek Informatie behorende bij het hoofdonderzoek HOVON 132 AML/SAKK 30/13: Onderzoek naar de
Patiënteninformatie ten behoeve van het verzamelen van beenmerg, bloed en speeksel voor wetenschappelijk onderzoek Informatie behorende bij het hoofdonderzoek HOVON 132 AML/SAKK 30/13: Onderzoek naar de
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Onderzoek naar de behandeling van patiënten met een specifiek type AML, met de middelen panobinstat en midostaurine gedurende
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Onderzoek naar de behandeling van patiënten met een specifiek type AML, met de middelen panobinstat en midostaurine gedurende
Informatie voor patiënten en toestemmingsformulier behorende bij het onderzoek:
 Informatie voor patiënten en toestemmingsformulier behorende bij het onderzoek: Titel: Karakterisering van buffycoat afgeleide granulocyten (witte bloedcellen) om klinische parameters te identificeren
Informatie voor patiënten en toestemmingsformulier behorende bij het onderzoek: Titel: Karakterisering van buffycoat afgeleide granulocyten (witte bloedcellen) om klinische parameters te identificeren
Titel van het onderzoek: Bepaling van Zink en het Ontstekingseiwit PTX3 bij Patiënten met Sikkelcelziekte (ZIP studie)
 INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR PATIËNTEN Titel van het onderzoek: Bepaling van Zink en het Ontstekingseiwit PTX3 bij Patiënten met Sikkelcelziekte () Geachte heer/mevrouw, Wij vragen u om
INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR PATIËNTEN Titel van het onderzoek: Bepaling van Zink en het Ontstekingseiwit PTX3 bij Patiënten met Sikkelcelziekte () Geachte heer/mevrouw, Wij vragen u om
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 [Logo] Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek ASPIRIN TRIAL De rol van aspirine op de overleving van patiënten met dikkedarmkanker Inleiding Geachte heer/mevrouw,
[Logo] Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek ASPIRIN TRIAL De rol van aspirine op de overleving van patiënten met dikkedarmkanker Inleiding Geachte heer/mevrouw,
Patiënten-informatiebrief Volwassenen ICOS
 Patiënteninformatiefolder Voor patiënten van 18 jaar en ouder Behorende bij het onderzoek: International CIDP Outcome Study (ICOS) Een studie naar de variatie en de voorspellers van het ziektebeloop bij
Patiënteninformatiefolder Voor patiënten van 18 jaar en ouder Behorende bij het onderzoek: International CIDP Outcome Study (ICOS) Een studie naar de variatie en de voorspellers van het ziektebeloop bij
Titel van het onderzoek: De rol van de vorming van neutrofiele extracellulaire traps (NETs) in sikkelcelziekte.
 INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR PATIËNTEN Titel van het onderzoek: De rol van de vorming van neutrofiele extracellulaire traps (NETs) in sikkelcelziekte. Geachte heer/mevrouw, Wij vragen
INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR PATIËNTEN Titel van het onderzoek: De rol van de vorming van neutrofiele extracellulaire traps (NETs) in sikkelcelziekte. Geachte heer/mevrouw, Wij vragen
HOVON 103: Een studie voor de oudere patiënt met onbehandelde AML of hoog risico MDS
 Informatie voor de proefpersoon behorende bij het onderzoek: HOVON 103: Een studie voor de oudere patiënt met onbehandelde AML of hoog risico MDS Officiële titel: A randomized phase II multicenter study
Informatie voor de proefpersoon behorende bij het onderzoek: HOVON 103: Een studie voor de oudere patiënt met onbehandelde AML of hoog risico MDS Officiële titel: A randomized phase II multicenter study
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe
LEVODOPA BIJ PATIËNTEN MET VROEGE ZIEKTE VAN PARKINSON informatie voor deelnemers
 LEVODOPA BIJ PATIËNTEN MET VROEGE ZIEKTE VAN PARKINSON informatie voor deelnemers Geachte heer/ mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek. U beslist zelf
LEVODOPA BIJ PATIËNTEN MET VROEGE ZIEKTE VAN PARKINSON informatie voor deelnemers Geachte heer/ mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek. U beslist zelf
INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR GEZONDE VRIJWILLIGERS
 INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR GEZONDE VRIJWILLIGERS Titel van het onderzoek: De rol van de vorming van neutrofiele extracellulaire traps (NETs) in sikkelcelziekte. Geachte heer/mevrouw,
INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR GEZONDE VRIJWILLIGERS Titel van het onderzoek: De rol van de vorming van neutrofiele extracellulaire traps (NETs) in sikkelcelziekte. Geachte heer/mevrouw,
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Titel onderzoek: Bepalen van nieuwe ziektevoorspellers bij colorectale levermetastasen. De MIRACLE studie.
 Titel onderzoek: Bepalen van nieuwe ziektevoorspellers bij colorectale levermetastasen. De studie. Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek.
Titel onderzoek: Bepalen van nieuwe ziektevoorspellers bij colorectale levermetastasen. De studie. Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek.
Invloed van weeënremming op de uitkomst van vroeggeboorte,
 Patiëntinformatie voor deelname aan medisch-wetenschappelijk onderzoek Invloed van weeënremming op de uitkomst van vroeggeboorte, de APOSTEL VIII studie. Geachte mevrouw, Wij vragen u om mee te doen aan
Patiëntinformatie voor deelname aan medisch-wetenschappelijk onderzoek Invloed van weeënremming op de uitkomst van vroeggeboorte, de APOSTEL VIII studie. Geachte mevrouw, Wij vragen u om mee te doen aan
Geachte heer, mevrouw,
 Proefpersoneninformatie ten behoeve van het verzamelen van extra bloed voor wetenschappelijk onderzoek bij patiënten met leukemie en MDS die worden behandeld met decitabine 9 oktober 2017 Geachte heer,
Proefpersoneninformatie ten behoeve van het verzamelen van extra bloed voor wetenschappelijk onderzoek bij patiënten met leukemie en MDS die worden behandeld met decitabine 9 oktober 2017 Geachte heer,
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Een experimentele scan-techniek om de doorbloeding van het netvlies en het vaatvlies in het oog te meten.
 Schiedamse Vest 180 1 Postbus 70030 3000 LM Rotterdam telefoon: : 010-4023449 e-mail: roi@oogziekenhuis.nl www.oogziekenhuis.nl Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Schiedamse Vest 180 1 Postbus 70030 3000 LM Rotterdam telefoon: : 010-4023449 e-mail: roi@oogziekenhuis.nl www.oogziekenhuis.nl Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe validatie van een risicostratificatie
voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe validatie van een risicostratificatie
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Een nieuw stroomschema voor de behandeling van een verlaagd calciumgehalte in het bloed na totale schildklierverwijdering Implementation
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Een nieuw stroomschema voor de behandeling van een verlaagd calciumgehalte in het bloed na totale schildklierverwijdering Implementation
LEVODOPA BIJ PATIËNTEN MET VROEGE ZIEKTE VAN PARKINSON informatie voor deelnemers
 LEVODOPA BIJ PATIËNTEN MET VROEGE ZIEKTE VAN PARKINSON informatie voor deelnemers Geachte heer/ mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek. U beslist zelf
LEVODOPA BIJ PATIËNTEN MET VROEGE ZIEKTE VAN PARKINSON informatie voor deelnemers Geachte heer/ mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek. U beslist zelf
Verkorte titel: de effecten van budesonide op de bijwerkingen van cabazitaxel bij patiënten met prostaatkanker
 PATIËNTENINFORMATIE EN TOESTEMMINGSVERKLARING SUBSTUDIE BEHOREND BIJ HET ONDERZOEK: Fase II onderzoek bij patiënten met prostaatkanker naar de effecten van budesonide op cabazitaxel (Jevatana ): een gerandomiseerd,
PATIËNTENINFORMATIE EN TOESTEMMINGSVERKLARING SUBSTUDIE BEHOREND BIJ HET ONDERZOEK: Fase II onderzoek bij patiënten met prostaatkanker naar de effecten van budesonide op cabazitaxel (Jevatana ): een gerandomiseerd,
Geachte heer, mevrouw,
 Proefpersoneninformatie ten behoeve van het verzamelen van extra beenmerg voor wetenschappelijk onderzoek bij patiënten met leukemie en MDS 06 januari 2014 Geachte heer, mevrouw, Uw behandelende arts heeft
Proefpersoneninformatie ten behoeve van het verzamelen van extra beenmerg voor wetenschappelijk onderzoek bij patiënten met leukemie en MDS 06 januari 2014 Geachte heer, mevrouw, Uw behandelende arts heeft
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe validatie van een risicostratificatie
voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe validatie van een risicostratificatie
OCT. Schiedamse Vest 160 Postbus LM Rotterdam. tel.:
 Schiedamse Vest 160 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan medisch-wetenschappelijk onderzoek (studie)
Schiedamse Vest 160 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan medisch-wetenschappelijk onderzoek (studie)
Patiënteninformatiefolder Voor patiënten van 12 t/m 17 jaar. Behorende bij het onderzoek:
 Patiënteninformatiefolder Voor patiënten van 12 t/m 17 jaar Behorende bij het onderzoek: International CIDP Outcome Study (ICOS) Een studie naar de variatie en de voorspellers van het ziektebeloop bij
Patiënteninformatiefolder Voor patiënten van 12 t/m 17 jaar Behorende bij het onderzoek: International CIDP Outcome Study (ICOS) Een studie naar de variatie en de voorspellers van het ziektebeloop bij
Inleiding Geachte heer/mevrouw,
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De werking van het afweersysteem bij eiceldonatie zwangerschappen DONatie van Oocyten in Reproductie (DONOR); klinische en immunologische
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De werking van het afweersysteem bij eiceldonatie zwangerschappen DONatie van Oocyten in Reproductie (DONOR); klinische en immunologische
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe validatie van een risicostratificatie
voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe validatie van een risicostratificatie
Titel van het onderzoek Inbrengen van continue ambulante peritoneaal dialyse katheters: Kijkoperatie of open techniek?
 Titel van het onderzoek Inbrengen van continue ambulante peritoneaal dialyse katheters: Kijkoperatie of open techniek? Inleiding Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Titel van het onderzoek Inbrengen van continue ambulante peritoneaal dialyse katheters: Kijkoperatie of open techniek? Inleiding Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Onderzoek naar het effect van body mass index (BMI) en het roken van sigaretten op de opname van fentanyl
 Patiënteninformatie Onderzoek naar het effect van body mass index (BMI) en het roken van sigaretten op de opname van fentanyl Geachte heer/mevrouw, U bent in het Erasmus MC onder behandeling voor een vorm
Patiënteninformatie Onderzoek naar het effect van body mass index (BMI) en het roken van sigaretten op de opname van fentanyl Geachte heer/mevrouw, U bent in het Erasmus MC onder behandeling voor een vorm
Onderzoek naar bloedtest voor de diagnose beroerte
 Onderzoek naar bloedtest voor de diagnose beroerte MicroRNA als biomarker voor acute beroerte Inleiding Geachte heer/mevrouw, Wij vragen u om mee te doen aan een medisch-wetenschappelijk onderzoek. Meedoen
Onderzoek naar bloedtest voor de diagnose beroerte MicroRNA als biomarker voor acute beroerte Inleiding Geachte heer/mevrouw, Wij vragen u om mee te doen aan een medisch-wetenschappelijk onderzoek. Meedoen
Klinische keuzes bij patiënten met staar en hoornvliesdystrofie van Fuchs
 Schiedamse Vest 180 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie)
Schiedamse Vest 180 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie)
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Observationeel onderzoek van de BioMimics 3D-stent bij de behandeling van perifeer vaatlijden Officiële titel: Een prospectief,
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Observationeel onderzoek van de BioMimics 3D-stent bij de behandeling van perifeer vaatlijden Officiële titel: Een prospectief,
HOVON 97 AML. Inleiding Geachte heer, mevrouw,
 Patiënteninformatie behorende bij de studie: HOVON 97: Gerandomiseerde onderhoudsbehandeling met Azacitidine bij oudere patiënten ( 60 jaar) met acute myeloïde leukemie- en Myelodysplasie (Type RAEB en
Patiënteninformatie behorende bij de studie: HOVON 97: Gerandomiseerde onderhoudsbehandeling met Azacitidine bij oudere patiënten ( 60 jaar) met acute myeloïde leukemie- en Myelodysplasie (Type RAEB en
Patiënteninformatie behorende bij de studie HOVON 97 AML:
 Patiënteninformatie behorende bij de studie HOVON 97 AML: Een gerandomiseerde fase III studie naar het effect van onderhoudsbehandeling met Azacitidine bij oudere patiënten ( 60 jaar) met Acute Myeloïde
Patiënteninformatie behorende bij de studie HOVON 97 AML: Een gerandomiseerde fase III studie naar het effect van onderhoudsbehandeling met Azacitidine bij oudere patiënten ( 60 jaar) met Acute Myeloïde
Patiënten-informatiebrief Ouders ICOS
 Patiënteninformatiefolder Voor ouders/verzorgers (van patienten van 12 t/m 17 jaar) Behorende bij het onderzoek: International CIDP Outcome Study (ICOS) Een studie naar de variatie en de voorspellers van
Patiënteninformatiefolder Voor ouders/verzorgers (van patienten van 12 t/m 17 jaar) Behorende bij het onderzoek: International CIDP Outcome Study (ICOS) Een studie naar de variatie en de voorspellers van
HOVON 127 BL NL
 Informatie voor de proefpersoon behorende bij het onderzoek: Gerandomiseerd fase II onderzoek waarin bij patiënten met een Burkitt lymfoom 2 behandelingen vergeleken worden (R-CODOX-M/R-IVAC versus DA-EPOCH-R).
Informatie voor de proefpersoon behorende bij het onderzoek: Gerandomiseerd fase II onderzoek waarin bij patiënten met een Burkitt lymfoom 2 behandelingen vergeleken worden (R-CODOX-M/R-IVAC versus DA-EPOCH-R).
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Evaluatie minimale restziekte in PTLD Respons evaluatie van lymfklierkanker na orgaantransplantatie met 18 F-FDG-PET/CT en minimale
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Evaluatie minimale restziekte in PTLD Respons evaluatie van lymfklierkanker na orgaantransplantatie met 18 F-FDG-PET/CT en minimale
Onderzoek naar het effect van antibiotica op het beloop van acute milde diverticulitis
 DIABOLO studie Onderzoek naar het effect van antibiotica op het beloop van acute milde diverticulitis Geachte heer/mevrouw, Wij doen onderzoek naar het effect van antibiotica op het beloop van milde diverticulitis.
DIABOLO studie Onderzoek naar het effect van antibiotica op het beloop van acute milde diverticulitis Geachte heer/mevrouw, Wij doen onderzoek naar het effect van antibiotica op het beloop van milde diverticulitis.
Verkorte titel: de effecten van budesonide op de bijwerkingen van cabazitaxel bij patiënten met prostaatkanker
 PATIËNTENINFORMATIE EN TOESTEMMINGSVERKLARING Fase II onderzoek bij patiënten met prostaatkanker naar de effecten van budesonide op cabazitaxel (Jevatana ): een gerandomiseerd, open onderzoek in meerdere
PATIËNTENINFORMATIE EN TOESTEMMINGSVERKLARING Fase II onderzoek bij patiënten met prostaatkanker naar de effecten van budesonide op cabazitaxel (Jevatana ): een gerandomiseerd, open onderzoek in meerdere
DEPTHip NL v
 De DEPTHip Studie Subtitel: een continu Fascia Iliaca zenuwblok of intraveneuze analgesie bij patiënten met een heupfractuur en de invloed op het ontwikkelen van een delier Inleiding U wordt behandeld
De DEPTHip Studie Subtitel: een continu Fascia Iliaca zenuwblok of intraveneuze analgesie bij patiënten met een heupfractuur en de invloed op het ontwikkelen van een delier Inleiding U wordt behandeld
De invloed van een uitwendige kracht op de oogdruk.
 1 www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie) naar de invloed die een uitwendige kracht heeft
1 www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie) naar de invloed die een uitwendige kracht heeft
Onderzoek naar het effect van aprepitant (Emend ) op de fentanylpijnpleister
 Patiënteninformatie Onderzoek naar het effect van aprepitant (Emend ) op de fentanylpijnpleister (Durogesic ) Geachte heer/mevrouw, U bent in het Erasmus MC onder behandeling voor een vorm van kanker.
Patiënteninformatie Onderzoek naar het effect van aprepitant (Emend ) op de fentanylpijnpleister (Durogesic ) Geachte heer/mevrouw, U bent in het Erasmus MC onder behandeling voor een vorm van kanker.
Patiënteninformatie PLMA34 UMCG versie 3.1, 18 december 2015 Gebaseerd op studie template versie 3.1, 18 december 2015 Pagina 1 van 7
 Toevoeging van 10-dagen decitabine aan de standaard voorbehandeling (fludarabine en 2 Gray totale lichaamsbestraling) bij allogene hematopoietische cel transplantatie bij ongunstig risico acute myeloide
Toevoeging van 10-dagen decitabine aan de standaard voorbehandeling (fludarabine en 2 Gray totale lichaamsbestraling) bij allogene hematopoietische cel transplantatie bij ongunstig risico acute myeloide
Hebt u na het lezen van de informatie nog vragen? Dan kunt u terecht bij de onderzoeker. In de bijlage vindt u de contactgegevens.
 Informatiebrief Little DAVID-studie Geachte patïent, Wij vragen u vriendelijk om mee te doen aan de Little DAVID-studie. Dit staat voor Desmopressin and FVIII concentrate combination treatment in non-severe
Informatiebrief Little DAVID-studie Geachte patïent, Wij vragen u vriendelijk om mee te doen aan de Little DAVID-studie. Dit staat voor Desmopressin and FVIII concentrate combination treatment in non-severe
INFORMATIEBRIEF VOOR DE PATIËNT
 INFORMATIEBRIEF VOOR DE PATIËNT Titel van het onderzoek Een gerandomiseerd onderzoek naar operatieve versus niet-operatieve behandeling van breuken van het kopje van het spaakbeen. Inleiding Geachte heer/mevrouw,
INFORMATIEBRIEF VOOR DE PATIËNT Titel van het onderzoek Een gerandomiseerd onderzoek naar operatieve versus niet-operatieve behandeling van breuken van het kopje van het spaakbeen. Inleiding Geachte heer/mevrouw,
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Routine versus op indicatie verwijderen van de stelschroef Routinematig versus op indicatie verwijderen van de stelschroef:
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Routine versus op indicatie verwijderen van de stelschroef Routinematig versus op indicatie verwijderen van de stelschroef:
Onderzoek naar de nazorg bij dikke darmkanker door de huisarts of de chirurg en het gebruik van een persoonlijke interactieve website (I CARE studie).
 Onderzoek naar de nazorg bij dikke darmkanker door de huisarts of de chirurg en het gebruik van een persoonlijke interactieve website (I CARE studie). Verbetert de zorg na de behandeling van dikke darmkanker
Onderzoek naar de nazorg bij dikke darmkanker door de huisarts of de chirurg en het gebruik van een persoonlijke interactieve website (I CARE studie). Verbetert de zorg na de behandeling van dikke darmkanker
Informatie voor de wettelijke vertegenwoordiger voor deelname aan het onderzoek
 PAIS2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden of hoger Geachte heer/ mevrouw, Uw partner/familielid is in ons ziekenhuis
PAIS2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden of hoger Geachte heer/ mevrouw, Uw partner/familielid is in ons ziekenhuis
Titel van het onderzoek Inbrengen van continue ambulante peritoneaal dialyse katheters: Kijkoperatie of open techniek?
 Titel van het onderzoek Inbrengen van continue ambulante peritoneaal dialyse katheters: Kijkoperatie of open techniek? Inleiding Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Titel van het onderzoek Inbrengen van continue ambulante peritoneaal dialyse katheters: Kijkoperatie of open techniek? Inleiding Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Routine versus op indicatie verwijderen van de stelschroef Routinematig versus op indicatie verwijderen van de stelschroef:
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Routine versus op indicatie verwijderen van de stelschroef Routinematig versus op indicatie verwijderen van de stelschroef:
INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN LONGEMBOLIE
 INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN LONGEMBOLIE Hokusai post VTE studie: Lange termijn uitkomst na edoxaban versus warfarine voor
INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN LONGEMBOLIE Hokusai post VTE studie: Lange termijn uitkomst na edoxaban versus warfarine voor
Onderzoek naar bloedtest voor de diagnose beroerte
 Onderzoek naar bloedtest voor de diagnose beroerte MicroRNA als biomarker voor acute beroerte Inleiding Geachte heer/mevrouw, Wij vragen u om mee te doen aan een medisch-wetenschappelijk onderzoek. Meedoen
Onderzoek naar bloedtest voor de diagnose beroerte MicroRNA als biomarker voor acute beroerte Inleiding Geachte heer/mevrouw, Wij vragen u om mee te doen aan een medisch-wetenschappelijk onderzoek. Meedoen
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk. De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak Officiële titel: De rol van endoscopische echografie
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak Officiële titel: De rol van endoscopische echografie
Patiëntinformatieformulier LOGICA-trial
 Informatiebrief LOGICA trial: Laparoscopische versus Open Maag Operatie Datum: Onderwerp Telefoon E-mail 1 november 2015 LOGICA trial 088-005 6908 espillenaarbilgen@rijnstate.nl Geachte heer/mevrouw, U
Informatiebrief LOGICA trial: Laparoscopische versus Open Maag Operatie Datum: Onderwerp Telefoon E-mail 1 november 2015 LOGICA trial 088-005 6908 espillenaarbilgen@rijnstate.nl Geachte heer/mevrouw, U
Biobank Leukemie, Myeloom, Lymfklierkanker
 Patiënteninformatie behorend bij het onderzoek Biobank Leukemie, Myeloom, Lymfklierkanker Geachte heer, mevrouw, Uw behandelend arts heeft u geïnformeerd over bovengenoemd medischwetenschappelijk onderzoek.
Patiënteninformatie behorend bij het onderzoek Biobank Leukemie, Myeloom, Lymfklierkanker Geachte heer, mevrouw, Uw behandelend arts heeft u geïnformeerd over bovengenoemd medischwetenschappelijk onderzoek.
Patiënteninformatiefolder Voor patiënten van 12 t/m 17 jaar
 Patiënteninformatiefolder Voor patiënten van 12 t/m 17 jaar Behorende bij het onderzoek: International GBS Outcome Study (IGOS) Een studie naar voorspellers van het ziektebeloop bij het Guillain-Barré
Patiënteninformatiefolder Voor patiënten van 12 t/m 17 jaar Behorende bij het onderzoek: International GBS Outcome Study (IGOS) Een studie naar voorspellers van het ziektebeloop bij het Guillain-Barré
HOVON 132 AML/ SAKK 30/13 - Part A Run-In
 Informatie voor de proefpersoon behorende bij het onderzoek: HOVON 132 AML/SAKK 30-13: Onderzoek naar de werkzaamheid van lenalidomide, wanneer het wordt toegevoegd aan standaard inductie chemotherapie
Informatie voor de proefpersoon behorende bij het onderzoek: HOVON 132 AML/SAKK 30-13: Onderzoek naar de werkzaamheid van lenalidomide, wanneer het wordt toegevoegd aan standaard inductie chemotherapie
Het gebruik van siliconenolie in vitreoretinale chirurgie.
 Schiedamse Vest 160 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie)
Schiedamse Vest 160 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie)
Effect van transverse versus longitudinale incisies op kniepijn na tibiapen plaatsing. Patiënten Informatie Folder
 Effect van transverse versus longitudinale incisies op kniepijn na tibiapen plaatsing Patiënten Informatie Folder PATIËNTEN INFORMATIE FOLDER Effect van transverse versus longitudinale incisies op kniepijn
Effect van transverse versus longitudinale incisies op kniepijn na tibiapen plaatsing Patiënten Informatie Folder PATIËNTEN INFORMATIE FOLDER Effect van transverse versus longitudinale incisies op kniepijn
Patiënten Informatie formulier. SPLINT-trial
 Patiënten Informatie formulier SPLINT-trial Preventie van urologische complicaties bij niertransplantaties van levende donoren: splint of geen splint? Versie 2 09-10-2013 pagina 1 van 8 Titel van het onderzoek
Patiënten Informatie formulier SPLINT-trial Preventie van urologische complicaties bij niertransplantaties van levende donoren: splint of geen splint? Versie 2 09-10-2013 pagina 1 van 8 Titel van het onderzoek
INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN TROMBOSEBEEN
 INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN TROMBOSEBEEN Hokusai post VTE studie: Lange termijn uitkomst na edoxaban versus warfarine voor
INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN TROMBOSEBEEN Hokusai post VTE studie: Lange termijn uitkomst na edoxaban versus warfarine voor
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk. De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak Officiële titel: De rol van endoscopische echografie
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak Officiële titel: De rol van endoscopische echografie
NL [BASICS PIF en IC wilsbekwaam Isala versie 2.0 dd ]
![NL [BASICS PIF en IC wilsbekwaam Isala versie 2.0 dd ] NL [BASICS PIF en IC wilsbekwaam Isala versie 2.0 dd ]](/thumbs/70/61932504.jpg) BASICS: Basilar Artery International Cooperation Study Een gerandomiseerd onderzoek naar de veiligheid en effectiviteit van de lokale intra-arteriële behandeling na intraveneuze trombolyse bij een acute
BASICS: Basilar Artery International Cooperation Study Een gerandomiseerd onderzoek naar de veiligheid en effectiviteit van de lokale intra-arteriële behandeling na intraveneuze trombolyse bij een acute
Patiënteninformatieformulier imprint studie
 Patiënteninformatieformulier imprint studie (imaging of PSMA: Registratie en Inventarisatie voor Nederlandse Toepassing) Inleiding Uw arts heeft voorgesteld een aanvraag te doen voor een PSMA-PET-scan.
Patiënteninformatieformulier imprint studie (imaging of PSMA: Registratie en Inventarisatie voor Nederlandse Toepassing) Inleiding Uw arts heeft voorgesteld een aanvraag te doen voor een PSMA-PET-scan.
Inbrengen van continue ambulante peritoneaal dialyse katheters: Kijkoperatie of open techniek?
 Inbrengen van continue ambulante peritoneaal dialyse katheters: Kijkoperatie of open techniek? Inleiding Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek
Inbrengen van continue ambulante peritoneaal dialyse katheters: Kijkoperatie of open techniek? Inleiding Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek
Cholinesteraseremmers tegen het verergeren van visuele hallucinaties bij de ziekte van Parkinson
 Informatie voor deelnemers Cholinesteraseremmers tegen het verergeren van visuele hallucinaties bij de ziekte van Parkinson Geachte heer/mevrouw, Met deze brief willen wij u vragen om mee te doen aan medisch-wetenschappelijk
Informatie voor deelnemers Cholinesteraseremmers tegen het verergeren van visuele hallucinaties bij de ziekte van Parkinson Geachte heer/mevrouw, Met deze brief willen wij u vragen om mee te doen aan medisch-wetenschappelijk
HOVON 103 AML/RAEB. Patiënteninformatie
 Patiënteninformatie HOVON 103: Een programma met gerandomiseerde fase-ii studies naar de verdraagbaarheid en werkzaamheid van het toevoegen van nieuwe geneesmiddelen aan standaard inductie chemotherapie
Patiënteninformatie HOVON 103: Een programma met gerandomiseerde fase-ii studies naar de verdraagbaarheid en werkzaamheid van het toevoegen van nieuwe geneesmiddelen aan standaard inductie chemotherapie
Tamil Study version 1.0 PatInfo (NKI)/ (AMC)
 Titel van het onderzoek Onderzoek naar door de behandeling veroorzaakte veranderingen in de omringende cellen van het folliculaire Non Hodgkin lymfoom. De TAMIL studie Inleiding Geachte heer/mevrouw, Wij
Titel van het onderzoek Onderzoek naar door de behandeling veroorzaakte veranderingen in de omringende cellen van het folliculaire Non Hodgkin lymfoom. De TAMIL studie Inleiding Geachte heer/mevrouw, Wij
Bedekte of onbedekte stents in de bekkenslagader. Informatiebrief - Bedekte of onbedekte stents in de bekkenslagader (DISCOVER-studie)
 Informatiebrief - (DISCOVER-studie) Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek. U wordt benaderd voor dit onderzoek, omdat er een vernauwing
Informatiebrief - (DISCOVER-studie) Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek. U wordt benaderd voor dit onderzoek, omdat er een vernauwing
EORTC-1301-LG NL
 Informatie voor proefpersonen die in aanmerking komen voor het onderzoek: Vergelijking van 10-daagse behandeling met decitabine versus standaard chemotherapie ( 3+7 ) gevolgd door allogene stamceltransplantatie
Informatie voor proefpersonen die in aanmerking komen voor het onderzoek: Vergelijking van 10-daagse behandeling met decitabine versus standaard chemotherapie ( 3+7 ) gevolgd door allogene stamceltransplantatie
Netvliesloslating op OCT
 Schiedamse Vest 180 1 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie)
Schiedamse Vest 180 1 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie)
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek Fysiotherapie na een totale knie of heup prothese, de PATIO studie Inleiding Geachte heer/mevrouw, Wij
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek Fysiotherapie na een totale knie of heup prothese, de PATIO studie Inleiding Geachte heer/mevrouw, Wij
Geachte heer, mevrouw,
 Proefpersoneninformatie ten behoeve van het verzamelen van extra beenmerg voor wetenschappelijk onderzoek bij patiënten met verdenking op een aplastische anemie Geachte heer, mevrouw, Uw behandelende arts
Proefpersoneninformatie ten behoeve van het verzamelen van extra beenmerg voor wetenschappelijk onderzoek bij patiënten met verdenking op een aplastische anemie Geachte heer, mevrouw, Uw behandelende arts
Effect van transverse versus longitudinale incisies op kniepijn na tibiapen plaatsing
 PATIËNTEN INFORMATIE FOLDER Effect van transverse versus longitudinale incisies op kniepijn na tibiapen plaatsing Geachte heer/mevrouw, U wordt in het ziekenhuis geopereerd aan een gebroken scheenbeen
PATIËNTEN INFORMATIE FOLDER Effect van transverse versus longitudinale incisies op kniepijn na tibiapen plaatsing Geachte heer/mevrouw, U wordt in het ziekenhuis geopereerd aan een gebroken scheenbeen
HOVON 132 AML/SAKK 30/13
 Informatie voor de proefpersoon behorende bij het onderzoek: HOVON 132 AML/SAKK 30/13: Onderzoek naar de werkzaamheid van Lenalidomide, wanneer het wordt toegevoegd aan standaard inductie chemotherapie
Informatie voor de proefpersoon behorende bij het onderzoek: HOVON 132 AML/SAKK 30/13: Onderzoek naar de werkzaamheid van Lenalidomide, wanneer het wordt toegevoegd aan standaard inductie chemotherapie
Informatie voor de wettelijke vertegenwoordiger voor deelname aan het onderzoek
 PAIS 2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden Celsius of hoger Geachte heer/ mevrouw, Uw partner/familielid is in ons
PAIS 2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden Celsius of hoger Geachte heer/ mevrouw, Uw partner/familielid is in ons
HOVON 109 CLL NL
 Patiënteninformatie behorende bij het onderzoek: HOVON 109 CLL: Een fase I/II onderzoek, waarbij de veiligheid en effectiviteit wordt onderzocht van eerstelijns behandeling met chloorambucil, rituximab
Patiënteninformatie behorende bij het onderzoek: HOVON 109 CLL: Een fase I/II onderzoek, waarbij de veiligheid en effectiviteit wordt onderzocht van eerstelijns behandeling met chloorambucil, rituximab
Plaatsing van voedingssondes in de dunne darm via elektromagnetische geleiding op de verpleegafdeling of via kijkonderzoek op de endoscopie-afdeling
 Patiënt informatiebrief Plaatsing van voedingssondes in de dunne darm via elektromagnetische geleiding op de verpleegafdeling of via kijkonderzoek op de endoscopie-afdeling Geachte heer/mevrouw, Wij vragen
Patiënt informatiebrief Plaatsing van voedingssondes in de dunne darm via elektromagnetische geleiding op de verpleegafdeling of via kijkonderzoek op de endoscopie-afdeling Geachte heer/mevrouw, Wij vragen
Antibiotica voor cellulitis: 6 of 12 dagen?
 Antibiotica voor cellulitis: 6 of 12 dagen? Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (zie titel). Dit onderzoek wordt uitgevoerd in ca. acht
Antibiotica voor cellulitis: 6 of 12 dagen? Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (zie titel). Dit onderzoek wordt uitgevoerd in ca. acht
HOVON 133 MCL TRIANGLE Aanvulling op de informatie voor de proefpersoon
 HOVON 133 MCL TRIANGLE Aanvulling op de informatie voor de proefpersoon NL56406.078.16 Aanvulling op informatie voor de proefpersoon behorende bij het onderzoek: HOVON 133 MCL TRIANGLE: Autologe stamceltransplantatie
HOVON 133 MCL TRIANGLE Aanvulling op de informatie voor de proefpersoon NL56406.078.16 Aanvulling op informatie voor de proefpersoon behorende bij het onderzoek: HOVON 133 MCL TRIANGLE: Autologe stamceltransplantatie
Titel van het onderzoek: Biobank voor chronische lymfatische leukemie, lymfeklierkanker en myeloom
 INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR PATIENTEN Titel van het onderzoek: Biobank voor chronische lymfatische leukemie, lymfeklierkanker en myeloom Geachte heer, mevrouw, Uw arts heeft u geïnformeerd
INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR PATIENTEN Titel van het onderzoek: Biobank voor chronische lymfatische leukemie, lymfeklierkanker en myeloom Geachte heer, mevrouw, Uw arts heeft u geïnformeerd
Patiënteninformatie voor deelname aan het onderzoek
 PAIS2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden Celsius of hoger Geachte heer/mevrouw, Wij vragen u via deze brief mee
PAIS2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden Celsius of hoger Geachte heer/mevrouw, Wij vragen u via deze brief mee
Het FORECAST onderzoek
 Het FORECAST onderzoek De werking van het antibioticum fosfomycine bij een opstijgende urineweginfectie Patiënteninformatie [Geef tekst op] Pagina 0 1 Het FORECAST onderzoek Het FORECAST onderzoek De werking
Het FORECAST onderzoek De werking van het antibioticum fosfomycine bij een opstijgende urineweginfectie Patiënteninformatie [Geef tekst op] Pagina 0 1 Het FORECAST onderzoek Het FORECAST onderzoek De werking
Heb je na het lezen van de brief nog vragen? Dan kun je terecht bij de onderzoeker. In de bijlage vind je de contactgegevens.
 Informatiebrief Little DAVID-studie Beste patiënt, Met deze brief willen we je vragen of je mee wilt doen aan de Little DAVID-studie (kleine DAVID). Dit staat voor Desmopressin and factor VIII concentrate
Informatiebrief Little DAVID-studie Beste patiënt, Met deze brief willen we je vragen of je mee wilt doen aan de Little DAVID-studie (kleine DAVID). Dit staat voor Desmopressin and factor VIII concentrate
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek DISTRICTS Het Nederlandse injectie versus operatie onderzoek bij patiënten met een zenuwbeknelling in de pols. Geachte heer/mevrouw,
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek DISTRICTS Het Nederlandse injectie versus operatie onderzoek bij patiënten met een zenuwbeknelling in de pols. Geachte heer/mevrouw,
Langdurige behandeling van diep veneuze trombose bij patiënten met kanker (Longheva) Academisch Medisch Centrum, Amsterdam (AMC)
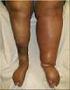 Titel studie: Opdrachtgever: Langdurige behandeling van diep veneuze trombose bij patiënten met kanker (Longheva) Academisch Medisch Centrum, Amsterdam (AMC) Hoofdonderzoeker: Dr. K. Meyer Introductie
Titel studie: Opdrachtgever: Langdurige behandeling van diep veneuze trombose bij patiënten met kanker (Longheva) Academisch Medisch Centrum, Amsterdam (AMC) Hoofdonderzoeker: Dr. K. Meyer Introductie
Metingen van de zenuwvezels in het netvlies met SD-OCT.
 Schiedamse Vest 160 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan medisch-wetenschappelijk onderzoek (studie)
Schiedamse Vest 160 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan medisch-wetenschappelijk onderzoek (studie)
Informatiebrief. Kies Gerust op maat. Versie 11 oktober 2016
 Informatiebrief Kies Gerust op maat Versie 11 oktober 2016 Inhoud 1. Wat is het doel van het onderzoek? 2. Hoe wordt de zorg vanuit de huisarts onderzocht? 3. Hoe wordt het onderzoek uitgevoerd? 4. Wat
Informatiebrief Kies Gerust op maat Versie 11 oktober 2016 Inhoud 1. Wat is het doel van het onderzoek? 2. Hoe wordt de zorg vanuit de huisarts onderzocht? 3. Hoe wordt het onderzoek uitgevoerd? 4. Wat
Drie-dimensionale echografie voor het verbeteren van cosmetisch resultaat bij borstkanker patiënten; TURACOS trial
 Drie-dimensionale echografie voor het verbeteren van cosmetisch resultaat bij borstkanker patiënten; Geachte mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek
Drie-dimensionale echografie voor het verbeteren van cosmetisch resultaat bij borstkanker patiënten; Geachte mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek
