PUBLICATIE VAN DE HOGE GEZONDHEIDSRAAD nr. 8318
|
|
|
- Julius de Graaf
- 8 jaren geleden
- Aantal bezoeken:
Transcriptie
1 PUBLICATIE VAN DE HOGE GEZONDHEIDSRAAD nr Specifieke kwaliteitsnormen voor humane cellen waarvoor geen andere specifieke kwaliteitsnormen bestaan en die voor toepassing op de mens bestemd zijn 7 november 2007 SAMENVATTING EN SLEUTELWOORDEN De kwaliteitsnormen vormen een geheel van regels inzake goede praktijk met betrekking tot de donatie, de verkrijging, de prelevatie, de controle, de bewerking, het bewaren en de distributie van weefsels en cellen die voor toepassing op de mens bestemd zijn. Ze houden rekening met de beschikkingen van de nationale wetgeving en ook met de Europese vereisten en aanbevelingen die van toepassing zijn. Ze vormen een basisdocument voor de directeurs van weefselbanken alsook voor de inspecteurs. Met het oog op de toekomstige omzetting van de Europese regelgeving inzake weefsels en cellen (richtlijnen 2004/23/EC, 2006/17/EC en 2006/86/EC), heeft de werkgroep Cellen, weefsels en organen van menselijke en dierlijke oorsprong actief gewerkt aan het opstellen van specifieke kwaliteitsnormen voor humane cellen waarvoor geen andere specifieke kwaliteitsnormen bestaan. Trefwoorden: kwaliteitsnormen, specifieke normen, menselijke toepassing, allogeen, autoloog, cellen, weefsels, humaan. 1
2 INHOUDSTAFEL 1. INLEIDING 4 2. SPECIFIEKE KWALITEITSNORMEN 5 SECTIE A: ALGEMENE INFORMATIE 5 A.1. KWALITEITSNORMEN 5 A.1.1. Kwaliteitsnormen 5 SECTIE B: ALGEMENE ORGANISATIE EN LOGISTIEK VAN EEN WEEFSEL- EN CELBANK 6 B.4. LOKALEN, UITRUSTINGEN EN LOGISTIEK 6 B.4.1. Lokalen 6 B Controle op lucht- en omgevingskwaliteit in bewerkingszones 6 SECTIE C: DOSSIERBEHEER 7 C.1. ALGEMENE RICHTLIJNEN 7 C.1.4. Traceerbaarheid 7 C.2. SAMENSTELLING VAN HET DOSSIER 7 C.2.1. Inhoudelijke vereisten 7 C Informatie betreffende de bewerking, de preservatie en het bewaren van weefsels en cellen 7 C Informatie betreffende de controle op weefsels en cellen 8 SECTIE D: VERKRIJGEN VAN WEEFSELS: DONATIE, DONORSCREENING EN PRELEVATIE 9 D.1. ALGEMEEN 9 D.4. SEROLOGISCH TESTS VOOR VIRUS- EN SYFILISVEILIGHEID 10 D.4.2. Minimale vereisten inzake serologische testen 10 D Allogene donatie 10 D Levende donoren 10 D.4.4. Leeftijdsgrenzen 10 D.5. PRELEVATIE 10 D.5.2. Prelevatie bij levende donoren 10 D.6. VERPAKKING EN TRANSPORT NAAR DE WEEFSEL- EN CELBANK 11 D.6.2. Transport 11 D Transportmodaliteiten van gepreleveerd menselijk materiaal 11 SECTIE E: BEWERKING, BEWAREN EN OPSLAG VAN WEEFSELS EN CELLEN 12 E.1. BEWERKING VAN WEEFSELS EN CELLEN 12 E.1.1. Algemeen 12 E.1.2. Bewerkingsprocedures 12 E Procedures voor celcultuur 12 E Cellencultuurtijden 13 E Cell Storage and Banking System (CSBS) 13 E Decontaminatie van weefsels en cellen 14 E Sterilisatie van cellen 14 E Inactivatie ten opzichte van prionen 14 E.1.3. Bewerkingsmedia en bijkomende therapeutische producten 14 E Materialen en reagentia gebruikt in het productieproces 14 E Algemeen 14 E Materialen en reagentia van menselijke oorsprong 16 2
3 E Materialen en reagentia van dierlijke oorsprong 16 E.1.5. Controle op weefsels en cellen tijdens hun bewerking 16 E.1.6. Maximale wachttijd voor de bewerking en het bewaren 17 E.2. BEWARING EN OPSLAG VAN WEEFSELS EN CELLEN 17 E.2.2. Bewaar- en opslagprocedures 17 E Bewaring bij +37 C 17 E Bewaring en opslag bij +4 C 17 E Cryopreservatie bij -80 C 18 E Cryopreservatie in vloeibare stikstof 18 E Lyofilisatie en dehydratatie 18 E Bewaring bij kamertemperatuur (+20 C +25 C) 18 SECTIE F: SECURISATIE VAN WEEFSELS EN CELLEN 19 F.1. MICROBIOLOGISCHE VEILIGHEID VAN WEEFSELS EN CELLEN 19 F.1.2. Bacteriologische en mycologische controles 19 SECTIE H: DISTRIBUTIE, IN- EN UITVOER VAN WEEFSELS EN CELLEN 20 H.1. Distributie van weefsels en cellen 20 H.1.2. Transport van weefsels en cellen 20 H Voorwaarden voor het transport van weefsels en cellen 20 H.3. Terugroeping en terugkeer van cellen 20 H.3.2. Terugkeer van (niet gebruikte) cellen SAMENSTELLING VAN DE WERKGROEP 21 3
4 1. INLEIDING De kwaliteitsnormen voor humane cellen houden rekening met de beschikkingen van de nationale wetgeving en ook met de Europese vereisten en aanbevelingen die van toepassing zijn. Ze vormen een geheel van regels inzake goede praktijk met betrekking tot de donatie, de verkrijging, de prelevatie, de controle, de bewerking, het bewaren en de distributie van weefsels en cellen die voor toepassing op de mens bestemd zijn. Gemeenschappelijke criteria voor alle verschillende types weefsels en cellen worden in een inleidende algemene publicatie samengebracht, met als titel Gemeenschappelijke kwaliteitsnormen voor alle weefsels en cellen die voor toepassing op de mens bestemd zijn. De specifieke vereisten die van toepassing zijn op een specifiek type weefsel of cel waarvoor een weefsel- en celbank een erkenning in België kan bekomen, worden in een tweede publicatie opgenomen, met als titel Specifieke kwaliteitsnormen ; in dit geval de humane cellen waarvoor geen specifieke kwaliteitsnormen bestaan. In geval van een verschil tussen de specificaties van de Gemeenschappelijke kwaliteitsnormen voor alle weefsels en cellen die voor toepassing op de mens bestemd zijn en die van de Specifieke kwaliteitsnormen hebben de vereisten van de specifieke normen de overhand op de gemeenschappelijke normen. 4
5 2. SPECIFIEKE KWALITEITSNORMEN SECTIE A: ALGEMENE INFORMATIE A.1. KWALITEITSNORMEN A.1.1. Kwaliteitsnormen De richtlijnen beschreven in dit document kunnen van toepassing zijn op verschillende celtypes waarvoor de celbank een erkenning heeft en die geïsoleerd worden uit humaan weefsel en verwerkt worden voor gebruik in het kader van de behandeling van een aandoening of van een ernstige deficiëntie bij de receptor. Het hoofddoel van deze tekst is ervoor te zorgen dat de auto- en allogreffen bestaande uit minimaal gemodificeerde cellen en die bij patiënten geïmplanteerd worden, een aanvaardbare kwaliteit en standaard bereiken en vrij zijn van potentieel infectieuze agenten en contaminanten. 5
6 SECTIE B: ALGEMENE ORGANISATIE EN LOGISTIEK VAN EEN WEEFSEL- EN CELBANK N / B.4. LOKALEN, UITRUSTINGEN EN LOGISTIEK B.4.1. Lokalen B Controle op lucht- en omgevingskwaliteit in bewerkingszones Alle manipulaties en bewerkingen van de cellen gebeuren onder aseptische omstandigheden in een omgeving waarvan de luchtkwaliteit, zoals beoordeeld aan de hand van het aantal deeltjes en het aantal kolonievormende eenheden, overeenkomt met klasse A (zoals omschreven in de European Guide to GMP en Richtlijn 2003/94/EG). De achtergrondomgeving dient overeen te komen met tenminste een GMP-klasse C. Zowel de cellen als de operator dienen beschermd te worden tegen contaminatie. Een verticale laminaire luchtstroom is dus aangewezen. De kwaliteit van de omgeving waaraan de cellen blootgesteld worden, wordt minimaal jaarlijks en extra wanneer nodig (vb.defect) gevalideerd. 6
7 SECTIE C: DOSSIERBEHEER C.1. ALGEMENE RICHTLIJNEN C.1.4. Traceerbaarheid Indien met eenzelfde bronmateriaal meerdere bewerkingen of producties gestart worden, zal door het toekennen van een uniek lotnummer per bewerking/productie een ondubbelzinnige link ontstaan met het uniek donor volgnummer. C.2. SAMENSTELLING VAN HET DOSSIER C.2.1. Inhoudelijke vereisten Het donordossier dat op de celbank bewaard wordt, bevat naast de inlichtingen vereist in hoofdstuk C.2.1. Inhoudelijke vereisten van de Gemeenschappelijke kwaliteitsnormen voor alle weefsels en cellen van menselijke oorsprong die voor toepassing op de mens bestemd zijn, de volgende inlichtingen die relevant zijn voor cellen: C Informatie betreffende de bewerking, de preservatie en het bewaren van weefsels en cellen - type bewerkte, gepreserveerde en/of bewaarde weefsels en cellen; - kwantitatieve en kwalitatieve beschrijving van de greffen (afhankelijk van de greffe); - datum en uur van elke stap van de bewerking en van de preservatie met identificatie van de verantwoordelijke personen voor deze stappen en identificatie van de gebruikte media en bijkomende producten (Lotnr. en vervaldatum); - status van de weefsels en cellen bij alle bewerkings- en bewaringsstappen (quarantaine, vrijgegeven voor therapeutisch gebruik, gebruik voor onderzoek in vitro, ); - gebruik van antibiotica, samenstelling van de antibiotica; indien van toepassing duur van de incubatie; - aard en hoeveelheid van het gebruikte medium voor de eindverpakking; indien van toepassing; - methodes en registraties betreffende de bewerking van weefsels en cellen; indien van toepassing: - gegevens betreffende de bewerking (preparatie, cultuurtechniek, incubatie, chemische behandelingen ); 7
8 - gegevens i.v.m. de cultuurtechniek; N / gegevens betreffende de preservatie (cryopreservatie, verloop van de koelingscurve, glycerolisering, lyofilisatie, ); - gegevens betreffende de technieken voor decontaminatie, sterilisatie en virale en/of bacteriële inactivatie; - resultaten van specifieke kwaliteitsonderzoeken afhankelijk van het type weefsels en cellen (HLA-typering, histologische resultaten, radiologische resultaten, viabiliteit van cellen of weelsels, ); - methodes en registraties betreffende de preservatie van weefsels en cellen; indien van toepassing: - datum en uur van het bewaren; - bewaringsmethode; - bewaringstemperatuur; - vervaldatum; - identificatie van de weefsels en bereide cellen: identificatiecode van de donatie + code product + splitsingcode (indien van toepassing) (cf. D Identificatie van weefsels en cellen ). C Informatie betreffende de controle op weefsels en cellen - bewaren van een serumstaal in serotheek gedurende 30 j. (verplicht voor Master Cell Bank); - resultaten van eventuele bio-veiligheidstesten uitgevoerd op de cellen (virussen, mycoplasma s, tumorgeniciteit, ); - resultaten van een eventuele fenotypische en/of genotypische karakterisatie van de cellen en histologie; - datum van vrijgave van de cellen. 8
9 SECTIE D: VERKRIJGEN VAN WEEFSELS: DONATIE, DONORSCREENING EN PRELEVATIE D.1. ALGEMEEN Voor het isoleren van cellen vertrekt men doorgaans van een volwaardig weefsel of orgaan. Voor de kwaliteitsnormen met betrekking tot de donatie, donorscreening, prelevatie, verpakking en transport van dit bronweefsel, waaruit de primaire cellen zullen worden geïsoleerd, wordt verwezen naar overeenkomstige specifieke kwaliteitsnormen. Voor humane huid keratinocyten is dit bijvoorbeeld SECTIE D: VERKRIJGEN VAN WEEFSELS: DONATIE, DONORSCREENING EN PRELEVATIE in de KWALITEITSNORMEN VOOR ALLOGREFFEN VAN DE HUID van de. Enkele uitzonderingen en bedenkingen worden hieronder beschreven. Weefsels waaruit cellen geïsoleerd worden die voor toepassing op de mens bestemd zijn, worden om bio-veiligheidsredenen bij voorkeur verkregen bij levende donoren. Alhoewel het technisch mogelijk is om cellen te isoleren uit nagenoeg elk weefsel, is het om bioveiligheids- en technische redenen aangeraden een bronmateriaal te kiezen dat cellen bevat met een groot potentieel (beperkt tot celtypen waarvoor men een Master Cell Bank kan aanleggen). Dit heeft tot gevolg dat een celbank minder donaties nodig heeft om te functioneren. Bijgevolg kan men meer investeren in bio-veiligheidstesten en testen op de cellen zelf. Bovendien laten cellen met een hoog en constant proliferatiepotentieel toe strikte en voorspelbare kweekschema s te hanteren waardoor het opzetten van een Cell Storage and Banking System (zie E Cell Storage and Banking System (CSBS)) mogelijk wordt. Dit stroomlijnt het productieproces en verhoogt de kwaliteit en veiligheid van het eindproduct. 9
10 D.4. SEROLOGISCH TESTS VOOR VIRUS- EN SYFILISVEILIGHEID N / D.4.2. Minimale vereisten inzake serologische testen D Allogene donatie D Levende donoren In bepaalde gevallen (bepaalde cellentypes en/of acceptoren) wordt het bronmateriaal bij voorkeur verkregen bij donoren met een negatieve CMV test. Bij neonatale donoren kunnen de biologische testen worden uitgevoerd op de moeder van de donor (binnen de 7 dagen na geboorte en minstens 6 maanden later) om uit medisch oogpunt onnodige testen op de pasgeborene te vermijden. D.4.4. Leeftijdsgrenzen Overleden donoren: geen leeftijdsgrenzen. Levende donoren: geen leeftijdsgrenzen. D.5. PRELEVATIE D.5.2. Prelevatie bij levende donoren Om een maximale kwaliteit van het gepreleveerde weefsel en dus ook van de te isoleren cellen te verzekeren moet een desinfecterend procédé bestaan, op voorwaarde dat data de nazorg van de levende donor niet beïnvloedt. 10
11 D.6. VERPAKKING EN TRANSPORT NAAR DE WEEFSEL- EN CELBANK N / D.6.2. Transport D Transportmodaliteiten van gepreleveerd menselijk materiaal Uitgenomen weefsel moet worden vervoerd in een geschikt transportmedium. Dit transportmedium kan eventueel één of meerdere antibiotica bevatten zodat onmiddellijk na de prelevatie een microbiële inactivatie gestart wordt. Bij de keuze van een transportmedium, de antibiotica en de temperatuur waarbij de cellen getransporteerd wordt, dient men een aanvaardbaar compromis te vinden tussen het verlies aan viabiliteit (de viabiliteit van de primaire cellen is cruciaal) en de efficiëntie van de decontaminatie. Het transport dient gevalideerd te zijn. Indien een microbiële inactivatie wordt toegepast, wordt de procedure gespecificeerd (in de standaardpraktijkvoorschriften van de celbank), gedocumenteerd, gevalideerd en aan de transplanterende arts meegedeeld. 11
12 SECTIE E: BEWERKING, BEWAREN EN OPSLAG VAN WEEFSELS EN CELLEN N / E.1. BEWERKING VAN WEEFSELS EN CELLEN E.1.1. Algemeen Alle manipulaties en bewerkingen van het bronweefsel en de cellen gebeuren in een omgeving zoals beschreven in punt B van dit document. De essentiële bewerkingsprocedures zijn gevalideerd en mogen het eindproduct niet klinisch onwerkzaam of schadelijk voor de ontvanger maken en worden regelmatig opnieuw geëvalueerd. De incubatie en kweekprocessen gebeuren in gekalibreerde incubatoren of thermische kamers met regulatie (voor zover relevant) van temperatuur, luchtvochtigheid en/of CO 2. Recente wetenschappelijke ontwikkelingen maken dat er steeds nieuwe vormen van klinisch bruikbare alternatieven ontstaan. Het gebruik van bio-compatibele dragers, cel encapsulatietechnologie en bio-compatibele componenten kan aanleiding geven tot klinisch bruikbare greffen. E.1.2. Bewerkingsprocedures E Procedures voor celcultuur Deze procedures moeten zo ontworpen zijn dat ze een optimale groei, manipulatie en behoud van integriteit en functie van de cellen verzekeren. Deze procedures moeten in detail gedocumenteerd en bewijsbaar gevolgd worden. Het risico op transmissie van infectieuze ziekten en de methodes om dit risico te beperken zijn afhankelijk van het type bronmateriaal. Men dient echter ook rekening te houden met een mogelijke contaminatie door de operatoren of via de materialen en reagentia gebruikt in het productieproces. Microbiële controles zijn van primordiaal belang. Op welbepaalde stadia in het productieproces dient men controles op de aanwezigheid van bacteriën, schimmels en gisten uit te voeren. Voor Master Cell Banken dient men ook controles op de aanwezigheid van mycoplasma s uit te voeren. De consistentie/regelmaat/reproduceerbaarheid van het celcultuurproces moet gedocumenteerd worden. Adequate limietwaarden voor kritieke parameters zoals viabiliteit, celdensiteit/confluentie, population doublings, zuiverheid en cultuurtijden moeten bepaald worden. 12
13 Indien verschillende cellulaire producten, afkomstig van verschillende donors, gepreleveerd, behandeld en bewaard worden in dezelfde celbank, dan moeten adequate controles uitgevoerd worden zodat de kans op kruisbesmetting (vb.via materialen en reagentia of in de stockage containers) tot een minimum beperkt wordt. E Cellencultuurtijden De belangrijkste eigenschappen van de primaire cellen en hun afgeleiden en de stabiliteit ervan in functie van de cellencultuurtijden moeten gedefinieerd worden. De cultuurcondities (incl. cultuurtijden) moeten geoptimaliseerd worden met de nadruk op het behoud van eigenschappen die belangrijk zijn voor het gewenste klinische gebruik van het eindproduct. E Cell Storage and Banking System (CSBS) Een adequaat gecontroleerd CSBS moet opgezet worden teneinde een degelijke bewaring en levering van cellen te verzekeren zonder enige wijziging in de eigenschappen van het eindproduct. Indien mogelijk, kan men ook een zogenaamde Master Cell Bank (MCB) en Working Cell Bank (WCB) aanleggen door stapsgewijs op te schalen en de celsuspensies in te vriezen. Dit laatste is aan te raden om verschillende redenen: ten eerste voor een optimaal (maximaal) gebruik van de gedoneerde cellen, ten tweede om de donorcellen te kunnen onderwerpen aan uitgebreide bioveiligheids- en kwaliteitstesten en tenslotte om consistente producties te kunnen verzekeren uitgaande van steeds hetzelfde startmateriaal. De MCB en WCB celpopulaties moeten gekarakteriseerd worden (relevante eigenschappen) en gecertificeerd vrij zijn van endogene en exogene contaminanten (bacteriën, schimmels, gisten, virussen en mycoplasma s). Deze cellen moeten bewaard worden onder gecontroleerde en optimale omstandigheden, zodat viabiliteit, densiteit, zuiverheid, steriliteit en activiteit verzekerd zijn. 13
14 E Decontaminatie van weefsels en cellen N / Bij het bewerken van bronmateriaal en het isoleren en kweken van de cellen kan men antibiotica aan de gebruikte media toevoegen. Er dient echter gestreefd te worden naar een antibiotica-vrije cellenkweek na de primaire cultuur of ten laatste na de MCB, indien van toepassing. De eventueel gebruikte decontaminatieprocedures dienen gespecificeerd (in de standaardpraktijkvoorschriften van de celbank), gedocumenteerd, gevalideerd en aan de transplanterende arts meegedeeld te worden. E Sterilisatie van cellen Voor cellen is er doorgaans geen extra sterilisatie mogelijk aangezien dit de viabiliteit van de cellen drastisch zou verlagen. Derhalve moeten in dat geval alle handelingen op aseptische wijze gebeuren en zullen er ook tijdens de bereidingen in-process controles noodzakelijk zijn die aantonen dat de cellensuspensies en greffen vrij zijn van microbiologische contaminatie. Indien de viabiliteit niet noodzakelijk is voor het beoogde klinisch gebruik van de cellen kan men ze steriliseren (vb.bestraling van gelyofiliseerde cellen). E Inactivatie ten opzichte van prionen Specifieke inactivatie ten opzichte van prionen is aanbevolen indien mogelijk. In de andere gevallen dienen alle gebruikte producten die een risico inhouden vergezeld te zijn van de nodige certificaten die dit risico tot een minimum herleiden E.1.3. Bewerkingsmedia en bijkomende therapeutische producten E Materialen en reagentia gebruikt in het productieproces E Algemeen Verschillende materialen en reagentia kunnen nodig zijn in het productieproces van cellen, zoals enzymen, sera, antibiotica en vaste structuren. Contact van de cellen met deze materialen en reagentia kan de kwaliteit, veiligheid en efficiëntie van het eindproduct compromitteren. Bijgevolg moet elk van deze gebruikte substanties duidelijk gedefinieerd zijn en moet er geëvalueerd worden of ze geschikt zijn voor het vooropgestelde gebruik. De materialen en methodes gebruikt in de prelevatie, isolatie, selectie en manipulatie van de cellen moeten in detail beschreven worden. De steriliteit, afwezigheid van contaminerende agenten en een voldoende laag endotoxinegehalte moeten verzekerd worden voor de betrokken materialen en reagentia. Dit geldt ook voor de materialen die dienst doen als drager voor de adhesie en groei van de cellen. 14
15 De kwaliteit van de cultuurmedia en de additieven (groeifactoren, trypsine, antibiotica, cytokines, sera, ) moet gedocumenteerd worden. Hierbij moet men vooral letten op volgende punten: - identiteit (afkomst); - zuiverheid; - steriliteit; - biologische activiteit; - afwezigheid van schadelijke of overbodige agenten. Indien het productieproces van de cellen geen strikte zuiverings- of virus inactivatie- of wasstappen bevat, dan dient men zeer strenge criteria te hanteren voor de materialen en reagentia van dierlijke of menselijke oorsprong. Kopieën van de relevante analysecertificaten van alle materialen en reagentia gebruikt in het productieproces van de cellen moeten voorhanden zijn. Van alle materialen en reagentia moeten volgende punten gedocumenteerd worden: - eindconcentratie van de component; - verkoper/verdeler; - bron; - land van herkomst (voor dierlijke componenten); - kwaliteit; - analysecertificaten. Het gebruik van materialen en reagentia van dierlijke of menselijke oorsprong moet zoveel mogelijk vermeden worden. Indien er op het ogenblik van applicatie restanten van schadelijke producten aanwezig zijn in de cellen (vb. DMSO afkomstig van het cryopreservatiemedium), dan dient men de maximaal toelaatbare hoeveelheid cellen per tijdseenheid te bepalen die men bij een patiënt mag aanbrengen. 15
16 E Materialen en reagentia van menselijke oorsprong Materialen en reagentia van menselijke oorsprong die een optimale groei van de cellen N / verzekeren (albumine, serum, immunoglobulines, ), moeten geëvalueerd worden volgens de criteria die van toepassing zijn op plasmaderivaten. De nodige maatregelen moeten genomen worden zodat het risico van transmissie van spongiforme encefalopathieën tot een minimum herleid wordt. Autoloog serum kan in sommige gevallen een oplossing bieden. E Materialen en reagentia van dierlijke oorsprong Vermits materialen en reagentia van dierlijke oorsprong die gebruikt worden in productieprocessen infectieuse agenten kunnen bevatten en ongewenste reacties in de ontvanger van het eindproduct kunnen veroorzaken, dient men zulke additieven te vermijden en te vervangen door gedefinieerde niet-dierlijke componenten indien beschikbaar. Cellen die toch in contact komen met boviene en/of porciene componenten moeten getest worden op de aanwezigheid van boviene en/of porciene infectieuse of schadelijke agenten. Voor porciene substanties moet gedocumenteerd worden dat ze vrij zijn van porcien parvovirus. Boviene substanties moeten beschikken over de noodzakelijke certificaten die aantonen dat het risico van TSE tot een minimum herleid werd. Het gebruik van volledig gedefinieerde media en zoveel mogelijk hulpmiddelen die vrij zijn van dierlijke componenten vermijdt de mogelijke transmissie van gekende en ongekende infectieuze agentia en verhoogt bijgevolg de bio-veiligheid van de greffen. Ook hier kan autoloog serum in sommige gevallen een oplossing bieden. E.1.5. Controle op weefsels en cellen tijdens hun bewerking Tijdens de bewerking van het weefsel zullen een aantal parameters geëvalueerd worden om de kwaliteit van de cellen tijdens de bewerking te beoordelen. Zo zal de opbrengst aan primaire cellen en hun viabiliteit en morfologie bepaald worden. Tijdens het opschalingsproces van de cellen dient het totale aantal behaalde cellen per passage en hun viabiliteit en morfologie bepaald te worden. 16
17 E.1.6. Maximale wachttijd voor de bewerking en het bewaren N / Het gepreleveerde weefsel dient binnen de 24 uren na de prelevatie op de celbank toe te komen. Na ontvangst van het weefsel op de celbank dient er binnen de 24 uren begonnen te worden met de bewerking van het weefsel. In afwachting van de bewerking wordt het weefsel bewaard bij 2 8 C in een geschikt fysiologisch medium met voldoende buffercapaciteit. E.2. BEWARING EN OPSLAG VAN WEEFSELS EN CELLEN E.2.2. Bewaar- en opslagprocedures Afhankelijk van het cellentype, de klinische toepassing en de vooropgestelde kwaliteit kunnen cellen op een aantal manieren bewaard worden. Cryopreservatie in vloeibare stikstof is de meest gebruikelijke methode. Elk bewaar- en opslagproces dient gespecificeerd (in de standaardpraktijkvoorschriften van de celbank), gedocumenteerd en gevalideerd te zijn. Voor elke bewaarconditie wordt een maximale bewaartijd gespecificeerd. Hierbij wordt onder andere rekening gehouden met een eventuele achteruitgang van de vereiste eigenschappen van de cellen. Deze maximale bewaartijd moet gedocumenteerd en gevalideerd zijn en aan de transplanterende arts meegedeeld worden. Volgende bewaar- en opslagprocessen zijn aanvaardbaar voor cellulaire greffen: E Bewaring bij +37 C Methode voor het bewaren van cellen gedurende korte periodes (dagen tot weken). Een geschikt preservatiemedium met nutriënten en een voldoende bufferend vermogen is aangeraden. E Bewaring en opslag bij +4 C Methode voor het bewaren van cellen gedurende korte periodes ( 4 dagen). Bewaring gedurende langere periode dient gevalideerd worden. Een geschikt preservatiemedium met nutriënten en een voldoende bufferend vermogen is aangeraden. 17
18 E Cryopreservatie bij -80 C Methode voor het bewaren van cellen gedurende middenlange periodes (6 maanden). Bewaring gedurende langere periode dient gevalideerd worden. Een gevalideerde invriesprocedure is aangeraden. E Cryopreservatie in vloeibare stikstof Methode bij uitstek voor het bewaren van cellen, gedurende langere periodes (5 jaren). Bewaring gedurende langere periode dient gevalideerd worden. Een gevalideerde invriesprocedure is aangeraden. De cellen worden doorgaans in de stikstofdampen bewaard bij een temperatuur lager dan -120 C. E Lyofilisatie en dehydratatie Methode voor het bewaren van cellen. Gelyofiliseerde cellen kunnen bij kamertemperatuur (+20 C +25 C) bewaard worden. E Bewaring bij kamertemperatuur (+20 C +25 C) Methode voor het bewaren van cellen gedurende korte periodes (dagen tot weken). Een geschikt preservatiemedium met nutriënten en een voldoende bufferend vermogen is aangeraden. 18
19 SECTIE F: SECURISATIE VAN WEEFSELS EN CELLEN F.1. MICROBIOLOGISCHE VEILIGHEID VAN WEEFSELS EN CELLEN F.1.2. Bacteriologische en mycologische controles Bacteriologische en mycologische controles dienen uitgevoerd te worden volgens gerechtvaardigde methoden aangepast aan het celtype of volgens de Europese Pharmacopoeia (EP5). Een bijkomende gevalideerde test voor de opsporing van mycoplasma s is aangeraden in het geval van expansie op een lange termijn. Indien antibiotica gebruikt werden in het productieproces, dan dient men deze te verwijderen vóór de bacteriologische en mycologische controles. 19
20 SECTIE H: DISTRIBUTIE, IN- EN UITVOER VAN WEEFSELS EN CELLEN H.1. DISTRIBUTIE VAN WEEFSELS EN CELLEN H.1.2. Transport van weefsels en cellen H Voorwaarden voor het transport van weefsels en cellen Cellen kunnen, afhankelijk van de bewaarmethode, op verschillende manieren naar derden getransporteerd worden. Belangrijk is dat de transportcondities (vb. temperatuur en maximale duur) de vereiste eigenschappen van de cellen behouden, beschreven worden in de standaardpraktijkvoorschriften van de celbank en gevalideerd zijn. Het vervoer van gecryopreserveerde cellen gebeurt doorgaans op droog ijs bij -80 C in een geschikte recipiënt. De koude keten mag op geen enkel ogenblik onderbroken worden. Bij aankomst dienen de cellen voor onmiddellijk gebruik verder ontdooid te worden volgens de aangewezen procedure of in een diepvries bij -80 C geplaatst te worden voor uitgesteld gebruik. Gelyofiliseerde cellen kunnen bij kamertemperatuur vervoerd worden. H.3. TERUGROEPING EN TERUGKEER VAN CELLEN H.3.2. Terugkeer van (niet gebruikte) cellen Terugkeer van (niet-gebruikte) cellen voor destructie wordt aanbevolen Heropname van (niet-gebruikte) cellen in de bank moet door een procedure geregeld worden om de kwaliteit en de veiligheid van de cellen te verzekeren. 20
21 3. SAMENSTELLING VAN DE WERKGROEP Al de deskundigen hebben op persoonlijke titel aan de werkgroep deelgenomen. De namen van de leden en de deskundigen van de HGR worden met een asterisk * aangeduid. De volgende deskundigen hebben hun medewerking verleend bij het opstellen van de kwaliteitsnormen: ANGENON Elyane BAUDOUX Etienne BEELE Hilde* BONTEZ Walter BOUTSEN-ECTORS Nadine* CORNU Olivier DELLOYE Christian* GUNS Johan LISMONT Daniel MUYLLE Ludo* PIRNAY Jean-Paul VAN GEYT Caroline VAN STEIRTEGHEM André VANDERKELEN Alain* VERBEKEN Gilbert (verpleegkunde, coördinatie van transplantatie ULB) (geneeskunde, celtherapie ULg) (geneeskunde, dermatologie UZ Gent) (volksgezondheid FAGG coördinatie bloed, weefsels en cellen) (geneeskunde, pathologische anatomie KUL) (geneeskunde, orthopedische chirurgie UCL) (geneeskunde, orthopedische chirurgie UCL) (medisch-sociale wetenschappen UZ Brussel) (verslaggever) (verpleegkunde KUL) (geneeskunde, klinische biologie FAGG Vigilantie UA) (medische wetenschappen LabMCT HCB-KA) (verslaggever) (medisch-sociale wetenschappen UZ Gent) (geneeskunde, voortplantingsgeneeskunde VUB) (geneeskunde, algemene chirurgie EHB) (biologie, QA/QC/RA LabMCT HCB-KA) (verslaggever) Het voorzitterschap werd verzekerd door VANDERKELEN Alain en het wetenschappelijk secretariaat door BALTES Muriel. 21
PUBLICATIE VAN DE HOGE GEZONDHEIDSRAAD nr. 8298
 PUBLICATIE VAN DE HOGE GEZONDHEIDSRAAD nr. 8298 Specifieke kwaliteitsnormen voor tympano-ossiculaire allogreffen van menselijke oorsprong die voor toepassing op de mens bestemd zijn Herziene versie 6 augustus
PUBLICATIE VAN DE HOGE GEZONDHEIDSRAAD nr. 8298 Specifieke kwaliteitsnormen voor tympano-ossiculaire allogreffen van menselijke oorsprong die voor toepassing op de mens bestemd zijn Herziene versie 6 augustus
KWALITEITSNORMEN VOOR ALLOGREFFEN VAN AMNIONMEMBRAAN. Herziene versie 2000
 KWALITEITSNORMEN VOOR ALLOGREFFEN VAN AMNIONMEMBRAAN Herziene versie 2000 Ministerie van Sociale Zaken, Volksgezondheid en Leefmilieu Hoge Gezondheidsraad Adres: Esplanadegebouw 718 R.A.C. Pachecolaan
KWALITEITSNORMEN VOOR ALLOGREFFEN VAN AMNIONMEMBRAAN Herziene versie 2000 Ministerie van Sociale Zaken, Volksgezondheid en Leefmilieu Hoge Gezondheidsraad Adres: Esplanadegebouw 718 R.A.C. Pachecolaan
PUBLICATIE VAN DE HOGE GEZONDHEIDSRAAD nr. 8296
 PUBLICATIE VAN DE HOGE GEZONDHEIDSRAAD nr. 8296 Specifieke kwaliteitsnormen voor huidallogreffen van menselijke oorsprong die voor toepassing op de mens bestemd zijn Herziene versie 2007 4 juli 2007 SAMENVATTING
PUBLICATIE VAN DE HOGE GEZONDHEIDSRAAD nr. 8296 Specifieke kwaliteitsnormen voor huidallogreffen van menselijke oorsprong die voor toepassing op de mens bestemd zijn Herziene versie 2007 4 juli 2007 SAMENVATTING
PUBLICATIE VAN DE HOGE GEZONDHEIDSRAAD Nr. 8295
 PUBLICATIE VAN DE HOGE GEZONDHEIDSRAAD Nr. 8295 Specifieke kwaliteitsnormen voor hartklep-allogreffen van menselijke oorsprong die voor toepassing op de mens bestemd zijn Herziening 2007 6 juni 2007 SAMENVATTING
PUBLICATIE VAN DE HOGE GEZONDHEIDSRAAD Nr. 8295 Specifieke kwaliteitsnormen voor hartklep-allogreffen van menselijke oorsprong die voor toepassing op de mens bestemd zijn Herziening 2007 6 juni 2007 SAMENVATTING
PUBLICATIE VAN DE HOGE GEZONDHEIDSRAAD nr. 8293
 PUBLICATIE VAN DE HOGE GEZONDHEIDSRAAD nr. 8293 Specifieke kwaliteitsnormen voor hoornvliesallogreffen en scleragreffen van menselijke oorsprong die voor toepassing op de mens bestemd zijn Herziene versie
PUBLICATIE VAN DE HOGE GEZONDHEIDSRAAD nr. 8293 Specifieke kwaliteitsnormen voor hoornvliesallogreffen en scleragreffen van menselijke oorsprong die voor toepassing op de mens bestemd zijn Herziene versie
KWALITEITSNORMEN VOOR DENTALE ALLOGREFFEN. Herziene versie Ministerie van Sociale Zaken, Volksgezondheid en Leefmilieu Hoge Gezondheidsraad
 KWALITEITSNORMEN VOOR DENTALE ALLOGREFFEN Herziene versie 2000 Ministerie van Sociale Zaken, Volksgezondheid en Leefmilieu Hoge Gezondheidsraad Adres: Esplanadegebouw 718 R.A.C. Pachecolaan 19 Bus 5 B-1010
KWALITEITSNORMEN VOOR DENTALE ALLOGREFFEN Herziene versie 2000 Ministerie van Sociale Zaken, Volksgezondheid en Leefmilieu Hoge Gezondheidsraad Adres: Esplanadegebouw 718 R.A.C. Pachecolaan 19 Bus 5 B-1010
PUBLICATIE VAN DE HOGE GEZONDHEIDSRAAD nr. 8317
 PUBLICATIE VAN DE HOGE GEZONDHEIDSRAAD nr. 8317 Specifieke kwaliteitsnormen voor vaatallogreffen van menselijke oorsprong die voor toepassing op de mens bestemd zijn Herziening 2007 7 november 2007 SAMENVATTING
PUBLICATIE VAN DE HOGE GEZONDHEIDSRAAD nr. 8317 Specifieke kwaliteitsnormen voor vaatallogreffen van menselijke oorsprong die voor toepassing op de mens bestemd zijn Herziening 2007 7 november 2007 SAMENVATTING
KWALITEITSNORMEN VOOR ALLOGREFFEN VAN HET LOCOMOTORISCH STELSEL. Herziene versie 2000
 KWALITEITSNORMEN VOOR ALLOGREFFEN VAN HET LOCOMOTORISCH STELSEL Herziene versie 2000 Ministerie van Sociale Zaken, Volksgezondheid en Leefmilieu Hoge Gezondheidsraad Adres: Esplanadegebouw 718 R.A.C. Pachecolaan
KWALITEITSNORMEN VOOR ALLOGREFFEN VAN HET LOCOMOTORISCH STELSEL Herziene versie 2000 Ministerie van Sociale Zaken, Volksgezondheid en Leefmilieu Hoge Gezondheidsraad Adres: Esplanadegebouw 718 R.A.C. Pachecolaan
5()(5(17,('266,(5 $ $OJHPHHQ
 )2508/,(50(7$$198//(1'(95$*(17(1%(+2(9(9$1'(3$57,-*(:,-=(95,-*,)7( 9$121*(5(*,675((5'(,00812/2*,6&+()$50$&(87,6&+(352'8&7(1&+(0,6&+( )$50$&(87,6&+('$7$ Met behulp van dit formulier kan aanvullende en meer
)2508/,(50(7$$198//(1'(95$*(17(1%(+2(9(9$1'(3$57,-*(:,-=(95,-*,)7( 9$121*(5(*,675((5'(,00812/2*,6&+()$50$&(87,6&+(352'8&7(1&+(0,6&+( )$50$&(87,6&+('$7$ Met behulp van dit formulier kan aanvullende en meer
ADVIES VAN DE HOGE GEZONDHEIDSRAAD nr. 8916
 ADVIES VAN DE HOGE GEZONDHEIDSRAAD nr. 8916 Omzetting in de Belgische wetgeving van richtlijn 2012/39/EU wat betreft bepaalde technische voorschriften voor het testen van menselijke weefsels en cellen
ADVIES VAN DE HOGE GEZONDHEIDSRAAD nr. 8916 Omzetting in de Belgische wetgeving van richtlijn 2012/39/EU wat betreft bepaalde technische voorschriften voor het testen van menselijke weefsels en cellen
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten (FAGG)
 Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten (FAGG) Wet van 19 december 2008 inzake het verkrijgen en het gebruik van menselijk lichaamsmateriaal met het oog op de geneeskundige toepassing
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten (FAGG) Wet van 19 december 2008 inzake het verkrijgen en het gebruik van menselijk lichaamsmateriaal met het oog op de geneeskundige toepassing
Weefselbanking. Kwaliteitsbeheer & donorselectie. Glorieux Sarah, PhD, ir. Matthys Conny, Dr. 07 november Universitair Ziekenhuis Gent 1
 Weefselbanking Kwaliteitsbeheer & donorselectie Glorieux Sarah, PhD, ir. Matthys Conny, Dr. 07 november 2016 1 Bank voor menselijk lichaamsmateriaal Definities uit 19 december 2008 - Wet inzake het verkrijgen
Weefselbanking Kwaliteitsbeheer & donorselectie Glorieux Sarah, PhD, ir. Matthys Conny, Dr. 07 november 2016 1 Bank voor menselijk lichaamsmateriaal Definities uit 19 december 2008 - Wet inzake het verkrijgen
KWALITEITSNORMEN VOOR ALLOGREFFEN VAN NAVELSTRENGBLOED (placentair bloed) H.G.R. : 7970
 KWALITEITSNORMEN VOOR ALLOGREFFEN VAN NAVELSTRENGBLOED (placentair bloed) H.G.R. : 7970 30 september 2003 Federale Overheidsdienst Volksgezondheid, Veiligheid van de Voedselketen en Leefmilieu Hoge Gezondheidsraad
KWALITEITSNORMEN VOOR ALLOGREFFEN VAN NAVELSTRENGBLOED (placentair bloed) H.G.R. : 7970 30 september 2003 Federale Overheidsdienst Volksgezondheid, Veiligheid van de Voedselketen en Leefmilieu Hoge Gezondheidsraad
Veel gestelde vragen Menselijk lichaamsmateriaal Laatst bijgewerkt op 28 februari 2010
 Veel gestelde vragen Menselijk lichaamsmateriaal Laatst bijgewerkt op 28 februari 2010 1 De wegneming van menselijk lichaamsmateriaal wordt bijgehouden in een register van het operatiekwartier. Mogen de
Veel gestelde vragen Menselijk lichaamsmateriaal Laatst bijgewerkt op 28 februari 2010 1 De wegneming van menselijk lichaamsmateriaal wordt bijgehouden in een register van het operatiekwartier. Mogen de
Weefselprelevatie, banking en transplantatie: Cornea. Hilde Beele. Weefselbank UZ Gent Universitair Ziekenhuis Gent. Cornea als deel van het oog
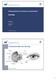 Weefselprelevatie, banking en transplantatie: Cornea Hilde Beele Weefselbank UZ Gent 1 Cornea als deel van het oog 2 2 1 cornea heldere cornea is nodig voor transmissie van licht en visuele perceptie endotheelcellen:
Weefselprelevatie, banking en transplantatie: Cornea Hilde Beele Weefselbank UZ Gent 1 Cornea als deel van het oog 2 2 1 cornea heldere cornea is nodig voor transmissie van licht en visuele perceptie endotheelcellen:
Wij Beatrix, bij de gratie Gods, Koningin der Nederlanden, Prinses van Oranje-Nassau, enz. enz. enz.
 (Tekst geldend op: 11-02-2013) Wet van 6 februari 2003, houdende regels inzake de veiligheid en kwaliteit van lichaamsmateriaal dat kan worden gebruikt bij een geneeskundige behandeling (Wet veiligheid
(Tekst geldend op: 11-02-2013) Wet van 6 februari 2003, houdende regels inzake de veiligheid en kwaliteit van lichaamsmateriaal dat kan worden gebruikt bij een geneeskundige behandeling (Wet veiligheid
FOD VOLKSGEZONDHEID, VEILIGHEID VAN DE VOEDSELKETEN EN LEEFMILIEU BRUSSEL, 09/04/2009
 FOD VOLKSGEZONDHEID, VEILIGHEID VAN DE VOEDSELKETEN EN LEEFMILIEU BRUSSEL, 09/04/2009 Directoraat-generaal Organisatie gezondheidszorgvoorzieningen --- NATIONALE RAAD VOOR ZIEKEN- HUISVOORZIENINGEN. ---
FOD VOLKSGEZONDHEID, VEILIGHEID VAN DE VOEDSELKETEN EN LEEFMILIEU BRUSSEL, 09/04/2009 Directoraat-generaal Organisatie gezondheidszorgvoorzieningen --- NATIONALE RAAD VOOR ZIEKEN- HUISVOORZIENINGEN. ---
De Patienten zijn ons dankbaar!
 De Patienten zijn ons dankbaar! Outline Weefselbanken in UZ Leuven Functie van clean rooms binnen weefselbanken Toepassing Technisch Personeel Materiaal Product Monitoring van clean rooms Besluit Weefselbanken
De Patienten zijn ons dankbaar! Outline Weefselbanken in UZ Leuven Functie van clean rooms binnen weefselbanken Toepassing Technisch Personeel Materiaal Product Monitoring van clean rooms Besluit Weefselbanken
Erkenningsvoorwaarden voor embryoteams en embryoproductieteams voor paarden VANAF 01/09/2010
 Erkenningsvoorwaarden voor embryoteams en embryoproductieteams voor paarden VANAF 01/09/2010 Bijlage II.9.3 bij het koninklijk besluit van 16 januari 2006 tot vaststelling van de nadere regels van de erkenningen,
Erkenningsvoorwaarden voor embryoteams en embryoproductieteams voor paarden VANAF 01/09/2010 Bijlage II.9.3 bij het koninklijk besluit van 16 januari 2006 tot vaststelling van de nadere regels van de erkenningen,
Inhoudstafel per onderwerp volume 2 experimenten op de mens en menselijk lichaamsmateriaal
 Inhoudstafel per onderwerp volume 2 experimenten op de mens en menselijk lichaamsmateriaal Pharma Codex Deel I vol. 2 vii Voor de bijlagen bij de omzendbrieven en de nota s, raadpleeg de website van het
Inhoudstafel per onderwerp volume 2 experimenten op de mens en menselijk lichaamsmateriaal Pharma Codex Deel I vol. 2 vii Voor de bijlagen bij de omzendbrieven en de nota s, raadpleeg de website van het
Toelatingsvoorwaarden voor opslagbedrijven voor producten afkomstig van categorie 2- en 3 materiaal
 Toelatingsvoorwaarden voor opslagbedrijven voor producten afkomstig van categorie 2- en 3 materiaal Bijlage III.7.1. bij het koninklijk besluit van 16 januari 2006 tot vaststelling van de nadere regels
Toelatingsvoorwaarden voor opslagbedrijven voor producten afkomstig van categorie 2- en 3 materiaal Bijlage III.7.1. bij het koninklijk besluit van 16 januari 2006 tot vaststelling van de nadere regels
Nieuwe wetgeving ten aanzien van orgaanvigilantie
 Nieuwe wetgeving ten aanzien van orgaanvigilantie 4e Symposium Weefselvigilantie, woensdag 30 november 2011 Hilga Katerberg Stafarts Orgaancentrum Inhoud Inleiding Wetgeving Definities Verantwoordelijkheden
Nieuwe wetgeving ten aanzien van orgaanvigilantie 4e Symposium Weefselvigilantie, woensdag 30 november 2011 Hilga Katerberg Stafarts Orgaancentrum Inhoud Inleiding Wetgeving Definities Verantwoordelijkheden
Weefseltransplantatie
 Weefseltransplantatie Hilde Beele 07/11/2016 2008 Universitair Ziekenhuis Gent 1 Do not take your organs to heaven Heaven knows we need them here 2 2 Do not take your tissues and cells to heaven Heaven
Weefseltransplantatie Hilde Beele 07/11/2016 2008 Universitair Ziekenhuis Gent 1 Do not take your organs to heaven Heaven knows we need them here 2 2 Do not take your tissues and cells to heaven Heaven
Wet veiligheid en kwaliteit lichaamsmateriaal. Meldingen
 Wet veiligheid en kwaliteit lichaamsmateriaal & Meldingen Jeroen van Baare, inspecteur IGZ, Bloed & Weefsels Programma 8 Geneesmiddelen en Medische Technologie TRIP Minisymposium Weefselvigilantie 10 juni
Wet veiligheid en kwaliteit lichaamsmateriaal & Meldingen Jeroen van Baare, inspecteur IGZ, Bloed & Weefsels Programma 8 Geneesmiddelen en Medische Technologie TRIP Minisymposium Weefselvigilantie 10 juni
Regelgeving inzake lichaamsmateriaal
 Regelgeving inzake lichaamsmateriaal Wegwijs in de wetgeving 1 Marie Claire de Vries Inhoud 1. VWS en medische producten 2. Wetgeving inzake lichaamsmateriaal 2 VWS en medische producten. Voorzien in de
Regelgeving inzake lichaamsmateriaal Wegwijs in de wetgeving 1 Marie Claire de Vries Inhoud 1. VWS en medische producten 2. Wetgeving inzake lichaamsmateriaal 2 VWS en medische producten. Voorzien in de
Prettige feestdagen. Meilleurs voeux. Season s greetings. December 12 TITEL
 TITEL 2013 Prettige feestdagen Meilleurs voeux Season s greetings Tervurenlaan 40 1040 Brussel Tel. 02/743.09.11 Fax 02/733.98.07 www.callens-law.be December 12 De functie Lokale donorcoördinatie Verschillende
TITEL 2013 Prettige feestdagen Meilleurs voeux Season s greetings Tervurenlaan 40 1040 Brussel Tel. 02/743.09.11 Fax 02/733.98.07 www.callens-law.be December 12 De functie Lokale donorcoördinatie Verschillende
15 FEBRUARI Koninklijk besluit houdende. vaststelling van de normen. waaraan de zorgprogramma's. reproductieve geneeskunde
 15 FEBRUARI 1999. - Koninklijk besluit houdende vaststelling van de normen waaraan de zorgprogramma's reproductieve geneeskunde moeten voldoen om erkend te worden. BS 25/03/1999 in voege 01/06/1999 Gewijzigd
15 FEBRUARI 1999. - Koninklijk besluit houdende vaststelling van de normen waaraan de zorgprogramma's reproductieve geneeskunde moeten voldoen om erkend te worden. BS 25/03/1999 in voege 01/06/1999 Gewijzigd
Coordinatie--Organen--Transplanteren--Bewaren-Bereiden-Vervoeren-Distribueren--KB doc
 23 DECEMBER 2002. - Koninklijk besluit betreffende het wegnemen, bewaren, bereiden, invoeren, vervoeren, distribueren en afleveren van weefsels van menselijke oorsprong alsook betreffende de banken voor
23 DECEMBER 2002. - Koninklijk besluit betreffende het wegnemen, bewaren, bereiden, invoeren, vervoeren, distribueren en afleveren van weefsels van menselijke oorsprong alsook betreffende de banken voor
BoneAlbumin. Vragen & Antwoorden. humaan allograft
 BoneAlbumin Vragen & Antwoorden humaan allograft BoneAlbumin is een humaan allograft. Wat betekent dat? Wat betekent menselijk bot graft? Bot vervangend materiaal kan zijn: synthetisch, mineraal-basis
BoneAlbumin Vragen & Antwoorden humaan allograft BoneAlbumin is een humaan allograft. Wat betekent dat? Wat betekent menselijk bot graft? Bot vervangend materiaal kan zijn: synthetisch, mineraal-basis
humaan allograft Vragen & Antwoorden
 humaan allograft Vragen & Antwoorden BoneAlbumin is een humaan allograft. Wat betekent dat? Bot vervangend materiaal kan zijn: synthetisch, mineraal-basis een xenograft uit dierlijk weefsel, een allograft
humaan allograft Vragen & Antwoorden BoneAlbumin is een humaan allograft. Wat betekent dat? Bot vervangend materiaal kan zijn: synthetisch, mineraal-basis een xenograft uit dierlijk weefsel, een allograft
Chapter 9. Nederlandse samenvatting
 Chapter 9 Nederlandse samenvatting 150 Samenvatting NEDERLANDSE SAMENVATTING De natuurlijke afweer van het lichaam wordt verzorgd door het immuunsysteem. Zonder immuunsysteem zouden pathogenen zoals virussen
Chapter 9 Nederlandse samenvatting 150 Samenvatting NEDERLANDSE SAMENVATTING De natuurlijke afweer van het lichaam wordt verzorgd door het immuunsysteem. Zonder immuunsysteem zouden pathogenen zoals virussen
BIOVEILIGHEIDSDOSSIER PUBLIEK DOSSIER DEEL 2: INFO ACTIVITEIT. 1. Algemene info
 BIOVEILIGHEIDSDOSSIER PUBLIEK DOSSIER DEEL 2: INFO ACTIVITEIT 1. Algemene info 1.1. Titel en beknopte beschrijving van de activiteit Nummer: Titel:.. Samenvatting van de doelstellingen: Form PUB OP Juli
BIOVEILIGHEIDSDOSSIER PUBLIEK DOSSIER DEEL 2: INFO ACTIVITEIT 1. Algemene info 1.1. Titel en beknopte beschrijving van de activiteit Nummer: Titel:.. Samenvatting van de doelstellingen: Form PUB OP Juli
PRI 2139 Laboratorium schadelijke organismen wetenschappelijke doeleinden [2139] v2
![PRI 2139 Laboratorium schadelijke organismen wetenschappelijke doeleinden [2139] v2 PRI 2139 Laboratorium schadelijke organismen wetenschappelijke doeleinden [2139] v2](/thumbs/95/124471997.jpg) Provinciale dienst van:... Datum:... Verantwoordelijke Controleur:... Nr:... Operator :... N uniek... Adres :...... PRI 219 Laboratorium schadelijke organismen wetenschappelijke doeleinden [219] v2 C :
Provinciale dienst van:... Datum:... Verantwoordelijke Controleur:... Nr:... Operator :... N uniek... Adres :...... PRI 219 Laboratorium schadelijke organismen wetenschappelijke doeleinden [219] v2 C :
Weefseldonatie. Van weefselaanvraag via donormelding tot vrijgave weefsel. Lennard Koster Coördinator Explantatie
 Weefseldonatie Van weefselaanvraag via donormelding tot vrijgave weefsel Lennard Koster Coördinator Explantatie Relatie met directe omgeving TRIP Donorlokatie Wet en Regelgeving BIS Ziekenhuizen / artsen
Weefseldonatie Van weefselaanvraag via donormelding tot vrijgave weefsel Lennard Koster Coördinator Explantatie Relatie met directe omgeving TRIP Donorlokatie Wet en Regelgeving BIS Ziekenhuizen / artsen
Tweede Kamer der Staten-Generaal
 Tweede Kamer der Staten-Generaal 2 Vergaderjaar 2005 2006 30 338 Aanpassing van de Wet veiligheid en kwaliteit lichaamsmateriaal en enkele andere wetten aan richtlijn 2004/23/EG van het Europees Parlement
Tweede Kamer der Staten-Generaal 2 Vergaderjaar 2005 2006 30 338 Aanpassing van de Wet veiligheid en kwaliteit lichaamsmateriaal en enkele andere wetten aan richtlijn 2004/23/EG van het Europees Parlement
Invriezen en bewaren van gameten in zorgprogramma s A
 Overleg A- en B-centra Nazareth, 21/09/2012 Invriezen en bewaren van gameten in zorgprogramma s A Dr. Tom Coetsier Medisch Coördinator zorgprogramma reproductieve geneeskunde Beheerder weefselbank voor
Overleg A- en B-centra Nazareth, 21/09/2012 Invriezen en bewaren van gameten in zorgprogramma s A Dr. Tom Coetsier Medisch Coördinator zorgprogramma reproductieve geneeskunde Beheerder weefselbank voor
PRI 3334 Laboratorium schadelijke organismen - Wetenschappelijke doeleinden - INFRASTRUCTUUR, INRICHTING EN HYGIËNE [3334] v1
![PRI 3334 Laboratorium schadelijke organismen - Wetenschappelijke doeleinden - INFRASTRUCTUUR, INRICHTING EN HYGIËNE [3334] v1 PRI 3334 Laboratorium schadelijke organismen - Wetenschappelijke doeleinden - INFRASTRUCTUUR, INRICHTING EN HYGIËNE [3334] v1](/thumbs/95/124471986.jpg) Provinciale dienst van : Datum : Veranwoordelijke controleur : Nr : Operator : N uniek : Adres : PRI 4 Laboratorium schadelijke organismen - Wetenschappelijke doeleinden - INFRASTRUCTUUR, INRICHTING EN
Provinciale dienst van : Datum : Veranwoordelijke controleur : Nr : Operator : N uniek : Adres : PRI 4 Laboratorium schadelijke organismen - Wetenschappelijke doeleinden - INFRASTRUCTUUR, INRICHTING EN
Gearchiveerd op 02/04/2013
 Provinciale dienst van:... Datum:... Verantwoordelijke Controleur:... Nr:... Operator :... N uniek... Adres :...... DPA 2422 Spermacentrum runderen - nationale handel - Infrastructuur, inrichting en hygiëne
Provinciale dienst van:... Datum:... Verantwoordelijke Controleur:... Nr:... Operator :... N uniek... Adres :...... DPA 2422 Spermacentrum runderen - nationale handel - Infrastructuur, inrichting en hygiëne
TRIP ATMP s en ziekenhuis uitzonderingen. Annie Rietveld Coördinerend/Specialistisch Senior inspecteur
 TRIP ATMP s en ziekenhuis uitzonderingen Annie Rietveld Coördinerend/Specialistisch Senior inspecteur INHOUD PRESENTATIE Wat is een ATMP volgens EU regelgeving? Toepassing in ziekenhuis uitzondering Hoe
TRIP ATMP s en ziekenhuis uitzonderingen Annie Rietveld Coördinerend/Specialistisch Senior inspecteur INHOUD PRESENTATIE Wat is een ATMP volgens EU regelgeving? Toepassing in ziekenhuis uitzondering Hoe
FOD VOLKSGEZONDHEID, VEILIGHEID VAN DE VOEDSELKETEN EN LEEFMILIEU. Federale wetgeving over hemovigilantie
 1 Federale wetgeving over hemovigilantie 2 Wettelijk kader Achtereenvolgens komen aan bod : a) - de Europese wetgeving; b) - het onderscheid ziekenhuisbloedbank - bloedinstelling; c) - de Belgische wetgeving.
1 Federale wetgeving over hemovigilantie 2 Wettelijk kader Achtereenvolgens komen aan bod : a) - de Europese wetgeving; b) - het onderscheid ziekenhuisbloedbank - bloedinstelling; c) - de Belgische wetgeving.
UITVOERINGSRICHTLIJN 2012/25/EU VAN DE COMMISSIE
 10.10.2012 Publicatieblad van de Europese Unie L 275/27 RICHTLIJNEN UITVOERINGSRICHTLIJN 2012/25/EU VAN DE COMMISSIE van 9 oktober 2012 tot vaststelling van informatieprocedures voor de uitwisseling tussen
10.10.2012 Publicatieblad van de Europese Unie L 275/27 RICHTLIJNEN UITVOERINGSRICHTLIJN 2012/25/EU VAN DE COMMISSIE van 9 oktober 2012 tot vaststelling van informatieprocedures voor de uitwisseling tussen
1 Algemene gegevens. 2 Categorie van het project
 1 Algemene gegevens 1.1 Titel van het project Ontwikkelen van een eilandjesbron ten behoeve van transplantatie van geëncapsuleerde eilandjes van Langerhans voor behandeling van diabetes 1.2 Looptijd van
1 Algemene gegevens 1.1 Titel van het project Ontwikkelen van een eilandjesbron ten behoeve van transplantatie van geëncapsuleerde eilandjes van Langerhans voor behandeling van diabetes 1.2 Looptijd van
Aanbevelingen voor sterilisatie
 Aanbevelingen voor sterilisatie W. Accoe UZ Gent Studiedag VSZ 27 oktober 2006 Aanbevelingen voor sterilisatie FOD Volksgezondheid, Veiligheid van de Voedselketen en Leefmilieu Hoge Gezondheidsraad Mei
Aanbevelingen voor sterilisatie W. Accoe UZ Gent Studiedag VSZ 27 oktober 2006 Aanbevelingen voor sterilisatie FOD Volksgezondheid, Veiligheid van de Voedselketen en Leefmilieu Hoge Gezondheidsraad Mei
Gearchiveerd op 01/01/2017
 Provinciale dienst van:... Datum:... Verantwoordelijke Controleur:... Nr:... Operator :... N uniek... Adres :...... TRA 2495 Productie van voeder voor gezelschapsdieren dat categorie materiaal bevat -
Provinciale dienst van:... Datum:... Verantwoordelijke Controleur:... Nr:... Operator :... N uniek... Adres :...... TRA 2495 Productie van voeder voor gezelschapsdieren dat categorie materiaal bevat -
Hartkleppen en vaten Veiligheid, traceerbaarheid en risicomomenten
 Hartkleppen en vaten Veiligheid, traceerbaarheid en risicomomenten Jos Bekkers, Cardio-thoracaal chirurg Antoon van den Bogaerdt, Erasmus MC Hartkleppen pulmonaalklep aortaklep tricuspidalis mitralis Veiligheid,
Hartkleppen en vaten Veiligheid, traceerbaarheid en risicomomenten Jos Bekkers, Cardio-thoracaal chirurg Antoon van den Bogaerdt, Erasmus MC Hartkleppen pulmonaalklep aortaklep tricuspidalis mitralis Veiligheid,
TRA 3047 Uitsnijden, uitbenen en (opnieuw) onmiddellijk verpakken van vers vlees - TRACEERBAARHEID [3047] v1
![TRA 3047 Uitsnijden, uitbenen en (opnieuw) onmiddellijk verpakken van vers vlees - TRACEERBAARHEID [3047] v1 TRA 3047 Uitsnijden, uitbenen en (opnieuw) onmiddellijk verpakken van vers vlees - TRACEERBAARHEID [3047] v1](/thumbs/93/112202102.jpg) Provinciale dienst van : Datum : Veranwoordelijke controleur : Nr : Operator : N uniek : Adres : TRA 047 Uitsnijden, uitbenen en (opnieuw) onmiddellijk verpakken van vers vlees - TRACEERBAARHEID [047]
Provinciale dienst van : Datum : Veranwoordelijke controleur : Nr : Operator : N uniek : Adres : TRA 047 Uitsnijden, uitbenen en (opnieuw) onmiddellijk verpakken van vers vlees - TRACEERBAARHEID [047]
TRA 3132 petfoodfabrikant - DIERLIJKE BIJPRODUCTEN NHC [3132] v1
![TRA 3132 petfoodfabrikant - DIERLIJKE BIJPRODUCTEN NHC [3132] v1 TRA 3132 petfoodfabrikant - DIERLIJKE BIJPRODUCTEN NHC [3132] v1](/thumbs/97/134338207.jpg) Provinciale dienst van : Datum : Veranwoordelijke controleur : Nr : Operator : N uniek : Adres : TRA 2 petfoodfabrikant - DIERLIJKE BIJPRODUCTEN NHC [2] v C: conform NC: Niet-conform NA: niet van toepassing
Provinciale dienst van : Datum : Veranwoordelijke controleur : Nr : Operator : N uniek : Adres : TRA 2 petfoodfabrikant - DIERLIJKE BIJPRODUCTEN NHC [2] v C: conform NC: Niet-conform NA: niet van toepassing
HOOFDSTUK I. - Definities. Toepassingsgebied. Afdeling 1. - Omzetting en definities
 28 SEPTEMBER 2009. - Koninklijk besluit tot vaststelling van de kwaliteits- en veiligheidsnormen voor het doneren, wegnemen, verkrijgen, testen, bewerken, bewaren en distribueren van menselijk lichaamsmateriaal,
28 SEPTEMBER 2009. - Koninklijk besluit tot vaststelling van de kwaliteits- en veiligheidsnormen voor het doneren, wegnemen, verkrijgen, testen, bewerken, bewaren en distribueren van menselijk lichaamsmateriaal,
L 294/32 Publicatieblad van de Europese Unie
 L 294/32 Publicatieblad van de Europese Unie 25.10.2006 RICHTLIJN 2006/86/EG VAN DE COMMISSIE van 24 oktober 2006 ter uitvoering van Richtlijn 2004/23/EG van het Europees Parlement en de Raad wat betreft
L 294/32 Publicatieblad van de Europese Unie 25.10.2006 RICHTLIJN 2006/86/EG VAN DE COMMISSIE van 24 oktober 2006 ter uitvoering van Richtlijn 2004/23/EG van het Europees Parlement en de Raad wat betreft
Medische hulpmiddelen. 5 e TRIP Weefselvigilantie Symposium. Vigilantie van biomaterialen, randgebieden en raakvlakken. Ed J.B.
 Medische hulpmiddelen Vigilantie van biomaterialen, randgebieden en raakvlakken. Ed J.B. Jansen, MD, MBA 5 e TRIP Weefselvigilantie Symposium Inhoud 1.Medisch hulpmiddel? 2.Raakvlak? 3.... en dus? 3 medisch
Medische hulpmiddelen Vigilantie van biomaterialen, randgebieden en raakvlakken. Ed J.B. Jansen, MD, MBA 5 e TRIP Weefselvigilantie Symposium Inhoud 1.Medisch hulpmiddel? 2.Raakvlak? 3.... en dus? 3 medisch
Publicatieblad van de Europese Unie
 L 93/56 RICHTLIJN (EU) 2015/566 VAN DE COMMISSIE van 8 april 2015 tot uitvoering van Richtlijn 2004/23/EG aangaande de procedures om na te gaan of er sprake is van gelijkwaardige kwaliteits- en veiligheidsnormen
L 93/56 RICHTLIJN (EU) 2015/566 VAN DE COMMISSIE van 8 april 2015 tot uitvoering van Richtlijn 2004/23/EG aangaande de procedures om na te gaan of er sprake is van gelijkwaardige kwaliteits- en veiligheidsnormen
Inhoud van het jaarrapport voor de bloedtransfusiecentrum (BTC) (herziening mei 2007)
 DATUM 28/02/07 BIJLAGE CONTACT Walter Bontez TEL. 02 524 83 79 FAX 02 524 80 01 E-MAIL walter.bontez@afmps.be Omzendbrief nr. 496 Ter attentie van de directeurs van de Bloedtransfusiecentra (BTC) Inhoud
DATUM 28/02/07 BIJLAGE CONTACT Walter Bontez TEL. 02 524 83 79 FAX 02 524 80 01 E-MAIL walter.bontez@afmps.be Omzendbrief nr. 496 Ter attentie van de directeurs van de Bloedtransfusiecentra (BTC) Inhoud
Minimumeisen didactische leskeukens met de nadruk op voedselveiligheid. Laatste nieuwe wetgeving
 Minimumeisen didactische leskeukens met de nadruk op voedselveiligheid Laatste nieuwe wetgeving VISIE VAN HET FAVV OP DIDACTISCHE LESKEUKENS Didactische leskeukens = klaslokalen of laboratoria waar beginselen
Minimumeisen didactische leskeukens met de nadruk op voedselveiligheid Laatste nieuwe wetgeving VISIE VAN HET FAVV OP DIDACTISCHE LESKEUKENS Didactische leskeukens = klaslokalen of laboratoria waar beginselen
Coordinatie--Organen--Transplanteren--Prijs-allogreffen-orthopedische--MB doc
 24 NOVEMBER 1999. - Ministerieel besluit tot vaststelling van de prijs van orthopedische allogreffen en van orthopedische celculturen van menselijke oorsprong. BS 04/01/2000 in voege 01/01/2000 1 / 5 Artikel
24 NOVEMBER 1999. - Ministerieel besluit tot vaststelling van de prijs van orthopedische allogreffen en van orthopedische celculturen van menselijke oorsprong. BS 04/01/2000 in voege 01/01/2000 1 / 5 Artikel
Omzendbrief met betrekking tot materialen en voorwerpen bestemd om met levensmiddelen in aanraking te komen.
 Federaal Agentschap voor de Veiligheid van de Voedselketen Omzendbrief met betrekking tot materialen en voorwerpen bestemd om met levensmiddelen in aanraking te komen. Referentie PCCB/S3/CDP/5200333 Datum
Federaal Agentschap voor de Veiligheid van de Voedselketen Omzendbrief met betrekking tot materialen en voorwerpen bestemd om met levensmiddelen in aanraking te komen. Referentie PCCB/S3/CDP/5200333 Datum
1. AANGIFTE IN DE GIP 2 2. CONTROLES 2 3. VERVOER NAAR SCHEEPSBEVOORRADER 3 4. ERKENNINGSVOORWAARDEN VOOR SCHEEPSBEVOORRADER 3
 SCHEEPSBEVOORRADER 1. AANGIFTE IN DE GIP 2 2. CONTROLES 2 3. VERVOER NAAR SCHEEPSBEVOORRADER 3 4. ERKENNINGSVOORWAARDEN VOOR SCHEEPSBEVOORRADER 3 5. VOORWAARDEN VOOR INSLAG, OPSLAG EN UITSLAG 4 5.1. INSLAGVOORWAARDEN
SCHEEPSBEVOORRADER 1. AANGIFTE IN DE GIP 2 2. CONTROLES 2 3. VERVOER NAAR SCHEEPSBEVOORRADER 3 4. ERKENNINGSVOORWAARDEN VOOR SCHEEPSBEVOORRADER 3 5. VOORWAARDEN VOOR INSLAG, OPSLAG EN UITSLAG 4 5.1. INSLAGVOORWAARDEN
Afdeling II. Genetische onderzoeken. 1. Worden beschouwd als verstrekkingen waarvoor de bekwaming van de in 2 bedoelde geneesheer vereist is :
 De RODE markeringen gaan in voege vanaf 01/07/2011 (blz. 4) ART. 33 Afdeling II. Genetische onderzoeken. Art. 33. 1. Worden beschouwd als verstrekkingen waarvoor de bekwaming van de in 2 bedoelde geneesheer
De RODE markeringen gaan in voege vanaf 01/07/2011 (blz. 4) ART. 33 Afdeling II. Genetische onderzoeken. Art. 33. 1. Worden beschouwd als verstrekkingen waarvoor de bekwaming van de in 2 bedoelde geneesheer
FAQ. 2. Op wie heeft de Europese Verordening 183/2005 betrekking?
 FAQ 1. Waaruit bestaat de Europese Verordening 183/2005? Deze nieuwe Verordening bepaalt de voorschriften voor diervoederhygiëne. Alle verschillende activiteiten in de diervoederketen worden onderverdeeld
FAQ 1. Waaruit bestaat de Europese Verordening 183/2005? Deze nieuwe Verordening bepaalt de voorschriften voor diervoederhygiëne. Alle verschillende activiteiten in de diervoederketen worden onderverdeeld
Aanbevelingen voor de aanpak van Carbapenemase Producerende Enterobacteriaceae (CPE)
 Aanbevelingen voor de aanpak van Carbapenemase Producerende Enterobacteriaceae (CPE) o Dit probleem vergt dringende maatregelen voor een snelle aanpak van CPE teneinde overdracht te beperken en epidemieën
Aanbevelingen voor de aanpak van Carbapenemase Producerende Enterobacteriaceae (CPE) o Dit probleem vergt dringende maatregelen voor een snelle aanpak van CPE teneinde overdracht te beperken en epidemieën
Jaarverslag 2016 Weefselinstelling, Semenbank en Intra-uteriene inseminatie
 Jaarverslag 2016 Weefselinstelling, Semenbank en Intra-uteriene inseminatie AKL Catharina Ziekenhuis Eindhoven Versie : 1 Datum : 14-02-2017 Inhoudsopgave 1. Voorwoord 2. Organogram, Organisatie of Bestuurlijke
Jaarverslag 2016 Weefselinstelling, Semenbank en Intra-uteriene inseminatie AKL Catharina Ziekenhuis Eindhoven Versie : 1 Datum : 14-02-2017 Inhoudsopgave 1. Voorwoord 2. Organogram, Organisatie of Bestuurlijke
Tweede Kamer der Staten-Generaal
 Tweede Kamer der Staten-Generaal 2 Vergaderjaar 2011 2012 33 063 Wijziging van de Wet veiligheid en kwaliteit lichaamsmateriaal ter implementatie van Richtlijn 2010/53/EU inzake kwaliteits- en veiligheidsnormen
Tweede Kamer der Staten-Generaal 2 Vergaderjaar 2011 2012 33 063 Wijziging van de Wet veiligheid en kwaliteit lichaamsmateriaal ter implementatie van Richtlijn 2010/53/EU inzake kwaliteits- en veiligheidsnormen
FEDERAAL AGENTSCHAP VOOR DE VEILIGHEID VAN DE VOEDSELKETEN
 FEDERAAL AGENTSCHAP VOOR DE VEILIGHEID VAN DE VOEDSELKETEN 22 MAART 2013. - Ministerieel besluit betreffende de van de toepassingsmodaliteiten van de en de traceerbaarheid
FEDERAAL AGENTSCHAP VOOR DE VEILIGHEID VAN DE VOEDSELKETEN 22 MAART 2013. - Ministerieel besluit betreffende de van de toepassingsmodaliteiten van de en de traceerbaarheid
ADVIES VAN DE HOGE GEZONDHEIDSRAAD BETREFFENDE DE HERZIENING VAN DE REGLEMENTERING OP DE WEEFSELBANKEN
 ADVIES VAN DE HOGE GEZONDHEIDSRAAD BETREFFENDE DE HERZIENING VAN DE REGLEMENTERING OP DE WEEFSELBANKEN Tijdens de vergadering van 7 december 2001 waarvan het verslag wat dit punt betreft, ter zitting werd
ADVIES VAN DE HOGE GEZONDHEIDSRAAD BETREFFENDE DE HERZIENING VAN DE REGLEMENTERING OP DE WEEFSELBANKEN Tijdens de vergadering van 7 december 2001 waarvan het verslag wat dit punt betreft, ter zitting werd
Instructie export varkenssperma en embryo s naar EU-lidstaten. code VRKES-01 versie 02 ingangsdatum pag. 1 van 7
 code VRKES-01 versie 02 ingangsdatum 19-10-2018 pag. 1 van 7 Versie Goedkeuring datum Wijzigingen ten opzichte van vorige versie 02 01-08-2018 Lay-out cf. voorgeschreven sjabloon en algemene/taalkundige
code VRKES-01 versie 02 ingangsdatum 19-10-2018 pag. 1 van 7 Versie Goedkeuring datum Wijzigingen ten opzichte van vorige versie 02 01-08-2018 Lay-out cf. voorgeschreven sjabloon en algemene/taalkundige
Provinciale dienst van : Datum : Veranwoordelijke controleur : Nr : Operator : N uniek : Adres :
 Provinciale dienst van : Datum : Veranwoordelijke controleur : Nr : Operator : N uniek : Adres : PRI 242 Winnen, behandelen, bewaren en opslag van rundersperma bestemd voor het nationaal handelsverkeer
Provinciale dienst van : Datum : Veranwoordelijke controleur : Nr : Operator : N uniek : Adres : PRI 242 Winnen, behandelen, bewaren en opslag van rundersperma bestemd voor het nationaal handelsverkeer
DEEL 2: INFO ACTIVITEIT
 FORMULIER BIOVEILIGHEIDSDOSSIER PUBLIEK DOSSIER DEEL 2: INFO ACTIVITEIT 1. Algemene info 1.1. Beknopte beschrijving van de activiteit Nummer: Titel: Startdatum en einddatum voorzien voor de activiteit
FORMULIER BIOVEILIGHEIDSDOSSIER PUBLIEK DOSSIER DEEL 2: INFO ACTIVITEIT 1. Algemene info 1.1. Beknopte beschrijving van de activiteit Nummer: Titel: Startdatum en einddatum voorzien voor de activiteit
AFNAME VAN ETTER-, WOND- EN PUNCTIEVOCHT EN ANDERE MONSTERS
 Laboratorium Klinische Biologie 1. Materiaal AFNAME VAN ETTER-, WOND- EN PUNCTIEVOCHT EN ANDERE MONSTERS E-swab met roze schroefdop (Flocked swab met 1 ml vloeibaar AMIES transportmedium) Steriele polypropyleen
Laboratorium Klinische Biologie 1. Materiaal AFNAME VAN ETTER-, WOND- EN PUNCTIEVOCHT EN ANDERE MONSTERS E-swab met roze schroefdop (Flocked swab met 1 ml vloeibaar AMIES transportmedium) Steriele polypropyleen
Aanbeveling: Ingangscontrole van antistoffen t.b.v. flowcytometrie
 Aanbeveling: Ingangscontrole van antistoffen t.b.v. flowcytometrie Augustus 2016 Werkgroep NVC ISO 15189 Leden: A. Bloem A. Claessen C. Koelman J. Lambers J. Leuvenink P. de Schouwer V.H.J. van der Velden
Aanbeveling: Ingangscontrole van antistoffen t.b.v. flowcytometrie Augustus 2016 Werkgroep NVC ISO 15189 Leden: A. Bloem A. Claessen C. Koelman J. Lambers J. Leuvenink P. de Schouwer V.H.J. van der Velden
Augustus Deze instructiebundel beschrijft de modaliteiten inzake pre-attestatie en precertificatie.
 I. Toepassingsgebied Omschrijving van het product GN-code Land Broedeieren Levende dieren Sperma Embryo s Eicellen Producten van dierlijke oorsprong bestemd voor humane consumptie Diervoeders Levensmiddelen
I. Toepassingsgebied Omschrijving van het product GN-code Land Broedeieren Levende dieren Sperma Embryo s Eicellen Producten van dierlijke oorsprong bestemd voor humane consumptie Diervoeders Levensmiddelen
Aseptische bereiding Steriele bereiding, die niet in de primaire verpakking kan worden gesteriliseerd.
 Definities GMP-Z API (Active pharmaceutical ingredient) Iedere substantie of mengsel van substanties waaraan het effect van een bereid geneesmiddel kan worden toegeschreven of dat als zodanig dient. Aseptische
Definities GMP-Z API (Active pharmaceutical ingredient) Iedere substantie of mengsel van substanties waaraan het effect van een bereid geneesmiddel kan worden toegeschreven of dat als zodanig dient. Aseptische
Varkenssperma naar lidstaten en derde landen, algemeen (VRKES-01) 14 augustus 2012 Versie: 1.0.3
 1 DOEL EN TOEPASSINGSGEBIED Algemene instructie voor het keuren en certificeren van varkenssperma i.v.m. export naar lidstaten en derde landen. 2 WETTELIJKE BASIS 2.1 EU-regelgeving RL 90/429/EEG RL 92/65/EEG
1 DOEL EN TOEPASSINGSGEBIED Algemene instructie voor het keuren en certificeren van varkenssperma i.v.m. export naar lidstaten en derde landen. 2 WETTELIJKE BASIS 2.1 EU-regelgeving RL 90/429/EEG RL 92/65/EEG
NCAE. Toelichting handelsnormen voor eieren - verzamelaars november 2013
 1 TOELICHTING HANDELSNORMEN VOOR EIEREN VERZAMELAARS Inhoud 1 Algemeen 2 Vergunning / registratie 3 Ontvangst, transportverpakking, begeleidend document eieren 4 Intraverkeer van eieren 5 Merken van de
1 TOELICHTING HANDELSNORMEN VOOR EIEREN VERZAMELAARS Inhoud 1 Algemeen 2 Vergunning / registratie 3 Ontvangst, transportverpakking, begeleidend document eieren 4 Intraverkeer van eieren 5 Merken van de
Provinciale dienst van : Datum : Veranwoordelijke controleur : Nr : Operator : N uniek : Adres :
 Provinciale dienst van : Datum : Veranwoordelijke controleur : Nr : Operator : N uniek : Adres : TRA 78 fabrikant van meststoffen/bodemverbeterende middelen bevattende van dierlijke bijproducten afgeleide
Provinciale dienst van : Datum : Veranwoordelijke controleur : Nr : Operator : N uniek : Adres : TRA 78 fabrikant van meststoffen/bodemverbeterende middelen bevattende van dierlijke bijproducten afgeleide
K.B In werking B.S
 K.B. 18.3.2011 In werking 1.5.2011 B.S. 30.3.2011 Artikel 33bis GENETISCHE ONDERZOEKEN Wijzigen Invoegen Verwijderen 1. Moleculaire Biologische testen op menselijk genetisch materiaal bij verworven aandoeningen.
K.B. 18.3.2011 In werking 1.5.2011 B.S. 30.3.2011 Artikel 33bis GENETISCHE ONDERZOEKEN Wijzigen Invoegen Verwijderen 1. Moleculaire Biologische testen op menselijk genetisch materiaal bij verworven aandoeningen.
GENETISCHE ONDERZOEKEN Art. 33bis pag. 1 officieuze coördinatie
 GENETISCHE ONDERZOEKEN Art. 33bis pag. 1 "Artikel 33bis. 1. Moleculaire Biologische testen op menselijk genetisch materiaal bij verworven aandoeningen." "K.B. 31.8.2009" (in werking 1.11.2009) "A." + "
GENETISCHE ONDERZOEKEN Art. 33bis pag. 1 "Artikel 33bis. 1. Moleculaire Biologische testen op menselijk genetisch materiaal bij verworven aandoeningen." "K.B. 31.8.2009" (in werking 1.11.2009) "A." + "
Juni , 0209, 0210, Frans-Polynesië
 I. TOEPASSINGSGEBIED Productomschrijving GN-Code Land Pluimveevlees en 0207, 0209, 0210, pluimveevleesproducten 1601, 1602 II. BILATERAAL CERTIFICAAT Code FAVV Titel van het certificaat EX.VTP.PF.03.01
I. TOEPASSINGSGEBIED Productomschrijving GN-Code Land Pluimveevlees en 0207, 0209, 0210, pluimveevleesproducten 1601, 1602 II. BILATERAAL CERTIFICAAT Code FAVV Titel van het certificaat EX.VTP.PF.03.01
Dit geneesmiddel is onderworpen aan aanvullende monitoring
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Alofisel. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Alofisel. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Provinciale dienst van : Datum : Veranwoordelijke controleur : Nr : Operator : N uniek : Adres :
 Provinciale dienst van : Datum : Veranwoordelijke controleur : Nr : Operator : N uniek : Adres : PRI 24 Winnen, behandelen, bewaren en opslag van rundersperma bestemd voor het intracommunautair handelsverkeer
Provinciale dienst van : Datum : Veranwoordelijke controleur : Nr : Operator : N uniek : Adres : PRI 24 Winnen, behandelen, bewaren en opslag van rundersperma bestemd voor het intracommunautair handelsverkeer
Patiënteninformatie. Bloedtransfusie. Bloedtransfusie
 Patiënteninformatie Bloedtransfusie Bloedtransfusie 1 Bloedtransfusie In deze folder vindt u informatie over bloedtransfusie. De folder is bedoeld als aanvulling op de mondelinge informatie van de specialist.
Patiënteninformatie Bloedtransfusie Bloedtransfusie 1 Bloedtransfusie In deze folder vindt u informatie over bloedtransfusie. De folder is bedoeld als aanvulling op de mondelinge informatie van de specialist.
Gebruikershandleiding Idexx SNAP BVD Test
 Snelle in vitro techniek voor detectie van boviene virus diarree virussen in serum of oorweefsel. Voorzorgsmaatregelen en waarschuwingen Behandel al het materiaal als in staat om BVD over te dragen. Niet
Snelle in vitro techniek voor detectie van boviene virus diarree virussen in serum of oorweefsel. Voorzorgsmaatregelen en waarschuwingen Behandel al het materiaal als in staat om BVD over te dragen. Niet
(Niet-wetgevingshandelingen) VERORDENINGEN
 14.1.2012 Publicatieblad van de Europese Unie L 12/1 II (Niet-wetgevingshandelingen) VERORDENINGEN VERORDENING (EU) Nr. 28/2012 VAN DE COMMISSIE van 11 januari 2012 tot vaststelling van voorschriften voor
14.1.2012 Publicatieblad van de Europese Unie L 12/1 II (Niet-wetgevingshandelingen) VERORDENINGEN VERORDENING (EU) Nr. 28/2012 VAN DE COMMISSIE van 11 januari 2012 tot vaststelling van voorschriften voor
Omzendbrief met betrekking tot slagerijscholen
 Federaal Agentschap voor de Veiligheid van de Voedselketen Omzendbrief met betrekking tot slagerijscholen Referentie PCCB/S3/EME/574427 Datum 04/06/2013 Huidige versie 2.0 Van toepassing vanaf Datum van
Federaal Agentschap voor de Veiligheid van de Voedselketen Omzendbrief met betrekking tot slagerijscholen Referentie PCCB/S3/EME/574427 Datum 04/06/2013 Huidige versie 2.0 Van toepassing vanaf Datum van
ADVIES BETREFFENDE DE ERKENNING VAN DE TRANSPLANTATIECENTRA ALS ZIEKENHUISFUNCTIE
 FOD VOLKSGEZONDHEID, VEILIGHEID VAN DE VOEDSELKETEN EN LEEFMILIEU Directoraat-generaal Organisatie gezondheidszorgvoorzieningen NATIONALE RAAD VOOR ZIEKEN- HUISVOORZIENINGEN. BRUSSEL, 13/03/2003 Afdeling
FOD VOLKSGEZONDHEID, VEILIGHEID VAN DE VOEDSELKETEN EN LEEFMILIEU Directoraat-generaal Organisatie gezondheidszorgvoorzieningen NATIONALE RAAD VOOR ZIEKEN- HUISVOORZIENINGEN. BRUSSEL, 13/03/2003 Afdeling
FAQ - Gids voor de invoering van een autocontrolesysteem voor de brood- en banketbakkerij in de sector transformatie
 PB 07 FAQ (G-026 B2B) REV0 2014-1/8 Federaal Agentschap voor de Veiligheid van de Voedselketen FAQ - Gids voor de invoering van een autocontrolesysteem voor de brood- en banketbakkerij in de sector transformatie
PB 07 FAQ (G-026 B2B) REV0 2014-1/8 Federaal Agentschap voor de Veiligheid van de Voedselketen FAQ - Gids voor de invoering van een autocontrolesysteem voor de brood- en banketbakkerij in de sector transformatie
ADVIES VAN DE HOGE GEZONDHEIDSRAAD nr. 9334
 ADVIES VAN DE HOGE GEZONDHEIDSRAAD nr. 9334 Ontwerp van koninklijk besluit ter omzetting van Europese richtlijnen 2015/565/EU en 2015/566/EU Versie gevalideerd op het College van 2 maart 2016 1 I INLEIDING
ADVIES VAN DE HOGE GEZONDHEIDSRAAD nr. 9334 Ontwerp van koninklijk besluit ter omzetting van Europese richtlijnen 2015/565/EU en 2015/566/EU Versie gevalideerd op het College van 2 maart 2016 1 I INLEIDING
Certificaat voor de intracommunautaire handel Deel I: Informatie betreffende de aangeboden zending
 Certificaat voor de intracommunautaire handel Deel I: Informatie betreffende de aangeboden zending I.1 Verzender I.2 Referentienummer certificaat I.2.a. Locaal referentienummmer: I.3 Bevoegde centrale
Certificaat voor de intracommunautaire handel Deel I: Informatie betreffende de aangeboden zending I.1 Verzender I.2 Referentienummer certificaat I.2.a. Locaal referentienummmer: I.3 Bevoegde centrale
Hoofdstuk 14. Autologe donaties
 ragenlijst audit, Hoofdstuk 14. Autologe donaties, HPZO versie 1.1/08-2010 Hoofdstuk 14. Autologe donaties Norm Zowel in het ziekenhuis als op de bloedbank dienen procedures voor bestellen, afnemen,testen,
ragenlijst audit, Hoofdstuk 14. Autologe donaties, HPZO versie 1.1/08-2010 Hoofdstuk 14. Autologe donaties Norm Zowel in het ziekenhuis als op de bloedbank dienen procedures voor bestellen, afnemen,testen,
Gearchiveerd op 03/01/2013
 Provinciale dienst van:... Datum:... Verantwoordelijke Controleur:... Nr:... Operator : Adres :............ N uniek PRI 296 Verzamelen, behandelen, overplanten en opslag van embryo's van éénhoevigen bestemd
Provinciale dienst van:... Datum:... Verantwoordelijke Controleur:... Nr:... Operator : Adres :............ N uniek PRI 296 Verzamelen, behandelen, overplanten en opslag van embryo's van éénhoevigen bestemd
(VO 183/2005 Bijlage III) De productie-eenheid is zo ontworpen dat zij adequaat kan worden gereinigd.
 Toelatingsvoorwaarden voor veehouderijen welke voedermiddelen van dierlijke oorsprong vervoederen aan veedieren gehouden voor de productie van levensmiddelen. (implementatie van VO 79/2005) Bijlage III.8.9.
Toelatingsvoorwaarden voor veehouderijen welke voedermiddelen van dierlijke oorsprong vervoederen aan veedieren gehouden voor de productie van levensmiddelen. (implementatie van VO 79/2005) Bijlage III.8.9.
Goede Hygiëne Praktijken ( GHP ) De opmaak van een GHP-plan
 Goede Hygiëne Praktijken ( GHP ) De opmaak van een GHP-plan Wetgeving KB 14-11-2003 Koninklijk besluit betreffende autocontrole, meldingsplicht en traceerbaarheid in de voedselketen KB 27-04-2007 Koninklijk
Goede Hygiëne Praktijken ( GHP ) De opmaak van een GHP-plan Wetgeving KB 14-11-2003 Koninklijk besluit betreffende autocontrole, meldingsplicht en traceerbaarheid in de voedselketen KB 27-04-2007 Koninklijk
Het CBP voldoet hierbij aan dit verzoek. Kader
 POSTADRES Postbus 93374, 2509 AJ Den Haag BEZOEKADRES Prins Clauslaan 20 TEL 070-381 13 00 FAX 070-381 13 01 E-MAIL info@cbpweb.nl INTERNET www.cbpweb.nl AAN Ministerie van Volksgezondheid, Welzijn en
POSTADRES Postbus 93374, 2509 AJ Den Haag BEZOEKADRES Prins Clauslaan 20 TEL 070-381 13 00 FAX 070-381 13 01 E-MAIL info@cbpweb.nl INTERNET www.cbpweb.nl AAN Ministerie van Volksgezondheid, Welzijn en
Gearchiveerd op 01/09/2014
 Provinciale dienst van:... Datum:... Verantwoordelijke Controleur:... Nr:... Operator :... N uniek... Adres :...... PPV 28 Infrastructuur, inrichting en hygiëne - Groothandel primaire plantaardige producten
Provinciale dienst van:... Datum:... Verantwoordelijke Controleur:... Nr:... Operator :... N uniek... Adres :...... PPV 28 Infrastructuur, inrichting en hygiëne - Groothandel primaire plantaardige producten
Federaal Agentschap voor de Veiligheid van de Voedselketen - 1 -
 Federaal Agentschap voor de Veiligheid van de Voedselketen - 1 - Ministerieel besluit houdende de veterinairrechtelijke voorschriften voor het handelsverkeer en de invoer uit derde landen van honden en
Federaal Agentschap voor de Veiligheid van de Voedselketen - 1 - Ministerieel besluit houdende de veterinairrechtelijke voorschriften voor het handelsverkeer en de invoer uit derde landen van honden en
GDP: Good Distribution Practices
 GDP: Good Distribution Practices De eisen in de GDP richtlijnen hebben betrekking op farmaceutische hulpstoffen. Deze eisen zijn voortgekomen uit GMP-richtlijnen van het IPEC (International Pharmaceutical
GDP: Good Distribution Practices De eisen in de GDP richtlijnen hebben betrekking op farmaceutische hulpstoffen. Deze eisen zijn voortgekomen uit GMP-richtlijnen van het IPEC (International Pharmaceutical
De EUSTITE matrix Wat moet er gemeld worden?
 De EUSTITE matrix Wat moet er gemeld worden? Minisymposium Weefselvigilantie juni 9 Marjan Happel, projectcoördinator weefselvigilantie EUSTITE EUSTITE (European Union Standards and Training in the Inspection
De EUSTITE matrix Wat moet er gemeld worden? Minisymposium Weefselvigilantie juni 9 Marjan Happel, projectcoördinator weefselvigilantie EUSTITE EUSTITE (European Union Standards and Training in the Inspection
Speed F-Corona TM. www.speedrange.nl. Virbac Nederland B.V., Postbus 313, 3770 AH Barneveld Tel. 0342 427 127 E-mail: info@virbac.
 Speed F-Corona TM www.speedrange.nl Virbac Nederland B.V., Postbus 313, 3770 AH Barneveld Tel. 0342 427 127 E-mail: info@virbac.nl ALLEEN VOOR IN VITRO GEBRUIK NEDERLANDS KLINISCHE TOEPASSING Katten die
Speed F-Corona TM www.speedrange.nl Virbac Nederland B.V., Postbus 313, 3770 AH Barneveld Tel. 0342 427 127 E-mail: info@virbac.nl ALLEEN VOOR IN VITRO GEBRUIK NEDERLANDS KLINISCHE TOEPASSING Katten die
ADVIES VAN DE HOGE GEZONDHEIDSRAAD nr. 9151
 ADVIES VAN DE HOGE GEZONDHEIDSRAAD nr. 9151 Serologische testen bij donatie in de perinatale-periode In this science-policy advisory report, the Superior Health Council recommends that serological tests
ADVIES VAN DE HOGE GEZONDHEIDSRAAD nr. 9151 Serologische testen bij donatie in de perinatale-periode In this science-policy advisory report, the Superior Health Council recommends that serological tests
BIJLAGE I SAMENVATTING VAN DE PRODUKTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUKTKENMERKEN 1. BENAMING VAN HET DIERGENEESMIDDEL Pentofel 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Per dosis van 1 ml : Actieve bestanddelen Geïnactiveerd kattenziekte
BIJLAGE I SAMENVATTING VAN DE PRODUKTKENMERKEN 1. BENAMING VAN HET DIERGENEESMIDDEL Pentofel 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Per dosis van 1 ml : Actieve bestanddelen Geïnactiveerd kattenziekte
Zelfevaluatie hoofdstuk logistiek
 Vragenlijst: Deze tool laat u toe om door middel van een aantal vragen een balans op te maken van de kwaliteit binnen uw apotheek, teneinde deze waar nodig te verbeteren. Kies bij elke vraag het meest
Vragenlijst: Deze tool laat u toe om door middel van een aantal vragen een balans op te maken van de kwaliteit binnen uw apotheek, teneinde deze waar nodig te verbeteren. Kies bij elke vraag het meest
