ThromboGenics ontvangt positieve beoordeling van CHMP voor
|
|
|
- Anke Jonker
- 7 jaren geleden
- Aantal bezoeken:
Transcriptie
1 ThromboGenics ontvangt positieve beoordeling van CHMP voor JETREA De positieve beoordeling maakt de weg vrij voor een mogelijke goedkeuring door EMA van JETREA als eerste farmacologische oplossing voor de behandeling van vitreomaculaire tractie (VMT), met inbegrip van de combinatie met een maculair gaatje met een diameter gelijk aan of kleiner dan 400 micron. Leuven, 18 januari 2013 ThromboGenics NV (Euronext Brussels: THR), een geïntegreerd biofarmaceutisch bedrijf dat zich toelegt op de ontwikkeling en verkoop van innovatieve geneesmiddelen voor oogaandoeningen, kondigt vandaag aan dat het Committee for Medicinal Products for Human Use (CHMP) van het Europese Geneesmiddelenagentschap (EMA) een positieve opinie heeft geformuleerd over JETREA (ocriplasmine), waarbij het JETREA aanbeveelt voor de behandeling van vitreomaculaire tractie (VMT), met inbegrip van de combinatie met een maculair gaatje met een diameter gelijk aan of kleiner dan 400 micron. VMT, dat in de Verenigde Staten wordt aangeduid met symptomatische vitreomaculaire adhesie (VMA), is een leeftijdsgebonden, progressieve gezichtsbedreigende aandoening die kan leiden tot beeldvertekening, verminderd gezichtsvermogen en centrale blindheid. Volgens ramingen zouden alleen al in Europa tot patiënten door deze aandoening getroffen worden. 1 JETREA, een verkorte vorm van een humaan proteïne (plasmine), wordt éénmalig toegediend met één enkele intravitreale injectie. Het middel richt zich op de proteïnevezels die een abnormale tractie veroorzaken tussen het glasvocht en de retina ter hoogte van de macula, waardoor VMT ontstaat. Door deze proteïnevezels op te lossen, verzwakt JETREA de tractie en helpt het om het glasvocht volledig los te maken van het netvlies. Alcon, een afdeling van Novartis, verwierf de rechten op de verkoop van JETREA buiten de Verenigde Staten. ThromboGenics behield de rechten op de verkoop van het geneesmiddel in de Verenigde Staten. In de VS werd JETREA door de FDA goedgekeurd voor de behandeling van symptomatische vitreomaculaire adhesie (VMA). ThromboGenics introduceerde JETREA eerder deze week in de VS en de eerste patiënten hebben deze vernieuwende behandeling reeds toegediend gekregen. Het doet ons veel genoegen dat het CHMP een positieve aanbeveling voor JETREA heeft verleend voor de behandeling van VMT met inbegrip van de combinatie met een maculair gaatje, verklaarde Dr. Patrik De Haes, CEO van ThromboGenics. Als houder van de vergunning voor het in de handel brengen zullen wij, samen met onze partner Alcon, blijven samenwerken met het Europese
2 Geneesmiddelenagentschap en de Europese Commissie voor de voltooiing van de European Marketing Authorisation Application (MAA). Aan de medische behoeften inzake vitreomaculaire tractie kon tot nu toe niet worden voldaan en wij zullen onze partner Alcon graag alle steun verlenen om deze vernieuwende behandelingsmogelijkheid buiten de VS zo snel mogelijk ter beschikking te stellen van de talrijke patiënten die er volgens ons baat bij kunnen hebben. JETREA wordt gebruikt om volwassenen te behandelen met een oogaandoening genaamd vitreomaculaire tractie (VMT) met inbegrip van de combinatie met een klein maculair gaatje in de retina (centrale deel van het lichtgevoelige laagje aan de achterkant van het oog). VMT ontstaat door tractie als gevolg van de hardnekkige verkleving van het glasvocht (gelachtige substantie in het midden van het oog) aan de gele vlek (macula) aan de achterkant van het oog. De macula is verantwoordelijk voor ons centrale gezichtsvermogen die we nodig hebben voor dagelijkse bezigheden zoals autorijden, lezen en herkennen van gezichten. VMT kan symptomen veroorzaken zoals beeldvertekening en verslechterd zicht. Als de ziekte vordert en er wordt niet ingegrepen kan de gele vlek scheuren waardoor er een gaatje in de macula ontstaat (maculair gaatje genaamd). JETREA werkt door het scheiden van het glasvocht van de gele vlek (macula) en helpt het maculair gaatje te sluiten, als er één is, hetgeen de symptomen veroorzaakt door VMT vermindert. De enige behandeling die in de EU momenteel beschikbaar is, is observatie of waakzaam afwachten tot de patiënt in aanmerking komt voor een chirurgische ingreep, meestal in een zeer late fase van de ziekte. 2,3 De chirurgische procedure bestaat uit een vitrectomie en het herstellen van het netvlies. Maar voor veel patiënten is dit geen geschikte behandeling en er kan al schade aan het netvlies zijn opgetreden 4,5. Vitreomaculaire tractie en de vorming van maculaire gaatjes zijn invaliderende oogaandoeningen die het gezichtsvermogen beïnvloeden en de dagelijkse activiteiten van patiënten verstoren zegt Prof. Dr. Peter Stalmans, Afdeling Oogziekten, UZ Leuven, België. Wanneer de ziekte verergert, is de enige beschikbare oplossing een operatie, vitrectomie genaamd. Het oplossen van de glasvocht tractie door een farmacologische oplossing kan een vitrectomy overbodig maken. Wanneer goedgekeurd, zal JETREA het eerste beschikbare product op de markt zijn met bewezen klinische doeltreffendheid om glasvocht tractie op te lossen en is derhalve een ommekeer in de behandeling van deze oogziektes, concludeert hij.
3 Dr. Albert Augustin, Professor Oftalmologie en Voorzitter van het Departement Oftalmologie aan het Klinikum Karlsruhe, Duitsland zegt: JETREA betekent een belangrijke doorbraak en men verwacht dat het de klinische praktijk van retinaspecialisten die patiënten met VMT en bijbehorende maculaire gaatjes behandelen ingrijpend zal veranderen. Na de goedkeuring wordt het mogelijk om met één enkele injectie van JETREA in het aangetaste oog in een vroeger stadium in te grijpen en te voorkomen dat de ziekte voortschrijdt en er gezichtsvermogen verloren gaat. Patiënten met VMT en maculaire gaatjes ondervinden grote moeilijkheden bij hun dagelijkse activiteiten zoals lezen, autorijden of werken en dit tast hun algemene levenskwaliteit aan, verklaarde Prof. Yit Yang, Oogheelkundig Consultant, Wolverhampton Eye Hospital en gastprofessor van Aston University, UK. Ik kijk er naar uit om JETREA toe te dienen aan patiënten die ik normaal gezien zou observeren totdat de ziekte verergert, in ons streven om hun levenskwaliteit te verbeteren De EU MAA-aanvraag steunde op gegevens uit twee cruciale klinische Fase IIIstudies om de veiligheid en de doeltreffendheid van één enkele toediening van JETREA na te gaan. Beide studies bereikten hun primaire eindpunt van resolutie en toonden aan dat JETREA bij significant meer patiënten VMT en maculaire gaatjes oplost dan placebo. Op dag 28 bereikte 26,5% van met JETREA behandelde patiënten resolutie (tegenover 10,1% met placebo [P<0.001]). 72% van de met JETREA behandelde patiënten met resolutie van VMT en maculaire gaatjes op dag 28, had dit reeds bereikt binnen zeven dagen. 6 Alle bijwerkingen hebben met het oog te maken. De bijwerkingen die het meest werden gerapporteerd, zijn glasvochttroebelingen, oogpijn en fotopsie, alsook bindvliesbloeding door de injectieprocedure. De meeste bijwerkingen deden zich binnen de eerste week na de injectie voor. De meeste bijwerkingen waren niet ernstig en mild in intensiteit en zij verdwenen binnen twee tot drie weken. 6 Referenties 1. Interne ramingen van ThromboGenics en Alcon 2. Idiopathic macular hole. American Academy of Ophthalmology; Stalmans P. Management and intervention strategies for symptomatic vitreomacular adhesions. Retinal Physician Koerner F & Garweg J. Vitrectomy for macular pucker and vitreomacular traction syndrome. Doc Ophthalmol 1999;97: Dugel PU, Brown DM, Humayun MS et al. Symptomatic vitreomacular adhesion: diagnosis, pathologic implications, and management. Retina Today 2011;(Suppl): Stalmans P, Benz MS, Gandorfer A et al. Enzymatic vitreolysis with ocriplasmin for vitreomacular traction and macular holes. N Engl J Med 2012;367: Einde -
4 Neem voor verdere informatie contact op met: ThromboGenics Wouter Piepers, Global Head of Corporate Communications / wouter.piepers@thrombogenics.com Dr. Patrik De Haes, CEO Patrik.dehaes@thrombogenics.com Chris Buyse, CFO Chris.buyse@thrombogenics.com Citigate Dewe Rogerson The Trout Group (relaties met investeerders in de VS) David Dible/ Nina Enegren/ Sita Shah Tel: sita.shah@citigatedr.co.uk Todd James/ Simon Harnest Tel: tjames@troutgroup.com Over JETREA (ocriplasmine) JETREA (ocriplasmine) is een gereduceerde vorm van humaan plasmine. In de VS is JETREA geïndiceerd voor de behandeling van symptomatisch VMA. In Europa is JETREA geïndiceerd voor de behandeling van vitreomaculaire tractie (VMT), met inbegrip van een maculair gaatje met een diameter gelijk aan of kleiner dan 400 micron. JETREA is een selectief proteolytisch enzyme dat fibronectine, laminine en collageen van elkaar scheidt, drie belangrijke componenten van de vitreoretinale interface die een belangrijke rol spelen bij vitreomaculaire adhesie. JETREA werd onderzocht in twee gerandomiseerde, dubbelblinde multicenter Fase III-studies in de VS en in Europa. In totaal waren er 652 patiënten met vitreomaculaire adhesie bij betrokken. Beide studies bereikten het primaire eindpunt van VMA-oplossing op dag 28. Het Fase III-programma van JETREA bracht aan het licht dat VMA werd opgelost bij 26,5% van de met JETREA behandelde patiënten, te vergelijken met 10,1% van de patiënten die een placebo ontvingen (p<0.001). Uit het Fase III-programma bleek
5 ook dat JETREA over het het algemeen veilig is en goed wordt verdragen. De meeste bijwerkingen zijn van voorbijgaande aard en niet ernstig. Over ThromboGenics ThromboGenics is een geïntegreerd biofarmaceutisch bedrijf dat zich toelegt op de ontwikkeling en verkoop van innovatieve geneesmiddelen voor oogaandoeningen. Het belangrijkste product van het bedrijf, JETREA (ocriplasmine), werd door de Amerikaanse FDA goedgekeurd voor de behandeling van symptomatische VMA. De behandeling werd in januari 2013 gelanceerd. In maart 2012 ondertekende ThromboGenics een strategisch partnership met Alcon (Novartis) om JETREA buiten de Verenigde Staten op de markt te brengen. Deze overeenkomst bepaalt dat ThromboGenics in totaal tot 375 miljoen in voorschoten mijlpaalbetalingen kan ontvangen. Het bedrijf zal aanzienlijke royalty s ontvangen op de netto-omzet van Alcon met JETREA. ThromboGenics en Alcon zijn van plan om de ontwikkelingskosten van JETREA voor een aantal nieuwe vitreoretinale indicaties gelijk te delen. De European Marketing Authorisation Application (MAA) voor JETREA wordt momenteel onderzocht door het Europese Geneesmiddelenagentschap. Na de positieve aanbeveling van het CHMP wordt de uiteindelijke beslissing van de Europese Commissie over de goedkeuring voor Europa in de eerste helft van 2013 verwacht. ThromboGenics onderzoekt ook verder anti-pigf (Placental Growth Factor), dat vroeger met TB-403 werd aangeduid, voor de behandeling van oftalmologische indicaties. Het hoofdkantoor van ThromboGenics bevindt zich in Leuven, België, en het bedrijf heeft kantoren in Iselin, NJ (VS) en Dublin, Ierland. De onderneming is genoteerd op NYSE Euronext Brussels onder THR. Meer informatie is beschikbaar op Belangrijke informatie met betrekking tot toekomstgerichte verklaringen Sommige verklaringen in dit persbericht kunnen beschouwd worden als toekomstgericht. Dergelijke toekomstgerichte verklaringen zijn gebaseerd op huidige verwachtigen en zij kunnen verscheidene risico's en onzekerheden teweegbrengen en zijn hierdoor beïnvloed. Thrombogenics kan daarom geen garantie bieden dat dergelijke toekomstgerichte verklaringen zullen gerealiseerd worden en wijst uitdrukkelijk elke verplichting af om toekomstgerichte verklaringen bij te werken,
6 hetzij als gevolg van nieuwe informatie, toekomstige gebeurtenissen of enige andere reden. Bijkomende informatie betreffende risico s en onzekerheden die de business beïnvloeden en andere factoren die zorgen dat actuele resultaten beduidend uiteenlopen van eender welke toekomstgerichte verklaring is opgenomen in het Jaarverslag van het Bedrijf. Dit persbericht vormt geen aanbieding of uitnodiging tot het kopen of verkopen van effecten of activa van ThromboGenics in welk rechtsgebied dan ook. In de Verenigde Staten mogen geen effecten van ThromboGenics worden aangeboden of verkocht zonder registratie volgens de U.S. Securities Act van 1933 en de amendementen erop, of krachtens een uitzondering hierop en in overeenstemming met de Amerikaanse wetgeving op effecten die van toepassing zou zijn.
Metamorphopsia (vervorming van het gezichtsveld) is een ernstig symptoom en rechtvaardigt een vroegtijdige behandeling mét terugbetaling
 Final Appraisal Determination (FAD) door NICE in de UK bevestigt aanbeveling tot terugbetaling van ThromboGenics JETREA voor de behandeling van vitreomaculaire tractie, inclusief in combinatie met een
Final Appraisal Determination (FAD) door NICE in de UK bevestigt aanbeveling tot terugbetaling van ThromboGenics JETREA voor de behandeling van vitreomaculaire tractie, inclusief in combinatie met een
De G-BA in Duitsland bevestigt dat JETREA
 De G-BA in Duitsland bevestigt dat JETREA van ThromboGenics significante therapeutische voordelen biedt aan patiënten met vitreomaculaire tractie (VMT), met inbegrip van de combinatie met een maculagat
De G-BA in Duitsland bevestigt dat JETREA van ThromboGenics significante therapeutische voordelen biedt aan patiënten met vitreomaculaire tractie (VMT), met inbegrip van de combinatie met een maculagat
ThromboGenics NV Business Update
 Gereglementeerde informatie Openbaarmaking overeenkomstig de wet van 2 mei 2007 ThromboGenics NV Business Update Leuven, België 8 november 2012 ThromboGenics NV (Euronext Brussels: THR), een geïntegreerd
Gereglementeerde informatie Openbaarmaking overeenkomstig de wet van 2 mei 2007 ThromboGenics NV Business Update Leuven, België 8 november 2012 ThromboGenics NV (Euronext Brussels: THR), een geïntegreerd
ThromboGenics Business Update
 GEREGLEMENTEERDE INFORMATIE ThromboGenics Business Update Aanvaarding van JETREA door de Amerikaanse retinagemeenschap. Tegen eind april 2013 bedroeg de omzet in de Verenigde Staten meer dan $ 10 miljoen.
GEREGLEMENTEERDE INFORMATIE ThromboGenics Business Update Aanvaarding van JETREA door de Amerikaanse retinagemeenschap. Tegen eind april 2013 bedroeg de omzet in de Verenigde Staten meer dan $ 10 miljoen.
ThromboGenics Business Update
 ThromboGenics Business Update JETREA vindt langzaamaan steeds meer ingang in de retinagemeenschap in de VS. Onderneming breidt medische educatie in VS uit: aantal Medical Science Liaison managers verhoogd
ThromboGenics Business Update JETREA vindt langzaamaan steeds meer ingang in de retinagemeenschap in de VS. Onderneming breidt medische educatie in VS uit: aantal Medical Science Liaison managers verhoogd
ThromboGenics Business Update H1 2013
 GEREGLEMENTEERDE INFORMATIE ThromboGenics Business Update H1 2013 Conference call en webcast gepland vandaag om 06:30 PM CET 12:30 PM EST De totale opbrengsten in H1 2013 bedragen 102.7 miljoenwinstgevende
GEREGLEMENTEERDE INFORMATIE ThromboGenics Business Update H1 2013 Conference call en webcast gepland vandaag om 06:30 PM CET 12:30 PM EST De totale opbrengsten in H1 2013 bedragen 102.7 miljoenwinstgevende
ThromboGenics NV Business Update
 Gereglementeerde informatie Aankondiging in overeenstemming met de wet van 2 mei 2007 ThromboGenics NV Business Update Leuven, België 10 mei 2012 ThromboGenics NV (NYSE Euronext Brussels: THR), een biofarmaceutisch
Gereglementeerde informatie Aankondiging in overeenstemming met de wet van 2 mei 2007 ThromboGenics NV Business Update Leuven, België 10 mei 2012 ThromboGenics NV (NYSE Euronext Brussels: THR), een biofarmaceutisch
ThromboGenics publiceert business update en jaarresultaten Transformatie levert 30 miljoen euro in netto winst op
 ThromboGenics publiceert business update en jaarresultaten 2012 2012 Transformatie levert 30 miljoen euro in netto winst op GEREGLEMENTEERDE INFORMATIE Leuven, België 14 maart 2013 - ThromboGenics NV (Euronext
ThromboGenics publiceert business update en jaarresultaten 2012 2012 Transformatie levert 30 miljoen euro in netto winst op GEREGLEMENTEERDE INFORMATIE Leuven, België 14 maart 2013 - ThromboGenics NV (Euronext
ThromboGenics NV Business Update
 Gereglementeerde informatie ThromboGenics NV Business Update Leuven, België 30 augustus 2012 ThromboGenics NV (Euronext Brussels: THR), een biofarmaceutisch bedrijf dat zich toelegt op de ontwikkeling
Gereglementeerde informatie ThromboGenics NV Business Update Leuven, België 30 augustus 2012 ThromboGenics NV (Euronext Brussels: THR), een biofarmaceutisch bedrijf dat zich toelegt op de ontwikkeling
ThromboGenics NV Business Update
 Gereglementeerde informatie Aankondiging in overeenstemming met de wet van 2 mei 2007 ThromboGenics NV Business Update Leuven, België 3 november 2011 ThromboGenics NV (Euronext Brussels: THR), een biofarmaceutische
Gereglementeerde informatie Aankondiging in overeenstemming met de wet van 2 mei 2007 ThromboGenics NV Business Update Leuven, België 3 november 2011 ThromboGenics NV (Euronext Brussels: THR), een biofarmaceutische
ThromboGenics Business Update Q3 2015
 Gereglementeerde informatie ThromboGenics Business Update Q3 2015 VS organisatie gereorganiseerd voor break-even vanaf 2016 Sinds lancering wereldwijd 20.000 patiënten behandeld met JETREA Klinische en
Gereglementeerde informatie ThromboGenics Business Update Q3 2015 VS organisatie gereorganiseerd voor break-even vanaf 2016 Sinds lancering wereldwijd 20.000 patiënten behandeld met JETREA Klinische en
Uw handleiding voor de behandeling met JETREA
 Uw handleiding voor de behandeling met JETREA (ocriplasmine) (ocriplasmin) (ocriplasmine) Concentraat voor oplossing, voor injectie, 0,5mg/0,2ml 2 Inleiding U heeft dit informatiepakket ontvangen omdat
Uw handleiding voor de behandeling met JETREA (ocriplasmine) (ocriplasmin) (ocriplasmine) Concentraat voor oplossing, voor injectie, 0,5mg/0,2ml 2 Inleiding U heeft dit informatiepakket ontvangen omdat
Business Update. Gereglementeerde informatie Aankondiging in overeenstemming met de wet van 2 mei 2007
 Gereglementeerde informatie Aankondiging in overeenstemming met de wet van 2 mei 2007 Business Update Leuven, België 14 mei 2009 ThromboGenics NV (Euronext Brussel:THR), een biofarmaceutisch bedrijf dat
Gereglementeerde informatie Aankondiging in overeenstemming met de wet van 2 mei 2007 Business Update Leuven, België 14 mei 2009 ThromboGenics NV (Euronext Brussel:THR), een biofarmaceutisch bedrijf dat
Gereglementeerde informatie Aankondiging in overeenstemming met de wet van 2 mei Business Update
 Gereglementeerde informatie Aankondiging in overeenstemming met de wet van 2 mei 2007 Business Update Leuven, België 12 mei 2011 ThromboGenics NV (Euronext Brussels: THR), een biofarmaceutisch bedrijf
Gereglementeerde informatie Aankondiging in overeenstemming met de wet van 2 mei 2007 Business Update Leuven, België 12 mei 2011 ThromboGenics NV (Euronext Brussels: THR), een biofarmaceutisch bedrijf
ThromboGenics NV Business Update
 Gereglementeerde informatie Aankondiging in overeenstemming met de wet van 2 mei 2007 ThromboGenics NV Business Update Leuven, België 24 augustus 2011 ThromboGenics NV (Euronext Brussels: THR), een biofarmaceutische
Gereglementeerde informatie Aankondiging in overeenstemming met de wet van 2 mei 2007 ThromboGenics NV Business Update Leuven, België 24 augustus 2011 ThromboGenics NV (Euronext Brussels: THR), een biofarmaceutische
ThromboGenics Business Update en Jaarresultaten 2013
 ThromboGenics Business Update en Jaarresultaten 2013 JETREA in de VS GEREGLEMENTEERDE INFORMATIE De verkoop van JETREA in de VS bedroeg 20,2 miljoen in 2013; er werden bijna 7.000 patiënten behandeld In
ThromboGenics Business Update en Jaarresultaten 2013 JETREA in de VS GEREGLEMENTEERDE INFORMATIE De verkoop van JETREA in de VS bedroeg 20,2 miljoen in 2013; er werden bijna 7.000 patiënten behandeld In
Business Update. Gereglementeerde Informatie
 Business Update Gereglementeerde Informatie Leuven, België 6 november 2008 ThromboGenics NV (Euronext Brussel: THR), een biofarmaceutisch bedrijf dat zich toelegt op innovatieve behandelingen voor oogaandoeningen,
Business Update Gereglementeerde Informatie Leuven, België 6 november 2008 ThromboGenics NV (Euronext Brussel: THR), een biofarmaceutisch bedrijf dat zich toelegt op innovatieve behandelingen voor oogaandoeningen,
ThromboGenics Q Business Update
 GEREGLEMENTEERDE INFORMATIE ThromboGenics Q1 2015 Business Update Nieuwe klinische studies met JETREA bevestigen positieve OASIS resultaten: slaagpercentages op dag 28 variëren tussen 40% en 58% Nieuwe
GEREGLEMENTEERDE INFORMATIE ThromboGenics Q1 2015 Business Update Nieuwe klinische studies met JETREA bevestigen positieve OASIS resultaten: slaagpercentages op dag 28 variëren tussen 40% en 58% Nieuwe
ThromboGenics NV Kondigt Halfjaarlijkse Resultaten aan voor 2010
 Gereglementeerde informatie Aankondiging in overeenstemming met de wet van 2 mei 2007 ThromboGenics NV Kondigt Halfjaarlijkse Resultaten aan voor 2010 Leuven, België 26 augustus, 2010 ThromboGenics NV
Gereglementeerde informatie Aankondiging in overeenstemming met de wet van 2 mei 2007 ThromboGenics NV Kondigt Halfjaarlijkse Resultaten aan voor 2010 Leuven, België 26 augustus, 2010 ThromboGenics NV
ThromboGenics Business Update en Jaarresultaten 2011
 Gereglementeerde informatie ThromboGenics Business Update en Jaarresultaten 2011 Leuven, België 8 maart 2012 - ThromboGenics NV (Euronext Brussels: THR), een biofarmaceutische onderneming die zich toelegt
Gereglementeerde informatie ThromboGenics Business Update en Jaarresultaten 2011 Leuven, België 8 maart 2012 - ThromboGenics NV (Euronext Brussels: THR), een biofarmaceutische onderneming die zich toelegt
ThromboGenics Business Update en Jaarcijfers 2009
 Gereglementeerde informatie Aankondiging in overeenstemming met de wet van 2 mei 2007 ThromboGenics Business Update en Jaarcijfers 2009 Record Kaspositie van 76,7 miljoen bij aanvang van een cruciaal 2010
Gereglementeerde informatie Aankondiging in overeenstemming met de wet van 2 mei 2007 ThromboGenics Business Update en Jaarcijfers 2009 Record Kaspositie van 76,7 miljoen bij aanvang van een cruciaal 2010
An Emerging Force in Ophthalmology and Vascular Medicine
 An Emerging Force in Ophthalmology and Vascular Medicine Jaarverslag 2009 Inhoud Over ThromboGenics........................................................... 02 Bouwen aan een succesvolle oftalmologische
An Emerging Force in Ophthalmology and Vascular Medicine Jaarverslag 2009 Inhoud Over ThromboGenics........................................................... 02 Bouwen aan een succesvolle oftalmologische
Nieuwe perspectieven. Van onderzoek tot toepassing
 Nieuwe perspectieven Van onderzoek tot toepassing ThromboGenics corporate highlights 2013 4 Voorzitter Dr. Staf Van Reet 2013, een jaar van groot belang We blijven geloven dat JETREA gaandeweg erkend
Nieuwe perspectieven Van onderzoek tot toepassing ThromboGenics corporate highlights 2013 4 Voorzitter Dr. Staf Van Reet 2013, een jaar van groot belang We blijven geloven dat JETREA gaandeweg erkend
Ontwikkelen van nieuwe geneesmiddelen voor diabetische oogziekten
 Persbericht 13 mei 2016 ThromboGenics Business Update Q1 2016 Ontwikkelen van nieuwe geneesmiddelen voor diabetische oogziekten Hoogtepunten ThromboGenics richt zich op de ontwikkeling van nieuwe geneesmiddelen
Persbericht 13 mei 2016 ThromboGenics Business Update Q1 2016 Ontwikkelen van nieuwe geneesmiddelen voor diabetische oogziekten Hoogtepunten ThromboGenics richt zich op de ontwikkeling van nieuwe geneesmiddelen
JETREA (ocriplasmine) PATIËNTENINFORMATIEPAKKET
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel JETREA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel JETREA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
ThromboGenics Business Update H1 2014
 GEREGLEMENTEERDE INFORMATIE ThromboGenics Business Update H1 2014 Financieel Inkomsten 7,1 miljoen in de eerste helft van 2014, vergeleken met 102,7 miljoen in dezelfde periode in 2013 (met inbegrip van
GEREGLEMENTEERDE INFORMATIE ThromboGenics Business Update H1 2014 Financieel Inkomsten 7,1 miljoen in de eerste helft van 2014, vergeleken met 102,7 miljoen in dezelfde periode in 2013 (met inbegrip van
ThromboGenics Business Update en Jaarcijfers 2010
 Gereglementeerde informatie ThromboGenics Business Update en Jaarcijfers 2010 Leuven, België 10 maart 2011 ThromboGenics NV (Euronext Brussels: THR), een biofarmaceutisch bedrijf dat zich toelegt op onderzoek
Gereglementeerde informatie ThromboGenics Business Update en Jaarcijfers 2010 Leuven, België 10 maart 2011 ThromboGenics NV (Euronext Brussels: THR), een biofarmaceutisch bedrijf dat zich toelegt op onderzoek
Innovatie tot bij de patiënt. Nieuwe behandelingen in de oogheelkunde
 Innovatie tot bij de patiënt Nieuwe behandelingen in de oogheelkunde Innovatie tot bij de patiënt Nieuwe behandelingen in de oogheelkunde 4 9 15 35 Innovatie tot bij de patiënt Overzicht Voorwoord - Dr.
Innovatie tot bij de patiënt Nieuwe behandelingen in de oogheelkunde Innovatie tot bij de patiënt Nieuwe behandelingen in de oogheelkunde 4 9 15 35 Innovatie tot bij de patiënt Overzicht Voorwoord - Dr.
INHOUD. 2 jaarverslag 2012 THROMBOGENICS
 JAARVERSLAG 2012 INHOUD 2 jaarverslag 2012 THROMBOGENICS Inhoud INLEIDING 4 Belangrijkste cijfers 2012 4 Interview met de CEO en de voorzitter 5 ThromboGenics in het kort 7 Missie 8 Ondernemingsdoelstellingen
JAARVERSLAG 2012 INHOUD 2 jaarverslag 2012 THROMBOGENICS Inhoud INLEIDING 4 Belangrijkste cijfers 2012 4 Interview met de CEO en de voorzitter 5 ThromboGenics in het kort 7 Missie 8 Ondernemingsdoelstellingen
ThromboGenics Business Update H1 2015
 Gereglementeerde informatie ThromboGenics Business Update H1 2015 ThromboGenics US herschikt in lijn met huidige JETREA marktvraag streefdoel break-even te zijn in US vanaf 2016 Voortgang klinische en
Gereglementeerde informatie ThromboGenics Business Update H1 2015 ThromboGenics US herschikt in lijn met huidige JETREA marktvraag streefdoel break-even te zijn in US vanaf 2016 Voortgang klinische en
Een kijk op 2011 Jaarverslag
 Een kijk op 2011 Jaarverslag 2 ThromboGenics Jaarverslag 2011 Inhoud Inleiding ThromboGenics in het kort...4 5 de IPO Anniversary...5 - Een toonaangevend oftalmologisch bedrijf worden...6 - Ocriplasmine
Een kijk op 2011 Jaarverslag 2 ThromboGenics Jaarverslag 2011 Inhoud Inleiding ThromboGenics in het kort...4 5 de IPO Anniversary...5 - Een toonaangevend oftalmologisch bedrijf worden...6 - Ocriplasmine
Gereglementeerde informatie Aankondiging in overeenstemming met de wet van 2 mei 2007
 Gereglementeerde informatie Aankondiging in overeenstemming met de wet van 2 mei 2007 ThromboGenics NV Geeft Business Update en Kondigt Halfjaarlijkse Resultaten aan voor 2009 Leuven, België 27 augustus
Gereglementeerde informatie Aankondiging in overeenstemming met de wet van 2 mei 2007 ThromboGenics NV Geeft Business Update en Kondigt Halfjaarlijkse Resultaten aan voor 2009 Leuven, België 27 augustus
ThromboGenics Business Update H1 2016
 Persbericht 25 augustus 2016 Gereglementeerde informatie ThromboGenics Business Update H1 2016 Voortgang ontwikkelingsportfolio: 4 programma s voor de ontwikkeling van nieuwe medicijnen voor de behandeling
Persbericht 25 augustus 2016 Gereglementeerde informatie ThromboGenics Business Update H1 2016 Voortgang ontwikkelingsportfolio: 4 programma s voor de ontwikkeling van nieuwe medicijnen voor de behandeling
Tussentijds Financieel Verslag Halfjaarcijfers per 30 juni 2013
 Onderstaand verslag betreft gereglementeerde informatie zoals bedoeld in het KB van 14/11/2007. Deze informatie kan u terugvinden op de website van ThromboGenics (www.thrombogenics.com) onder de sectie
Onderstaand verslag betreft gereglementeerde informatie zoals bedoeld in het KB van 14/11/2007. Deze informatie kan u terugvinden op de website van ThromboGenics (www.thrombogenics.com) onder de sectie
Samenvatting. Fase I. Fase II. Fase III. Tijdlijn klinische ontwikkeling
 Jaarverslag 2010 Samenvatting Tijdlijn klinische ontwikkeling Fase I De veiligheid van een nieuw kandidaat-geneesmiddel wordt voor het eerst geëvalueerd bij mensen. Fase II Het nieuwe kandidaat-geneesmiddel
Jaarverslag 2010 Samenvatting Tijdlijn klinische ontwikkeling Fase I De veiligheid van een nieuw kandidaat-geneesmiddel wordt voor het eerst geëvalueerd bij mensen. Fase II Het nieuwe kandidaat-geneesmiddel
Business update ThromboGenics volledig boekjaar 2014
 GEREGLEMENTEERDE INFORMATIE Business update ThromboGenics volledig boekjaar 2014 Financieel De totale inkomsten bedroegen 13,8 miljoen in 2014 (2013-112,8 miljoen, inclusief 90 miljoen aan mijlpaalbetalingen
GEREGLEMENTEERDE INFORMATIE Business update ThromboGenics volledig boekjaar 2014 Financieel De totale inkomsten bedroegen 13,8 miljoen in 2014 (2013-112,8 miljoen, inclusief 90 miljoen aan mijlpaalbetalingen
JETREA (ocriplasmine)
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel JETREA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel JETREA. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
zichtstoornissen als gevolg van maculaoedeem dat veroorzaakt wordt door diabetes;
 EMA/677928/2015 EMEA/H/C/002392 EPAR-samenvatting voor het publiek aflibercept Dit document is een samenvatting van het Europees openbaar beoordelingsrapport (EPAR) voor. Het geeft uitleg over de aanpak
EMA/677928/2015 EMEA/H/C/002392 EPAR-samenvatting voor het publiek aflibercept Dit document is een samenvatting van het Europees openbaar beoordelingsrapport (EPAR) voor. Het geeft uitleg over de aanpak
ThromboGenics Business Update H1 2018
 Persbericht 6 september 2018 Gereglementeerde informatie ThromboGenics Business Update H1 2018 Positieve topline resultaten van portfolio voor diabetische oogziekten Aandeelhouders geven goedkeuring naamsverandering
Persbericht 6 september 2018 Gereglementeerde informatie ThromboGenics Business Update H1 2018 Positieve topline resultaten van portfolio voor diabetische oogziekten Aandeelhouders geven goedkeuring naamsverandering
PERSBERICHT. Oxurion NV Business Update Boekjaar 2018
 Oxurion NV Business Update Boekjaar 2018 Significante vooruitgang met klinische ontwikkeling voor diabetische oogziekten Positieve toplijn resultaten van Fase 1/2 studie met THR-317 voor DME Meerdere klinische
Oxurion NV Business Update Boekjaar 2018 Significante vooruitgang met klinische ontwikkeling voor diabetische oogziekten Positieve toplijn resultaten van Fase 1/2 studie met THR-317 voor DME Meerdere klinische
Business Update. Gereglementeerde Informatie
 Business Update Gereglementeerde Informatie Leuven, België 13 mei 2008 (na beurstijd) ThromboGenics NV (Euronext Brussels: THR), een biotechnologisch bedrijf dat zich toespitst op innovatieve behandelingen
Business Update Gereglementeerde Informatie Leuven, België 13 mei 2008 (na beurstijd) ThromboGenics NV (Euronext Brussels: THR), een biotechnologisch bedrijf dat zich toespitst op innovatieve behandelingen
JETREA (ocriplasmine)
 Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel JETREA, om voor een goed gebruik ervan te zorgen en om de ongewenste effecten ervan te beperken, zijn er bepaalde
Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel JETREA, om voor een goed gebruik ervan te zorgen en om de ongewenste effecten ervan te beperken, zijn er bepaalde
Tussentijds Financieel Verslag Halfjaarcijfers per 30 Juni 2011
 Onderstaand verslag betreft gereglementeerde informatie zoals bedoeld in het KB van 14/11/2007. Deze informatie kan u terugvinden op de website van ThromboGenics (www.thrombogenics.com) onder de sectie
Onderstaand verslag betreft gereglementeerde informatie zoals bedoeld in het KB van 14/11/2007. Deze informatie kan u terugvinden op de website van ThromboGenics (www.thrombogenics.com) onder de sectie
LUCENTIS (ranibizumab)
 Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel LUCENTIS, om voor een goed gebruik ervan te zorgen en om de ongewenste effecten ervan te beperken, zijn er bepaalde
Om een maximaal voordeel te halen voor uw gezondheid uit de effecten van het geneesmiddel LUCENTIS, om voor een goed gebruik ervan te zorgen en om de ongewenste effecten ervan te beperken, zijn er bepaalde
Tussentijds Financieel Verslag Halfjaarcijfers per 30 juni 2012
 Onderstaand verslag betreft gereglementeerde informatie zoals bedoeld in het KB van 14/11/2007. Deze informatie kan u terugvinden op de website van ThromboGenics (www.thrombogenics.com) onder de sectie
Onderstaand verslag betreft gereglementeerde informatie zoals bedoeld in het KB van 14/11/2007. Deze informatie kan u terugvinden op de website van ThromboGenics (www.thrombogenics.com) onder de sectie
ThromboGenics Business Update FY 2017
 Persbericht 15 maart 2018 Gereglementeerde informatie ThromboGenics Business Update FY 2017 Vorderingen in preklinisch en klinisch onderzoek voor ontwikkeling portfolio diabetische oogziekten Wereldwijde
Persbericht 15 maart 2018 Gereglementeerde informatie ThromboGenics Business Update FY 2017 Vorderingen in preklinisch en klinisch onderzoek voor ontwikkeling portfolio diabetische oogziekten Wereldwijde
UITOEFENING VAN DE OVERTOEWIJZINGSOPTIE EN VERSTRIJKEN VAN DE STABILISATIEPERIODE IN VERBAND MET DE EERSTE OPENBARE AANBIEDING
 Gereglementeerde informatie UITOEFENING VAN DE OVERTOEWIJZINGSOPTIE EN VERSTRIJKEN VAN DE STABILISATIEPERIODE IN VERBAND MET DE EERSTE OPENBARE AANBIEDING Luik, België, 30 juli 2015-17.45 CEST Mithra Pharmaceuticals
Gereglementeerde informatie UITOEFENING VAN DE OVERTOEWIJZINGSOPTIE EN VERSTRIJKEN VAN DE STABILISATIEPERIODE IN VERBAND MET DE EERSTE OPENBARE AANBIEDING Luik, België, 30 juli 2015-17.45 CEST Mithra Pharmaceuticals
ThromboGenics kondigt halfjaarlijkse resultaten aan voor 2008
 ThromboGenics kondigt halfjaarlijkse resultaten aan voor 2008 Leuven, België 28 augustus 2008 - ThromboGenics NV (Euronext Brussel: THR), een biofarmaceutisch bedrijf dat zich toelegt op innovatieve behandelingen
ThromboGenics kondigt halfjaarlijkse resultaten aan voor 2008 Leuven, België 28 augustus 2008 - ThromboGenics NV (Euronext Brussel: THR), een biofarmaceutisch bedrijf dat zich toelegt op innovatieve behandelingen
Neuropore en UCB gaan wereldwijde samenwerking aan en sluiten overeenkomst
 Neuropore en UCB gaan wereldwijde samenwerking aan en sluiten overeenkomst Bedrijven werken samen aan de ontwikkeling van een ziekteveranderende behandelmogelijkheid met kleinmoleculair middel voor mensen
Neuropore en UCB gaan wereldwijde samenwerking aan en sluiten overeenkomst Bedrijven werken samen aan de ontwikkeling van een ziekteveranderende behandelmogelijkheid met kleinmoleculair middel voor mensen
Macula degeneratie. Naar het ziekenhuis? Lees eerst de informatie op
 Macula degeneratie Naar het ziekenhuis? Lees eerst de informatie op www.asz.nl/brmo. Inleiding Uw oogarts heeft met u besproken dat u een oogziekte heeft die macula degeneratie wordt genoemd. In deze
Macula degeneratie Naar het ziekenhuis? Lees eerst de informatie op www.asz.nl/brmo. Inleiding Uw oogarts heeft met u besproken dat u een oogziekte heeft die macula degeneratie wordt genoemd. In deze
LUCENTIS (ranibizumab)
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel LUCENTIS. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel LUCENTIS. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
ONBETREDEN PADEN VERKENNEN. Grensverleggende behandelingen voor diabetische retinopathie
 ONBETREDEN PADEN VERKENNEN Grensverleggende behandelingen voor diabetische retinopathie ONBETREDEN PADEN VERKENNEN Grensverleggende behandelingen voor diabetische retinopathie overzicht ONBETREDEN PADEN
ONBETREDEN PADEN VERKENNEN Grensverleggende behandelingen voor diabetische retinopathie ONBETREDEN PADEN VERKENNEN Grensverleggende behandelingen voor diabetische retinopathie overzicht ONBETREDEN PADEN
Zeldzame ziekten, weesgeneesmiddelen
 niet geautoriseerde Nederlandse vertaling Zeldzame ziekten, weesgeneesmiddelen De feiten op een rijtje De EMA wil graag dat Europese burgers met zeldzame ziekten toegang hebben tot specifieke en werkzame
niet geautoriseerde Nederlandse vertaling Zeldzame ziekten, weesgeneesmiddelen De feiten op een rijtje De EMA wil graag dat Europese burgers met zeldzame ziekten toegang hebben tot specifieke en werkzame
Capecitabine Accord moet permanent worden stopgezet bij patiënten die een ernstige huidreactie hebben gehad tijdens de behandeling.
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Lucentis (ranibizumab)
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Lucentis. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Lucentis. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
ThromboGenics Business Update H1 2017
 Persbericht 7 september 2017 Gereglementeerde informatie ThromboGenics Business Update H1 2017 Goede vordering in ontwikkeling portfolio voor diabetische oogziekten Oncurious nv breidt pijplijn uit met
Persbericht 7 september 2017 Gereglementeerde informatie ThromboGenics Business Update H1 2017 Goede vordering in ontwikkeling portfolio voor diabetische oogziekten Oncurious nv breidt pijplijn uit met
BIJLAGE 1 SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE 1 SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL JETREA 0,5 mg/0,2 ml concentraat voor oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke injectieflacon
BIJLAGE 1 SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL JETREA 0,5 mg/0,2 ml concentraat voor oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke injectieflacon
Onderwerp: Ernstige huidreacties geassocieerd met Capecitabine (Xeloda )
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Transparantiekennisgevingen overeenkomstig Artikel 14 van de wet van 2 mei 2007
 GEREGLEMENTEERDE INFORMATIE PERSBERICHT Transparantiekennisgevingen overeenkomstig Artikel 14 van de wet van 2 mei 2007 Leuven (BELGIË) 26 januari 2018, 22:00u CET TiGenix NV (Euronext Brussels en Nasdaq:
GEREGLEMENTEERDE INFORMATIE PERSBERICHT Transparantiekennisgevingen overeenkomstig Artikel 14 van de wet van 2 mei 2007 Leuven (BELGIË) 26 januari 2018, 22:00u CET TiGenix NV (Euronext Brussels en Nasdaq:
ThromboGenics Full Year 2016 Business Update
 Persbericht 16 maart 2017 Gereglementeerde informatie ThromboGenics Full Year 2016 Business Update Innovatief klinisch en pre-klinisch onderzoeksportfolio met focus op diabetische oogziekten biedt meerdere
Persbericht 16 maart 2017 Gereglementeerde informatie ThromboGenics Full Year 2016 Business Update Innovatief klinisch en pre-klinisch onderzoeksportfolio met focus op diabetische oogziekten biedt meerdere
UCB rapporteert solide groei van Cimzia, Vimpat en Neupro, positieve pijplijnontwikkelingen, en bevestigt financiële vooruitzichten
 Tussentijds verslag UCB voor de eerste negen maanden van 2013 UCB rapporteert solide groei van Cimzia, Vimpat en Neupro, positieve pijplijnontwikkelingen, en bevestigt financiële vooruitzichten Stabiele
Tussentijds verslag UCB voor de eerste negen maanden van 2013 UCB rapporteert solide groei van Cimzia, Vimpat en Neupro, positieve pijplijnontwikkelingen, en bevestigt financiële vooruitzichten Stabiele
Suikerziekte en het oog
 DIENST OOGZIEKTEN Campus Brugge Stafleden Dr. Dewachter Anne Dr. Pollet Luc Dr. Lafaut Bart Dr. Vandelanotte Sylvie Geconsulteerde artsen Dr. Miroir Claire Dr. Kempeneers Anne t: 050 45 23 40 f: 050 45
DIENST OOGZIEKTEN Campus Brugge Stafleden Dr. Dewachter Anne Dr. Pollet Luc Dr. Lafaut Bart Dr. Vandelanotte Sylvie Geconsulteerde artsen Dr. Miroir Claire Dr. Kempeneers Anne t: 050 45 23 40 f: 050 45
Persbericht. Brussel, België, 23 november 2006-7:00 am CET: UCB kondigde vandaag aan
 UCB S.A. Allée de la Recherche 60, B-1070 Brussels (Belgium) Persbericht CHMP geeft positief advies en beveelt goedkeuring aan van Keppra als adjuvante behandeling van primair veralgemeende tonisch-clonische
UCB S.A. Allée de la Recherche 60, B-1070 Brussels (Belgium) Persbericht CHMP geeft positief advies en beveelt goedkeuring aan van Keppra als adjuvante behandeling van primair veralgemeende tonisch-clonische
Bijsluiter: Informatie voor de patiënt. JETREA, 0,5 mg/0,2 ml, concentraat voor oplossing voor injectie Ocriplasmine
 Bijsluiter: Informatie voor de patiënt JETREA, 0,5 mg/0,2 ml, Ocriplasmine Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld.
Bijsluiter: Informatie voor de patiënt JETREA, 0,5 mg/0,2 ml, Ocriplasmine Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld.
Behandeling van macula oedeem met Avastin
 Behandeling van macula oedeem met Avastin De oogarts heeft bij u een oogafwijking vastgesteld en heeft in overleg met u besloten om dit te gaan behandelen met Avastin. De meest voorkomende oorzaken om
Behandeling van macula oedeem met Avastin De oogarts heeft bij u een oogafwijking vastgesteld en heeft in overleg met u besloten om dit te gaan behandelen met Avastin. De meest voorkomende oorzaken om
oplossing voor injectie
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Eylea. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Eylea. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
BEHANDELING VAN HET OOG MET AVASTING, LUCENTIS OF EYLEA FRANCISCUS VLIETLAND
 BEHANDELING VAN HET OOG MET AVASTING, LUCENTIS OF EYLEA FRANCISCUS VLIETLAND Inleiding Uw arts heeft bij u een aandoening aan uw netvlies vastgesteld. Het centrale gedeelte van uw netvlies (macula lutea)
BEHANDELING VAN HET OOG MET AVASTING, LUCENTIS OF EYLEA FRANCISCUS VLIETLAND Inleiding Uw arts heeft bij u een aandoening aan uw netvlies vastgesteld. Het centrale gedeelte van uw netvlies (macula lutea)
Bijsluiter: informatie voor de patiënt. JETREA, 0,5 mg/0,2 ml, concentraat voor oplossing voor injectie Ocriplasmine
 Bijsluiter: informatie voor de patiënt JETREA, 0,5 mg/0,2 ml, concentraat voor oplossing voor injectie Ocriplasmine Lees goed de hele bijsluiter voordat u dit geneesmiddel toegediend krijgt, want er staat
Bijsluiter: informatie voor de patiënt JETREA, 0,5 mg/0,2 ml, concentraat voor oplossing voor injectie Ocriplasmine Lees goed de hele bijsluiter voordat u dit geneesmiddel toegediend krijgt, want er staat
Bijsluiter: Informatie voor de patiënt. JETREA, 0,5 mg/0,2 ml, concentraat voor oplossing voor injectie Ocriplasmine
 Bijsluiter: Informatie voor de patiënt JETREA, 0,5 mg/0,2 ml, concentraat voor oplossing voor injectie Ocriplasmine Lees goed de hele bijsluiter voordat u dit geneesmiddel toegediend krijgt, want er staat
Bijsluiter: Informatie voor de patiënt JETREA, 0,5 mg/0,2 ml, concentraat voor oplossing voor injectie Ocriplasmine Lees goed de hele bijsluiter voordat u dit geneesmiddel toegediend krijgt, want er staat
PERSPECTIEVEN FOCUS OP NIEUWE BEHANDELINGEN TEGEN VERMINDERD GEZICHTSVERMOGEN
 PERSPECTIEVEN FOCUS OP NIEUWE BEHANDELINGEN TEGEN VERMINDERD GEZICHTSVERMOGEN Belangrijke mijlpalen in de strijd tegen verminderd gezichtsvermogen p. 4 Ontwikkeling van nieuwe geneesmiddelen op basis van
PERSPECTIEVEN FOCUS OP NIEUWE BEHANDELINGEN TEGEN VERMINDERD GEZICHTSVERMOGEN Belangrijke mijlpalen in de strijd tegen verminderd gezichtsvermogen p. 4 Ontwikkeling van nieuwe geneesmiddelen op basis van
OOGHEELKUNDE. Macula-degeneratie
 OOGHEELKUNDE Macula-degeneratie Macula-degeneratie Uw oogarts heeft u verteld dat de gele vlek (=macula) in uw oog door slijtage is aangetast. Deze aandoening wordt ook wel macula-degeneratie genoemd.
OOGHEELKUNDE Macula-degeneratie Macula-degeneratie Uw oogarts heeft u verteld dat de gele vlek (=macula) in uw oog door slijtage is aangetast. Deze aandoening wordt ook wel macula-degeneratie genoemd.
Avastin injecties in het oog. Poli Oogheelkunde
 00 Avastin injecties in het oog Poli Oogheelkunde 1 Inleiding Uw behandelend arts heeft met u gesproken over de behandeling van uw oogaandoening met Avastin injecties. Om de behandeling die bij u wordt
00 Avastin injecties in het oog Poli Oogheelkunde 1 Inleiding Uw behandelend arts heeft met u gesproken over de behandeling van uw oogaandoening met Avastin injecties. Om de behandeling die bij u wordt
Wat is een klinische studie?
 Wat is een klinische studie? Klinische studies Klinische studies Klinische studies worden verricht om de werkzaamheid van geneesmiddelen alsook combinaties van verschillende behandelingen te testen. Klinische
Wat is een klinische studie? Klinische studies Klinische studies Klinische studies worden verricht om de werkzaamheid van geneesmiddelen alsook combinaties van verschillende behandelingen te testen. Klinische
Tussentijds Financieel Verslag Halfjaarcijfers per 30 juni 2015
 Onderstaand verslag betreft gereglementeerde informatie zoals bedoeld in het KB van 14/11/2007. Deze informatie kan u terugvinden op de website van ThromboGenics (www.thrombogenics.com) onder de sectie
Onderstaand verslag betreft gereglementeerde informatie zoals bedoeld in het KB van 14/11/2007. Deze informatie kan u terugvinden op de website van ThromboGenics (www.thrombogenics.com) onder de sectie
UCB verbetert financiële vooruitzichten 2017 na sterke prestaties in eerste 9 maanden
 Brussel (België), vrijdag 20 oktober 2017 7:00 (CEST) gereguleerde informatie Tussentijds verslag UCB voor de eerste negen maanden van 2017: UCB verbetert financiële vooruitzichten 2017 na sterke prestaties
Brussel (België), vrijdag 20 oktober 2017 7:00 (CEST) gereguleerde informatie Tussentijds verslag UCB voor de eerste negen maanden van 2017: UCB verbetert financiële vooruitzichten 2017 na sterke prestaties
Maculadegeneratie (MD)
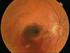 Maculadegeneratie (MD) Deze folder is samengesteld door de oogartsen prof.dr. C. B. Hoyng en prof.dr. J.E.E. Keunen. Inleiding In deze folder vindt u informatie over de leeftijdsgebonden maculadegeneratie
Maculadegeneratie (MD) Deze folder is samengesteld door de oogartsen prof.dr. C. B. Hoyng en prof.dr. J.E.E. Keunen. Inleiding In deze folder vindt u informatie over de leeftijdsgebonden maculadegeneratie
Financiële informatie
 Financiële informatie 2012 Inhoud Toekomstgerichte informatie Dit Jaarverslag bevat toekomstgerichte verklaringen, verwachtingen en inschattingen met betrekking tot de verwachte toekomstige prestaties
Financiële informatie 2012 Inhoud Toekomstgerichte informatie Dit Jaarverslag bevat toekomstgerichte verklaringen, verwachtingen en inschattingen met betrekking tot de verwachte toekomstige prestaties
Avastin-injecties. bij natte maculadegeneratie en maculaoedeem. Naar het ziekenhuis? Lees eerst de informatie op
 Avastin-injecties bij natte maculadegeneratie en maculaoedeem Naar het ziekenhuis? Lees eerst de informatie op www.asz.nl/brmo. Inleiding Uw oogarts heeft met u besproken dat uw oogaandoening behandeld
Avastin-injecties bij natte maculadegeneratie en maculaoedeem Naar het ziekenhuis? Lees eerst de informatie op www.asz.nl/brmo. Inleiding Uw oogarts heeft met u besproken dat uw oogaandoening behandeld
Avastin-injecties. bij natte maculadegeneratie en macula-oedeem
 Avastin-injecties bij natte maculadegeneratie en macula-oedeem Inleiding Uw oogarts heeft met u besproken dat uw oogaandoening behandeld kan worden met Avastin-injecties. In deze folder leest u meer over
Avastin-injecties bij natte maculadegeneratie en macula-oedeem Inleiding Uw oogarts heeft met u besproken dat uw oogaandoening behandeld kan worden met Avastin-injecties. In deze folder leest u meer over
Hoogtepunten. Persbericht 17 maart 2016. Strategische update
 Persbericht 17 maart 2016 Hoogtepunten Strategische update ThromboGenics strategie beoogt aandeelhouderswaarde te genereren met de ontwikkeling van innovatieve geneesmiddelen voor ziekten aan de achterkant
Persbericht 17 maart 2016 Hoogtepunten Strategische update ThromboGenics strategie beoogt aandeelhouderswaarde te genereren met de ontwikkeling van innovatieve geneesmiddelen voor ziekten aan de achterkant
JAARVERSLAG FINANCIËLE INFORMATIE
 2017 JAARVERSLAG FINANCIËLE INFORMATIE 2017 JAARVERSLAG FINANCIËLE INFORMATIE Inhoud 1. ALGEMENE INFORMATIE EN INFORMATIE BETREFFENDE DE VERANTWOORDELIJKHEID VOOR HET JAARVERSLAG EN VOOR DE CONTROLE
2017 JAARVERSLAG FINANCIËLE INFORMATIE 2017 JAARVERSLAG FINANCIËLE INFORMATIE Inhoud 1. ALGEMENE INFORMATIE EN INFORMATIE BETREFFENDE DE VERANTWOORDELIJKHEID VOOR HET JAARVERSLAG EN VOOR DE CONTROLE
1. NAAM VAN HET GENEESMIDDEL. JETREA 0,5 mg/0,2 ml concentraat voor oplossing voor injectie 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
 Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de gezondheidszorg worden verzocht alle vermoedelijke
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de gezondheidszorg worden verzocht alle vermoedelijke
UCB zet groeikoers voort in 2016
 Brussel (België), maandag 25 april 2016 7:00 (CEST) gereguleerde informatie Tussentijds verslag UCB voor de eerste drie maanden van 2016: UCB zet groeikoers voort in 2016 Productgroei zorgt voor omzetgroei
Brussel (België), maandag 25 april 2016 7:00 (CEST) gereguleerde informatie Tussentijds verslag UCB voor de eerste drie maanden van 2016: UCB zet groeikoers voort in 2016 Productgroei zorgt voor omzetgroei
oplossing voor injectie
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Eylea. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Eylea. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
1. NAAM VAN HET GENEESMIDDEL
 1. NAAM VAN HET GENEESMIDDEL DURATEARS oogzalf 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Dit geneesmiddel bevat geen werkzame stoffen. Hulpstof met gekend effect: 1 g oogzalf bevat 30 mg lanoline.
1. NAAM VAN HET GENEESMIDDEL DURATEARS oogzalf 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Dit geneesmiddel bevat geen werkzame stoffen. Hulpstof met gekend effect: 1 g oogzalf bevat 30 mg lanoline.
Diabetische Oogziekten
 Diabetische Oogziekten F. Hageman, Oogarts OPSIS oogziekenhuis Amstelveen Den Burg DIABETES MELLITUS GLUCOSE Bloedglucosespiegel : Maat voor hoeveelheid glucose opgelost in het bloed. Wordt uitgedrukt
Diabetische Oogziekten F. Hageman, Oogarts OPSIS oogziekenhuis Amstelveen Den Burg DIABETES MELLITUS GLUCOSE Bloedglucosespiegel : Maat voor hoeveelheid glucose opgelost in het bloed. Wordt uitgedrukt
Fagron zet sterke omzetgroei van eerste halfjaar door in derde kwartaal Fagron realiseert organische omzetgroei van 10,1%
 Gereglementeerde informatie Nazareth (België)/Rotterdam (Nederland) 1, 11 oktober 2018 Fagron zet sterke omzetgroei van eerste halfjaar door in derde kwartaal 2018 Fagron realiseert organische omzetgroei
Gereglementeerde informatie Nazareth (België)/Rotterdam (Nederland) 1, 11 oktober 2018 Fagron zet sterke omzetgroei van eerste halfjaar door in derde kwartaal 2018 Fagron realiseert organische omzetgroei
1. &NBSP;&NBSP;&NBSP;&NBSP;&NBSP; WAT IS THILO-TEARS EN WAARVOOR WORDT DIT MIDDEL
 THILOTEARS Bijsluiter: informatie voor de gebruiker THILOTEARS 3 mg/g ooggel Carbomeer Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor
THILOTEARS Bijsluiter: informatie voor de gebruiker THILOTEARS 3 mg/g ooggel Carbomeer Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor
ThromboGenics maakt jaarcijfers 2007 bekend
 ThromboGenics maakt jaarcijfers 2007 bekend Leuven, België - 13 maart 2008 - ThromboGenics NV (Euronext Brussels: THR), een biotechnologisch bedrijf dat zich toespitst op vasculaire ziekten, geeft vandaag
ThromboGenics maakt jaarcijfers 2007 bekend Leuven, België - 13 maart 2008 - ThromboGenics NV (Euronext Brussels: THR), een biotechnologisch bedrijf dat zich toespitst op vasculaire ziekten, geeft vandaag
Avastin injecties in het oog
 Avastin injecties in het oog Inleiding Uw behandelend arts heeft met u gesproken over de behandeling van uw oogaandoening met Avastin injecties. Om de behandeling die bij u wordt voorgesteld beter te begrijpen
Avastin injecties in het oog Inleiding Uw behandelend arts heeft met u gesproken over de behandeling van uw oogaandoening met Avastin injecties. Om de behandeling die bij u wordt voorgesteld beter te begrijpen
Inhoudsopgave. O ver Thro m b o G e n i c s 4. I n t e r v i ew met de Vo o r z i t t e r e n d e C E O van Thro m b o G e n i c s 1 0
 ThromboGenics Jaarverslag 2008 O ver Thro m b o G e n i c s 4 I n t e r v i ew met de Vo o r z i t t e r e n d e C E O van Thro m b o G e n i c s 1 0 B e l a n g r i j k ste ontwikkelingspro g ramma s
ThromboGenics Jaarverslag 2008 O ver Thro m b o G e n i c s 4 I n t e r v i ew met de Vo o r z i t t e r e n d e C E O van Thro m b o G e n i c s 1 0 B e l a n g r i j k ste ontwikkelingspro g ramma s
Behandeling maculadegeneratie
 Een echte behandeling die de oorzaak van maculadegeneratie (MD) aanpakt, is er helaas niet. De behandeling is erop gericht om het ziekteproces stabiel te krijgen. Door uw leefgewoonten aan te passen, kunnen
Een echte behandeling die de oorzaak van maculadegeneratie (MD) aanpakt, is er helaas niet. De behandeling is erop gericht om het ziekteproces stabiel te krijgen. Door uw leefgewoonten aan te passen, kunnen
MINNELIJKE SCHIKKING GEFORMULEERD DOOR DE AUDITEUR VAN DE FSMA EN WAARMEE THROMBOGENICS NV HEEFT INGESTEMD
 MINNELIJKE SCHIKKING GEFORMULEERD DOOR DE AUDITEUR VAN DE FSMA EN WAARMEE THROMBOGENICS NV HEEFT INGESTEMD Deze minnelijke schikking, waarmee ThromboGenics NV op 12 december 2016 voorafgaandelijk heeft
MINNELIJKE SCHIKKING GEFORMULEERD DOOR DE AUDITEUR VAN DE FSMA EN WAARMEE THROMBOGENICS NV HEEFT INGESTEMD Deze minnelijke schikking, waarmee ThromboGenics NV op 12 december 2016 voorafgaandelijk heeft
MACULA PUCKER FRANCISCUS GASTHUIS
 MACULA PUCKER FRANCISCUS GASTHUIS Inleiding Een Macula Pucker is een dun vliesje op het netvlies op de plaats van het scherp zien (de gele vlek of macula). Rondom de gele vlek wordt het netvlies in plooitjes
MACULA PUCKER FRANCISCUS GASTHUIS Inleiding Een Macula Pucker is een dun vliesje op het netvlies op de plaats van het scherp zien (de gele vlek of macula). Rondom de gele vlek wordt het netvlies in plooitjes
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL DURATEARS Z, oogzalf. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING DURATEARS Z oogzalf bevat geen werkzame stof. Voor de
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1 1. NAAM VAN HET GENEESMIDDEL DURATEARS Z, oogzalf. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING DURATEARS Z oogzalf bevat geen werkzame stof. Voor de
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER. ALCON EYE GEL 3 mg/g ooggel Carbomeer
 BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER ALCON EYE GEL 3 mg/g ooggel Carbomeer Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor u. Gebruik
BIJSLUITER: INFORMATIE VOOR DE GEBRUIKER ALCON EYE GEL 3 mg/g ooggel Carbomeer Lees goed de hele bijsluiter voordat u dit geneesmiddel gaat gebruiken want er staat belangrijke informatie in voor u. Gebruik
Oogheelkunde Behandeling van natte maculadegeneratie met Avastin
 Oogheelkunde Behandeling van natte maculadegeneratie met Avastin Inleiding De oogarts heeft bij u de diagnose natte maculadegeneratie (zie folder maculadegeneratie) gesteld. In overleg met u is besloten
Oogheelkunde Behandeling van natte maculadegeneratie met Avastin Inleiding De oogarts heeft bij u de diagnose natte maculadegeneratie (zie folder maculadegeneratie) gesteld. In overleg met u is besloten
JAARVERSLAG. Financiële informatie 2015
 JAARVERSLAG Financiële informatie 2015 JAARVERSLAG FINANCIËLE INFORMATIE 2015 Inhoud 1. ALGEMENE INFORMATIE EN INFORMATIE BETREFFENDE DE VERANTWOORDELIJKHEID VOOR HET JAARVERSLAG EN VOOR DE CONTROLE
JAARVERSLAG Financiële informatie 2015 JAARVERSLAG FINANCIËLE INFORMATIE 2015 Inhoud 1. ALGEMENE INFORMATIE EN INFORMATIE BETREFFENDE DE VERANTWOORDELIJKHEID VOOR HET JAARVERSLAG EN VOOR DE CONTROLE
Macula degeneratie. Albert Schweitzer ziekenhuis polikliniek Oogheelkunde augustus 2014 pavo 0536
 Macula degeneratie Albert Schweitzer ziekenhuis polikliniek Oogheelkunde augustus 2014 pavo 0536 Inleiding Uw oogarts heeft met u besproken dat u een oogaandoening heeft die macula degeneratie genoemd
Macula degeneratie Albert Schweitzer ziekenhuis polikliniek Oogheelkunde augustus 2014 pavo 0536 Inleiding Uw oogarts heeft met u besproken dat u een oogaandoening heeft die macula degeneratie genoemd
