Richtlijn voor diagnostiek en behandeling van de ziekte van Waldenström
|
|
|
- Thomas de Graaf
- 8 jaren geleden
- Aantal bezoeken:
Transcriptie
1 Richtlijn voor diagnostiek en behandeling van de ziekte van Waldenström Guidelines for diagnosis and management of Waldenström s macroglobulinemia J.M.I. Vos, M.C. Minnema, P.W. Wijermans, S. Croockewit, M.E.D. Chamuleau, S.T. Pals, S.K. Klein, M. Delforge, G.W. van Imhoff en M.J. Kersten, namens de HOVON Multipel Myeloomwerkgroep en de HOVON Lymfoomwerkgroep Samenvatting Namens de Werkgroepen Lymfoom en Multipel Myeloom van de Nederlands/Belgische stichting Hemato-Oncologie voor Volwassenen Nederland (HOVON) is een richtlijn voor diagnostiek en behandeling van morbus Waldenström (MW) opgesteld. Gezien het indolente beloop en de heterogene, deels unieke symptomatologie zijn de juiste behandelindicatie en geïndividualiseerde therapiekeuze voor patiënten met MW belangrijk. Grote onderzoeken ontbreken gezien de zeldzaamheid van deze aandoening. In deze richtlijn geven wij, op basis van de beschikbare gegevens, een praktische diagnostische classificatie en aanbevelingen voor eerstelijnsbehandeling, alsook mogelijkheden bij recidief. (Ned Tijdschr Hematol 2012;9:219-31) Summary On behalf of the lymphoma and multiple myeloma working parties of the Dutch/Belgian Haemato- Oncology Foundation for Adults in the Netherlands (HOVON), we present a guideline for diagnosis and management of Waldenström s macroglobulinemia (WM). Considering the indolent behavior and heterogeneous clinical presentation of WM, it is crucial to determine the right indications for treatment, as well as to individualize therapeutic options. There is a lack of large clinical trials due to the low incidence of WM. Based on the available data, we provide a practical diagnostic classification, as well as recommendations for first line therapy and options for treating relapsed disease. Inleiding Morbus Waldenström (MW) is in de laatste World Health Organization (WHO)-classificatie (2008) gedefinieerd als een maligniteit bestaande uit kleine B-lymfocyten, plasmacytoïde lymfocyten en plasmacellen, gepaard gaande met een paraproteïnemie Auteurs: mw. drs. J.M.I. Vos, internist-hematoloog, afdeling Interne Geneeskunde/Hematologie, St. Antonius Ziekenhuis Nieuwegein, mw. dr. M.C. Minnema, internist-hematoloog, afdeling Hematologie, UMC Utrecht, dhr. dr. P.W. Wijermans, internist-hematoloog, afdeling Hematologie, Haga ziekenhuis, dhr. dr. S. Croockewit, internist-hematoloog, afdeling Hematologie, UMC St Radboud, mw. dr. M.E.D. Chamuleau, internist-hematoloog, afdeling Hematologie, VU medisch centrum, dhr. prof. dr. S.T. Pals, patholoog, afdeling Pathologie, Academisch Medisch Centrum, mw. dr. S.K. Klein, internist-hematoloog, afdeling Interne Geneeskunde/Hematologie, Meander Medisch Centrum, dhr. prof. dr. M. Delforge, hematoloog, afdeling Hematologie, KU Leuven, dhr. dr. G.W. van Imhoff, internist-hematoloog, afdeling Interne Geneeskunde/Hematologie, UMC Groningen, mw. dr. M.J. Kersten, internist-hematoloog, afdeling Interne Geneeskunde/Hematologie, Academisch Medisch Centrum, namens de HOVON Multipel Myeloomwerkgroep en de HOVON Lymfoomwerkgroep. Correspondentie graag richten aan mw. dr. M.J. Kersten, internist-hematoloog, afdeling Interne Geneeskunde/Hematologie, F4-224, Academisch Medisch Centrum, Meibergdreef 9, 1105 AZ Amsterdam, tel.: , adres: m.j.kersten@amc.nl Belangenconflict: geen gemeld. Financiële ondersteuning: geen gemeld. Trefwoorden: HOVON, lymfoomwerkgroep, lymfoplasmacytair lymfoom, m. Waldenström, multipelmyeloomwerkgroep, NHL, richtlijn Key words: guideline, HOVON, lymphoma working party, lymphoplasmacytic lymphoma, multiple myeloma working party, NHL, Waldenström s macroglobulinemia 219
2 (M-proteïne) van het IgM-type, waarbij niet wordt voldaan aan diagnostische criteria voor andere kleincellige B-celmaligniteiten. De term lymfoplasmocytair lymfoom (LPL) wordt gebruikt voor die zeldzame gevallen waarbij het IgM-M-proteïne ontbreekt (minder dan 5%). In deze richtlijn zal dan ook de term MW (M. Waldenström) worden gebruikt. In de Engelstalige literatuur is de meest gebruikte term Waldenström s macroglobulinaemia. 1-4 De Zweedse arts Jan Gösta Waldenström ( ) beschreef deze ziekte voor het eerst in Het betreft een zeldzaam type lymfoom: wereldwijd is de incidentie ongeveer 3 per miljoen personen per jaar. In Nederland zijn er ongeveer nieuwe gevallen per jaar (bron: Nederlandse kankerregistratie). De gemiddelde leeftijd bij diagnose is 5 jaar. Hoewel het therapeutisch arsenaal zeer uitgebreid is, is MW niet te genezen. Vaak is, conform het beleid bij andere indolente lymfomen, bij asymptomatische patiënten dan ook een wait and see -beleid aangewezen. De prognose is zeer wisselend met een mediane overleving van 5 tot meer dan 10 jaar. Door het feit dat het een oudere populatie betreft in combinatie met het indolente beloop, overlijdt echter de helft van de patiënten aan een andere oorzaak dan aan het lymfoom. In deze richtlijn leest u over de diagnostiek, de prognose en de behandeling van MW. Diagnostiek en indeling Voor het stellen van de diagnose M. Waldenström dient sprake te zijn van een IgM-M-proteïne en een lymfoplasmocellulair infiltraat, vrijwel altijd gelokaliseerd in het beenmerg. Afhankelijk van wel of niet aan MW te relateren klachten is er sprake van symptomatische MW (met behandelindicatie) of asymptomatische MW (dit laatste geeft een grotere kans op progressie dan IgM- monoclonal gammopathy of unknown significance (MGUS)) (zie Tabel 1, 2 en 3). Met nadruk is een IgM-paraproteïne van welke hoogte dan ook op zichzelf niet voldoende voor de diagnose MW, aangezien ook andere lymfoproliferatieve ziekten met IgM-productie gepaard kunnen gaan (zie Differentiaaldiagnose). De hoogte van het IgM is zelden voorspellend voor het ontstaan van klachten en ook niet altijd een betrouwbare marker voor de tumorlast en de mate van beenmerginfiltratie. 1-4 Symptomatologie, anamnese en lichamelijk onderzoek Ongeveer eenderde van de patiënten is asymptomatisch bij diagnose. De morbiditeit van MW wordt zowel bepaald door de weefselinfiltratie en immunologische eigenschappen van de neoplastische cellen, als door de fysisch-chemische en immunologische eigenschappen van het monoklonale IgM-eiwit. In de klinische presentatie verschilt MW daarom duidelijk van andere maligne lymfomen. Een uitgebreide anamnese is essentieel, evenals een volledig lichamelijk onderzoek, met speciale aandacht voor lymfadenopathie, hepatosplenomegalie, neuropathie, auto-immuunfenomenen en verschijnselen van hyperviscositeit (voor een uitgebreid overzicht van symptomatologie zie Tabel 1). 5 De meest voorkomende klacht is vermoeidheid, soms veroorzaakt door een diepe anemie. De anemie is vaak meer uitgesproken dan op basis van de mate van beenmerginfiltratie zou worden verwacht. Hemolyse, anemie van de chronische ziekte door pro-inflammatoire factoren, verdunning door toegenomen plasmavolume, en gastro-intestinaal bloedverlies kunnen hieraan bijdragen. Een verhoogde bloedingsneiging kan via verschillende mechanismen bij tot 20% van de patiënten voorkomen. Hepatosplenomegalie en lymfadenopathie door infiltratie van lymfoomcellen zijn zeker niet obligaat en komen slechts bij 15-20% van de patiënten bij presentatie voor. IgM-gemedieerde auto-immuunfenomenen zijn een heel kenmerkende manifestatie van MW en kunnen ook de presenterende klacht zijn. Het meest voorkomend zijn neuropathie door anti-mag ( myelin associated glycoprotein )-IgM-antistoffen en autoimmuunhemolyse veroorzaakt door anti-i- of anti-i- IgM-antistofwerking met complementactivatie (koude agglutininen). Bij ongeveer 10% van de gevallen vormt het IgM een precipitaat (cryoglobuline) wanneer de temperatuur onder 37 C zakt; dit kan leiden tot klachten als vasculitis, raynaudfenomeen, glomerulonefritis of gewrichtsklachten. Neerslag van het M- proteïne als amyloïd kan leiden tot orgaanschade, zoals nefropathie, cardiomyopathie, neuropathie of gastro-intestinale problemen. Aangeraden wordt ook aandacht aan de familieanamnese te besteden, aangezien bij MW soms sprake 220
3 NEDERLANDS TIJDSCHRIFT VOOR HEMATOLOGIE Tabel 1. Klinische verschijnselen bij M. Waldenström, frequentie en mechanisme. Verschijnsel Percentage aanwezig bij diagnose Mechanisme/letten op vermoeidheid ±70% anemie constitutioneel cave amyloïdose constitutionele symptomen (nachtzweten, afvallen) 20-25% constitutioneel lymfadenopathie/organomegalie 15-25% tumorinfiltratie anemie 40% beenmerginfiltratie hemolyse ijzergebrek door bloedverlies uit tractus digestivus hyperviscositeit: hoofdpijn, visusklachten, verwardheid, bloedneuzen 15% direct doen: fundoscopie overweeg spoedplasmaferese hemorragische diathese 20-30% trombopenie, eventueel ook door idiopathische trombocytopenische purpura verworven vonwillebrandziekte amyloïdose neurologische klachten (vooral polyneuropathie) 20-25% IgM-antistoffen tegen myelin-associated glycoprotein (MAG), ganglioside M1 (GM1) of myopathie (antidecorineantistoffen) amyloïdose bing-neelsyndroom: neurologisch beeld met vaak lokalisatie MW in de liquor en afwijkende MRI hersenen. raynaudfenomeen (11%), acrocyanose of perifere ulcera zeldzaam tot 20% heeft aantoonbare cryoglobulines, slechts <5% heeft klachten daarbij 5-10% koude agglutinatie door tumorinfiltratie of nog onbegrepen humorale factoren, zoals depositie van IgM in cerebro cryoglobulinemie koude agglutinatie let op: IgM ook meten onder warme omstandigheden maag-darmklachten, vooral diarree, kolieken onbekend amyloïdose of IgM-depositie lokale tumorinfiltratie zeldzamer: op basis van autonome neuropathie gehoorverlies onbekend hyperviscositeit, sensorineuraal op basis van neuropathie tumorlokalisatie, trombusvorming trombose onbekend antifosfolipidensyndroom op basis van IgM-antifosfolipidenantistoffen huidproblemen: urticaria, papuleuze of bulleuze dermatitis, vasculitis <5% schnitzlersyndroom (IgM-paraproteïne en urticariële huidafwijkingen), tumorinfiltratie, amyloïdose, koude agglutinatie cryoglobulinemie nierinsufficiëntie zeldzaam glomerulonefritis door specifiek IgM amyloïdose, vasculitis overweeg nierbiopt osteolytische laesies in principe niet bij aanwezigheid osteolytische laesies: toch multipel myeloom als diagnose overwegen! recidiverende infecties onbekend door hypogammaglobulinemie, overweeg antibioticaprofylaxe of suppletie met intraveneuze immuunglobuline 221
4 Tabel 2. Diagnostiek (vetgedrukte items bij iedere nieuwe patiënt bepalen). Test serumeiwitelektroforese met kwantitatieve M-proteïnebepaling; immuunfixatie immuunglobulines IgA, IgM, IgG bloedbeeld, protrombinetijd, activated partial-thromboplastin time (APTT), leverenzymen, nierfunctie beenmergonderzoek (botbiopt) met morfologie (en eventueel immuunfenotypering, cytogenetica, alleen bij diagnostische twijfel) computertomografie hals/thorax/abdomen hemolyseparameters (lactaatdehydrogenase, haptoglobine, reticulocyten), eventueel gevolgd door coombs-test, koude agglutinines B2-microglobuline en albumine viscositeitmeting en consult oogarts hepatitis-c- en hepatitis-b-serologie antimyelineglycoproteïne, anti-ganglioside- M1, antisulfatide IgM en neurologische evaluatie inclusief elektromyogram bij verdenking amyloïdose gericht biopt Opmerkingen lichte ketens serum/urine: in principe niet let op: bij verdenking cryoglobulinemie ook afname van IgM onder warme omstandigheden eventueel ijzerstatus bij verdenking ijzergebreksanemie zie tekst immuunofenotypering optioneel, kan soms bijdragen aan de differentiaaldiagnose ten opzichte van andere kleincellige B-cel-non-hodgkinlymfomen wordt aanbevolen ter stadiëring voor start behandeling bij anemie hoewel <5% van de patiënten met MW koude agglutinines heeft, heeft andersom 50% van de patiënten met koude agglutinatie MW prognostische markers bij klinische verdenking op hyperviscositeit kan een viscositeitsmeting worden gedaan, maar de diagnose kan ook alleen op de kliniek worden gesteld, waarbij ook oogheelkundig onderzoek dient plaats te vinden mixed (type II) cryoglobulinemie is sterk geassocieerd met hepatitis C. De associatie met MW zelf is onduidelijk. Beide zijn relevant voor start van eventuele immuun(chemo)therapie bij polyneuropathie ter differentiatie oorzaak buikvetaspiraat als er geen gemakkelijk te biopteren aangedaan orgaan is, ook beenmerg laten kleuren op congorood is van familiaire clustering, ook van andere lymfoproliferatieve ziekten. Tot slot is er door de grootte van het IgM-paraproteïne kans op hyperviscositeit met daarbij behorende klachten: visusstoornissen, hoofdpijn, duizeligheid, hartfalen en neurologische uitvalsverschijnselen. Bij verdenking op hyperviscositeit dient direct een oogheelkundig onderzoek ter diagnostiek te worden verricht. Aanvullend onderzoek Zie Tabel 2 voor te verrichten aanvullend onderzoek bij diagnose. Beenmergonderzoek Beenmergonderzoek (in elk geval een botbiopt) is nodig voor het stellen van de diagnose, aangezien dit lymfoom zich bij voorkeur, en vaak alleen maar, in het beenmerg manifesteert. Kenmerkend is een infiltratie van het beenmerg met kleine B-lymfocy- 222
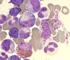
5 NEDERLANDS TIJDSCHRIFT VOOR HEMATOLOGIE Figuur 1. Beenmerg met lokalisatie M. Waldenström. Diffuse infiltratie van het beenmerg door kleine B-lymfocyten (links). Deze cellen zijn CD20-positief (midden). Een deel toont plasmacytaire differentiatie met intracytoplasmatische expressie van IgM (rechts). ten, plasmacytoïde lymfocyten en plasmacellen (zie Figuur 1). Karakteristieke kenmerken bij immuunfenotypering zijn expressie van B-celantigenen (CD19/20/22/79a), membraangebonden IgM en in de plasmacytaire cellen cytoplasmatisch IgM; afwezigheid van expressie van IgD, CD10, CD23 en CD103. CD5 is meestal negatief, indien positief moeten chronische lymfatische leukemie (CLL) en mantelcellymfoom (MCL) worden uitgesloten. Verder zijn CD38 en CD27 vaak positief. De plasmacellen zijn CD138-positief. 1,4,7 Immuunfenotypering van het beenmergaspiraat is niet obligaat indien immuunhistochemie wordt verricht op het botbiopt, maar kan bijdragen aan de differentiaaldiagnose ten opzichte van andere indolente B- cellymfomen. Cytogenetica/moleculaire markers Bij MW zijn verschillende cytogenetische afwijkingen beschreven, zoals een q-deletie en t(9;14)(p13;q32) die beiden bij 40-50% van de patiënten voorkomen. Op de jaarlijkse bijeenkomst van de American Society of Hematology (ASH) in december 2011 werd door Steve Treon et al. gepresenteerd dat bij 27 van 30 patiënten 1 specifieke puntmutatie (L25P) in het bij de NFκB-cascade betrokken gen MYD88 bleek te bestaan. Deze afwijkingen hebben vooralsnog echter geen prognostische of therapeutische consequenties. 8 Routinematig cytogenetisch of moleculair onderzoek is derhalve op dit moment niet geïndiceerd. Wel kan gerichte fluorescentie-in-situhybridisatieonderzoek (FISH)-analyse worden verricht als er verdenking is op multipel myeloom of folliculair lymfoom (zie Differentiaaldiagnose). Beeldvorming Ter stadiëring, bijvoorbeeld voor start behandeling, wordt een conventionele computertomografie (CT)- scan aanbevolen van hals, thorax en abdomen. Een positronemissietomografie (PET)-scan is niet geïndiceerd, tenzij er verdenking op transformatie bestaat. Indeling IgM-gerelateerde aandoeningen (zie Tabel 3, pagina 224) Qua diagnostische indeling ligt MW tussen de plasmaceldyscrasieën en non-hodgkinlymfomen in. De WHOclassificatie en belangrijke internationale richtlijnen verschillen hierin op sommige punten. 1,4 Voor de clinicus is vooral relevant dat er situaties zijn die een afwachtend beleid rechtvaardigen (IgM-MGUS, asymptomatische MW) en situaties die therapie behoeven (symptomatische MW, IgM-gerelateerde aandoeningen). IgM-MGUS/asymptomatische M. Waldenström De kans op progressie van een IgM-MGUS naar MW 223
6 Tabel 3. Diagnostische indeling van M. Waldenström (MW). IgM-MGUS asymptomatische MW symptomatische MW IgM-gerelateerde ziekte IgM-M-proteïne (serum) ja ja ja ja lymfoplasmocytair infiltraat (beenmerg) MW-gerelateerde symptomatologie nee ja ja nee nee nee ja ja beleid vervolgen wait and see behandeling afhankelijk van welke manifestatie, zie tekst kans op progressie naar MW 1,5% per jaar 50-0% na 5 jaar n.v.t. onbekend is ongeveer 1,5% per jaar. Als er wel duidelijke beenmerginfiltratie is (asymptomatische MW) is de kans op het ontstaan van een behandelindicatie in een recente retrospectieve studie % na 1 jaar, 39% na 3 jaar, 59% na 5 jaar en 8% na 10 jaar. 9,10 Symptomatische MW en IgM-gerelateerde ziekte Als er sprake is van IgM-M-proteïne, beenmerginfiltratie en bij het lymfoom passende symptomen, wordt de diagnose symptomatische MW gesteld en bestaat er dus een behandelindicatie. Tegelijkertijd kan echter een kleine hoeveelheid IgMparaproteïne ook al klachten geven, bijvoorbeeld door het ontstaan van neuropathie, amyloïdose of autoimmuniteit, zonder dat er daarbij aanwijzingen zijn voor LPL in het beenmerg. Deze patiënten voldoen dus niet aan de criteria voor MW, maar hebben wel daarbij passende symptomatologie. Daarvoor is de term IgM-gerelateerde ziekte bedacht. Ondanks een kleine tumorload kan er in zo n geval dan wel degelijk een behandelindicatie zijn, waarbij de therapiekeuze wordt bepaald door de specifieke uitingsvorm. 4 Differentiaaldiagnose: lymfoplasmocytair lymfoom zonder IgM-paraproteïne, andere indolente lymfomen en IgMmultipel myeloom Vooral bij het zeldzame LPL zonder IgM-paraproteïne (<5%) is de diagnose lastig en afhankelijk van het uitsluiten van andere kleincellige lymfomen, zoals het marginalezonelymfoom. Soms kan geen definitief onderscheid worden gemaakt. Bij opvallende paratrabeculaire infiltratie (in tegenstelling tot interstitieel) moet ook worden gedacht aan folliculair lymfoom, wat meestal CD10-positief is en eventueel kan worden bevestigd door aantonen van de t(14;18)-translocatie. Bij een LPL met een IgA- of IgG-type paraproteïne kan het onderscheid met een multipel myeloom een valkuil zijn. Andersom bestaat ook het multipel myeloom met een IgM-paraproteïne, hoewel zeldzaam. In tegenstelling tot MW is er bij een IgM-multipel myeloom meestal een translocatie t(11;14) aanwezig en zijn er vaak lytische botlaesies. Prognose De mediane overleving ligt tussen 5 en 11 jaar met een grote spreiding, waarbij er ook een groep patiënten bestaat die langdurig (>10 jaar) klachtenvrij kan blijven zonder behandeling. De IPSS-WM ( International Prognostic Scoring System for WM ) geeft een idee over de prognose (zie Tabel 4). Deze IPSS-score is gebaseerd op patiëntengegevens uit het pre-rituximab-tijdperk, maar is na die tijd in ieder geval in 1 studie gevalideerd, waarbij de prognose nog wat beter lijkt. De IPSS-score is geen leidraad voor behandelindicatie of behandelstrategie, maar is wel belangrijk bij het vergelijken van patiëntenuitkomsten, bijvoorbeeld bij klinische studies. 11 Behandeling Door de zeldzaamheid van MW en het daardoor 224
7 NEDERLANDS TIJDSCHRIFT VOOR HEMATOLOGIE Tabel 4. De International Prognostic Scoring System for Waldenström s macroglobulinemia (IPSS-WM). Item Score leeftijd >5 jaar 1 hemoglobine <7,2 mmol/l 1 trombocytengetal <100 x 10 9 /l 1 β2-microglobuline >3 mg/l 1 IgM-M-proteïne >70 g/l 1 Risicogroep Score Mediane overleving (maanden) laag 0-1 (m.u.v. leeftijd) 143 intermediair 2, of leeftijd >5 jaar 99 hoog 3 44 grotendeels ontbreken van gerandomiseerde studies, is het niet eenvoudig evidence-based richtlijnen voor de behandeling te geven. Dit geldt ook voor de keuze van eerstelijnstherapie. In Tabel 5, pagina 22, worden verschillende behandelschema s beschreven. In de literatuur zijn recente overzichten beschikbaar van de (soms schaarse) gepubliceerde gegevens betreffende effectiviteit. 2,3,5,12-14 Uitgangspunt is dat er vele werkzame combinaties zijn en dat de therapiekeuze aan de patiënt kan worden aangepast, vooral gebaseerd op leeftijd, levensverwachting, comorbiditeit en klinische noodzaak tot snelle respons. Op dit moment zijn sommige zeer effectieve middelen, zoals bortezomib, niet specifiek geregistreerd voor de indicatie MW, wat tot problemen met betrekking tot de vergoeding kan leiden. Overigens is bendamustine inmiddels in Nederland goedgekeurd voor de indicatie rituximab-refractair indolent nonhodgkinlymfoom. Plasmaferese Bij patiënten met hyperviscositeitssyndroom is er een indicatie voor plasmaferese en dient direct te worden gestart met een behandeling waarvan snelle respons kan worden verwacht om de productie van het M- proteïne af te remmen. Plasmaferese kan eventueel ook worden toegepast als preventieve maatregel bij patiënten die starten met rituximab en een totaal IgM-gehalte >40 g/l hebben, vanwege de kans op het ontstaan van hyperviscositeit door een IgM- flare na rituximab. Een praktisch alternatief is in deze situatie te starten met chemotherapie en pas rituximab toe te voegen als het IgM-gehalte is gedaald. Keuze van systemische behandeling Eerstelijnstherapie Immuunchemotherapie In 1 van de weinige gerandomiseerde studies uitgevoerd bij patiënten met MW, lieten Buske et al. zien dat ook bij MW de toevoeging van rituximab aan chemotherapie leidt tot hogere responspercentages en langere tijd tot progressie. 15 Op dit moment wordt immuunchemotherapie dan ook gezien als standaard voor de eerstelijnsbehandeling. De combinatie rituximab met alkylerende middelen, zoals cyclofosfamide en steroïden, wordt meestal goed verdragen. In een vergelijkend overzichtsartikel (er is geen gerandomiseerd onderzoek hiernaar verricht) bleek dat de responspercentages en -duur voor R-CP versus R-CHOP en R-CVP ongeveer vergelijkbaar zijn, terwijl de laatste 2 schema s meer toxiciteit geven (voornamelijk neutropene koorts en neuropathie). 1 Een goed alternatief is het DRC-schema (dexamethason, rituximab, cyclofosfamide), wat als voordeel heeft dat het weinig myelosuppressief is door de lagere dosis 225
8 Tabel 5. Kuurschema s. Verschillende schema s worden gebruikt. Dit geldt als globale leidraad zoals beschreven in de desbetreffende literatuur. Voor comedicatie zoals anti-emetica en antimicrobiële profylaxe verwijzen wij naar uw lokale protocol. Naam Interval Aantal cycli R-CP interval: 21 dagen aantal cycli: -8 DRC interval: 21 dagen aantal cycli: -8 Rituximab-monotherapie interval: 1 x/week aantal toedieningen: 4 chloorambucil eventueel in combinatie met rituximab (375 mg/m 2 op dag 1) bijvoorbeeld: interval: 28 dagen aantal cycli: afhankelijk van respons (na bereiken maximale respons nog 2 cycli) fludarabine-rituximab interval: 4 weken aantal cycli: 4- F-CR interval: 28 dagen aantal cycli: 4- R-bendamustine interval: 28 dagen aantal cycli: BRD interval: eerste 4 kuren van 3 weken, vervolgens van 3 maanden aantal cycli: 4 inductiekuren, 4 onderhoudskuren Dosis rituximab 375 mg/m 2 i.v. dag 1 cyclofosfamide 300 mg/m 2 per os dag 1 t/m 5 prednisolon 40 mg/m 2 per os dag 1 t/m 5 dexamethason 20 mg i.v. dag 1 rituximab 375 mg/m 2 i.v. dag 1 cyclofosfamide 100 mg/m 2 2 dd per os dag 1 t/m 5 rituximab 375 mg/m 2 i.v. dag 1, 8, 15, 22 chloorambucil: bijvoorbeeld 10 mg/m 2 per os dag 1 t/m 7 of 10 mg 1 dd flat dose dag 1-14 (N.B. er zijn veel alternatieve schema s in omloop en geen vergelijkende studies) fludarabine 40 mg/m 2 /dag per os dag 1-5 (ook wordt gebruikt 25 mg/m 2 i.v. dag 1-5), rituximab 375 mg/m 2 i.v. dag 1 fludarabine 40 mg/m 2 p.o. dag 1-3 (ook wordt gebruikt 25 mg/m 2 i.v.) cyclofosfamide 250 mg/m 2 p.o. dag 1-3 (i.v. dosis idem) rituximab 375 mg/m 2 i.v. dag 1 rituximab 375 mg/m 2 i.v. dag 1 bendamustine 90 mg/m 2 i.v. dag 1, 2 bortezomib 1,3 mg/m 2 i.v. dag 1, 4, 8, 11 dexamethason 40 mg per os dag 1, 4, 8, 11 rituximab 375 mg/m 2 i.v. dag 11 N.B. overweeg bortezomib s.c. toe te dienen in plaats van i.v. cyclofosfamide, terwijl de effectiviteit vergelijkbaar lijkt. 17 DRC zal als standaardgroep worden gebruikt in de eerstelijnsstudie van het European Myeloma Network, waaraan ook HOVON zal deelnemen. Ook chloorambucil, al dan niet in combinatie met rituximab, is nog steeds een goede mogelijkheid, mits er geen hyperviscositeit is. Het duurt namelijk wat langer voor een respons wordt bereikt dan met bijvoorbeeld DRC. Chloorambucil en combinatiechemotherapie zijn nooit rechtstreeks vergeleken. Bij 22
9 NEDERLANDS TIJDSCHRIFT VOOR HEMATOLOGIE jongere patiënten, die potentieel kandidaat zijn voor autologe stamceltransplantatie, wordt het langdurig gebruik van alkylerende middelen zoals chloorambucil ontraden, mede vanwege de kans op ontwikkeling van MDS/AML. Rituximab in combinatie met purineanaloga zoals fludarabine en cladribine, al dan niet met cyclofosfamide (bijvoorbeeld FC-R) is heel effectief en leidt vaak snel tot respons (mediaan na 2,5 maand). 18 In een grote gerandomiseerde studie van Leblond et al. die binnenkort gepubliceerd wordt, is monotherapie fludarabine netto effectiever dan monotherapie chloorambucil. Ook is er bezorgdheid over een verhoogde kans op MDS/AML en transformatie naar agressief NHL, daarom wordt geadviseerd maximaal 4- kuren te geven. Met cladribine is net wat minder ervaring, maar dit lijkt op grond van de beschikbare gegevens als monotherapie even effectief als fludarabine. Beide middelen dienen te worden vermeden als in de toekomst autologe stamceltransplantatie wordt overwogen. Bij elke rituximab-bevattende therapie kan een IgM- flare optreden, zie hieronder. Bij hoge IgM-uitgangswaarde of hyperviscositeit: zie aanbevelingen bij Plasmaferese. Rituximab-monotherapie Bij patiënten met contra-indicaties voor chemotherapie, bijvoorbeeld cytopenie of ernstige neuropathie, kan dit een aantrekkelijke mogelijkheid zijn. De kans op respons is echter lager en responsen treden pas veel later op dan bij de combinatie van rituximab met (milde) chemotherapie en steroïden. 5 Belangrijk is het fenomeen IgM-flare : bij ongeveer de helft van de patiënten stijgt het IgM-gehalte eerst, maar zet de daling alsnog in na 4 maanden. Het stijgen van IgM na behandeling met rituximab is dus zeker geen teken van therapiefalen! Onbekend is of dit fenomeen enige prognostische betekenis heeft. Specifieke situaties: anti-mag-polyneuropathie en koude hemolyse als uiting van IgM-gerelateerde ziekte Dit betreft patiënten die niet voldoen aan de criteria voor MW, maar wel een ziekte-uiting hebben die daarbij past, en een IgM-paraproteïne in het bloed hebben. 4 Dit zijn stuk voor stuk zeldzame ziektebeelden, variërend van verworven hemofilie tot vasculitis, en zij verdienen elk een eigen therapeutische benadering, waarover weinig klinische gegevens beschikbaar zijn. De meest voorkomende situaties worden hieronder besproken. Ongeveer 50% van de patiënten met aan IgM gerelateerde demyeliniserende polyneuropathie heeft aantoonbare anti-mag-antilichamen (overigens ook amyloïdose als oorzaak overwegen). Niet altijd is behandeling nodig, omdat de polyneuropathie vaak langzaam progressief is en symptomatische ondersteuning dan voldoende is. Bij een behandelindicatie is rituximab-monotherapie de behandeling van eerste keuze met bij maximaal 50% van de patiënten een verbetering van de klachten. Zo nodig kan worden gekozen voor immuunchemotherapie, dit laatste bijvoorbeeld bij snel progressieve klachten. 19 In een cohort van patiënten met koude agglutininen voldeed 50% aan de criteria voor MW. De overige patiënten hadden bijna allemaal een IgM-paraproteïne en, na uitsluiten van andere indolente lymfomen, was er bij de meesten van hen sprake van koude agglutinen als uiting van IgM-gerelateerde ziekte. Er treedt agglutinatie en daarna complementgeïnduceerde hemolyse op bij koude. Wederom is behandeling lastig en niet altijd nodig. Bij een behandelindicatie kan rituximab-monotherapie worden geprobeerd, met wederom rond 50% kans op respons. Bij onvoldoende respons zijn er verschillende mogelijkheden, zoals immuunchemotherapie met bijvoorbeeld rituximabfludarabine, maar ook andere behandelschema s zouden kunnen worden overwogen. 20 Tweedelijnstherapie In principe gelden hiervoor dezelfde behandelindicaties (pas behandelen als er weer sprake is van MWgerelateerde klachten of symptomen) en dezelfde behandelingsmogelijkheden. Als het ontstaan van opnieuw behandelindicatie na eerstelijnsbehandeling langer dan 2 jaar heeft geduurd, kan deze behandeling worden herhaald. Zo niet, dan kan worden gekozen voor een van de andere mogelijkheden. Bortezomib Proteasoomremmers blijken zeer effectief voor de behandeling van MW. Monotherapie met bortezomib gaf in 3 studies met totaal 4 grotendeels voorbehandelde patiënten responspercentages van ongeveer 80% (o.a. referentie 12). De respons werd snel bereikt, ongeveer na 1,5 maand, terwijl de gebruikelijke meer op de klonale B-cellen gerichte therapievarianten meestal pas na 4 maanden een respons laten zien. 227
10 Tabel. Responscriteria conform de International WM workshop. Respons complete remissie (CR) partiële respons (PR) minor respons (MR) Criteria verdwijnen van M-proteïne (immuunfixatie); beenmerg histologisch vrij van ziekte, verdwijnen van eventuele lymfadenopathie of organomegalie op computertomografie (CT) en verdwijnen van klachten passend bij MW. Na weken moet de CR worden bevestigd met opnieuw bepalen M-proteïne met immuunfixatie. 50% afname van het M-proteïne (eiwitelektroforese) en 50% afname van eventuele lymfomen of organomegalie op CT of bij lichamelijk onderzoek. Geen nieuwe klinische verschijnselen passend bij MW. 25%, maar minder dan 50% afname van het M-proteïne (eiwitelektroforese) zonder progressie van lymfadenopathie/organomegalie, cytopenie of klinische verschijnselen passend bij MW. stabiele ziekte een stabiel M-proteïne (eiwitelektroforese), dat wil zeggen <25% afname en <25% toename, zonder progressie van lymfadenopathie/organomegalie, cytopenie of klinische verschijnselen passend bij MW. progressie 25% toename van het M-proteïne (eiwitelektroforese), bevestigd door een tweede meting, of progressie van klinische verschijnselen horend bij MW (bijvoorbeeld anemie, trombopenie, kliergrootte, nachtzweten, neuropathie) De progressievrije overleving bedroeg ten minste 1 jaar. In een kleine eerstelijnsstudie, waarbij de combinatie rituximab, bortezomib, dexamethason werd gegeven, werd een nog hoger responspercentage gezien, waarbij na 2 jaar 80% van de patiënten nog progressievrij was. 21 De voornaamste bijwerking is neuropathie (circa 70% van patiënten, tot 30% graad 3, wel vaak reversibel na dosisaanpassing). Dit komt duidelijk vaker voor dan bij andere behandelindicaties zoals multipel myeloom: Mogelijk kan ook hier de kans op neuropathie worden verminderd door bortezomib anders te doseren (bijvoorbeeld wekelijks in plaats van tweemaal per week) en subcutaan toe te dienen. Verder is uiteraard van belang neuropathie tijdig te constateren en zo nodig dosisaanpassing toe te passen, danwel de therapie te onderbreken. Met de nieuwe proteasoomremmer carfilzomib, die beduidend minder neurotoxiciteit geeft, worden de eerste studies bij patiënten met MW gedaan. Binnen het European Myeloma Network (EMN) is momenteel een studie in voorbereiding naar de waarde van het gebruik van bortezomib in de eerste lijn. In deze grote Europese studie, waarin ook HOVON zal participeren, zal worden gerandomiseerd tussen DRC en DRC plus bortezomib. Bendamustine In de studie van Rummel et al., die werd gepresenteerd op de ASH in 2009, maar nog niet is gepubliceerd, werden 54 patiënten met verschillende indolente lymfomen in de eerste lijn gerandomiseerd voor R- bendamustine versus R-CHOP, waaronder 40 patiënten met MW. Bij de patiënten met MW was het responspercentage in beide groepen vergelijkbaar hoog (9% en 94%), echter de progressievrije overleving was significant beter in de bendamustine-groep. Ook was de toxiciteit beduidend lager in de gehele R-bendamustine-groep (onder andere minder infecties, geen alopecia, minder neuropathie). 22 In maart 2011 publiceerden Treon et al. een serie van 30 patiënten met een recidief of refractaire MW. Met de combinatie rituximab-bendamustine werd bij 83% een respons gezien; de mediane progressievrije overleving was 13 maanden. De therapie werd goed verdragen. De voornaamste bijwerking was myelosuppressie, vooral bij patiënten die eerder werden behandeld met purineanaloga. 23 Rituximab in combinatie met bendamustine lijkt dus (op basis van een kleine groep patiënten in 2 studies), een effectieve mogelijkheid met relatief langdurige respons en weinig toxiciteit. Over de langetermijn- 228
11 NEDERLANDS TIJDSCHRIFT VOOR HEMATOLOGIE bijwerkingen van bendamustine (secundaire MDS, stamceltoxiciteit) is echter nog vrij weinig bekend. Middelen die vooralsnog niet worden aangeraden Met alemtuzumab is erg weinig ervaring en behandeling hiermee lijkt bij patiënten met MW veel toxiciteit te geven. 24 Thalidomide heeft een te beperkt effect om als monotherapie te worden toegepast. Voordeel is dat het niet myelosuppressief is, en in combinatie met rituximab zijn de resultaten iets beter. Er is echter nog relatief weinig ervaring mee en vanwege de neurotoxiciteit is thalidomide geen voor de hand liggende keuze. Het gebruik van lenalidomide wordt afgeraden, omdat bij patiënten met MW een onbegrepen ernstige en moeilijk te behandelen anemie kan optreden, die ook persisteert na dosisreductie (o.a. referentie 12). De rol van stamceltransplantatie Verreweg de meeste patiënten komen gezien leeftijd, comorbiditeit en prognose niet in aanmerking voor stamceltransplantatie. Bij een selecte groep jongere en fitte patiënten, die een snel recidief hebben na immuunchemotherapie, kan autologe stamceltransplantatie worden overwogen. In een recente serie bij uitgebreid voorbehandelde MW-patiënten was de nonrelapsmortaliteit 4-% in het eerste jaar. De mediane progressievrije overleving was ongeveer 4 jaar en na 5 jaar was nog 0% van de patiënten in leven. 25,2 De non-relapsmortaliteit na allogene stamceltransplantatie is erg hoog bij MW: in de grootste serie 23-40% na 1 jaar, afhankelijk van de conditionering (respectievelijk reduced-intensity of myeloablatief). 27 De vijfjaars progressievrije overleving was ongeveer 45-50% en de totale overleving 50-0%. Chronische graft-versus-hostziekte was geassocieerd met een hogere non-relapsmortaliteit en een lagere relapse rate. Gezien de beschikbare alternatieven en de hoge behandelinggerelateerde mortaliteit wordt allogene transplantatie niet standaard aanbevolen bij MW, maar moet deze mogelijkheid worden overwogen bij de zeldzame jonge patiënt met snel recidiverende ziekte. Onderhoudsbehandeling Er zijn geen prospectieve studies naar de rol van onderhoudsbehandeling. Recentelijk werd wel een retrospectieve studie gepubliceerd waarbij 8 van 248 MW-patiënten onderhoudsbehandeling met rituximab kregen, mediaan 8 giften in de 2 jaar na inductietherapie met een rituximabbevattend regime. Zowel de progressievrije overleving (5 versus 29 maanden) als de totale overleving (niet behaald versus 11 maanden) waren beter in de onderhoudsgroep. Onderhoudsbehandeling met rituximab moet bij tweedelijnsbehandeling van MW, net zoals bij andere indolente non-hodgkinlymfomen, zeker worden overwogen. 28 Responsbepaling Tijdens de derde International WM workshop zijn uniforme responscriteria opgesteld, die in Tabel worden samengevat. 29 Omdat het M-proteïne soms slechts langzaam daalt met de huidige behandelingen en de hoogte van het M-proteïne niet altijd een betrouwbare weergave geeft van de tumormassa, moet bij twijfel over de respons ook beenmergonderzoek worden herhaald. Ook gaat bij verschillende middelen de daling sneller (purineanalogen, proteasoomremmers) of juist langzamer (chloorambucil, rituximab). Indien beenmergonderzoek tussentijds wordt verricht bij bijvoorbeeld chloorambucil-therapie, valt vaak op dat er wel een goede beenmergrespons is met vermindering van de klonale B-lymfocyten, maar dat de plasmacellen nog aanwezig zijn en de bron kunnen zijn van het persisterende M-proteïne. 30 Conclusies en aanbevelingen Zowel qua symptomatologie, pathofysiologie, als behandeling neemt MW een bijzondere positie in binnen de groep indolente maligne lymfomen. Er is absoluut ruimte voor verbetering van de behandelingsresultaten van deze vrij zeldzame ziekte en om die reden is het belangrijk patiënten waar mogelijk in studieverband te behandelen, gestratificeerd voor IPSS-WM-score en gebruikmakend van uniforme responscriteria. Een van de uitdagingen voor de toekomst is, zoals bij vele indolente non-hodgkinlymfomen, om sneller en beter respons te kunnen definiëren, zodat refractaire/ hoogrisicopatiënten sneller kunnen worden geïdentificeerd en dit ook richting kan geven aan de keuze van therapie. Vanwege de toxiciteit, die voor een deel ziektespecifiek blijkt te zijn (ernstige anemie bij gebruik van lenalidomide, hoger risico op neuropathie bij proteasoomremmers), kunnen resultaten van therapie bij andere typen indolente lymfomen niet zonder meer worden geëxtrapoleerd. 229
12 Aanwijzingen voor de praktijk 1. Gezien de diverse symptomatologie die deels uniek is voor dit ziektebeeld, is een zorgvuldige anamnese, compleet lichamelijk onderzoek en gericht aanvullend onderzoek belangrijk. 2. Niet alleen symptomatologie als gevolg van lymfoominfiltratie, maar ook de specifieke aan IgM-paraproteïne gerelateerde symptomatologie zijn bepalend voor het moment van starten en de keuze van de therapie. 3. De hoogte van het M-proteïne (zelfs als >30 g/l) hoeft op zichzelf geen reden te zijn voor behandeling, indien de patiënt asymptomatisch is. Andersom kan een kleine hoeveelheid M-proteïne wel aanleiding geven tot klachten en een behandelindicatie vormen. 4. Bij hyperviscositeit direct plasmafereren en tegelijkertijd starten met therapie, gericht op het snel afremmen van de IgM-productie, zoals een fludarabine- of bortezomib-bevattend schema. Wachten met het geven van rituximab in verband met IgM- flare. 5. Als eerstelijnsbehandeling bij symptomatische patiënten wordt immuunchemotherapie aanbevolen, zoals het DRC-schema of R-CP. Chloorambucil, in combinatie met rituximab en/of steroïden, is een goed alternatief, vooral ook bij de oudere patiënt.. Bij jonge patiënten (en/of patiënten die potentieel kandidaat zijn voor autologe stamceltransplantatie): langdurig gebruik van purineanaloga en alkylerende middelen vermijden. 7. Bij de eerste gift rituximab moet rekening worden gehouden met het optreden van een IgM- flare. 8. Bij het opnieuw ontstaan van een behandelindicatie 2 jaar of langer na eerstelijnsbehandeling kan deze behandeling worden herhaald. 9. Bij het opnieuw ontstaan van een behandelindicatie binnen 2 jaar na eerstelijnsbehandeling is er een groot arsenaal aan werkzame middelen en behandelingsmodaliteiten, waaronder transplantatie. Hierbij geven onder andere leeftijd, comorbiditeit en bestaan van cytopenieën en/of neuropathie richting aan de keuze. Referenties 1. SH Swerdlow, E Campo, Harris NL, et al.who classification of tumours of haematopoietic and lymphoid tissues: lymphoplasmocytic lymphoma. IARC, Lyon; Gertz MA. Waldenstrom macroglobulinemia: 2011 update on diagnosis, risk stratification, and management. Am J Hematol 2011;8(5): Ansell SM, Kyle RA, Reeder CB, et al. Diagnosis and management of Waldenstrom macroglobulinemia: Mayo stratification of macroglobulinemia and risk-adapted therapy (msmart) guidelines. Mayo Clin Proc 2010;85(9): Owen RG, Treon SP, Al-Katib A, et al. Clinicopathological definition of Waldenstrom s macroglobulinemia: consensus panel recommendations from the Second International Workshop on Waldenstrom s Macroglobulinemia. Semin Oncol 2003;30(2): Treon SP. How I treat Waldenstrom macroglobulinemia. Blood 2009; 114(12): Kristinsson SY, Goldin LR, Turesson I, et al. Familial aggregation of lymphoplasmacytic lymphoma/waldenstrom macroglobulinemia with solid tumors and myeloid malignancies. Acta Haematol 2012;127(3): Konoplev S, Medeiros LJ, Bueso-Ramos CE, et al. Immunophenotypic profile of lymphoplasmacytic lymphoma/waldenstrom macroglobulinemia. Am J Clin Pathol 2005;124(3): Treon SP, Xu L, Zhou Y, et al. Whole genome sequencing reveals a widely expressed mutation (MYD88 L25P) with oncogenic activity in Waldenstrom s macroglobulinemia. ASH annual meeting 2011;118: Kyle RA, Dispenzieri A, Kumar S, et al. IgM monoclonal gammopathy of 230
13 NEDERLANDS TIJDSCHRIFT VOOR HEMATOLOGIE undetermined significance (MGUS) and smoldering Waldenstrom s macroglobulinemia (SWM). Clin Lymphoma Myeloma Leuk 2011;11(1): Kyle RA, Benson JT, Larson DR, et al. Progression in smoldering Waldenstrom macroglobulinemia: long-term results. Blood 2012;119(19): Morel P, Duhamel A, Gobbi P, et al. International prognostic scoring system for Waldenstrom macroglobulinemia. Blood 2009;113(18): Kastritis E, Terpos E, Dimopoulos MA. Emerging drugs for Waldenstrom s macroglobulinemia. Expert Opin Emerg Drugs 2011;1(1): Dimopoulos MA, Gertz MA, Kastritis E, et al. Update on treatment recommendations from the Fourth International Workshop on Waldenstrom s Macroglobulinemia. J Clin Oncol 2009;27(1): Rourke M, Anderson KC, Ghobrial IM. Review of clinical trials conducted in Waldenstrom macroglobulinemia and recommendations for reporting clinical trial responses in these patients. Leuk Lymphoma 2010;51(10): Buske C, Hoster E, Dreyling M, et al. The addition of rituximab to front-line therapy with CHOP (R-CHOP) results in a higher response rate and longer time to treatment failure in patients with lymphoplasmacytic lymphoma: results of a randomized trial of the German Low-Grade Lymphoma Study Group (GLSG). Leukemia 2009;23(1): Ioakimidis L, Patterson CJ, Hunter ZR, et al. Comparative outcomes following CP-R, CVP-R, and CHOP-R in Waldenstrom s macroglobulinemia. Clin Lymphoma Myeloma 2009;9(1): Dimopoulos MA, Anagnostopoulos A, Kyrtsonis MC, et al. Primary treatment of Waldenstrom macroglobulinemia with dexamethasone, rituximab, and cyclophosphamide. J Clin Oncol 2007;25(22): Leblond V, Levy V, Maloisel F, et al. Multicenter, randomized comparative trial of fludarabine and the combination of cyclophosphamide-doxorubicinprednisone in 92 patients with Waldenstrom macroglobulinemia in first relapse or with primary refractory disease. Blood 2001;98(9): Niermeijer JM, Fischer K, Eurelings M, et al. Prognosis of polyneuropathy due to IgM monoclonal gammopathy: a prospective cohort study. Neurology 2010;74(5): Berentsen S. Cold agglutinin-mediated autoimmune hemolytic anemia in Waldenstrom s macroglobulinemia. Clin Lymphoma Myeloma 2009;9(1): Treon SP, Ioakimidis L, Soumerai JD, et al. Primary therapy of Waldenstrom macroglobulinemia with bortezomib, dexamethasone, and rituximab: WMCTG clinical trial J Clin Oncol 2009;27(23): Rummel MJ, Von Gruenhagen U, Norbert Niederle N, et al. Bendamustine plus rituximab versus CHOP plus rituximab in the first-line-treatment of patients with follicular, indolent and mantle cell lymphomas: results of a randomized phase III study of the Study Group Indolent Lymphomas (StiL). ASH annual meeting 2008;112: Treon SP, Hanzis C, Tripsas C, et al. Bendamustine therapy in patients with relapsed or refractory Waldenström s macroglobulinemia. Clin Lymphoma Myeloma Leuk 2011;11(1): Treon SP, Soumerai JD, Hunter ZR, et al. Long-term follow-up of symptomatic patients with lymphoplasmacytic lymphoma/waldenstrom macroglobulinemia treated with the anti-cd52 monoclonal antibody alemtuzumab. Blood 2011; 118(2): Gertz MA, Reeder CB, Kyle RA, et al. Stem cell transplant for Waldenstrom macroglobulinemia: an underutilized technique. Bone Marrow Transplant 2011, Aug 29 [E-pub ahead of print]. 2. Kyriakou C, Canals C, Cornelissen JJ, et al. Allogeneic stem-cell transplantation in patients with Waldenstrom macroglobulinemia: report from the Lymphoma Working Party of the European Group for Blood and Marrow Transplantation. J Clin Oncol 2010;28(33): Kyriakou C, Canals C, Sibon D, et al. High-dose therapy and autologous stem-cell transplantation in Waldenstrom macroglobulinemia: the Lymphoma Working Party of the European Group for Blood and Marrow Transplantation. J Clin Oncol 2010;28(13): Treon SP, Hanzis C, Manning RJ, et al. Maintenance rituximab is associated with improved clinical outcome in rituximab naive patients with Waldenstrom macroglobulinaemia who respond to a rituximab-containing regimen. Br J Haematol 2011;154(3): Kimby E, Treon SP, Anagnostopoulos A, et al. Update on recommendations for assessing response from the Third International Workshop on Waldenstrom s macroglobulinemia. Clin Lymphoma Myeloma 200;(5): Barakat FH, Medeiros LJ, Wei EX, et al. Residual monotypic plasma cells in patients with waldenstrom macroglobulinemia after therapy. Am J Clin Pathol 2011;135(3): Ontvangen 2 juli 2012, geaccepteerd 2 juli
Richtlijn voor diagnostiek en behandeling van de ziekte van Waldenström
 Richtlijn voor diagnostiek en behandeling van de ziekte van Waldenström Guidelines for diagnosis and management of Waldenström s macroglobulinemia J.M.I. Vos, M.C. Minnema, P.W. Wijermans, S. Croockewit,
Richtlijn voor diagnostiek en behandeling van de ziekte van Waldenström Guidelines for diagnosis and management of Waldenström s macroglobulinemia J.M.I. Vos, M.C. Minnema, P.W. Wijermans, S. Croockewit,
De ziekte van Waldenström: nieuwe behandelingsmogelijkheden. Marie José Kersten Internist-hematoloog AMC, Amsterdam
 De ziekte van Waldenström: nieuwe behandelingsmogelijkheden Marie José Kersten Internist-hematoloog AMC, Amsterdam De ziekte van Waldenström Inleiding: klachten, ziekteverschijnselen, complicaties Standaardbehandeling
De ziekte van Waldenström: nieuwe behandelingsmogelijkheden Marie José Kersten Internist-hematoloog AMC, Amsterdam De ziekte van Waldenström Inleiding: klachten, ziekteverschijnselen, complicaties Standaardbehandeling
Klinische Dag. 3 oktober 2013 Disclosure belangen spreker. (potentiële) belangenverstrengeling
 Klinische Dag 3 oktober 2013 Disclosure belangen spreker (potentiële) belangenverstrengeling Geen How we treat: Morbus Waldenström Josephine Vos Internist-hematoloog Wie is we Newport, aug 2012, 7th International
Klinische Dag 3 oktober 2013 Disclosure belangen spreker (potentiële) belangenverstrengeling Geen How we treat: Morbus Waldenström Josephine Vos Internist-hematoloog Wie is we Newport, aug 2012, 7th International
Morbus Waldenström en de nieuwste ontwikkelingen
 Morbus Waldenström en de nieuwste ontwikkelingen Landelijke patienten contactdag 2015 Monique Minnema, internist-hematoloog Inhoud 1. Hoe zit deze ziekte in elkaar? 2. Behandelingen 3. Polyneuropathie
Morbus Waldenström en de nieuwste ontwikkelingen Landelijke patienten contactdag 2015 Monique Minnema, internist-hematoloog Inhoud 1. Hoe zit deze ziekte in elkaar? 2. Behandelingen 3. Polyneuropathie
De eerste HOVON-studie voor patiënten met de ziekte van Waldenström
 HOVON 12-studie: een multicentrum fase 1/2-studie met ixazomib, dexamethason en rituximab bij patiënten met recidief of progressie van de ziekte van Waldenström De eerste HOVON-studie voor patiënten met
HOVON 12-studie: een multicentrum fase 1/2-studie met ixazomib, dexamethason en rituximab bij patiënten met recidief of progressie van de ziekte van Waldenström De eerste HOVON-studie voor patiënten met
Disease morbidities 1; Polyneuropathy, Bing Neel, Amyloid
 International Waldentrom s Patient Meeting 9 oct 2016, Amsterdam Disease morbidities 1; Polyneuropathy, Bing Neel, Amyloid Monique Minnema, internist-hematoloog Morbus Waldenström Kankercellen : Waldenström
International Waldentrom s Patient Meeting 9 oct 2016, Amsterdam Disease morbidities 1; Polyneuropathy, Bing Neel, Amyloid Monique Minnema, internist-hematoloog Morbus Waldenström Kankercellen : Waldenström
Morbus Waldenström en IgM geassocieerde polyneuropathie. Anna van Rhenen Klinische dag NVVH
 Morbus Waldenström en IgM geassocieerde polyneuropathie Anna van Rhenen Klinische dag NVVH 1 Inhoud Casus Morbus Waldenström IgM geassocieerde polyneuropathie Literatuur Conclusies Dia 2 1 zou deze dia
Morbus Waldenström en IgM geassocieerde polyneuropathie Anna van Rhenen Klinische dag NVVH 1 Inhoud Casus Morbus Waldenström IgM geassocieerde polyneuropathie Literatuur Conclusies Dia 2 1 zou deze dia
Welkom in Meander Medisch Centrum. Informatieavond non-hodgkinlymfoom en stamceltransplantatie 25 november 2014
 Welkom in Meander Medisch Centrum Informatieavond non-hodgkinlymfoom en stamceltransplantatie 25 november 2014 Indolent non Hodgkin lymfoom en chronischlymfatischeleukemie Van oorzaaktot (nieuwe ontwikkelingen
Welkom in Meander Medisch Centrum Informatieavond non-hodgkinlymfoom en stamceltransplantatie 25 november 2014 Indolent non Hodgkin lymfoom en chronischlymfatischeleukemie Van oorzaaktot (nieuwe ontwikkelingen
De ziekte van Waldenström: nieuwe behandelingsmogelijkheden. Marie José Kersten AMC, Amsterdam www.lymmcare.nl
 De ziekte van Waldenström: nieuwe behandelingsmogelijkheden Marie José Kersten AMC, Amsterdam www.lymmcare.nl De ziekte van Waldenström Inleiding: klachten ziekteverschijnselen complicaties Standaardbehandeling
De ziekte van Waldenström: nieuwe behandelingsmogelijkheden Marie José Kersten AMC, Amsterdam www.lymmcare.nl De ziekte van Waldenström Inleiding: klachten ziekteverschijnselen complicaties Standaardbehandeling
Klinische Dag. 3 oktober 2013 Disclosure belangen spreker. (potentiële) belangenverstrengeling
 Klinische Dag 3 oktober 2013 Disclosure belangen spreker (potentiële) belangenverstrengeling Geen Papiloedeem als eerste presentatie van het POEMS syndroom Dieneke Breukink, ANIOS Interne Geneeskunde R.
Klinische Dag 3 oktober 2013 Disclosure belangen spreker (potentiële) belangenverstrengeling Geen Papiloedeem als eerste presentatie van het POEMS syndroom Dieneke Breukink, ANIOS Interne Geneeskunde R.
Multipel myeloom: van molecuul tot medicijn. Marie José Kersten Afdeling Hematologie, AMC
 Multipel myeloom: van molecuul tot medicijn Marie José Kersten Afdeling Hematologie, AMC Multipel myeloom: ziekte van Kahler Otto Kahler Sarah Newbury, 1844 Rajkumar & Kyle, Blood 2008 Multipel myeloom
Multipel myeloom: van molecuul tot medicijn Marie José Kersten Afdeling Hematologie, AMC Multipel myeloom: ziekte van Kahler Otto Kahler Sarah Newbury, 1844 Rajkumar & Kyle, Blood 2008 Multipel myeloom
Presentatie Een 24-jarige vrouw presenteert zich met hypermenorrhoea, veel hematomen en bloedneuzen. Haar vorige menstruatie verliep normaal.
 CASUS 2 Presentatie Een 24-jarige vrouw presenteert zich met hypermenorrhoea, veel hematomen en bloedneuzen. Haar vorige menstruatie verliep normaal. Lichamelijk onderzoek Bleek, veel hematomen, veel bloed
CASUS 2 Presentatie Een 24-jarige vrouw presenteert zich met hypermenorrhoea, veel hematomen en bloedneuzen. Haar vorige menstruatie verliep normaal. Lichamelijk onderzoek Bleek, veel hematomen, veel bloed
Multipel myeloom 2012
 Multipel myeloom 2012 Op weg naar genezing? Prof. Dr. R Schots MYELOOMKLINIEK UZ Brussel Mijlpalen in de geschiedenis 1969 2008 1996 Mijlpalen in de behandeling van multipel myeloom Autologe stamceltransplantatie
Multipel myeloom 2012 Op weg naar genezing? Prof. Dr. R Schots MYELOOMKLINIEK UZ Brussel Mijlpalen in de geschiedenis 1969 2008 1996 Mijlpalen in de behandeling van multipel myeloom Autologe stamceltransplantatie
IN DE EERSTE LIJN INFORMATIE VOOR DE HUISARTS ZIEKTE VAN WALDENSTRÖM
 IN DE EERSTE LIJN INFORMATIE VOOR DE HUISARTS ZIEKTE VAN WALDENSTRÖM IN DE EERSTE LIJN INFORMATIE VOOR DE HUISARTS ZIEKTE VAN WALDENSTRÖM Prof. dr. M.J. Kersten Hematon Tweede druk Utrecht, 2015 Omslagfoto:
IN DE EERSTE LIJN INFORMATIE VOOR DE HUISARTS ZIEKTE VAN WALDENSTRÖM IN DE EERSTE LIJN INFORMATIE VOOR DE HUISARTS ZIEKTE VAN WALDENSTRÖM Prof. dr. M.J. Kersten Hematon Tweede druk Utrecht, 2015 Omslagfoto:
Multipel myeloom en de ziekte van Waldenström: overeenkomsten en verschillen! Marie José Kersten
 Multipel myeloom en de ziekte van Waldenström: overeenkomsten en verschillen! Marie José Kersten Multipel myeloom en de ziekte van Waldenström Overeenkomsten en verschillen: Voorkomen van de ziekte Klachten,
Multipel myeloom en de ziekte van Waldenström: overeenkomsten en verschillen! Marie José Kersten Multipel myeloom en de ziekte van Waldenström Overeenkomsten en verschillen: Voorkomen van de ziekte Klachten,
Eerstelijns behandelopties bij Waldenström Macroglobulinemie. Jorge J. Castillo, MD Assistant Professor of Medicine Harvard Medical School
 Eerstelijns behandelopties bij Waldenström Macroglobulinemie Jorge J. Castillo, MD Assistant Professor of Medicine Harvard Medical School Disclosures Consulterend Otsuka Pharmaceuticals Biogen IDEC Alexion
Eerstelijns behandelopties bij Waldenström Macroglobulinemie Jorge J. Castillo, MD Assistant Professor of Medicine Harvard Medical School Disclosures Consulterend Otsuka Pharmaceuticals Biogen IDEC Alexion
26 Behandeling van de ziekte van Waldenström
 26 Behandeling van de ziekte van Waldenström 26 Behandeling van de ziekte van Waldenström Drs. J.M.I. Vos, dr. M.J. Kersten en dr. P.W. Wijermans Inleiding De ziekte van Waldenström behoort volgens de
26 Behandeling van de ziekte van Waldenström 26 Behandeling van de ziekte van Waldenström Drs. J.M.I. Vos, dr. M.J. Kersten en dr. P.W. Wijermans Inleiding De ziekte van Waldenström behoort volgens de
HOVON EDUCATIONAL MYELOOM. Case 2
 HOVON EDUCATIONAL MYELOOM Case 2 NIELS VAN DE DONK SONJA ZWEEGMAN Department of Hematology, Amsterdam, Netherlands Amsterdam, Netherlands Clinical case: presentation 54-year-old patient with a diagnosis
HOVON EDUCATIONAL MYELOOM Case 2 NIELS VAN DE DONK SONJA ZWEEGMAN Department of Hematology, Amsterdam, Netherlands Amsterdam, Netherlands Clinical case: presentation 54-year-old patient with a diagnosis
Waldenström s Macroglobulinemia familie en secundaire maligniteiten
 familie en secundaire maligniteiten Patient Session October 9, 2016 Amsterdam, The Netherlands Robert A. Kyle, MD Mayo Clinic Rochester, MN, USA Scottsdale, Arizona Rochester, Minnesota Jacksonville, Florida
familie en secundaire maligniteiten Patient Session October 9, 2016 Amsterdam, The Netherlands Robert A. Kyle, MD Mayo Clinic Rochester, MN, USA Scottsdale, Arizona Rochester, Minnesota Jacksonville, Florida
Blasten in perifeer bloed
 Man 50 jaar Chronische lymfatische leukemie, RAI stadium 0, zonder criteria van actieve ziekte waarvoor wait and see beleid diep veneuze trombose. 2 dagen later: presentatie op SEH in verband met veel
Man 50 jaar Chronische lymfatische leukemie, RAI stadium 0, zonder criteria van actieve ziekte waarvoor wait and see beleid diep veneuze trombose. 2 dagen later: presentatie op SEH in verband met veel
Folliculair lymfoom Diagnostiek en Behandeling. Rondzending beenmerg morfologie Marie Jose Claessen
 Folliculair lymfoom Diagnostiek en Behandeling Rondzending beenmerg morfologie 07 01 2014 Marie Jose Claessen Casus I 45 jarige vrouw (1968). Verwijsbrief: Palpabele zwelling hals. Uitslag punctie: Cytologie:
Folliculair lymfoom Diagnostiek en Behandeling Rondzending beenmerg morfologie 07 01 2014 Marie Jose Claessen Casus I 45 jarige vrouw (1968). Verwijsbrief: Palpabele zwelling hals. Uitslag punctie: Cytologie:
anemie 1.1 Overzicht van de anemieën 1.2 Congenitale anemieën 1.3 Verworven anemieën
 I N H O U D hoofdstuk 1 anemie 13 1.1 Overzicht van de anemieën 13 1.2 Congenitale anemieën 16 1.2.1 De thalassemieën 16 1.2.2 Sikkelcelanemie 19 1.2.3 Andere hemoglobinopathieën 22 1.2.4 Aangeboren membraanafwijkingen
I N H O U D hoofdstuk 1 anemie 13 1.1 Overzicht van de anemieën 13 1.2 Congenitale anemieën 16 1.2.1 De thalassemieën 16 1.2.2 Sikkelcelanemie 19 1.2.3 Andere hemoglobinopathieën 22 1.2.4 Aangeboren membraanafwijkingen
MULTIPLE MYELOOM Doneer voor genezing
 MULTIPLE MYELOOM Doneer voor genezing Luister en leer Marlies Van Hoef, MD, PhD, MBA Multiple Myeloom Ziekte van Kahler werd aanvankelijk gediagnostiseerd in 1848 Kwaardaardige abnormaliteit van plasmacellen;
MULTIPLE MYELOOM Doneer voor genezing Luister en leer Marlies Van Hoef, MD, PhD, MBA Multiple Myeloom Ziekte van Kahler werd aanvankelijk gediagnostiseerd in 1848 Kwaardaardige abnormaliteit van plasmacellen;
belangrijke cijfers over hematologische kankersoorten
 belangrijke cijfers over hematologische kankersoorten Een overzicht van het voorkomen, de behandeling en overleving van hematologische kankersoorten gebaseerd op cijfers uit de Nederlandse Kankerregistratie
belangrijke cijfers over hematologische kankersoorten Een overzicht van het voorkomen, de behandeling en overleving van hematologische kankersoorten gebaseerd op cijfers uit de Nederlandse Kankerregistratie
Chronische Lymfatische Leukemie. anno 2015
 Chronische Lymfatische Leukemie anno 2015 Marten R. Nijziel, internist-hematoloog Máxima Medisch Centrum Eindhoven/Veldhoven Hematon Leukemiedag Soesterberg, 3 oktober 2015 Wat is CLL? Wat is nodig voor
Chronische Lymfatische Leukemie anno 2015 Marten R. Nijziel, internist-hematoloog Máxima Medisch Centrum Eindhoven/Veldhoven Hematon Leukemiedag Soesterberg, 3 oktober 2015 Wat is CLL? Wat is nodig voor
Klinische Dag. 3 oktober 2013 Disclosure belangen spreker. (potentiële) belangenverstrengeling
 Klinische Dag 3 oktober 2013 Disclosure belangen spreker (potentiële) belangenverstrengeling Geen Reversibele cardiale betrokkenheid bij multipel myeloom met AL-amyloidose Klinische hematologiedag 2013
Klinische Dag 3 oktober 2013 Disclosure belangen spreker (potentiële) belangenverstrengeling Geen Reversibele cardiale betrokkenheid bij multipel myeloom met AL-amyloidose Klinische hematologiedag 2013
Acute myeloïde leukemie. Annoek Broers 7e nascholing hematologie 20-03-2014
 Acute myeloïde leukemie Annoek Broers 7e nascholing hematologie 20-03-2014 Bloedcelvorming - hematopoiese selfrenewal Multilineage differentiation Acute myeloïde leukemie - AML Normaal beenmerg Bloedarmoede
Acute myeloïde leukemie Annoek Broers 7e nascholing hematologie 20-03-2014 Bloedcelvorming - hematopoiese selfrenewal Multilineage differentiation Acute myeloïde leukemie - AML Normaal beenmerg Bloedarmoede
ZIEKTE VAN WALDENSTRÖM
 IN DE EERSTE LIJN INFORMATIE VOOR DE HUISARTS ZIEKTE VAN WALDENSTRÖM Auteur Prof. dr. M.J. Kersten patiëntenorganisatie bloedkanker lymfklierkanker stamceltransplantatie IN DE EERSTE LIJN INFORMATIE VOOR
IN DE EERSTE LIJN INFORMATIE VOOR DE HUISARTS ZIEKTE VAN WALDENSTRÖM Auteur Prof. dr. M.J. Kersten patiëntenorganisatie bloedkanker lymfklierkanker stamceltransplantatie IN DE EERSTE LIJN INFORMATIE VOOR
Klinische Dag NVvH 2 oktober 2014 Claudia Ootjers
 Dhr O., 60 jaar Klinische Dag NVvH 2 oktober 2014 Claudia Ootjers Klinische Dag NVvH 2 oktober 2014 Disclosure belangen Claudia Ootjers Geen (potentiële) belangenverstrengeling Klinische Dag NVvH 2 Relevante
Dhr O., 60 jaar Klinische Dag NVvH 2 oktober 2014 Claudia Ootjers Klinische Dag NVvH 2 oktober 2014 Disclosure belangen Claudia Ootjers Geen (potentiële) belangenverstrengeling Klinische Dag NVvH 2 Relevante
Ontwikkelingen voor de behandeling van AL amyloïdose
 Ontwikkelingen voor de behandeling van AL amyloïdose Reinier Raymakers, internist-hematoloog Patientendag 17 feb 2018 Plasmacellen in Multipel Myeloom, MGUS en AL amyloidose (voorloper) kwaadaardige plasmacellen
Ontwikkelingen voor de behandeling van AL amyloïdose Reinier Raymakers, internist-hematoloog Patientendag 17 feb 2018 Plasmacellen in Multipel Myeloom, MGUS en AL amyloidose (voorloper) kwaadaardige plasmacellen
Chronische lymfatische leukemie 2018
 Chronische lymfatische leukemie 2018 Arnon Kater Afd. Hematologie Academisch Medisch Centrum, Amsterdam beenmerg plaatjes witte bloedcellen rode bloedcellen antistof producerende cel milt en lymfekier
Chronische lymfatische leukemie 2018 Arnon Kater Afd. Hematologie Academisch Medisch Centrum, Amsterdam beenmerg plaatjes witte bloedcellen rode bloedcellen antistof producerende cel milt en lymfekier
HOVON-Hematologie scholingsdag donderdag 1 okt 2015
 HOVON-Hematologie scholingsdag donderdag 1 okt 2015 Josée Zijlstra VUMC www.hematologie.nl/ j.zijlstra@vumc.nl Thomas Hodgkin 1798-1866 Hodgkin lymfoom Diagnostiek Pathologie Epidemiologie Symptomen Beeldvorming
HOVON-Hematologie scholingsdag donderdag 1 okt 2015 Josée Zijlstra VUMC www.hematologie.nl/ j.zijlstra@vumc.nl Thomas Hodgkin 1798-1866 Hodgkin lymfoom Diagnostiek Pathologie Epidemiologie Symptomen Beeldvorming
AL amyloïdose oorzaak, behandeling en nieuwe ontwikkelingen
 AL amyloïdose oorzaak, behandeling en nieuwe ontwikkelingen Monique Minnema, internist-hematoloog Patientendag 9 jan 2016 AL (en AH) amyloidose AL = Amyloid Light chain AH = Amyloid Heay chain + serum
AL amyloïdose oorzaak, behandeling en nieuwe ontwikkelingen Monique Minnema, internist-hematoloog Patientendag 9 jan 2016 AL (en AH) amyloidose AL = Amyloid Light chain AH = Amyloid Heay chain + serum
Multipel Myeloom; Diagnose, behandeling en de consequenties daarvan. Esther de Waal Medisch Centrum Leeuwarden 1 november 2014
 Multipel Myeloom; Diagnose, behandeling en de consequenties daarvan Esther de Waal Medisch Centrum Leeuwarden 1 november 2014 Indeling Introductie Wat is het multipel myeloom Hoe stel je de diagnose Behandeling
Multipel Myeloom; Diagnose, behandeling en de consequenties daarvan Esther de Waal Medisch Centrum Leeuwarden 1 november 2014 Indeling Introductie Wat is het multipel myeloom Hoe stel je de diagnose Behandeling
B-Cel lymfomen en hun behandeling. K. Van Eygen Symposium LVV 14 oktober 2017
 B-Cel lymfomen en hun behandeling K. Van Eygen Symposium LVV 14 oktober 2017 B-cel lymfomen Inleiding B-cel lymfomen: waarover praten we? De belangrijkste wapens in de strijd tegen lymfomen: enkele begrippen
B-Cel lymfomen en hun behandeling K. Van Eygen Symposium LVV 14 oktober 2017 B-cel lymfomen Inleiding B-cel lymfomen: waarover praten we? De belangrijkste wapens in de strijd tegen lymfomen: enkele begrippen
Ontwikkelingen in de behandeling van AL amyloïdose. Monique Minnema, internist-hematoloog UMC Utrecht Patiëntendag 9 maart 2019
 Ontwikkelingen in de behandeling van AL amyloïdose Monique Minnema, internist-hematoloog UMC Utrecht Patiëntendag 9 maart 2019 Inhoud Algemene inleiding AL amyloïdose Behandeling en symptoombestrijding
Ontwikkelingen in de behandeling van AL amyloïdose Monique Minnema, internist-hematoloog UMC Utrecht Patiëntendag 9 maart 2019 Inhoud Algemene inleiding AL amyloïdose Behandeling en symptoombestrijding
Voor patiënten die buiten studieverband worden behandeld gelden de volgende aanbevelingen:
 Addendum bij richtlijn 2015 ADVIES VAN DE Myeloom Werkgroep (MWG) VOOR DE BEHANDELING MULTIPEL MYELOOM 2016 S. Zweegman, H.M. Lokhorst, M-D. Levin, E. de Waal, G.M.J. Bos, M.J. Kersten, A. Croockewit,
Addendum bij richtlijn 2015 ADVIES VAN DE Myeloom Werkgroep (MWG) VOOR DE BEHANDELING MULTIPEL MYELOOM 2016 S. Zweegman, H.M. Lokhorst, M-D. Levin, E. de Waal, G.M.J. Bos, M.J. Kersten, A. Croockewit,
Nederlandse samenvatting
 Nederlandse samenvatting Het multipel myeloom of de ziekte van Kahler is een kwaadaardige celwoekering van plasmacellen in het beenmerg die een monoklonale zware of lichte keten immunoglobuline produceren.
Nederlandse samenvatting Het multipel myeloom of de ziekte van Kahler is een kwaadaardige celwoekering van plasmacellen in het beenmerg die een monoklonale zware of lichte keten immunoglobuline produceren.
Wait and See. Arnon Kater. Afdeling Hematologie AMC Amsterdam
 Wait and See Arnon Kater Afdeling Hematologie AMC Amsterdam Onderwerpen Algemene aspecten CLL en non-hodgkin lymfomen Wait and See beleid Therapie CLL en indolente lymfomen anno 2015 Nieuwe ontwikkelingen..?
Wait and See Arnon Kater Afdeling Hematologie AMC Amsterdam Onderwerpen Algemene aspecten CLL en non-hodgkin lymfomen Wait and See beleid Therapie CLL en indolente lymfomen anno 2015 Nieuwe ontwikkelingen..?
Maligne hematologie. Asia Ropela, internist-oncoloog St.Jansdal ziekenhuis 22 maart 2014
 Maligne hematologie Asia Ropela, internist-oncoloog St.Jansdal ziekenhuis 22 maart 2014 Indeling Leukemie acuut AML (acute myeloïde leukemie) ALL (acute lymfoïde leukemie) chronisch CML (chronische myeloïde
Maligne hematologie Asia Ropela, internist-oncoloog St.Jansdal ziekenhuis 22 maart 2014 Indeling Leukemie acuut AML (acute myeloïde leukemie) ALL (acute lymfoïde leukemie) chronisch CML (chronische myeloïde
Multipel Myeloom diagnose en behandeling anno 2015
 Multipel Myeloom diagnose en behandeling anno 2015 Oncologie dag NVvO 30 sept 3015 Monique Minnema, internist-hematoloog Disclosure belangen spreker (potentiële) belangenverstrengeling Voor bijeenkomst
Multipel Myeloom diagnose en behandeling anno 2015 Oncologie dag NVvO 30 sept 3015 Monique Minnema, internist-hematoloog Disclosure belangen spreker (potentiële) belangenverstrengeling Voor bijeenkomst
Chronische lymfatische leukemie Arnon Kater
 Chronische lymfatische leukemie Arnon Kater http://www.lymmcare.nl/ CLL Epidemiologie Prognostische factoren Biologie en targeted therapy Huidige behandeling en studies CLL: epidemiologie CLL is de meest
Chronische lymfatische leukemie Arnon Kater http://www.lymmcare.nl/ CLL Epidemiologie Prognostische factoren Biologie en targeted therapy Huidige behandeling en studies CLL: epidemiologie CLL is de meest
Pacman eats everything... Marie-José Claessen UMCU
 Pacman eats everything... Marie-José Claessen UMCU Casus - presentatie I Casus presentatie I 58- jarige man Voorgeschiedenis o.a.: Oktober - november 2011 Sint Elsewhere : kortademigheid, lymfadenopathie,
Pacman eats everything... Marie-José Claessen UMCU Casus - presentatie I Casus presentatie I 58- jarige man Voorgeschiedenis o.a.: Oktober - november 2011 Sint Elsewhere : kortademigheid, lymfadenopathie,
Nederlandse samenvatting
 Nederlandse samenvatting 147 148 Maligne lymfomen zijn kwaadaardige woekeringen van verschillende typen witte bloedcellen. Deze aandoeningen ontstaan meestal in lymfklieren, maar in ongeveer 40% van de
Nederlandse samenvatting 147 148 Maligne lymfomen zijn kwaadaardige woekeringen van verschillende typen witte bloedcellen. Deze aandoeningen ontstaan meestal in lymfklieren, maar in ongeveer 40% van de
De achilleshiel van CLL
 De achilleshiel van CLL Dr. S.H. Tonino 22 november 2012 Afdeling Hematologie AMC, Amsterdam Chronische lymfatische leukemie 1. wat is chronische lymfatische leukemie (CLL?) 2. behandeling anno 2012 3.
De achilleshiel van CLL Dr. S.H. Tonino 22 november 2012 Afdeling Hematologie AMC, Amsterdam Chronische lymfatische leukemie 1. wat is chronische lymfatische leukemie (CLL?) 2. behandeling anno 2012 3.
Nut en noodzaak van CZS profylaxe bij DLBCL in rituximab tijdperk
 Nut en noodzaak van CZS profylaxe bij DLBCL in rituximab tijdperk Moderator P.J. Lugtenburg speaker Jeanette Doorduijn Belangenverklaring In overeenstemming met de regels van de Inspectie van de Gezondheidszorg
Nut en noodzaak van CZS profylaxe bij DLBCL in rituximab tijdperk Moderator P.J. Lugtenburg speaker Jeanette Doorduijn Belangenverklaring In overeenstemming met de regels van de Inspectie van de Gezondheidszorg
Neoplastische proliferatie van mestcellen
 Mastocytose 4580403 Mastocytose Neoplastische proliferatie van mestcellen Symptomen : Constitutioneel: moe gewichtsverlies koorts, zweten Huid (pruritus, urticaria, dermatografie) Buikpijn, GI-problemen,
Mastocytose 4580403 Mastocytose Neoplastische proliferatie van mestcellen Symptomen : Constitutioneel: moe gewichtsverlies koorts, zweten Huid (pruritus, urticaria, dermatografie) Buikpijn, GI-problemen,
Een abnormale eiwitelectroforese: wat nu? J. Lemmens 21/5/2019
 & Een abnormale eiwitelectroforese: wat nu? J. Lemmens 21/5/2019 1 Abnormale piek in het eiwitprofiel Albumine, A1: antitrypsine/orosmucoid, A2: macroglobuline, haptoglobine, ceruloplasm B: transferrine,
& Een abnormale eiwitelectroforese: wat nu? J. Lemmens 21/5/2019 1 Abnormale piek in het eiwitprofiel Albumine, A1: antitrypsine/orosmucoid, A2: macroglobuline, haptoglobine, ceruloplasm B: transferrine,
Behandeling Mantelcellymfoom anno 2019
 Behandeling Mantelcellymfoom anno 2019 Tom van Meerten Internist-hematoloog Belangenverklaring In overeenstemming met de regels van de Inspectie van de Gezondheidszorg (IGZ) Naam: Tom van Meerten Organisatie
Behandeling Mantelcellymfoom anno 2019 Tom van Meerten Internist-hematoloog Belangenverklaring In overeenstemming met de regels van de Inspectie van de Gezondheidszorg (IGZ) Naam: Tom van Meerten Organisatie
Achtergrond Gerandomiseerde studie om de waarde van autologe stamceltransplantatie aan te tonen bij nieuw gediagnosteerde multipel myeloom.
 Samenvatting Hovon 95 Achtergrond Gerandomiseerde studie om de waarde van autologe stamceltransplantatie aan te tonen bij nieuw gediagnosteerde multipel myeloom. Populatie Eerstelijns behandeling bij multipel
Samenvatting Hovon 95 Achtergrond Gerandomiseerde studie om de waarde van autologe stamceltransplantatie aan te tonen bij nieuw gediagnosteerde multipel myeloom. Populatie Eerstelijns behandeling bij multipel
Wait and See. Hematon, 29 maart 2014 Nieuwegein. Rien van Oers. Afdeling Hematologie AMC Amsterdam
 Wait and See Hematon, 29 maart 2014 Nieuwegein Rien van Oers Afdeling Hematologie AMC Amsterdam Keuze menu voor uw vragen Wait and See beleid Algemene aspecten non-hodgkin lymfomen Indeling lymfomen Klachten
Wait and See Hematon, 29 maart 2014 Nieuwegein Rien van Oers Afdeling Hematologie AMC Amsterdam Keuze menu voor uw vragen Wait and See beleid Algemene aspecten non-hodgkin lymfomen Indeling lymfomen Klachten
HOVON 114 MM (Multiple Myeloom) / multipel myeloom
 HOVON 114 MM (Multiple Myeloom) / multipel myeloom Onderzoek voor patiënten met teruggekeerde of verslechterde multipel myeloom (ziekte van Kahler). Onderzocht wordt of een nieuw medicijn veilig en werkzaam
HOVON 114 MM (Multiple Myeloom) / multipel myeloom Onderzoek voor patiënten met teruggekeerde of verslechterde multipel myeloom (ziekte van Kahler). Onderzocht wordt of een nieuw medicijn veilig en werkzaam
Hooggradige B-cellymfomen met MYC-, BCL2- en/of BCL6- afwijkingen. dr. Lianne Koens Patholoog AMC, Amsterdam
 Hooggradige B-cellymfomen met MYC-, BCL2- en/of BCL6- afwijkingen dr. Lianne Koens Patholoog AMC, Amsterdam l.koens@amc.uva.nl Disclosure belangen spreker (potentiële) belangenverstrengeling Voor bijeenkomst
Hooggradige B-cellymfomen met MYC-, BCL2- en/of BCL6- afwijkingen dr. Lianne Koens Patholoog AMC, Amsterdam l.koens@amc.uva.nl Disclosure belangen spreker (potentiële) belangenverstrengeling Voor bijeenkomst
De ziekte van Waldenström: nieuwe behandelingsmogelijkheden als de ziekte terugkomt. Marie José Kersten AMC, Amsterdam
 De ziekte van Waldenström: nieuwe behandelingsmogelijkheden als de ziekte terugkomt Marie José Kersten AMC, Amsterdam www.lymmcare.nl Behandeling recidief MW Behandeling recidief ziekte van Waldenstrom
De ziekte van Waldenström: nieuwe behandelingsmogelijkheden als de ziekte terugkomt Marie José Kersten AMC, Amsterdam www.lymmcare.nl Behandeling recidief MW Behandeling recidief ziekte van Waldenstrom
Klinische Dag. 3 oktober 2013 Disclosure belangen spreker. (potentiële) belangenverstrengeling
 Klinische Dag 3 oktober 2013 Disclosure belangen spreker (potentiële) belangenverstrengeling Geen 14:30-15:15 dr. Monique Minnema - amyloïdose en andere gevaarlijke kleine klonen: pathogenese en behandeling
Klinische Dag 3 oktober 2013 Disclosure belangen spreker (potentiële) belangenverstrengeling Geen 14:30-15:15 dr. Monique Minnema - amyloïdose en andere gevaarlijke kleine klonen: pathogenese en behandeling
Alles onder controle? Dr. J.J. Uil, MDL-arts
 Alles onder controle? Dr. J.J. Uil, MDL-arts Aanleiding: Risico op kanker bij coeliakie; Kwartaal blad NCV 2014: Artikel van Frederico Biagi Controle intervallen worden verruimd kan dat ongestraft? N.B.
Alles onder controle? Dr. J.J. Uil, MDL-arts Aanleiding: Risico op kanker bij coeliakie; Kwartaal blad NCV 2014: Artikel van Frederico Biagi Controle intervallen worden verruimd kan dat ongestraft? N.B.
Uitkomstenonderzoek in non-hodgkin lymphoma. Hedwig Blommestein
 Uitkomstenonderzoek in non-hodgkin lymphoma ~Kansen en uitdagingen~ Hedwig Blommestein Inleiding Inhoud presentatie Uitkomstenonderzoek Casus rituximab maintenance Achtergrond Resultaten t Conclusie Uitkomstenonderzoek
Uitkomstenonderzoek in non-hodgkin lymphoma ~Kansen en uitdagingen~ Hedwig Blommestein Inleiding Inhoud presentatie Uitkomstenonderzoek Casus rituximab maintenance Achtergrond Resultaten t Conclusie Uitkomstenonderzoek
Nieuwe middelen in acute lymfatische leukemie. Anita W Rijneveld Erasmus MC, Rotterdam
 Nieuwe middelen in acute lymfatische leukemie Anita W Rijneveld Erasmus MC, Rotterdam EFS bij volwassenen 100% 80% 1989-1994 1995-2000 2001-2006 2007-2012 RSR 60% 40% 2007-2012 20% 0% 1989-1994 0 1 2 3
Nieuwe middelen in acute lymfatische leukemie Anita W Rijneveld Erasmus MC, Rotterdam EFS bij volwassenen 100% 80% 1989-1994 1995-2000 2001-2006 2007-2012 RSR 60% 40% 2007-2012 20% 0% 1989-1994 0 1 2 3
Opmerkingen: Inductie 1, level 2, kuur 1 LET OP: alleen kuur 1 (langzaam R schema):
 In studieverband :.. Buiten studieverband HOVON 109 inductie 1, level 2 Rituximab, Chloorambucil, Lenalidomide Therapielijst\ aftekenlijst\aanvraag cytostatica Patiëntsticker: Datum aanvraag Afdeling 12-NAT
In studieverband :.. Buiten studieverband HOVON 109 inductie 1, level 2 Rituximab, Chloorambucil, Lenalidomide Therapielijst\ aftekenlijst\aanvraag cytostatica Patiëntsticker: Datum aanvraag Afdeling 12-NAT
Innovatie in de Hematologie. het belang van onderzoek en toetsing. Prof. Dr. P. Sonneveld Afdeling Hematologie Erasmus MC Rotterdam
 Innovatie in de Hematologie het belang van onderzoek en toetsing Prof. Dr. P. Sonneveld Afdeling Hematologie Erasmus MC Rotterdam Hematologie Ziekten van bloed, beenmerg en lymfeklieren Acute en chronische
Innovatie in de Hematologie het belang van onderzoek en toetsing Prof. Dr. P. Sonneveld Afdeling Hematologie Erasmus MC Rotterdam Hematologie Ziekten van bloed, beenmerg en lymfeklieren Acute en chronische
Hairy cell leukemie. Mariëlle Wondergem hematoloog VUmc
 Hairy cell leukemie Mariëlle Wondergem hematoloog VUmc Wie krijgen leukemie? Elk jaar krijgen in Nederland rond de 1500 mensen leukemie Ongeveer 750 acute leukemie Bij de anderen gaat het om chronische
Hairy cell leukemie Mariëlle Wondergem hematoloog VUmc Wie krijgen leukemie? Elk jaar krijgen in Nederland rond de 1500 mensen leukemie Ongeveer 750 acute leukemie Bij de anderen gaat het om chronische
Moderator. Speaker Drs. A.M.P. Demandt Internist-hematoloog MUMC
 MYELOFIBROSE: DILEMMA VAN TRANSPLANTEREN Moderator Dr. B.J. Biemond Speaker Drs. A.M.P. Demandt Internist-hematoloog MUMC Belangenverklaring In overeenstemming met de regels van de Inspectie van de Gezondheidszorg
MYELOFIBROSE: DILEMMA VAN TRANSPLANTEREN Moderator Dr. B.J. Biemond Speaker Drs. A.M.P. Demandt Internist-hematoloog MUMC Belangenverklaring In overeenstemming met de regels van de Inspectie van de Gezondheidszorg
Myelodysplastisch syndroom
 Myelodysplastisch syndroom Dr. A.H.E. Herbers Hematoloog-Oncoloog 7 februari 2018 Myelodysplastisch syndroom Masterclass 7/2/18 Myelodysplastisch syndroom= MDS Opbouw presentatie: Meeste informatie is
Myelodysplastisch syndroom Dr. A.H.E. Herbers Hematoloog-Oncoloog 7 februari 2018 Myelodysplastisch syndroom Masterclass 7/2/18 Myelodysplastisch syndroom= MDS Opbouw presentatie: Meeste informatie is
Nederlandse samenvatting
 Nederlandse samenvatting nederlandse samenvatting Algemene inleiding Primair bot lymfoom is een zeldzame aandoening. Het is een extranodaal subtype van het grootcellig B non Hodgkin lymfoom, dat zich
Nederlandse samenvatting nederlandse samenvatting Algemene inleiding Primair bot lymfoom is een zeldzame aandoening. Het is een extranodaal subtype van het grootcellig B non Hodgkin lymfoom, dat zich
Stamceltransplantatie
 Autologe en allogene Stamceltransplantatie -een wereld van verschil - Dr. S.K. Klein internist-hematoloog 41 Geschiedenis 1950 eerste beenmergtransplantatie 1990 Edward DonnallThomas & Joseph Edward Murray
Autologe en allogene Stamceltransplantatie -een wereld van verschil - Dr. S.K. Klein internist-hematoloog 41 Geschiedenis 1950 eerste beenmergtransplantatie 1990 Edward DonnallThomas & Joseph Edward Murray
Klinische Dag NVvH 2 oktober 2014 Disclosure belangen S. Boerman. Geen (potentiële) belangenverstrengeling
 Klinische Dag NVvH 2 oktober 2014 Disclosure belangen S. Boerman Geen (potentiële) belangenverstrengeling Hemofagocytair syndroom klinische presentatie, behandeling en complicaties S. Boerman, AIOS St
Klinische Dag NVvH 2 oktober 2014 Disclosure belangen S. Boerman Geen (potentiële) belangenverstrengeling Hemofagocytair syndroom klinische presentatie, behandeling en complicaties S. Boerman, AIOS St
Mantelcellymfoom Versie 18 augustus
 Mantelcellymfoom Versie 18 augustus 2016 -------------------------------------------------------------------------------- HOVON studies HOVON 119: 1e lijn 65 jaar (of > 60 jaar en ineligible voor SCT),
Mantelcellymfoom Versie 18 augustus 2016 -------------------------------------------------------------------------------- HOVON studies HOVON 119: 1e lijn 65 jaar (of > 60 jaar en ineligible voor SCT),
Hodgkin lymfoom. Elly Lugtenburg 11 de nascholing hematologie verpleegkundigen 16 Maart 2018
 Hodgkin lymfoom Elly Lugtenburg 11 de nascholing hematologie verpleegkundigen 16 Maart 2018 11 de nascholing Hematologie verpleegkundigen 16 Maart 2018 Disclosure belangen: PJ Lugtenburg Voor bijeenkomst
Hodgkin lymfoom Elly Lugtenburg 11 de nascholing hematologie verpleegkundigen 16 Maart 2018 11 de nascholing Hematologie verpleegkundigen 16 Maart 2018 Disclosure belangen: PJ Lugtenburg Voor bijeenkomst
M studie (Longkanker) / luchtpijp & longkanker
 M14-361-studie (Longkanker) / luchtpijp & longkanker Onderzoek naar een nieuwe behandeling voor patiënten met vergevorderde kleincellige longkanker die behandeld worden met carboplatine en etoposide (standaardbehandeling).
M14-361-studie (Longkanker) / luchtpijp & longkanker Onderzoek naar een nieuwe behandeling voor patiënten met vergevorderde kleincellige longkanker die behandeld worden met carboplatine en etoposide (standaardbehandeling).
Hematologie voor de huisarts: Lymfocytose en paraproteïne.
 Hematologie voor de huisarts: Lymfocytose en paraproteïne. Jan Van Droogenbroeck 11 maart 2017 INLEIDING: CASUS. BDZ, 03.06.1942 - VG: Hysterectomie 86, postop LE; Herpes zoster 09, Bilaterale knieprothese
Hematologie voor de huisarts: Lymfocytose en paraproteïne. Jan Van Droogenbroeck 11 maart 2017 INLEIDING: CASUS. BDZ, 03.06.1942 - VG: Hysterectomie 86, postop LE; Herpes zoster 09, Bilaterale knieprothese
Non-Hodgkin Lymfomen: naar therapie op maat?
 Non-Hodgkin Lymfomen: naar therapie op maat? LYMMCARE Patiëntensymposium 13 november 2014 Rien van Oers non-hodgkin lymfomen Inleiding: indeling non-hodgkin lymfomen Behandeling anno 2014 Nieuwe ontwikkelingen
Non-Hodgkin Lymfomen: naar therapie op maat? LYMMCARE Patiëntensymposium 13 november 2014 Rien van Oers non-hodgkin lymfomen Inleiding: indeling non-hodgkin lymfomen Behandeling anno 2014 Nieuwe ontwikkelingen
HOVON 93 (Leukemie, AML) / acute myeloïde leukemie
 HOVON 93 (Leukemie, AML) / acute myeloïde leukemie Onderzoek naar een nieuwe behandeling voor patiënten met acute leukemie (acute myeloïde leukemie (AML) of myelodysplasie (MDS) type RAEB of RAEB-t) die
HOVON 93 (Leukemie, AML) / acute myeloïde leukemie Onderzoek naar een nieuwe behandeling voor patiënten met acute leukemie (acute myeloïde leukemie (AML) of myelodysplasie (MDS) type RAEB of RAEB-t) die
HOVON 119 (Mantelcel lymfoom, MCL) / Lymfomen & Reticuloendotheliale Tumoren, non-hodgkinlymfoom
 HOVON 119 (Mantelcel lymfoom, MCL) / Lymfomen & Reticuloendotheliale Tumoren, non-hodgkinlymfoom Onderzoek naar een nieuwe behandeling voor oudere patiënten met mantelcel lymfoom (MCL). Onderzocht wordt
HOVON 119 (Mantelcel lymfoom, MCL) / Lymfomen & Reticuloendotheliale Tumoren, non-hodgkinlymfoom Onderzoek naar een nieuwe behandeling voor oudere patiënten met mantelcel lymfoom (MCL). Onderzocht wordt
Het belang van tijdige herkenning van myeloma defining events (MDE) in het smoldering myeloom: een case report
 Het belang van tijdige herkenning van myeloma defining events (MDE) in het smoldering myeloom: een case report The importance of early recognition of myeloma defining events (MDE) in smoldering myeloma:
Het belang van tijdige herkenning van myeloma defining events (MDE) in het smoldering myeloom: een case report The importance of early recognition of myeloma defining events (MDE) in smoldering myeloma:
Richtlijn Chronische Lymfatische Leukemie. Arnon Kater, Sabina Kersting, Rogier Mous
 Richtlijn Chronische Lymfatische Leukemie Arnon Kater, Sabina Kersting, Rogier Mous 26 januari 2017 Belangenverklaring In overeenstemming met de regels van de Inspectie van de Gezondheidszorg (IGZ) Naam:
Richtlijn Chronische Lymfatische Leukemie Arnon Kater, Sabina Kersting, Rogier Mous 26 januari 2017 Belangenverklaring In overeenstemming met de regels van de Inspectie van de Gezondheidszorg (IGZ) Naam:
ZIEKTE VAN WALDENSTRÖM. Patiëntenboekje. Waldenström heeft een. langzaam progressief. verloop. Dat betekent. dat de aandoening wel
 Waldenström heeft een langzaam progressief verloop. Dat betekent dat de aandoening wel steeds ernstiger wordt, maar dat dit proces heel geleidelijk verloopt Patiëntenboekje ZIEKTE VAN WALDENSTRÖM Waldenström
Waldenström heeft een langzaam progressief verloop. Dat betekent dat de aandoening wel steeds ernstiger wordt, maar dat dit proces heel geleidelijk verloopt Patiëntenboekje ZIEKTE VAN WALDENSTRÖM Waldenström
Nederlandse samenvatting voor medisch niet-ingewijden
 Chapter 9 Beeldvorming rond transformatie: diagnose en behandeling van getransformeerd folliculair lymfoom. Nederlandse samenvatting voor medisch niet-ingewijden Het getransformeerd folliculair lymfoom
Chapter 9 Beeldvorming rond transformatie: diagnose en behandeling van getransformeerd folliculair lymfoom. Nederlandse samenvatting voor medisch niet-ingewijden Het getransformeerd folliculair lymfoom
Monoclonal gammopathy of undetermined significance (MGUS)
 Monoclonal gammopathy of undetermined significance (MGUS) Daan Dierickx Oudenaarde, 18 november 2014 MGUS Basisprincipes: plasmacellen, immuunglobulines, zware en lichte ketens MGUS SMM MM WM AL amyloidose
Monoclonal gammopathy of undetermined significance (MGUS) Daan Dierickx Oudenaarde, 18 november 2014 MGUS Basisprincipes: plasmacellen, immuunglobulines, zware en lichte ketens MGUS SMM MM WM AL amyloidose
Het solitair plasmacytoom
 Het solitair plasmacytoom Moderator Prof. Dr. G.M.J. Bos. E.G.M. de Waal Afdeling Hematologie, UMCG Groningen. Belangenverklaring In overeenstemming met de regels van de Inspectie van de Gezondheidszorg
Het solitair plasmacytoom Moderator Prof. Dr. G.M.J. Bos. E.G.M. de Waal Afdeling Hematologie, UMCG Groningen. Belangenverklaring In overeenstemming met de regels van de Inspectie van de Gezondheidszorg
Intensivering deel IIA en IIB (duur circa 50 dagen)
 HOVON 70 Samenvatting + Checklist Geheugensteun HOVON 70 studie opbergen in polistatus, kopie klinische status Naam patiënt.. AZG nummer.. Geboortedatum.. -.. 19.. Datum Dag 0: Pre-fase (duur 1 week) Dag
HOVON 70 Samenvatting + Checklist Geheugensteun HOVON 70 studie opbergen in polistatus, kopie klinische status Naam patiënt.. AZG nummer.. Geboortedatum.. -.. 19.. Datum Dag 0: Pre-fase (duur 1 week) Dag
Nederlandse samenvatting
 Nieuwe vooruitzichten in de karakterisering en behandeling van acute myeloïde leukemie Nederlandse samenvatting 134 Acute myeloïde leukemie (AML) is een vorm van bloedkanker, een kwaadaardige aandoening
Nieuwe vooruitzichten in de karakterisering en behandeling van acute myeloïde leukemie Nederlandse samenvatting 134 Acute myeloïde leukemie (AML) is een vorm van bloedkanker, een kwaadaardige aandoening
Verminderde perifere neuropathie bij subcutaan bortezomib-gebruik, ook na eerdere intraveneuze toediening
 Verminderde perifere neuropathie bij subcutaan bortezomib-gebruik, ook na eerdere intraveneuze toediening Reduced peripheral neuropathy in subcutaneously administered bortezomib, even after previous intravenous
Verminderde perifere neuropathie bij subcutaan bortezomib-gebruik, ook na eerdere intraveneuze toediening Reduced peripheral neuropathy in subcutaneously administered bortezomib, even after previous intravenous
Officiële uitgave van het Koninkrijk der Nederlanden sinds Gelet op artikel 2.4a, eerste lid, van het Besluit zorgverzekering;
 STAATSCOURANT Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814. Nr. 31881 11 juni 2019 Regeling van de Minister voor Medische Zorg van 3 juni 2019, kenmerk 1535339-191328-Z, houdende wijziging
STAATSCOURANT Officiële uitgave van het Koninkrijk der Nederlanden sinds 1814. Nr. 31881 11 juni 2019 Regeling van de Minister voor Medische Zorg van 3 juni 2019, kenmerk 1535339-191328-Z, houdende wijziging
Nieuwe. behandelingen. bij inhl/cll. Ann Janssens, MD, PhD Hematology, Leuven 14 oct 2016
 Nieuwe behandelingen bij inhl/cll Ann Janssens, MD, PhD Hematology, Leuven 14 oct 2016 Indicaties voor behandeling CLL/iNHL Diagnose Behandeling Uitgebreide ziekte aantal en grootte klieren Grootte milt,
Nieuwe behandelingen bij inhl/cll Ann Janssens, MD, PhD Hematology, Leuven 14 oct 2016 Indicaties voor behandeling CLL/iNHL Diagnose Behandeling Uitgebreide ziekte aantal en grootte klieren Grootte milt,
Andromeda, CyBorD, Arm A, inductiekuur Therapielijst\ aftekenlijst\aanvraag cytostatica Patiëntgegevens: Datum aanvraag Afdeling IHMP
 Andromeda, CyBorD, Arm A, inductiekuur Therapielijst\ aftekenlijst\aanvraag cytostatica Patiëntgegevens: Datum aanvraag Afdeling IHMP 12-NAT: 02274 Lengte (cm) Gewicht (kg) Lich.opp (m²) Gefaxt naar apotheek
Andromeda, CyBorD, Arm A, inductiekuur Therapielijst\ aftekenlijst\aanvraag cytostatica Patiëntgegevens: Datum aanvraag Afdeling IHMP 12-NAT: 02274 Lengte (cm) Gewicht (kg) Lich.opp (m²) Gefaxt naar apotheek
a. RR, pols, ah, temp, gewicht Dexamethason (thuis) (op dag 1,2,8,9,15,16,22,23)
 Andromeda, -CyBorD, Arm B, inductiekuur cyclus 3 t/m 6 Therapielijst\ aftekenlijst\aanvraag cytostatica Patiëntgegevens: Datum aanvraag Afdeling IHMP 12-NAT: 02274 Lengte (cm) Gewicht (kg) Lich.opp (m²)
Andromeda, -CyBorD, Arm B, inductiekuur cyclus 3 t/m 6 Therapielijst\ aftekenlijst\aanvraag cytostatica Patiëntgegevens: Datum aanvraag Afdeling IHMP 12-NAT: 02274 Lengte (cm) Gewicht (kg) Lich.opp (m²)
Casus hematologie Huisarts Danny Hiel Hematoloog Inge Vrelust
 Gevorderde ziekte: geen curatie, wel controle! Casus hematologie Huisarts Danny Hiel Hematoloog Inge Vrelust Casus Plasmacelleukemie Man 1965, gezond leven Opname ICU met septische shock en multiorgaanfalen.
Gevorderde ziekte: geen curatie, wel controle! Casus hematologie Huisarts Danny Hiel Hematoloog Inge Vrelust Casus Plasmacelleukemie Man 1965, gezond leven Opname ICU met septische shock en multiorgaanfalen.
Belangenverklaring. In overeenstemming met de regels van de Inspectie van de Gezondheidszorg (IGZ)
 Belangenverklaring In overeenstemming met de regels van de Inspectie van de Gezondheidszorg (IGZ) Naam: Organisatie: AC Abrahams UMC Utrecht Ik heb geen 'potentiële' belangenverstrengeling Ik heb de volgende
Belangenverklaring In overeenstemming met de regels van de Inspectie van de Gezondheidszorg (IGZ) Naam: Organisatie: AC Abrahams UMC Utrecht Ik heb geen 'potentiële' belangenverstrengeling Ik heb de volgende
Acute myeloïde leukemie. Dimitri A. Breems, MD, PhD Internist-Hematoloog Ziekenhuis Netwerk Antwerpen
 Acute myeloïde leukemie Dimitri A. Breems, MD, PhD Internist-Hematoloog Ziekenhuis Netwerk Antwerpen Normale bloedcelvorming Acute myeloïde leukemie (AML) Klonale proliferatie van immature hematopoëtische
Acute myeloïde leukemie Dimitri A. Breems, MD, PhD Internist-Hematoloog Ziekenhuis Netwerk Antwerpen Normale bloedcelvorming Acute myeloïde leukemie (AML) Klonale proliferatie van immature hematopoëtische
Maligne pleura exsudaat
 Maligne pleura exsudaat Regionale richtlijn IKL, Versie: 1.1 Laatst gewijzigd : 25-10-2005 Methodiek: Consensus based Verantwoording: IKL werkgroep bronchuscarcinomen Inhoudsopgave Algemeen...1 Diagnostiek...2
Maligne pleura exsudaat Regionale richtlijn IKL, Versie: 1.1 Laatst gewijzigd : 25-10-2005 Methodiek: Consensus based Verantwoording: IKL werkgroep bronchuscarcinomen Inhoudsopgave Algemeen...1 Diagnostiek...2
Ontwikkelingen in de behandeling van het indolente non-hodgkin lymfoom Hematon/LVN Patiëntensymposium
 Ontwikkelingen in de behandeling van het indolente non-hodgkin lymfoom Hematon/LVN Patiëntensymposium 13 september 2014 Marie José Kersten non-hodgkin lymfomen Inleiding: indeling non-hodgkin lymfomen
Ontwikkelingen in de behandeling van het indolente non-hodgkin lymfoom Hematon/LVN Patiëntensymposium 13 september 2014 Marie José Kersten non-hodgkin lymfomen Inleiding: indeling non-hodgkin lymfomen
Nederlandse samenvatting
 Nederlandse samenvatting In dit proefschrift worden diagnostische en therapeutische aspecten van acute leukemie bij kinderen beschreven, o.a. cyto-immunologische en farmacologische aspecten en allogene
Nederlandse samenvatting In dit proefschrift worden diagnostische en therapeutische aspecten van acute leukemie bij kinderen beschreven, o.a. cyto-immunologische en farmacologische aspecten en allogene
Cover Page. The following handle holds various files of this Leiden University dissertation:
 Cover Page The following handle holds various files of this Leiden University dissertation: http://hdl.handle.net/1887/61127 Author: Hulle, T. van der Title: The diagnostic and therapeutic management of
Cover Page The following handle holds various files of this Leiden University dissertation: http://hdl.handle.net/1887/61127 Author: Hulle, T. van der Title: The diagnostic and therapeutic management of
Casuistiek met aandacht voor nieuwe therapieën bij Ziekte van Waldenström en Multipel myeloom
 Casuistiek met aandacht voor nieuwe therapieën bij Ziekte van Waldenström en Multipel myeloom Dr Vincent Maertens hematologie AZ St-Maarten Mechelen/ Imeldaziekenhuis Bonheiden Abnormaal eiwitje = monoclonaal
Casuistiek met aandacht voor nieuwe therapieën bij Ziekte van Waldenström en Multipel myeloom Dr Vincent Maertens hematologie AZ St-Maarten Mechelen/ Imeldaziekenhuis Bonheiden Abnormaal eiwitje = monoclonaal
Hoofdstuk 2 Hoofdstuk 3
 Samenvatting 11 Samenvatting Bloedarmoede, vaak aangeduid als anemie, is een veelbesproken onderwerp in de medische literatuur. Clinici en onderzoekers buigen zich al vele jaren over de oorzaken en gevolgen
Samenvatting 11 Samenvatting Bloedarmoede, vaak aangeduid als anemie, is een veelbesproken onderwerp in de medische literatuur. Clinici en onderzoekers buigen zich al vele jaren over de oorzaken en gevolgen
Een patiente met acute leukemie Bloed en beenmerg Acute leukemie Chronische leukemie
 Thema: Leukemie Een patiente met acute leukemie Bloed en beenmerg Acute leukemie Chronische leukemie Prof.dr. Hanneke C. Kluin-Nelemans Afdeling Hematologie Samenstelling van onstolbaar gemaakt bloed Bloedcellen
Thema: Leukemie Een patiente met acute leukemie Bloed en beenmerg Acute leukemie Chronische leukemie Prof.dr. Hanneke C. Kluin-Nelemans Afdeling Hematologie Samenstelling van onstolbaar gemaakt bloed Bloedcellen
WORKSHOP ANEMIE. een Maastrichtse aanpak. Michel van Gelder internist-hematoloog
 WORKSHOP ANEMIE een Maastrichtse aanpak Michel van Gelder internist-hematoloog met dan aan: Sacha Zeerleder(hematoloog, AMC) & Arno Gingele(1 e jaarsaios, MUMC) Na deze Workshop ben je ONGETWIJFELD in
WORKSHOP ANEMIE een Maastrichtse aanpak Michel van Gelder internist-hematoloog met dan aan: Sacha Zeerleder(hematoloog, AMC) & Arno Gingele(1 e jaarsaios, MUMC) Na deze Workshop ben je ONGETWIJFELD in
PJP profylaxe bij prednison. Amelieke Cremers, AIOS MMB
 PJP profylaxe bij prednison Amelieke Cremers, AIOS MMB 30-10-2018 Q 1. Indicatie 2. Wanneer starten PJP Prednison Profylaxe PJP Wat is het Waar komt het vandaan Welke problemen Hoe toon je het aan Lymfocyten
PJP profylaxe bij prednison Amelieke Cremers, AIOS MMB 30-10-2018 Q 1. Indicatie 2. Wanneer starten PJP Prednison Profylaxe PJP Wat is het Waar komt het vandaan Welke problemen Hoe toon je het aan Lymfocyten
Chronische lymfoproliferatieve aandoeningen
 Lessenreeks Hematologie Chronische lymfoproliferatieve aandoeningen Caroline Brusselmans & Mieke Develter LAG chronische lymfoproliferatieve aandoeningen chronische lymfoproliferatieve aandoeningen chronische
Lessenreeks Hematologie Chronische lymfoproliferatieve aandoeningen Caroline Brusselmans & Mieke Develter LAG chronische lymfoproliferatieve aandoeningen chronische lymfoproliferatieve aandoeningen chronische
