gea CHEMISCHE FORMULES: hulpmiddel, geen toverspreuken II december 1980, vol. 13, nr. 4, pag Drie belangrijke antwoorden
|
|
|
- Rosalia Peeters
- 7 jaren geleden
- Aantal bezoeken:
Transcriptie
1 gea december 1980, vol. 13, nr. 4, pag driemaandelijks tijdschrift van de Stichting Geologische Aktiviteiten voor belangstellenden in de geologie en mineralogie Inhoud: Chemische formules 93 De Geologische Tijdschaal 97 Fossiele getuigen van het oudste leven 100 Groeilijntjes 107 Meteorietinslag markeert overgang Krijt-Tertiair? 114 Het Ultramafisch massief bij Kraubath an der Mur 117 Kunststoffen voor de fossielenverzamelaar 121 Macrofoto's van mineralen 125 Trillingen en macrofotografie 132 Ultrasoon reinigen. 133 Boekbesprekingen 133 Krokoiet naast pag. 136 Bijlage: Cursusprogramma 1981 Kringprogramma's, mededelingen. CHEMISCHE FORMULES: hulpmiddel, geen toverspreuken II door drs. W.R. Moorer In de horeca betekent de afkorting MgC0 3, dat aan één tafel is besteld: één Grand Marnier (Mg), één Cognac (C) en drie koffie (O). Kijkt u in uw mineralenboeken bij "magnesiet" dan ziet u MgC0 3 staan. Dit is de afkorting die slaat op de gang van zaken in de Zaak der Stenen en Mineralen en met behulp van uw grondstoffen- of elementenlijst (die u op slinkse wijze bij-de-hand houdt) ziet u dus dat het mineraal magnesiet is samengesteld uit één eenheid magnesium (Mg), één eenheid koolstof (C) en drie eenheden zuurstof (O). Heeft u per ongeluk bij magnetiet in plaats van bij magnesiet gekeken dan bemerkt u de vergissing al meteen aan de formule; die voor magnetiet luidt: Fe 3, dat is samengesteld uit 3x ijzer (Fe) en 4x zuurstof. U begrijpt inmiddels de verwarrende naamgeving al: "magnesiet" omdat het magnesium bevat, "magnetiet" vanwege de magnetische eigenschappen van dit ijzermineraal. Bezit u een heel goed mineralenboek, dan is het aardig eens naar de mineralen van de spinel-groep te kijken. U vindt daar o.a. het "magnesioferriet". De formule van magnesioferriet zal u nu niet meer verbazen: MgFe 2. Degene die dit mineraal van een naam heeft voorzien keek domweg naar de samenstelling ervan! Steeds weer zien we dat die "onbegrijpelijke" formule domweg een simpele afkorting is van de samenstelling en dus van de ge-aard-heid van ons mineraal. Geen toverspreuk, maar hulpmiddel. Geen gewichtig gedoe, gewoon een afkortingensysteem. En tóch vraagt u, cursist, zich af wat we er nou helemaal mee opschieten, met die afkortingen, formules, elementen. Want het is misschien wel aardig dat we weten dat het mineraal magnesiet uit magnesium, koolstof en zuurstof bestaat maar wat hebben we daar dan aan?! Tja, we kunnen in onze encyclopedie natuurlijk opzoeken wat b.v. magnesium voor een soort spul is, maar dan? Bovendien, zult u opmerken, lijkt het onwaarschijnlijk dat het witte mineraal magnesiet o.a. (zwarte) koolstof bevat! Hoe zit dat eigenlijk? Drie belangrijke antwoorden Op deze vragen, geachte cursist, moeten drie belangrijke antwoorden worden gegeven. 1. Formules leren ons niet alleen uit welke elementen onze mineralen bestaan, ze leren ons tevens de hoeveelheid van elk element te bepalen. Naast kwalitatieve dus ook kwantitatieve informatie. U zult straks op simpele wijze leren berekenen, dat 1 ons magnesiet 14 gram koolstof bevat! Of, om een praktischer voorbeeld te noemen, dat er ruim 3 ton zuiver magnesiet-erts nodig is om 1 ton van het begeerde lichtmetaal magnesium te verkrijgen. 2. Formules leren ons de verwantschap en daarmee de systematiek van de mineralen beheersen. Magnesiet (MgC0 3 ) is niet verwant aan magnetiet (Fe 3 ), maar wél aan calciet CaC0 3, rhodochrosiet MnC0 3 en andere C0 3 mineralen. Een groot aantal belangrijke eigenschappen en eigenaardigheden wordt daarmee duidelijk. 3. De formule van een mineraal geeft aan dat de samenstellende elementen niet vrij maar gebonden aanwezig zijn. 93
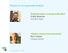
2 Het gebonden zijn van de elementen ontdoet ze blijkbaar van hun eigenschappen. Zo'n verbinding van verschillende elementen komt op de proppen met geheel nieuwe eigenschappen! We kunnen ons als mineraalverzamelaar verheugen over het avontuur van het handjevol elementen dat door middel van het vermogen om duizenden verbindingen aan te gaan, ook duizenden nieuwe eigenschappen oplevert. Als magnesium, koolstof en zuurstof zich tijdens de mineraalvorming verbinden tot magnesiet zijn daarmee de individuele eigenschappen van magnesium, koolstof en zuurstof verdwenen, ze hebben plaatsgemaakt voor de eigenschappen van magnesiet. Chemici spreken trots over chemische verbindingen en bestuderen ijverig de nieuwe eigenschappen ervan. Hun wetenschap is nogal vluchtig als je nagaat dat alles toch maar berust op ons handjevol elementen. Maar u zult moeten toegeven dat het natuurlijk erg aardig is om je bezig te houden met steeds weer nieuwe en soms verrassende eigenschappen. Dit maakt ook het verzamelen interessant! Stel je voor dat er geen nieuwe eigenschappen vastzaten aan verbindingen, dan viel er weinig meer te verzamelen dan alleen de elementen. Dan was onze vitrine gevuld met ijzer, koper, zwavel, een flesje zuurstof en nog 46 elementen en daarmee basta. De architekt Mendeleëv Eind vorige eeuw vermoedde Mendeleëv dat de duizenden en duizenden eigenschappen van mineralen en andere verbindingen toch op de een of andere manier direkt van de samenstellende elementen moesten zijn af te leiden. In veel gevallen was dat duidelijk: alle verbindingen van het fig. 6. Russische postzegel, gewijd aan Mendeleëv, tezamen afgedrukt met een pagina van zijn aantekeningen. element lood bleken nogal zwaar te zijn en ook voor de tinverbindingen gold dat. De moeilijkheid was echter dat weliswaar de verbindingen van kwik ook zwaar waren, maar verder geheel andere eigenschappen bleken te hebben dan die van lood en tin. Dit type moeilijkheden was zelfs ervaren systematici te bar: uit de chaos van eigenschappen konden zij geen zinvolle ordening scheppen. Mendeleëv echter bleef puzzelen en op een goede dag had hij het gevonden: bij rangschikking van de elementen niet op alfabet of zo maar op hun gewicht, bleken overeenkomstige eigenschappen te behoren bij verbindingen van de elementen die acht öf achttien plaatsen in rangvolgorde verschilden. Dus: twee rijen van acht en drie rijen van achttien = 18 kolommen van elementen met overeenkomstige eigenschappen. Een soort getallen-gegoochel dus. Figuur 6. Hoe dan ook: het resultaat van Mendeleëvs gepuzzle ziet u in fig. 7. De 50 zo langzamerhand vertrouwde afkortingen zijn nu voorzien van hun relatief gewicht. Dit zogenaamde atoomgewicht geeft aan hoeveel maal zo zwaar een element is als waterstof (H = 1). U ziet dat de elementen in (horizontale) rijen volgens hun atoomgewicht zijn gerangschikt. De grap is dus nu, dat in de (vertikale) kolommen de elementen staan die verbindingen (en mineralen) vormen met overeenkomstige formules, overeenkomstig gedrag en andere overeenkomstige eigenschappen. Eigenlijk komt het erop neer dat de toch al kleine groep van elementen periodiek verdeeld kan worden in 18 kolommen of groepjes met overeenkomstig gedrag. Je zou kunnen zeggen: 18 families. Onder dit periodiek systeem der elementen hebben generaties lang de scheikunde-leerlingen geleden. Dit was echter niet de schuld van Mendeleëv. Wij, cursisten, gaan integendeel nog veel plezier beleven aan het periodiek systeem! "Met figuur 7 in de hand,!" En inderdaad loont het de moeite om figuur 7 (stiekum) in uw handtasje of binnenzak te dragen. Periodieke eigenschappen De eerste kolom bevat H (waterstof), Li(thium), Na(trium) en K(alium). Dit is de kolom van de alkalimetalen. In de mineralenwereld komen de elementen H, Na en K zéér veel voor. In tabel I van de vorige aflevering ziet u, dat deze drie goed zijn voor ruim 5,5 gewichtsprocenten van de vaste aardkorst. Het verbaast u dan ook niet dat ze veel voorkomen in de gesteentevormende mineralen: veldspaten, glimmers, pyroxenen, amfibolen, foi'den enz. U struikelt er letterlijk over! Nu komen ook uw kopieën van fig. 3 uit de vorige aflevering goed te pas: Als u de 10 of 15 meest voorkomende elementen op zo'n kopie arceert of omcirkelt ziet u als het ware de samenstelling van de aardkorst voor 99% respektievelijk 99,5% weerspiegeld op het periodiek systeem. Kolom twee bevat de zgn. aardalkali-metalen: Be(ryllium), Magnesium, Ca(lcium), Strontium en Ba(rium). Voor magnesium en calcium geldt eigenlijk hetzelfde als voor de alkali-metalen Na en K: ze representeren zo'n 5,5% van het gewicht van de aardkorst en we vinden magnesium en calcium zéér vaak in gesteentevormende mineralen. (Magnesium echter komt niet voor in de veldspaten!) Strontium en Barium kennen we allemaal als hoofdbestanddeel van de prachtige verzamelaarsmineralen celestien SrS, strontianiet SrC0 3 en bariet BaS, respektievelijk witheriet BaC0 3. Bovendien worden deze Sr- en Ba-verbindingen gebruikt in vuurwerk, en geven als zodanig kleur aan het leven bij nacht! Kijkt u ook eens in 94 Gea, vol. 13, nr. 4
3 H 1 Li 7 Be 9 B 11 C 12 N F 19 Na 23 Mg 24 Al 27 Si 28 P 31 S 32 Cl 35 K 39 Ca 40 Ti 48 V 51 Cr 52 Mn 55 Fe 56 Co 59 Ni 59 Cu 64 Zn 65 Ge 73 As 75 Se 79 Br 80 Sr 88 Y 89 Zr 91 Nb 93 Mo 96 Ag 108 Sn 119 Sb 122 Te 128 I 127 Ba 137 (ZA) Ta 181 W 184 Pt 195 Au 197 Hg 201 Pb 207 Bi 209 Th U fig- 7. De 50 elementen, gerangschikt op hun (relatief) gewicht, en ondergebracht in horizontale rijen, zodanig dat de overeenkomstige eigenschappen in 18 vertikale kolommen terechtkomen. De atoomgewichten van de zeldzame-aardmetalen lopen van 139 tot 175. Th(orium) heeft 232 en U(ranium) heeft 238. De atoomgewichten zijn afgerond. uw mineralenboeken naar harmotoon en naar brewsteriet of svanbergiet. U ziet dat deze "exotische" mineralen behoorlijke hoeveelheden Ba of Sr bevatten! Beryllium is verreweg het lichtste en zeldzaamste aardalkali-metaal uit onze reeks. Dat zou je ook wel denken bij de herinnering aan smaragd en aquamarijn, de edele variëteiten van het mineraal beryl en dat klinkt behoorlijk duur en zeldzaam. "Gewone" beryl heeft u echter ongetwijfeld in de verzameling omdat het een normaal bestanddeel van vele pegmatieten is. Hier zien we weer één van de manieren waarop zeldzame elementen tóch goed bekend en toegankelijk kunnen zijn: nl. lokaal geconcentreerd in bijzondere chemische omgevingen (pegmatieten, hydrothermale ertsaders en nog wel andere kraamkamers van in feite bijzondere verbindingen). Behalve beryl kennen we van beryllium nog enkele tientallen zelfstandige mineralen zoals u kunt nakijken in de boeken: chrysoberyl, hamliniet, gadoliniet, euklaas, phenakiet, helvien zijn de meest bekende. De aantrekkingskracht van uitersten De alkali- en aardalkali-metalen van kolom I en II staan helemaal links in het periodiek systeem. Naarmate we verder naar rechts gaan, gaan de eigenschappen steeds meer verschillen van die van I en II. U herinnert het zich: overeenkomstige eigenschappen vinden we in de (vertikale) kolommen, niet bij naast gelegen elementen. Zijn we rechts aangekomen, bij F(luor) en Chloor, dan blijken deze elementen F en Cl zó verschillend te zijn van de (aard)alkali-metalen, dat we zoals zo vaak in dit soort gevallen kunnen spreken van een grote aantrekkingskracht. Hetgeen resulteert in verbindingen. En in mineralen! Wie zou de talloze klei r- en vormvarianten van CaF 2 (fluoriet) willen missen, of de gladde kubussen van steenzout (NaCI)? Carnailliet: KMgCI 3.6H 2 0, sellaiet: MgF 2, sylvien: KCI en kryoliet: Na 3 AIF 6 zijn de gevolgen van dit soort aantrekkingskracht. Nu zouden we kunnen vermoeden dat alles wat ergens rechts staat, verbindingen aangaat met alles van links!? Dit is een goede gedachte en in navolging van CaF 2 (fluoriet) zou er dus CaCI 2, CaBr 2 en Cal 2 moeten bestaan. Of b.v. BaF 2, SrBr 2, LiBr 2 enz. enz. Deze verbindingen bestaan inderdaad: ze kunnen in het laboratorium gemaakt worden, soms onder bijzondere omstandigheden. Er zijn echter twee redenen waarom fluoriet wél en b.v. LiBr 2 niet als mineraal te boek staat. Ten eerste zijn Br, I en - in mindere mate - Li, Sr en Ba tamelijk zeldzame bestanddelen van de aardkorst (tabel I) zodat hun kontaktkans klein is en daarmee de verbinding zeldzaam zal zijn. Ten tweede heersen in de aardkorst andere omstandigheden dan in het laboratorium die maken dat als er al sprake is van een ontmoeting tussen Li en Br deze mogelijke partners onder de daar heersende omstandigheden eenvoudigweg de voorkeur geven aan andere partners. Als gevolg van gewone concurrentie gaat de verbintenis niet door! Zo gaat dat nu eenmaal ook bij mineraalvorming. Het element zuurstof (O) bevindt zich naast F, vrijwel helemaal rechts in het systeem. Het ligt dan ook voor de hand om aantrekkingskracht tussen zuurstof en onze twee linker kolommen te verwachten. Inderdaad. Eigenlijk nog veel belangrijker dan de verbindingen met F en Cl zijn de verbindingen van onze (aard)alkali-metalen met zuurstof. Kijkt u er uw boeken maar op na: komt er in een formule een (aard)alkali-element voor dan kunt u ervan op aan dat in diezelfde formule ook O aanwezig is. Afgezien van de paar F- en Ci-mineralen (zonder zuurstof) gaat deze regel altijd op! Er is nl. 1) érg veel zuurstof in onze aardkorst en 2) de aantrekkingskracht van onze (aard)alkali-metalen tot zuurstof is hevig. Vandaar. Die neiging zich met zuurstof te verbinden bezitten ook andere "linkse" elementen. Met gedeeltelijke uitzondering van Mo(lybdeen) vinden we in de kolommen lll-vii dan ook elementen die bijna altijd mineralen vormen waarin zuurstof een belangrijke rol speelt. Zeer veel interessante mineralen danken we daaraan: monaziet, torberniet, rutiel, anataas, titaniet, zirkoon, vanadiniet, pyrochloor, chromiet, crocoiet, wulfeniet, wolframiet, scheel iet, manganiet, rhodochrosiet, spessartien. Al deze fraaie mineralen komen öf als accessorische bestanddelen in kleine hoeveelheden in gesteenten voor (met name monaziet, rutiel, zirkoon) óf ze vormen mooie kristallen in bijzondere chemische en mineralogische omstandigheden. 95
4 Daarnaast zijn er nog talloze Ti-, Zr- en Nb-houdende silicaten die als bijzondere gesteentevormers voorkomen in zeldzame (alkali)gesteenten. In fig. 8 is - samenvattend - aangegeven dat het linker blok metalen zich vrijwel altijd verbindt met zuurstof. Ook hebben we gezien dat F en Cl soms graag geziene partners zijn voor de (aard)alkali-metalen. In feite is het zo dat het komplete rechter bovenblok, maar natuurlijk vooral de meest voorkomende elementen daarvan, veelvuldige en vaak gekombineerde partners zijn voor de metalen uit kolom l-vii. Met behulp van uw kopieën van fig. 3 uit de vorige aflevering kunt u dit aangeven b.v. op de manier van fig. 9, en kontroleren via de formules in de boeken. fig. 8. De reactieve metalen van het linker blok (I - VII). Zij vormen met zuurstof (O) hechte verbindingen. Hoeveel lood zit er in zwaarspaat? Om deze vraag te kunnen beantwoorden moeten we eerst weten wat zwaarspaat is. Welnu, u zult wel weten dat zwaarspaat een aardig synoniem is voor wat officieel het mineraal bariet heet. Deze naam is weer afgeleid van het Griekse "barüs" = zwaar. Gewicht alom dus, en inderdaad voelt u dat het mineraal zwaar op de hand ligt en ook soms! zwaar op de maag. Dit laatste dan als u in het ziekenhuis "bariumpap" = een papje van gepoederd bariet moet slikken om röntgencontrastfoto's mogelijk te maken. Maar, we moesten weten wat bariet nu eigenlijk is. In zo'n geval, cursisten, kijken we gewoon naar de formule. In ieder mineralenboek vinden we die formule: BaS. In de horeca zouden ze komen aandragen met een brandewijn, een sherry en vier koffie. Wi'j weten nu dat bariet bestaat uit barium, zwavel en zuurstof en wel in de verhouding 1:1:4. Chemici en andere formule-freaks zouden het héél n H ü ü tl I I 1 I 31 T7TT B C N F Al Si P S Cl ft Él m ü Hl Fe Co Ni Cu Zn Ge As Se Br Él m n ik ü 1 in ü n n ü m Ag Sn Sb Te 1 Pt Au Hg Pb Bi fig. 9. De reactieve metalen van het linker blok "reageren' bij voorkeur met de 10 van rechts. De minerale verbindingen die zo worden gevormd kennen we uit eigen ervaring van onze verzamelingen. De meeste van deze verbindingen zijn natuurlijk die, die tussen de meestvoorkomende elementen (O, Si, Al, resp. Ca, Na, K, Mg, Ti, H, P) worden gevormd. Hl ü iiiiill ü Hl in Hl ü Hl ü m H WW Fe Co Ni Cu Zn Ge As St! Br Hl H ü P Ag Sn Sb T e 1 Hl Pt Au Hg Pb Bi H Él ü IP n W< 96 Gea, vol. 13, nr. 4
5 mooi weten te brengen: ''bariet (BaS ) is een verbinding waarvan het molecuul bestaat uit 1 atoom Ba, 1 atoom S en 4 atomen O". Je zou ook gewoon kunnen zeggen: bariet bestaat uit 1 deel Ba, 1 deel S en 4 delen O. Het enige nadeel van de term "deel" ligt daarin, dat niet altijd precies duidelijk is wat ermee wordt bedoeld. Veel recepten waarin de term "deel" voorkomt zijn bij voorbaat weinig nauwkeurig in elkaar gezet. (Dit is één van de redenen waarom grootmoeders cake later niet goed nagemaakt kan worden.) Wat chemici en ook wijzelf willen bedoelen met "deel" is eigenlijk het stoffelijke "deeltje". Het gaat om de aantallen deeltjes of eenheden van elk element waaruit een verbinding is opgebouwd. Dus: een eenheid BaS is opgebouwd uit 1 eenheid Ba, 1 eenheid S en vier eenheden O. Of, wat hetzelfde is: duizend eenheden BaS zijn opgebouwd uit 1000 eenheden Ba, 1000 eenheden S en 4000 eenheden O. Omdat de (mineralogische) formules verhoudingsformules zijn doet het er niet toe met welk getal we alles vermenigvuldigen. Immers 1:1:4 is hetzelfde als 25:25:100 of 3.000:3.000: enz. enz. We weten nu dus dat bariet bestaat uit Ba, S en O en wel wat de aantallen betreft in een verhouding 1:1:4. En lood dan? Waar zit het lood in ons zwaarspaat? Juist, nergens dus. Als er lood in bariet zou zitten zou dat in de formule moeten staan, de formule geeft immers de samenstelling! Lood (Pb) komt in de formule niet voor en zit dus ook niet in bariet. Het enige wat in bariet wél zit is barium, zwavel en zuurstof, maar dat wisten we inmiddels tot in den treure. Hoewel we het misschien vreemd vinden dat het ons zo bekende bariet blijkbaar zwavel bevat, realiseren we ons dat bij het vormen van verbindingen uit elementen nieuwe eigenschappen optreden, tegelijk met het "verdwijnen" van de eigenschappen van de "losse" elementen. U weet het: het bakken van een cake leidt tot nieuwe eigenschappen, de oorspronkelijke eigenschappen van de bestanddelen van het beslag: suiker, boter, bloem, water, lijken "verdwenen" te zijn. O.K., zwavel dus in bariet. Maar als we nu eens een stuk van, zeg, één ons bariet uit onze verzameling pakken, hoeveel zwavel zit daar dan wel in? En met "hoeveel" wordt nu bedoeld: hoeveel aan gewicht, of: hoeveel grammen zwavel? Mendeleev had de elementen op hun gewicht gerangschikt nietwaar: bij elk element hoorde een eigen gewicht. H=1, Ba=137x zo zwaar als H, S=32x, 0=16x zo zwaar als H enz. Figuur 7 toont deze zgn. atoomgewichten. Als we willen weten hoeveel grammen zwavel ergens in zit, dan nemen we het (atoom)gewicht van zwavel (32 dus) en delen dat door het totale gewicht van de verbinding. Dit totale verbindingsgewicht (molecuulgewicht heet dat eigenlijk) is voor bariet de optelsom van de gewichten van 1Ba + 1S + 4x0 = x16 = 233. Het gewichtsaandeel van zwavel in bariet is dus het 32/233 deel = 13,7%. Ons stuk bariet van een ons bevat 13,7 gram zwavel. Op dezelfde manier zien we dat ons stuk 137/233 = 58,8 gram barium bevat en 4x16/233 = 27,5 gram zuurstof. Samen: 13,7 + 58,8 + 27,5= 100 gram = 1 ons. Het feit dat ieder element een vast gewicht (het atoomgewicht) bezit, leidt ertoe dat formules niet alleen de samenstelling (de kwaliteit) vertegenwoordigen, maar ook de kwantiteit mededelen. Dit laatste in - na enig rekenwerk hele praktische eenheden zoals grammen, kilogrammen of tonnen. Met behulp van figuur 7 kunt u de gewichtshoeveelheden van elk element in welk mineraal dan ook uitrekenen. Stel dat u nu eindelijk wel eens de hoeveelheid fluor in fluoriet wilt weten. Dan pakt u een mineralenboek, zoekt de formule van fluoriet op: CaF 2 en noteert de atoomgewichten (fig. 7) van Ca(lcium) = 40 en F(luor) = 19. Het fluoraandeel in fluoriet is dus 2 x 19 gedeeld door 2x = 38/78 x 100% =48,1%. Zo'n bergje fluoriet bij Hoogovens van bv. 100 ton vertegenwoordigt dus een hoeveelheid van kg fluor. Een hoeveelheid die tandartsen tot nadenken zal stemmen: in principe kunnen met die hoeveelheid fluor zeker 12 miljoen kinderen 10 jaar lang profiteren van fluoridetabletjes! In het begin van dit artikel wilden we het koolstof-gehalte in magnesiet (MgC0 3 ) uitrekenen. We maken dan het sommetje op: MiTÜT3*3 = x16 = 84 < x100% > = 1 4 ' 3 % " U kunt zelf nagaan dat een mijningenieur aan drie ton magnesiet te weinig heeft om een ton magnesium te produceren. (wordt vervolgd) De Geologische Tijdschaal: een raamwerk voor de stratigrafie en paleontologie In dit Gea-nummer, waarin verscheidene stratigrafisch en paleontologisch getinte artikelen zijn opgenomen, leek ons de publicatie van de Geologische Tijdschaal weer eens op zijn plaats. Het is handig, de namen van de era en perioden met hun volgorde paraat in het hoofd te hebben. De 80 namen voor de etages (tijden) zijn meer als naslagmogelijkheid bedoeld! De aardkorst is opgebouwd uit verschillende lagen, die in verschillende geologische perioden zijn ontstaan. In een serie van normaal op elkaar liggende aardlagen is een hogere laag jonger dan de daaronder liggende laag (Wet van de superpositie, door Nicolaus Steno in 1669 geformuleerd). De ouderdom van een aardlaag ten opzichte van een andere laag in een laagpakket kan vastgesteld worden, al naar gelang deze hoger of lager in het pakket ligt. Bij o.a. plooibewegingen, waardoor scheef stel ling of zelfs omkering van lagen optrad, is de Wet van superpositie niet zonder meer te hanteren. Maar fossiele fauna's en flora's volgen elkaar op karakteristieke en herkenbare wijze op (Wet van de faunale successie, ontdekt door William Smith, 1815). Hierdoor kan de opeenvolging van fossielhoudende sedimentlagen in een pakket worden vastgesteld. Ook is correlatie mogelijk: door vergelijking van aanwezige fossielen kunnen lagen die op grote afstand van elkaar liggen met elkaar in verband worden gebracht. In de Geologische Tijdschaal is de relatieve opeenvolging 97
gelijk aan het aantal protonen in de kern. hebben allemaal hetzelfde aantal protonen in de kern.
 1 Atoombouw 1.1 Atoomnummer en massagetal Er bestaan vele miljoenen verschillende stoffen, die allemaal zijn opgebouwd uit ongeveer 100 verschillende atomen. Deze atomen zijn zelf ook weer opgebouwd uit
1 Atoombouw 1.1 Atoomnummer en massagetal Er bestaan vele miljoenen verschillende stoffen, die allemaal zijn opgebouwd uit ongeveer 100 verschillende atomen. Deze atomen zijn zelf ook weer opgebouwd uit
5 Formules en reactievergelijkingen
 5 Formules en reactievergelijkingen Stoffen bestaan uit moleculen en moleculen uit atomen (5.1) Stoffen bestaan uit moleculen. Een zuivere stof bestaat uit één soort moleculen. Een molecuul is een groepje
5 Formules en reactievergelijkingen Stoffen bestaan uit moleculen en moleculen uit atomen (5.1) Stoffen bestaan uit moleculen. Een zuivere stof bestaat uit één soort moleculen. Een molecuul is een groepje
Voorstelling van moleculen en atomen in chemische symbolentaal
 Voorstelling van moleculen en atomen in chemische symbolentaal 1 Atoomsoorten of chemische elementen De verschillende soorten atomen worden elementen genoemd. Momenteel zijn er 116 chemische elementen
Voorstelling van moleculen en atomen in chemische symbolentaal 1 Atoomsoorten of chemische elementen De verschillende soorten atomen worden elementen genoemd. Momenteel zijn er 116 chemische elementen
Samenvatting Scheikunde H3 Reacties
 Samenvatting Scheikunde H3 Reacties Samenvatting door L. 710 woorden 7 december 2016 6,8 24 keer beoordeeld Vak Methode Scheikunde Chemie overal Scheikunde Hoofdstuk 3: Reacties 3.2 Kenmerken van een chemische
Samenvatting Scheikunde H3 Reacties Samenvatting door L. 710 woorden 7 december 2016 6,8 24 keer beoordeeld Vak Methode Scheikunde Chemie overal Scheikunde Hoofdstuk 3: Reacties 3.2 Kenmerken van een chemische
Atoommodel van Rutherford
 Samenvatting scheikunde havo 4 hoofdstuk 2 bouwstenen van stoffen 2.2 de bouw van een atoom Atoommodel val Een atoom is een massief bolletje. Elk atoomsoort heeft zijn eigen Dalton afmetingen Ook gaf hij
Samenvatting scheikunde havo 4 hoofdstuk 2 bouwstenen van stoffen 2.2 de bouw van een atoom Atoommodel val Een atoom is een massief bolletje. Elk atoomsoort heeft zijn eigen Dalton afmetingen Ook gaf hij
Tabellen. Thermodynamica voor ingenieurs, Tabellen 1
 abellen abel 1. De elementen (molaire massa s) abel 2. Soortelijke warmte c p (bij lage drukken 0 1 ) in.k abel 3. Soortelijke warmte c p an lucht abel 4. Van der Waals coëfficiënten* abel 5. Gemiddelde
abellen abel 1. De elementen (molaire massa s) abel 2. Soortelijke warmte c p (bij lage drukken 0 1 ) in.k abel 3. Soortelijke warmte c p an lucht abel 4. Van der Waals coëfficiënten* abel 5. Gemiddelde
Aantekening Scheikunde Chemie Overal
 Aantekening Scheikunde Chemie Overal Aantekening door Jenayra 772 woorden 11 februari 2018 5,5 1 keer beoordeeld Vak Methode Scheikunde Chemie overal Hoofdstuk 3 Scheikunde Paragraaf 3.1 Fossiele brandstoffen:
Aantekening Scheikunde Chemie Overal Aantekening door Jenayra 772 woorden 11 februari 2018 5,5 1 keer beoordeeld Vak Methode Scheikunde Chemie overal Hoofdstuk 3 Scheikunde Paragraaf 3.1 Fossiele brandstoffen:
THEORIE UIT EXPERIMENTEN TABELLEN SCIENCE / NATUURKUNDE / SCHEIKUNDE
 THEORIE UIT EXPERIMENTEN ONDERBOUW TABELLEN SCIENCE / NATUURKUNDE / SCHEIKUNDE TABEL 1 DICHTHEID (bij 25 C) gram per cm 3 = g cm -3 aardgas 0,00076 alcohol 0,8 aluminium 2,7 broom 3,1 butagas 0,0024 eikenhout
THEORIE UIT EXPERIMENTEN ONDERBOUW TABELLEN SCIENCE / NATUURKUNDE / SCHEIKUNDE TABEL 1 DICHTHEID (bij 25 C) gram per cm 3 = g cm -3 aardgas 0,00076 alcohol 0,8 aluminium 2,7 broom 3,1 butagas 0,0024 eikenhout
Het smelten van tin is géén reactie.
 3 Reacties Reacties herkennen (3.1 en 3.2 ) Een chemische reactie is een gebeurtenis waarbij stoffen verdwijnen en nieuwe stoffen ontstaan. Bij een reactie verdwijnen de beginstoffen. Er ontstaan nieuwe
3 Reacties Reacties herkennen (3.1 en 3.2 ) Een chemische reactie is een gebeurtenis waarbij stoffen verdwijnen en nieuwe stoffen ontstaan. Bij een reactie verdwijnen de beginstoffen. Er ontstaan nieuwe
Niet-metalen + metalen. Uit welk soort atomen is een ionbinding opgebouwd? Geef de chemische formule van gedemineraliseerd water.
 Uit welk soort atomen is een ionbinding opgebouwd? Niet-metalen + metalen. Geef de chemische formule van gedemineraliseerd water. H2O. Wat is de structuur van een metaalbinding? Metaalrooster. Geef een
Uit welk soort atomen is een ionbinding opgebouwd? Niet-metalen + metalen. Geef de chemische formule van gedemineraliseerd water. H2O. Wat is de structuur van een metaalbinding? Metaalrooster. Geef een
ZUIVERE STOF één stof, gekenmerkt door welbepaalde fysische constanten zoals kooktemperatuur, massadichtheid,.
 PARATE KENNIS CHEMIE 4 e JAAR SCHEMA ZUIVERE STOF één stof, gekenmerkt door welbepaalde fysische constanten zoals kooktemperatuur, massadichtheid,. MENGSEL bestaat uit meerdere zuivere stoffen, de kooktemperatuur,
PARATE KENNIS CHEMIE 4 e JAAR SCHEMA ZUIVERE STOF één stof, gekenmerkt door welbepaalde fysische constanten zoals kooktemperatuur, massadichtheid,. MENGSEL bestaat uit meerdere zuivere stoffen, de kooktemperatuur,
Deel 2. Basiskennis chemie
 Deel 2. Basiskennis chemie Achteraan vind je een periodiek systeem van de elementen. Gebruik dit waar nodig. Vraag 21 Koolstofmonoxide (C) kan gesynthetiseerd worden door stoom met methaan (CH4 ) te laten
Deel 2. Basiskennis chemie Achteraan vind je een periodiek systeem van de elementen. Gebruik dit waar nodig. Vraag 21 Koolstofmonoxide (C) kan gesynthetiseerd worden door stoom met methaan (CH4 ) te laten
1) Stoffen, moleculen en atomen
 Herhaling leerstof klas 3 1) Stoffen, moleculen en atomen Scheikundigen houden zich bezig met stoffen. Betekenissen van stof zijn onder andere: - Het materiaal waar kleding van gemaakt is; - Fijne vuildeeltjes;
Herhaling leerstof klas 3 1) Stoffen, moleculen en atomen Scheikundigen houden zich bezig met stoffen. Betekenissen van stof zijn onder andere: - Het materiaal waar kleding van gemaakt is; - Fijne vuildeeltjes;
Samenvatting Scheikunde Hoofdstuk 3
 Samenvatting Scheikunde Hoofdstuk 3 Samenvatting door K. 1467 woorden 5 maart 2016 5,5 2 keer beoordeeld Vak Scheikunde Scheikunde Samenvatting H3 3V 3.1 Energie Fossiele brandstoffen -> nu nog er afhankelijk
Samenvatting Scheikunde Hoofdstuk 3 Samenvatting door K. 1467 woorden 5 maart 2016 5,5 2 keer beoordeeld Vak Scheikunde Scheikunde Samenvatting H3 3V 3.1 Energie Fossiele brandstoffen -> nu nog er afhankelijk
Wednesday, 28September, :13:59 PM Netherlands Time. Chemie Overal. Sk Havo deel 1
 Chemie Overal Sk Havo deel 1 Website van de methode www.h1.chemieoveral.epn.nl Probeer thuis of het werkt. Aanbevolen browser: internet explorer Neem onderstaande tabel over en rond af Atoomsoort Zuurstof
Chemie Overal Sk Havo deel 1 Website van de methode www.h1.chemieoveral.epn.nl Probeer thuis of het werkt. Aanbevolen browser: internet explorer Neem onderstaande tabel over en rond af Atoomsoort Zuurstof
Scheikunde Samenvatting H4+H5
 Scheikunde Samenvatting H4+H5 Hoofdstuk 4 4.2 Stoffen worden ingedeeld op grond van hun eigenschappen. Er zijn niet-ontleedbare stoffen en ontleedbare stoffen. De niet-ontleedbare stoffen zijn verdeeld
Scheikunde Samenvatting H4+H5 Hoofdstuk 4 4.2 Stoffen worden ingedeeld op grond van hun eigenschappen. Er zijn niet-ontleedbare stoffen en ontleedbare stoffen. De niet-ontleedbare stoffen zijn verdeeld
Klas 4 GT. Atomen en ionen 3(4) VMBO-TG
 Klas 4 GT Atomen en ionen 3(4) VMBO-TG De kracht van het atoom Een atoom bevat enorme krachten proefwerkstof Proefwerk 14-10-05 Nask2 3(4) VMBO TG deel B hoofdstuk3 Hoofdstuk 4 atomen en ionen blz2 tot
Klas 4 GT Atomen en ionen 3(4) VMBO-TG De kracht van het atoom Een atoom bevat enorme krachten proefwerkstof Proefwerk 14-10-05 Nask2 3(4) VMBO TG deel B hoofdstuk3 Hoofdstuk 4 atomen en ionen blz2 tot
TWEELINGKRISTALLEN. Inleiding. Tweelingen van aragoniet. door drs. E.A.J. Burke Instituut voor Aardwetenschappen Vrije Universiteit, Amsterdam
 TWEELINGKRISTALLEN door drs. E.A.J. Burke Instituut voor Aardwetenschappen Vrije Universiteit, Amsterdam Inleiding Als mineralen onbelemmerd kunnen groeien vormen zij kristallen met hun eigen karakteristieke
TWEELINGKRISTALLEN door drs. E.A.J. Burke Instituut voor Aardwetenschappen Vrije Universiteit, Amsterdam Inleiding Als mineralen onbelemmerd kunnen groeien vormen zij kristallen met hun eigen karakteristieke
INTRODUCTIECURSUS BOUWCHEMIE HOOFDSTUK 1: INLEIDING MOLECULEN EN ATOMEN
 INTRODUCTIECURSUS BOUWCHEMIE HOOFDSTUK 1: INLEIDING MOLECULEN EN ATOMEN 1 OVERZICHT 1. Zuivere stof, moleculen en atomen 1. Moleculeformules 2. Elementen 3. Atoomtheorie 4. Atoommassa 5. Moleculemassa
INTRODUCTIECURSUS BOUWCHEMIE HOOFDSTUK 1: INLEIDING MOLECULEN EN ATOMEN 1 OVERZICHT 1. Zuivere stof, moleculen en atomen 1. Moleculeformules 2. Elementen 3. Atoomtheorie 4. Atoommassa 5. Moleculemassa
1 Voedingselementen Voedingselementen Zuurgraad Elektrische geleidbaarheid (EC) Afsluiting 14
 Inhoud Voorwoord 5 Inleiding 6 1 Voedingselementen 9 1.1 Voedingselementen 9 1.2 Zuurgraad 12 1.3 Elektrische geleidbaarheid (EC) 13 1.4 Afsluiting 14 2 Kunstmeststoffen 15 2.1 Indeling kunstmeststoffen
Inhoud Voorwoord 5 Inleiding 6 1 Voedingselementen 9 1.1 Voedingselementen 9 1.2 Zuurgraad 12 1.3 Elektrische geleidbaarheid (EC) 13 1.4 Afsluiting 14 2 Kunstmeststoffen 15 2.1 Indeling kunstmeststoffen
Algemene en Technische Scheikunde
 Algemene en Technische Scheikunde Naam en voornaam: Examennummer: Reeks: Theorie: Oefeningen: Totaal: 1A 2A 3B 4B 5B 6B 7B 8B 1B 2B 3A 4A 5A 6A 7A 8A 1 1 H 1.008 2 He 4.003 2 3 Li 6.941 4 Be 9.012 5 B
Algemene en Technische Scheikunde Naam en voornaam: Examennummer: Reeks: Theorie: Oefeningen: Totaal: 1A 2A 3B 4B 5B 6B 7B 8B 1B 2B 3A 4A 5A 6A 7A 8A 1 1 H 1.008 2 He 4.003 2 3 Li 6.941 4 Be 9.012 5 B
Solepura is gelegen in de Noord centrale provincie van Sri Lanka, ruim 3 uur rijden vanaf vliegveld Colombo naar het Noorden.
 Waterzuivering regio Solepura, Sri Lanka Solepura is gelegen in de Noord centrale provincie van Sri Lanka, ruim 3 uur rijden vanaf vliegveld Colombo naar het Noorden. In mei 2012 ging Father Ajith Rohan
Waterzuivering regio Solepura, Sri Lanka Solepura is gelegen in de Noord centrale provincie van Sri Lanka, ruim 3 uur rijden vanaf vliegveld Colombo naar het Noorden. In mei 2012 ging Father Ajith Rohan
07 MOLECUULFORMULES & CHEMISCHE BINDINGEN PROCESTECHNIEK
 PROCESTECHNIEK Wat leer je? het verschil uitleggen tussen symbolenformules en molecuulformules; molecuulformules opstellen aan de hand van tekeningen van moleculen; het aantal en de soort atomen van een
PROCESTECHNIEK Wat leer je? het verschil uitleggen tussen symbolenformules en molecuulformules; molecuulformules opstellen aan de hand van tekeningen van moleculen; het aantal en de soort atomen van een
Samenvatting Scheikunde Hoofdstuk 2 stoffen en reacties
 Samenvatting Scheikunde Hoofdstuk 2 stoffen en reacties Samenvatting door F. 1622 woorden 22 mei 2015 6,1 40 keer beoordeeld Vak Methode Scheikunde Nova Paragraaf 1 Gloeien, smelten en verdampen Als je
Samenvatting Scheikunde Hoofdstuk 2 stoffen en reacties Samenvatting door F. 1622 woorden 22 mei 2015 6,1 40 keer beoordeeld Vak Methode Scheikunde Nova Paragraaf 1 Gloeien, smelten en verdampen Als je
Samenvatting Scheikunde H3 Door: Immanuel Bendahan
 Samenvatting Scheikunde H3 Door: Immanuel Bendahan Inhoudsopgave 1 Atoommodel... 1 Moleculen... 1 De ontwikkeling van het atoommodel... 1 Atoommodel van Bohr... 2 Indicatoren van atomen... 3 2 Periodiek
Samenvatting Scheikunde H3 Door: Immanuel Bendahan Inhoudsopgave 1 Atoommodel... 1 Moleculen... 1 De ontwikkeling van het atoommodel... 1 Atoommodel van Bohr... 2 Indicatoren van atomen... 3 2 Periodiek
Hoofdstuk 4. Chemische reacties. J.A.W. Faes (2019)
 Hoofdstuk 4 Chemische reacties J.A.W. Faes (2019) Hoofdstuk 4 Chemische reacties Paragrafen 4.1 Kenmerken van een reactie 4.2 Reactievergelijkingen 4.3 Rekenen aan reacties Practica Exp. 1 Waarnemen Exp.
Hoofdstuk 4 Chemische reacties J.A.W. Faes (2019) Hoofdstuk 4 Chemische reacties Paragrafen 4.1 Kenmerken van een reactie 4.2 Reactievergelijkingen 4.3 Rekenen aan reacties Practica Exp. 1 Waarnemen Exp.
namen formules ionogene stoffen van Als je de negatieve ionen (behalve OH - ) koppelt aan H + - ionen ontstaan verbindingen die men zuren noemt.
 namen en formules van ionogene stoffen CH 3 COO - acetaat afkomstig van azijnzuur (ethaanzuur) C 2 O 4 samengestelde ionen HC 2 O 4 - oxalaat beide afkomstig van oxaalzuur (ethaandizuur) waterstofoxalaat
namen en formules van ionogene stoffen CH 3 COO - acetaat afkomstig van azijnzuur (ethaanzuur) C 2 O 4 samengestelde ionen HC 2 O 4 - oxalaat beide afkomstig van oxaalzuur (ethaandizuur) waterstofoxalaat
14 DE ATOOMTHEORIE VAN DALTON PROCESTECHNIEK
 PROCESTECHNIEK Wat leer je? uitleggen wat een reactieschema is; reactieschema's in woorden en symbolen opstellen; de kenmerken van de atoomtheorie van Dalton noemen; moleculen en atomen tekenen; scheikundige
PROCESTECHNIEK Wat leer je? uitleggen wat een reactieschema is; reactieschema's in woorden en symbolen opstellen; de kenmerken van de atoomtheorie van Dalton noemen; moleculen en atomen tekenen; scheikundige
Stoffen en Reacties 2
 Stoffen en Reacties 2 Practicum Metalen Naam student 1. Naam student2..... Pagina 2 van 13 Inleiding Reageert metaal met zuurstof? Sinds de mensheid metalen kent worden ze voor allerlei toepassingen gebruikt
Stoffen en Reacties 2 Practicum Metalen Naam student 1. Naam student2..... Pagina 2 van 13 Inleiding Reageert metaal met zuurstof? Sinds de mensheid metalen kent worden ze voor allerlei toepassingen gebruikt
Oefenvragen Hoofdstuk 3 Bouwstenen van stoffen antwoorden
 Vraag 1 Geef het symbool van: Oefenvragen Hoofdstuk 3 Bouwstenen van stoffen antwoorden I. IJzer Fe Aluminium Al Koolstof C IV. Lood Pb V. Chloor Cl VI. Silicium Si Vraag 2 Geef de naam van de atoomsoort.
Vraag 1 Geef het symbool van: Oefenvragen Hoofdstuk 3 Bouwstenen van stoffen antwoorden I. IJzer Fe Aluminium Al Koolstof C IV. Lood Pb V. Chloor Cl VI. Silicium Si Vraag 2 Geef de naam van de atoomsoort.
Stoffen, structuur en bindingen
 Hoofdstuk 1: Stoffen, structuur en bindingen Scheikunde vwo 2011/2012 www.lyceo.nl Onderwerpen Scheikunde 2011 2012 Stoffen, structuur en binding Kenmerken van Reacties Zuren en base Redox Chemische technieken
Hoofdstuk 1: Stoffen, structuur en bindingen Scheikunde vwo 2011/2012 www.lyceo.nl Onderwerpen Scheikunde 2011 2012 Stoffen, structuur en binding Kenmerken van Reacties Zuren en base Redox Chemische technieken
Helium atoom = kern met 2 protonen en 2 neutronen met eromheen draaiend 2 elektronen
 Cursus Chemie 1-1 Hoofdstuk 1 : De atoombouw en het Periodiek Systeem 1. SAMENSTELLING VAN HET ATOOM Een atoom bestaat uit: een positief geladen kern, opgebouwd uit protonen en neutronen en (een of meer)
Cursus Chemie 1-1 Hoofdstuk 1 : De atoombouw en het Periodiek Systeem 1. SAMENSTELLING VAN HET ATOOM Een atoom bestaat uit: een positief geladen kern, opgebouwd uit protonen en neutronen en (een of meer)
Opgave 1. n = m / M. e 500 mg soda (Na 2CO 3) = 0,00472 mol. Opgave 2. m = n x M
 Hoofdstuk 8 Rekenen met de mol bladzijde 1 Opgave 1 n = m / M a 64,0 g zuurstofgas (O 2) = 2,00 mol (want n = 64,0 / 32,0) enz b 10,0 g butaan (C 4H 10) = 0,172 mol c 1,00 g suiker (C 12H 22O 11) = 0,00292
Hoofdstuk 8 Rekenen met de mol bladzijde 1 Opgave 1 n = m / M a 64,0 g zuurstofgas (O 2) = 2,00 mol (want n = 64,0 / 32,0) enz b 10,0 g butaan (C 4H 10) = 0,172 mol c 1,00 g suiker (C 12H 22O 11) = 0,00292
Antwoorden deel 1. Scheikunde Chemie overal
 Antwoorden deel 1 Scheikunde Chemie overal Huiswerk 2. a. Zuivere berglucht is scheikundig gezien geen zuivere stof omdat er in lucht verschillende moleculen zitten (zuurstof, stikstof enz.) b. Niet vervuild
Antwoorden deel 1 Scheikunde Chemie overal Huiswerk 2. a. Zuivere berglucht is scheikundig gezien geen zuivere stof omdat er in lucht verschillende moleculen zitten (zuurstof, stikstof enz.) b. Niet vervuild
Samenvatting Scheikunde Hoofdstuk 1
 Samenvatting Scheikunde Hoofdstuk 1 Samenvatting door Sarah 1515 woorden 3 april 2017 6 12 keer beoordeeld Vak Methode Scheikunde Chemie overal Scheikunde PW Hoofdstuk 1 1.1 Zwart goud aardolie is ontstaan
Samenvatting Scheikunde Hoofdstuk 1 Samenvatting door Sarah 1515 woorden 3 april 2017 6 12 keer beoordeeld Vak Methode Scheikunde Chemie overal Scheikunde PW Hoofdstuk 1 1.1 Zwart goud aardolie is ontstaan
Scheikunde Chemie overal Week 1. Kelly van Helden
 Scheikunde Chemie overal Week 1 Kelly van Helden 1.1 Chemie om je heen Scheikunde is overal Scheiden of zuiveren van stoffen Veranderen van grondstoffen in bruikbare stoffen Drinkwater uit zeewater Poetsen
Scheikunde Chemie overal Week 1 Kelly van Helden 1.1 Chemie om je heen Scheikunde is overal Scheiden of zuiveren van stoffen Veranderen van grondstoffen in bruikbare stoffen Drinkwater uit zeewater Poetsen
Hoofdstuk 3-5. Reacties. Klas
 Hoofdstuk 3-5 Reacties Klas 3 MOLECUULFORMULES OPDRACHT 1: MOLECUULFORMULES LEVEL 1 A H 2O C 2H 6 C C 2H 6O D CO 2 E F C 4H 8O CHN OPDRACHT 2: MOLECUULFORMULES LEVEL 1 A HNO C 3H 6O C C 2H 2 D C 6H 5NO
Hoofdstuk 3-5 Reacties Klas 3 MOLECUULFORMULES OPDRACHT 1: MOLECUULFORMULES LEVEL 1 A H 2O C 2H 6 C C 2H 6O D CO 2 E F C 4H 8O CHN OPDRACHT 2: MOLECUULFORMULES LEVEL 1 A HNO C 3H 6O C C 2H 2 D C 6H 5NO
Elektriciteit. Elektriciteit
 Elektriciteit Alles wat we kunnen zien en alles wat we niet kunnen zien bestaat uit kleine deeltjes. Zo is een blok staal gemaakt van staaldeeltjes, bestaat water uit waterdeeltjes en hout uit houtdeeltjes.
Elektriciteit Alles wat we kunnen zien en alles wat we niet kunnen zien bestaat uit kleine deeltjes. Zo is een blok staal gemaakt van staaldeeltjes, bestaat water uit waterdeeltjes en hout uit houtdeeltjes.
1 Gewassen en hun afwijkingen Kennismaking met de plant Afwijkingen in de teelt Afsluiting 24
 Inhoud Voorwoord 5 Inleiding 6 1 Gewassen en hun afwijkingen 9 1.1 Kennismaking met de plant 10 1.2 Afwijkingen in de teelt 17 1.3 Afsluiting 24 2 Afwijkingen voorkomen en bestrijdingsmethoden 25 2.1 Niet-parasitaire
Inhoud Voorwoord 5 Inleiding 6 1 Gewassen en hun afwijkingen 9 1.1 Kennismaking met de plant 10 1.2 Afwijkingen in de teelt 17 1.3 Afsluiting 24 2 Afwijkingen voorkomen en bestrijdingsmethoden 25 2.1 Niet-parasitaire
Samenvatting Scheikunde Hoofdstuk 1 en 2
 Samenvatting Scheikunde Hoofdstuk 1 en 2 Samenvatting door een scholier 918 woorden 13 januari 2005 6,3 193 keer beoordeeld Vak Methode Scheikunde Chemie overal Hoofdstuk 1 1.2: De bouw van een atoom.
Samenvatting Scheikunde Hoofdstuk 1 en 2 Samenvatting door een scholier 918 woorden 13 januari 2005 6,3 193 keer beoordeeld Vak Methode Scheikunde Chemie overal Hoofdstuk 1 1.2: De bouw van een atoom.
SCHEIKUNDE KLAS 3 REACTIES SKILL TREE
 SKILL TREE MOLECUULFORMULES OPDRACHT 1: MOLECUULFORMULES LEVEL 1 A H 2 O C 2 H 6 C C 2 H 6 O D CO 2 E F C 4 H 8 O CHN OPDRACHT 2: MOLECUULFORMULES LEVEL 1 A HNO C 3 H 6 O C C 2 H 2 D C 6 H 5 NO E C 5 H
SKILL TREE MOLECUULFORMULES OPDRACHT 1: MOLECUULFORMULES LEVEL 1 A H 2 O C 2 H 6 C C 2 H 6 O D CO 2 E F C 4 H 8 O CHN OPDRACHT 2: MOLECUULFORMULES LEVEL 1 A HNO C 3 H 6 O C C 2 H 2 D C 6 H 5 NO E C 5 H
Alles om je heen is opgebouwd uit atomen. En elk atoom is weer bestaat uit protonen, elektronen en neutronen.
 2 ELEKTRICITEITSLEER 2.1. Inleiding Je hebt al geleerd dat elektriciteit kan worden opgewekt door allerlei energievormen om te zetten in elektrische energie. Maar hoe kan elektriciteit ontstaan? En waarom
2 ELEKTRICITEITSLEER 2.1. Inleiding Je hebt al geleerd dat elektriciteit kan worden opgewekt door allerlei energievormen om te zetten in elektrische energie. Maar hoe kan elektriciteit ontstaan? En waarom
http://www.kuurwater.nl/gebruik.html
 http://www.kuurwater.nl/gebruik.html Overgewicht, vermoeidheid, veel zitten, stress, dat zijn problemen die vaak te maken hebben met het leven van vandaag. De hydroxydase kuur kan u helpen deze problemen
http://www.kuurwater.nl/gebruik.html Overgewicht, vermoeidheid, veel zitten, stress, dat zijn problemen die vaak te maken hebben met het leven van vandaag. De hydroxydase kuur kan u helpen deze problemen
Cursus Chemie 5-1. Hoofdstuk 5: KWANTITATIEVE ASPECTEN VAN CHEMISCHE REACTIES 1. BELANGRIJKE BEGRIPPEN. 1.1. Relatieve Atoommassa (A r)
 Cursus Chemie 5-1 Hoofdstuk 5: KWANTITATIEVE ASPECTEN VAN CHEMISCHE REACTIES 1. BELANGRIJKE BEGRIPPEN 1.1. Relatieve Atoommassa (A r) A r = een onbenoemd getal dat de verhouding weergeeft van de atoommassa
Cursus Chemie 5-1 Hoofdstuk 5: KWANTITATIEVE ASPECTEN VAN CHEMISCHE REACTIES 1. BELANGRIJKE BEGRIPPEN 1.1. Relatieve Atoommassa (A r) A r = een onbenoemd getal dat de verhouding weergeeft van de atoommassa
In het dagelijks leven - Mooi om te weten
 In het dagelijks leven - Mooi om te weten Zoek het eens op. Je kan hiertoe gebruiken: www.periodictableonline.org of CD-rom Een elementaire wereld (EOS- mei 2002). 1 Rangschikking volgens % voorkomen in
In het dagelijks leven - Mooi om te weten Zoek het eens op. Je kan hiertoe gebruiken: www.periodictableonline.org of CD-rom Een elementaire wereld (EOS- mei 2002). 1 Rangschikking volgens % voorkomen in
Samenvatting Scheikunde Hoofdstuk 1, 2.4, 4, 5.1 t/m 5.3
 Samenvatting Scheikunde Hoofdstuk 1, 2.4, 4, 5.1 t/m 5.3 Samenvatting door een scholier 1619 woorden 9 oktober 2005 7,2 12 keer beoordeeld Vak Methode Scheikunde Pulsar chemie Scheikunde, hoofstuk 1, 2.4,
Samenvatting Scheikunde Hoofdstuk 1, 2.4, 4, 5.1 t/m 5.3 Samenvatting door een scholier 1619 woorden 9 oktober 2005 7,2 12 keer beoordeeld Vak Methode Scheikunde Pulsar chemie Scheikunde, hoofstuk 1, 2.4,
CHEMIELEERKRACHT VAN HET JAAR. Onderwerp: het periodiek systeem. Liesbeth Van Goethem
 CHEMIELEERKRACHT VAN HET JAAR Onderwerp: het periodiek systeem Liesbeth Van Goethem liesbeth.vangoethem@gmail.com Inhoud 1. Algemene gegevens... 2 2. Leerplandoelstellingen... 3 3. Beginsituatie... 3 4.
CHEMIELEERKRACHT VAN HET JAAR Onderwerp: het periodiek systeem Liesbeth Van Goethem liesbeth.vangoethem@gmail.com Inhoud 1. Algemene gegevens... 2 2. Leerplandoelstellingen... 3 3. Beginsituatie... 3 4.
Elektronenoverdracht (1)
 Redoxreacties 1 Elektronenoverdracht (1) Een bekende reactie is: 2 Na(s) + Cl 2 (g) 2 NaCl(s) (oude notatie: Na + Cl - ) Hierbij is sprake van elektronenoverdracht. Dit kan als volgt worden voorgesteld:
Redoxreacties 1 Elektronenoverdracht (1) Een bekende reactie is: 2 Na(s) + Cl 2 (g) 2 NaCl(s) (oude notatie: Na + Cl - ) Hierbij is sprake van elektronenoverdracht. Dit kan als volgt worden voorgesteld:
Elementen; atomen en moleculen
 Elementen; atomen en moleculen In de natuur komen veel stoffen voor die we niet meer kunnen splitsen in andere stoffen. Ze zijn dus te beschouwen als de grondstoffen. Deze stoffen worden elementen genoemd.
Elementen; atomen en moleculen In de natuur komen veel stoffen voor die we niet meer kunnen splitsen in andere stoffen. Ze zijn dus te beschouwen als de grondstoffen. Deze stoffen worden elementen genoemd.
Vraag 1 : Beschrijf het verschil tussen een atoom en een molecule.
 1) sim15 http://www.teachchemistry.org/bonding Vraag 1 : Beschrijf het verschil tussen een atoom en een molecule. Vraag 2 : Duid aan in het PSE: Metalen : groen Niet-metalen : rood Vraag 3 : Welke elementaire
1) sim15 http://www.teachchemistry.org/bonding Vraag 1 : Beschrijf het verschil tussen een atoom en een molecule. Vraag 2 : Duid aan in het PSE: Metalen : groen Niet-metalen : rood Vraag 3 : Welke elementaire
Laslegeringen voor kwalitatieve onderhoudswerke
 , Laslegeringen voor kwalitatieve onderhoudswerke Reparaturschweißlegierungen GmbH Am Kavitt 4 D-47877 Willich Postfach 237 D-47863 Willich (+49) 2154 95 55-0 FAX (+49) 2154 95 55-55 e-mail: info @ omniweld.de
, Laslegeringen voor kwalitatieve onderhoudswerke Reparaturschweißlegierungen GmbH Am Kavitt 4 D-47877 Willich Postfach 237 D-47863 Willich (+49) 2154 95 55-0 FAX (+49) 2154 95 55-55 e-mail: info @ omniweld.de
Antwoorden deel 1. Scheikunde Chemie overal
 Antwoorden deel 1 Scheikunde Chemie overal Huiswerk 2. a. Zuivere berglucht is scheikundig gezien geen zuivere stof omdat er in lucht verschillende moleculen zitten (zuurstof, stikstof enz.) b. Niet vervuild
Antwoorden deel 1 Scheikunde Chemie overal Huiswerk 2. a. Zuivere berglucht is scheikundig gezien geen zuivere stof omdat er in lucht verschillende moleculen zitten (zuurstof, stikstof enz.) b. Niet vervuild
SCHEIKUNDE VWO 4 MOLBEREKENINGEN ANTW.
 OPGAVE 1 LEVEL 1 Uit de opgave haal je dat koper en zuurstof links van de pijl moeten staan en koper(ii)oxide rechts van de pijl. Daarna maak je de reactievergelijking kloppend. 2 Cu + O 2 à 2 CuO Filmpje
OPGAVE 1 LEVEL 1 Uit de opgave haal je dat koper en zuurstof links van de pijl moeten staan en koper(ii)oxide rechts van de pijl. Daarna maak je de reactievergelijking kloppend. 2 Cu + O 2 à 2 CuO Filmpje
THEORIE UIT EXPERIMENTEN TABELLEN (macro) 12(micro) SCHEIKUNDE HAVO/VWO
 THEORIE UIT EXPERIMENTEN TABELLEN 1 2 3 4 5 6 7 8 9 10 11 12(macro) 12(micro) SCHEIKUNDE HAVO/VWO TABEL 1 DICHTHEID (bij 25 C) gram per cm 3 = g cm -3 aardgas 0,00076 alcohol 0,8 aluminium 2,7 broom 3,1
THEORIE UIT EXPERIMENTEN TABELLEN 1 2 3 4 5 6 7 8 9 10 11 12(macro) 12(micro) SCHEIKUNDE HAVO/VWO TABEL 1 DICHTHEID (bij 25 C) gram per cm 3 = g cm -3 aardgas 0,00076 alcohol 0,8 aluminium 2,7 broom 3,1
Toets HAVO 4 Chemie Hfdst. 2 Schatkamer aarde
 Toets HAVO 4 Chemie Hfdst. 2 Schatkamer aarde Opgave 1 Op het etiket van een pot pindakaas staat als een van de ingrediënten magnesium genoemd. Scheikundig is dit niet juist. Pindakaas bevat geen magnesium
Toets HAVO 4 Chemie Hfdst. 2 Schatkamer aarde Opgave 1 Op het etiket van een pot pindakaas staat als een van de ingrediënten magnesium genoemd. Scheikundig is dit niet juist. Pindakaas bevat geen magnesium
DE KRACHT VAN HET GEMINERALISEERDE WATER VAN VICHY VOOR EEN STERKERE HUID GEBOREN IN DE OMGEVING VAN DE FRANSE VULKANEN.
 DE KRACHT VAN HET GEMINERALISEERDE WATER VAN VICHY VOOR EEN STERKERE HUID GEBOREN IN DE OMGEVING VAN DE FRANSE VULKANEN. EEN BRON VAN KRACHT VOOR UW HUID VICHY GEBOREN IN DE OMGEVING VAN DE FRANSE VULKANEN.
DE KRACHT VAN HET GEMINERALISEERDE WATER VAN VICHY VOOR EEN STERKERE HUID GEBOREN IN DE OMGEVING VAN DE FRANSE VULKANEN. EEN BRON VAN KRACHT VOOR UW HUID VICHY GEBOREN IN DE OMGEVING VAN DE FRANSE VULKANEN.
Cover Page. The handle holds various files of this Leiden University dissertation.
 Cover Page The handle http://hdl.handle.net/1887/20310 holds various files of this Leiden University dissertation. Author: Jansen, Bas Title: Mersenne primes and class field theory Date: 2012-12-18 Samenvatting
Cover Page The handle http://hdl.handle.net/1887/20310 holds various files of this Leiden University dissertation. Author: Jansen, Bas Title: Mersenne primes and class field theory Date: 2012-12-18 Samenvatting
Curie Hoofdstuk 6 HAVO 4
 Rekenen aan reacties Curie Hoofdstuk 6 HAVO 4 6.1 Rekenen met de mol 6.2 Rekenen met massa s 6.3 Concentratie 6.4 SPA en Stappenplan 6.1 Rekenen met de mol Eenheden en grootheden 1d dozijn potloden 12
Rekenen aan reacties Curie Hoofdstuk 6 HAVO 4 6.1 Rekenen met de mol 6.2 Rekenen met massa s 6.3 Concentratie 6.4 SPA en Stappenplan 6.1 Rekenen met de mol Eenheden en grootheden 1d dozijn potloden 12
Samenvatting Scheikunde Hoofdstuk 1
 Samenvatting Scheikunde Hoofdstuk 1 Samenvatting door W. 1173 woorden 23 juni 2016 6,9 16 keer beoordeeld Vak Methode Scheikunde Nova Scheikunde Samenvatting H1 1 t/m 7 1 Atoombouw: Atoom: Opgebouwd uit
Samenvatting Scheikunde Hoofdstuk 1 Samenvatting door W. 1173 woorden 23 juni 2016 6,9 16 keer beoordeeld Vak Methode Scheikunde Nova Scheikunde Samenvatting H1 1 t/m 7 1 Atoombouw: Atoom: Opgebouwd uit
MS_0100_GWL_1. Stroomgebiedbeheerplan - informatie per grondwaterlichaam. Karakteristieken. Quartair Aquifersysteem Maassysteem Maas.
 Stroomgebiedbeheerplan - informatie per grondwaterlichaam naam grondwaterlichaam naam grondwatersysteem naam stroomgebied Quartair Aquifersysteem Maassysteem Maas Karakteristieken oppervlakte (km²) 876
Stroomgebiedbeheerplan - informatie per grondwaterlichaam naam grondwaterlichaam naam grondwatersysteem naam stroomgebied Quartair Aquifersysteem Maassysteem Maas Karakteristieken oppervlakte (km²) 876
Fosfor kan met waterstof reageren. d Geef de vergelijking van de reactie van fosfor met waterstof.
 1 Een oplossing van zwavelzuur en een oplossing van bariumhydroxide geladen beide elektriciteit. Wordt bij de zwavelzuuroplossing een oplossing van bariumhydroxide gedruppeld, dan neemt het elektrisch
1 Een oplossing van zwavelzuur en een oplossing van bariumhydroxide geladen beide elektriciteit. Wordt bij de zwavelzuuroplossing een oplossing van bariumhydroxide gedruppeld, dan neemt het elektrisch
CVS_0400_GWL_1. Stroomgebiedbeheerplan - informatie per grondwaterlichaam. Karakteristieken
 Stroomgebiedbeheerplan - informatie per grondwaterlichaam naam grondwaterlichaam naam grondwatersysteem naam stroomgebied Oligoceen Aquifersysteem (gespannen) Centraal Vlaams Systeem Schelde Karakteristieken
Stroomgebiedbeheerplan - informatie per grondwaterlichaam naam grondwaterlichaam naam grondwatersysteem naam stroomgebied Oligoceen Aquifersysteem (gespannen) Centraal Vlaams Systeem Schelde Karakteristieken
Thema 4: Een gezonde bodem
 Thema 4: Een gezonde bodem Bodemanalyse en de gezonde plant Emile Bezemer Eurofins Agro Minder chemie met steenmeel Bert Carpay Carpay Advies 25 september 2018 ConGRAS 1 Bodemanalyse en gezonde grasplant!
Thema 4: Een gezonde bodem Bodemanalyse en de gezonde plant Emile Bezemer Eurofins Agro Minder chemie met steenmeel Bert Carpay Carpay Advies 25 september 2018 ConGRAS 1 Bodemanalyse en gezonde grasplant!
Oxidator = het deeltje dat elektronen onttrekt aan een ander deeltje Reductor = het deeltje dat elektronen afstaat aan een ander deeltje
 Cursus Chemie 6-1 Hoofdstuk 6: REDOX REACTIES 1. INLEIDING In vroegere tijden werd de term oxideren gebruikt om een reactie met zuurstof aan te geven. Bvb. de reactie waarbij koolstof verbrandt is C +
Cursus Chemie 6-1 Hoofdstuk 6: REDOX REACTIES 1. INLEIDING In vroegere tijden werd de term oxideren gebruikt om een reactie met zuurstof aan te geven. Bvb. de reactie waarbij koolstof verbrandt is C +
SECTIE : Anorganische chemie VALIDATIERAPPORT
 VALIDATIERAPPORT Analysemethode Techniek Drinkwater - Kwantitatieve bepaling van 21 elementen met ICP-MS (FLVVG-I-MET-196E : met E = element) en Drinkwater Kwantitatieve bepaling van kwik met ICP-MS (FLVVG-I-MET-196Hg)
VALIDATIERAPPORT Analysemethode Techniek Drinkwater - Kwantitatieve bepaling van 21 elementen met ICP-MS (FLVVG-I-MET-196E : met E = element) en Drinkwater Kwantitatieve bepaling van kwik met ICP-MS (FLVVG-I-MET-196Hg)
Samenvatting Scheikunde Scheikunde Chemie overal H1 3 vwo
 Samenvatting Scheikunde Scheikunde Chemie overal H1 3 vwo Samenvatting door een scholier 1193 woorden 30 oktober 2012 5,8 23 keer beoordeeld Vak Methode Scheikunde Chemie overal Samenvatting Scheikunde
Samenvatting Scheikunde Scheikunde Chemie overal H1 3 vwo Samenvatting door een scholier 1193 woorden 30 oktober 2012 5,8 23 keer beoordeeld Vak Methode Scheikunde Chemie overal Samenvatting Scheikunde
Hierbij is sprake van elektronenoverdracht; elk Na atoom draagt een elektron over aan Cl-atoom onder vorming van een ionrooster.
 Redoxreacties 1. Elektronenoverdracht In dit hoofdstuk maken we kennis met zogenaamde redoxreacties. Dit zijn reacties waarbij elektronenoverdracht plaatsvindt. De naam redoxreactie is een samentrekking
Redoxreacties 1. Elektronenoverdracht In dit hoofdstuk maken we kennis met zogenaamde redoxreacties. Dit zijn reacties waarbij elektronenoverdracht plaatsvindt. De naam redoxreactie is een samentrekking
Oefententamen CTO dell II (2009-2010)
 1 Oefententamen CTO dell II (009-010) Schrijf duidelijk je naam en studentnummer op Tentamenduur: 3 uur Totale punten: 40 1. De volgende vragen betreffen de perovskieten met de formule ABO 3. (18p) a)
1 Oefententamen CTO dell II (009-010) Schrijf duidelijk je naam en studentnummer op Tentamenduur: 3 uur Totale punten: 40 1. De volgende vragen betreffen de perovskieten met de formule ABO 3. (18p) a)
fax 09/ Laboratorium voor Toegepaste Geologie en Hydrogeologie UNIVERSITEITGENT. Geologisch Instituut Krijgslaan 281, S8 B-9000 Gent
 UNVERSTETGENT Labratrium vr Tegepaste Gelgie en Hydrgelgie ECONOMSCHE PRE-EVALUATE VAN MNERALJSATES N BOORKERNEN VAN HET MASSEF VAN BRABANT Tabellen en figuren Gelgisch nstituut Krijgslaan 281, S8 B-9
UNVERSTETGENT Labratrium vr Tegepaste Gelgie en Hydrgelgie ECONOMSCHE PRE-EVALUATE VAN MNERALJSATES N BOORKERNEN VAN HET MASSEF VAN BRABANT Tabellen en figuren Gelgisch nstituut Krijgslaan 281, S8 B-9
Hoofdstuk 17 Redoxreacties
 Hoofdstuk 17 Redoxreacties bladzijde 1 Opgave 1 Bepaal de oxidatiegetallen van alle atomen in: Waterstof H: altijd +1 Zuurstof O: altijd 2 Som ladingen steeds 0 a H 2O H: +1 O: 2 2 x +1 + 2 = 0 b SO 2
Hoofdstuk 17 Redoxreacties bladzijde 1 Opgave 1 Bepaal de oxidatiegetallen van alle atomen in: Waterstof H: altijd +1 Zuurstof O: altijd 2 Som ladingen steeds 0 a H 2O H: +1 O: 2 2 x +1 + 2 = 0 b SO 2
Uitwerkingen van de opgaven uit: CHEMISCHE ANALYSE ISBN , 1 e druk, Uitgeverij Syntax Media Hoofdstuk 15 Elektrochemie bladzijde 1
 Hoofdstuk 15 Elektrochemie bladzijde 1 Opgave 1 Welke halfreactie kan men verwachten in de volgende gevallen? a Br ionen bij een positieve elektrode Br kan gemakkelijk elektronen afstaan, is dan reductor:
Hoofdstuk 15 Elektrochemie bladzijde 1 Opgave 1 Welke halfreactie kan men verwachten in de volgende gevallen? a Br ionen bij een positieve elektrode Br kan gemakkelijk elektronen afstaan, is dan reductor:
Atoombinding structuurformules nader beschouwd (aanvulling 2.4)
 Atoombinding structuurformules nader beschouwd (aanvulling 2.4) 1. Atoommodel van Bohr Uitgaande van het atoommodel van Rutherford (kern bestaande uit protonen en neutronen met daaromheen een elektronenwolk)
Atoombinding structuurformules nader beschouwd (aanvulling 2.4) 1. Atoommodel van Bohr Uitgaande van het atoommodel van Rutherford (kern bestaande uit protonen en neutronen met daaromheen een elektronenwolk)
Samenvatting Scheikunde Hoofdstuk 8
 Samenvatting Scheikunde Hoofdstuk 8 Samenvatting door Dylan 748 woorden 30 december 2016 5,8 4 keer beoordeeld Vak Methode Scheikunde Nova Scheikunde Paragraaf 1 Gemeenschappelijke eigenschappen metalen:
Samenvatting Scheikunde Hoofdstuk 8 Samenvatting door Dylan 748 woorden 30 december 2016 5,8 4 keer beoordeeld Vak Methode Scheikunde Nova Scheikunde Paragraaf 1 Gemeenschappelijke eigenschappen metalen:
KPS_0120_GWL_2. Stroomgebiedbeheerplan - informatie per grondwaterlichaam. Karakteristieken
 Stroomgebiedbeheerplan - informatie per grondwaterlichaam naam grondwaterlichaam naam grondwatersysteem naam stroomgebied Duin- en kreekgebieden Oostvlaamse polders Kust- en Poldersysteem Schelde Karakteristieken
Stroomgebiedbeheerplan - informatie per grondwaterlichaam naam grondwaterlichaam naam grondwatersysteem naam stroomgebied Duin- en kreekgebieden Oostvlaamse polders Kust- en Poldersysteem Schelde Karakteristieken
3.1 Energie. 3.2 Kenmerken chemische reactie
 3.1 Energie Wat is energie? Energie voorziening Fossiele brandstof verbranden Co2 komt vrij slecht voor het broeikaseffect Windmolen park Zonnepanelen Energie is iets wat nodig is voor een verbrandingsreactie
3.1 Energie Wat is energie? Energie voorziening Fossiele brandstof verbranden Co2 komt vrij slecht voor het broeikaseffect Windmolen park Zonnepanelen Energie is iets wat nodig is voor een verbrandingsreactie
 Bijlage A., behorende bij paragraaf 3.3 van de Regeling bodemkwaliteit Maximale samenstellings- en emissiewaarden bouwstoffen Tabel 1. Maximale emissiewaarden anorganische parameters Parameter Vormgegeven
Bijlage A., behorende bij paragraaf 3.3 van de Regeling bodemkwaliteit Maximale samenstellings- en emissiewaarden bouwstoffen Tabel 1. Maximale emissiewaarden anorganische parameters Parameter Vormgegeven
Redoxreacties; een aanvulling op hoofdstuk 13
 Redoxreacties; een aanvulling op hoofdstuk 13 1. Elektronenoverdracht In dit hoofdstuk maken we kennis met zogenaamde redoxreacties. Dit zijn reacties waarbij elektronenoverdracht plaatsvindt. De naam
Redoxreacties; een aanvulling op hoofdstuk 13 1. Elektronenoverdracht In dit hoofdstuk maken we kennis met zogenaamde redoxreacties. Dit zijn reacties waarbij elektronenoverdracht plaatsvindt. De naam
Standaardcondities FAAS
 Universiteit Utrecht Faculteit Bètawetenschappen Departement Scheikunde Scheikunde Practicum R.J. Baars, J.J. Hermans juli 29 Zilver Ag 328.683 nm (primaire lijn) lucht/acetyleen, 4 L/h, 7 mm -5 mg/l.2542
Universiteit Utrecht Faculteit Bètawetenschappen Departement Scheikunde Scheikunde Practicum R.J. Baars, J.J. Hermans juli 29 Zilver Ag 328.683 nm (primaire lijn) lucht/acetyleen, 4 L/h, 7 mm -5 mg/l.2542
Samenvatting Chemie Overal 3 havo
 Samenvatting Chemie Overal 3 havo Hoofdstuk 3: Reacties 3.1 Energie Energievoorziening Fossiele brandstoffen zijn nog steeds belangrijk voor onze energievoorziening. We zijn druk op zoek naar duurzame
Samenvatting Chemie Overal 3 havo Hoofdstuk 3: Reacties 3.1 Energie Energievoorziening Fossiele brandstoffen zijn nog steeds belangrijk voor onze energievoorziening. We zijn druk op zoek naar duurzame
Reacties en stroom 1
 Reacties en stroom 1 Elektronenoverdracht (1) Een bekende reactie is: 2 Na(s) + Cl 2 (g) 2 NaCl(s) (oude notatie: Na + Cl - ) Hierbij is sprake van elektronenoverdracht. Dit kan als volgt worden voorgesteld:
Reacties en stroom 1 Elektronenoverdracht (1) Een bekende reactie is: 2 Na(s) + Cl 2 (g) 2 NaCl(s) (oude notatie: Na + Cl - ) Hierbij is sprake van elektronenoverdracht. Dit kan als volgt worden voorgesteld:
1. Geef bij de volgende reactievergelijkingen steeds aan:
 Antwoorden Bijlage VI Oxidatiegetallen 1. Geef bij de volgende reactievergelijkingen steeds aan: welke stof wordt er geoxideerd +II +I II +I 0 +III +I +III II II +I +I II C 2 H 5 OH + O 2 CH 3 COOH + H
Antwoorden Bijlage VI Oxidatiegetallen 1. Geef bij de volgende reactievergelijkingen steeds aan: welke stof wordt er geoxideerd +II +I II +I 0 +III +I +III II II +I +I II C 2 H 5 OH + O 2 CH 3 COOH + H
1. Elementaire chemie en chemisch rekenen
 In onderstaande zelftest zijn de vragen gebundeld die als voorbeeldvragen zijn opgenomen in het bijhorend overzicht van de verwachte voorkennis chemie 1. Elementaire chemie en chemisch rekenen 1.1 Grootheden
In onderstaande zelftest zijn de vragen gebundeld die als voorbeeldvragen zijn opgenomen in het bijhorend overzicht van de verwachte voorkennis chemie 1. Elementaire chemie en chemisch rekenen 1.1 Grootheden
Chemie 4: Atoommodellen
 Chemie 4: Atoommodellen Van de oude Grieken tot het kwantummodel Het woord atoom komt va, het Griekse woord atomos dat ondeelbaar betekent. Voor de Griekse geleerde Democritos die leefde in het jaar 400
Chemie 4: Atoommodellen Van de oude Grieken tot het kwantummodel Het woord atoom komt va, het Griekse woord atomos dat ondeelbaar betekent. Voor de Griekse geleerde Democritos die leefde in het jaar 400
Tentamen Anorganische Chemie I
 Tentamen Anorganische Chemie I 29-3-2006 et tentamen bestaat uit vijf onderdelen (A,, C, D en E). De eerste tien vragen zijn meerkeuze vragen, het is hierbij voldoende om het nummer van de vraag en het
Tentamen Anorganische Chemie I 29-3-2006 et tentamen bestaat uit vijf onderdelen (A,, C, D en E). De eerste tien vragen zijn meerkeuze vragen, het is hierbij voldoende om het nummer van de vraag en het
SS_1300_GWL_4. Stroomgebiedbeheerplan - informatie per grondwaterlichaam. Karakteristieken
 Stroomgebiedbeheerplan - informatie per grondwaterlichaam naam grondwaterlichaam naam grondwatersysteem naam stroomgebied Sokkel+Krijt Aquifersysteem (gespannen deel) Sokkelsysteem Schelde Karakteristieken
Stroomgebiedbeheerplan - informatie per grondwaterlichaam naam grondwaterlichaam naam grondwatersysteem naam stroomgebied Sokkel+Krijt Aquifersysteem (gespannen deel) Sokkelsysteem Schelde Karakteristieken
Biogene Mineralen een nieuwe kijk op mineraalevolutie
 Biogene Mineralen een nieuwe kijk op mineraalevolutie Biogene mineralen in strikte zin: Gevormd (aan aardoppervlak) door: Biochemische processen. (in organismen of daardoor uitgescheiden) exoskelet - calciet,
Biogene Mineralen een nieuwe kijk op mineraalevolutie Biogene mineralen in strikte zin: Gevormd (aan aardoppervlak) door: Biochemische processen. (in organismen of daardoor uitgescheiden) exoskelet - calciet,
De metallische elementen in de mineralen
 De metallische elementen in de mineralen J. Tichelman. Mineralen zijn, behoudens de sporadisch vrij voorkomende elementen, samengesteld uit verbindingen van verschillende elementen. In de lijst van elementen
De metallische elementen in de mineralen J. Tichelman. Mineralen zijn, behoudens de sporadisch vrij voorkomende elementen, samengesteld uit verbindingen van verschillende elementen. In de lijst van elementen
Module 8 Chemisch Rekenen aan reacties
 1 Inleiding In deze module ga je leren hoe je allerlei rekenwerk kunt uitvoeren aan chemische reacties. Dat is van belang omdat in veel bedrijven wordt gerekend aan reacties onder andere om te bepalen
1 Inleiding In deze module ga je leren hoe je allerlei rekenwerk kunt uitvoeren aan chemische reacties. Dat is van belang omdat in veel bedrijven wordt gerekend aan reacties onder andere om te bepalen
KLASTOETS GRAAD 11. FISIESE WETENSKAPPE: CHEMIE Toets 4: Materie en materiale 1
 KLASTOETS GRAAD FISIESE WETENSKAPPE: CHEMIE Toets 4: Materie en materiale PUNTE: 45 TYD: uur INSTRUKSIES EN INLIGTING. Beantwoord AL die vrae. 2. Nieprogrammeerbare sakrekenaars mag gebruik word. 3. Toepaslike
KLASTOETS GRAAD FISIESE WETENSKAPPE: CHEMIE Toets 4: Materie en materiale PUNTE: 45 TYD: uur INSTRUKSIES EN INLIGTING. Beantwoord AL die vrae. 2. Nieprogrammeerbare sakrekenaars mag gebruik word. 3. Toepaslike
CVS_0160_GWL_1. Stroomgebiedbeheerplan - informatie per grondwaterlichaam. Karakteristieken
 Stroomgebiedbeheerplan - informatie per grondwaterlichaam naam grondwaterlichaam naam grondwatersysteem naam stroomgebied Pleistocene Afzettingen (freatisch) Centraal Vlaams Systeem Schelde Karakteristieken
Stroomgebiedbeheerplan - informatie per grondwaterlichaam naam grondwaterlichaam naam grondwatersysteem naam stroomgebied Pleistocene Afzettingen (freatisch) Centraal Vlaams Systeem Schelde Karakteristieken
Samenvatting Scheikunde Samenvatting hoofdstuk 2, Nova Scheikunde klas 3
 Samenvatting Scheikunde Samenvatting hoofdstuk 2, Nova Scheikunde klas 3 Samenvatting door een scholier 1298 woorden 14 januari 2019 0 keer beoordeeld Vak Methode Scheikunde Nova Paragraaf 1 Ontledingsreactie:
Samenvatting Scheikunde Samenvatting hoofdstuk 2, Nova Scheikunde klas 3 Samenvatting door een scholier 1298 woorden 14 januari 2019 0 keer beoordeeld Vak Methode Scheikunde Nova Paragraaf 1 Ontledingsreactie:
woensdag 14 december 2011 16:06:43 Midden-Europese standaardtijd
 INLEIDING Geef de reactievergelijking van de ontleding van aluminiumoxide. 2 Al 2 O 3 4 Al + 3 O 2 Massaverhouding tussen Al en O 2 1,00 : 0,889 Hoeveel ton Al 2 O 3 is er nodig om 1,50 ton O 2 te produceren?
INLEIDING Geef de reactievergelijking van de ontleding van aluminiumoxide. 2 Al 2 O 3 4 Al + 3 O 2 Massaverhouding tussen Al en O 2 1,00 : 0,889 Hoeveel ton Al 2 O 3 is er nodig om 1,50 ton O 2 te produceren?
Basisvaardigheden Microsoft Excel
 Basisvaardigheden Microsoft Excel Met behulp van deze handleiding kun je de basisvaardigheden leren die nodig zijn om meetresultaten van een practicum te verwerken. Je kunt dan het verband tussen twee
Basisvaardigheden Microsoft Excel Met behulp van deze handleiding kun je de basisvaardigheden leren die nodig zijn om meetresultaten van een practicum te verwerken. Je kunt dan het verband tussen twee
Samenvatting Scheikunde Hoofdstuk 1, 2, 3
 Samenvatting Scheikunde Hoofdstuk 1, 2, 3 4 Samenvatting door Syb 1176 woorden 4 keer beoordeeld 4 maart 2018 Vak Scheikunde Methode Chemie overal Scheikunde H1/H2/H3 Samenvatting PARAGRAAF 1.1 Een stof
Samenvatting Scheikunde Hoofdstuk 1, 2, 3 4 Samenvatting door Syb 1176 woorden 4 keer beoordeeld 4 maart 2018 Vak Scheikunde Methode Chemie overal Scheikunde H1/H2/H3 Samenvatting PARAGRAAF 1.1 Een stof
Voederwaarde-onderzoek Gras ingekuild Kuilkenner Excellent kuil 1
 Onderzoek Onderzoek-/ordernummer: Datum verslag: 731267/002743994 22-07-2011 Oogstdatum: Datum monstername: Monster genomen door: Contactpersoon monstername: 16-05-2011 07-07-2011 Dick Huiberts: 0652002131
Onderzoek Onderzoek-/ordernummer: Datum verslag: 731267/002743994 22-07-2011 Oogstdatum: Datum monstername: Monster genomen door: Contactpersoon monstername: 16-05-2011 07-07-2011 Dick Huiberts: 0652002131
Waaruit bestaan de dingen? (deel 1)
 Waaruit bestaan de dingen? (deel 1) Elementen en atomen Verbindingen van atomen tot moleculen Het binnenste van een atoom Elementen en atomen Lees bladzijde 76, bladzijde 77 en van bladzijde 78 de linkerkolom
Waaruit bestaan de dingen? (deel 1) Elementen en atomen Verbindingen van atomen tot moleculen Het binnenste van een atoom Elementen en atomen Lees bladzijde 76, bladzijde 77 en van bladzijde 78 de linkerkolom
EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN Dit examen bestaat uit twintig vragen
 MAVO -C I EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN 1985 MAVO -C Vrijdag 10 mei, 9.00-11.00 uur SCHEIKUNDE- meerkeuzevragen Dit examen bestaat uit twintig vragen Bij het examen scheikunde wordt
MAVO -C I EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN 1985 MAVO -C Vrijdag 10 mei, 9.00-11.00 uur SCHEIKUNDE- meerkeuzevragen Dit examen bestaat uit twintig vragen Bij het examen scheikunde wordt
1 Binaire plaatjes en Japanse puzzels
 Samenvatting Deze samenvatting is voor iedereen die graag wil weten waar mijn proefschrift over gaat, maar de wiskundige notatie in de andere hoofdstukken wat te veel van het goede vindt. Ga er even voor
Samenvatting Deze samenvatting is voor iedereen die graag wil weten waar mijn proefschrift over gaat, maar de wiskundige notatie in de andere hoofdstukken wat te veel van het goede vindt. Ga er even voor
Inhoud LEERPLANDOELSTELLINGEN LEERINHOUDEN. De leerlingen kunnen
 Inhoud 1. Inleiding... 2 2. Het spectrum van waterstof en het atoommodel van Bohr... 5 3. Het atoommodel van BohrSommerfeld... 8 4. Elektronenconfiguratie... 10 5. Het periodiek systeem... 11 5.1. Historiek...
Inhoud 1. Inleiding... 2 2. Het spectrum van waterstof en het atoommodel van Bohr... 5 3. Het atoommodel van BohrSommerfeld... 8 4. Elektronenconfiguratie... 10 5. Het periodiek systeem... 11 5.1. Historiek...
I. Basiskennis. Zuivere stof*: Is materie die uit 1 stof bestaat en niet meer gescheiden kan worden door fysische scheidingstechnieken.
 Basiskennis 5 chemie 3 de graad, 1 ste jaar = 5avv, 5av, 5bv 1 1.1 Opbouw van de materie I. Basiskennis Zuivere stof*: Is materie die uit 1 stof bestaat en niet meer gescheiden kan worden door fysische
Basiskennis 5 chemie 3 de graad, 1 ste jaar = 5avv, 5av, 5bv 1 1.1 Opbouw van de materie I. Basiskennis Zuivere stof*: Is materie die uit 1 stof bestaat en niet meer gescheiden kan worden door fysische
