Farmacovigilantie. Veilige en doeltreffende geneesmiddelen met de inzet van alle gezondheidspartners. Wat is farmacovigilantie? december 07 nr 145
|
|
|
- Greta Bosmans
- 7 jaren geleden
- Aantal bezoeken:
Transcriptie
1 Newsletter van pharma.be vzw Verschijnt niet in juli en augustus Afgiftekantoor Brussel X december 07 nr 145 Veilige en doeltreffende geneesmiddelen met de inzet van alle gezondheidspartners Wat is farmacovigilantie? De Wereldgezondheidsorganisatie (WGO) beschrijft farmacovigilantie als de wetenschap en de activiteiten betreffende het opsporen, evalueren, begrijpen en voorkomen van bijwerkingen of om het even welk ander probleem met een geneesmiddel. Met de term farmacovigilantie of geneesmiddelenbewaking wordt het geheel van processen van bewaking en evaluatie van bijwerkingen van geneesmiddelen aangeduid (FAGG). Met farmacovigilantie willen alle gezondheidspartners door samenwerking onder meer het volgende stimuleren: de zorg en de veiligheid van patiënten bij het gebruik van geneesmiddelen en andere medische hulpmiddelen; het veilig en goed gebruik van geneesmiddelen; de kennis en de vorming inzake geneesmiddelenbewaking en de communicatie ervan. 1
2 Veilige geneesmiddelen, een must De veiligheid van de patiënt is primordiaal voor de farmaceutische researchindustrie. In België zetten meer dan 5000 onderzoekers in farmaceutische labo s zich elke dag in om tot kwalitatief hoogstaande en innoverende behandelingen te komen. De ontwikkeling van één nieuw geneesmiddel neemt 10 tot 12 jaar in beslag. Na preklinisch onderzoek volgt klinisch onderzoek. Beide voldoen aan de meest strikte vereisten. De uitvoering van de klinische studies wordt opgevolgd door de gezondheidsinstanties en de ethische comités 1. Daarnaast zijn de zorgverstrekkers, in het bijzonder de artsen, van meet af aan nauw betrokken bij de ontwikkeling van het geneesmiddel. De informatie-uitwisseling met de artsen is essentieel voor het onderzoek naar goede en veilige geneesmiddelen. De bijdrage van de artsen is vanaf het begin van de onderzoeksfase onontbeerlijk en blijft ook na de toelating op de markt van fundamenteel belang. Vooraleer de klinische studies van start gaan, wordt de veiligheid van het actieve bestanddeel van een geneesmiddel uitgebreid getest en geverifieerd, onder meer via toxicologische studies. Duizenden mensen zijn betrokken bij die klinische studies. Niets wordt dan ook aan het toeval overgelaten eens die deelnemers, eerst gezonde vrijwilligers en in een latere fase patiënten, bij de verdere ontwikkeling van een behandeling worden betrokken. Eenmaal een geneesmiddel zich op de markt bevindt blijft de informatie-uitwisseling tussen de farmaceutische labo s, de gezondheidsinstanties en de artsen een centrale rol spelen om de veiligheid van patiënten te verzekeren. Wat voorafgaat aan de marktintroductie... Vooraleer een geneesmiddel beschikbaar wordt voor de patiënten, hebben ook de gezondheidsinstanties, tijdens de administratieve procedures, alle gegevens over het geneesmiddel grondig bestudeerd. Tijdens de registratieprocedure buigen experten van het Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten (FAGG) zich over de veiligheid, de kwaliteit en de doeltreffendheid van het nieuwe geneesmiddel. Bij de aanvraag tot een vergunning voor het in de handel brengen (VHB) of registratie wordt een dossier met alle wetenschappelijke data over het nieuwe geneesmiddel aan het FAGG afgeleverd. Tijdens de beslissing tot terugbetaling onderzoekt de CTG (Commissie Tegemoetkoming geneesmiddelen) nogmaals de wetenschappelijke gegevens van het nieuwe geneesmiddel. Deze keer richt men zich evenwel vooral op de toegevoegde waarde van de behandeling. Er wordt een vergelijking gemaakt met de bestaande behandelingen. In deze fase bepaalt Sociale Zaken om al dan niet een geneesmiddel toe te laten tot terugbetaling. De veiligheid en de toegevoegde waarde van de behandeling worden dus minutieus onderzocht vooraleer het geneesmiddel op de markt komt. 2 1 Een Onafhankelijk Ethisch Comité (OEC) bestaat uit een aantal artsen, een jurist, ethicus en een vertegenwoordiger van de patiënten. Een OEC verstrekt advies over geplande klinische studies, volgt die op en onderzoekt en beoordeelt de gegevens van de farmaceutische labo s. Elk ziekenhuis waar klinische studies worden uitgevoerd dienen bij wet een OEC te hebben.
3 Het federale geneesmiddelenagentschap en de CTG spelen hierbij een vooraanstaande rol. Beide organen kunnen alvorens een beslissing te treffen bijkomende studies en onderzoeken vereisen van de vergunningaanvrager of -houder, die vaak eveneens de farmaceutische producent is. Wat volgt op de marktintroductie... Ook de farmaceutische labo s zetten hun inspanningen naarstig verder. Tot aan de marktintroductie wordt het gebruik van een geneesmiddel strikt beperkt gehouden. In de meeste klinische van het systeem van geneesmiddelenbewaking opgesteld. Hier wordt onder meer gewezen op de gekwalificeerde persoon voor de geneesmiddelenbewaking ( qualified person ; QP). De QP beschikt over de nodige expertise terzake en is verantwoordelijk voor de geneesmiddelenbewaking. Hij beheert onder meer het volledige systeem inzake de melding van alle vermoedelijke bijwerkingen, staat steeds ter beschikking van de vergunninghouder en fungeert ononderbroken als contactpersoon voor het FAGG. Bij bepaalde geneesmiddelen, waaronder deze die een nieuwe actieve substantie bevatten, wordt ook een risicobeheerprogramma ( Risk management plan ; RMP) opgemaakt. Dat programma bevat een overzicht van de geplande acties die mogelijke risico s verbonden aan het geneesmiddel identificeren, karakteriseren, voorkomen of in sterke mate reduceren. De hierboven vermelde QP is ook verantwoordelijk voor de veiligheidsrapporten die het farmaceutische labo op regelmatige tijdstippen indient bij de bevoegde gezondheidsinstanties, met name het Belgisch Centrum voor Geneesmiddelenbewaking (BCGH) dat verbonden is aan het geneesmiddelenagentschap (FAGG). Dat veiligheidsrapport vormt een lijvig dossier waarin onder meer een wetenschappelijke evaluatie van de risico/baten verhouding is opgenomen; in dit rapport worden ook alle voorgekomen meldingen van bijwerkingen en andere nieuwe of gewijzigde data met betrekking tot het veiligheidsprofiel van het geneesmiddel in kwestie weergegeven. studies wordt immers gewerkt met vrij homogene populaties binnen vooraf vastgelegde omstandigheden. De onderzoekers stellen alles in het werk om de verwachtingen van een behandeling in kaart te brengen. Elke patiënt is evenwel anders met specifieke individuele eigenschappen. Op het ogenblik dat het geneesmiddel wijdverspreid beschikbaar wordt voor alle patiënten kunnen daarom bijvoorbeeld nog interacties met andere terzelfdertijd ingenomen geneesmiddelen of voorheen nog niet opgemerkte bijwerkingen aan de oppervlakte komen. Reeds bij de vergunningsaanvraag heeft het farmaceutisch labo een uitvoerige beschrijving De eerste jaren na de marktintroductie dient de vergunninghouder, die vaak ook het nieuwe geneesmiddel produceert, zesmaandelijks het betreffende veiligheidsrapport in. De vergunninghouder blijft dit volhouden op geregelde tijdstippen die na verloop van tijd evenwel afnemen. Gedurende die hele periode blijven onderzoekers de risico/baten verhoudingen opvolgen, via o.a. wetenschappelijke literatuurstudies, farmacoepidemologische studies of eventueel bijkomende klinische studies. Na enkele jaren, waarbij het geneesmiddel op grote schaal werd gebruikt, heeft een behandeling nog weinig geheimen voor de farmaceutische onderzoekers. 3
4 Indien er na de marktintroductie een probleem rijst met het gebruik van een geneesmiddel, reageert de vergunninghouder meteen. Bij de minste twijfel wordt er niet getalmd om een geneesmiddel tijdelijk of definitief van de markt te halen. Dit is echter een worst case scenario. Meestal is het aanscherpen en bijsturen van de behandeling toereikend, zoals o.a. het aanpassen van de dosis of het opnemen van een nieuwe contraindicatie of waarschuwing. Het Risk Management Plan (RMP) Het RMP maakt deel uit van het Risk Management System dat gericht is op de identificatie, de karakterisering, de preventie of het minimaliseren van de mogelijke risico s verbonden aan een geneesmiddel. Dat systeem waarborgt dat de voordelen van een geneesmiddel de risico s met een zo ruim mogelijke marge overstijgen. Een RMP is nodig bij het indienen van een nieuwe aanvraag voor o.a. een geneesmiddel dat een nieuwe actieve substantie bevat of een biologisch gelijkwaardig geneesmiddel. Een efficiënt opsporingssysteem ondersteund door alle gezondheidsactoren De veiligheid van de patiënt is de hoofdbekommernis van alle gezondheidspartners. Onder meer de gezondheidsinstanties, de zorgverstrekkers en de farmaceutische researchindustrie zetten zich samen in om problemen met geneesmiddelen te vermijden en eventuele onverwachte gebeurtenissen zo snel mogelijk op te sporen en te verhelpen. Op nationaal niveau is het Belgisch Centrum voor Geneesmiddelenbewaking (BCGH), dat verbonden is aan het geneesmiddelenagentschap, de spil van het meldsysteem. Het BCGH speelt de relevante info door aan het Europese netwerk voor gegevensverwerking Eudravigilance, dat ontwikkeld werd door het Europese geneesmiddelenagentschap (EMEA). Op zijn beurt licht Eudravigilance alle Europese lidstaten in. De procedure Het meldsysteem van bijwerkingen van het BCGH is afhankelijk van de meldingen van de vergunninghouders en van de gezondheidszorgbeoefenaars. Een RMP bestaat uit twee delen, met name: Deel I met een samenvatting van het zogenaamde veiligheidsprofiel van het geneesmiddel en een farmacovigilantieplan; Deel II met een evaluatie inzake het al dan niet nodig zijn van acties om de risico s tot een minimum te herleiden, en, indien geacht wordt dat deze acties noodzakelijk zijn, het risk minimisation plan. Een belangrijke component van het risk minimisation plan is de communicatie naar en de educatie van de zorgverstrekkers en de patiënten over bepaalde potentiële risico s van een geneesmiddel en hoe die kunnen worden gereduceerd. Daartoe wordt de nodige informatie en educatiemateriaal ter beschikking gesteld. De apothekers kunnen dan de patiënt van extra informatie voorzien bij het afleveren van het geneesmiddel. 4
5 1) de vergunninghouder, die vaak ook het nieuwe geneesmiddel produceert, dient binnen de 15 dagen, nadat hij de nodige gegevens heeft verkregen, elke vermoedelijke ernstige bijwerking aan het BCGH te melden; 2) de gezondheidszorgbeoefenaars, o.a. artsen, apothekers en tandartsen, zijn vrij om alle bijwerkingen spontaan aan het FAGG te melden. Hoewel de vergunninghouders tijdens het verder onderzoek nog geconfonteerd kunnen worden met bijwerkingen of interacties met andere aandoeningen en/of ingenomen geneesmiddelen, zijn het voornamelijk de gezondheidszorgbeoefenaars die onverwachte bijwerkingen detecteren. Vanuit hun dagelijkse praktische ervaringen met individuele patiënten zitten zij in de beste positie om anomalieën op het spoor te komen. Daarom is het essentieel dat men blijft hameren op het grote belang van geneesmiddelenbewaking bij de zorgverstrekkers. Het aantal meldingen van bijwerkingen bedroeg in 2004 in België Het aantal meldingen in ons land overstijgt daarmee ruim het Europese gemiddelde. De praktijk leert ons dat een groot aantal zorgverstrekkers bij de vaststelling van een onverwachte bijwerking contact opnemen met de vergunninghouder, die daarna het BCGH inlicht. Hierdoor is het merendeel van de meldingen afkomstig van de farmaceutische industrie. Het percentage meldingen door de vergunninghouders in België bedroeg in %. Op Europees niveau nam de gemiddelde bijdrage van de vergunninghouders 37 % in. Daarenboven stegen in 2006 in ons land de meldingen van de vergunninghouders tot 87,5 %. 2 Met de steun van de farmaceutische researchindustrie heeft het FAGG het project Actieve geneesmiddelenbewaking gelanceerd. De bedoeling is de zorgverstrekkers te sensibiliseren voor een systematische of actieve geneesmiddelenbewaking ter vervanging van het spontane karakter die hun meldingen vandaag kennen. 2 Bron cijfermateriaal: FAGG 5
6 Interview met de heer Xavier De Cuyper, Administrateur-generaal van het FAGG Xavier De Cuyper 1. Wat houdt het concept van actieve geneesmiddelenbewaking door de gezondheidsprofessionals concreet in? Xavier De Cuyper: Actieve geneesmiddelenbewaking in het algemeen veronderstelt a priori de systematische melding van bijwerkingen met geneesmiddelen die optreden binnen een gedefinieerde bevolkingsgroep. Praktisch zal men aan de actief deelnemende gezondheidszorgbeoefenaars vragen om bepaalde types van bijwerkingen (vb. ernstige, onverwachte), die zij in hun praktijk ondervinden, systematisch te rapporteren. Het project rond actieve geneesmiddelenbewaking dat het FAGG in de loop van 2008 opstart, heeft tot doel de kennis van het veiligheidsprofiel van geneesmiddelen te verbeteren door het aantal kwalitatief hoogstaande (evalueerbare) en relevante meldingen van (vb. onverwachte) bijwerkingen die rechtsreeks door de gezondheidszorgbeoefenaars aan het FAGG worden doorgegeven, te verhogen. Deze situaties kunnen o.a. te maken hebben met kwetsbare bevolkingsgroepen (vb. kinderen, zwangere vrouwen en vrouwen die borstvoeding geven, oudere mensen), een eerste toediening van innovatieve en generische geneesmiddelen en toediening van vaccins. 2. Hoe percipieert u de bijdrage van de farmaceutische industrie bij de meldingen van onverwachte bijwerkingen bij het BCGH? XDC: Tot op vandaag is de meerderheid van de meldingen van ernstige bijwerkingen aan het BCGH afkomstig van de farmaceutische industrie, nl. méér dan 85 %. Een groot deel van deze meldingen heeft te maken met klinische studies waarbij de vergunninghouder zelf de verantwoordelijkheid draagt. Daarnaast ontvangt de farmaceutische industrie ook meldingen van gezondheidszorgbeoefenaars via vertegenwoordigers die artsen en apothekers bezoeken. Het doorgeven van deze informatie naar het BCGH is wettelijk bepaald. Voor de meldingen vanuit klinische studies is en blijft de goede samenwerking tussen de farmaceutische industrie en het BCGH noodzakelijk. Hierbij wil men de gezondheidszorgbeoefenaars meer bewust maken van de doelstellingen en van het nut van geneesmiddelenbewaking via sensibiliseringsacties van het FAGG. Er zal ook een doeltreffende informaticatool (webbased system) ter beschikking gesteld worden aan de gezondheidszorgbeoefenaars dat de melding van bijwerkingen moet vergemakkelijken en de kwaliteit ervan moet verhogen. In een eerste fase van dit project zullen een 200-tal huisartsen, voorschrijvende artsen in ziekenhuizen en officina-apothekers uit Brussel, Vlaanderen en Wallonië, die zich hiervoor vrijwillig kandidaat zullen stellen, de nodige specifieke opleiding krijgen betreffende actieve geneesmiddelenbewaking. Er zal hen gevraagd worden om ernstige, onverwachte of verdachte bijwerkingen, die gekoppeld zijn aan bijzondere situaties, te rapporteren. 6
7 Het overmaken van individuele rapporten van onverwachte bijwerkingen zowel vanuit klinische studies voor (nog) niet vergunde geneesmiddelen als vanuit klinische studies met vergunde geneesmiddelen alsook spontane meldingen voor vergunde geneesmiddelen, is de snelste manier om nieuwe, ongekende bijwerkingen te leren kennen of signalen op te vangen. 3. Hoe verloopt de samenwerking inzake geneesmiddelenbewaking met de farmaceutische industrie? XDC: De samenwerking die bestaat tussen het FAGG (O&O en het BCGH die beiden toezien op de veiligheid van een geneesmiddel) met de farmaceutische industrie is volledig wettelijk bepaald. De Europese Richtlijnen aangaande klinische studies (Richtlijn 2001/20) en de desbetreffende Belgische wetgeving, in het bijzonder de wet van 7 mei 2004 inzake experimenten op de menselijke persoon die deze samenwerking verplichten, garanderen in de eerste plaats de rechten, de veiligheid en het welzijn van alle deelnemers aan klinische studies; deze regelgeving voorziet ook een constructieve manier van uitwisseling van veiligheidsgegevens tussen de betrokken partijen, wat enkel een goede samenwerking kan bevorderen. Het begint al met de verplichting die een opdrachtgever van een klinische studie heeft om vergunning te vragen voor de eerste studie die hij met een nieuw geneesmiddel wil uitvoeren op menselijke proefpersonen. De instemming van het FAGG en Ethische Comités is hierbij ver- eist. Eénmaal de studie opgestart is, dient de opdrachtgever het FAGG en de Ethische Comités op regelmatige basis te informeren over bijwerkingen met geneesmiddelen (binnen de 7/15 dagen alle zogenaamde SUSARs Suspected Unexpected Serious Adverse Reactions, zesmaandelijkse line listings en jaarlijkse verslagen; deze laatste geven een overzicht van de bij- werkingen die voorkomen tijdens de voorgaande periode, dit niet alleen voor bijwerkingen die voorkomen in België maar ook alle andere bijwerkingen buiten België die betrekking heb- ben op hetzelfde onderzoeksproduct). Steeds opnieuw wordt de vraag gesteld of het geneesmiddel veilig genoeg is. Deze procedure geldt zolang er klinische studies op Belgisch grondgebied worden uitgevoerd. Tijdens de aanvraag tot het bekomen van een vergunning voor het in de handel brengen van een geneesmiddel worden opnieuw alle veiligheidsgegevens, bekomen tijdens onderzoek voorafgaand aan de aanvraag, bij elkaar gelegd en opnieuw geëvalueerd. In het kader van dit dossier wordt de vergunninghouder gevraagd ook het zogenaamde risk management plan op te stellen. Hiertoe verbindt deze zich ertoe verder onderzoek te doen naar de veiligheid van het geneesmiddel na het vergunnen ervan 7
8 of soms specifiek onderzoek naar een signaal of een bezorgdheid over het geneesmiddel. Na het vergunnen en het commercialiseren van het geneesmiddel zal de vergunninghouder het FAGG nog informeren over bijwerkingen, zowel verwachte als onverwachte, die volgens de farmacovigilantiewetgeving dienen gerapporteerd te worden. Daarnaast worden veilgheidsverslagen op vaste tijdstippen, over een periode van 6 maanden tot 3 jaar, en éénmalig na 5 jaar na het verlenen van de vergunnning, opgevraagd. De respectievelijke nationale en Europese wetteksten die hiervan aan de basis liggen, zijn de wet van 25 maart 1964 op de geneesmiddel, herziening van 1 mei 2006 en het zogenoemde Mammoet-KB van 14 december 2006, de verordening 726/2004, de richtlijn 2004/27 en de zogenoemde Volume 9A of the Rules Governing Medicinal Products in the European Union: Pharmacovigilance for medicinal products for human use, die de praktische organisatie van deze taken voorzien. Reeds tijdens de eerste stadia in de ontwikkeling van een nieuw geneesmiddel, worden door het farmaceutisch labo markante inspanningen geleverd om de veiligheid van het geneesmiddel zoveel mogelijk te garanderen. Het optimaliseren van de risico/baten verhouding van het nieuwe geneesmiddel is dan ook een continue zorg van het farmaceutisch labo, niet Annemie Decostere alleen tijdens de ontwikkelingsfase, maar ook éénmaal het geneesmiddel op de markt is gebracht. Immers, wanneer het geneesmiddel wijdverspreid ter beschikking wordt gesteld van de patiënt, kunnen voordien onopgemerkte bijwerkingen of mogelijke interacties met andere ingenomen geneesmiddelen of onderliggende aandoeningen niet helemaal worden uitgesloten. Om hier zo adequaat mogelijk op in te spelen, is een efficiënt werkend systeem van geneesmiddelenbewaking een conditio sine qua non. Hierin speelt het FAGG, meer specifiek het Belgisch centrum voor Geneesmiddelenbewaking voor Humaan gebruik (BCGH), een cruciale rol als centraal meldpunt voor bijwerkingen en andere veiligheidsaspecten gelieerd aan het gebruik van geneesmiddelen. In dit kader is het dan ook onontbeerlijk dat de uitwisseling van informatie tussen het BCGH, de gezondheidszorgbeoefenaars en het farmaceutisch labo als gezondheidszorgpartners optimaal verloopt en dit zowel vóór als na het op de markt brengen van het geneesmiddel. Annemie Decostere, Regulatory Affairs Manager, pharma.be >>> RAADPLEEG ONZE VORIGE FACTUA S OP > PUBLICATIES > FACTUA NEWSLETTER: > Klinische studies (06/2007) > Het Geneesmiddelenagentschap en de Pharmaceutical Review : twee sleutels tot innovatie (03/2007) > Innovatie: vanuit het perspectief van de patiëntenverenigingen (11/2006) > Belgium as host location for Biopharma (11/2006) pharma.be vzw Terhulpsesteenweg Brussel info@pharma.be fax Verantwoordelijke uitgever: Leo Neels Voor meer informatie kunt u contact opnemen met de Dienst Communicatie. Artikels of delen van artikels en illustraties mogen alleen worden overgenomen na toestemming van de redactie. Lid van de Unie van de Uitgevers van de Periodieke Pers. Version française sur demande. Zolang er onderzoek is, is er hoop
Online melden van bijwerkingen via de website www.gelefiche.be
 Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten Uw geneesmiddelen en gezondheidsproducten, onze zorg Online melden van bijwerkingen via de website www.gelefiche.be Het Federaal Agentschap
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten Uw geneesmiddelen en gezondheidsproducten, onze zorg Online melden van bijwerkingen via de website www.gelefiche.be Het Federaal Agentschap
Sildenafil mag niet gebruikt worden voor de behandeling van intrauteriene
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Hoe garanderen België en Europa veilige vaccins? Pieter Neels, FAGG
 Hoe garanderen België en Europa veilige vaccins? Pieter Neels, FAGG Disclaimer Niettegenstaande mijn betrokkenheid bij het Comité voor geneesmiddelen voor menselijk gebruik (CHMP), kan deze presentatie
Hoe garanderen België en Europa veilige vaccins? Pieter Neels, FAGG Disclaimer Niettegenstaande mijn betrokkenheid bij het Comité voor geneesmiddelen voor menselijk gebruik (CHMP), kan deze presentatie
FOD Volksgezondheid, Veiligheid van de Voedselketen en Leefmilieu. Directoraat-generaal Geneesmiddelen
 Afdeling Wig ilantie' Amazone Afdeling `138(D'(Onderzoek&Ontwikkeling) Bischoffsheimlaan 33 B-1000 BRUSSEL Belgisch Centrum voor Geneesmiddelenbewaking voor geneeesmiddelen voor humaan gebruik Uw brief
Afdeling Wig ilantie' Amazone Afdeling `138(D'(Onderzoek&Ontwikkeling) Bischoffsheimlaan 33 B-1000 BRUSSEL Belgisch Centrum voor Geneesmiddelenbewaking voor geneeesmiddelen voor humaan gebruik Uw brief
Centrum klinische farmacologie: deelnemen aan een klinische studie
 Centrum klinische farmacologie: deelnemen aan een klinische studie informatie voor gezonde proefpersonen en patïenten INLEIDING 3 KLINISCHE STUDIES: EEN INLEIDING 4 De ontwikkeling van een nieuw geneesmiddel
Centrum klinische farmacologie: deelnemen aan een klinische studie informatie voor gezonde proefpersonen en patïenten INLEIDING 3 KLINISCHE STUDIES: EEN INLEIDING 4 De ontwikkeling van een nieuw geneesmiddel
Generisch of origineel: geen verschil voor uw gezondheid
 Federaal agentschap voor geneesmiddelen en gezondheidsproducten Generisch of origineel: geen verschil voor uw gezondheid Nieuwe bewustmakingscampagne van het fagg Xavier De Cuyper, Administrateur-generaal
Federaal agentschap voor geneesmiddelen en gezondheidsproducten Generisch of origineel: geen verschil voor uw gezondheid Nieuwe bewustmakingscampagne van het fagg Xavier De Cuyper, Administrateur-generaal
Het melden van bijwerkingen van geneesmiddelen: vaak gestelde vragen
 Afdeling Vigilantie Het melden van bijwerkingen van geneesmiddelen: vaak gestelde vragen Wat is een bijwerking van een geneesmiddel? Een bijwerking van een geneesmiddel is een schadelijke en ongewilde
Afdeling Vigilantie Het melden van bijwerkingen van geneesmiddelen: vaak gestelde vragen Wat is een bijwerking van een geneesmiddel? Een bijwerking van een geneesmiddel is een schadelijke en ongewilde
Rechtstreekse mededeling aan de Gezondheidszorgbeoefenaars
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Informatiefiche voor artsen voor een veilig en doeltreffend gebruik van het geneesmiddel
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Informatie verspreid onder het gezag van het federaal agentschap voor geneesmiddelen en gezondheidsproducten
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Capecitabine Accord moet permanent worden stopgezet bij patiënten die een ernstige huidreactie hebben gehad tijdens de behandeling.
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Bent u gevraagd voor medisch wetenschappelijk onderzoek?
 Bent u gevraagd voor medisch wetenschappelijk onderzoek? Inhoud Pagina Inleiding... 2 Medisch wetenschappelijk onderzoek... 3 Waarom zou u meedoen... 4 Onderzoeksfasen... 5 Medisch Ethische Commissie...
Bent u gevraagd voor medisch wetenschappelijk onderzoek? Inhoud Pagina Inleiding... 2 Medisch wetenschappelijk onderzoek... 3 Waarom zou u meedoen... 4 Onderzoeksfasen... 5 Medisch Ethische Commissie...
Deelnemen aan een klinische studie in Az Damiaan. Informatie voor de patiënt SAP 12496
 Deelnemen aan een klinische studie in Az Damiaan Informatie voor de patiënt SAP 12496 Bron: clinical trial center UZ Leuven 2010 2 Inhoud Inleiding 4 Wat is een klinische studie? 5 Waarom deelnemen aan
Deelnemen aan een klinische studie in Az Damiaan Informatie voor de patiënt SAP 12496 Bron: clinical trial center UZ Leuven 2010 2 Inhoud Inleiding 4 Wat is een klinische studie? 5 Waarom deelnemen aan
PROCEDURE BETREFFENDE DE VERZENDING VAN BRIEVEN TER ATTENTIE VAN DE GEZONDHEIDSZORGBEOEFENAARS (DHPC's)
 PROCEDURE BETREFFENDE DE VERZENDING VAN BRIEVEN TER ATTENTIE VAN DE GEZONDHEIDSZORGBEOEFENAARS (DHPC's) 8/10/2015 (v2) Deze procedure werd opgesteld op initiatief van de vertegenwoordigers van de industrie
PROCEDURE BETREFFENDE DE VERZENDING VAN BRIEVEN TER ATTENTIE VAN DE GEZONDHEIDSZORGBEOEFENAARS (DHPC's) 8/10/2015 (v2) Deze procedure werd opgesteld op initiatief van de vertegenwoordigers van de industrie
FAGG advies in functie van procedures voor aanvragen tot klinische studies en VHB
 DG Pre Vergunning Federaal agentschap voor geneesmiddelen en gezondheidsproducten Eurostation II Victor Hortaplein 40/40 1060 Brussel Internetadres: www.fagg.be FAGG advies in functie van procedures voor
DG Pre Vergunning Federaal agentschap voor geneesmiddelen en gezondheidsproducten Eurostation II Victor Hortaplein 40/40 1060 Brussel Internetadres: www.fagg.be FAGG advies in functie van procedures voor
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek
 Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
Veel gestelde vragen Melden voorvallen/bijwerkingen bij geneesmiddelenonderzoek Wat is een SUSAR? SUSAR is de afkorting van Suspected Unexpected Serious Adverse Reaction. In het Nederlands betekent dit
Deelnemen aan een klinische studie. informatie voor patiënten
 Deelnemen aan een klinische studie informatie voor patiënten INLEIDING 3 KLINISCHE STUDIES: INLEIDENDE INFO 5 Wat is een klinische studie? Klinische studies in UZ Leuven Waarom deelnemen aan een klinische
Deelnemen aan een klinische studie informatie voor patiënten INLEIDING 3 KLINISCHE STUDIES: INLEIDENDE INFO 5 Wat is een klinische studie? Klinische studies in UZ Leuven Waarom deelnemen aan een klinische
KLINISCHE STUDIES. in AZ Sint-Lucas
 KLINISCHE STUDIES in AZ Sint-Lucas KLINISCHE STUDIES in AZ Sint-Lucas Overweegt u om, al dan niet op verzoek van uw arts, deel te nemen aan een klinische studie? Het is belangrijk dat u vooraf goed geïnformeerd
KLINISCHE STUDIES in AZ Sint-Lucas KLINISCHE STUDIES in AZ Sint-Lucas Overweegt u om, al dan niet op verzoek van uw arts, deel te nemen aan een klinische studie? Het is belangrijk dat u vooraf goed geïnformeerd
Q&A - KB 28 MEI 2013 EN OMZENDBRIEF NR 601
 Q&A - KB 28 MEI 2013 EN OMZENDBRIEF NR 601 1. Welke procedure moet gevolgd worden om zich als lokale contactpersoon aan te melden bij het fagg en aan welke vereisten moet de contactpersoon voldoen? In
Q&A - KB 28 MEI 2013 EN OMZENDBRIEF NR 601 1. Welke procedure moet gevolgd worden om zich als lokale contactpersoon aan te melden bij het fagg en aan welke vereisten moet de contactpersoon voldoen? In
VISTABEL (botulinum toxine type A) Educatieve brochure voor artsen. 50 Allerganeenheden Poeder voor oplossing voor injectie
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VISTABEL. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel VISTABEL. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Belangrijke informatie voor beroepsbeoefenaren
 De gezondheidsautoriteiten van de Europese Unie hebben het in de handel brengen van het geneesmiddel Kadcyla verbonden aan bepaalde voorwaarden. Het verplichte farmacovigilantieplan ter minimalisatie van
De gezondheidsautoriteiten van de Europese Unie hebben het in de handel brengen van het geneesmiddel Kadcyla verbonden aan bepaalde voorwaarden. Het verplichte farmacovigilantieplan ter minimalisatie van
Gids voor het interpreteren van spontane meldingen van vermoedelijke bijwerkingen van geneesmiddelen
 30 januari 2017 Inspecties, bewaking voor menselijk gebruik en comités EMA/749446/2016 Herziening 1* Gids voor het interpreteren van spontane meldingen van vermoedelijke bijwerkingen Overeenstemming door
30 januari 2017 Inspecties, bewaking voor menselijk gebruik en comités EMA/749446/2016 Herziening 1* Gids voor het interpreteren van spontane meldingen van vermoedelijke bijwerkingen Overeenstemming door
Onderwerp: Ernstige huidreacties geassocieerd met Capecitabine (Xeloda )
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
DE CODE VOOR DEONTOLOGIE VAN MDEON
 DE CODE VOOR DEONTOLOGIE VAN MDEON De interacties tussen de BEROEPSBEOEFENAARS UIT DE GEZONDHEIDSSECTOR en de industrie VAN DE GENEESMIDDELEN en van de MEDISCHE HULPMIDDELEN Deontologisch gezondheidsplatform
DE CODE VOOR DEONTOLOGIE VAN MDEON De interacties tussen de BEROEPSBEOEFENAARS UIT DE GEZONDHEIDSSECTOR en de industrie VAN DE GENEESMIDDELEN en van de MEDISCHE HULPMIDDELEN Deontologisch gezondheidsplatform
ZELDZAME ZIEKTEN & WEESGENEESMIDDELEN. Een unieke uitdaging voor de kwalitatieve gezondheidszorg
 ZELDZAME ZIEKTEN & WEESGENEESMIDDELEN Een unieke uitdaging voor de kwalitatieve gezondheidszorg 2 ZELDZAAM, MAAR NIET UITZONDERLIJK Een ziekte is zeldzaam wanneer deze voorkomt bij niet meer dan 5 op 10.000
ZELDZAME ZIEKTEN & WEESGENEESMIDDELEN Een unieke uitdaging voor de kwalitatieve gezondheidszorg 2 ZELDZAAM, MAAR NIET UITZONDERLIJK Een ziekte is zeldzaam wanneer deze voorkomt bij niet meer dan 5 op 10.000
Deelname aan een klinische studie informatie voor patiënten
 Deelname aan een klinische studie informatie voor patiënten Jan Yperman Ziekenhuis Briekestraat 12 8900 Ieper 32.037N 20170901 www.yperman.net 057 35 35 35 info@yperman.net diensthoofd klinische studies
Deelname aan een klinische studie informatie voor patiënten Jan Yperman Ziekenhuis Briekestraat 12 8900 Ieper 32.037N 20170901 www.yperman.net 057 35 35 35 info@yperman.net diensthoofd klinische studies
Het melden van bijwerkingen van geneesmiddelen: vaak gestelde vragen
 Afdeling Vigilantie Het melden van bijwerkingen van geneesmiddelen: vaak gestelde vragen Wat is een bijwerking van een geneesmiddel? Een bijwerking van een geneesmiddel is een schadelijke en ongewilde
Afdeling Vigilantie Het melden van bijwerkingen van geneesmiddelen: vaak gestelde vragen Wat is een bijwerking van een geneesmiddel? Een bijwerking van een geneesmiddel is een schadelijke en ongewilde
Informatie verstrekt onder het gezag van het Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Codex Pharma Commenté / Becommentarieerde Codex Pharma Artikel 6, 1
 Lid 1 Een geneesmiddel mag slechts in de handel worden gebracht, nadat een vergunning voor het in de handel brengen, hierna VHB genoemd, is verleend hetzij door de minister of zijn afgevaardigde overeenkomstig
Lid 1 Een geneesmiddel mag slechts in de handel worden gebracht, nadat een vergunning voor het in de handel brengen, hierna VHB genoemd, is verleend hetzij door de minister of zijn afgevaardigde overeenkomstig
Impact op de Belgische gezondheidszorg
 EUROPESE UNIE EN GEZONDHEIDSZORG OSE-IZRI studiedag EU geneesmiddelenbeleid: toegankelijkheid of concurrentiepositie versterken? Impact op de Belgische gezondheidszorg Minne Casteels Katholieke Universiteit
EUROPESE UNIE EN GEZONDHEIDSZORG OSE-IZRI studiedag EU geneesmiddelenbeleid: toegankelijkheid of concurrentiepositie versterken? Impact op de Belgische gezondheidszorg Minne Casteels Katholieke Universiteit
Directe communicatie aan gezondheidszorgbeoefenaars over de associatie van Sprycel (dasatinib) met Pulmonaire Arteriële Hypertensie (PAH)
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Q&A - KB 28 MEI 2013 EN OMZENDBRIEF NR 600
 Q&A - KB 28 MEI 2013 EN OMZENDBRIEF NR 600 1. Welke procedure moet gevolgd worden om zich als lokale contactpersoon aan te melden bij het fagg en aan welke vereisten moet de contactpersoon voldoen? In
Q&A - KB 28 MEI 2013 EN OMZENDBRIEF NR 600 1. Welke procedure moet gevolgd worden om zich als lokale contactpersoon aan te melden bij het fagg en aan welke vereisten moet de contactpersoon voldoen? In
Federgon kwaliteitscharter
 N2010 100 Federgon kwaliteitscharter Het kwaliteitscharter van Federgon is een basisdocument van de federatie en een instrument om de kwaliteit van de dienstverlening van de leden te waarborgen. Het beoogt
N2010 100 Federgon kwaliteitscharter Het kwaliteitscharter van Federgon is een basisdocument van de federatie en een instrument om de kwaliteit van de dienstverlening van de leden te waarborgen. Het beoogt
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Neurexan; Tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 tablet (301,5 mg) bevat: Avena sativa D2 0,6 mg Coffea cruda
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Neurexan; Tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 tablet (301,5 mg) bevat: Avena sativa D2 0,6 mg Coffea cruda
Rechtstreekse mededeling aan de Gezondheidszorgbeoefenaars
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Groep.10 : Uitzonderlijke spelers binnen het biopharma ecosysteem ALGEMENE VERENIGING VAN DE GENEESMIDDELENINDUSTRIE
 Groep.0 : Uitzonderlijke spelers binnen het biopharma ecosysteem ALGEMENE VERENIGING VAN DE GENEESMIDDELENINDUSTRIE Groep.0 waardevolle spelers in de economie en tewerkstelling pharma.be groepeert meer
Groep.0 : Uitzonderlijke spelers binnen het biopharma ecosysteem ALGEMENE VERENIGING VAN DE GENEESMIDDELENINDUSTRIE Groep.0 waardevolle spelers in de economie en tewerkstelling pharma.be groepeert meer
Meewerken aan medische vooruitgang. Klinische proeven
 Meewerken aan medische vooruitgang Klinische proeven De medische wereld heeft de voorbije vijftig jaar een enorme vooruitgang gekend. En met de technologische ontwikkelingen van vandaag zal de medische
Meewerken aan medische vooruitgang Klinische proeven De medische wereld heeft de voorbije vijftig jaar een enorme vooruitgang gekend. En met de technologische ontwikkelingen van vandaag zal de medische
President BeCRO organisatie van bedrijven die aktief zijn in het organiseren van klinische studies. Wat is? Medicament geneesmiddel device therapie?
 Melanoomstudiedag Els Vanpee President BeCRO organisatie van bedrijven die aktief zijn in het organiseren van klinische studies Hoofd klinische studies bij PAREXEL België Wat is? Medicament geneesmiddel
Melanoomstudiedag Els Vanpee President BeCRO organisatie van bedrijven die aktief zijn in het organiseren van klinische studies Hoofd klinische studies bij PAREXEL België Wat is? Medicament geneesmiddel
Deelnemen aan een klinische studie. Informatiebrochure
 Deelnemen aan een klinische studie Informatiebrochure Inhoud Deelnemen aan een klinische studie Informatiebrochure 1 Klinische studies 3 1.1 Wat en waarom? 3 1.2 Academische en commerciële studies 4 1.3
Deelnemen aan een klinische studie Informatiebrochure Inhoud Deelnemen aan een klinische studie Informatiebrochure 1 Klinische studies 3 1.1 Wat en waarom? 3 1.2 Academische en commerciële studies 4 1.3
Selectie en training van patiënten voor thuistoediening van Nplate
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Dit verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Nplate. Dit verplicht plan voor risicobeperking in België, waarvan deze informatie
Inleiding farmacovigilantie geneesmiddelen voor diergeneeskundig gebruik
 Inleiding farmacovigilantie geneesmiddelen voor diergeneeskundig gebruik 5de Vigilantiedag BRUSSEL Els Dewaele Inhoud Inleiding Bijwerkingen in EU en BE Verdeling van bijwerkingen Melden promoten? Toekomst
Inleiding farmacovigilantie geneesmiddelen voor diergeneeskundig gebruik 5de Vigilantiedag BRUSSEL Els Dewaele Inhoud Inleiding Bijwerkingen in EU en BE Verdeling van bijwerkingen Melden promoten? Toekomst
CERULYX 1. NAAM VAN HET GENEESMIDDEL 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 3. FARMACEUTISCHE VORM 4. KLINISCHE GEGEVENS
 CERULYX SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL CERULYX 4,55% oordruppels, oplossing. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Xyleen mengsel van isomeren: Xylol: 455mg/10ml
CERULYX SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL CERULYX 4,55% oordruppels, oplossing. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Xyleen mengsel van isomeren: Xylol: 455mg/10ml
DIFFERENT STEPS IN DRUG DEVELOPMENT: FROM THEORETICAL CONCEPT TO ACCESS FOR PATIENTS ROLE OF THE ETHICAL COMMITTEES
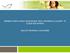 DIFFERENT STEPS IN DRUG DEVELOPMENT: FROM THEORETICAL CONCEPT TO ACCESS FOR PATIENTS ROLE OF THE ETHICAL COMMITTEES Klinische trials Verplicht vooraleer een geneesmiddel een marketing autorisatie kan krijgen
DIFFERENT STEPS IN DRUG DEVELOPMENT: FROM THEORETICAL CONCEPT TO ACCESS FOR PATIENTS ROLE OF THE ETHICAL COMMITTEES Klinische trials Verplicht vooraleer een geneesmiddel een marketing autorisatie kan krijgen
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Vertigoheel; Tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 tablet (301,5 mg) bevat: Cocculus indicus D4 210 mg Conium
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Vertigoheel; Tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 tablet (301,5 mg) bevat: Cocculus indicus D4 210 mg Conium
Vroege fase ontwikkeling en klinische proeven: evolutie over de voorbije jaren en een blik op de toekomst
 Vroege fase ontwikkeling en klinische proeven: evolutie over de voorbije jaren en een blik op de toekomst FAGG BRUSSEL 25.09.2018 Walter Janssens DG PRE vergunning Inleiding Klinische proeven worden traditioneel
Vroege fase ontwikkeling en klinische proeven: evolutie over de voorbije jaren en een blik op de toekomst FAGG BRUSSEL 25.09.2018 Walter Janssens DG PRE vergunning Inleiding Klinische proeven worden traditioneel
Dit geneesmiddel is een traditioneel kruidengeneesmiddel. De toepassing is uitsluitend gebaseerd op het langdurige gebruik.
 SEDISTRESS 1. NAAM VAN HET GENEESMIDDEL Sedistress 200 omhulde tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke omhulde tablet bevat 200 mg droogextract van de bovengrondse delen van passiebloem
SEDISTRESS 1. NAAM VAN HET GENEESMIDDEL Sedistress 200 omhulde tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke omhulde tablet bevat 200 mg droogextract van de bovengrondse delen van passiebloem
Publicatieblad van de Europese Unie
 25.3.2017 L 80/7 UITVOERINGSVERORDENING (EU) 2017/556 VAN DE COMMISSIE van 24 maart 2017 houdende de nadere regeling voor de inspectieprocedures inzake goede klinische praktijken overeenkomstig Verordening
25.3.2017 L 80/7 UITVOERINGSVERORDENING (EU) 2017/556 VAN DE COMMISSIE van 24 maart 2017 houdende de nadere regeling voor de inspectieprocedures inzake goede klinische praktijken overeenkomstig Verordening
INFORMATIE VERSTREKT ONDER HET GEZAG VAN HET FAGG RECHTSTREEKSE MEDEDELING AAN DE GEZONDHEIDSZORGBEOEFENAARS
 Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
Een Direct Healthcare Professional Communication (DHPC) is een schrijven dat naar de gezondheidszorgbeoefenaars wordt gezonden door de farmaceutische firma s, om hen te informeren over mogelijke risico
FLOLAN INFORMATIEGIDS VOOR PATIENTEN - FLOLAN
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
FAQ Administratief afsluiten
 FAQ Administratief afsluiten Iris Geussens 1 Vragen betreffende de afsluitdocumenten in het algemeen Algemeen kan gesteld worden, dat in alle omstandigheden in eerste instantie de final SPC, harmonized
FAQ Administratief afsluiten Iris Geussens 1 Vragen betreffende de afsluitdocumenten in het algemeen Algemeen kan gesteld worden, dat in alle omstandigheden in eerste instantie de final SPC, harmonized
Imnovid (pomalidomide) Directe berichtgeving aan gezondheidszorgbeoefenaars
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Imnovid. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Imnovid. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Federaal agentschap voor geneesmiddelen en gezondheidsproducten Traceerbaarheid van implantaten De implantaatkaart
 Federaal agentschap voor geneesmiddelen en gezondheidsproducten Traceerbaarheid van implantaten De implantaatkaart Vanessa Binamé- 13/03/15 Agenda Inleiding Traceerbaarheid van implantaten Implantaatkaart
Federaal agentschap voor geneesmiddelen en gezondheidsproducten Traceerbaarheid van implantaten De implantaatkaart Vanessa Binamé- 13/03/15 Agenda Inleiding Traceerbaarheid van implantaten Implantaatkaart
REGISTRATIEFORMULIER KLINISCHE STUDIES UZ /KULEUVEN BIJ HET CLINICAL TRIAL CENTER (CTC)
 Elke klinische studie die wordt opgestart in UZ/, wordt eenmalig geregistreerd via loketfunctie CTC. Na registratie ontvangt de hoofdonderzoeker een S nummer (via e mail aangeduide e mailadressen). De
Elke klinische studie die wordt opgestart in UZ/, wordt eenmalig geregistreerd via loketfunctie CTC. Na registratie ontvangt de hoofdonderzoeker een S nummer (via e mail aangeduide e mailadressen). De
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Oteel; Oordruppels, oplossing. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 monodosis van 0,45 ml (= 0,45 g) bevat: Arnica
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Oteel; Oordruppels, oplossing. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 monodosis van 0,45 ml (= 0,45 g) bevat: Arnica
Inhoudstafel per onderwerp volume 2 experimenten op de mens en menselijk lichaamsmateriaal
 Inhoudstafel per onderwerp volume 2 experimenten op de mens en menselijk lichaamsmateriaal Pharma Codex Deel I vol. 2 vii Voor de bijlagen bij de omzendbrieven en de nota s, raadpleeg de website van het
Inhoudstafel per onderwerp volume 2 experimenten op de mens en menselijk lichaamsmateriaal Pharma Codex Deel I vol. 2 vii Voor de bijlagen bij de omzendbrieven en de nota s, raadpleeg de website van het
Rol van European Organisa4on for Research and Treatment of Cancer (EORTC)
 Overzicht Verschillende partners Klinische studies binnen de farmaceu4sche industrie Protocol bij klinische studies Goedkeuring klinische studies Regels bij klinische studies Rol van European Medicines
Overzicht Verschillende partners Klinische studies binnen de farmaceu4sche industrie Protocol bij klinische studies Goedkeuring klinische studies Regels bij klinische studies Rol van European Medicines
MEDICATIESCHEMA, EEN VERSNELLING HOGER Wim Van Slambrouck, Senior Projectleider ICT, Agentschap Zorg en Gezondheid
 MEDICATIESCHEMA, EEN VERSNELLING HOGER Wim Van Slambrouck, Senior Projectleider ICT, Agentschap Zorg en Gezondheid MEDICATIESCHEL OP VITALINK BEKNOPTE INTRODUCTIE > Waarom? Voor het veilig delen van zorg
MEDICATIESCHEMA, EEN VERSNELLING HOGER Wim Van Slambrouck, Senior Projectleider ICT, Agentschap Zorg en Gezondheid MEDICATIESCHEL OP VITALINK BEKNOPTE INTRODUCTIE > Waarom? Voor het veilig delen van zorg
Projectoproep Kankerplan Actie 24 : Wetenschappelijke analyse in de onco-geriatrie
 B Projectoproep Kankerplan Actie 24 : Wetenschappelijke analyse in de onco-geriatrie Inleiding Deze projectoproep kadert binnen de verderzetting van Actie 24 van het Kankerplan: Steun aan pilootprojecten
B Projectoproep Kankerplan Actie 24 : Wetenschappelijke analyse in de onco-geriatrie Inleiding Deze projectoproep kadert binnen de verderzetting van Actie 24 van het Kankerplan: Steun aan pilootprojecten
Postdatum. Geachte Dokter,
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Quetiapine Krka 50 mg / 200 mg / 300 mg/400 mg tabletten met verlengde afgifte.
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Quetiapine Krka 50 mg / 200 mg / 300 mg/400 mg tabletten met verlengde afgifte.
Vectibix (panitumumab) Educatief materiaal voor de arts
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Vectibix. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Vectibix. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Datum 1 juli 2014 Onderwerp Beantwoording Kamervragen over het onderzoek naar het verband tussen medicijngebruik en agressie
 1 > Retouradres Postbus 20301 2500 EH Den Haag De Voorzitter van de Tweede Kamer der Staten-Generaal Postbus 20018 2500 EA DEN HAAG Turfmarkt 147 2511 DP Den Haag Postbus 20301 2500 EH Den Haag www.rijksoverheid.nl/venj
1 > Retouradres Postbus 20301 2500 EH Den Haag De Voorzitter van de Tweede Kamer der Staten-Generaal Postbus 20018 2500 EA DEN HAAG Turfmarkt 147 2511 DP Den Haag Postbus 20301 2500 EH Den Haag www.rijksoverheid.nl/venj
Procedure voor de verwerking van een aanvraag tot onderzoek
 Procedure voor de verwerking van een aanvraag tot onderzoek A Doel De doelstelling van deze procedure is het waarborgen van een standaardverloop bij aanvragen tot het uitvoeren van wetenschappelijk onderzoek
Procedure voor de verwerking van een aanvraag tot onderzoek A Doel De doelstelling van deze procedure is het waarborgen van een standaardverloop bij aanvragen tot het uitvoeren van wetenschappelijk onderzoek
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen. Farmaceutische Bedrijven Deelteam Klinisch Onderzoek
 Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Farmaceutische Bedrijven Deelteam Klinisch Onderzoek Toezicht op klinisch onderzoek bij STZ-ziekenhuizen Bevindingen vanuit de praktijk Conclusies en
9. Farmaceutische zorg en farmaceutisch dossier
 INFO-FICHE - KB 2009 9. Farmaceutische zorg en farmaceutisch dossier 1. BEGRIP De farmaceutische zorg is sinds 1 mei 2006 door de wetgever erkend als een kerntaak van de apotheker: als geneesmiddelenexpert
INFO-FICHE - KB 2009 9. Farmaceutische zorg en farmaceutisch dossier 1. BEGRIP De farmaceutische zorg is sinds 1 mei 2006 door de wetgever erkend als een kerntaak van de apotheker: als geneesmiddelenexpert
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Ferrum-Homaccord; Druppels voor oraal gebruik, oplossing 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 100 g oplossing bevat:
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Ferrum-Homaccord; Druppels voor oraal gebruik, oplossing 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 100 g oplossing bevat:
BOTOX (botulinum toxine type A) Educatieve brochure voor artsen. 100 Allerganeenheden Poeder voor oplossing voor injectie
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel BOTOX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel BOTOX. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Deelnemen aan een klinische studie
 Deelnemen aan een klinische studie Informatiebrochure 1. Klinische studies... 4 1.1 Wat en waarom?... 4 1.2 Academische en commerciële studies... 5 1.3 Onderzoek in vier fasen... 6 1.4 Wetgeving... 7
Deelnemen aan een klinische studie Informatiebrochure 1. Klinische studies... 4 1.1 Wat en waarom?... 4 1.2 Academische en commerciële studies... 5 1.3 Onderzoek in vier fasen... 6 1.4 Wetgeving... 7
Na consultatie herziene vertaling van de QRD-template
 Na consultatie herziene vertaling van de QRD-template Deelrapport voortkomend uit het adviestraject Het verbeteren van de begrijpelijkheid van patiëntenbijsluiters 10 juli 2009 Dr. Leo Lentz UiL-OTS Universiteit
Na consultatie herziene vertaling van de QRD-template Deelrapport voortkomend uit het adviestraject Het verbeteren van de begrijpelijkheid van patiëntenbijsluiters 10 juli 2009 Dr. Leo Lentz UiL-OTS Universiteit
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Hepeel; Tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 tablet (301,5 mg) bevat: Colocynthis D6 90 mg Veratrum album
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Hepeel; Tabletten 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 1 tablet (301,5 mg) bevat: Colocynthis D6 90 mg Veratrum album
Canestene Intim 1. NAAM VAN HET GENEESMIDDEL 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 3. FARMACEUTISCHE VORM 4. KLINISCHE GEGEVENS
 Canestene Intim 1. NAAM VAN HET GENEESMIDDEL Canestene Intim 1% crème 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Werkzame stof: Clotrimazole 1% Hulpstof(fen) met bekend effect: Cetylstearylalcohol
Canestene Intim 1. NAAM VAN HET GENEESMIDDEL Canestene Intim 1% crème 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Werkzame stof: Clotrimazole 1% Hulpstof(fen) met bekend effect: Cetylstearylalcohol
Intern kwaliteitscharter
 Intern kwaliteitscharter Ons intern kwaliteitscharter is samen met het kwaliteitscharter van Federgon (zie volgende pagina) een instrument om de kwaliteit van onze dienstverlening te waarborgen. Al onze
Intern kwaliteitscharter Ons intern kwaliteitscharter is samen met het kwaliteitscharter van Federgon (zie volgende pagina) een instrument om de kwaliteit van onze dienstverlening te waarborgen. Al onze
VALDOXAN. (agomelatine) Informatie voor beroepsbeoefenaren in de gezondheidszorg: Aanbevelingen met betrekking tot:
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Valdoxan 25 mg. Het verplicht plan voor risicobeperking in België, waarvan deze
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel Valdoxan 25 mg. Het verplicht plan voor risicobeperking in België, waarvan deze
FOD VOLKSGEZONDHEID, Brussel, 11/06/2009 VEILIGHEID VAN DE VOEDSELKETEN EN LEEFMILIEU
 FOD VOLKSGEZONDHEID, Brussel, 11/06/2009 VEILIGHEID VAN DE VOEDSELKETEN EN LEEFMILIEU DIRECTORAAT-GENERAAL ORGANISATIE VAN DE GEZONDHEIDSZORGVOORZIENINGEN NATIONALE RAAD VOOR ZIEKENHUISVOORZIENINGEN --------
FOD VOLKSGEZONDHEID, Brussel, 11/06/2009 VEILIGHEID VAN DE VOEDSELKETEN EN LEEFMILIEU DIRECTORAAT-GENERAAL ORGANISATIE VAN DE GEZONDHEIDSZORGVOORZIENINGEN NATIONALE RAAD VOOR ZIEKENHUISVOORZIENINGEN --------
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Oculo-Heel; Oogdruppels, oplossing 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Oculo-Heel bevat per monodosis van 0,45 ml
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Oculo-Heel; Oogdruppels, oplossing 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Oculo-Heel bevat per monodosis van 0,45 ml
1. Aangepaste bedragen of percentages van een aantal retributies en contributies
 Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten Eurostation II - Victor Hortaplein 40/40 1060 BRUSSEL www.fagg.be Transversale Ondersteuning/afdeling Budget & Beheerscontrole Afdeling Budget
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten Eurostation II - Victor Hortaplein 40/40 1060 BRUSSEL www.fagg.be Transversale Ondersteuning/afdeling Budget & Beheerscontrole Afdeling Budget
worden en hoe deze methode toegepast kan worden om de veiligheid van geneesmiddelen te bewaken.
 Samenvatting Geneesmiddelen worden toegepast om ziektes te behandelen, te voorkomen en te diagnosticeren. In sommige gevallen ervaart de patiënt niet alleen het gewenste effect, maar kunnen ook ongewenste
Samenvatting Geneesmiddelen worden toegepast om ziektes te behandelen, te voorkomen en te diagnosticeren. In sommige gevallen ervaart de patiënt niet alleen het gewenste effect, maar kunnen ook ongewenste
DEELNAME AAN EEN KLINISCHE STUDIE
 DEELNAME AAN EEN KLINISCHE STUDIE MB2948 Brochure: Klinische studies l Ziekenhuis Oost-Limburg 1 WELKOM U kreeg deze brochure omdat u meer wilt weten over klinische studies. We informeren u daarom over
DEELNAME AAN EEN KLINISCHE STUDIE MB2948 Brochure: Klinische studies l Ziekenhuis Oost-Limburg 1 WELKOM U kreeg deze brochure omdat u meer wilt weten over klinische studies. We informeren u daarom over
Handleiding voor zorgverleners
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel Toujeo. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in handel brengen van het geneesmiddel Toujeo. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Belangrijke informatie voor zorgverleners over de nieuwe formulering van FLOLAN
 De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Belgische gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel FLOLAN. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
SAMENVATTING VAN DE PRODUCTKENMERKEN
 1. NAAM VAN HET GENEESMIDDEL Sedistress 100 harde capsules. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Iedere capsule bevat 100 mg zuiver droog extract van de bovengrondse delen van Passiflora incarnata
1. NAAM VAN HET GENEESMIDDEL Sedistress 100 harde capsules. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Iedere capsule bevat 100 mg zuiver droog extract van de bovengrondse delen van Passiflora incarnata
Wet van 13 maart 2016 op het statuut van en het toezicht op de verzekerings- of herverzekeringsondernemingen, de artikelen 107 tot 122.
 de Berlaimontlaan 14 BE-1000 Brussel tel. +32 2 221 35 88 fax + 32 2 221 31 04 ondernemingsnummer: 0203.201.340 RPR Brussel www.nbb.be Mededeling Brussel, 2 juni 2017 Kenmerk: NBB_2017_18 uw correspondent:
de Berlaimontlaan 14 BE-1000 Brussel tel. +32 2 221 35 88 fax + 32 2 221 31 04 ondernemingsnummer: 0203.201.340 RPR Brussel www.nbb.be Mededeling Brussel, 2 juni 2017 Kenmerk: NBB_2017_18 uw correspondent:
Educatief materiaal. EFIENT (Prasugrel) Dit geneesmiddel is onderworpen aan aanvullende monitoring.
 De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel EFIENT. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
De Europese gezondheidsautoriteiten hebben bepaalde voorwaarden verbonden aan het in de handel brengen van het geneesmiddel EFIENT. Het verplicht plan voor risicobeperking in België, waarvan deze informatie
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten (FAGG)
 Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten (FAGG) Wet van 19 december 2008 inzake het verkrijgen en het gebruik van menselijk lichaamsmateriaal met het oog op de geneeskundige toepassing
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten (FAGG) Wet van 19 december 2008 inzake het verkrijgen en het gebruik van menselijk lichaamsmateriaal met het oog op de geneeskundige toepassing
Wat is een klinische studie?
 Wat is een klinische studie? Klinische studies Klinische studies Klinische studies worden verricht om de werkzaamheid van geneesmiddelen alsook combinaties van verschillende behandelingen te testen. Klinische
Wat is een klinische studie? Klinische studies Klinische studies Klinische studies worden verricht om de werkzaamheid van geneesmiddelen alsook combinaties van verschillende behandelingen te testen. Klinische
Actieplan 2009 / 2010 Vraag- en antwoorddocument
 Actieplan 2009 / 2010 Vraag- en antwoorddocument 28/01/2009 Page 1 sur 7 Inactivatie 1. Welk e-mailadres gebruikt het FAGG om ontbrekende documenten op te vragen die noodzakelijk zijn voor de administratieve
Actieplan 2009 / 2010 Vraag- en antwoorddocument 28/01/2009 Page 1 sur 7 Inactivatie 1. Welk e-mailadres gebruikt het FAGG om ontbrekende documenten op te vragen die noodzakelijk zijn voor de administratieve
BIJLAGE VOORWAARDEN OF BEPERKINGEN MET BETREKKING TOT EEN VEILIG EN DOELTREFFEND GEBRUIK VAN HET GENEESMIDDEL TER IMPLEMENTATIE DOOR DE LIDSTATEN.
 BIJLAGE VOORWAARDEN OF BEPERKINGEN MET BETREKKING TOT EEN VEILIG EN DOELTREFFEND GEBRUIK VAN HET GENEESMIDDEL TER IMPLEMENTATIE DOOR DE LIDSTATEN. 1 De lidstaten moeten ervoor zorgen dat alle voorwaarden
BIJLAGE VOORWAARDEN OF BEPERKINGEN MET BETREKKING TOT EEN VEILIG EN DOELTREFFEND GEBRUIK VAN HET GENEESMIDDEL TER IMPLEMENTATIE DOOR DE LIDSTATEN. 1 De lidstaten moeten ervoor zorgen dat alle voorwaarden
Medisch Farmaceutisch Overleg
 Medisch Farmaceutisch Overleg Een MFO (medisch farmaceutisch overleg) wordt georganiseerd om de multidisciplinaire samenwerking tussen artsen en apothekers te stimuleren. Het belangrijkste doel is het
Medisch Farmaceutisch Overleg Een MFO (medisch farmaceutisch overleg) wordt georganiseerd om de multidisciplinaire samenwerking tussen artsen en apothekers te stimuleren. Het belangrijkste doel is het
Leidraad voor type II variaties met herziening van de rubrieken 4.6, 5.3 en 6.6 van de SKP
 Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten Leidraad voor type II variaties met herziening van de rubrieken 4.6, 5.3 en 6.6 van de SKP Inleiding Gezien de vaak terugkerende opmerkingen
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten Leidraad voor type II variaties met herziening van de rubrieken 4.6, 5.3 en 6.6 van de SKP Inleiding Gezien de vaak terugkerende opmerkingen
Sectoraal Comité van de Sociale Zekerheid en van de Gezondheid Afdeling «Sociale Zekerheid»
 Sectoraal Comité van de Sociale Zekerheid en van de Gezondheid Afdeling «Sociale Zekerheid» SCSZG/16/155 BERAADSLAGING NR. 16/070 VAN 5 JULI 2016 OVER DE UITWISSELING VAN PERSOONSGEGEVENS TUSSEN DE FEDERALE
Sectoraal Comité van de Sociale Zekerheid en van de Gezondheid Afdeling «Sociale Zekerheid» SCSZG/16/155 BERAADSLAGING NR. 16/070 VAN 5 JULI 2016 OVER DE UITWISSELING VAN PERSOONSGEGEVENS TUSSEN DE FEDERALE
Beleidsdocument: Herregistratie van geneesmiddelen voor humaan gebruik ingeschreven via de nationale procedure
 OLLEGE TER BEOORDELING VAN GENEESIDDELEN Beleidsdocument: Herregistratie van geneesmiddelen voor humaan gebruik ingeschreven via de nationale procedure EB 42 14 maart 2013 EB-42 Inhoudsopgave 1. Inleiding
OLLEGE TER BEOORDELING VAN GENEESIDDELEN Beleidsdocument: Herregistratie van geneesmiddelen voor humaan gebruik ingeschreven via de nationale procedure EB 42 14 maart 2013 EB-42 Inhoudsopgave 1. Inleiding
Basistekst. Niet-interventionele studies. Opzet van deze voordracht
 Niet-interventionele studies prof. dr. P. Cras Ethisch Comité UZA Opzet van deze voordracht FAQs bloemlezing uit de wetteksten aangeven waar er ruimte voor interpretatie is nadruk op nuttige termen en
Niet-interventionele studies prof. dr. P. Cras Ethisch Comité UZA Opzet van deze voordracht FAQs bloemlezing uit de wetteksten aangeven waar er ruimte voor interpretatie is nadruk op nuttige termen en
Sectoraal Comité van de Sociale Zekerheid en van de Gezondheid Afdeling «Gezondheid»
 Sectoraal Comité van de Sociale Zekerheid en van de Gezondheid Afdeling «Gezondheid» SCSZG/11/134 BERAADSLAGING NR 11/088 VAN 18 OKTOBER 2011 MET BETREKKING TOT DE NOTA BETREFFENDE DE ELEKTRONISCHE BEWIJSMIDDELEN
Sectoraal Comité van de Sociale Zekerheid en van de Gezondheid Afdeling «Gezondheid» SCSZG/11/134 BERAADSLAGING NR 11/088 VAN 18 OKTOBER 2011 MET BETREKKING TOT DE NOTA BETREFFENDE DE ELEKTRONISCHE BEWIJSMIDDELEN
Verzoek tot advies van de Commissie Medische Ethiek betreffende een klinische studie
 Titel van het onderzoek: EudraCT nummer, indien van toepassing: Arts-onderzoeker HHZH Lier + medische discipline: PI (Naam, adres, tel en e-mail): Sponsor (Naam, contactpersoon, adres, tel en e-mail):
Titel van het onderzoek: EudraCT nummer, indien van toepassing: Arts-onderzoeker HHZH Lier + medische discipline: PI (Naam, adres, tel en e-mail): Sponsor (Naam, contactpersoon, adres, tel en e-mail):
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN
 BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Nux vomica-homaccord; Druppels voor oraal gebruik, oplossing. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 100 g oplossing
BIJLAGE I SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL Nux vomica-homaccord; Druppels voor oraal gebruik, oplossing. 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING 100 g oplossing
SAMENVATTING VAN DE PRODUCTKENMERKEN
 SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL trianal vitis caps harde capsules 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke harde capsule bevat 300 mg Vitis vinifera L., folium
SAMENVATTING VAN DE PRODUCTKENMERKEN 1. NAAM VAN HET GENEESMIDDEL trianal vitis caps harde capsules 2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING Elke harde capsule bevat 300 mg Vitis vinifera L., folium
Studie namiddag Evidence Based Zorg
 Studie namiddag Evidence Based Zorg Ann Van den Bruel, MD PhD Clinical Lecturer, University of Oxford Huisarts Programma Ethische commissie Serious Gaming Recrutering Care4Safety Uitkomsten 1Heart2Care4
Studie namiddag Evidence Based Zorg Ann Van den Bruel, MD PhD Clinical Lecturer, University of Oxford Huisarts Programma Ethische commissie Serious Gaming Recrutering Care4Safety Uitkomsten 1Heart2Care4
AANVRAAGFORMULIER VOOR DE ACCREDITATIE VAN CERTIFICATIEDIENSTVERLENERS
 AANVRAAGFORMULIER VOOR DE ACCREDITATIE VAN CERTIFICATIEDIENSTVERLENERS INFORMATIE 1. Conform artikel 3, 1 van het koninklijk besluit van 6 december 2002 houdende de organisatie van de controle en de accreditatie
AANVRAAGFORMULIER VOOR DE ACCREDITATIE VAN CERTIFICATIEDIENSTVERLENERS INFORMATIE 1. Conform artikel 3, 1 van het koninklijk besluit van 6 december 2002 houdende de organisatie van de controle en de accreditatie
De aanstelling van de drie directeurs-generaal van het FAGG lanceert de implementatie van het nieuwe organogram
 21.01.2009 Uw geneesmiddelen en gezondheidsproducten, onze zorg Woordje van de Administrateur-generaal De aanstelling van de drie directeurs-generaal van het FAGG lanceert de implementatie van het nieuwe
21.01.2009 Uw geneesmiddelen en gezondheidsproducten, onze zorg Woordje van de Administrateur-generaal De aanstelling van de drie directeurs-generaal van het FAGG lanceert de implementatie van het nieuwe
BUURTINFORMATIENETWERKEN ZELFSTANDIGE ONDERNEMERS
 COD24_BROCH BlauwOK2deV_NL 26-09-2005 14:33 Page 1 BUURTINFORMATIENETWERKEN ZELFSTANDIGE ONDERNEMERS OPSTART - PROCEDURE Preventie ter bevordering van veiligheidsgevoel en sociale betrokkenheid Stap mee
COD24_BROCH BlauwOK2deV_NL 26-09-2005 14:33 Page 1 BUURTINFORMATIENETWERKEN ZELFSTANDIGE ONDERNEMERS OPSTART - PROCEDURE Preventie ter bevordering van veiligheidsgevoel en sociale betrokkenheid Stap mee
