INFORMATIE- EN TOESTEMMINGSFORMULIER
|
|
|
- Gerda de Koning
- 8 jaren geleden
- Aantal bezoeken:
Transcriptie
1 ID-nr. onderzoeksdeelnemer : INFORMATIE- EN TOESTEMMINGSFORMULIER Een fase 3b, prospectief, gerandomiseerd, open-label, geblindeerd evaluatieonderzoek (PROBE) ter beoordeling van de werkzaamheid en veiligheid van (LMW)-heparine/edoxaban versus dalteparine bij veneuze trombo-embolie gerelateerd aan kanker (DU176b-D-U311) Geachte mevrouw, mijnheer, U wordt uitgenodigd om deel te nemen aan een klinisch onderzoek. Om u te helpen besluiten of u wel of niet wilt deelnemen, is het belangrijk dat u begrijpt wat het onderzoek inhoudt en wat het voor u betekent. Om een geïnformeerd besluit over deelname te kunnen nemen, is het belangrijk dat u weet wat het doel, de procedures, de voordelen en risico's, de ongemakken en de genomen voorzorgsmaatregelen van het onderzoek zijn. Dit proces wordt geïnformeerde toestemming genoemd. Neem rustig de tijd om de volgende informatie zorgvuldig te lezen en met anderen te bespreken. Als iets niet duidelijk is of als u meer informatie wilt, kunt u altijd terecht bij uw onderzoeks-arts. Lees ook de algemene brochure. Deze brochure bevat veel algemene informatie over medisch onderzoek. Als u na het doorlezen van de informatie nog vragen hebt, kunt u deze stellen aan de onderzoeks-arts. U kunt ook contact opnemen met een onafhankelijke arts/deskundige die veel over het onderzoek weet. Alle contactgegevens staan vermeld in bijlage 2. Als u besluit deel te nemen aan dit onderzoek dient u het toestemmingsformulier te ondertekenen om aan te geven dat u de informatiebrief en alle bijlagen van dit document accepteert en ermee instemt. U krijgt een kopie van het ondertekende formulier mee om te bewaren. Het origineel blijft in het onderzoekscentrum. 1. WAT IS HET DOEL VAN HET ONDERZOEK? U wordt gevraagd deel te nemen aan dit wetenschappelijk onderzoek omdat u een bloedstolsel heeft in een ader die diep in uw been (diepe veneuze trombose of DVT) of in uw longen (longembolie of LE) ligt en die in verband wordt gebracht met uw kanker. Patiënten met kanker en DVT of LE worden doorgaans behandeld met een antistollend middel of bloedverdunner zoals dalteparine of een andere laag-moleculair-gewicht heparine (LMWH). Deze geneesmiddelen worden met onderhuidse injecties toegediend. De onderhuidse injecties zijn vaak moeilijk te verdragen en ongemakkelijk voor patiënten met kanker. Het doel van dit onderzoek is het vergelijken van edoxaban, een nieuw geneesmiddel, met de LMWH dalteparine voor de behandeling van DVT en LE bij deelnemers met kanker. Edoxaban is een geneesmiddel in tabletvorm. Wanneer edoxaban even veilig en effectief blijkt te zijn als LMWH, is dit een aantrekkelijk alternatief voor de behandeling van DVT en LE bij patiënten met kanker. Wereldwijd nemen er ongeveer deelnemers deel vanuit circa 130 onderzoekscentra. Om deel te kunnen nemen moet u minimaal 18 jaar zijn, gediagnosticeerd zijn met DVT of LE, en aan de onderzoeks-vereisten kunnen voldoen. Pagina 1 van 16
2 2. WELK ONDERZOEKSMIDDEL WORDT ONDERZOCHT? Het onderzoeksmiddel edoxaban is een product van Daiichi Sankyo. In het vervolg van dit toestemmingsformulier wordt Daiichi Sankyo de sponsor genoemd. Edoxaban is in de VS, Europa en Japan goedgekeurd door Gezondheidsautoriteiten voor de behandeling van patiënten met DVT en LE. Dalteparine is goedgekeurd door de Amerikaanse Food and Drug Administration (FDA) voor de behandeling van DVT en LE bij deelnemers met kanker. 3. HOE WORDT HET ONDERZOEK UITGEVOERD? Wanneer een arts vermoedt dat u DVT of een LE heeft, voert hij of zij bepaalde onderzoeken en procedures uit als onderdeel van uw medische zorg. De meeste onderzoeksprocedures waaraan u moet deelnemen in dit onderzoek worden uitgevoerd als onderdeel van uw gebruikelijke medische zorg. Als de informatie niet is verzameld als onderdeel van de gebruikelijke zorg, of als onderzoeken onvolledig waren of niet zijn uitgevoerd, dan moet dit alsnog gebeuren. Deze onderzoeken/procedures kunnen het volgende omvatten: diagnostische onderzoeken om te bevestigen dat u DVT of een LE heeft, beoordeling van eerdere en huidige medische aandoeningen en geneesmiddelen, bloedtesten (ongeveer 10 ml), lichamelijk onderzoek, bloeddruk, hartslag, lichaamsgewicht en -lengte, en beoordeling van uw kanker, medische en chirurgische voorgeschiedenis. Deze testen/procedures kunnen tijdens het onderzoek worden herhaald. In totaal wordt er tijdens het onderzoek 60 ml bloed afgenomen. Als er leverafwijkingen worden gevonden, dan kan het mogelijk zijn dat uw bloed ook getest wordt op hepatitis A, B, C en E, en wordt u geïnformeerd over het resultaat. Als u dit resultaat niet wilt krijgen, kunt u niet deelnemen aan dit onderzoek. Meer informatie over de onderzoeksbezoeken en de beoordelingen die tijdens elk bezoek worden uitgevoerd, vindt u in bijlage 3. Uw deelname aan het onderzoek duurt maximaal 12 maanden. U wordt willekeuring ingedeeld (zoals bij het opgooien van een munt. Dit proces heet randomisatie ) naar een van de volgende groepen: 1. Laagmoleculaire heparine (LMWH)/edoxaban-behandelgroep 2. Dalteparine-groep De helft van de deelnemers wordt toegewezen aan de LMWH/edoxaban-groep en de andere helft wordt toegewezen aan de dalteparine-groep. U heeft een gelijke kans (50%) op behandeling in elk van beide hieronder beschreven behandelgroepen. Laag-moleculaire-heparine (LMWH)/edoxaban-groep Als u wordt gerandomiseerd naar deze groep begint u met het gebruik van LMWH in de vorm van injecties onder de huid, een- of tweemaal daags gedurende circa de eerste vijf dagen van uw behandelingsperiode. Daarna stopt u met het gebruik van LMWH en begint u met het innemen van twee tabletten 30 mg edoxaban, eenmaal daags via de mond. Als u minder dan 60 kg weegt, een verminderde nierfunctie heeft of bepaalde geneesmiddelen gebruikt, dan neemt u één tablet 30 mg edoxaban in, eenmaal daags via de mond. Uw onderzoeks-arts zal de juiste dosis voor u bepalen. U blijft edoxaban maximaal 12 maanden innemen. Pagina 2 van 16
3 Dalteparine-groep Uw dagelijkse dosis dalteparine is afhankelijk van uw lichaamsgewicht. U begint met een hoge dosis dalteparine als een onderhuidse injectie eenmaal daags gedurende de eerste dertig dagen van uw behandelingsperiode. Daarna blijft u een lagere dosis dalteparine gebruiken in de vorm van een onderhuidse injectie eenmaal daags gedurende maximaal 12 maanden. De dosis dalteparine die u ontvangt kan worden gewijzigd op basis van bepaalde laboratoriumcriteria, waaronder uw bloedplaatjeswaarde. De dosis en duur van de behandeling worden bepaald door de onderzoeksarts in nauw overleg met uw behandelend arts. 4. WAT WORDT ER VAN U VERWACHT? Als u instemt met deelname aan dit onderzoek en u komt ervoor in aanmerking, dan vraagt het onderzoekspersoneel u om het volgende te doen: dit toestemmingsformulier ondertekenen; verstrekken van standaard demografische informatie, zoals leeftijd, geslacht en etniciteit; instructies opvolgen die u over het onderzoek krijgt; ons informeren als u de onderzoeksinstructies vergeet op te volgen of ervoor kiest deze niet op te volgen; ons informeren als u op enig moment wilt stoppen met deelname aan het onderzoek; het onderzoeksmiddel buiten bereik houden van kinderen of personen die het etiket niet kunnen lezen en begrijpen; activiteiten of contactsport vermijden die letsel zouden kunnen veroorzaken met bloeding tot gevolg. 5. WAARIN VERSCHILT DE ONDERZOEKSBEHANDELING VAN DE REGULIERE BEHANDELING(EN) DIE U KRIJGT? De meeste onderzoeksprocedures waaraan u moet deelnemen in dit onderzoek worden uitgevoerd als onderdeel van uw gebruikelijke medische zorg. Als de informatie niet is verzameld als onderdeel van de gebruikelijke zorg of als onderzoeken onvolledig waren of niet zijn uitgevoerd, dan moet dit alsnog gebeuren. 6. WAT ZIJN DE ANDERE MOGELIJKE BEHANDELINGEN? U hoeft niet deel te nemen aan dit onderzoek om medische zorg voor uw aandoening te krijgen. Deelname aan dit onderzoek is vrijwillig. Als u besluit niet deel te nemen aan dit onderzoek, heeft dit geen invloed op de medische zorg die u kunt krijgen. Er bestaan alternatieven voor deelname aan dit onderzoek, waaronder de standaardbehandeling voor DVT of LE met LMWH. U kunt deze alternatieven en de voordelen en risico's ervan met de onderzoeks-arts bespreken. Pagina 3 van 16
4 7. WELKE BIJWERKINGEN KUNT U VERWACHTEN? De bekende risico's of bijwerkingen gerelateerd aan het krijgen van antistollingsmiddelen (of bloedverdunners) zoals edoxaban, LMWH inclusief dalteparine zijn: opnieuw optreden van een DVT of LE en bloedingen, die kunnen leiden tot blauwe plekken, duizeligheid, zich licht in het hoofd voelen, zwakheid, vermoeidheid, onverklaarbare pijn of zwelling, en die zelfs dodelijk kunnen zijn wanneer de bloeding ernstig is. Na behandeling met edoxaban, LMWH inclusief dalteparine, zijn ook veranderingen in leverbloedtesten waargenomen met mogelijk misselijkheid, braken, buikpijn, vermoeidheid, verlies van eetlust, donkere urine, of gele huid of ogen tot gevolg. Meer specifiek: De bekende risico's of bijwerkingen gerelateerd aan het gebruik van het antistollend middel edoxaban zijn bloedingen en veranderingen in leverbloedtesten. Andere bijwerkingen zijn anemie (weinig rode bloedcellen) en uitslag. Veranderingen in bloedtesten en leverfunctietesten zijn waargenomen bij sommige deelnemers die met edoxaban werden behandeld. Deze veranderingen waren mild en gingen meestal over wanneer de patiënt geen andere leverziekte had, zoals besmettelijke hepatitis. Behandeling met dit onderzoeksmiddel edoxaban kan ook risico's met zich meebrengen voor uw toekomstige gezondheid waarvan we nu nog niets weten. Over deze mogelijke risico s zal u worden geïnformeerd zodra deze informatie beschikbaar is. De vaakst voorkomende bijwerking die in verband wordt gebracht met het gebruik van laagmoleculaire heparine (LMWH) waaronder dalteparine zijn wederom bloedingen en ook veranderingen in leverfunctietesten. Deze veranderingen waren mild en gingen meestal over wanneer de deelnemers geen andere leverziekte hadden, zoals besmettelijke hepatitis. Andere bijwerkingen zijn verminderde bloedplaatjes die in verband kunnen worden gebracht met nieuwe bloedstolselvorming, koorts, misselijkheid, anemie, zwelling en allergische reacties. LMWH kan ook pijn, irritatie, roodheid en afstervende huid op de injectieplaats veroorzaken. Raadpleeg bijlage 4 voor meer informatie over mogelijke bijwerkingen van de behandeling. Als u een van deze bijwerkingen ervaart (of andere die niet genoemd staan) of als u denkt dat u een bijwerking ervaart tijdens dit onderzoek, meld dit dan onmiddellijk aan uw onderzoeks-arts. Soms reageren mensen allergisch op geneesmiddelen. Een ernstige allergische reactie kan levensbedreigend zijn. Bijwerkingen of andere gezondheidsproblemen die optreden tijdens het onderzoek worden opgevolgd door de onderzoeks-arts. Edoxaban is niet getest op zwangere vrouwen of vrouwen die borstvoeding geven. De gevolgen van dit geneesmiddel op een ongeboren menselijke baby of een kind dat borstvoeding krijgt, zijn onbekend. Indien u tijdens het onderzoek of binnen 30 dagen nadat u bent gestopt met het onderzoeksmiddel zwanger wordt, moet u de onderzoeks-arts of het onderzoekspersoneel onmiddellijk informeren. Pagina 4 van 16
5 8. WAT ZIJN MOGELIJKE VOOR- EN NADELEN VAN DEELNAME AAN DIT ONDERZOEK? Als u besluit deel te nemen aan dit wetenschappelijk onderzoek, is er geen garantie dat er voor u enig voordeel is. Uw toestand kan verslechteren of verbeteren. Er is nu mogelijk geen voordeel voor u, maar andere mensen nu of in de toekomst kunnen baat hebben bij informatie uit dit onderzoek. De resultaten van dit onderzoek kunnen helpen bepalen welke behandelingen voor DVT of een LE veilig en/of effectief zijn bij patiënten met kanker. Dit onderzoek kan aanleiding geven tot nieuwe of betere behandelingen met geneesmiddelen. 9. WAT GEBEURT ER ALS U NIET WENST DEEL TE NEMEN AAN DIT ONDERZOEK? U beslist zelf of u meedoet aan dit onderzoek. Deelname is vrijwillig. Als u besluit niet deel te nemen, hoeft u niets te doen. U hoeft niets te ondertekenen. U hoeft ook niet te zeggen waarom u niet wilt deelnemen. Als u een patiënt bent, krijgt u de behandeling die u anders ook zou hebben gekregen. Niet deelnemen heeft geen consequenties voor u. Ook als u wel deelneemt, kunt u altijd van gedachten veranderen en u terugtrekken zonder een reden op te geven, zonder dat dit consequenties heeft voor u of uw verdere behandeling. Als u besluit te stoppen met deelname aan dit onderzoek, moet u allereerst onmiddellijk de onderzoeks-arts informeren. Hij/zij regelt zonodig uw verdere medische zorg. Wanneer u stopt met deelname aan het onderzoek, wordt u gevraagd terug te komen voor een laatste veiligheidsbeoordeling. Bij dit laatste bezoek wordt uw medische aandoening gecontroleerd en worden de laatste vereiste onderzoeksprocedures uitgevoerd. Voor uw eigen veiligheid moet u deze procedures doorlopen als u het onderzoek verlaat. Deze procedures staan vermeld in de sectie Einde van het onderzoek. U wordt gevolgd voor de volledige duur van dit onderzoek, zo lang als u personeel van het onderzoekscentrum toestaat persoonlijk of telefonisch contact met u op te nemen. Voor het onderzoek is het van belang dat uw gegevens verzameld worden tot het einde van de studie (dwz tot 12 maanden na inclusie), ook als u gestopt zou zijn met het onderzoeksmiddel. Indien dit gebeurt zal er met u besproken worden hoe het verdere contact zal verlopen: of u toestemming geeft om contact op te nemen per telefoon met uzelf of uw familie of met uw huisarts en of er toestemming is om de gegevens uit uw ziekenhuisdossier of bij de huisarts op te vragen. Wanneer u dit niet wenst stopt uw deelname aan het onderzoek volledig en dit wordt genoteerd. Informatie die is verzameld voordat u uw goedkeuring intrekt kan toch worden gebruikt in het onderzoek en met anderen worden gedeeld. Als u zich heeft teruggetrokken uit dit wetenschappelijk onderzoek, bespreek dan met uw onderzoeks-arts of u wilt dat uw resterende afgenomen lichaamsmateriaal wordt bewaard of vernietigd. Dit kan bloed of ander lichaamsmateriaal zijn dat bij u is afgenomen tijdens het onderzoek. U kunt ook vragen om het resterende lichaamsmateriaal op enig moment op een later tijdstip te laten vernietigen. Testresultaten die zijn verzameld voordat u vraagt om uw lichaamsmateriaal te laten vernietigen, blijven deel uitmaken van de onderzoeksresultaten. 10. WAT GEBEURT ER ALS HET ONDERZOEK IS AFGELOPEN? Er is geen garantie dat u dit specifieke geneesmiddel of deze specifieke behandeling blijft ontvangen wanneer uw deelname aan het onderzoek is beëindigd. Pagina 5 van 16
6 Voor de zorg die u ontvangt nadat het onderzoek is beëindigd, kan een ander geneesmiddel of andere behandeling nodig zijn. Het ziekenhuis bepaalt dan samen met uw onderzoeks-arts wat het meest geschikte alternatief is. Uw onderzoeks-arts of de opdrachtgever kan uw deelname aan dit onderzoek op ieder moment beëindigen. Dit kan gebeuren als u de instructies van de onderzoeks-arts niet opvolgt. Het kan ook gebeuren als de onderzoeks-arts denkt dat dit in uw belang is. Het onderzoek kan ook worden gestopt om organisatorische, medische of andere redenen door de onderzoeks-arts, de sponsor, de FDA of andere gezondheidszorgautoriteiten. Zodra u niet meer deelneemt aan het onderzoek, heeft u geen toegang meer tot het onderzoeksmiddel of de onderzoeksprocedures. Als het onderzoek wordt stopgezet, wordt u geïnformeerd en uw onderzoeks-arts zorgt voor de continuïteit van uw zorg. Nadat u bent gestopt met het gebruik van het onderzoeksmiddel, kunt u worden gevraagd deel te nemen aan opvolging na het onderzoek. Hiervoor kunnen bezoeken aan de arts of telefonische opvolging nodig zijn. U heeft het recht om te weigeren of te stoppen met deelname aan deze opvolging na het onderzoek zonder dat dit consequenties heeft voor u. 11. BENT U VERZEKERD WANNEER U AAN HET ONDERZOEK MEEDOET? Voor iedereen die meedoet aan dit onderzoek is een verzekering afgesloten. Deze verzekeringspolis dekt schade als gevolg van het onderzoek. Dit geldt voor schade die tot uiting komt tijdens het onderzoek of binnen vier jaar na afloop van het onderzoek. In bijlage 5 vindt u de verzekerde bedragen, de uitzonderingen en de adresgegevens van de verzekeraar. 12. WORDT U GEÏNFORMEERD ALS ER TUSSENTIJDS VOOR U RELEVANTE INFORMATIE OVER HET ONDERZOEK BEKEND WORDT? Soms komt er nieuwe informatie beschikbaar over het onderzoeksmiddel of de ziekte. U wordt geïnformeerd als er relevante nieuwe informatie beschikbaar komt die uw bereidheid om aan het onderzoek te blijven deelnemen kan beïnvloeden. Als dit gebeurt, neemt uw onderzoeks-arts zo spoedig mogelijk contact met u op en bespreekt of u aan het onderzoek moet blijven deelnemen. Als u besluit niet verder te gaan, regelt uw onderzoeks-arts de continuïteit van uw zorg. Als u besluit met het onderzoek door te gaan, kunt u worden gevraagd een nieuw toestemmingsformulier te ondertekenen. Als nieuwe informatie beschikbaar komt, kan uw onderzoeks-arts ook zonder uw toestemming uw deelname stopzetten als dit in uw belang is. Als dit gebeurt, worden de redenen uitgelegd en wordt de continuïteit van uw zorg geregeld. 13. WAT GEBEURT ER MET UW GEGEVENS EN LICHAAMSMATERIAAL? Gegevens en informatie De onderzoeks-arts en het onderzoeksteam verzamelen informatie over u, leggen deze vast en gebruiken deze voor onderzoeksdoeleinden. De informatie die tijdens het onderzoek over u wordt verzameld, kan gevoelige informatie bevatten over uw fysieke en mentale gezondheid of aandoening, uw ras en etniciteit en gezondheidsinformatie over u uit uw medische dossiers. Alle informatie die verzameld wordt tijdens de onderzoeksperiode, wordt vertrouwelijk behandeld in overeenstemming met de richtlijn inzake gegevensbescherming van de Europese Unie en de Wet bescherming persoonsgegevens. Dossiers aan de hand waarvan uw identiteit kan worden vastgesteld, worden, voor zover toegestaan door wet- en/of regelgeving, niet openbaar gemaakt. Pagina 6 van 16
7 De monitor(en), auditor(en), de ethische commissie en regelgevende autoriteit(en), waaronder de Inspectie voor de Gezondheidszorg krijgen rechtstreeks toegang tot uw originele medische dossiers (waarin ook persoonlijke informatie zoals uw naam, adres, telefoonnummer, geboortedatum en geslacht staan genoteerd) ter verificatie van klinische onderzoeksprocedures en/of -gegevens, voor zover toegestaan door wetten en/of regelgeving, zonder uw vertrouwelijkheid te schenden. Door het tekenen van het toestemmingsformulier geeft u toestemming voor een dergelijke toegang. Alle over u verzamelde onderzoeksgerelateerde informatie die het onderzoekscentrum verlaat, wordt middels een code geïdentificeerd (zonder gebruik van geboortedatum en initialen). Alle verzamelde gegevens worden tot 15 jaar na het afsluiten van het onderzoek bewaard en zijn toegankelijk voor: - desbetreffende overheidsinstanties, waaronder de Inspectie voor de Gezondheidszorg; - de ethische commissie; - de sponsor; - de vertegenwoordiger van de sponsor. Een lijst waarin uw identiteit is gekoppeld aan uw code wordt door het onderzoeksteam gedurende 15 jaar op de onderzoekslocatie bewaard. De onderzoeker is verantwoordelijk voor het bewaren ervan en beheert de toegang tot de lijst. Door het ondertekenen van dit toestemmingsformulier geeft u toestemming voor het verwerken en gebruiken van uw informatie voor dit onderzoek door de sponsor, Daiichi Sankyo Pharma Development en de vertegenwoordiger(s) van de sponsor, waaronder Quintiles en ITREAS. U geeft ook toestemming dat uw informatie of delen daarvan worden verwerkt of verstuurd naar personen en organisaties buiten uw land, waar wetten inzake gegevensbescherming minder streng kunnen zijn en waar we niet hetzelfde niveau van vertrouwelijkheid kunnen garanderen. U heeft het recht de over u verzamelde informatie in te zien, te corrigeren of te laten verwijderen. U kunt bij uw onderzoeks-arts bezwaar aantekenen tegen de verdere verwerking van uw informatie. Lichaamsmateriaal Uw lichaamsmateriaal (bloed) kan tot het einde van het onderzoek (december 2017) voor onderzoeksdoeleinden worden bewaard, waarna het wordt vernietigd. De resultaten van dit onderzoek worden gebruikt voor het nemen van geïnformeerde klinische besluiten inzake de ontwikkeling van dit nieuwe geneesmiddel. Als u wilt dat de resultaten beschikbaar worden gesteld aan u, neem dan contact op met uw onderzoeks-arts. Een beschrijving van dit klinische onderzoek is beschikbaar op zoals vereist door Amerikaanse wetgeving. Deze website bevat geen informatie waaruit uw identiteit kan worden opgemaakt. De website bevat hoogstens een samenvatting van de resultaten. U kunt deze website te allen tijde doorzoeken. Als de resultaten van het onderzoek worden gepubliceerd, wordt uw identiteit vertrouwelijk gehouden. Pagina 7 van 16
8 14. WORDT UW HUISARTS EN/OF BEHANDELEND SPECIALIST GEÏNFORMEERD OVER UW DEELNAME? Als u besluit deel te nemen aan dit onderzoek worden uw huisarts en behandelend specialist (indien van toepassing) geïnformeerd over uw deelname aan het onderzoek, en hij/zij kan gegevens over uw medische voorgeschiedenis aan de onderzoeks-arts of het onderzoekspersoneel verstrekken. 15. ZIJN ER EXTRA KOSTEN/IS ER EEN VERGOEDING WANNEER U BESLUIT AAN DIT ONDERZOEK MEE TE DOEN? U hoeft niet te betalen voor de onderzoeksmiddelen of voor gerelateerde testen en kliniekbezoeken die specifiek voor dit onderzoek plaatsvinden. Er kunnen enkele testen en procedures zijn die de onderzoeks-arts als standaardzorg beschouwt (dat wil zeggen dat u deze zorg zou krijgen ongeacht of u aan dit onderzoek deelneemt). Deze testen en procedures worden bij u en/of uw verzekeringsmaatschappij in rekening gebracht. U ontvangt een vergoeding voor de gemaakte reiskosten terwijl u aan het onderzoek deelneemt. Het onderzoek heeft geen invloed op uw recht op noodhulp en/of andere medische diensten, indien deze nodig zijn. De sponsor betaalt redelijke medische kosten die hoger zijn dan het bedrag dat uw verzekering betaalt voor letsel dat rechtstreeks het gevolg is van het onderzoek. Het bedrag van deze betaling kan variëren, afhankelijk van de details van uw casus. Aanvullende betalingen (zoals voor loonschade of immateriële schade) zijn niet beschikbaar. 16. WELKE MEDISCH-ETHISCHE TOETSINGSCOMMISSIE HEEFT DIT ONDERZOEK GOEDGEKEURD? De ethische toetsingscommissie van het Academisch Medisch Centrum (AMC) heeft dit onderzoek goedgekeurd. U vindt meer informatie over het goedkeuringsproces in de algemene brochure. 17. WILT U VERDER NOG IETS WETEN? Voor vragen, twijfels of klachten over welk deel van dit onderzoek dan ook, kunt u contact opnemen met het onderzoeksteam, een onafhankelijke arts/deskundige of een onafhankelijke klachtencommissie. U vindt de contactgegevens in bijlage 2. BIJLAGEN Bijlage 1: Toestemmingsformulier Bijlage 2: Contactgegevens Bijlage 3: Mogelijke testen/procedures voor elk onderzoeksbezoek Bijlage 4: Mogelijke bijwerkingen, risico's en ongemakken Bijlage 5: Verzekering Algemene brochure medisch-wetenschappelijk onderzoek Pagina 8 van 16
9 Hartelijk dank voor het lezen van deze informatiebrief en de bijbehorende bijlagen, en voor het overwegen of u aan dit onderzoek wilt deelnemen. Pagina 9 van 16
10 BIJLAGE 1: Toestemmingsformulier Titel van het onderzoek: Een fase 3b, prospectief, gerandomiseerd, open-label, geblindeerd evaluatieonderzoek (PROBE) ter beoordeling van de werkzaamheid en veiligheid van (LMW)- heparine/edoxaban versus dalteparine bij veneuze trombo-embolie gerelateerd aan kanker Onderzoeksprotocol: DU176b-D-U311 Ik bevestig het volgende: Ik heb de informatiebrief voor de deelnemer gelezen. Ik kon aanvullende vragen stellen. Mijn vragen zijn voldoende beantwoord. Ik begrijp de procedure die voor dit onderzoek wordt uitgevoerd. Ik had genoeg tijd om te beslissen of ik meedoe. Ik weet dat meedoen geheel vrijwillig is. Ik weet dat ik op ieder moment kan beslissen om toch niet mee te doen, zonder dat dit invloed heeft op mijn medische zorg of rechten. Daarvoor hoef ik geen reden te geven. Ik geef toestemming om mijn huisarts en de specialist(en) die mij behandelt(/behandelen) te vertellen dat ik meedoe aan dit onderzoek en dat zij medische informatie over mij mogen verstrekken. Ik weet dat sommige mensen mijn gegevens en medische dossiers kunnen inzien. Deze mensen staan vermeld in deze informatiebrief en in de algemene brochure. Ik geef toestemming om mijn gegevens te gebruiken voor de doelen die in de informatiebrief staan. Ik geef toestemming dat mijn persoonlijke informatie die wordt verzameld als onderdeel van dit klinisch onderzoek kan worden overgedragen aan andere landen buiten de EU, waar de wetgeving met betrekking tot bescherming van de persoonsgegevens minder streng kan zijn. Ik geef toestemming voor het verzamelen en gebruik van gegevens met betrekking tot mijn ras en etnische afkomst voor de doelen die worden omschreven in de informatiebrief. Ik geef toestemming om mijn onderzoeksgegevens tot 15 jaar na afloop van dit onderzoek te bewaren Ik ga ermee akkoord dat mijn lichaamsmateriaal wordt afgenomen en gebruikt zoals beschreven in deze informatiebrief. Ik geef toestemming om mijn lichaamsmateriaal te bewaren tot de afronding van dit onderzoek. Ik begrijp dat er mogelijk een hepatitis A-, B-, C- en E-test gedaan wordt en dat ik geïnformeerd wordt over het resultaat/de resultaten. Ik begrijp dat er op een later tijdstip contact met mij kan worden opgenomen voor mijn toestemming in verband met een opvolgingsonderzoek of een gerelateerd subonderzoek. Ik begrijp dat mijn deelname vertrouwelijk is. Ik wil deelnemen aan dit onderzoek. Pagina 10 van 16
11 Door dit document te ondertekenen stem ik in met deelname aan dit onderzoek, zoals beschreven in dit informatie- en toestemmingsformulier en ik krijg een kopie van dit ondertekende en gedateerde toestemmingsformulier. Naam deelnemer Handtekening deelnemer Datum Onderzoeker/geautoriseerd afgevaardigde*: Ik heb het onderzoek volledig en zorgvuldig toegelicht aan de hierboven genoemde persoon en ik bevestig dat hij/zij, voor zover ik weet, de aard, de risico s en de voordelen van deelname aan dit onderzoek duidelijk begrijpt. Ik bevestig dat ik hem/haar alle gelegenheid heb geboden om vragen te stellen over het onderzoek en dat ik alle vragen die hij/zij stelde correct en naar beste vermogen heb beantwoord. Ik bevestig dat hij/zij niet is gedwongen om toestemming te verlenen en dat hij/zij zijn/haar toestemming vrijwillig heeft gegeven. Ik bevestig dat hij/zij een ondertekende kopie ontvangt van deze informatiebrief en dit toestemmingsformulier. * Een geautoriseerde afgevaardigde is een arts of verpleegkundige die toestemming heeft van de hoofdonderzoeker om de patiënt te informeren over het onderzoek en om het toestemmingsformulier te ondertekenen. Onderzoeksarts (of afgevaardigde) (in blokletters) Handtekening Datum (moet dezelfde zijn als die van deelnemer) Pagina 11 van 16
12 BIJLAGE 2: Contactgegevens Als u vragen hebt over het onderzoek, over uw rechten als deelnemer of als u vragen hebt met betrekking tot letsel dat u hebt opgelopen in verband met het onderzoek, kunt u contact opnemen met: Prof. Dr. K. Meijer op telefoonnummer Voor meer informatie en/of advies over deelname aan het onderzoek kunt u ook contact opnemen met een onafhankelijke arts/deskundige die niet betrokken is bij het onderzoek, maar die een expert is op het gebied van het onderzoek. Ook als u vragen heeft met betrekking tot het onderzoek die u liever niet aan de onderzoekers stelt, kunt u deze onafhankelijke arts/deskundige raadplegen: Dr M. R. de Groot op telefoonnummer Als u niet tevreden bent over het onderzoek of de behandeling dan kunt u contact opnemen met de onafhankelijke klachtencommissie van het UMCG. Tijdens kantooruren kunt u met hen contact opnemen via telefoonnummer (050) Bent u in het ziekenhuis, dan kunt u een gesprek aanvragen bij de informatiebalie in de ontvangsthal van het UMCG. Een medewerker van Klachtopvang staat u dan zo snel mogelijk te woord. Pagina 12 van 16
13 BIJLAGE 3: Mogelijke testen/procedures bij elk onderzoeksbezoek Behandelingsperiode Op uw eerste dag van behandeling worden uw bloeddruk, hartslag en lichaamsgewicht gemeten. Er worden bloedtesten gedaan om te controleren of het veilig is onderzoeksmiddel toe te dienen. Er wordt extra bloed bij u afgenomen en in het laboratorium bewaard. Dit extra bloed wordt alleen gebruikt indien u een onverwachte complicatie heeft tijdens het onderzoek en baseline-informatie nodig is (zodat we de informatie kunnen vergelijken). U wordt verteld hoe en wanneer u het onderzoeksmiddel moet innemen. Dit staat beschreven in een patiëntenbrochure die aan u wordt verstrekt. U krijgt minimaal eens per 3 maanden een voorraad onderzoeksmiddel. Neem alle gebruikte en ongebruikte verpakkingen van het onderzoeksmiddel of spuiten mee terug bij elk beoordeling in het ziekenhuis zodat we er zeker van kunnen zijn dat u het onderzoeksmiddel juist inneemt. Onderzoeksbezoeken U moet op dag 31 naar het ziekenhuis komen zodat uw arts uw veiligheid kan controleren, uw geneesmiddelen kan noteren en kan beoordelen of u het onderzoeksmiddel juist inneemt. Zolang u het onderzoeksmiddel gebruikt, vindt er minimaal eens per 3 maanden een beoordeling in het ziekenhuis plaats. Tijdens deze beoordelingsbezoeken wordt er bloed bij u afgenomen, controleert uw arts uw veiligheid, noteert uw geneesmiddelen en beoordeelt of u het onderzoeksmiddel juist inneemt. U krijgt dan ook een nieuwe voorraad onderzoeksmiddel. Uw voorraad onderzoeksmiddel is voldoende voor 3 maanden of tot uw volgende bezoek aan het ziekenhuis. Deze tabel laat zien welke onderzoeken en procedures plaatsvinden tijdens uw bezoeken aan het ziekenhuis. Procedure Bij welk bezoek aan het ziekenhuis wordt deze procedure uitgevoerd? Lichaamsgewicht Dag 1, dag 31, maand 3, maand 6, maand 9, maand 12 Bloedtesten Dag 1, dag 31, maand 3, maand 6, maand 9, maand 12 Vragen over uw gezondheid Dag 1, dag 31, maand 3, maand 6, maand 9, maand 12 Vragen over uw Dag 1, dag 31, maand 3, maand 6, maand 9, maand 12 geneesmiddelen Einde behandeling Als u met uw onderzoeksbehandeling stopt: neemt u al het ongebruikte en gebruikte onderzoeksmiddel mee bij uw bezoek; uw arts controleert uw veiligheid en noteert uw geneesmiddelen. Uw onderzoeks-arts laat u weten of u nog bloedverdunners moet nemen nadat u uw deelname aan dit onderzoek heeft beëindigd. Als dit nodig is worden bloedverdunners aan u voorgeschreven volgens lokale praktijk. Pagina 13 van 16
14 BIJLAGE 4: Mogelijke bijwerkingen, risico's en ongemakken De bekende risico's of bijwerkingen gerelateerd aan het krijgen van antistollingsmiddelen (of bloedverdunners) zijn: Het is soms moeilijk de juiste hoeveelheid geneesmiddel te bepalen. Indien het bloed teveel stolt, kan opnieuw DVT of LE optreden, die gevaarlijk en zelfs dodelijk kunnen zijn. Indien het bloed te weinig stolt kunnen er meer bloedingen zijn. Dit kan gebeuren met alle antistollingsmiddelen, waaronder edoxaban, laagmoleculaire heparine en dalteparine. Bloedingen zijn meestal licht tot matig ernstig en stoppen vanzelf; het gaat om onder meer blauwe plekken of bloedend tandvlees, bloed in de urine, toegenomen menstruele bloedingen, langere bloeding na snijden of wonden, maagbloeding of bloeding in andere delen van het darmsysteem en ophoesten van bloed. In zeldzame gevallen is de bloeding ernstig en mogelijk dodelijk. Bloedingen kunnen zich voordoen in de hersenen en andere organen of weefsels. Een bloeding in de hersenen kan beroerte en/of overlijden tot gevolg hebben. Een ernstige bloeding kan zich voordoen bij het gebruik van alle antistollingsmiddelen waaronder edoxaban, laagmoleculaire heparine zoals dalteparine. Informeer uw onderzoeks-arts als u bloedingen krijgt of symptomen van een bloeding, zoals blauwe plekken, duizeligheid, zich licht in het hoofd voelen, zwakheid, vermoeidheid, onverklaarde pijn of zwelling. Dit geldt ook als u bent gestopt met het zelf innemen van het onderzoeksmiddel. Indien een bloeding is bevestigd, behandelt de onderzoeks-arts u afhankelijk van de locatie en de ernst van de bloeding. De bekende risico's of bijwerkingen gerelateerd aan het gebruik van edoxaban zijn bloedingen en veranderingen in leverbloedtesten. Andere bijwerkingen zijn anemie (weinig rode bloedcellen) en uitslag. Bekende veranderingen in bloedtesten en leverfunctietesten zijn waargenomen bij sommige deelnemers die met edoxaban werden behandeld. Deze veranderingen waren mild en gingen meestal over wanneer de patiënt geen andere leverziekte had, zoals besmettelijke hepatitis. Er worden bloedtesten waaronder leverfunctietesten bij u gedaan. Informeer uw onderzoeks-arts als u last blijft houden van misselijkheid, braken, buikpijn, vermoeidheid, verlies van eetlust, donkere urine of gele huid of ogen, aangezien dit kan duiden op leverproblemen. De vaakst voorkomende bijwerking die in verband wordt gebracht met het gebruik van laagmoleculaire heparine waaronder dalteparine zijn bloedingen. Veranderingen in leverfunctietesten zijn waargenomen bij deelnemers die met laagmoleculaire heparine werden behandeld. Deze veranderingen waren mild en gingen meestal over wanneer de deelnemers geen andere leverziekte hadden, zoals besmettelijke hepatitis. Andere bijwerkingen zijn verminderde bloedplaatjes die in verband kunnen worden gebracht met nieuwe bloedstolselvorming, koorts, misselijkheid, anemie, zwelling en allergische reacties. Laagmoleculaire heparine kan ook pijn, irritatie, roodheid en afstervende huid op de injectieplaats veroorzaken. Risico s en voorzorgsmaatregelen; contra-indicaties Allergische reacties: Soms reageren mensen allergisch op geneesmiddelen. Een ernstige allergische reactie kan levensbedreigend zijn. Pagina 14 van 16
15 Uw onderzoeks-arts/onderzoekspersoneel controleert u regelmatig om ervoor te zorgen dat risico's van het voortzetten van de behandeling worden afgewogen tegen de beoogde effecten (voordelen). Risico's van bloedafname: Het afnemen van bloed uit een ader met behulp van een naald wordt een bloedafname genoemd. Het kan nodig zijn meer dan eens te proberen. Voor elke bloedafname wordt een nieuwe naald gebruikt. Tijdens het gehele onderzoek wordt bloed afgenomen. U kunt hierdoor pijn of zich licht in het hoofd voelen. U kunt enig tijdelijk ongemak ervaren, bloedingen, blauwe plekken en zwelling, of in zeldzame gevallen infectie op de plek waar de naald wordt ingebracht. In totaal worden circa 8 eetlepels bloed afgenomen bij elk bezoek aan het ziekenhuis. Onverwachte risico's: De onderzoeksmiddelen kunnen andere bijwerkingen hebben die nu nog niet bekend zijn. U wordt geïnformeerd over nieuwe informatie die uw beslissing om in dit onderzoek te blijven kan veranderen. Risico's voor zwangerschap: Edoxaban is niet getest op zwangere vrouwen of vrouwen die borstvoeding geven. De gevolgen van dit geneesmiddel op een ongeboren menselijke baby of een kind dat borstvoeding krijgt, zijn onbekend. Als u zwanger bent of wordt, kan het onderzoeksmiddel geboorteafwijkingen of overlijden veroorzaken van uw ongeboren baby of kind dat borstvoeding krijgt. Als u een zwangere vrouw bent, borstvoeding geeft aan uw baby of dit wilt gaan doen, kunt u niet deelnemen aan dit onderzoek. Als u een vrouw bent die zwanger kan worden, moet u een betrouwbare anticonceptiemethode toepassen (implantaten/injectiemiddelen die hormonen bevatten, combinatiepil, spiraaltjes met hormonen, chirurgische sterilisatie, onthouding of vasectomie van uw mannelijke partner) om aan dit onderzoek deel te nemen. Indien u tijdens het onderzoek of binnen 30 dagen nadat u bent gestopt met het onderzoeksmiddel zwanger wordt, moet u de onderzoeks-arts of het onderzoekspersoneel onmiddellijk informeren. Als u zwanger wordt, mag u niet meer deelnemen aan het onderzoek. De onderzoeks-arts volgt uw zwangerschap en rapporteert het resultaat aan de sponsor. De institutionele toetsingscommissie (IRB), een groep die toezicht houdt op patiëntveiligheid, wordt geïnformeerd over de zwangerschap. Pagina 15 van 16
16 BIJLAGE 5: Informatie over de verzekering Voor iedereen die meedoet aan dit onderzoek is een verzekering afgesloten. De verzekering dekt schade die het gevolg is van deelname aan dit onderzoek. Dit geldt voor schade die naar boven komt tijdens het onderzoek, of binnen vier jaar na beëindiging van deelname aan het onderzoek. U moet de schade ook binnen die vier jaar aan de verzekeraar hebben gemeld. Voor de verzekering gelden een aantal uitsluitingen die u hieronder kort weergegeven aantreft. De precieze bepalingen zijn neergelegd in het Besluit verplichte verzekering bij medisch-wetenschappelijk onderzoek met mensen. De tekst daarvan kunt u vinden op de website van de Centrale Commissie Mensgebonden Onderzoek: In geval van schade kunt u zich direct wenden tot de verzekeraar of schaderegelaar. De verzekeraar van het onderzoek is: Naam: ACE European Group Limited Adres: Marten Meesweg 8-10, 3068 AV Rotterdam Telefoonnummer: De verzekering biedt een maximumdekking van ,- per deelnemer en ,- voor het gehele onderzoek. Voor alle onderzoeken van dezelfde sponsor is de maximumdekking ,- per jaar. De dekking van specifieke schades en kosten is verder tot bepaalde bedragen beperkt. De verzekering dekt de volgende schade niet: - schade die het gevolg is van het optreden van een risico waarover u in de schriftelijke informatie bent ingelicht, tenzij het risico zich in ernstiger mate voordoet dan was voorzien of het risico uiterst onwaarschijnlijk was; - schade aan de gezondheid die ook zou zijn ontstaan als u niet aan het onderzoek had deelgenomen; - schade die het gevolg is van het niet (volledig) nakomen van aanwijzingen of instructies; - schade aan nakomelingen, als gevolg van een nadelig effect van het onderzoek op u of uw nakomeling; - bij onderzoek naar bestaande behandelmethoden: schade die het gevolg is van een van deze behandelmethoden; - bij onderzoek naar de behandeling van specifieke gezondheidsproblemen: schade die het gevolg is van uitblijvende verbetering of van verslechtering van deze gezondheidsproblemen. Pagina 16 van 16
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek PACER-onderzoek: Onderzoek naar de noodzaak van correctie van bloedplaatjestekort voor het plaatsen van een centraal veneuze
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek PACER-onderzoek: Onderzoek naar de noodzaak van correctie van bloedplaatjestekort voor het plaatsen van een centraal veneuze
INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN TROMBOSEBEEN
 INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN TROMBOSEBEEN Hokusai post VTE studie: Lange termijn uitkomst na edoxaban versus warfarine voor
INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN TROMBOSEBEEN Hokusai post VTE studie: Lange termijn uitkomst na edoxaban versus warfarine voor
Langdurige behandeling van diep veneuze trombose bij patiënten met kanker (Longheva) Academisch Medisch Centrum, Amsterdam (AMC)
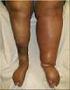 Titel studie: Opdrachtgever: Langdurige behandeling van diep veneuze trombose bij patiënten met kanker (Longheva) Academisch Medisch Centrum, Amsterdam (AMC) Hoofdonderzoeker: Dr. K. Meyer Introductie
Titel studie: Opdrachtgever: Langdurige behandeling van diep veneuze trombose bij patiënten met kanker (Longheva) Academisch Medisch Centrum, Amsterdam (AMC) Hoofdonderzoeker: Dr. K. Meyer Introductie
LEVODOPA BIJ PATIËNTEN MET VROEGE ZIEKTE VAN PARKINSON informatie voor deelnemers
 LEVODOPA BIJ PATIËNTEN MET VROEGE ZIEKTE VAN PARKINSON informatie voor deelnemers Geachte heer/ mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek. U beslist zelf
LEVODOPA BIJ PATIËNTEN MET VROEGE ZIEKTE VAN PARKINSON informatie voor deelnemers Geachte heer/ mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek. U beslist zelf
Dit onderzoek wordt uitgevoerd en gefinancierd door Acerta (een farmaceutisch bedrijf).
 Titel: Een gerandomiseerd, multicenter, open-label, fase 3-onderzoek naar de nietinferioriteit van ACP-196 versus Ibrutinib bij eerder behandelde proefpersonen met hoog-risico chronische lymfatische leukemie
Titel: Een gerandomiseerd, multicenter, open-label, fase 3-onderzoek naar de nietinferioriteit van ACP-196 versus Ibrutinib bij eerder behandelde proefpersonen met hoog-risico chronische lymfatische leukemie
INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN LONGEMBOLIE
 INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN LONGEMBOLIE Hokusai post VTE studie: Lange termijn uitkomst na edoxaban versus warfarine voor
INFORMATIE DEELNAME MEDISCH-WETENSCHAPPELIJK ONDERZOEK EN TOESTEMMINGSVERKLARING VOOR DE PROEFPERSOON MET EEN LONGEMBOLIE Hokusai post VTE studie: Lange termijn uitkomst na edoxaban versus warfarine voor
De invloed van een uitwendige kracht op de oogdruk.
 1 www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie) naar de invloed die een uitwendige kracht heeft
1 www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie) naar de invloed die een uitwendige kracht heeft
Titel onderzoek: Bepalen van nieuwe ziektevoorspellers bij colorectale levermetastasen. De MIRACLE studie.
 Titel onderzoek: Bepalen van nieuwe ziektevoorspellers bij colorectale levermetastasen. De studie. Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek.
Titel onderzoek: Bepalen van nieuwe ziektevoorspellers bij colorectale levermetastasen. De studie. Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek.
Informatie voor de wettelijke vertegenwoordiger voor deelname aan het onderzoek
 PAIS2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden of hoger Geachte heer/ mevrouw, Uw partner/familielid is in ons ziekenhuis
PAIS2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden of hoger Geachte heer/ mevrouw, Uw partner/familielid is in ons ziekenhuis
LEVODOPA BIJ PATIËNTEN MET VROEGE ZIEKTE VAN PARKINSON informatie voor deelnemers
 LEVODOPA BIJ PATIËNTEN MET VROEGE ZIEKTE VAN PARKINSON informatie voor deelnemers Geachte heer/ mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek. U beslist zelf
LEVODOPA BIJ PATIËNTEN MET VROEGE ZIEKTE VAN PARKINSON informatie voor deelnemers Geachte heer/ mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek. U beslist zelf
Onderzoek naar het effect van body mass index (BMI) en het roken van sigaretten op de opname van fentanyl
 Patiënteninformatie Onderzoek naar het effect van body mass index (BMI) en het roken van sigaretten op de opname van fentanyl Geachte heer/mevrouw, U bent in het Erasmus MC onder behandeling voor een vorm
Patiënteninformatie Onderzoek naar het effect van body mass index (BMI) en het roken van sigaretten op de opname van fentanyl Geachte heer/mevrouw, U bent in het Erasmus MC onder behandeling voor een vorm
Drie-dimensionale echografie voor het verbeteren van cosmetisch resultaat bij borstkanker patiënten; TURACOS trial
 Drie-dimensionale echografie voor het verbeteren van cosmetisch resultaat bij borstkanker patiënten; Geachte mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek
Drie-dimensionale echografie voor het verbeteren van cosmetisch resultaat bij borstkanker patiënten; Geachte mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek
Plaatsing van voedingssondes in de dunne darm via elektromagnetische geleiding op de verpleegafdeling of via kijkonderzoek op de endoscopie-afdeling
 Patiënt informatiebrief Plaatsing van voedingssondes in de dunne darm via elektromagnetische geleiding op de verpleegafdeling of via kijkonderzoek op de endoscopie-afdeling Geachte heer/mevrouw, Wij vragen
Patiënt informatiebrief Plaatsing van voedingssondes in de dunne darm via elektromagnetische geleiding op de verpleegafdeling of via kijkonderzoek op de endoscopie-afdeling Geachte heer/mevrouw, Wij vragen
Onderzoek naar bloedtest voor de diagnose beroerte
 Onderzoek naar bloedtest voor de diagnose beroerte MicroRNA als biomarker voor acute beroerte Inleiding Geachte heer/mevrouw, Wij vragen u om mee te doen aan een medisch-wetenschappelijk onderzoek. Meedoen
Onderzoek naar bloedtest voor de diagnose beroerte MicroRNA als biomarker voor acute beroerte Inleiding Geachte heer/mevrouw, Wij vragen u om mee te doen aan een medisch-wetenschappelijk onderzoek. Meedoen
INFORMATIEBRIEF VOOR DE PATIËNT
 INFORMATIEBRIEF VOOR DE PATIËNT Titel van het onderzoek Een gerandomiseerd onderzoek naar operatieve versus niet-operatieve behandeling van breuken van het kopje van het spaakbeen. Inleiding Geachte heer/mevrouw,
INFORMATIEBRIEF VOOR DE PATIËNT Titel van het onderzoek Een gerandomiseerd onderzoek naar operatieve versus niet-operatieve behandeling van breuken van het kopje van het spaakbeen. Inleiding Geachte heer/mevrouw,
Informatie voor patiënten en toestemmingsformulier behorende bij het onderzoek:
 Informatie voor patiënten en toestemmingsformulier behorende bij het onderzoek: Titel: Karakterisering van buffycoat afgeleide granulocyten (witte bloedcellen) om klinische parameters te identificeren
Informatie voor patiënten en toestemmingsformulier behorende bij het onderzoek: Titel: Karakterisering van buffycoat afgeleide granulocyten (witte bloedcellen) om klinische parameters te identificeren
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe
INFORMATIE VOOR PROEFPERSONEN VOOR TOESTEMMING VOOR GEGEVENSVERZAMELING OVER DE ZWANGERSCHAP EN OVER HET KIND
 INFORMATIE VOOR PROEFPERSONEN VOOR TOESTEMMING VOOR GEGEVENSVERZAMELING OVER DE ZWANGERSCHAP EN OVER HET KIND Titel van het onderzoek: Officiële titel van het protocol: Sponsor: Onderzoek naar een nieuw
INFORMATIE VOOR PROEFPERSONEN VOOR TOESTEMMING VOOR GEGEVENSVERZAMELING OVER DE ZWANGERSCHAP EN OVER HET KIND Titel van het onderzoek: Officiële titel van het protocol: Sponsor: Onderzoek naar een nieuw
Onderzoek naar de nazorg bij dikke darmkanker door de huisarts of de chirurg en het gebruik van een persoonlijke interactieve website (I CARE studie).
 Onderzoek naar de nazorg bij dikke darmkanker door de huisarts of de chirurg en het gebruik van een persoonlijke interactieve website (I CARE studie). Verbetert de zorg na de behandeling van dikke darmkanker
Onderzoek naar de nazorg bij dikke darmkanker door de huisarts of de chirurg en het gebruik van een persoonlijke interactieve website (I CARE studie). Verbetert de zorg na de behandeling van dikke darmkanker
Informatiebrief voor de patiënt
 Informatiebrief voor de patiënt Informatiebrief over de studie naar Geachte mevrouw / mijnheer, Uw arts vermoedt dat u de ziekte sinustrombose heeft. Op dit moment wordt er wetenschappelijk onderzoek gedaan
Informatiebrief voor de patiënt Informatiebrief over de studie naar Geachte mevrouw / mijnheer, Uw arts vermoedt dat u de ziekte sinustrombose heeft. Op dit moment wordt er wetenschappelijk onderzoek gedaan
Informatiebrief D-dimer and AP-FXIII in CVT studie, versie 1.2 3 november 2011. D-dimer en AP-FXIII in de diagnostiek van sinustrombose
 Informatiebrief voor de patiënt in tweede instantie Informatiebrief over de studie naar Geachte mevrouw / mijnheer, Op het moment dat u deze brief leest bent u herstellende van klachten waarvoor u werd
Informatiebrief voor de patiënt in tweede instantie Informatiebrief over de studie naar Geachte mevrouw / mijnheer, Op het moment dat u deze brief leest bent u herstellende van klachten waarvoor u werd
Klinische keuzes bij patiënten met staar en hoornvliesdystrofie van Fuchs
 Schiedamse Vest 180 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie)
Schiedamse Vest 180 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie)
OCT. Schiedamse Vest 160 Postbus LM Rotterdam. tel.:
 Schiedamse Vest 160 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan medisch-wetenschappelijk onderzoek (studie)
Schiedamse Vest 160 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan medisch-wetenschappelijk onderzoek (studie)
INFORMATIEBLAD VOOR PROEFPERSONEN ONDERZOEK VAN TRANSTHYRETINE-GEASSOCICIEERDE AMYLOÏDOSEN (THAOS)
 INFORMATIEBLAD VOOR PROEFPERSONEN ONDERZOEK VAN TRANSTHYRETINE-GEASSOCICIEERDE AMYLOÏDOSEN (THAOS) Protocoltitel: Protocolnummer: Naam opdrachtgever: Naam van THAOS-arts, contactgegevens en telefoonnummer:
INFORMATIEBLAD VOOR PROEFPERSONEN ONDERZOEK VAN TRANSTHYRETINE-GEASSOCICIEERDE AMYLOÏDOSEN (THAOS) Protocoltitel: Protocolnummer: Naam opdrachtgever: Naam van THAOS-arts, contactgegevens en telefoonnummer:
Inleiding Geachte heer/mevrouw,
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De werking van het afweersysteem bij eiceldonatie zwangerschappen DONatie van Oocyten in Reproductie (DONOR); klinische en immunologische
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De werking van het afweersysteem bij eiceldonatie zwangerschappen DONatie van Oocyten in Reproductie (DONOR); klinische en immunologische
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Observationeel onderzoek van de BioMimics 3D-stent bij de behandeling van perifeer vaatlijden Officiële titel: Een prospectief,
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Observationeel onderzoek van de BioMimics 3D-stent bij de behandeling van perifeer vaatlijden Officiële titel: Een prospectief,
INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR GEZONDE VRIJWILLIGERS
 INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR GEZONDE VRIJWILLIGERS Titel van het onderzoek: De rol van de vorming van neutrofiele extracellulaire traps (NETs) in sikkelcelziekte. Geachte heer/mevrouw,
INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR GEZONDE VRIJWILLIGERS Titel van het onderzoek: De rol van de vorming van neutrofiele extracellulaire traps (NETs) in sikkelcelziekte. Geachte heer/mevrouw,
Informatie voor de wettelijke vertegenwoordiger voor deelname aan het onderzoek
 PAIS 2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden Celsius of hoger Geachte heer/ mevrouw, Uw partner/familielid is in ons
PAIS 2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden Celsius of hoger Geachte heer/ mevrouw, Uw partner/familielid is in ons
Invloed van weeënremming op de uitkomst van vroeggeboorte,
 Patiëntinformatie voor deelname aan medisch-wetenschappelijk onderzoek Invloed van weeënremming op de uitkomst van vroeggeboorte, de APOSTEL VIII studie. Geachte mevrouw, Wij vragen u om mee te doen aan
Patiëntinformatie voor deelname aan medisch-wetenschappelijk onderzoek Invloed van weeënremming op de uitkomst van vroeggeboorte, de APOSTEL VIII studie. Geachte mevrouw, Wij vragen u om mee te doen aan
Titel van het onderzoek: De rol van de vorming van neutrofiele extracellulaire traps (NETs) in sikkelcelziekte.
 INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR PATIËNTEN Titel van het onderzoek: De rol van de vorming van neutrofiele extracellulaire traps (NETs) in sikkelcelziekte. Geachte heer/mevrouw, Wij vragen
INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR PATIËNTEN Titel van het onderzoek: De rol van de vorming van neutrofiele extracellulaire traps (NETs) in sikkelcelziekte. Geachte heer/mevrouw, Wij vragen
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek. 16 jaar en ouder.
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek. 16 jaar en ouder. Allo-antistofvorming bij sikkelcelziekte na transfusie: Wat is de rol van ontsteking en erfelijke aanleg?
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek. 16 jaar en ouder. Allo-antistofvorming bij sikkelcelziekte na transfusie: Wat is de rol van ontsteking en erfelijke aanleg?
Onderzoek naar het effect van aprepitant (Emend ) op de fentanylpijnpleister
 Patiënteninformatie Onderzoek naar het effect van aprepitant (Emend ) op de fentanylpijnpleister (Durogesic ) Geachte heer/mevrouw, U bent in het Erasmus MC onder behandeling voor een vorm van kanker.
Patiënteninformatie Onderzoek naar het effect van aprepitant (Emend ) op de fentanylpijnpleister (Durogesic ) Geachte heer/mevrouw, U bent in het Erasmus MC onder behandeling voor een vorm van kanker.
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe validatie van een risicostratificatie
voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe validatie van een risicostratificatie
Titel van het onderzoek: Bepaling van Zink en het Ontstekingseiwit PTX3 bij Patiënten met Sikkelcelziekte (ZIP studie)
 INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR PATIËNTEN Titel van het onderzoek: Bepaling van Zink en het Ontstekingseiwit PTX3 bij Patiënten met Sikkelcelziekte () Geachte heer/mevrouw, Wij vragen u om
INFORMATIEBRIEF EN TOESTEMMINGSFORMULIER VOOR PATIËNTEN Titel van het onderzoek: Bepaling van Zink en het Ontstekingseiwit PTX3 bij Patiënten met Sikkelcelziekte () Geachte heer/mevrouw, Wij vragen u om
SPLINT-trial Preventie van urologische complicaties bij niertransplantaties van levende donoren: splint of geen splint
 SPLINT-trial Preventie van urologische complicaties bij niertransplantaties van levende donoren: splint of geen splint Uw behandelend arts heeft u geïnformeerd over het SPLINT medisch-wetenschappelijk
SPLINT-trial Preventie van urologische complicaties bij niertransplantaties van levende donoren: splint of geen splint Uw behandelend arts heeft u geïnformeerd over het SPLINT medisch-wetenschappelijk
Effect van transverse versus longitudinale incisies op kniepijn na tibiapen plaatsing
 PATIËNTEN INFORMATIE FOLDER Effect van transverse versus longitudinale incisies op kniepijn na tibiapen plaatsing Geachte heer/mevrouw, U wordt in het ziekenhuis geopereerd aan een gebroken scheenbeen
PATIËNTEN INFORMATIE FOLDER Effect van transverse versus longitudinale incisies op kniepijn na tibiapen plaatsing Geachte heer/mevrouw, U wordt in het ziekenhuis geopereerd aan een gebroken scheenbeen
Een experimentele scan-techniek om de doorbloeding van het netvlies en het vaatvlies in het oog te meten.
 Schiedamse Vest 180 1 Postbus 70030 3000 LM Rotterdam telefoon: : 010-4023449 e-mail: roi@oogziekenhuis.nl www.oogziekenhuis.nl Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Schiedamse Vest 180 1 Postbus 70030 3000 LM Rotterdam telefoon: : 010-4023449 e-mail: roi@oogziekenhuis.nl www.oogziekenhuis.nl Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Patiënteninformatie voor deelname aan het onderzoek
 PAIS 2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden Celsius of hoger Geachte heer/mevrouw, Wij vragen u via deze brief mee
PAIS 2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden Celsius of hoger Geachte heer/mevrouw, Wij vragen u via deze brief mee
Antibiotica voor cellulitis: 6 of 12 dagen?
 Antibiotica voor cellulitis: 6 of 12 dagen? Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (zie titel). Dit onderzoek wordt uitgevoerd in ca. acht
Antibiotica voor cellulitis: 6 of 12 dagen? Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (zie titel). Dit onderzoek wordt uitgevoerd in ca. acht
Effect van transverse versus longitudinale incisies op kniepijn na tibiapen plaatsing. Patiënten Informatie Folder
 Effect van transverse versus longitudinale incisies op kniepijn na tibiapen plaatsing Patiënten Informatie Folder PATIËNTEN INFORMATIE FOLDER Effect van transverse versus longitudinale incisies op kniepijn
Effect van transverse versus longitudinale incisies op kniepijn na tibiapen plaatsing Patiënten Informatie Folder PATIËNTEN INFORMATIE FOLDER Effect van transverse versus longitudinale incisies op kniepijn
Titel van het onderzoek Inbrengen van continue ambulante peritoneaal dialyse katheters: Kijkoperatie of open techniek?
 Titel van het onderzoek Inbrengen van continue ambulante peritoneaal dialyse katheters: Kijkoperatie of open techniek? Inleiding Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Titel van het onderzoek Inbrengen van continue ambulante peritoneaal dialyse katheters: Kijkoperatie of open techniek? Inleiding Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe validatie van een risicostratificatie
voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe validatie van een risicostratificatie
Patiënteninformatie voor deelname aan het onderzoek
 PAIS2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden Celsius of hoger Geachte heer/mevrouw, Wij vragen u via deze brief mee
PAIS2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden Celsius of hoger Geachte heer/mevrouw, Wij vragen u via deze brief mee
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe
Informatiebrief deelnemers MIND-TIA: De waarde van een bloedtest bij verdenking op een TIA
 Informatiebrief deelnemers MIND-TIA: De waarde van een bloedtest bij verdenking op een TIA Julius Centrum UMC Utrecht Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Informatiebrief deelnemers MIND-TIA: De waarde van een bloedtest bij verdenking op een TIA Julius Centrum UMC Utrecht Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Informatiebrief voor de patiënt
 Informatiebrief voor de patiënt Geachte mevrouw / mijnheer, U bent getroffen door een beroerte (herseninfarct of hersenbloeding). Vanuit het Academisch Medisch Centrum (AMC) in Amsterdam wordt onderzoek
Informatiebrief voor de patiënt Geachte mevrouw / mijnheer, U bent getroffen door een beroerte (herseninfarct of hersenbloeding). Vanuit het Academisch Medisch Centrum (AMC) in Amsterdam wordt onderzoek
Inbrengen van continue ambulante peritoneaal dialyse katheters: Kijkoperatie of open techniek?
 Inbrengen van continue ambulante peritoneaal dialyse katheters: Kijkoperatie of open techniek? Inleiding Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek
Inbrengen van continue ambulante peritoneaal dialyse katheters: Kijkoperatie of open techniek? Inleiding Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek
onderzoek Invloed van UVB lichttherapie op huid en darmflora.
 Uw behandelend arts of de onderzoeker heeft u geïnformeerd over het medisch-wetenschappelijk onderzoek Invloed van UVB lichttherapie op huid en darmflora. U beslist zelf of u wilt meedoen. Om deze beslissing
Uw behandelend arts of de onderzoeker heeft u geïnformeerd over het medisch-wetenschappelijk onderzoek Invloed van UVB lichttherapie op huid en darmflora. U beslist zelf of u wilt meedoen. Om deze beslissing
Informatiebrief voor zwangere partners behorende bij het hoofdonderzoek
 Informatiebrief voor zwangere partners behorende bij het hoofdonderzoek Onderzoek naar de werkzaamheid en veiligheid van Venetoclax bij patiënten met terugkerende Chronische Lymfatische Leukemie Officiële
Informatiebrief voor zwangere partners behorende bij het hoofdonderzoek Onderzoek naar de werkzaamheid en veiligheid van Venetoclax bij patiënten met terugkerende Chronische Lymfatische Leukemie Officiële
PATIËNTINFORMATIEBRIEF OVER FARMACOGENETISCHE TEST. U bent gevraagd om tijdens uw deelname aan het onderzoek getiteld:
 PATIËNTINFORMATIEBRIEF OVER FARMACOGENETISCHE TEST Studie nr.: 1321.3 EudraCT nr. : 2013 004813 41 Geachte mevrouw, mijnheer, U bent gevraagd om tijdens uw deelname aan het onderzoek getiteld: Een fase
PATIËNTINFORMATIEBRIEF OVER FARMACOGENETISCHE TEST Studie nr.: 1321.3 EudraCT nr. : 2013 004813 41 Geachte mevrouw, mijnheer, U bent gevraagd om tijdens uw deelname aan het onderzoek getiteld: Een fase
Titel van het onderzoek Inbrengen van continue ambulante peritoneaal dialyse katheters: Kijkoperatie of open techniek?
 Titel van het onderzoek Inbrengen van continue ambulante peritoneaal dialyse katheters: Kijkoperatie of open techniek? Inleiding Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Titel van het onderzoek Inbrengen van continue ambulante peritoneaal dialyse katheters: Kijkoperatie of open techniek? Inleiding Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
PATIËNTINFORMATIE STUDIE NAAR HET EFFECT VAN INTRA ARTERIËLE
 PATIËNTINFORMATIE STUDIE NAAR HET EFFECT VAN INTRA ARTERIËLE BEHANDELING OP DE GEZONDHEIDSTOESTAND BIJ EEN HERSENINFARCT Geachte heer / mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch
PATIËNTINFORMATIE STUDIE NAAR HET EFFECT VAN INTRA ARTERIËLE BEHANDELING OP DE GEZONDHEIDSTOESTAND BIJ EEN HERSENINFARCT Geachte heer / mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch
INFORMATIEBRIEF HOSPITAL-ADL STUDIE
 INFORMATIEBRIEF HOSPITAL-ADL STUDIE Titel van het onderzoek: Ontrafelen van het mechanisme achter ziekenhuis-gerelateerd functieverlies (Hospital-ADL studie). Geachte heer/mevrouw, Wij vragen u vriendelijk
INFORMATIEBRIEF HOSPITAL-ADL STUDIE Titel van het onderzoek: Ontrafelen van het mechanisme achter ziekenhuis-gerelateerd functieverlies (Hospital-ADL studie). Geachte heer/mevrouw, Wij vragen u vriendelijk
Patiënten-informatiebrief Volwassenen ICOS
 Patiënteninformatiefolder Voor patiënten van 18 jaar en ouder Behorende bij het onderzoek: International CIDP Outcome Study (ICOS) Een studie naar de variatie en de voorspellers van het ziektebeloop bij
Patiënteninformatiefolder Voor patiënten van 18 jaar en ouder Behorende bij het onderzoek: International CIDP Outcome Study (ICOS) Een studie naar de variatie en de voorspellers van het ziektebeloop bij
Type darmoperatie voor geperforeerde diverticulitis
 Type darmoperatie voor geperforeerde diverticulitis Geachte heer, mevrouw, Bij u is vastgesteld, dat er mogelijk sprake is van een perforatie (gaatje) van de dikke darm ten gevolge van divertikels (uitstulpingen).
Type darmoperatie voor geperforeerde diverticulitis Geachte heer, mevrouw, Bij u is vastgesteld, dat er mogelijk sprake is van een perforatie (gaatje) van de dikke darm ten gevolge van divertikels (uitstulpingen).
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe validatie van een risicostratificatie
voor deelname aan medisch-wetenschappelijk onderzoek Bloedonderzoek als voorspeller van de kans op een tekort aan schildklierhormoon na verwijdering van één schildklierhelft Externe validatie van een risicostratificatie
Patiëntinformatieformulier LOGICA-trial
 Informatiebrief LOGICA trial: Laparoscopische versus Open Maag Operatie Datum: Onderwerp Telefoon E-mail 1 november 2015 LOGICA trial 088-005 6908 espillenaarbilgen@rijnstate.nl Geachte heer/mevrouw, U
Informatiebrief LOGICA trial: Laparoscopische versus Open Maag Operatie Datum: Onderwerp Telefoon E-mail 1 november 2015 LOGICA trial 088-005 6908 espillenaarbilgen@rijnstate.nl Geachte heer/mevrouw, U
Gamma-probe en echografisch geleide punctie van de schildwachtklier bij melanoom en borstkankerpatiënten; GULF Trial.
 Gamma-probe en echografisch geleide punctie van de schildwachtklier bij melanoom en borstkankerpatiënten; GULF Trial. Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Gamma-probe en echografisch geleide punctie van de schildwachtklier bij melanoom en borstkankerpatiënten; GULF Trial. Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Routine versus op indicatie verwijderen van de stelschroef Routinematig versus op indicatie verwijderen van de stelschroef:
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Routine versus op indicatie verwijderen van de stelschroef Routinematig versus op indicatie verwijderen van de stelschroef:
Platelet Transfusion in Cerebral Haemorrhage PATCH
 Platelet Transfusion in Cerebral Haemorrhage PATCH Patiënten-informatie bij het onderzoek naar de behandeling van een hersenbloeding bij patiënten die bloedplaatjes remmende medicijnen gebruiken Geachte
Platelet Transfusion in Cerebral Haemorrhage PATCH Patiënten-informatie bij het onderzoek naar de behandeling van een hersenbloeding bij patiënten die bloedplaatjes remmende medicijnen gebruiken Geachte
Extra Informatiebrief voor de Patiënt en Toestemmingsverklaring optioneel herkenningsstoffenonderzoek
 Extra Informatiebrief voor de Patiënt en Toestemmingsverklaring optioneel herkenningsstoffenonderzoek Een fase 1 onderzoek met AEB071 bij patiënten met diffuus grootcellig B-lymfoom waarbij CD79 veranderd
Extra Informatiebrief voor de Patiënt en Toestemmingsverklaring optioneel herkenningsstoffenonderzoek Een fase 1 onderzoek met AEB071 bij patiënten met diffuus grootcellig B-lymfoom waarbij CD79 veranderd
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
INFORMATIEBRIEF VOOR DE PATIËNT
 INFORMATIEBRIEF VOOR DE PATIËNT Titel van het onderzoek Een gerandomiseerd onderzoek naar operatieve versus niet-operatieve behandeling van breuken van het kopje van het spaakbeen. Inleiding Geachte heer/mevrouw,
INFORMATIEBRIEF VOOR DE PATIËNT Titel van het onderzoek Een gerandomiseerd onderzoek naar operatieve versus niet-operatieve behandeling van breuken van het kopje van het spaakbeen. Inleiding Geachte heer/mevrouw,
Het gebruik van siliconenolie in vitreoretinale chirurgie.
 Schiedamse Vest 160 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie)
Schiedamse Vest 160 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie)
Een onderzoek naar de werkzaamheid van assisted hatching
 Een onderzoek naar de werkzaamheid van assisted hatching Inleiding Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek naar de werkzaamheid van assisted
Een onderzoek naar de werkzaamheid van assisted hatching Inleiding Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek naar de werkzaamheid van assisted
Informatie over onderzoek naar de determinanten voor de respons op DDAVP
 Informatie over onderzoek naar de determinanten voor de respons op DDAVP (The RISE study: Response to DDAVP In mild hemophilia A patients, in Search for determinants) Plaats.. Datum.. Geachte mijnheer,
Informatie over onderzoek naar de determinanten voor de respons op DDAVP (The RISE study: Response to DDAVP In mild hemophilia A patients, in Search for determinants) Plaats.. Datum.. Geachte mijnheer,
Informatie voor de wettelijke vertegenwoordiger voor deelname aan het onderzoek
 PAIS2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden of hoger Geachte heer/ mevrouw, Uw partner/familielid is in ons ziekenhuis
PAIS2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden of hoger Geachte heer/ mevrouw, Uw partner/familielid is in ons ziekenhuis
INFORMATIEBRIEF VOOR DE PATIËNT
 INFORMATIEBRIEF VOOR DE PATIËNT Titel van het onderzoek Een gerandomiseerd onderzoek naar operatieve versus niet-operatieve behandeling van breuken van het kopje van het spaakbeen. Inleiding Geachte heer/mevrouw,
INFORMATIEBRIEF VOOR DE PATIËNT Titel van het onderzoek Een gerandomiseerd onderzoek naar operatieve versus niet-operatieve behandeling van breuken van het kopje van het spaakbeen. Inleiding Geachte heer/mevrouw,
Het onderzoek waarvoor uw medewerking wordt gevraagd
 Proefpersoneninformatie: Effectiviteit van behandeling van migraine door manueel therapeut en huisarts: een pilot study Hoofddorp, versie 5 18-06-2015 Geachte heer/mevrouw, Wij vragen u vriendelijk om
Proefpersoneninformatie: Effectiviteit van behandeling van migraine door manueel therapeut en huisarts: een pilot study Hoofddorp, versie 5 18-06-2015 Geachte heer/mevrouw, Wij vragen u vriendelijk om
Informatiebrief en Toestemmingsformulier Pre-Screening
 Informatiebrief en Toestemmingsformulier Pre-Screening Behorend bij het hoofdonderzoek: Een onderzoek naar de werking van ABT-414 ter aanvulling op de standaardbehandeling bij patiënten, waarbij onlangs
Informatiebrief en Toestemmingsformulier Pre-Screening Behorend bij het hoofdonderzoek: Een onderzoek naar de werking van ABT-414 ter aanvulling op de standaardbehandeling bij patiënten, waarbij onlangs
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Informatie voor donoren over UMC Utrecht Biobank TiN
 Informatie voor donoren over UMC Utrecht Biobank TiN Geachte mevrouw/mijnheer, In het kader van de Trombocytopathie in Nederland studie wordt een gedeelte van het extra afgenomen bloed opgeslagen in een
Informatie voor donoren over UMC Utrecht Biobank TiN Geachte mevrouw/mijnheer, In het kader van de Trombocytopathie in Nederland studie wordt een gedeelte van het extra afgenomen bloed opgeslagen in een
Netvliesloslating op OCT
 Schiedamse Vest 180 1 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie)
Schiedamse Vest 180 1 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie)
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Routine versus op indicatie verwijderen van de stelschroef Routinematig versus op indicatie verwijderen van de stelschroef:
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Routine versus op indicatie verwijderen van de stelschroef Routinematig versus op indicatie verwijderen van de stelschroef:
Patiënteninformatie voor deelname aan het onderzoek
 PAIS2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden Celsius of hoger Geachte heer/mevrouw, Wij vragen u via deze brief mee
PAIS2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden Celsius of hoger Geachte heer/mevrouw, Wij vragen u via deze brief mee
Medischwetenschappelijk. onderzoek. Algemene informatie voor de proefpersoon
 Medischwetenschappelijk onderzoek Algemene informatie voor de proefpersoon Inhoud Inleiding 5 Medisch-wetenschappelijk onderzoek 6 Wat is medisch-wetenschappelijk onderzoek? Wat zijn proefpersonen? Wie
Medischwetenschappelijk onderzoek Algemene informatie voor de proefpersoon Inhoud Inleiding 5 Medisch-wetenschappelijk onderzoek 6 Wat is medisch-wetenschappelijk onderzoek? Wat zijn proefpersonen? Wie
Patiënten Informatie formulier. SPLINT-trial
 Patiënten Informatie formulier SPLINT-trial Preventie van urologische complicaties bij niertransplantaties van levende donoren: splint of geen splint? Versie 2 09-10-2013 pagina 1 van 8 Titel van het onderzoek
Patiënten Informatie formulier SPLINT-trial Preventie van urologische complicaties bij niertransplantaties van levende donoren: splint of geen splint? Versie 2 09-10-2013 pagina 1 van 8 Titel van het onderzoek
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 [Logo] Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek ASPIRIN TRIAL De rol van aspirine op de overleving van patiënten met dikkedarmkanker Inleiding Geachte heer/mevrouw,
[Logo] Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek ASPIRIN TRIAL De rol van aspirine op de overleving van patiënten met dikkedarmkanker Inleiding Geachte heer/mevrouw,
Informatiebrief MIRA-onderzoek: MIRena-spiraal versus endometriumablatie in de behandeling van hevig menstrueel bloedverlies
 Informatiebrief MIRA-onderzoek: MIRena-spiraal versus endometriumablatie in de behandeling van hevig menstrueel bloedverlies Geachte mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Informatiebrief MIRA-onderzoek: MIRena-spiraal versus endometriumablatie in de behandeling van hevig menstrueel bloedverlies Geachte mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek Titel van het onderzoek: Sneller behandelen van patiënten met een acute beroerte door een volgsysteem met directe visuele feedback
Informatiebrief voor patiënten. Vullingsstrategie bij bloedverlies tijdens de bevalling
 Informatiebrief voor patiënten Vullingsstrategie bij bloedverlies tijdens de bevalling NL42942.068.13 Versie 4 18-11.2013 Geachte mevrouw, U bent voor uw zwangerschap onder controle in het academisch ziekenhuis
Informatiebrief voor patiënten Vullingsstrategie bij bloedverlies tijdens de bevalling NL42942.068.13 Versie 4 18-11.2013 Geachte mevrouw, U bent voor uw zwangerschap onder controle in het academisch ziekenhuis
Verkorte titel: de effecten van budesonide op de bijwerkingen van cabazitaxel bij patiënten met prostaatkanker
 PATIËNTENINFORMATIE EN TOESTEMMINGSVERKLARING SUBSTUDIE BEHOREND BIJ HET ONDERZOEK: Fase II onderzoek bij patiënten met prostaatkanker naar de effecten van budesonide op cabazitaxel (Jevatana ): een gerandomiseerd,
PATIËNTENINFORMATIE EN TOESTEMMINGSVERKLARING SUBSTUDIE BEHOREND BIJ HET ONDERZOEK: Fase II onderzoek bij patiënten met prostaatkanker naar de effecten van budesonide op cabazitaxel (Jevatana ): een gerandomiseerd,
PATIËNTEN INFORMATIE BRIEF PROSPECTIEVE DATA REGISTRATIE VAN PATIËNTEN MET EEN AANGEBOREN ZELDZAME STOLLINGSAFWIJKING (PRO-RBDD)
 PATIËNTEN INFORMATIE BRIEF PROSPECTIEVE DATA REGISTRATIE VAN PATIËNTEN MET EEN AANGEBOREN ZELDZAME STOLLINGSAFWIJKING (PRO-RBDD) Geachte mevrouw / mijnheer, Uw behandelend arts heeft u geïnformeerd over
PATIËNTEN INFORMATIE BRIEF PROSPECTIEVE DATA REGISTRATIE VAN PATIËNTEN MET EEN AANGEBOREN ZELDZAME STOLLINGSAFWIJKING (PRO-RBDD) Geachte mevrouw / mijnheer, Uw behandelend arts heeft u geïnformeerd over
Patiënten-informatiebrief Ouders ICOS
 Patiënteninformatiefolder Voor ouders/verzorgers (van patienten van 12 t/m 17 jaar) Behorende bij het onderzoek: International CIDP Outcome Study (ICOS) Een studie naar de variatie en de voorspellers van
Patiënteninformatiefolder Voor ouders/verzorgers (van patienten van 12 t/m 17 jaar) Behorende bij het onderzoek: International CIDP Outcome Study (ICOS) Een studie naar de variatie en de voorspellers van
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk. De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak Officiële titel: De rol van endoscopische echografie
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek De waarde van inwendige echo in alvleesklierontsteking met onbekende oorzaak Officiële titel: De rol van endoscopische echografie
Informatiebrief voor de vertegenwoordiger
 Informatiebrief voor de vertegenwoordiger Preventive Antibiotics in Stroke Study (PASS) Informatiebrief over de studie naar preventief gebruik van antibiotica bij patiënten met een herseninfarct of hersenbloeding.
Informatiebrief voor de vertegenwoordiger Preventive Antibiotics in Stroke Study (PASS) Informatiebrief over de studie naar preventief gebruik van antibiotica bij patiënten met een herseninfarct of hersenbloeding.
Patiënteninformatie voor deelname aan het onderzoek
 PAIS 2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden Celsius of hoger Geachte heer/mevrouw, Wij vragen u via deze brief mee
PAIS 2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden Celsius of hoger Geachte heer/mevrouw, Wij vragen u via deze brief mee
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek
 Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek DISTRICTS Het Nederlandse injectie versus operatie onderzoek bij patiënten met een zenuwbeknelling in de pols. Geachte heer/mevrouw,
Proefpersoneninformatie voor deelname aan medisch-wetenschappelijk onderzoek DISTRICTS Het Nederlandse injectie versus operatie onderzoek bij patiënten met een zenuwbeknelling in de pols. Geachte heer/mevrouw,
Officiële titel: Toepassen van farmacokinetische of voorspellende doseermodellen bij operaties in hemofilie patiënten ( OPTI-CLOT")
 Informatie over wetenschappelijk onderzoek naar de effecten van farmacokinetische modellen bij het doseren van stollingsfactor VIII (FVIII) in hemofilie bij operaties Officiële titel: Toepassen van farmacokinetische
Informatie over wetenschappelijk onderzoek naar de effecten van farmacokinetische modellen bij het doseren van stollingsfactor VIII (FVIII) in hemofilie bij operaties Officiële titel: Toepassen van farmacokinetische
Informatie voor de wettelijke vertegenwoordiger voor deelname aan het onderzoek
 PAIS2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden Celsius of hoger Geachte heer/ mevrouw, Uw partner/familielid is in ons
PAIS2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden Celsius of hoger Geachte heer/ mevrouw, Uw partner/familielid is in ons
Geachte heer, mevrouw,
 Patiënten informatiebrief Behorend bij het onderzoek naar het verschil in pijnvermindering en kwaliteit van leven na behandeling van werveluitzaaiing(en) met conventionele radiotherapie of stereotactische
Patiënten informatiebrief Behorend bij het onderzoek naar het verschil in pijnvermindering en kwaliteit van leven na behandeling van werveluitzaaiing(en) met conventionele radiotherapie of stereotactische
Aanvullende informatie bij het informatie- en toestemmingsformulier versie OCT2013
 Aanvullende informatie bij het informatie- en toestemmingsformulier versie 5.1 08OCT2013 Studie: Titel: Protocol C16010 Een fase 3, gerandomiseerd, dubbelblind, multicenter-onderzoek waarbij oraal MLN9708
Aanvullende informatie bij het informatie- en toestemmingsformulier versie 5.1 08OCT2013 Studie: Titel: Protocol C16010 Een fase 3, gerandomiseerd, dubbelblind, multicenter-onderzoek waarbij oraal MLN9708
Metingen van de zenuwvezels in het netvlies met SD-OCT.
 Schiedamse Vest 160 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan medisch-wetenschappelijk onderzoek (studie)
Schiedamse Vest 160 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan medisch-wetenschappelijk onderzoek (studie)
bij de laserbehandeling van hinderlijke glasvochttroebelingen.
 Schiedamse Vest 180 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie)
Schiedamse Vest 180 Postbus 70030 3000 LM Rotterdam www.oogziekenhuis.nl tel.: 010-4023449 Geachte heer/mevrouw, Wij vragen u vriendelijk om mee te doen aan een medisch-wetenschappelijk onderzoek (studie)
Informatiebrief voor de patiënt in tweede instantie
 Informatiebrief voor de patiënt in tweede instantie Geachte mevrouw / mijnheer, Op het moment dat u deze brief leest bent u aan het herstellen van een beroerte (herseninfarct of hersenbloeding). Vanuit
Informatiebrief voor de patiënt in tweede instantie Geachte mevrouw / mijnheer, Op het moment dat u deze brief leest bent u aan het herstellen van een beroerte (herseninfarct of hersenbloeding). Vanuit
Informatie voor de wettelijke vertegenwoordiger voor deelname aan het onderzoek
 PAIS 2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden Celsius of hoger Geachte heer/ mevrouw, Uw partner/familielid is in ons
PAIS 2: Het effect van hoge dosis paracetamol op de uitkomst na een beroerte bij mensen met een lichaamstemperatuur van 36.5 graden Celsius of hoger Geachte heer/ mevrouw, Uw partner/familielid is in ons
Chemotherapie gevolgd door chirurgie versus chirurgie alleen in hoog-risico patiënten met colorectale levermetastasen. De CHARISMA trial.
 Patiëntinformatie bij het onderzoek: Chemotherapie gevolgd door chirurgie versus chirurgie alleen in hoog-risico patiënten met colorectale levermetastasen. De CHARISMA trial. Geachte heer/mevrouw, U bent
Patiëntinformatie bij het onderzoek: Chemotherapie gevolgd door chirurgie versus chirurgie alleen in hoog-risico patiënten met colorectale levermetastasen. De CHARISMA trial. Geachte heer/mevrouw, U bent
Medisch-wetenschappelijk onderzoek Algemene informatie voor de proefpersoon
 Uitgave Ministerie van Volksgezondheid, Welzijn en Sport Postadres Postbus 20350 2500 EJ Den Haag Bezoekadres Parnassusplein 5 2511 VX Den Haag Telefoon (070) 340 79 11 Informatie Voor informatie en vragen
Uitgave Ministerie van Volksgezondheid, Welzijn en Sport Postadres Postbus 20350 2500 EJ Den Haag Bezoekadres Parnassusplein 5 2511 VX Den Haag Telefoon (070) 340 79 11 Informatie Voor informatie en vragen
Patiënteninformatie ALIFE2 Studie
 Patiënteninformatie ALIFE2 Studie De invloed van LMWH toediening ter verkleining van de miskraamkans bij vrouwen met herhaalde miskramen en erfelijke trombofilie. Geachte mevrouw, In aansluiting op het
Patiënteninformatie ALIFE2 Studie De invloed van LMWH toediening ter verkleining van de miskraamkans bij vrouwen met herhaalde miskramen en erfelijke trombofilie. Geachte mevrouw, In aansluiting op het
