Chemlab proef: vetten Kwalitatieve en kwantitatieve analyse van vetten (en olie)
|
|
|
- Fien Lenaerts
- 8 jaren geleden
- Aantal bezoeken:
Transcriptie
1 1 Chemlab proef: vetten Kwalitatieve en kwantitatieve analyse van vetten (en olie) 1 Voorbereiding 1.1 Inleiding Lipiden, de verzamelnaam voor vetten (vast bij kamertemperatuur) en olie (vloeibaar bij kamertemperatuur) zijn apolaire of hydrofobe verbindingen: ze lossen zeer slecht op in H 2 O (het voorbeeld van een polair solvent), doch goed in apolaire solventen als chloroform (CH 3 Cl), CCl 4, petroleumether en ether. Lipiden bevatten chemisch zeer verschillende moleculen; de best gekende zijn echter triglyceriden: drie vetzuren veresterd aan glycerol en fosfolipiden, de basismoleculen van membranen. Teken de structuurformule van glycerol, een vetzuur, een triglyceride en een fosfoglyceride; je mag schematiseren ( of R) als je weet wat het betekent. glycerol: vetzuur: triglyceride: fosfoglyceride: Let op het onderscheid vetzuur en vet (meestal triglyceride bedoeld)!
2 2 Vetzuren verschillen in lengte en in graad van onverzadigdheid (of aantal dubbele bindingen). Plantaardige lipiden bezitten in de regel veel dubbele bindingen, planten en micro-organismen bezitten immers enzymen om meerdere dubbele bindingen in één vetzuur aan te leggen. Hogere dieren (en de mens) missen deze enzymen. Toch zijn lipiden met meervoudig onverzadigde vetzuren (de zogenaamde essentiële vetzuren) onmisbaar in ons dieet omdat ze nodig zijn om vetopslag en membranen vloeibaar te maken. Dubbele bindingen in natuurlijk voorkomende vetzuren zijn immers altijd aangelegd in de cis-configuratie. Teken dit (structuurformule): Leg uit hoe dit de vloeibaarheid in vetlagen (triglyceride stapelingen) en membranen bevordert:
3 3 De vloeibaarheid bij kamertemperatuur van vetdepots en membranen is zeer belangrijk voor enzymen (opbouw- en afbraak) en andere eiwitten (bijv. transportproteïnen) die erin moeten werken en daarvoor moeten kunnen bewegen. In een vloeibare omgeving kan dit, in een starre vaste structuur niet! Dierlijk vet, dat beduidend minder dubbele bindingen bevat, omdat de syntheseenzymen voor meervoudig onverzadigde vetzuren ontbreken, wordt vloeibaar gehouden door vetten en vetzuren met dubbele bindingen uit de voeding, maar ook door cholesterol (eigen of uit de voeding). Plantaardige olie en vetten zijn voor onze voeding erg belangrijk: ze bevatten essentiële vetzuren en geen cholesterol (wel andere steroïden). 1.2 Het joodgetal Het aantal dubbele bindingen in een vet of olie, bepaald via het joodgetal, is meteen een gezondheidsindicator voor voedingsvetten. Hou echter eveneens rekening met het feit dat de moderne minarines ongeveer 50% water bevatten, gebonden in de apolaire lipide-massa via gelatine (eiwit uit beenderen en bindweefsel). Bij consumptie van deze minarines krijg je dan ook slechts de helft vetten binnen, hetgeen eveneens belangrijk kan zijn in onze maatschappij van over consumptie. Een idee over het watergehalte van vetten krijg je door vet te smelten en het vormen van 2 lagen (zie lab) na afkoeling: boven de vetlaag, beneden de waterlaag (hogere dichtheid). Zoek de definitie van het joodgetal op; let op dat deze definitie praktisch hanteerbaar is: hoeveel g vet, welke eenheden (zie 3. kwantitatieve testen). Schrijf de chemische reactie die aan de basis ligt van de berekening van het joodgetal voor een vet (triglyceride) en een vetzuur met x dubbele bindingen.
4 4 vetzuur: triglyceride: Als je het M r kent (symbool M r ) en het aantal dubbele bindingen (x) geef dan aan hoeveel mol en hoeveel gram I 2 verbruikt wordt in de reactie per 100 g vet of vetzuur: noteer dit onder de reacties. (voorgaande kaders) Hieronder worden de formules van twee vetzuren gegeven. Bereken van elk de molecuulmassa en het joodgetal: Arachidonzuur: CH 3 (CH 2 ) 4 CH = CH CH 2 CH = CH CH 2 CH = CH CH 2 CH =CH CH 2 CH 2 CH 2 - COOH M r : X: JG:
5 5 Linoleenzuur: CH 3 CH 2 CH = CH CH 2 CH = CH CH 2 CH = CH (CH 2 ) 7 - COOH M r : X: JG: De methode om het joodgetal te bepalen steunt op het volgende principe: een gekende hoeveelheid te onderzoeken margarine of vet wordt opgelost in een vetoplosmiddel, waaraan vervolgens een gekende hoeveelheid broom-oplossing wordt toegevoegd. Br 2 reageert identiek, maar sneller met de dubbele bindingen dan I 2. Nadien doen we alsof het niet Br 2 maar I 2 was dat aan het vet geaddeerd werd. Daarna wordt een KI-oplossing toegevoegd, die met de overmaat Br 2 reageert tot I 2 en KBr. Het vrijgestelde I 2 wordt tenslotte getitreerd met een natriumthiosulfaatoplossing (Na 2 S 2 O 3 ). Schrijf de gebruikte reacties, uitgaande van de deelreacties. Duid onder de redoxreactie telkens aan wat in overmaat toegevoegd wordt. Welke concentratie, welk volume of welke hoeveelheid bepalen we via de titratie? Schrijf dit eveneens onder de betreffende reactie. Redeneer dan terug als we dit weten, kunnen we berekenen Beredeneer stap voor stap hoe je het jood (of praktisch broom ) getal uit deze titratie bekomt:
6 6 Br 2 -additie: Overmaat Br 2 + KI: Titratie van I 2 : Doe dezelfde redenering bij de blanco-proef. Er is dan geen vet, toch voeg je Br 2 bij (precies hetzelfde volume, uit dezelfde oplossing), er zal niets wegreageren,.enzovoort.
7 7 Ter illustratie geven we in volgende tabel voor enkele soorten vetten en oliën de waarde van het joodgetal. Vet kokosvet boter kakaoboter varkensvet olijfolie maïskiemolie zonnebloemolie lijnolie JG
8 8 1.3 Het verzepingsgetal De esterbindingen in triglyceriden (en ook fosfolipiden) kunnen gehydrolyseerd worden. Hydrolyse is splitsen met H 2 O. Als dit uitgevoerd wordt met NaOH of KOH als katalysatoren (boven pijl schrijven) ontstaan uit de gevormde vetzuren in reactie met deze basen, zogenaamde zouten (dus K + of Na + zouten) van vetzuren (dus zepen). Deze totale reactie noemt men de verzepingsreactie. Schrijf ze voor een triglyceride met de 2 deelreacties (hydrolyse en zuur-base reactie):
9 9 Omdat deze reactie stoechiometrisch uit te voeren is (aflopend en volgens de voorgetallen), kan je uit de verbruikte hoeveelheid base de hoeveelheid triglyceride per gewichtseenheid vet (in de veronderstelling dat al het vet bestaat uit triglyceriden) bepalen en dus ook het gemiddeld molecuulgewicht van de aanwezige vetzuren. Zo komt men tot het zogenaamde verzepingsgetal, dat een aanduiding is van de gemiddelde lengte van de vetzuurketens in de triglyceriden. Zoek de (hanteerbare!) definitie van het verzepingsgetal op: (eenheden!) Bereken hoeveel mol en hoeveel mg KOH nodig zijn uitgaande van g vet voor de verzepingsreactie en noteer dit onder de betreffende reactievergelijking van vorige bladzijde. Uit het verzepingsgetal (VP) haal je ook het (gemiddeld) molecuulgewicht (M r ) van de triglyceriden uit het vet of de olie. Leid een formule af (onder de reactievergelijking van vorige blz. Schrijf de formule dan over: Of M r omgekeerd: (triglyceride) als = je de lengte kent van de 3 vetzuren uit een triglyceride (n 1, n 2, n 3 : aantal koolstoffen) kan je het molecuulgewicht berekenen en het verzepingsgetal (VP). Of omgekeerd: als je de lengte kent van de 3 vetzuren uit een triglyceride kan je het molecuulgewicht berekenen en het verzepingsgetal (VP).
10 10 Boter bevat bijvoorbeeld nogal wat boterzuur (vandaar de benaming!), een zeer kort vetzuur (4 koolstoffen). Levert dit een relatief hoog of laag verzepingsgetal? Leg uit! Oefening: In een triglyceride hebben de eerste en de derde alkylgroep als formule (CH 2 ) 16 CH 3, en de tweede alkylgroep - (CH 2 ) 12 CH 3. Bereken het verzepingsgetal van dit triglyceride.
11 11 2 Kwalitatieve testen: lab 2.1 Oplosbaarheid van vetten a) In een reageerbuisje wordt een kleine hoeveelheid olie gebracht, er wordt 10 ml water toegevoegd, en er wordt krachtig geschud. b) Doe hetzelfde met telkens 10 ml van een organisch solvent zoals chloroform, ether of petroleumether. Noteer je waarnemingen (wat zie je?) en conclusies (hoe komt dit of wat betekent dit?): a. olie + water: b. olie + organisch solvent: 2.2 Emulgerende (emulsievorming) werking van zepen en detergenten 1. Principe De reinigende werking van zepen en detergenten steunt op het feit dat deze moleculen tensidemoleculen zijn of oppervlak actieve stoffen, die een hydrofiel (polair) en een hydrofoob (apolair) gedeelte in de molecule bezitten, wat hen geschikt maakt om vuildeeltjes (meestal apolair!) te omringen en zo in emulsie te houden in H 2 O via micelvorming. 2. Recept Breng in reageerbuis 1: 5 ml water reageerbuis 2: 5 ml water en enkele druppels zeepoplossing reageerbuis 3: 5 ml water en enkele druppels detergentoplossing Voeg bij elke reageerbuis 2 druppels olie, schud krachtig, en voeg vervolgens 2 druppels (niet teveel) Sudan III (0.1% in ethanol) toe, waardoor de vetten
12 12 gekleurd worden. Meng door krachtig schudden, en laat even rusten. Waar bevindt zich de kleurstof en waar dus de vetten? Conclusie? 1. olie + water + kleurstof: 2. olie + zeep + kleurstof: 3. olie + detergent + kleurstof 2.3 De onoplosbaarheid van calciumzepen 1. Principe Eén van de nadelen van de klassieke zepen is het feit dat ze met calciumionen onoplosbare calciumzepen vormen. Dit is trouwens één van de redenen waarom klassieke zepen niet meer gebruikt worden in waspoeder: de gevormde calciumzouten slaan neer op de te reinigen weefsels, en op de machineonderdelen. In deze test wordt de onoplosbaarheid in water van calciumzouten van zeep aangetoond. 2. Recept Breng in een reageerbuisje 5 ml zeepoplossing, en voeg druppel per druppel een 10% oplossing van CaCl 2 in water toe. Het ontstaan van een vlokkig neerslag wijst op de aanwezigheid van (RCOO) 2 Ca(v) (wit) Noteer je waarnemingen en conclusies: reactie:
13 13 3 Kwantitatieve testen: lab 3.1 Het joodgetal Principe Een maat voor het aantal dubbele bindingen in vetten of vetzuren is het joodgetal JG. Een typische organische reactie van koolstof-koolstof dubbele bindingen is de electrofiele additie van halogenen X 2 (Br 2 of I 2 ). Bij onverzadigde vetten of oliën kan men aan de C=C bindingen X 2 adderen, en bovendien is de hoeveelheid X 2 die hierbij geaddeerd wordt een maat voor het aantal koolstof-koolstof dubbele bindingen dat aanwezig is. Schrijf de reactie: Een maat voor de hoeveelheid X 2 die reageert met een bepaalde hoeveelheid vet of olie is het joodadditiegetal of joodgetal: het joodgetal geeft per definitie het aantal gram jood aan dat gebonden wordt door 100 gram vet of olie. Werk uit in een formule (JG) hoe je uit dit joodgetal het aantal dubbele bindingen (x) van een vet of olie (met gemiddeld M r ) bepaalt: (zie voorbereiding) formule: x = In deze proef bepalen we experimenteel het joodgetal van enkele merken van margarines, of van vetten.
14 14 gebruikt vet of olie: Recept: Weeg in een miniatuurbekertje (afgeslepen reageerbuisje) een hoeveelheid margarine of vet (na ontmengen: neem enkel uit de vetlaag!) af, in functie van het te verwachten jood-getal: verwacht joodgetal af te wegen aantal gram > Het vet wordt vooraf gesmolten en gefilterd om een emulsie (met H 2 O en gelatine) te breken. Je krijgt dan twee lagen. Let op dat je enkel materiaal neemt uit de apolaire laag (lichter). Breng het bekertje in een erlenmeyer van 500 ml, voeg 10 ml chloroform toe, en zwenk goed om, om de margarine of het vet op te lossen (bekertje niet uit de erlenmeyer nemen!). Voeg voorzichtig 25.0 ml broomreagens volgens Kaufmann toe, meng zeer voorzichtig door omzwenken, sluit de erlenmeyer met de stop, en laat 1 uur in het donker rusten. Voeg na 1 uur rusten 20 ml van een 10% KI oplossing in water toe, en 100 ml gedeïoniseerd water, en meng. Titreer met een natriumthiosulfaat-oplossing (ongeveer 0.1 N). Voeg aan het einde van de titratie enkele druppels zetmeeloplossing toe als indicator. Voer gelijktijdig hiermee op identieke wijze een blancoproef uit. Hiervoor wordt alleen 10 ml chloroform gebruikt, en 25.0 ml broomreagens (ook 1 uur in donker!). Bereken het joodgetal van het opgegeven vet. Controleer jezelf via de tabel!
15 15 Berekening: Besluit:
16 Het verzepingsgetal Principe: Zoals eerder vermeld zijn vetten en oliën triglyceriden. Deze triglyceriden kunnen door reactie met kaliumhydroxide gehydrolyseerd worden tot enerzijds glycerol en anderzijds tot zouten van vetzuren. Deze zouten van vetzuren worden gebruikt als zeep, en om die reden wordt de hydrolyse van triglyceriden ook de verzeping van de triglyceriden genoemd. De hoeveelheid KOH die nodig is om een welbepaalde hoeveelheid triglyceride te verzepen bepaalt het verzepingsgetal VP. Het verzepingsgetal geeft per definitie het aantal mg KOH aan dat nodig is voor de volledige verzeping van 1 gram triglyceride. Dit verzepingsgetal is een maat voor de molecuulmassa van het triglyceride. Inderdaad, indien het gaat om korte vetzuurketens in het triglyceride dan heeft dit triglyceride een relatief kleine molecuulmassa, zodat 1 gram triglyceride een relatief groot aantal mol vertegenwoordigt. Bij de hydrolyse is dan ook meer KOH nodig dan bij de hydrolyse van 1 gram triglyceride met langere ketens, dat dus ook een grotere molecuulmassa bezit. Het verzepingsgetal is dus omgekeerd evenredig met de molecuulmassa van het triglyceride. Dit verzepingsgetal kan experimenteel bepaald worden: een gekende hoeveelheid triglyceride wordt verhit met een gekende overmaat KOH tot volledige verzeping. De overmaat KOH wordt vervolgens teruggetitreerd met een zuur van gekende normaliteit. Een blanco-proef completeert het geheel. Recept: Ongeveer 1 gram margarine of vet wordt nauwkeurig afgewogen in een erlenmeyer van 250 ml. Met een pipet wordt 25.0 ml van een 0.5 N KOH oplossing in ethanol toegevoegd, en enkele kooksteentjes. De erlenmeyer wordt verbonden met een terugvloeikoeler, en op een draadnet aan de kook gebracht. Er wordt gedurende 30 minuten zachtjes gekookt, waarbij de vloeistof helder wordt. In het begin wordt regelmatig omgezwenkt om de margarine of het vet te laten oplossen.
17 17 Aan de nog warme vloeistof wordt 1 ml fenolftaleïne-indicator (1%) toegevoegd, en de warme vloeistof wordt getitreerd met een HCl oplossing van ongeveer 0.5 N. Op identieke wijze (ook 30 min. refluxen!) wordt een blancoproef uitgevoerd, waarbij het vet of de olie vervangen wordt door 1 ml water. Bepaal het verzepingsgetal van je vet of olie. Bereken het gemiddeld M r van de vetzuren erin en vergelijk met de andere onderzochte vetten. Berekening: Conclusie:
18 Samenvatting Gemiddeld aantal dubbele bindingen Uit het joodgetal kan je het aantal dubbele bindingen (X) halen als je het gemiddeld Mvan r de triglyceriden uit het vet of de olie kent. Deze heb je berekend bij het verzepingsgetal. Bereken nu het gemiddeld aantal dubbele bindingen in de triglyceriden: - gebruikte olie of vet: - Joodgetal: JG = in juiste eenheden - Verzepingsgetal: VP = in juiste eenheden - gemiddeld M r : = - formule: X = - berekening: - conclusie:
19 Vergelijking van diverse oliën en vetten In de loop der jaren verzamelden we volgende gegevens: Staal Joodgetal Verzepingsgetal Molecuulmassa Boter Solo Planta (bakboter) Bertolli (bakboter) Olijfolie Vitelma (bakken en braden) Minelma (minarine) , Vitelma (smeren) Walnotenolie Effi Witte producten - braad Becel Roda Alpro Minarine Santane Maïskiemolie Solo vloeibaar Becel Essential
20 20 Bespreek deze tabel (inclusief jouw resultaten en deze van je medestudenten). Houd hierbij ook rekening met de (na smelten) zichtbare hoeveelheid water in het vet: kijk dit na voor de verschillende vetten die dit jaar rondgedeeld werden. bespreking: Let op dat je de betekenis van de verschillende begrippen benadrukt! Dus niet enkel getallen en groter of kleiner, ook de consequentie ervan.
H C H. 4-amino-2-pentanon propylmethanoaat 4-hydroxy-2-methyl-2-buteenzuur. 2,3-dihydroxypropanal
 efenopgaven hoofdstuk 12 1 pgave 1 Geef de systematische naam van de volgende stoffen: 2 2 2 4-amino-2-pentanon propylmethanoaat 4-hydroxy-2-methyl-2-buteenzuur 2 2 -methoxycycolpentaancarbonzuur de ester
efenopgaven hoofdstuk 12 1 pgave 1 Geef de systematische naam van de volgende stoffen: 2 2 2 4-amino-2-pentanon propylmethanoaat 4-hydroxy-2-methyl-2-buteenzuur 2 2 -methoxycycolpentaancarbonzuur de ester
Basisscheikunde voor het hbo ISBN e druk Uitgeverij Syntax media
 Hoofdstuk 11 Biomoleculen bladzijde 1 Opgave 1 Geef de reactie van de verbranding van glucose (C 6H 12O 6) tot CO 2 en water. C 6H 12O 6 + 6 O 2 6 CO 2 + 6 H 2O Opgave 2 Hoe luidt de reactie (bruto formules)
Hoofdstuk 11 Biomoleculen bladzijde 1 Opgave 1 Geef de reactie van de verbranding van glucose (C 6H 12O 6) tot CO 2 en water. C 6H 12O 6 + 6 O 2 6 CO 2 + 6 H 2O Opgave 2 Hoe luidt de reactie (bruto formules)
INHOUDSTAFEL IN TE VULLEN PRACTICAVERSLAGEN
 1 INHOUDSTAFEL IN TE VULLEN PRACTICAVERSLAGEN VERSLAG PRACTICUM 1: VASTE EN VLOEIBARE ZEEP UIT OLIËN BEREIDEN 5 1 DOELSTELLING 5 2 PRINCIPE EN PROCEDURE 5 3 REACTIEVERGELIJKINGEN 6 4 OPSTELLING 6 5 WAARNEMINGEN
1 INHOUDSTAFEL IN TE VULLEN PRACTICAVERSLAGEN VERSLAG PRACTICUM 1: VASTE EN VLOEIBARE ZEEP UIT OLIËN BEREIDEN 5 1 DOELSTELLING 5 2 PRINCIPE EN PROCEDURE 5 3 REACTIEVERGELIJKINGEN 6 4 OPSTELLING 6 5 WAARNEMINGEN
ßCalciumChloride oplossing
 Samenvatting door R. 1673 woorden 17 februari 2013 8 1 keer beoordeeld Vak Methode Scheikunde Pulsar chemie Additiereactie Bij een reactie tussen hexeen en broom springt de C=C binding open. Aan het molecuul
Samenvatting door R. 1673 woorden 17 februari 2013 8 1 keer beoordeeld Vak Methode Scheikunde Pulsar chemie Additiereactie Bij een reactie tussen hexeen en broom springt de C=C binding open. Aan het molecuul
H18 Opdracht 5: Voedingsstoffen in blanke vla
 H18 Opdracht 5: Voedingsstoffen in blanke vla Hoe toon je aan welke voedingsstoffen blanke vla bevat? In je onderzoek probeer je water, suiker, zetmeel, eiwit en vet aan te tonen. a. Bedenk zelf een methode
H18 Opdracht 5: Voedingsstoffen in blanke vla Hoe toon je aan welke voedingsstoffen blanke vla bevat? In je onderzoek probeer je water, suiker, zetmeel, eiwit en vet aan te tonen. a. Bedenk zelf een methode
Koolstofverbindingen 2
 Koolstofverbindingen 2 Een samenvatting van hoofdstuk 15 1 Inleiding Koolstofverbindingen uit hoofdstuk 5 algemene voorbeeld naam formule Alkanen C n H 2n+2 2,3-dimethylbutaan Alkenen C n H 2n 2-methyl-2-
Koolstofverbindingen 2 Een samenvatting van hoofdstuk 15 1 Inleiding Koolstofverbindingen uit hoofdstuk 5 algemene voorbeeld naam formule Alkanen C n H 2n+2 2,3-dimethylbutaan Alkenen C n H 2n 2-methyl-2-
Esters. Versie 1 November 2014
 Esters Versie 1 November 2014 Gepubliceerd en gedistribueerd door Universiteit Utrecht Departement Scheikunde Onderwijsinstituut Scheikunde Padualaan 8 3584 CH Utrecht Nederland Ontwikkelaar: Anneke Drost,
Esters Versie 1 November 2014 Gepubliceerd en gedistribueerd door Universiteit Utrecht Departement Scheikunde Onderwijsinstituut Scheikunde Padualaan 8 3584 CH Utrecht Nederland Ontwikkelaar: Anneke Drost,
Overzicht van reactievergelijkingen Scheikunde
 verzicht van reactievergelijkingen Scheikunde Algemeen Verbranding Een verbranding is een reactie met zuurstof. ierbij ontstaan de oxiden van de elementen. Volledige verbranding Bij volledige verbranding
verzicht van reactievergelijkingen Scheikunde Algemeen Verbranding Een verbranding is een reactie met zuurstof. ierbij ontstaan de oxiden van de elementen. Volledige verbranding Bij volledige verbranding
Examen VWO. scheikunde 1,2. tijdvak 1 dinsdag 26 mei 13.30-16.30 uur. Bij dit examen horen een bijlage en een uitwerkbijlage.
 Examen VWO 2009 tijdvak 1 dinsdag 26 mei 13.30-16.30 uur scheikunde 1,2 Bij dit examen horen een bijlage en een uitwerkbijlage. Dit examen bestaat uit 23 vragen. Voor dit examen zijn maximaal 68 punten
Examen VWO 2009 tijdvak 1 dinsdag 26 mei 13.30-16.30 uur scheikunde 1,2 Bij dit examen horen een bijlage en een uitwerkbijlage. Dit examen bestaat uit 23 vragen. Voor dit examen zijn maximaal 68 punten
Samenvatting Scheikunde Hoofdstuk 1 + 2
 Samenvatting Scheikunde Hoofdstuk 1 + 2 Samenvatting door K. 1077 woorden 22 maart 2016 6,1 9 keer beoordeeld Vak Scheikunde Impact 3 vwo Scheikunde hoofdstuk 1 + 2 Paragraaf 1: Stoffen bijv. Glas en hout,
Samenvatting Scheikunde Hoofdstuk 1 + 2 Samenvatting door K. 1077 woorden 22 maart 2016 6,1 9 keer beoordeeld Vak Scheikunde Impact 3 vwo Scheikunde hoofdstuk 1 + 2 Paragraaf 1: Stoffen bijv. Glas en hout,
Natuurlijk heb je nu nog géén massa s berekend. Maar dat kan altijd later nog. En dan kun je mooi kiezen, van welke stoffen je de massa wil berekenen.
 Hoofdstuk 17: Rekenen in molverhoudingen 17.1 Rekenen aan reacties: een terugblik én een alternatief In hoofdstuk 11 hebben we gerekend aan reacties. Het achterliggende idee was vaak, dat je bij een reactie
Hoofdstuk 17: Rekenen in molverhoudingen 17.1 Rekenen aan reacties: een terugblik én een alternatief In hoofdstuk 11 hebben we gerekend aan reacties. Het achterliggende idee was vaak, dat je bij een reactie
Vitamine C bepalen uit fruitsap
 Vitamine C bepalen uit fruitsap 1. Onderzoeksvraag Hoe kunnen we de gehalte vitamine C in fruitsap bepalen? 2. Voorbereiding a. Begrippen als achtergrond voor experiment Zuur-basetitratie : een titratietechniek
Vitamine C bepalen uit fruitsap 1. Onderzoeksvraag Hoe kunnen we de gehalte vitamine C in fruitsap bepalen? 2. Voorbereiding a. Begrippen als achtergrond voor experiment Zuur-basetitratie : een titratietechniek
Oefenvraagstukken 4 VWO Hoofdstuk 6 antwoordmodel
 efenvraagstukken 4 VW oofdstuk 6 antwoordmodel Een 0 D komt overeen met 7,1 mg a 2+ per liter water. 1 In 0,5 liter water is 58,3 mg a 2+ opgelost. oeveel 0 D is dit? Per L opgelost: 2 x 58,3 mg a 2+ =
efenvraagstukken 4 VW oofdstuk 6 antwoordmodel Een 0 D komt overeen met 7,1 mg a 2+ per liter water. 1 In 0,5 liter water is 58,3 mg a 2+ opgelost. oeveel 0 D is dit? Per L opgelost: 2 x 58,3 mg a 2+ =
NATIONALE SCHEIKUNDEOLYMPIADE
 NATIONALE SCHEIKUNDEOLYMPIADE CORRECTIEMODEL VOORRONDE 1 af te nemen in de periode van woensdag 5 januari 01 tot en met woensdag 1 februari 01 Deze voorronde bestaat uit 4 meerkeuzevragen verdeeld over
NATIONALE SCHEIKUNDEOLYMPIADE CORRECTIEMODEL VOORRONDE 1 af te nemen in de periode van woensdag 5 januari 01 tot en met woensdag 1 februari 01 Deze voorronde bestaat uit 4 meerkeuzevragen verdeeld over
Examen VWO. Scheikunde 1 (nieuwe stijl)
 Scheikunde 1 (nieuwe stijl) Examen VW Voorbereidend Wetenschappelijk nderwijs Tijdvak 1 Maandag 27 mei 13.30 16.30 uur 20 02 Voor dit examen zijn maximaal 66 punten te behalen; het examen bestaat uit 24
Scheikunde 1 (nieuwe stijl) Examen VW Voorbereidend Wetenschappelijk nderwijs Tijdvak 1 Maandag 27 mei 13.30 16.30 uur 20 02 Voor dit examen zijn maximaal 66 punten te behalen; het examen bestaat uit 24
Vraag Antwoord Scores
 Ademtest 1 maximumscore 2 Voorbeelden van een juist antwoord zijn: Een ureummolecuul bevat NH 2 groepen / N-H bindingen, zodat er waterstbruggen (met watermoleculen) gevormd kunnen worden. (Dus ureum is
Ademtest 1 maximumscore 2 Voorbeelden van een juist antwoord zijn: Een ureummolecuul bevat NH 2 groepen / N-H bindingen, zodat er waterstbruggen (met watermoleculen) gevormd kunnen worden. (Dus ureum is
Eindexamen scheikunde havo 2008-I
 Beoordelingsmodel Uraan 1 maximumscore 2 aantal protonen: 92 aantal neutronen: 146 aantal protonen: 92 1 aantal neutronen: 238 verminderen met het aantal protonen 1 2 maximumscore 2 UO 2 + 4 HF UF 4 +
Beoordelingsmodel Uraan 1 maximumscore 2 aantal protonen: 92 aantal neutronen: 146 aantal protonen: 92 1 aantal neutronen: 238 verminderen met het aantal protonen 1 2 maximumscore 2 UO 2 + 4 HF UF 4 +
Bacteriën maken zwavel Vragen en opdrachten bij de poster
 Vragen en opdrachten bij de poster Bacteriën maken zwavel Vragen en opdrachten bij de poster 3 vwo Probleem: Zuur gas T1 Waterstofsulfide ontstaat bij de afbraak van zwavelhoudende organische stoffen.
Vragen en opdrachten bij de poster Bacteriën maken zwavel Vragen en opdrachten bij de poster 3 vwo Probleem: Zuur gas T1 Waterstofsulfide ontstaat bij de afbraak van zwavelhoudende organische stoffen.
(2) 1 Geef de systematische naam van de volgende stof. C CH 3. (2) 2 Geef de systematische naam van de volgende stof.
 Bij alle berekeningen moeten de antwoorden in wetenschappelijke notatie, in het juiste aantal significante cijfers en indien nodig met de juiste eenheid weergegeven worden. (2) 1 Geef de systematische
Bij alle berekeningen moeten de antwoorden in wetenschappelijke notatie, in het juiste aantal significante cijfers en indien nodig met de juiste eenheid weergegeven worden. (2) 1 Geef de systematische
Opgave 1. Opgave 2. b En bij een verbruik van 10 ml? Dan wordt de procentuele onnauwkeurigheid 2 x zo groot: 0,03 / 20 x 100% = 0,3% Opgave 3
 Hoofdstuk 13 Titratieberekeningen bladzijde 1 Opgave 1 Wat is het theoretisch eindpunt? Het theoretisch eindpunt is het titratievolume waarbij de bedoelde reactie precies is afgelopen. En wat is dan het
Hoofdstuk 13 Titratieberekeningen bladzijde 1 Opgave 1 Wat is het theoretisch eindpunt? Het theoretisch eindpunt is het titratievolume waarbij de bedoelde reactie precies is afgelopen. En wat is dan het
Eindexamen scheikunde havo 2001-II
 Eindexamen scheikunde havo 00-II 4 Antwoordmodel Energievoorziening in de ruimte et (uiteenvallen van de Pu-38 atomen) levert energie dus het is een exotherm proces. er komt energie vrij aantal protonen:
Eindexamen scheikunde havo 00-II 4 Antwoordmodel Energievoorziening in de ruimte et (uiteenvallen van de Pu-38 atomen) levert energie dus het is een exotherm proces. er komt energie vrij aantal protonen:
Samenvatting Scheikunde H6 (Chemie)
 Samenvatting Scheikunde H6 (Chemie) Samenvatting door een scholier 892 woorden 18 maart 2004 5,1 73 keer beoordeeld Vak Scheikunde Scheikunde Hoofdstuk 6 Twee soorten bindingen bij moleculaire stoffen:
Samenvatting Scheikunde H6 (Chemie) Samenvatting door een scholier 892 woorden 18 maart 2004 5,1 73 keer beoordeeld Vak Scheikunde Scheikunde Hoofdstuk 6 Twee soorten bindingen bij moleculaire stoffen:
1. Elementaire chemie en chemisch rekenen
 In onderstaande zelftest zijn de vragen gebundeld die als voorbeeldvragen zijn opgenomen in het bijhorend overzicht van de verwachte voorkennis chemie 1. Elementaire chemie en chemisch rekenen 1.1 Grootheden
In onderstaande zelftest zijn de vragen gebundeld die als voorbeeldvragen zijn opgenomen in het bijhorend overzicht van de verwachte voorkennis chemie 1. Elementaire chemie en chemisch rekenen 1.1 Grootheden
Uitwerkingen van de opgaven uit: BASISCHEMIE voor het MLO ISBN , 3 e druk, Uitgeverij Syntax Media Hoofdstuk 18 Oxidimetrie bladzijde 1
 Hoofdstuk 18 Oxidimetrie bladzijde 1 Opgave 1 Bepaal met behulp van tabel II de reactie tussen kaliumpermanganaat in zuur milieu met: a Sn 2+ ionen MnO 4 + 8 H 3O + + 5 e Mn 2+ + 12 H 2O x 2 Sn 2+ Sn 4+
Hoofdstuk 18 Oxidimetrie bladzijde 1 Opgave 1 Bepaal met behulp van tabel II de reactie tussen kaliumpermanganaat in zuur milieu met: a Sn 2+ ionen MnO 4 + 8 H 3O + + 5 e Mn 2+ + 12 H 2O x 2 Sn 2+ Sn 4+
Uitwerkingen. T2: Verbranden en Ontleden, De snelheid van een reactie en Verbindingen en elementen
 Uitwerkingen T2: Verbranden en Ontleden, De snelheid van een reactie en Verbindingen en elementen 2008 Voorbeeld toets dinsdag 29 februari 60 minuten NASK 2, 2(3) VMBO-TGK, DEEL B. H5: VERBRANDEN EN ONTLEDEN
Uitwerkingen T2: Verbranden en Ontleden, De snelheid van een reactie en Verbindingen en elementen 2008 Voorbeeld toets dinsdag 29 februari 60 minuten NASK 2, 2(3) VMBO-TGK, DEEL B. H5: VERBRANDEN EN ONTLEDEN
T2: Verbranden en Ontleden, De snelheid van een reactie en Verbindingen en elementen
 T2: Verbranden en Ontleden, De snelheid van een reactie en Verbindingen en elementen 2008 Voorbeeld toets dinsdag 29 februari 60 minuten NASK 2, 2(3) VMBO-TGK, DEEL B. H5: VERBRANDEN EN ONTLEDEN 3(4) VMBO-TGK,
T2: Verbranden en Ontleden, De snelheid van een reactie en Verbindingen en elementen 2008 Voorbeeld toets dinsdag 29 februari 60 minuten NASK 2, 2(3) VMBO-TGK, DEEL B. H5: VERBRANDEN EN ONTLEDEN 3(4) VMBO-TGK,
Eindexamen scheikunde 1 vwo 2008-I
 Beoordelingsmodel Vrije vetzuren in olijfolie 1 maximumscore 1 hydrolyse Indien het antwoord verzeping of ontleding of evenwichtsreactie is gegeven 0 2 maximumscore 2 Een juist antwoord kan als volgt zijn
Beoordelingsmodel Vrije vetzuren in olijfolie 1 maximumscore 1 hydrolyse Indien het antwoord verzeping of ontleding of evenwichtsreactie is gegeven 0 2 maximumscore 2 Een juist antwoord kan als volgt zijn
Dit examen bestaat voor iedere kandidaat uit 20 vragen
 MAVO-4 II EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN 1982 MAVO-4 Woensdag 15 juni, 9.00 11.00 NATUUR-EN SCHEIKUNDE II (Scheikunde) MEERKEUZETOETS Dit examen bestaat voor iedere kandidaat uit 20
MAVO-4 II EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN 1982 MAVO-4 Woensdag 15 juni, 9.00 11.00 NATUUR-EN SCHEIKUNDE II (Scheikunde) MEERKEUZETOETS Dit examen bestaat voor iedere kandidaat uit 20
Hoofdstuk 4 Kwantitatieve aspecten
 Hoofdstuk 4 Kwantitatieve aspecten 4.1 Deeltjesmassa 4.1.1 Atoommassa De SI-eenheid van massa is het kilogram (kg). De massa van een H-atoom is gelijk aan 1,66 10 27 kg. m(h) = 0,000 000 000 000 000 000
Hoofdstuk 4 Kwantitatieve aspecten 4.1 Deeltjesmassa 4.1.1 Atoommassa De SI-eenheid van massa is het kilogram (kg). De massa van een H-atoom is gelijk aan 1,66 10 27 kg. m(h) = 0,000 000 000 000 000 000
Eindexamen scheikunde pilot vwo II
 Beoordelingsmodel Zelfherstellende verf 1 maximumscore 2 Voorbeelden van een juist antwoord zijn: C C C ( ) 6 C dubbele binding tussen en C in de isocyanaatgroepen 1 dubbele binding tussen C en in de isocyanaatgroepen
Beoordelingsmodel Zelfherstellende verf 1 maximumscore 2 Voorbeelden van een juist antwoord zijn: C C C ( ) 6 C dubbele binding tussen en C in de isocyanaatgroepen 1 dubbele binding tussen C en in de isocyanaatgroepen
Scheikunde VWO. Vrijdag 19 mei 1995 13.30 16.30 uur. vragen
 Scheikunde VWO vragen Vrijdag 19 mei 1995 1330 1630 uur toelichting Dit examen bestaat uit 23 vragen Voor elk vraagnummer is aangegeven hoeveel punten met een goed antwoord behaald kunnen worden instructie
Scheikunde VWO vragen Vrijdag 19 mei 1995 1330 1630 uur toelichting Dit examen bestaat uit 23 vragen Voor elk vraagnummer is aangegeven hoeveel punten met een goed antwoord behaald kunnen worden instructie
Een stof heeft altijd stofeigenschappen. Door hier gebruik van te maken, kun je stoffen makkelijk scheiden.
 Stoffen scheiden Schrijf bij elke proef steeds je waarnemingen in je schrift. Bij het doen van experimenten is het belangrijk dat je goed opschrijft wat je hebt gedaan, zodat andere mensen jouw experiment
Stoffen scheiden Schrijf bij elke proef steeds je waarnemingen in je schrift. Bij het doen van experimenten is het belangrijk dat je goed opschrijft wat je hebt gedaan, zodat andere mensen jouw experiment
Uitwerkingen van de opgaven uit: CHEMISCHE ANALYSE ISBN , 1 e druk, Uitgeverij Syntax Media Hoofdstuk 4 Oxidimetrie bladzijde 1
 Hoofdstuk 4 Oxidimetrie bladzijde 1 Opgave 1 Hoe groot is het oxidatiegetal van elk atoom in de onderstaande deeltjes? Uitgangspunten: H = +1 O = 2 metaalion (K + ) krijgt ionlading. som van de ladingen
Hoofdstuk 4 Oxidimetrie bladzijde 1 Opgave 1 Hoe groot is het oxidatiegetal van elk atoom in de onderstaande deeltjes? Uitgangspunten: H = +1 O = 2 metaalion (K + ) krijgt ionlading. som van de ladingen
Samenvatting Scheikunde Hoofdstuk 1
 Samenvatting Scheikunde Hoofdstuk 1 Samenvatting door W. 1173 woorden 23 juni 2016 6,9 16 keer beoordeeld Vak Methode Scheikunde Nova Scheikunde Samenvatting H1 1 t/m 7 1 Atoombouw: Atoom: Opgebouwd uit
Samenvatting Scheikunde Hoofdstuk 1 Samenvatting door W. 1173 woorden 23 juni 2016 6,9 16 keer beoordeeld Vak Methode Scheikunde Nova Scheikunde Samenvatting H1 1 t/m 7 1 Atoombouw: Atoom: Opgebouwd uit
scheikunde havo 2017-I
 Contrastmiddel voor MRI-scans 1 maximumscore 3 aantal protonen: 64 aantal neutronen: 94 aantal elektronen: 61 aantal protonen juist 1 aantal neutronen: 158 verminderd met het aantal protonen 1 aantal elektronen:
Contrastmiddel voor MRI-scans 1 maximumscore 3 aantal protonen: 64 aantal neutronen: 94 aantal elektronen: 61 aantal protonen juist 1 aantal neutronen: 158 verminderd met het aantal protonen 1 aantal elektronen:
30 ste Vlaamse Chemie Olympiade
 30 ste Vlaamse Chemie Olympiade 2012-2013 2 de ronde 20 februari 2013 Je naam en voornaam: E-mail: Je adres: De naam van je school: Het adres van je school: Je leerjaar: Aantal lesuren chemie per week
30 ste Vlaamse Chemie Olympiade 2012-2013 2 de ronde 20 februari 2013 Je naam en voornaam: E-mail: Je adres: De naam van je school: Het adres van je school: Je leerjaar: Aantal lesuren chemie per week
5 Water, het begrip ph
 5 Water, het begrip ph 5.1 Water Waterstofchloride is een sterk zuur, het reageert als volgt met water: HCI(g) + H 2 0(I) Cl (aq) + H 3 O + (aq) z b Hierbij reageert water als base. Ammoniak is een zwakke
5 Water, het begrip ph 5.1 Water Waterstofchloride is een sterk zuur, het reageert als volgt met water: HCI(g) + H 2 0(I) Cl (aq) + H 3 O + (aq) z b Hierbij reageert water als base. Ammoniak is een zwakke
SE voorbeeldtoets 5HAVO antwoordmodel
 SE voorbeeldtoets 5AV antwoordmodel Stikstof Zwaar stikstofgas bestaat uit stikstofmoleculen waarin uitsluitend stikstofatomen voorkomen met massagetal 15. 2p 1 oeveel protonen en hoeveel neutronen bevat
SE voorbeeldtoets 5AV antwoordmodel Stikstof Zwaar stikstofgas bestaat uit stikstofmoleculen waarin uitsluitend stikstofatomen voorkomen met massagetal 15. 2p 1 oeveel protonen en hoeveel neutronen bevat
Hoofdstuk 6: Zure en base oplossingen / ph
 Hoofdstuk 6: Zure en base oplossingen / ph 6.1 Herhaling: zure en basische oplossingen Arrhenius definieerde zuren als volgt: zuren zijn polaire covalente verbindingen die bij het oplossen in water H +
Hoofdstuk 6: Zure en base oplossingen / ph 6.1 Herhaling: zure en basische oplossingen Arrhenius definieerde zuren als volgt: zuren zijn polaire covalente verbindingen die bij het oplossen in water H +
5 VWO. H8 zuren en basen
 5 VWO H8 zuren en basen Inleiding Opdracht 1, 20 min in tweetallen Nakijken; eventueel vragen stellen 8.2 Zure, neutrale en basische oplossingen 8.2 Zure, neutrale en Indicator (tabel 52A) Zuurgraad 0-14?
5 VWO H8 zuren en basen Inleiding Opdracht 1, 20 min in tweetallen Nakijken; eventueel vragen stellen 8.2 Zure, neutrale en basische oplossingen 8.2 Zure, neutrale en Indicator (tabel 52A) Zuurgraad 0-14?
Fosfor kan met waterstof reageren. d Geef de vergelijking van de reactie van fosfor met waterstof.
 1 Een oplossing van zwavelzuur en een oplossing van bariumhydroxide geladen beide elektriciteit. Wordt bij de zwavelzuuroplossing een oplossing van bariumhydroxide gedruppeld, dan neemt het elektrisch
1 Een oplossing van zwavelzuur en een oplossing van bariumhydroxide geladen beide elektriciteit. Wordt bij de zwavelzuuroplossing een oplossing van bariumhydroxide gedruppeld, dan neemt het elektrisch
scheikunde bezem vwo 2016-I
 Polyaspartaat 1 maximumscore 3 Ca 2+ + 2 HCO 3 CaCO 3 + H 2 O + CO 2 Ca 2+ en HCO 3 voor de pijl 1 CaCO 3, H 2 O en CO 2 na de pijl 1 juiste coëfficiënten 1 Opmerking Wanneer de vergelijking Ca 2+ + 2
Polyaspartaat 1 maximumscore 3 Ca 2+ + 2 HCO 3 CaCO 3 + H 2 O + CO 2 Ca 2+ en HCO 3 voor de pijl 1 CaCO 3, H 2 O en CO 2 na de pijl 1 juiste coëfficiënten 1 Opmerking Wanneer de vergelijking Ca 2+ + 2
TITRATIES Een korte inleiding en voorbeelden voor het HAVO en VWO
 TITRATIES Een korte inleiding en voorbeelden voor het HAVO en VWO versie juli 2017 WOORD VOORAF De in dit document besproken titratiemethoden vormen de basis van de diverse varianten die in de loop der
TITRATIES Een korte inleiding en voorbeelden voor het HAVO en VWO versie juli 2017 WOORD VOORAF De in dit document besproken titratiemethoden vormen de basis van de diverse varianten die in de loop der
Werkboek: Excursie Sonac Vuren. Docent: R. van Hemert
 Werkboek: Excursie Sonac Vuren Namen: Datum Docent: R. van Hemert Inhoud Inleiding... 3 Productieproces... 3 Routebeschrijving... 4 Regels... 6 Voorschriften... 7 Deeltjesgrootteverdeling van beenderschroot....
Werkboek: Excursie Sonac Vuren Namen: Datum Docent: R. van Hemert Inhoud Inleiding... 3 Productieproces... 3 Routebeschrijving... 4 Regels... 6 Voorschriften... 7 Deeltjesgrootteverdeling van beenderschroot....
Om een zo duidelijk mogelijk verslag te maken, hebben we de vragen onderverdeeld in 4 categorieën.
 Beste leerling, Dit document bevat het examenverslag voor leerlingen van het scheikunde havo, tweede tijdvak (2017). In dit examenverslag proberen we een zo goed mogelijk antwoord te geven op de volgende
Beste leerling, Dit document bevat het examenverslag voor leerlingen van het scheikunde havo, tweede tijdvak (2017). In dit examenverslag proberen we een zo goed mogelijk antwoord te geven op de volgende
Eindexamen scheikunde havo 2001-I
 Eindexamen scheikunde havo -I 4 Antwoordmodel Nieuw element (in de tekst staat:) deze atomen zijn eerst ontdaan van een aantal elektronen dus de nikkeldeeltjes zijn positief geladen Indien in een overigens
Eindexamen scheikunde havo -I 4 Antwoordmodel Nieuw element (in de tekst staat:) deze atomen zijn eerst ontdaan van een aantal elektronen dus de nikkeldeeltjes zijn positief geladen Indien in een overigens
EXAMEN SCHEIKUNDE VWO 1983 EERSTE TIJDVAK opgaven
 EXAMEN SCHEIKUNDE VWO 1983 EERSTE TIJDVAK opgaven Eliminatie 1983-I(I) Als uit een molecuul twee atomen of atoomgroepen worden verwijderd waarbij in het molecuul een meervoudige binding ontstaat, dan spreekt
EXAMEN SCHEIKUNDE VWO 1983 EERSTE TIJDVAK opgaven Eliminatie 1983-I(I) Als uit een molecuul twee atomen of atoomgroepen worden verwijderd waarbij in het molecuul een meervoudige binding ontstaat, dan spreekt
Redoxreacties. Gegeven zijn de volgende reactievergelijkingen: Reactie 1: Pd Cl - 2- PdCl 4 Reactie 2: 2 Cu I - -
 Redoxreacties 5vwo Opgave 1 Redox of niet? Gegeven zijn de volgende reactievergelijkingen: Reactie 1: Pd 2+ + 4 Cl - 2- PdCl 4 Reactie 2: 2 Cu 2+ + 5 I - - 2 CuI + I 3 Leg voor elk van beide reacties uit
Redoxreacties 5vwo Opgave 1 Redox of niet? Gegeven zijn de volgende reactievergelijkingen: Reactie 1: Pd 2+ + 4 Cl - 2- PdCl 4 Reactie 2: 2 Cu 2+ + 5 I - - 2 CuI + I 3 Leg voor elk van beide reacties uit
Scheikunde SE2. Hoofdstuk 8
 Scheikunde SE2 Hoofdstuk 8 Paragraaf 2 Indicatoren: stoffen waarmee je kunt bepalen of een oplossing zuur of basisch is. Zuur: als een oplossing een ph heeft van minder dan 7. Basisch: als een oplossing
Scheikunde SE2 Hoofdstuk 8 Paragraaf 2 Indicatoren: stoffen waarmee je kunt bepalen of een oplossing zuur of basisch is. Zuur: als een oplossing een ph heeft van minder dan 7. Basisch: als een oplossing
NATIONALE SCHEIKUNDEOLYMPIADE
 NATIONALE SCHEIKUNDEOLYMPIADE CORRECTIEMODEL VOORRONDE 1 (de week van) woensdag 3 februari 2010 Deze voorronde bestaat uit 24 meerkeuzevragen verdeeld over 6 onderwerpen en 3 open vragen met in totaal
NATIONALE SCHEIKUNDEOLYMPIADE CORRECTIEMODEL VOORRONDE 1 (de week van) woensdag 3 februari 2010 Deze voorronde bestaat uit 24 meerkeuzevragen verdeeld over 6 onderwerpen en 3 open vragen met in totaal
Scheikundige begrippen
 Scheikundige begrippen Door: Ruby Vreedenburgh, Jesse Bosman, Colana van Klink en Fleur Jansen Scheikunde begrippen 1 Chemische reactie Ruby Vreedenburgh Overal om ons heen vinden er chemische reacties
Scheikundige begrippen Door: Ruby Vreedenburgh, Jesse Bosman, Colana van Klink en Fleur Jansen Scheikunde begrippen 1 Chemische reactie Ruby Vreedenburgh Overal om ons heen vinden er chemische reacties
Exo-energetische reactie: Een chemische reactie waarbij energie vrijgegeven wordt.
 Onweer onder water 1. Onderzoeksvraag Hoe kunnen we een onweer onder water nabootsen? 2. Voorbereiding a. Begrippen als achtergrond voor experiment Redoxreactie: Een reactie tussen atomen, moleculen en/of
Onweer onder water 1. Onderzoeksvraag Hoe kunnen we een onweer onder water nabootsen? 2. Voorbereiding a. Begrippen als achtergrond voor experiment Redoxreactie: Een reactie tussen atomen, moleculen en/of
Het is echter waarschijnlijker dat rood kwik bestaat uit Hg 2+ ionen en het biantimonaation met de formule Sb2O7 4.
 Lyceum Oudehoven Hoefslag 4 4205 NK Gorinchem Schoolexamen Leerjaar: 4 Vak: Scheikunde Datum: 26-06-2013 Tijd: 13.00 14.30 uur Uitdelen: opgavenvellen + proefwerkpapier Toegestaan: rekenmachine, potlood,
Lyceum Oudehoven Hoefslag 4 4205 NK Gorinchem Schoolexamen Leerjaar: 4 Vak: Scheikunde Datum: 26-06-2013 Tijd: 13.00 14.30 uur Uitdelen: opgavenvellen + proefwerkpapier Toegestaan: rekenmachine, potlood,
Mens erger je niet: chemistry edition
 Mens erger je niet: chemistry edition Behandelde leerstof: Het spel gaat over het thema: gedrag van stoffen in water. Inhoud: Het spel Mens erger je niet: chemistry edition bevat: - 1 spelbord - 1 dobbelsteen
Mens erger je niet: chemistry edition Behandelde leerstof: Het spel gaat over het thema: gedrag van stoffen in water. Inhoud: Het spel Mens erger je niet: chemistry edition bevat: - 1 spelbord - 1 dobbelsteen
Hoofdstuk 3: Zuren en basen
 Hoofdstuk 3: Zuren en basen Scheikunde VWO 2011/2012 www.lyceo.nl Onderwerpen Scheikunde 2011 2012 Stoffen, structuur en binding Kenmerken van Reacties Zuren en base Redox Chemische technieken Koolstofchemie
Hoofdstuk 3: Zuren en basen Scheikunde VWO 2011/2012 www.lyceo.nl Onderwerpen Scheikunde 2011 2012 Stoffen, structuur en binding Kenmerken van Reacties Zuren en base Redox Chemische technieken Koolstofchemie
1. Onderzoeksvraag Hoe kunnen we aan de hand van chemische reacties een oplossing de kleuren van een stoplicht krijgen?
 Chemisch stoplicht 1. Onderzoeksvraag Hoe kunnen we aan de hand van chemische reacties een oplossing de kleuren van een stoplicht krijgen? 2. Voorbereiding a. Begrippen als achtergrond voor experiment
Chemisch stoplicht 1. Onderzoeksvraag Hoe kunnen we aan de hand van chemische reacties een oplossing de kleuren van een stoplicht krijgen? 2. Voorbereiding a. Begrippen als achtergrond voor experiment
EUROPEAN UNION SCIENCE OLYMPIAD ANTWOORDENBUNDEL TEST 1 13 APRIL 13, 2010. Land:
 EUROPEAN UNION SCIENCE OLYMPIAD ANTWOORDENBUNDEL TEST 1 13 APRIL 13, 2010 Land: Team: Namen en handtekeningen 1 OPDRACHT 1 Relatieve vochtigheid van de lucht 1.1: Het dauwpunt is (noteer ook de eenheid)
EUROPEAN UNION SCIENCE OLYMPIAD ANTWOORDENBUNDEL TEST 1 13 APRIL 13, 2010 Land: Team: Namen en handtekeningen 1 OPDRACHT 1 Relatieve vochtigheid van de lucht 1.1: Het dauwpunt is (noteer ook de eenheid)
INSTITUUT VOOR BIOLOGISCH EN SCHEIKUNDIG ONDERZOEK VAN LANDBOUWGEWASSEN. Wageningen. Verslagen nr. 37, 1965
 INSTITUUT VOOR BIOLOGISCH EN SCHEIKUNDIG ONDERZOEK VAN LANDBOUWGEWASSEN Wageningen Verslagen nr. 37, 1965 VOORSCHRIFT VOOR HET ONDERZOEK VAN LIPIDEN IN RUWVOEDER EN IN FAECES VAN RUNDEREN dr. W.B. Deljs
INSTITUUT VOOR BIOLOGISCH EN SCHEIKUNDIG ONDERZOEK VAN LANDBOUWGEWASSEN Wageningen Verslagen nr. 37, 1965 VOORSCHRIFT VOOR HET ONDERZOEK VAN LIPIDEN IN RUWVOEDER EN IN FAECES VAN RUNDEREN dr. W.B. Deljs
Oplossingen oefeningenreeks 1
 Oplossingen oefeningenreeks 1 4. Door diffractie van X-stralen in natriumchloride-kristallen stelt men vast dat de eenheidscel van dit zout een kubus is waarvan de ribbe een lengte heeft van 5.64 10-10
Oplossingen oefeningenreeks 1 4. Door diffractie van X-stralen in natriumchloride-kristallen stelt men vast dat de eenheidscel van dit zout een kubus is waarvan de ribbe een lengte heeft van 5.64 10-10
Voor op brood (kuipjes 41 % totaal vet) Voor op brood (kuipjes > 41 % vet) Twenty Four Brio Light Becel pro.activ Calorie Light
 INFOKAART n van margarine-, halvarine- en bak- en braadproducten December 2016 - Het assortiment margarineproducten wordt steeds groter en sluit steeds beter aan op de wensen en eisen van de consument.
INFOKAART n van margarine-, halvarine- en bak- en braadproducten December 2016 - Het assortiment margarineproducten wordt steeds groter en sluit steeds beter aan op de wensen en eisen van de consument.
BUFFEROPLOSSINGEN. Inleiding
 BUFFEROPLOSSINGEN Inleiding Zowel in de analytische chemie als in de biochemie is het van belang de ph van een oplossing te regelen. Denk bijvoorbeeld aan een complexometrische titratie met behulp van
BUFFEROPLOSSINGEN Inleiding Zowel in de analytische chemie als in de biochemie is het van belang de ph van een oplossing te regelen. Denk bijvoorbeeld aan een complexometrische titratie met behulp van
Opgave 1. n = m / M. e 500 mg soda (Na 2CO 3) = 0,00472 mol. Opgave 2. m = n x M
 Hoofdstuk 8 Rekenen met de mol bladzijde 1 Opgave 1 n = m / M a 64,0 g zuurstofgas (O 2) = 2,00 mol (want n = 64,0 / 32,0) enz b 10,0 g butaan (C 4H 10) = 0,172 mol c 1,00 g suiker (C 12H 22O 11) = 0,00292
Hoofdstuk 8 Rekenen met de mol bladzijde 1 Opgave 1 n = m / M a 64,0 g zuurstofgas (O 2) = 2,00 mol (want n = 64,0 / 32,0) enz b 10,0 g butaan (C 4H 10) = 0,172 mol c 1,00 g suiker (C 12H 22O 11) = 0,00292
CENTRALE COMMISSIE VOORTENTAMEN SCHEIKUNDE TENTAMEN SCHEIKUNDE. datum : woensdag 26 januari 2011
 CENTRALE COMMISSIE VOORTENTAMEN SCHEIKUNDE TENTAMEN SCHEIKUNDE datum : woensdag 26 januari 2011 tijd : 19.00 tot 22.00 uur aantal opgaven : 6 Iedere opgave dient op een afzonderlijk vel te worden gemaakt
CENTRALE COMMISSIE VOORTENTAMEN SCHEIKUNDE TENTAMEN SCHEIKUNDE datum : woensdag 26 januari 2011 tijd : 19.00 tot 22.00 uur aantal opgaven : 6 Iedere opgave dient op een afzonderlijk vel te worden gemaakt
Om een zo duidelijk mogelijk verslag te maken, hebben we de examenvragen onderverdeeld in 4 categorieën.
 Beste leerling, Dit document bevat het examenverslag van het vak Scheikunde havo, eerste tijdvak (2014). In dit examenverslag proberen we zo goed mogelijk antwoord te geven op de volgende vraag: In hoeverre
Beste leerling, Dit document bevat het examenverslag van het vak Scheikunde havo, eerste tijdvak (2014). In dit examenverslag proberen we zo goed mogelijk antwoord te geven op de volgende vraag: In hoeverre
Opgaven zuurgraad (ph) berekenen. ph = -log [H + ] poh = -log [OH - ] [H + ] = 10 -ph [OH - ] = 10 -poh. ph = 14 poh poh = 14 ph ph + poh = 14
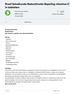
![Opgaven zuurgraad (ph) berekenen. ph = -log [H + ] poh = -log [OH - ] [H + ] = 10 -ph [OH - ] = 10 -poh. ph = 14 poh poh = 14 ph ph + poh = 14 Opgaven zuurgraad (ph) berekenen. ph = -log [H + ] poh = -log [OH - ] [H + ] = 10 -ph [OH - ] = 10 -poh. ph = 14 poh poh = 14 ph ph + poh = 14](/thumbs/82/85039734.jpg) Opgaven zuurgraad (ph) berekenen Met behulp van deze formules dien je berekeningen te kunnen uitvoeren. Deze hoef je niet uit je hoofd te leren, maar je moet ze wel kunnen toepassen. Bij een toets zullen
Opgaven zuurgraad (ph) berekenen Met behulp van deze formules dien je berekeningen te kunnen uitvoeren. Deze hoef je niet uit je hoofd te leren, maar je moet ze wel kunnen toepassen. Bij een toets zullen
Wat is de formule van het metaalchloride waarin M het symbool van het metaal voorstelt?
 Chemie Vraag 1 5,0.10-4 mol van een metaalchloride wordt opgelost in water. Er is 60 ml van een 2,5.10-2 mol.l -1 zilvernitraatoplossing nodig om alle chlorideionen neer te slaan onder de vorm van zilverchloride.
Chemie Vraag 1 5,0.10-4 mol van een metaalchloride wordt opgelost in water. Er is 60 ml van een 2,5.10-2 mol.l -1 zilvernitraatoplossing nodig om alle chlorideionen neer te slaan onder de vorm van zilverchloride.
Wat is de formule van het metaalchloride waarin M het symbool van het metaal voorstelt?
 Chemie Vraag 1 5,0.10-4 mol van een metaalchloride wordt opgelost in water. Er is 60 ml van een 2,5.10-2 mol.l -1 zilvernitraatoplossing nodig om alle chlorideionen neer te slaan onder de vorm van zilverchloride.
Chemie Vraag 1 5,0.10-4 mol van een metaalchloride wordt opgelost in water. Er is 60 ml van een 2,5.10-2 mol.l -1 zilvernitraatoplossing nodig om alle chlorideionen neer te slaan onder de vorm van zilverchloride.
Proef Scheikunde Redoxtitratie Bepaling vitamine C in tabletten
 Proef Scheikunde Redoxtitratie Bepaling vitamine C in tabletten Proef door een scholier 2025 woorden 19 maart 2010 6,2 112 keer beoordeeld Vak Scheikunde Verslag scheikunde Redoxtitratie Het vitamine c-gehalte
Proef Scheikunde Redoxtitratie Bepaling vitamine C in tabletten Proef door een scholier 2025 woorden 19 maart 2010 6,2 112 keer beoordeeld Vak Scheikunde Verslag scheikunde Redoxtitratie Het vitamine c-gehalte
Chemisch rekenen, zo doe je dat!
 1 Chemisch rekenen, zo doe je dat! GOE Opmerkingen vooraf: 1. Belangrijke schrijfwijzen: 100 = 10 2 ; 1000 = 10 3, enz. 0,1 = 1/10 = 10-1 ; 0,001 = 1/1000 = 10-3 ; 0,000.000.1 = 10-7, enz. gram/kg = gram
1 Chemisch rekenen, zo doe je dat! GOE Opmerkingen vooraf: 1. Belangrijke schrijfwijzen: 100 = 10 2 ; 1000 = 10 3, enz. 0,1 = 1/10 = 10-1 ; 0,001 = 1/1000 = 10-3 ; 0,000.000.1 = 10-7, enz. gram/kg = gram
Eindexamen scheikunde havo 2005-I
 4 Beoordelingsmodel Zeewater 1 Sr 2+ juist symbool 1 juiste lading bij gegeven symbool 1 2 aantal protonen: 6 aantal neutronen: 8 juiste aantal protonen 1 aantal neutronen: 14 verminderen met het aantal
4 Beoordelingsmodel Zeewater 1 Sr 2+ juist symbool 1 juiste lading bij gegeven symbool 1 2 aantal protonen: 6 aantal neutronen: 8 juiste aantal protonen 1 aantal neutronen: 14 verminderen met het aantal
Proef Scheikunde Het suikergehalte in Cola en Cola Light bepalen
 Proef Scheikunde Het suikergehalte in Cola en Cola Light bepalen Proef door een scholier 597 woorden 11 maart 24 5,6 22 keer beoordeeld Vak Scheikunde Proeven i.v.m. G.I.P. (suiker) Het suikergehalte in
Proef Scheikunde Het suikergehalte in Cola en Cola Light bepalen Proef door een scholier 597 woorden 11 maart 24 5,6 22 keer beoordeeld Vak Scheikunde Proeven i.v.m. G.I.P. (suiker) Het suikergehalte in
Eindexamen scheikunde havo I
 pgave (mono)stikstofmono-oxide Indien als antwoord stikstofoxide is gegeven 2 Een juiste verklaring leidt tot de uitkomst 7 (elektronen). elk atoom bevat 8 elektronen in totaal bevat het 2 - ion dus 2
pgave (mono)stikstofmono-oxide Indien als antwoord stikstofoxide is gegeven 2 Een juiste verklaring leidt tot de uitkomst 7 (elektronen). elk atoom bevat 8 elektronen in totaal bevat het 2 - ion dus 2
Oplosbaarheid van CO2 in water aantonen bij verschillende temperaturen 10 C 10 C
 Oplosbaarheid van CO 2 in water aantonen bij verschillende temperaturen Materiaal: (Titratie) A - Statief + klemmen - Buret - Thermometer - Bekerglas 250 / 500ml - Ijs - Gedestilleerd water => 10 C - Fenolftaleïne
Oplosbaarheid van CO 2 in water aantonen bij verschillende temperaturen Materiaal: (Titratie) A - Statief + klemmen - Buret - Thermometer - Bekerglas 250 / 500ml - Ijs - Gedestilleerd water => 10 C - Fenolftaleïne
Examen VWO. scheikunde 1,2. tijdvak 1 vrijdag 23 mei 13.30-16.30 uur. Bij dit examen horen een bijlage en een uitwerkbijlage.
 Examen VW 2008 tijdvak 1 vrijdag 23 mei 13.30-16.30 uur scheikunde 1,2 Bij dit examen horen een bijlage en een uitwerkbijlage. Dit examen bestaat uit 25 vragen. Voor dit examen zijn maximaal 69 punten
Examen VW 2008 tijdvak 1 vrijdag 23 mei 13.30-16.30 uur scheikunde 1,2 Bij dit examen horen een bijlage en een uitwerkbijlage. Dit examen bestaat uit 25 vragen. Voor dit examen zijn maximaal 69 punten
ZUUR-BASE BUFFERS Samenvatting voor het VWO
 ZUUR-BASE BUFFERS Samenvatting voor het VWO versie december 2014 INHOUDSOPGAVE 1. Vooraf 2. Wat is een buffer? 3. Hoe werkt een buffer? 4. Geconjugeerd zuur/base-paar 5. De ph van een buffer De volgende
ZUUR-BASE BUFFERS Samenvatting voor het VWO versie december 2014 INHOUDSOPGAVE 1. Vooraf 2. Wat is een buffer? 3. Hoe werkt een buffer? 4. Geconjugeerd zuur/base-paar 5. De ph van een buffer De volgende
1. Elementaire chemie en chemisch rekenen
 In onderstaande zelftest zijn de vragen gebundeld die als voorbeeldvragen zijn opgenomen in het bijhorend overzicht van de verwachte voorkennis chemie. 1. Elementaire chemie en chemisch rekenen 1.1 Grootheden
In onderstaande zelftest zijn de vragen gebundeld die als voorbeeldvragen zijn opgenomen in het bijhorend overzicht van de verwachte voorkennis chemie. 1. Elementaire chemie en chemisch rekenen 1.1 Grootheden
Practicum Emulsies. Leerdoelen
 Moleculaire gastronomie is een wetenschapsveld dat zich richt op het verbeteren van bestaande recepten, door bijvoorbeeld te onderzoeken wat de oorzaak is van veelvoorkomende problemen bij het uitvoeren
Moleculaire gastronomie is een wetenschapsveld dat zich richt op het verbeteren van bestaande recepten, door bijvoorbeeld te onderzoeken wat de oorzaak is van veelvoorkomende problemen bij het uitvoeren
WATER. Krachten tussen deeltjes
 WATER Krachten tussen deeltjes Krachten tussen deeltjes (1) Atoombinding en molecuulbinding De atomen in een molecuul blijven samen door het gemeenschappelijk gebruik van één of meer elektronenparen (=
WATER Krachten tussen deeltjes Krachten tussen deeltjes (1) Atoombinding en molecuulbinding De atomen in een molecuul blijven samen door het gemeenschappelijk gebruik van één of meer elektronenparen (=
toelatingsexamen-geneeskunde.be Vraag 2 Wat is de ph van een zwakke base in een waterige oplossing met een concentratie van 0,1 M?
 Chemie juli 2009 Laatste wijziging: 31/07/09 Gebaseerd op vragen uit het examen. Vraag 1 Geef de structuurformule van nitriet. A. B. C. D. Vraag 2 Wat is de ph van een zwakke base in een waterige oplossing
Chemie juli 2009 Laatste wijziging: 31/07/09 Gebaseerd op vragen uit het examen. Vraag 1 Geef de structuurformule van nitriet. A. B. C. D. Vraag 2 Wat is de ph van een zwakke base in een waterige oplossing
5 Formules en reactievergelijkingen
 5 Formules en reactievergelijkingen Stoffen bestaan uit moleculen en moleculen uit atomen (5.1) Stoffen bestaan uit moleculen. Een zuivere stof bestaat uit één soort moleculen. Een molecuul is een groepje
5 Formules en reactievergelijkingen Stoffen bestaan uit moleculen en moleculen uit atomen (5.1) Stoffen bestaan uit moleculen. Een zuivere stof bestaat uit één soort moleculen. Een molecuul is een groepje
Practicum Zouten 2 VMBO 4 Zouten Zoutoplossingen bij elkaar Slecht oplosbare zouten maken Ionen verwijderen Herkennen van een zout
 Practicum Zouten 2 Niveau: VMBO 4 Onderdeel: Zouten Proeven: Zoutoplossingen bij elkaar Slecht oplosbare zouten maken Ionen verwijderen Herkennen van een zout 1 Proef 1 Zoutoplossingen bij elkaar Nodig:
Practicum Zouten 2 Niveau: VMBO 4 Onderdeel: Zouten Proeven: Zoutoplossingen bij elkaar Slecht oplosbare zouten maken Ionen verwijderen Herkennen van een zout 1 Proef 1 Zoutoplossingen bij elkaar Nodig:
Bepaling van het onverzadigd karakter (joodgetal) van vetten (margarines)
 Bepaling van het onverzadigd karakter (joodgetal) van vetten (margarines) Auteur Laatst gewijzigd Licentie Webadres Dick Naafs 22 december 2016 CC Naamsvermelding 3.0 Nederland licentie https://maken.wikiwijs.nl/35388
Bepaling van het onverzadigd karakter (joodgetal) van vetten (margarines) Auteur Laatst gewijzigd Licentie Webadres Dick Naafs 22 december 2016 CC Naamsvermelding 3.0 Nederland licentie https://maken.wikiwijs.nl/35388
1 De bouw van stoffen
 Inhoud 1 De bouw van stoffen 1 eigenschappen van stoffen 13 Mengsels en zuivere stoffen 13 D Oplossingen 15 Zuivere stoffen herkennen 15 Scheiding van mengsels 17 2 de opbouw van de materie 19 Moleculen
Inhoud 1 De bouw van stoffen 1 eigenschappen van stoffen 13 Mengsels en zuivere stoffen 13 D Oplossingen 15 Zuivere stoffen herkennen 15 Scheiding van mengsels 17 2 de opbouw van de materie 19 Moleculen
CENTRALE COMMISSIE VOORTENTAMEN SCHEIKUNDE TENTAMEN SCHEIKUNDE. datum : donderdag 29 juli 2010
 CENTRALE COMMISSIE VOORTENTAMEN SCHEIKUNDE TENTAMEN SCHEIKUNDE datum : donderdag 29 juli 2010 tijd : 14.00 tot 17.00 uur aantal opgaven : 6 Iedere opgave dient op een afzonderlijk vel te worden gemaakt
CENTRALE COMMISSIE VOORTENTAMEN SCHEIKUNDE TENTAMEN SCHEIKUNDE datum : donderdag 29 juli 2010 tijd : 14.00 tot 17.00 uur aantal opgaven : 6 Iedere opgave dient op een afzonderlijk vel te worden gemaakt
Wet van Behoud van Massa
 Les 3 E42 Wet van Behoud van Massa In 1789 door Antoine Lavoiser ontdekt dat : De totale massa tijdens een reactie altijd gelijk blijft. Bij chemische reacties worden moleculen dus veranderd in andere
Les 3 E42 Wet van Behoud van Massa In 1789 door Antoine Lavoiser ontdekt dat : De totale massa tijdens een reactie altijd gelijk blijft. Bij chemische reacties worden moleculen dus veranderd in andere
Onderzoekscompetenties. 3 de jaar. Hoe verlopen chemische reacties? A Tekst leerlingen: leerwerkboek
 Onderzoekscompetenties 3 de jaar Hfdst 4 Hoe verlopen chemische reacties? A Tekst leerlingen: leerwerkboek Onderzoek: het behoud van atoomsoorten in een reactiereeks Werkmethode 1. Wat onderzoeken? Probleemstelling
Onderzoekscompetenties 3 de jaar Hfdst 4 Hoe verlopen chemische reacties? A Tekst leerlingen: leerwerkboek Onderzoek: het behoud van atoomsoorten in een reactiereeks Werkmethode 1. Wat onderzoeken? Probleemstelling
Eindexamen scheikunde havo 2002-II
 4 Antwoordmodel Zuurstofvoorziening 1 aantal protonen: 16 aantal elektronen: 17 aantal protonen: 16 1 aantal elektronen: aantal protonen vermeerderd met 1 1 2 4 KO 2 2 K 2 O + 3 O 2 alleen KO 2 voor de
4 Antwoordmodel Zuurstofvoorziening 1 aantal protonen: 16 aantal elektronen: 17 aantal protonen: 16 1 aantal elektronen: aantal protonen vermeerderd met 1 1 2 4 KO 2 2 K 2 O + 3 O 2 alleen KO 2 voor de
Bepaling van het onverzadigd karakter (joodgetal) van vetten (margarines)
 Bepaling van het onverzadigd karakter (joodgetal) van vetten (margarines) Auteur Laatst gewijzigd Licentie Webadres Dick Naafs 22 December 2016 CC Naamsvermelding 3.0 Nederland licentie http://maken.wikiwijs.nl/35388
Bepaling van het onverzadigd karakter (joodgetal) van vetten (margarines) Auteur Laatst gewijzigd Licentie Webadres Dick Naafs 22 December 2016 CC Naamsvermelding 3.0 Nederland licentie http://maken.wikiwijs.nl/35388
NATIONALE SCHEIKUNDEOLYMPIADE
 ATIALE SEIKUDELYMPIADE RRETIEMDEL VRRDE 1 (de week van) woensdag 2 februari 2011 Deze voorronde bestaat uit 24 meerkeuzevragen verdeeld over 6 onderwerpen en 3 open vragen met in totaal 15 deelvragen.
ATIALE SEIKUDELYMPIADE RRETIEMDEL VRRDE 1 (de week van) woensdag 2 februari 2011 Deze voorronde bestaat uit 24 meerkeuzevragen verdeeld over 6 onderwerpen en 3 open vragen met in totaal 15 deelvragen.
1 Verdringingsreacties niet-metalen met lucifers
 Verdringingsreacties niet-metalen met lucifers Plaats in de leerplannen VVKSO leerplan derde graad ASO Chemie LICAP Brussel D20060279040:. Oriënteren Achtergrondinformatie Herhaal de begrippen oxidator-
Verdringingsreacties niet-metalen met lucifers Plaats in de leerplannen VVKSO leerplan derde graad ASO Chemie LICAP Brussel D20060279040:. Oriënteren Achtergrondinformatie Herhaal de begrippen oxidator-
Eindexamen scheikunde 1 vwo 2004-I
 Eindexamen scheikunde 1 vwo 004-I 4 Beoordelingsmodel Zink 1 Een juist antwoord kan als volgt zijn geformuleerd: IJzerionen zijn Fe + of Fe 3+ en sulfide-ionen zijn en dat leidt tot de formule Fe of Fe
Eindexamen scheikunde 1 vwo 004-I 4 Beoordelingsmodel Zink 1 Een juist antwoord kan als volgt zijn geformuleerd: IJzerionen zijn Fe + of Fe 3+ en sulfide-ionen zijn en dat leidt tot de formule Fe of Fe
TF5 Scheikunde 4 VWO H 8 en H 9 16 juni 2011
 TF5 Scheikunde 4 VWO H 8 en H 9 16 juni 2011 Deze toets bestaat uit 28 onderdelen. Hiervoor zijn in totaal X punten te behalen. Kalkwater Calciumhydroxide, Ca(OH) 2 (s) is matig oplosbaar in water. Als
TF5 Scheikunde 4 VWO H 8 en H 9 16 juni 2011 Deze toets bestaat uit 28 onderdelen. Hiervoor zijn in totaal X punten te behalen. Kalkwater Calciumhydroxide, Ca(OH) 2 (s) is matig oplosbaar in water. Als
Hoofdstuk 2: Kenmerken van reacties
 Hoofdstuk 2: Kenmerken van reacties Scheikunde VWO 2011/2012 www.lyceo.nl Onderwerpen Scheikunde 2011 20122012 Stoffen, structuur en binding Kenmerken van Reacties Zuren en base Redox Chemische technieken
Hoofdstuk 2: Kenmerken van reacties Scheikunde VWO 2011/2012 www.lyceo.nl Onderwerpen Scheikunde 2011 20122012 Stoffen, structuur en binding Kenmerken van Reacties Zuren en base Redox Chemische technieken
ZUREN EN BASEN. Samenvatting voor het HAVO. versie mei 2013
 ZUREN EN BASEN Samenvatting voor het HAVO versie mei 2013 INHOUDSOPGAVE 1. Vooraf 2. Algemeen 3. Zuren 4. Basen 5. Het waterevenwicht 6. Definities ph en poh 7. ph BEREKENINGEN 7.1. Algemeen 7.2. Water
ZUREN EN BASEN Samenvatting voor het HAVO versie mei 2013 INHOUDSOPGAVE 1. Vooraf 2. Algemeen 3. Zuren 4. Basen 5. Het waterevenwicht 6. Definities ph en poh 7. ph BEREKENINGEN 7.1. Algemeen 7.2. Water
Bollen, kolommen, platen en achtvlakken
 Bollen, kolommen, platen en achtvlakken 1 D (het aantal moleculen is evenredig met de dichtheid gedeeld door de molecuulmassa) C (De loopsnelheid van Q is hier in beide proeven groter dan die van P) 3
Bollen, kolommen, platen en achtvlakken 1 D (het aantal moleculen is evenredig met de dichtheid gedeeld door de molecuulmassa) C (De loopsnelheid van Q is hier in beide proeven groter dan die van P) 3
woensdag 14 december 2011 16:06:43 Midden-Europese standaardtijd
 INLEIDING Geef de reactievergelijking van de ontleding van aluminiumoxide. 2 Al 2 O 3 4 Al + 3 O 2 Massaverhouding tussen Al en O 2 1,00 : 0,889 Hoeveel ton Al 2 O 3 is er nodig om 1,50 ton O 2 te produceren?
INLEIDING Geef de reactievergelijking van de ontleding van aluminiumoxide. 2 Al 2 O 3 4 Al + 3 O 2 Massaverhouding tussen Al en O 2 1,00 : 0,889 Hoeveel ton Al 2 O 3 is er nodig om 1,50 ton O 2 te produceren?
Deze Informatie is gratis en mag op geen enkele wijze tegen betaling aangeboden worden
 Vraag 1 Welke van volgende formules stemt overeen met magnesiumchloriet? MgCl Mg(ClO 2 ) 2 Mg(ClO 3 ) 2 Mg3(ClO 3 ) 2 Optie A: Hier is wat kennis over het periodiek systeem der elementen
Vraag 1 Welke van volgende formules stemt overeen met magnesiumchloriet? MgCl Mg(ClO 2 ) 2 Mg(ClO 3 ) 2 Mg3(ClO 3 ) 2 Optie A: Hier is wat kennis over het periodiek systeem der elementen
a) Teken molecuul I op het antwoordblad en omcirkel alle stereocentra.(5)
 Hertentamen Bio-organische Chemie (8RB19) Maandag, 30 juni, 2014, 14:00 17:00 (3 uur) Bij het begin van elke opgave staat het aantal punten dat te verdienen is en de geadviseerde tijdsbesteding. Er zijn
Hertentamen Bio-organische Chemie (8RB19) Maandag, 30 juni, 2014, 14:00 17:00 (3 uur) Bij het begin van elke opgave staat het aantal punten dat te verdienen is en de geadviseerde tijdsbesteding. Er zijn
Eindexamen vwo scheikunde pilot II
 Selectieve opname koolstofdioxide 1 maximumscore 2 Een juist antwoord kan als volgt zijn weergegeven: rechts van de pijl H + 1 juiste coëfficiënten 1 Indien in een overigens juiste vergelijking H 2 is
Selectieve opname koolstofdioxide 1 maximumscore 2 Een juist antwoord kan als volgt zijn weergegeven: rechts van de pijl H + 1 juiste coëfficiënten 1 Indien in een overigens juiste vergelijking H 2 is
vrijdag 28 oktober :40:59 Nederland-tijd Moleculaire stoffen 4havo hoofdstuk 2; Chemie Overal
 + Moleculaire stoffen 4havo hoofdstuk 2; Chemie Overal + 2.2 Elektrisch geleidingsvermogen Demo 2.1 Geleidt stroom als vaste stof: ja / nee Geleidt stroom als vloeistof: ja/nee Opgebouwd uit welke atoomsoorten?
+ Moleculaire stoffen 4havo hoofdstuk 2; Chemie Overal + 2.2 Elektrisch geleidingsvermogen Demo 2.1 Geleidt stroom als vaste stof: ja / nee Geleidt stroom als vloeistof: ja/nee Opgebouwd uit welke atoomsoorten?
