Moderne biotechnologie
|
|
|
- Victor van der Wal
- 8 jaren geleden
- Aantal bezoeken:
Transcriptie
1 Moderne biotechnologie 6 vwo Van cel naar fabriek 1
2 COLOFON Het ontwikkelteam: Ingeborg de Kooter, Christelijk Lyceum te Delft Daan Robeerst, student LST, TU Delft Sander Haemers, Stanislas College te Pijnacker Juleke van Rhijn, Coornhert-gymnasium te Gouda (tevens eindredactie) Dirk Hillenga, Grotius College te Delft Coach: Aonne Kerkstra, TU Delft Dank aan de volgende deskundigen, die een belangrijke inbreng hadden bij het maken van de module: Dr. Olav Sliekers, Purac te Gorichem Drs. Willem Buitelaar, DuPont te Dordrecht Prof.Dr.Ir.Sef Heijnen verbonden aan het Kluyver Centre van de TU Delft 2010 De Vereniging van de Nederlandse Chemische Industrie (VNCI), Den Haag. Het auteursrecht op dit onderwijsmateriaal voor Nieuwe Scheikunde berust bij de VNCI te Den Haag. De VNCI is derhalve de rechthebbende zoals bedoeld in de hieronder vermelde creative commons licentie. Hoewel het onderwijsmateriaal met zorg is samengesteld, is het mogelijk dat deze onjuistheden en/ of onvolledigheden bevatten. De VNCI aanvaardt derhalve geen enkele aansprakelijkheid voor enige schade, voortkomend uit (het gebruik van) dit materiaal. Voor dit onderwijsmateriaal geldt een Creative Commons Naamsvermelding-Niet-Commercieel-Gelijk delen 3.0 Nederland licentie Aangepaste versies hiervan mogen alleen verspreid worden indien het in het colofon vermeld wordt dat het een aangepaste versie betreft, onder vermelding van de naam van de auteur van de wijzingen. VNCI, Den Haag, november
3 Inhoudsopgave Blz. Hoofdstuk 1 Inleiding 4 Hoofdstuk 2 Bacteriën 7 Hoofdstuk 3 De cel als fabriek 12 Hoofdstuk 4 Klassieke biotechnologie: de melkzuurfabriek 26 Hoofdstuk 5 Moderne biotechnologie: de productie van 1,3-propaandiol 58 Hoofdstuk 6 Gibbs energie 86 Hoofdstuk 7 - Gibbs energie en de dissimilatie van glucose 95 3
4 Hoofdstuk 1 Inleiding De bacterie als fabriek: biotechnologie op micro- en macroschaal In winkels zie je steeds vaker producten met het woord biologisch op de verpakking. Hierdoor lijkt het wel of het maken van biologische producten iets van deze tijd is. Maar dat is bepaald niet het geval. Al in de jonge steentijd, zo n jaar geleden, maakte de mens gebruik van bacteriën, schimmels en gisten om brood, bier, yoghurt en kaas te maken. De productie van deze voedingsmiddelen met micro-organismen noemen we daarom klassieke biotechnologie. Wetenschappers bekijken bacteriën en schimmels tegenwoordig als kleine fabriekjes die je kunt gebruiken om allerlei stoffen te produceren. Van nature maken micro-organismen al veel bruikbare stoffen. Maar dat doen ze meestal in hele kleine hoeveelheden. Om te bereiken dat ze meer gaan maken of zelfs hele nieuwe stoffen gaan produceren moet je microorganismen aanpassen. In de 21 e eeuw zullen micro-organismen compleet hergeprogrammeerd of zelfs volledig geconstrueerd worden om zo door de mens gemaakte microfabrieken te vormen. De productie van stoffen met deze genetisch gemodificeerde micro-organismen noemen we moderne biotechnologie. In de moderne biotechnologie wordt veel gebruik gemaakt van productieprocessen zoals fermentatie en biokatalyse. Fermentatie is het gebruiken van micro-organismen om basisgrondstof- Figuur 1:Biologische yoghurt fen zoals suikers om te zetten in bruikbare producten als ethanol of melkzuur. Biokatalyse is het gebruiken van enzymen om een industrieel proces te versnellen. In deze module over biotechnologie gaan we kijken naar de productie van melkzuur, als voorbeeld van een productieproces uit de klassieke biotechnologie. De productie van 1,3- propaandiol wordt het voorbeeld uit de moderne biotechnologie. Om beide processen te kunnen begrijpen wordt in hoofdstuk 2 eerste de stof over bacteriën herhaald. Er wordt ingezoomd op de bacteriecel. Voor leerlingen met een N&G profiel is dit herhaalstof. In hoofdstuk 3 wordt de cel als fabriek behandeld met de belangrijkste biosynthetische routes. En hoe zit het met de energievoorziening in de cel? Klassieke biotechnologie: Melkzuurproductie Melkzuur is de triviale naam voor 2 hydroxypropaanzuur. De grote uitdaging is om melkzuurbacteriën grote hoeveelheden melkzuur te laten produceren en het melkzuur zuiver in handen te krijgen. Je zult ontdekken dat daar een behoorlijke hoeveelheid chemische technologie voor nodig is. Figuur 2: Melkzuurbacteriën 4
5 Melkzuur is de grondstof (het monomeer) voor de productie van polymelkzuur (PLA). PLA (polylactic-acid) is een bioplastic dat wordt gebruikt voor veel verschillende doeleinden zoals draad, schroeven en pinnen voor chirurgie, plastic tasjes en kleding. PLA wordt gemaakt van natuurlijk melkzuur, een product van melkzuurbacteriën. Het is een biodegradeerbaar polymeer. ( ) Figuur 3: Bioplastic schroeven en pinnen van PLA worden gebruikt in de chirurgie Contextvragen 1. Hoe kunnen bacteriën melkzuur maken? 2. Op welk manieren krijg je zuiver melkzuur? 3. Hoe verloopt op industriële schaal de productie van PLA? Moderne biotechnologie: productie van 1,3-propaandiol Wetenschappers gingen op zoek naar een organisme dat zowel 1,3- propaandiol produceert, als glucose kan gebruiken voor zijn cellulaire processen. Deze micro-organismen waren er echter niet. Daarom heeft men de bacterie Escherichia coli (E.coli) genetisch zo gemodificeerd dat de nieuwe stam 1,3-propaandiol uit glucose kan maken. In het DNA van E.coli moesten dus een aantal veranderingen worden gemaakt, zodat de bacterie met behulp van de biosynthetische routes die het van oorsprong al had, 1,3-propaandiol kan maken. Wetenschappelijk heet dit metabolic engineering. 1,3-propaandiol is de grondstof (het monomeer) voor de productie van het polymeer Sorona. Sorona is een polymeer die veel gebruikt wordt in de textielindustrie voor de productie van (sport)kleding en vloerbedekking. Figuur 4: wedstrijd badpak gemaakt van Sorona www2.dupont.com/sorona/ en_us/ Contextvragen 4. Hoe gaat de metabolic engineering van E.coli? 5. Op welk manier krijg je zuiver 1,3-propaandiol? 6. Hoe verloopt op industriële schaal de productie van Sorona? 5
6 Gibbs energie Voor biologen en chemici is het energieverschil van een reactie die verloopt bij constante temperatuur en constante druk een belangrijke grootheid. Het verschil van energie bij deze omstandigheden bepaalt namelijk of reacties spontaan kunnen verlopen en bij evenwichtsreacties bepaalt het de ligging van het evenwicht. Deze energie wordt de Gibbs energie (G) genoemd. De rol van de Gibbs energie in de regulatie van de biosynthetische routes in de cel is erg belangrijk. Gibbs Energie is voor jullie één van de nieuwe vakbegrippen die in dit hoofdstuk behandeld worden. Slot Bovenstaande onderwerpen komen aan de orde in een module waarin biologie, natuurkunde en scheikunde samenvloeien. Een lessenserie waarin je anders leert te kijken naar microorganismen en je de fascinerende wereld van de snelst groeiende tak van de chemische industrie leert kennen: de moderne biotechnologie! 6
7 Hoofdstuk 2 Bacteriën Biotechnologen werken onder andere met bacteriën. Ze selecteren uit de vele verschillende bacteriën de meest geschikte bacterie voor een bepaald productieproces of ze proberen een bacterie genetisch aan te passen zodat deze gaat doen wat de biotechnologen willen. Voordat we hier dieper op ingaan bekijken we hoe een bacterie eruit ziet. Organismen bestaan uit een of meerdere cellen, de kleinste fundamentele eenheid van leven. Er zijn eencellige organismen zoals bacteriën en gisten en er zijn meercellige organismen zoals de mens. Het volwassen lichaam van een mens bestaat uit zo n 50 miljard cellen. Er wordt onderscheid gemaakt tussen twee typen cellen: prokaryoten en eukaryoten. Bij de cellen van prokaryoten ligt het DNA los in de cel en is niet verpakt in een celkern. Voorbeelden van prokaryoten zijn bacteriën. Eukaryoten zijn cellen met een celkern, waarin zich het DNA bevindt, en in de cel nog andere celstructuren met een bepaalde functie (organellen). Meercellige organismen zoals mensen en dieren zijn eukaryoot, maar er zijn ook eencellige eukaryoten zoals gisten. Bacteriecel Er zijn vele soorten bacteriën die je overal terug vindt. Ze komen los in de natuur voor maar ook binnen in organismen. Er zijn nuttige bacteriën, zoals de bacteriën in de menselijke darmen en bacteriën die ziekten veroorzaken. De grootte van een bacteriecel varieert van 0,0001 tot 0,02 mm. Het meest voorkomende gemiddelde is 0,001 mm, duizend keer zo klein als een millimeter. Met het blote oog kan je ze daarom niet zien. Alleen onder een microscoop met een 1000 keer vergroting zijn ze zichtbaar. Bacteriën zijn daarmee de kleinste organismen die nog met een lichtmicroscoop zijn waar te nemen. Alle soorten bacteriën planten zich voort door te delen. Een moedercel splitst zich in tweeën in twee dochtercellen. Hierbij wordt de inhoud van de moedercel eerlijk verdeeld zodat de inhoud van de twee dochtercellen hetzelfde is als van de moedercel. Figuur 1: Een bacteriecel van dichtbij bekeken Celwand De celwand van bacteriën bestaat uit polysachariden en zorgt voor extra stevigheid van de cel. Aan de binnenzijde van de celwand bevindt zich tegen de celwand aan het celmembraan, ook wel plasmamembraan geheten. Binnenin de cel bevindt zich het cytoplasma met het DNA, de plasmiden en de ribosomen. 7
8 DNA Het DNA van een bacterie bevindt zich los in de cel en bestaat uit het DNA van de chromosomen en uit het DNA van één of meerdere plasmiden. Het chromosomaal DNA en het DNA van de plasmiden vormen samen het genetisch materiaal van een bacterie. Hierop liggen verschillende genen die gebruikt worden om eiwitten te maken. Ieder gen bevat de code voor een ander eiwit. Een cel heeft niet evenveel van ieder eiwit nodig. Wanneer een gen gebruikt wordt om een eiwit te maken, zeggen we dat het gen tot expressie komt. Om de hoeveelheid eiwit in een cel te beïnvloeden zal het dus belangrijk zijn om de expressie van een gen te kunnen beïnvloeden. Dit doet een cel door de expressie van een gen te reguleren: genregulatie. De genregulatie bepaalt of en hoeveel er van ieder eiwit wordt gemaakt. Deze regulatie gebeurt door regulatie-eiwitten. Vaak zal een bepaalde concentratie van een eiwit gewenst zijn. Wanneer er genoeg van dit eiwit aanwezig is, zal er een regulatie-eiwit zijn dat ervoor zorgt dat er niet nog meer van het bepaalde eiwit wordt geproduceerd. Plasmiden Plasmiden zijn kleine ringvormige stukken DNA, die bacteriën onderling kunnen uitwisselen. De plasmiden worden door biotechnologen gebruikt om de genetische informatie van een ander organisme op te slaan. De plasmide bevat dan een stukje DNA van een ander organisme. Flagellen De flagellen zijn lange eiwitdraden die verankerd zijn in de celwand en die voor de beweeglijkheid van bacteriën kunnen zorgen. Pili Pili hebben geen invloed op de beweeglijkheid, zij zorgen er voor dat een (aerobe) bacterie aan de oppervlakte van een vloeistof blijft. Bacteriën kunnen met hun pili samen een velletje vormen en op die manier gebruik maken van de beschikbare zuurstof aan de oppervlakte. Ribosomen Op de ribosomen vindt de eiwitsynthese plaats. Heel beknopt komt het er op neer dat een soort werkkopie van het DNA, namelijk het RNA, op de ribosomen wordt vertaald in een keten van aminozuren, dat wil zeggen een eiwitmolecuul. Vragen 1. Leg uit hoe een bacterie resistent kan worden voor een bepaald antibioticum. 2. Hoe komt het dat biotechnologen graag met prokaryoten werken? Celmembraan Om goed te kunnen functioneren moet de cel zorgen voor een gecontroleerd intern milieu. Als bij een reactie in de cel doorlopend beginstoffen worden aangevoerd en reactieproducten worden afgevoerd ontstaat een situatie, waarbij de reactie verloopt terwijl de concentraties van de reagerende stoffen toch constant blijven. Dit wordt steady-state genoemd. In cellen komen veel steady-state processen voor. Het vermogen van een organisme om het interne milieu, waarin deze steady-state processen constant te houden noemen we homeostase. Bij het constant houden van het interne milieu speelt het celmembraan een belangrijke rol. Voor een bacterie betekent dit eveneens, dat de concentraties van stoffen binnen de cel constant gehouden worden. De omgeving waarin de bacterie zich bevindt, speelt hierbij een belangrijke rol. Eventuele beperkingen in het interne milieu moeten met behulp van de omgeving aangepast kunnen worden. Voldoet de omgeving niet aan de eisen, dan zullen bacteriën niet of niet zo goed groeien of zelfs dood gaan. Omgekeerd kunnen gunstige omge- 8
9 vingsfactoren de groei en vermenigvuldiging weer stimuleren. Factoren die hierbij een rol spelen zijn de temperatuur, ph, osmotische waarde en zuurstofspanning. Bouw van het celmembraan Het celmembraan is een dubbellaag van fosfolipiden, die ervoor zorgt dat niet alle moleculen en ionen zomaar de cel in en uit kunnen. Figuur 2: Het celmembraan bestaat uit fosfolipiden (4), suikers (3) en verschillende soorten eiwitten (1, 2 en 5) De fosfolipiden zorgen voor zo n dubbellaag doordat de hydrofiele 'fosfaatkoppen" zich naar de buitenkanten van het celmembraan richten (naar de waterkanten) en de hydrofobe vetzuurstaarten zich naar de binnenkant van het membraan richten. Deze fosfolipiden zijn voortdurend in beweging en vormen dus geen starre structuur. ( zie animatie celmembraan ) In het celmembraan zitten naast fosfolipiden veel grote eiwitten, die door het membraan steken (zie figuur 2). Deze zijn belangrijk voor bepaalde processen in de cel en zijn vaak betrokken bij het doorlaten van voedingsstoffen voor de cel en van producten uit de cel. Figuur 3: Een fosfolipide heeft een hydrofiele fosfaatkop en een hydrofobe vetzuurstaart. Binas tabel 67 B3. Transport via het celmembraan In de cel vinden verschillende reacties plaats. Voor deze reacties zijn stoffen nodig, daarnaast ontstaan er reactieproducten. Om de concentratie van stoffen in de cel constant te houden zal er daarom transport van stoffen nodig zijn. Stoffen moeten de cel in en uit kunnen. Omdat het celmembraan stoffen door kan laten, kunnen essentiële stoffen als glucose 9
10 en vetten de cel in, blijven de benodigde stoffen in de cel en kunnen (afval)producten de cel uit. Passief transport Zoals eerder besproken is het celmembraan een dubbellaag van fosfolipiden met hydrofiele koppen aan de buitenkant en hydrofobe staarten naar binnen gericht. Hierdoor is het niet voor iedere stof mogelijk om gemakkelijk de cel in of uit te gaan. Stoffen die uit kleine ongeladen moleculen bestaan zoals de gassen CO 2, O 2 en N 2 en bijvoorbeeld ethanol kunnen het celmembraan passief passeren. De drijvende kracht bij dit transport is het verschil in concentratie van deze stoffen binnen in de cel en buiten de cel. Dit transport gaat door totdat aan beide zijden van het membraan de concentraties van de stoffen gelijk zijn. Dit transport kost de cel geen energie en wordt daarom passief transport genoemd. Omdat de stoffen letterlijk door het membraan gaan spreken we bij passief transport over transport door het membraan. Figuur 4: Actief en passief transport over het celmembraan, zie ook de animatie Actief transport Stoffen die uit grote moleculen of ionen bestaan kunnen vaak alleen actief over het membraan getransporteerd worden. Dit transport gebeurt door transporteiwitten in het membraan. Voor actief transport is energie nodig. We spreken in dit geval van transport over het membraan. Naast energie voor het transport, heeft een cel energie nodig voor processen binnen de cel en om te groeien. De meeste bacteriën halen deze energie uit de enzymatische afbraak van voedingsstoffen. 10
11 Omdat ionen niet passief over het membraan getransporteerd kunnen worden is het ook mogelijk, dat er een ladingverschil kan ontstaan tussen de binnen- en de buitenkant van een cel. Dit ladingverschil is één van de manieren van energieopslag door een cel, een andere is de stof ATP (adenosine trifosfaat). Deze energie wordt gebruikt voor verschillende processen in de cel, waaronder dus het actieve transport over het membraan. Vragen 3. Leg uit waarom er voor homeostase actief en passief transport nodig zijn. 4. Wat heeft een cel nodig voor actief transport? 5. Wanneer spreekt men van transport over het membraan? Wat je nu moet weten Bouw bacteriecel o Celwand o DNA o Plasmiden o Flagellen o Pili Celmembraan o Bouw o Passief transport o Actief transport 11
12 Hoofdstuk 3 Cel als fabriek 3.1 Bacteriën Bacteriën vormen een grote groep van microorganismen die uit slechts één cel bestaan. De grootte van een bacteriecel varieert, maar gemiddeld zijn bacteriën een paar micrometer lang, een factor 10 kleiner dan overige celtypen. Je hebt daarom een lichtmicroscoop nodig om ze te kunnen zien, maar zelfs dat is meestal niet voldoende; een elektronenmicroscoop volstaat beter. Er zijn vele soorten bacteriën met allerlei vormen: bolletjes, staafjes, kommavormig en spiralen. Bacteriën zijn veelzijdig, ze kunnen onder bijna alle mogelijke omstandigheden leven. Ze komen overal in de natuur voor: van diep in de bodem tot in hoge lagen van de atmosfeer, van in het ijs op Antarctica tot in kokendhete waterbronnen op de bodem van de oceanen. Zelfs binnen in planten en in dieren leven ze. Men schat dat er op de aarde ongeveer Figuur 1: Bacteriën hebben verschillende vormen bacteriën voorkomen: in één gram grond leven gemiddeld al zo n 40 miljoen bacteriën. In ieder mens bevinden zich ongeveer 1 kg bacteriën die bijdragen aan de spijsvertering en afweer van ons lichaam. Door de veelzijdigheid van bacteriën zijn ze heel geschikt om allerlei stoffen te produceren. Vaak doen ze dat al van nature, maar dan maken ze over het algemeen maar heel weinig van die stof. Biotechnologen zoeken daarom tussen de vele verschillende bacteriën die er zijn naar de meest geschikte voor een bepaald productieproces. Daarna passen ze de uitgekozen bacterie aan zodat deze doet wat ze willen, zo maken ze van de bacterie als het ware een fabriek in het klein. Om duidelijk te maken hoe biotechnologen een bacterie als een kleine fabriek kunnen gebruiken gaan we eerst wat beter naar een bacterie kijken. Daarbij kunnen de volgende vragen helpen: Hoe deelt een bacterie? Waaruit bestaat een bacterie? Wat heeft een bacterie nodig om te leven? Hoe kan een bacterie zo veel verschillende stoffen maken? Om stoffen te kunnen produceren zijn er heel veel bacteriën nodig. Die bacteriën moeten dus eerst groeien. Alle soorten bacteriën planten zich voort door te delen. Een cel splitst zich in twee dochtercellen waarbij de inhoud van de moedercel eerst wordt verdubbeld en daarna verdeeld wordt over de dochtercellen. 12
13 Bacteriën hebben een vrij eenvoudige bouw (zie figuur 2). Het inwendige van een bacterie bestaat uit cytoplasma met onder andere het cirkelvormig DNA, dat los in het cytoplasma drijft (dat maakt bacteriën zo geschikt voor biotechnologische toepassingen, in tegenstelling tot eencellige organismen, plantaardige en dierlijke cellen waar DNA in een kern verstopt zit). Het cytoplasma wordt omgeven door een celmembraan. Bij de meeste bacteriesoorten zit hier omheen een celwand op basis van peptidoglycan. Veel bacteriën kunnen om de celwand nog een kapsel of een slijmlaag hebben. Bacteriën kunnen verder uitsteeksels hebben aan de buitenkant in de vorm van flagellen (zweepstaarten) en/of pili (haren). Figuur 2: Een bacteriecel van dichtbij bekeken Hoewel een bacterie een eenvoudig organisme is, bestaat het toch uit honderden verschillende stoffen. De hoofdbestanddelen van een bacterie zijn naast water: eiwitten, polysacchariden, vetten en de nucleïnezuren DNA en RNA (zie tabel 1). De meeste van deze stoffen zijn polymeren, grote moleculen die gemaakt worden uit kleinere moleculen. Om deze polymeren en andere stoffen te maken, heeft een bacterie de juiste bouwstenen nodig. Bacteriën halen deze bouwstenen uit allerlei voedingsstoffen. Ze breken die voedingsstoffen af tot een gering aantal soorten eenvoudige moleculen. Deze moleculen vormen dan de grondstoffen waaruit de bacterie allerlei producten kan maken ten behoeve van zichzelf. 13
14 Tabel 1: Globale chemische samenstelling van een snel delende bacteriecel (E.coli) Stof %-natgewicht Verschillende soorten moleculen per cel Water 70 1 DNA 1 1 RNA Nucleotiden en metabolieten 0,8 200 Eiwitten Aminozuren en metabolieten 0,8 100 Polysacchariden Vetten en metabolieten 2 50 Zouten en spoorelementen 1 20 Overige 0,4 200 Om bacteriën de juiste voedingsstoffen te geven kijkt men meestal naar hoeveel en welke elementen in een bacterie voorkomen ( tabel 2). Op basis hiervan kiest men verschillende voedingsbronnen die men aangeeft als C-bron, N-bron etc. De meeste stoffen die men gebruikt bevatten een combinatie van deze noodzakelijke elementen. Tabel 2: Belangrijke elementen en hun bronnen voor bacteriën Element %-drooggewicht Bron C 50 Organische verbindingen of CO 2 O 20 H 2 O, CO 2, O 2 en organische verbindingen N 14 NH 3, NO 3, N 2 en organische verbindingen H 8 H 2 O, organische verbindingen P 3 anorganische fosfaten (PO 4 3- ) S 1 SO 4, H 2 S, S, organische zwavelverbindingen K 1 Kaliumzouten Mg 0.5 Magnesiumzouten Ca 0.5 Calciumzouten Fe 0.2 IJzerzouten 14
15 3.2 Biosynthetische routes Voor het afbreken van de voedingsstoffen en het vormen van alle benodigde moleculen maken bacteriën gebruik van reacties die gekatalyseerd (versneld) worden door enzymen. Doordat het product van het ene enzym het substraat van het volgende enzym is, zijn deze reacties aan elkaar gekoppeld. Zo worden biosynthetische routes gevormd die soms heel eenvoudig zijn, maar meestal vertakt zijn doordat het tussenproduct van een route het startpunt vormt voor een andere route (zie figuur 3). Figuur 3: Biosynthetische routes. 1. Enkelvoudig proces; 2. Lineaire route; 3. Vertakte route. Samen vormen alle biosynthetische routes in een bacterie een netwerk van processen. Het geheel van deze chemische processen die nodig zijn om het leven in stand te houden noemen we het metabolisme. Soorten vragen Staat ergens in de module uitgelegd of verwijst naar het antwoord van een andere vraag. Opzoeken op Internet of in chemiekaarten. Herhaling scheikunde kennis Vragen 1. Wat zijn de vijf basisfuncties van het metabolisme? 2. De stof acetyl-coa (zie figuur 4, na pyruvaat) is een belangrijke stof in het metabolisme. Het kan gevormd worden uit suikers, aminozuren en vetten. Via welk proces worden vetten afgebroken tot acetyl-coa? 15
16 Figuur 4: Biosynthetische routes vormen een netwerk waardoor uit een klein aantal grondstoffen heel veel producten gevormd kunnen worden. Hier krijgt de bacterie glucose als C-bron. De gele route geeft de afbraak tot lactaat aan. (., stoffen;, route tussen twee stoffen) 16
17 Hoewel het geheel aan chemische processen dat in een bacterie plaatsvindt heel complex lijkt, is het totaal aantal reacties toch veel kleiner dan je zou verwachten. In figuur 4 is een dergelijk netwerk van een aantal routes aangegeven met als startpunt het molecuul glucose dat vaak wordt gebruikt als C-bron. Een bacterie kan energie halen uit glucose door het af te breken tot bijvoorbeeld ethanol of lactaat/melkzuur (gele route). Maar de bacterie kan glucose ook gebruiken voor het maken van zetmeel of peptidoglycan (aangegeven met rood). Je kunt dit netwerk van biosynthetische routes het best vergelijken met het alle leidingen die door een fabriek lopen. Via die leidingen worden allerlei stofstromen aan elkaar gekoppeld en uit een gering aantal stoffen veel verschillende eindproducten gemaakt (figuur 5). Natuurlijk moet de bacterie er wel voor zorgen dat het de stoffen maakt die het nodig heeft. In de bacterie vindt een netwerk van chemische processen plaats die heel nauwkeurig worden gereguleerd. Net als men in een chemische fabriek afsluiters en kleppen gebruikt om de juiste stoffen samen te voegen en de gewenste producten te maken. Figuur 5: Een netwerk van leidingen in een chemische fabriek. Vragen 3. In figuur 4 zie je bovenaan in het midden histidine staan. Via welke twee routes kun je deze stof maken? 4. Uit figuur 4 blijkt dat er veel processen in de bacterie aan elkaar gekoppeld zijn, er kunnen blijkbaar allerlei stoffen ontstaan uit glucose of een ander voedingsmiddel. Stel; je geeft een bacterie maar een beperkte hoeveelheid glucose. Hoe zorgt deze bacterie er dan voor dat er genoeg energie uit de glucose wordt vrijgemaakt, maar dat er ook voldoende peptidoglycan gemaakt wordt voor de celwand of andere stoffen die hij nodig heeft? 5. Onder welke omstandigheden denk je dat een bacterie zetmeel gaat vormen?tip: zoek eerst op wat de functie is van zetmeel en bedenk dan waarom een bacterie zo n stof maakt! 17
18 3.3 Energie voorziening van de cel Energiedragers: betaalmiddelen in de cel Een bacterie heeft voor het afbreken en vormen van stoffen en het uitvoeren van allerlei processen energie nodig. Deze energie haalt de bacterie meestal uit de afbraak van organische moleculen zoals glucose. Om de energie die vrijkomt bij de afbraak van deze stoffen te benutten, maken bacteriën gebruik van zogenaamde energiedragers. Deze energiedragers zijn moleculen waarin energie kan worden opgeslagen of waaruit energie kan worden vrijgemaakt. Je kunt deze energiedragers het best vergelijken met een betaalmiddel: geld. Het zou heel onhandig zijn wanneer je bij de bakker met ander geld moet betalen dan bij de slager, en nog weer met ander geld bij de supermarkt. Als je ergens geld voor krijgt, wil je dat geld het liefst overal kunnen gebruiken om voor iets te betalen. Daarom gebruikt de bacterie maar een klein aantal energiedragers die het bij veel processen die energie kosten weer kan gebruiken. Twee belangrijke zaken die energiedragers in de cel kunnen leveren zijn Gibbs energie en elektronen. Gibbs energie is de bruikbare energie die bij reacties uit moleculen gehaald kan worden, later in deze module gaan we verder in op de Gibbs energie. Elektronen zijn nodig voor het laten verlopen van redoxreacties in de cel. Gibbs energie en elektronen kun je niet oplossen in water, daarvoor heb je dragers nodig. Dus als er voldoende Gibbs energie vrijkomt bij een reactie dan wordt het op een drager gezet. Als er bij een andere reactie juist Gibbs energie nodig is dan wordt het van de drager afgehaald. Dit geldt natuurlijk ook voor elektronen. Ook hier zijn dragers nodig die de elektronen transporteren. ATP: de drager van Gibbs energie In de cel is adenosinetrifosfaat (ATP, figuur 6) de belangrijkste drager van de Gibbs energie. ATP wordt gebruikt in vrijwel alle levensprocessen die energie kosten, zoals de synthese van organische moleculen en het transporteren van stoffen door het celmembraan de cel in en uit. Bij de hydrolyse van ATP in adenosinedifosfaat (ADP) en fosfaat (HPO 4 2-, dit is een anorganische fosfaatgroep weergegeven met het symbool P i ) komt onder standaardomstandigheden 30,5 kj/mol aan energie vrij. Figuur 6: ATP in geïoniseerde toestand ATP 4- + H 2 O ADP 3- + HPO H kj mol -1 18
19 Verschillende factoren zorgen voor een groot verschil in Gibbs energie tussen ATP enerzijds en ADP + P i anderzijds: De negatief geladen zuurstofatomen in de fosfaatgroepen van ATP en ADP stoten elkaar af. Deze afstoting is kleiner in ADP dan in ATP. De producten van de hydrolyse van ATP, ADP en HPO 4 2- (P i ), zijn beter oplosbaar dan ATP. Wanneer ionen goed oplosbaar zijn, wordt er door hydratatie een watermantel gevormd die de afstoting tussen de ionen vermindert. Dit is de belangrijkste factor die zorgt voor het grote verschil in Gibbs energie tussen ATP en ADP + P i. ADP kan door nog een fosfaatgroep af te splitsen verder omgezet worden naar adenosinemonofosfaat (AMP), waarbij weer 30,5 kj/mol vrijkomt. Vragen 6. De molecuulformule van ATP is C 10 H 16 N 5 O 13 P 3. In de biosynthese en de biochemie kom je vaak afkortingen en triviale namen van stoffen tegen ook in reactievergelijkingen. Waarom maakt de biochemie vaak gebruik van afkortingen en triviale namen? 7. Net als de meeste andere stoffen maakt de cel op meer dan één manier gebruik van ATP. Noem een paar toepassingen van ATP in de cel? 8. Geef de reactie voor de hydrolyse van ADP tot AMP en fosfaat. 9. Vaak wordt er gezegd dat de binding tussen de fosfaatgroepen van ATP veel energie bevat. Hierdoor ontstaat de indruk dat er bij het verbreken van deze bindingen energie vrijkomt. Waarom is dit onjuist? NADH de drager van elektronen Op verschillende plekken in de cel vinden reductie- en oxidatiereacties plaats. Elektronen moeten worden overgedragen tussen redox-reacties, maar electronen kun je niet oplossen in water. Daarom gebruikt de cel Nicotinamide Adenine Dinucleotide, NADH, (figuur 7 en Binas tabel 67F) als drager van elektronen. De gereduceerde vorm van NADH, NAD +, kan van een donormolecuul (RH 2 ) twee waterstofatomen opnemen. Hierbij worden NADH en een proton gevormd: NAD + + RH 2 NADH + H + + R De oxidatie van NADH verloopt via de volgende reactie: NADH NAD + +H e - NADH kan dus twee elektronen en H + overdragen tussen verschillende processen. Figuur 7: NADH in geïoniseerde toestand. 19
20 Tabel 3: Betaalmiddelen en de bijbehorende energiedragers. Betaalmiddel Energiedrager Geladen vorm Gibbs energie ADP + P i ATP Elektron NAD + NADH Vragen 10. Niet alleen in bacteriën maar ook in onze cellen wordt NADH gebruikt voor de overdracht van elektronen. Waarom is NAD + zo geschikt als elektronenacceptor en NADH als elektronendonor? 20
21 Hoe maakt een bacterie ATP en NADH? Een bacterie kan ATP en NADH maken door o.a. glucose af te breken, dit wordt ook wel de dissimilatie van glucose genoemd. Deze dissimilatie gaat, afhankelijk van de beschikbaarheid van zuurstof, via verschillende routes (figuur 8). De aerobe afbraak van glucose gaat via drie opeenvolgende biosynthetische routes: o de glycolyse, o de citoenzuurcyclus, o de oxidatieve fosforylering (ademhalingsketen). De anaerobe afbraak van glucose verloopt via 2 routes: o de glycolyse o de fermentatie, de omzetting van glucose met behulp van micro-organismen Figuur 8: De afbraak van glucose met zuurstof (aeroob) en zonder zuurstof (anaeroob). Wat betreft ATP en NADH zijn alleen de plaatsen waar het gevormd en verbruikt wordt aangegeven. Vraag 11. Onder welke omstandigheden wordt er in onze spiercellen lactaat gevormd? 21
22 De glycolyse De eerste route voor de afbraak van glucose heet dus de glycolyse ( zie hiervoor ook Binastabel 68). Voor de glycolyse is geen zuurstof nodig en daarom maakt deze route onderdeel uit van zowel de aerobe als de anaerobe afbraak van glucose. Nadat glucose in de cel is opgenomen wordt het via de glycolyse omgezet in twee moleculen pyruvaat (CH 3 COCOO - ). Biologen noemen pyruvaat meestal pyrodruivenzuur, afgekort pdz. De glycolyse bestaat uit 10 stappen die je kunt splitsen in twee delen. 1. Eerst worden er 2 moleculen ATP verbruikt om fructose-1,6-bifosfaat te maken (stap 1 t/m 3). 2. Tijdens het volgende deel van de glycolyse wordt 2 glyceraldehyde-3-fosfaat omgezet in 2 pyruvaat waarbij er 4 ATP en 2 NADH gevormd worden (stap 6 t/m 10). De totaalreactie van de glycolyse is: C 6 H 12 O NAD HPO ADP 3-2 CH 3 COCOO - + 2NADH + 2ATP H 2 O + 2H + Figuur 9: De 10 stappen van de glycolyse. Bij de moleculen is alleen het aantal C-atomen (zwarte bolletjes) en de posities van de fosfaatgroepen (gele P) weergegeven. 22
23 Aerobe afbraak van glucose Na de glycolyse volgen nog twee routes: de citroenzuurcyclus en de oxidatieve fosforylering. Voordat de citroenzuurcyclus kan worden begonnen moet pyruvaat/pyrodruivenzuur worden aangepast. Eerst wordt de carboxylgroep van pyruvaat afgehaald en dit verdwijnt als koolstofdioxide, deze stap noemt men dan ook decarboxylering. Ook bevat het molecuul energie in de vorm van elektronen, die elektronen worden opgenomen door NAD + waardoor er NADH gevormd wordt. De derde aanpassing is het koppelen van een speciaal molecuul, Coenzym-A (CoA) aan de overgebleven acetylgroep waardoor er acetyl-coa ontstaat. De citroenzuurcyclus bestaat uit 8 stappen, in die stappen wordt acetyl-coa omgezet in 2 koolstofdioxide moleculen. Per keer wordt in de cyclus 1 ATP gemaakt, maar de meeste energie gaat via elektronenoverdracht naar NAD + en FAD (FAD is de afkorting van flavine adenine dinucleotide, een stof die net als NAD + als drager van elektronen functioneert, de geladen vorm is FADH 2 ). De tijdens de glycolyse en citroenzuurcyclus gevormde NADH is de beginstof voor de laatste grote stap in de vorming van energie uit glucose: de oxidatieve fosforylering. NADH geeft de opgeslagen electronen af aan enzymen in de celmembraan. Hierna wordt via een serie redoxreacties zuurstof gereduceerd tot water. Hierdoor kunnen deze enzymen de energie uit NADH gebruiken om protonen van binnen de cel naar buiten te transporteren. Op deze manier ontstaat er een verschil in de concentratie van protonen in de cel en buiten de cel (in de cel is de ph hoger dan buiten de cel!). Dit concentratieverschil kan de bacterie (of een andere levende cel) gebruiken voor de synthese van ATP door het enzym ATP-synthetase. De reacties voor de aerobe omzetting van glucose zijn: Glycolyse C 6 H 12 O NAD HPO ADP 3-2 CH 3 COCOO NADH + 2 H ATP H 2 O Decarboxylering 2 CH 3 COCOO HSCoA + 2 NAD + 2 Acetyl-S-CoA + 2 NADH + 2 CO 2 Citroenzuurcyclus 2 Acetyl-S-CoA + 6 NAD FAD + 2 ADP HPO H 2 O 2 HSCoA + 6 NADH + 2 FADH H ATP CO 2 Oxidatieve fosforylering 2 NADH + O 2 +2 H + 2 H 2 O + 2 NAD + 2 FADH 2 + O 2 2 H 2 O + 2 FAD Per NADH wordt er maximaal 3 ATP gevormd en per FADH 2 2 ATP. Aangezien er tijdens de glycolyse, decarboxylering en citroenzuurcyclus 10 NADH en 2 FADH 2 gevormd worden, levert de oxidatieve fosforylering in totaal 34 ATP op. De totaalreactie van de aerobe dissimilatie van glucose is: C 6 H 12 O O ADP P i 6CO H 2 O + 38 ATP 4- Vragen 12. Leg uit waarom tijdens de eerste stap in de glycolyse een fosfaatgroep aan glucose wordt gekoppeld? 13. Leg uit waarom chemici het over pyruvaat hebben en niet over pyrodruivenzuur zoals biologen? 14. Wat is het belangrijkste verschil in reactiemechanisme tussen de verbranding van glucose en de aerobe dissimilatie van glucose? 23
24 Anaerobe afbraak van glucose Als er geen zuurstof aanwezig is, vindt de afbraak van organische moleculen plaats door middel van fermentatie (gisting). Omdat er geen zuurstof nodig is voor de glycolyse verloopt de afbraak van glucose zonder zuurstof ook via deze route. Het gevormde pyruvaat wordt hierna omgezet in koolstofdioxide, lactaat, ethanol of andere alcoholen en carbonzuren. De reactie voor de vorming van lactaat uit pyruvaat is: CH 3 COCOO - + NADH + H + CH 3 CHOHCOO - + NAD + De totaalreactie van de anaerobe dissimilatie van glucose tot lactaat is: C 6 H 12 O ADP HPO CH 3 CHOHCOO ATP H 2 O De energieopbrengst van de anaerobe afbraak van glucose is dus veel lager dan van de aerobe afbraak! Vraag 15. Bereken het verschil in energieopbrengst tussen de anaerobe en aerobe dissimilatie van glucose in kj per mol glucose. 3.4 Basisprincipes in de biosynthese In dit hoofdstuk zijn een aantal basis principes van de biosynthese behandeld aan de hand van de afbraak van glucose. Deze basis principes of beter gezegd algemene regels gelden niet alleen voor de biosynthetische routes die je nu geleerd hebt, maar kun je veel breder toepassen. De volgende regels kun je algemeen toepassen: Bijna alle processen in levende organismen spelen zich af in water en dus in oplossingen Voor niets gaat de zon op geldt ook voor alle biosynthetische processen. Voor het maken van allerlei stoffen moet betaald worden. In de biosynthese wordt gebruik gemaakt van algemene betaalmiddelen. Als je energie nodig hebt moet je ATP verbruiken, als je elektronen nodig hebt kun je gebruik maken van NADH. Biosynthetische processen mogen niet spontaan verlopen en er mag niet zo maar ATP of NADH gevormd of verbruikt worden. Daarom gelden er basisprincipes voor de regulering van activiteiten. De Gibbs energie speelt hierbij altijd een belangrijke rol. In de chemische industrie moeten de wetenschappers die productieprocessen ontwerpen rekening houden met deze basisprincipes. De komende twee hoofdstukken worden er twee productieprocessen besproken: Melkzuur productie als voorbeeld uit de klassiek biotechnologie. De grote uitdaging is om melkzuurbacteriën grote hoeveelheden melkzuur te laten produceren en het melkzuur zuiver in handen te krijgen. De productie van 1,3-propaandiol, een voorbeeld van moderne biotechnologie uit de 21 e eeuw. In eerste instantie waren er geen micro-organismen die deze stof kunnen maken. Daarom heeft men de bacterie Escherichia coli (E.coli) genetisch zo gemodificeerd dat de nieuwe stam 1,3-propaandiol uit glucose kan produceren. Na de fermentatie vinden er een aantal zuiveringstappen plaats om het product in handen te krijgen. 24
25 Wat je nu moet weten Metabolisme o Vijf basisfuncties Energievoorziening van de cel o ATP o NADH o Actief transport Dissimilatie van glucose o Aerobe afbraak Glycolyse Citroenzuurcyclus Oxidatieve fosforylering o Anaerobe afbraak Glycolyse Fermentatie 25
26 Hoofdstuk 4 Klassieke biotechnologie: de melkzuurfabriek Melkzuur Eigenschappen Melkzuur is de triviale naam voor 2-hydroxypropaanzuur. Melkzuur is in zuivere vorm een witte vaste stof met een smeltpunt van 53 0 C. Een melkzuurmolecuul bevat een asymmetrisch koolstofatoom en van melkzuur komen daarom twee optische isomeren voor, linksdraaiend melkzuur en rechtsdraaiend melkzuur. Zie voor het onderwerp optische isomerie de website Melkzuur behoort tot de carbonzuren en is dus een zwak zuur. De geconjugeerde base van melkzuur heet lactaat ion. Het lactaat ion kan met metaalionen lactaatzouten vormen. Van deze lactaatzouten is calciumlactaat matig oplosbaar en zouten met andere metaalionen, bijvoorbeeld zink, zijn meestal slecht oplosbaar. Toepassingen Melkzuur en lactaten kennen veel toepassingen, vooral in de levensmiddelen-, cosmetische-, farmaceutische- en medische industrie. De productie groeide van circa ton per jaar in 1960 tot meer dan in Figuur 1: Toepassingen van melkzuur. Zie ook (applications) Omdat een melkzuurmolecuul zowel een carboxyl-groep als een hydroxyl-groep bevat, kan er onder bepaalde omstandigheden polycondensatie optreden. Er ontstaat dan polymelkzuur. Polymelkzuur met een hoog moleculair gewicht heeft de mechanische eigenschappen die vereist zijn voor toepassingen zoals hechtdraad, vezels voor beschadigde pezen en kruisbanden, of materialen voor het herstellen van botfracturen en sportblessures. Voorbeelden hiervan zijn schroeven 26
27 voor het vastzetten van een nieuwe kruisband in de knie of weerhaakjes voor reparatie van een gescheurde meniscus. Een niet-medische toepassing is de vervanging van plastics, die op basis van aardolie zijn gemaakt. In 1997 is Cargill Dow ontstaan, gericht op productie op grote schaal van polymelkzuur voor afbreekbare plastics, coatings en verpakkingsmateriaal. Vragen 1. Geef de structuurformules van melkzuur en zijn geconjugeerde base. 2. Geef in de structuurformule van melkzuur met een sterretje het asymmetrische koolstof atoom aan. Experiment: Productie van melkzuur door melkzuurbacteriën. Vraag het werkblad productie van melkzuur door melkzuurbacteriën. 4.1 Synthese van melkzuur Het gegeven dat melkzuurbacteriën melkzuur kunnen produceren, wordt al eeuwen gebruikt in de productie van yoghurt en zuurkool. Maar kun je deze bacteriën ook gebruiken om zuiver melkzuur te produceren in plaats van melkzuur chemisch te synthetiseren? De meest gebruikte chemische synthese route voor de productie van melkzuur is via de hydrolyse van 2-hydroxypropaannitril (CH 3 CHOHCN) m.b.v. een oplossing van zwavelzuur. Het 2-hydroxypropaannitril dat hiervoor nodig is, wordt gevormd uit waterstofcyanide en ethanal. De grondstof voor ethanal is aardolie. Vragen 3. Geef de reactievergelijking in structuurformules voor de vorming van 2-hydroxypropaannitril uit waterstofcyanide en ethanal. 4. Geef de reactievergelijking in structuurformules voor de hydrolyse van 2- hydroxypropaannitril waarbij een molecuul melkzuur en een ammoniumion gevormd wordt. De chemische synthese levert een mengsel waarin beide optische isomeren van melkzuur evenveel voorkomen. Vooral bij het gebruik in voedingsmiddelen en medicijnen is dit bezwaarlijk omdat linksdraaiend melkzuur allergieën kan veroorzaken. Veel soorten melkzuurbacteriën maken alleen rechtsdraaiend melkzuur, dit is dus een duidelijk punt in het voordeel van de bacteriële productie. Een ander voordeel van het gebruik van melkzuurbacteriën is dat ze glucose als grondstof gebruiken. Meestal is glucose van plantaardige oorsprong en is dus een hernieuwbare grondstof die niet uitgeput raakt. De grote uitdaging is om melkzuurbacteriën grote hoeveelheden melkzuur te laten produceren en het melkzuur zuiver in handen te krijgen. Dit hoofdstuk laat zien dat daar een behoorlijke hoeveelheid chemische technologie voor nodig is. Vragen 5. Wat zijn de afvalstoffen bij de chemische synthese van melkzuur? 6. Hoe komt het dat de melkzuur die door bacteriën wordt gemaakt vaak stereospecifiek is? 27
28 4.2 Melkzuurfabriek In het vorige hoofdstuk heb je gezien dat glucose in een zuurstofarm milieu door bacteriën wordt omgezet in melkzuur of ethanol. Figuur 4 uit hoofdstuk 3 laat zien dat om van glucose melkzuur (lactaat) te maken eerst de horizontale hoofdroute gevolgd moet worden tot pyruvaat. Dit is zoals je geleerd hebt de glycolyse. Pyruvaat wordt via fermentatie omgezet in lactaat. Om zoveel mogelijk van het gewenste melkzuur te maken heb je heel veel melkzuurbacteriën nodig. Bacteriën vermenigvuldigen zich door middel van deling. Dit gebeurt gecontroleerd in een zogenaamde fermentor. Dit is een apparaat waarin de temperatuur, de ph, de toevoer van zuurstof en de toevoer van voedingsstoffen gemeten, geregeld en bewaakt kunnen worden. Er zijn fermentoren voor proeven in laboratoria waar één tot tientallen liters vloeistof in kunnen voor onderzoek. Maar bedrijven die een stof produceren doen dit op grote schaal en gebruiken fermentoren waar wel liter in kan! Figuur 2: Links een afbeelding van een grote industriële fermentor. Rechts de verschillende fasen van bacteriegroei De groeicurve van bacteriën heeft 4 fasen. A. De aanpassingsfase; als bacteriën in een medium komen duurt het even voordat de bacteriecellen kunnen gaan delen. Een medium is de vloeistof/suspensie waarin bacteriën groeien, deze bevat alle voedingsstoffen die bacteriën nodig hebben. De groei komt dus langzaam op gang. B. De groeifase; na de aanpassingsfase gaan de bacteriecellen met optimale snelheid delen. C. De stationaire fase; in deze fase is er geen groei of afname van de hoeveelheid bacteriecellen. De totale hoeveelheid bacteriecellen blijft dus gelijk. Als de bacteriën in de stationaire fase zijn gekomen gaan ze melkzuur produceren. D. De drie groeifasen worden gevolgd door de afstervingsfase. Het groeien gaat niet eindeloos door. Als de voedingstoffen op zijn of bepaalde bacteriële producten zich ophopen, stopt de groei. Vragen 7. Bestudeer in figuur 4 van hoofdstuk 3 de biosynthetische routes. Welke routes zijn belangrijk als de cel aan het groeien en of delen is? Tip: bedenk wat de belangrijke bouwstenen van de celwand en het cytoplasma zijn, zie figuur 2 en bladzijde 1 en 2 van hoofdstuk Waarom laat men bacteriën pas in de stationaire fase melkzuur produceren en niet ook in de groeifase? Melkzuur wordt geproduceerd door middel van een batch- of een fed-batch proces. Een batch reactor is een gesloten, goed gemengd vat. Een productiecyclus wordt gestart door alle grondstoffen en de bacteriën in de reactor te brengen. Tijdens een productiecyclus, ook wel batch genoemd, worden geen stoffen aan- of afgevoerd, behalve eventueel zuurstof en/of stoffen om de ph aan te passen. 28
29 Tijdens een batch proces is, als gevolg van de reacties die plaatsvinden tijdens het proces, sprake van continu veranderende concentraties van de diverse stoffen, dus een continu veranderende omgeving. Dit heeft ten gevolge dat de melkzuurproductie niet maximaal is. Daarom wordt voor de productie van melkzuur gebruik gemaakt van een fed-batch proces. Bij een fed- batch reactor is er, anders dan bij de batch reactor, sprake van een instroom van stoffen tijdens het proces. Figuur 3: Links een schematische voorstelling van een batch reactor en rechts van een fed-batch reactor De reactor wordt gevuld met bacteriën en medium. Dit medium bevat behalve de glucose oplossing (het substraat) ook voedingsstoffen die de bacterie nodig heeft om te groeien en te overleven zoals stikstofbronnen, vitamines, aminozuren en metaalionen. Tijdens de groeifase (B) gebruiken de bacteriën glucose en voedingsstoffen. Als de optimale hoeveelheid bacteriën is gevormd gaat er een toenemend tekort aan voedingsstoffen ontstaan. Een deel van de bacteriën sterft daardoor af. Dit is het begin van de stationaire fase (C). Het aantal bacteriën dat in deze fase afsterft, is even groot als het aantal bacteriën dat gevormd wordt. Om de bacteriën optimaal te laten produceren worden gedurende de stationaire fase gedoseerd glucose (substraat) en één of meer voedingscomponenten toegevoegd. De concentraties van de in de reactor aanwezige stoffen zijn daardoor minder aan veranderingen onderhevig en dit resulteert in een grotere melkzuur productie. Bij de productie van melkzuur wordt het medium steeds zuurder. De bacteriën kunnen hier niet goed tegen. Vaak wordt daarom calciumcarbonaat toegevoegd als buffer. Mocht de ph erg wisselen, dan kan er tijdens het proces een zuur of een base worden toegevoegd. Als er zoveel melkzuur in het mengsel zit, dat de leefomstandigheden voor de bacterie heel ongunstig worden, begint de afstervingsfase (D). Dat is het einde van het fed-batch proces. Na dit fermentatieproces heb je een vloeistof waarin zich melkzuur, medium en bacteriën bevinden. Het medium en de bacteriën zullen eerst van het melkzuur gescheiden moeten worden. 4.3 Zuivering melkzuur Na fermentatie zijn er verschillende mogelijkheden om het melkzuur te scheiden van het fermentatie mengsel. Meestal wordt de productie van melkzuur gestopt door het verhogen van de zuurgraad m.b.v. calciumcarbonaat tot ph =10, gevolgd door verhitten. De hoge ph doodt de bacteriën, de combinatie van hoge temperatuur en hoge ph breekt overgebleven suikers af. De calciumionen laten de eiwitten en cellen samenklonteren zodat ze sneller neerslaan. Verhitten zorgt ook voor het neerslaan van een eventuele overmaat aan calciumcarbonaat. Na verhitten wordt het fermentatiemengsel gefiltreerd. 29
30 Vraag 9. Noem 4 stoffen die in ieder geval in het residu aanwezig zullen zijn. Kijk even naar de samenstelling van de cel in hoofdstuk 2. Blokschema melkzuurproductie Het filtraat van het fermentatiemengsel bevat een lage concentratie melkzuur en nog allerlei andere stoffen. Voor de meeste toepassingen moet de concentratie melkzuur verhoogd worden en verder gezuiverd worden. In figuur 4 staan de blokschema s van vijf routes voor het zuiveren van het melkzuur. In elk schema staan de belangrijkste bewerkingen in blokken gegeven en de stofstromen zijn de pijlen tussen de blokken. Voor de productie van glucose uit ruwe grondstoffen is in de figuur route -1 opgenomen. Opdracht Zuivering melkzuur Maak een groepje van 3 of 4 personen en kies een route die je nader gaat bestuderen. In deze opdracht zijn jullie samen een chemisch adviesbureau dat moet adviseren over een te kiezen scheidingsroute voor een nieuw te bouwen melkzuurfabriek. Maak de vragen bij de route en bereid daarna een presentatie voor van maximaal 5 minuten waarin je de directie (de rest van de klas) uitlegt hoe de door jullie gekozen scheidingsroute werkt. De antwoorden van de vragen bij de route moeten in je presentatie voorkomen. Het laatste gedeelte van de les worden de voor- en nadelen van de verschillende routes besproken. Soorten vragen Staat ergens in de module uitgelegd of verwijst naar het antwoord van een andere vraag. Opzoeken op Internet of in chemiekaarten. Herhaling scheikunde kennis. 30
31 Figuur 4: Blokschema voor de melkzuur productie volgens het fed-batch proces. In het blokschema staan de belangrijkste bewerkingen in de blokken aangegeven en de stofstromen zijn de pijlen tussen de blokken. De route begint bij 0 (glucose). De routes 1 t/ 5 zijn de verschillende methodes die gebruikt worden om het melkzuur te zuiveren. Route -1 wordt gevolgd indien er ruwe grondstoffen gebruikt worden 31
32 Route -1 Figuur 5: blokschema route -1 Vragen bij route -1 De prijs van technisch zuiver melkzuur (± 90%) wordt voor 65% tot 80% bepaald door de prijs van de grondstof. Vooral voor toepassingen in de chemische bulk chemie is het erg belangrijk dat de grondstoffen goedkoop zijn. Daarom wordt er op dit moment veel onderzoek gedaan naar de mogelijkheid om ruwe grondstoffen uit de landbouw en voedingsindustrie te gebruiken als grondstof. Naast de prijs is het ook belangrijk dat de grondstof niet te veel restafval geeft en dat de grondstoffen redelijk zuiver zijn. Ook is het van belang dat grondstoffen het hele jaar beschikbaar zijn. 1. Leg uit of bij de productie van medicijnen de prijs van de grondstof erg belangrijk of minder belangrijk is. / 2. Leg uit waarom het belangrijk is dat een grondstof het hele jaar te verkrijgen is. Welke van de grondstoffen in tabel 1 zijn dat? / In de meeste van de grondstoffen in tabel 1 zijn opgebouwd uit cellulose en/of zetmeel Deze stoffen moeten eerst omgezet worden in glucose voordat ze gebruikt kunnen worden in de melkzuur productie. 3. Welke grondstoffen leveren cellulose en welke zetmeel? / Tabel 1:recent onderzochte bacteriesoorten en ruwe grondstoffen Ruwe grondstof Soort bacterie Opbrengst (gl -1 ) Productiesnelheid (gl -1 h -1 ) 1 Melasse Lactobacillus delbrueckii 90,0 3,8 2 Enterococcus faecalis RKY1 95,7 4,0 3 Rogge Lactobacillus paracasei No. 8 84,5 2,4 4 Gierst Lactobacillus paracasei No ,0 3,5 5 Tarwe Lactobacillus lactis ssp, lactis ATCC ,0 1,0 6 Enterococcus faecalis RKY1 102,0 4,8 7 Maïs Enterococcus faecalis RKY1 63,5 0,5 8 Lactobacillus amylovorus ATCC ,1 0,8 9 Cassave Lactobacillus amylovorus ATCC ,8 0,2 10 Aardappel Lactobacillus amylovorus ATCC ,2 0,1 11 Rijst Lactobacillus sp, RKY2 129,0 2,9 12 Gerst Lactobacillus casei NRRL B ,0 3,4 13 Lactobacillus amylophilus GV6 27,3 0,3 14 Cellulose 1 Lactobacillus corniformis ssp, Torquens ATCC 24,0 0, Corncob 2 Rhizopus sp, MK ,0 0,3 16 Papierafval Lactobacillus corniformis ssp, Torquens ATCC 23,1 0, Rhizopus oryzae NRRL ,1 0,7 18 Hout Lactobacillus delbrueckii NRRl B ,0 0,9 19 Enterococcus faecalis RKY1 93,0 1,7 20 Wei Lactobacillus helveticus R211 66,0 1,4 21 Lactobacillus casei NRRL B ,0 4,0 1- stro, zemelen, maïsstengels etc, 2- maïskolven zonder maïskorrels 32
33 Uit zetmeel en cellulose bevattende grondstoffen moet eerst door hydrolyse de glucose vrijgemaakt worden. Dit kan met geconcentreerd zwavelzuur of door verhitten, maar een energiezuiniger en schonere methode is om met behulp van enzymen de cellulose en/of het zetmeel af te breken. Zie Binas tabel 82H. 4. Welke enzym kan gebruikt worden om zetmeel om te zetten in glucose? / 5. Welke enzym kan gebruikt worden om cellulose om te zetten in glucose? / Wei is een restproduct van de productie van kaas. Het bevat onder andere lactose, eiwitten en vetten 6. Uit welke van de hierboven genoemde drie stoffen kan je glucose maken? Welk enzym is daarvoor nodig? / 7. Is wei een geschikte grondstof voor de productie van melkzuur? Baseer je conclusie op prijs, beschikbaarheid, zuiverheid, oplosbaarheid en hoeveelheid restafval. / Uit ethische en economische overwegingen is het niet wenselijk om gebruik te maken van grondstoffen, die ook belangrijk zijn voor de voedselproductie. Tabel 1 geeft voor een aantal grondstoffen de opbrengst aan melkzuur in gram per liter medium en de productiesnelheid in gram per liter medium per uur. 8. Welke 5 grondstoffen leveren het meeste melkzuur per liter medium? 9. Welke van in vraag 8 gevonden 5 grondstoffen is geen belangrijke voedingsstof? Wat is het belangrijke nadeel van deze grondstof? Een andere studie laat zien welke optische isomeer van melkzuur gemaakt wordt en of de melkzuurbacteriën homofermenterend of heterofermenterend zijn. Homofermentatieve melkzuurbacteriën produceren alleen melkzuur uit maltose of glucose in anaërobe omstandigheden. Heterofermentatieve melkzuurbacteriën produceren naast melkzuur ook ethanol en CO 2 uit allerlei hexosen. In de tabel wordt voor de twee optische isomeren van melkzuur de aanduiding D of L gebruikt. De groepen rond het asymmetrisch koolstofatoom kunnen ruimtelijk gezien op twee manieren gerangschikt zijn. Vaak wordt in dit verband van de D- en L- configuratie gesproken. Zie voor dit onderwerp Als in de tabel DL staat betekent dit dat de bacteriën een racemisch mengsel produceren. Tabel 2: recent onderzochte melkzuur bacteriën Lactobacillus Homofermenterend Heterofermenterend Melkzuur isomeer L. delbrueckii + - D L. lactis + - D L. bulgaricus + - D L. casei + - L L. plantarum + - DL L. curvatus + - DL L. brevis - + DL L. fermentum - + DL Sporolactobacillus S. inulinus + - D Streptococcus S. faecalis + - L S. cremoris + - L S. lactis + - L Leuconostoc L. mesenteroides - + D L. dextranicum - + D 33
34 Omdat D-melkzuur allergieën kan veroorzaken, wordt in medicijnen en cosmetica alleen L-melkzuur gebruikt. 10. Welke ruwe grondstof kan gebruikt worden voor de productie van L-melkzuur? Combineer hiervoor de gegevens uit de tabellen 1 en Als grondstof voor een kleurstof in LCD schermen voor kleurentelevisies wordt D- melkzuur gebruikt. Welke ruwe grondstoffen kunnen hiervoor gebruikt worden? 12. Bereid een les voor waarin je de voor en nadelen van het gebruik van verschillende grondstoffen toelicht. Kies daarna de (volgens jullie) optimale grondstof, zoek uit welk enzym daarvoor nodig is. 13. Geef bij de pijlen tussen de blokken aan welke stoffen er worden vervoerd. 34
35 Route 1 Figuur 6: blokschema route 1 Vragen bij route 1 In blok 1.1 wordt kalk aan het fermentatiemengsel toegevoegd om de ph te verhogen. 1. Geef de naam en de formule van de stof die met de triviale naam kalk wordt bedoeld? 2. Leg met behulp van een reactievergelijking uit waarom de ph van het mengsel stijgt door het toevoegen van kalk. 3. Geef de reactievergelijking voor het ontstaan van een neerslag bij verhitten. 4. Welke stof(fen) zit(ten) er in het residu van blok 1.1? Voor het goed verlopen van de processen in blok 1.2 is de ph belangrijk. De ph van het filtraat uit blok 1.1 is ongeveer 10 en moet verlaagd worden om zo veel mogelijk lactaat weer om te zetten in melkzuur. In dit blok moet ook de eventuele overmaat aan Ca 2+ ionen verwijderd worden. 5. Welke stof kan je gebruiken om de ph te verlagen? Tip: bedenk daarbij of deze stof in je eindproduct terechtkomt. 6. Welke stof zal in het residu aanwezig zijn? 7. De pk z van melkzuur is 3,95. Bereken de verhouding melkzuur : lactaat-ion bij ph = pk z. 8. Bereken bij welke ph de verhouding melkzuur : lactaat-ion gelijk is aan 9 : 1. In blok 1.2 wordt diisopropylether gebruikt voor de extractie van melkzuur uit het mengsel. 9. Geef de structuurformule en de systematische naam van diisopropylether 10. Is diisopropylether een veilige stof om mee te werken? Om te weten welke gevolgen blootstelling aan deze stof kan hebben ga je naar de site met Ïnternational Chemical Safety Cards Leg uit waarom diisopropylether een geschikt extractiemiddel is om melkzuur uit water te extraheren. 12. Leg uit waarom het lactaat-ion niet goed oplost in diisopropylether. Licht je antwoord toe. In blok 1.3 moet het mengsel van melkzuur en diisopropylether weer gescheiden worden. Daarvoor wordt gebruik gemaakt van tegenstroomwassen. 13. a. Wat verstaan we onder tegenstroomwassen. b. Leg uit waarom melkzuur van de diisopropyletherstroom naar de waterstroom gaat. c. Leg met behulp van een tekening uit hoe je een tegenstroomopstelling zou kunnen bouwen m.b.v. practicumspullen op school. Tip: denk aan een gaswasflesje. 14. Geef bij de pijlen tussen de blokken aan welke stoffen er worden vervoerd. 35
36 Route 2 Figuur 7: blokschema route 2 Vragen bij route 2 In blok 2.2 wordt gesproken van extractie. Voor de extractie van melkzuur wordt bijv. trioctylamine, N(C 8 H 17 ) 3, toegevoegd aan heptaan. Trioctylamine, een tertiaire amine, is dus een hulpstof bij de extractie. 1. Geef de structuurformule van trioctylamine en heptaan. 2. Leg uit waarom heptaan geen geschikt extractiemiddel is voor melkzuur? 3. Leg uit waarom trioctylamine goed oplost in heptaan. 4. Trioctylamine kan net als NH 3 in water als base reageren. Laat dit zien m.b.v. een reactievergelijking. Tijdens de extractie in blok 2.2 vindt er een reactie plaats waarbij een organisch zout wordt gevormd. Een organisch zout is een zout waarin het positieve metaalion is vervangen door een positief organisch ion. Voor deze techniek wordt vaak de term reactieve extractie gebruikt. 5. Geef de reactievergelijking voor de reactie die plaatsvindt in blok 2.2. / 6. Leg uit waarom dit organisch zout oplost in heptaan. Het verdelingsevenwicht van melkzuur, zowel in de lactaatvorm als in de zure vorm, over de waterfase en de heptaanfase is gegeven door: [ Melkzuur] heptaan+trioctylamine K = Melkzuur [ ] water De waarde van K wordt bepaald als functie van de ph. De resultaten zijn weergeven in de grafiek hiernaast met de waarde van K op de verticale as. 7. In welk ph gebied extraheer je de maximale hoeveelheid melkzuur in blok 2.2? 8. Bereken het percentage melkzuur dat geëxtraheerd wordt bij ph = 2,5. 9. Leg nu uit waarom het filtraat uit blok 2.2 wordt aangezuurd. Figuur 8: De verdelingsconstante K voor de verdeling van melkzuur over de waterfase en de heptaan+trioctylamine fase als functie van de ph van de waterfase. Na indampen in blok 2.3 wordt een zout gevormd. Bij de hoge temperatuur in blok 2.4 ontleedt dit zout in melkzuur en trioctylamine. 10. Zoek het kookpunt en smeltpunt van heptaan op. 11. Zoek het kookpunt en smeltpunt van trioctylamine op 12. Wat is het kookpunt en smeltpunt van melkzuur. 13. Bij welke temperatuur kan het mengsel van het oplosmiddel en het zout van melkzuur en trioctylamine in blok 2.3 gescheiden worden? 14. Geef van de reactie, die in blok 2.4 verloopt, de reactievergelijking. 36
37 15. Geef bij de pijlen tussen de blokken aan welke stoffen er worden vervoerd. 37
38 Route 3 Figuur 9: blokschema route 3 Vragen bij route 3 In blok 3.1 wordt kalk aan het fermentatiemengsel toegevoegd om de ph te verhogen. 1. Geef de naam en de formule van de stof die met de triviale naam kalk wordt bedoeld? 2. Leg met behulp van een reactievergelijking uit waarom de ph van het mengsel stijgt door het toevoegen van kalk. 3. Geef de reactievergelijking voor het weer neerslaan van de overmaat aan kalk bij verhitten. 4. Welke stof(fen) zit(ten) in het residu van blok 3.1. In blok 3.2 wordt methanol toegevoegd. In de reactor reageert melkzuur met methanol. 5. Geef van deze reactie de reactievergelijking in structuurformules. / 6. Geef de systematische naam van de gevormde stof. 7. Verwacht je dat het reactieproduct van blok 3.2 goed oplosbaar is in water? Licht je antwoord toe! 8. Zal de reactie in blok 3.2 beter verlopen bij een hoge of bij een lage ph. Licht je antwoord toe. Bij het productieproces kan afhankelijk van het soort bacteriën dat gebruikt wordt, een van de optische isomeren van melkzuur gevormd worden. Het is ook mogelijk dat de bacteriën een racemisch mengsel produceren. Voor de twee optische isomeren van melkzuur wordt de aanduiding D of L gebruikt. De groepen rond het asymmetrisch koolstofatoom kunnen ruimtelijk gezien op twee manieren gerangschikt zijn. Men spreekt dan van de D- en L- configuratie van melkzuur. Zie voor dit onderwerp DL betekent dat de bacteriën een racemisch mengsel geproduceerd hebben. We gaan er bij dit proces vanuit dat de gebruikte bacterie L-melkzuur produceert. 9. Wat zijn de kookpunten van het L-, DL- en D-melkzuur? Je kunt dit opzoeken op het internet of in het Handbook of Chemistry and Physics. In moderne fabrieken worden blokken 3.2 en 3.3 samengevoegd. In dit geval spreken we van reactieve destillatie. 10. Leg uit wat we onder reactieve destillatie verstaan. In blok 3.4 wordt het reactieproduct van blok 3.2 gehydrolyseerd (zie vraag 6). 11. Geef de reactievergelijking van deze hydrolyse. 12. Welke stof wordt toegevoegd om ervoor te zorgen dat deze hydrolyse volledig verloopt? 13. Bij welke ph zal deze hydrolyse optimaal verlopen? Licht je antwoord toe. / 14. Levert deze route gemakkelijk een verdunde of een geconcentreerde melkzuuroplossing? Licht je antwoord toe. / 15. Geef bij de pijlen tussen de blokken aan welke stoffen er worden vervoerd. 38
39 Route 4 Figuur 10: blokschema route 4 Vragen bij route 4 In blok 4.1 wordt kalk aan het fermentatiemengsel toegevoegd om de ph te verhogen. 1. Geef de naam en de formule van de stof die met de triviale naam kalk wordt bedoeld? 2. Leg met behulp van een reactievergelijking uit waarom de ph van het mengsel stijgt door het toevoegen van kalk. 3. Geef de reactievergelijking voor het weer neerslaan van de overmaat aan kalk bij verhitten. 4. Welke stof(fen) zit(ten) in het residu van blok 4.1. Het mengsel van stoffen dat van blok 4.1 naar blok 4.2 gaat wordt in blok 4.2 ingedampt. Door het indampen ontstaan er zoutkristallen. 5. Geef de verhoudingsformule en de naam van het ontstane zout. / In blok 4.3 wordt zwavelzuur toegevoegd om de vaste stof uit blok 4.2 om te zetten. Hierbij verlopen er twee reacties na elkaar, waarbij onder andere de calciumionen neerslaan. Tevens wordt in dit blok actieve kool toegevoegd. 6. Geef de reactievergelijkingen van de twee reacties die plaatsvinden in blok 4.3. / 7. Welke stoffen worden in het algemeen verwijderd door het toevoegen van de actieve kool. 8. Hoe heet deze methode en op welk principe berust deze methode? / De oplossing uit blok 4.3 wordt in blok 4.4 opnieuw ingedampt. De kristallen in blok 4.2 worden dus in blok 4.3 opgelost om vervolgens in blok 4.4 opnieuw gevormd te worden. Deze handeling wordt ook wel herkristallisatie genoemd. 9. Waarom wordt deze herkristallisatie uitgevoerd? 10. Geef de vergelijking van de reactie in blok 4.4. / 11. Hoe maakt men uit het eindproduct van deze route (Ca(C 3 H 5 O 3 ) 2 ) het melkzuur? 12. Geef bij de pijlen tussen de blokken aan welke stoffen er worden vervoerd. 39
40 Route 5 Figuur 11: blokschema route 5 Vragen bij route 5 In de figuur rechts staat een elektrodialyse cel afgebeeld. Als de twee elektroden via een stroombron met elkaar worden verbonden gaat er een elektrische stroom door de oplossing open. 1. Geef in de figuur aan naar welke richting de ionen gaan bewegen ten gevolge van de aangelegde bronspanning. 2. Naast de lading is er nog een andere eigenschap die bepaalt hoe snel de ionen zich in de oplossing kunnen bewegen. Welke eigenschap van de ionen is dat? In de figuur rechts staat dezelfde cel maar nu zijn semi-permeabele membranen voor de elektroden geplaatst. Deze membranen scheiden op grootte en op lading. De ionen moeten door de poriën heen kunnen. Door elektrisch afstoting kunnen positief geladen ionen niet door een positief geladen membraan en vice versa 3. Kunnen in de cel rechts de natriumionen de negatieve pool bereiken? Licht je antwoord toe. 4. Kunnen de sulfaationen de positieve pool bereiken? Licht je antwoord toe. 5. Kunnen natriumionen en sulfaationen op deze wijze volledig van elkaar gescheiden worden? Licht je antwoord toe. In de cel rechts is nu in de ruimte tussen de membranen het fermentatiemengsel uit blok 0.0 gebracht. De membranen zijn zo gemaakt dat lactaat ionen deze kunnen passeren maar grotere negatief geladen ionen niet. 6. Geef in de figuur rechts aan hoe lactaat ionen, waterstofionen en calcium ionen zich door de cel bewegen. /ι 7. Waarom is het bij deze scheidingsmethode niet noodzakelijk om eerst suikers, bacteriëncellen en eiwitten uit het fermentatiemengsel te verwijderen? Figuur 12 Uit onderzoek blijkt ook dat als tijdens elektrodialyse ook de elektrolyse van water plaatsvindt de scheiding nog efficiënter verloopt. Er wordt dan meteen melkzuur verkregen i.p.v. een lactaatzout 8. Geef de reactie van water aan de negatieve pool. 9. Geef de reactie van water aan de positieve pool. 10. Leg uit waarom nu meteen melkzuur gevormd wordt. / 11. Geef aan uit welke stoffen het neerslag bestaat. / 12. Geef bij de pijlen tussen de blokken aan welke stoffen er worden vervoerd. 40
41 _ 4.4 Productie van polymelkzuur Polymelkzuur Polymelkzuur is het polymeer van melkzuur. Hieronder is een deel van een polymelkzuurmolecuul (PLA=poly lactic acid) weergegeven: H O H O H O O C C CH 3 O C C CH 3 O C C CH 3 n Figuur 13: Een deel van een polymelkzuurmolecuul (PLA) De materiaaleigenschappen van PLA zijn vergelijkbaar met die van polyetheen. PLA en polyetheen zijn allebei kleurloze thermoplasten met relatief lage smeltpunten. Net als bij polyetheen hangen de materiaaleigenschappen van PLA sterk af van de ketenlengte. Beide polymeren kunnen zowel in amorfe als kristallijne structuur ( ) voorkomen. Dit verschil in structuur heeft een groot effect op de smeltpunten. Het amorf of kristallijn zijn van PLA wordt in hoge mate bepaald door de ruimtelijke structuur van de asymmetrische koolstofatomen in de keten. Het grote verschil tussen polyetheen en PLA is dat polymelkzuur in aanwezigheid van enzymen of bij hogere temperaturen gemakkelijk hydrolyseert. Het daarbij ontstane melkzuur kan door aërobe organismen afgebroken worden tot koolstofdioxide en water. Wel is het zo dat kristallijn PLA veel langzamer hydrolyseert dan amorf PLA. Vraag 1. Verklaar waarom kristallijn PLA zoveel slechter biologisch afbreekbaar is dan amorf PLA. Productie polymelkzuur Door polycondensatie kan polymelkzuur gevormd worden uit melkzuur n H OH _ H C C O C OH H H H O _ C C O CH 3 _ n + n H 2 O Figuur 14: De polycondensatie van melkzuur tot PLA De gemakkelijke hydrolyse van PLA suggereert al dat bovenstaande reactie omkeerbaar is en dat het onder de meeste omstandigheden een evenwichtsreactie is. In de synthese van PLA is het moeilijk om lange ketens te maken, omdat door de aanwezigheid van het gevormde water, de gevormde ketens weer gemakkelijk verbroken worden. Ook vormt het mengsel van polymelkzuur en water een stroperig mengsel dat moeilijk te verwerken is. Experiment: Productie polymelkzuur Vraag het werkblad productie polymelkzuur aan bij je docent en maak ook de vragen bij de proef 41
42 Voor de synthese van PLA met goede materiaaleigenschappen is het belangrijk te voorkomen dat de terugreactie plaatsvindt. Voor de industriële productie van PLA worden op dit moment daarvoor twee methoden gebruikt: I) In de eerste methode wordt melkzuur eerst omgezet in een dilactide Het dilactide wordt vervolgens gepolymeriseerd tot PLA. Het dilactidemolecuul is op te vatten als een veresteringsproduct, dat is ontstaan uit twee melkzuurmoleculen. (zie figuur 15) II) In de tweede methode wordt zoveel mogelijk water aan het reactiemengsel ontrokken waardoor de terugreactie niet meer kan plaatsvinden. Figuur 15: De structuurformule van het dilactide ook vaak lactide genoemd. Opdracht Productie van PLA Er moet een keuze gemaakt worden tussen een productieproces gebaseerd op de directe polymerisatie van melkzuur of het productieproces via dilactide. In figuur 16 staan de blokschema s van de twee routes voor de productie van polymelkzuur, PLA. In elk schema staan de belangrijkste bewerkingen in blokken gegeven en de stofstromen zijn de pijlen tussen de blokken. Maak groepjes van 3 of 4 personen en kies een route Maak de vragen bij de route en bereid daarna een presentatie voor van maximaal 5 minuten waarin je de directie (de rest van de klas) uitlegt hoe de door jullie gekozen productie route werkt. Daarbij is het belangrijk te beseffen dat elke stap in een productieproces geld kost, je moet dus goed uitleggen waarom alle stappen aanwezig zijn. De antwoorden van de vragen bij de route moeten ook in je presentatie voorkomen. Het laatste gedeelte van de les worden de voor- en nadelen van de verschillende routes en grondstoffen besproken. Staat ergens in de module uitgelegd of verwijst naar het antwoord van een andere vraag..opzoeken op Internet of in chemiekaarten. Herhaling scheikunde kennis 42
43 Blokschema voor de productie van PLA (polymelkzuur). Figuur 16: Blokschema met twee productieprocessen voor de productie van PLA. In het blokschema staan de belangrijkste bewerkingen in de blokken aangegeven en de stofstromen zijn de pijlen tussen de blokken. 43
44 Route 6 Figuur 17: De productie van PLA via dilactide. Vragen bij route 6 Deze route is ontwikkeld door Cargill DOW LLC in 1995 als een oplosmiddelvrije productie route voor hoog molecuulgewicht PLA (dus lange ketens). De productie vindt sinds 2002 plaats bij NatureWorks LLC. De essentie van deze productieroute is dat in blok 6.2 laag molecuulgewicht PLA gevormd wordt. Dit PLA wordt in blok 6.4 afgebroken tot dilactides, welke weer als monomeer gebruikt worden voor de vorming van hoog molecuulgewicht PLA. De vloeibare PLA, die ontstaat in blok 6.6, kan direct in een spuitgietmachine of extruder tot het uiteindelijke product verwerkt worden. In blok 6.2 wordt laag molecuulgewicht PLA gevormd. 1. Geef de reactievergelijking in structuurformules van de reactie die plaatsvindt in blok Leg aan de hand van de reactievergelijking uit vraag 1 uit waarom in blok 6.1 zoveel mogelijk water uit het beginproduct, het ruwe melkzuur, wordt verwijderd. / Water en melkzuur vormen samen een azeotroop mengsel. 3. Zoek op wat een azeotroop mengsel is. Leg uit waarom het niet mogelijk is om in blok 6.1 het water volledig uit het ruwe melkzuur te verwijderen.. De stoffen uit blok 6.2 gaan naar blok 6.3 voor een azeotrope destillatie. 4. Welke stoffen zitten in het mengsel, dat van blok 6.2 naar blok 6.3 gaat? 5. Leg uit wat azeotrope destillatie is en wat de rol is van deze destillatie in dit blok is. In blok 6.4 wordt het laag molecuulgewicht PLA afgebroken tot dilactide. 6. Geef de reactievergelijking in structuurformules van de reactie in blok 6.4. Het in blok 6.4 ontstane mengsel wordt in blok 6.5 via gefractioneerde destillatie gescheiden. 7. Leg uit wat gefractioneerde destillatie is.. 8. Leg uit waarom bij gefractioneerde het dilactide in gasfase gebracht moet worden. 9. Zoek het kookpunt op van het dilactide. Bij welke druk wordt het kookpunt bereikt? Wat betekent dit voor de procesomstandigheden in blok 6.5? / 44
45 Het gebruik van oplosmiddelen wordt vermeden door de polymerisatie in blok 6.6 in gesmolten dilactide uit te voeren. 10. Zoek het smeltpunt op van dilactide. Is dit ook de reactietemperatuur in blok 6.6? Leg je antwoord uit. /. 11. Geef de reactievergelijking van de reactie, die in blok 6.6 verloopt. 12. Waarom kunnen nu wel lange PLA ketens gevormd worden? 13. Als katalysator 2 wordt vaak tinoctalaat gebruikt. Waar blijft deze katalysator na de reactie? 14. Geef bij de pijlen tussen de blokken aan welke stoffen in welke fase er worden vervoerd.. 45
46 Route 7 Figuur 18: De productie van PLA via directe polycondensatie Vragen bij route 7 In Japan is bij Mitsui Toastu Chemicals een route ontwikkeld voor de vorming van hoog molecuulgewicht PLA. In een enkele reactie, er wordt dus niet eerst laag molecuulgewicht PLA geproduceerd. Dit is een batch proces. In blok 7.2 wordt het hoog molecuulgewicht PLA gevormd. De polymerisatie reactie verloopt in het oplosmiddel difenylether. 1. Geef de reactievergelijking in structuurformules van de evenwichtsreactie die plaatsvindt in blok Hoe wordt de hydrolyse van de gevormde PLA voorkomen?, 3. Waarom wordt zoveel mogelijk water aan het ruwe melkzuur ontrokken?, 4. De droger is een grote pijp gevuld met een moleculaire zeef, waardoor het melkzuur/water mengsel gepompt wordt. Leg uit, hoe de moleculaire zeef het water verwijderd. 5. Welke drie stofeigenschappen maken difenylether tot een goed oplosmiddel voor de polymerisatie? / / De polymerisatie reactie in blok 7.2 verloopt vrij langzaam. De reactietijd is soms meer dan 24 uur. De reactie wordt nog versneld door een katalysator toe te voegen, waarvoor tin poeder of tinoctalaat gebruikt wordt. Temperatuur verhogen zou de reactie nog verder kunnen versnellen, maar bij temperatuurverhoging wordt de hydrolyse reactie meer versneld dan de polymerisatie reactie. 6. Geef twee redenen waarom toch gekozen wordt voor een vrije hoge reactietemperatuur van 150 C. / In blok 7.3 wordt het reactiemengsel uit blok 7.2 geëxtraheerd met chloroform. 7. Welk stof zal zeker in het residu van blok 7.3 aanwezig zijn?. In blok 7.4 wordt de oplossing van PLA in chloroform gemengd met een veel groter volume ethanol waardoor het PLA kristalliseert. 8. Verklaar het verschil in oplosbaarheid van PLA in ethanol en chloroform. Gebruik voor de verklaring Binas tabel 55., 9. Leg uit waarom de PLA uit blok 7.2 eerst in blok 7.3 wordt geëxtraheerd in chloroform voordat men het kristalliseert m.b.v. ethanol.. Het patent waarop dit blokschema gebaseerd is, zegt niets over het recyclen van de gebruikte oplosmiddelen. 46
47 10. Uit welke stoffen bestaat het filtraat van blok 7.5? 11. Zoek de kookpunten op van difenylether, chloroform en ethanol. 12. Geef in het blokschema met pijlen aan hoe de gebruikte oplosmiddelen hergebruikt kunnen worden in het productieproces. Geef ook duidelijk aan welke extra processtappen daarvoor nodig zijn. 13. Geef bij alle pijlen tussen de blokken aan welke stoffen in welke fase er worden vervoerd. Opdracht plastic zakken voor India In India is het gebruik van op aardolie gebaseerde plastic zakken verboden. Biologische afbreekbare, uit biomassa geproduceerde zakken, zijn wel toegestaan. Vraag aan je docent het werkblad Plastic zakken voor India Combineer de routes uit de opdrachten uit paragrafen 4.3 en 4.4 zodanig dat op een zo groen mogelijk manier PLA wordt geproduceerd. Gebruik daarbij een non-food grondstof en kies voor een snel afbreekbare PLA. Geef het complete blokschema, maak een lijst van alle gebruikte chemicaliën en toets het proces aan de principes opgesteld voor de groene chemie. (zie werkblad) Meer informatie over groene chemie vind je op: 47
48 4.5 Oefenopgaven Opgave 1: De productie van calciumlactaat Calciumlactaat wordt in de cosmetische industrie gebruikt als ph-regulator. Voor een huidcrème fabriek in Ommen is jaarlijks 600 ton zuiver calciumlactaat nodig. Literatuur onderzoek laat zien dat de melkzuurbacterie Lactobacillus delbrueckii melasse in redelijke grote snelheid en met hoge opbrengst kan omzetten in D-melkzuur dat vervolgens weer in calciumlactaat kan worden omgezet. Melasse is een bijproduct van de productie van kristalsuiker en door de aanwezigheid van een grote suikerfabriek in Groningen ruim beschikbaar. Melasse bestaat ongeveer voor 50% uit sacharose dat in water gemakkelijk hydrolyseert tot twee moleculen glucose. De glucose wordt vervolgens door Lactobacillus delbrueckii omgezet in melkzuur. 1. Laat m.b.v. reactievergelijkingen zien dat per molecuul sacharose vier moleculen melkzuur gevormd worden. 2. Hoeveel gram melkzuur wordt er per gram glucose gevormd? In de praktijk wordt glucose met een efficiëntie van 92% (gram melkzuur per gram glucose) omgezet in melkzuur. Dit melkzuur wordt daarna omgezet in calciumlactaat. 3. Bereken hoeveel ton melasse nodig is voor de jaarproductie van 600 ton calciumlactaat. Neem aan dat in het productieproces melkzuur volledig wordt omgezet in calciumlactaat. Besloten is om met behulp van een fed-batch reactor het melkzuur te produceren. De benodigde grootte van de fermentor hangt af van de groeisnelheid van Lactobacillus delbrueckii, de tijdsduur van de stationaire fase en de snelheid waarmee Lactobacillus delbrueckii glucose omzet. Laboratorium experimenten lieten zien dat de groeisnelheid en productie optimaal zijn bij een temperatuur van 42 C en ph = 6,0. Hieronder is de gemeten groeicurve van bij 42 C en ph = 6.0 weergegeven. Figuur 19 De groeicurve van Lactobacillus delbrueckii bij ph = 6,0 en T= 42 C 4. Hoeveel uur duurt het voordat de stationaire fase is bereikt? Tabel 1 (zie route -1) Laat zien dat de opbrengst in een fed-batch proces voor Lactobacillus delbrueckii met melasse als substraat 90,0 g L -1 is en dat de productie snelheid tijdens de stationaire fase 3,8 g L -1 h -1 48
49 5. Neem aan dat de melkzuurproductie tijdens de groeifase te verwaarlozen is. Bereken uit bovenstaande gegevens de tijdsduur van de stationaire fase bij ph = 6,0 en T = 42 C. Het schoonmaken van de fed-batch reactor en opnieuw vullen met medium voor een nieuwe cyclus kost 6 uur. 6. Hoeveel cycli kan je maximaal per jaar doorlopen in één batchreactor? 7. Bereken het minimale volume wat de fed-batchreactor moet hebben om een productie van 600 ton calciumlactaat per jaar te halen. De ph in het reactiemengsel mag niet onder de ph = 6,0 komen omdat anders de bacteriën minder melkzuur gaan produceren. 8. Laat m.b.v. van een berekening zien dat de ph van een melkzuur oplossing van 90,0 gram per liter inderdaad lager is dan ph = 6,0. Gebruik hiervoor het gegeven dat de pkz van melkzuur 3,95 is. Tijdens de stationaire fase wordt calciumcarbonaat toegevoegd om de ph constant te houden. Melkzuur wordt hierbij omgezet in calciumlactaat wat bij ph 6,0 goed oplosbaar is. Door het ontwijken van CO 2 is de reactie aflopend. 9. Geef de reactievergelijking voor de reactie tussen melkzuur en calciumcarbonaat 10. Bereken hoeveel ton kalk je voor ph- regulatie nodig hebt om 600 ton calciumlactaat te produceren. De productie van melkzuur wordt gestopt door het verhogen van de zuurgraad tot ph = 10 m.b.v. calciumcarbonaat gevolgd door verhitten. De hoge ph doodt de bacteriën, en de calciumionen laten de eiwitten en cellen samenklonteren zodat ze sneller neerslaan. Verhitten zorgt ook voor het neerslaan van een eventuele overmaat aan calciumcarbonaat. Na verhitten wordt het fermentatiemengsel gefilterd. 11. Bereken hoeveel kg kalk moet worden toegevoegd om in een reactor met een inhoud van 25 m 3 de ph van 6,0 naar ph = 10,00 te brengen. Neem hierbij aan dat elk toegevoegd carbonaation anderhalf hydroxide-ion oplevert. 12. Bereken hoeveel kg kalk nodig is om voor de jaarproductie van 600 ton calciumlactaat in de fed-batchreactor de ph van 6,0 naar 10,00 te brengen. Neem hierbij weer aan dat elk toegevoegd carbonaation anderhalf hydroxide-ion oplevert. Om zuiver calciumlactaat te produceren wordt eerst het filtraat ingedampt. Daarbij kristalliseert het calciumlactaat uit. Om de zuiverheid te vergroten wordt daarna een herkristallisatie van het calciumlactaat uitgevoerd. Daartoe wordt het calciumlactaat met 98 % zwavelzuur weer omgezet in melkzuur. De bij de reactie gevormde sulfaationen slaan met de calciumionen neer als calciumsulfaat. Kleur en geur stoffen worden verwijderd met behulp van actieve kool. Daarna worden door middel van filtratie de actieve kool en het calciumsulfaat verwijderd. Vervolgens wordt met zuiver calciumcarbonaat het melkzuur weer omgezet in calciumlactaat en dit kristalliseert bij ph> 7 uit tot Ca(C 3 H 5 O 3 ) 2 (s). De efficiëntie van deze kristallisatiestap is 96% 49
50 13. Hoeveel liter 98% zwavelzuur is er nodig om 600 ton calciumlactaat te produceren? Gebruik Binas tabel 43A De totale efficiëntie van de productie van het lactaat kan berekend worden door de totale massa van de gebruikte grondstoffen per kg geproduceerd zuiver calciumlactaat te berekenen. 14. Bereken hoeveel kg grondstoffen nodig is voor de productie van 1,0 kg calciumlactaat. Neem als grondstoffen calciumcarbonaat, glucose en zwavelzuur. 15. Bereken de efficiëntie van het proces. 16. Zwavelzuur (98 %) kost ongeveer 90 euro per ton, melasse 20 eurocent per kg, calciumcarbonaat (87,5 massa %) 35 euro per ton, en zuiver calciumcarbonaat (98%) 270 euro per ton. Bereken de grondstofprijs per kg geproduceerd calciumlactaat. Neem aan dat de 87,5 % calciumcarbonaat gebruikt wordt in de fed-batch reactor en de 98% calciumcarbonaat voor de herkristallisatie. Opgave 2: Polymelkzuur Van melkzuur (2-hydroxypropaanzuur) bestaan twee stereo-isomeren, die respectievelijk D- en L-melkzuur worden genoemd. L-melkzuur speelt een rol in de stofwisseling in het menselijk lichaam. Hieronder is weergegeven hoe de bindingen rondom een asymmetrisch koolstofatoom zijn georiënteerd: In deze structuur liggen de bindingen die zijn getekend met in het vlak van tekening; de binding die is getekend met komt uit het vlak van tekening naar voren en de binding die is getekend met ligt achter het vlak van tekening. Op de uitwerkbijlage bij deze opgave is deze ruimtelijke structuur nog tweemaal opgenomen. 1. Teken op de uitwerkbijlage onderaan deze opgave de ruimtelijke structuurformules van beide stereo-isomeren van melkzuur, door het tekenen van een waterstofatoom, een methylgroep, een alcoholgroep en een carbonzuurgroep aan de bindingen in elk van de gegeven structuren. Noteer hierin het waterstofatoom als H, de methylgroep als CH 3, de alcoholgroep als OH en de carbonzuurgroep als COOH. Het polymeer van melkzuur, het zogenoemde polymelkzuur, wordt onder meer gebruikt als chirurgisch hechtdraad. Hieronder is een uiteinde van een polymelkzuurmolecuul weergegeven: 50
51 In het lichaam wordt polymelkzuur, bijvoorbeeld na gebruik als hechtdraad, geleidelijk door hydrolyse afgebroken tot melkzuur. 2. Geef de reactievergelijking van de hydrolyse van het hierboven weergegeven fragment waarbij uit dit fragment onder andere twee melkzuurmoleculen ontstaan. Noteer hierin de organische stoffen in structuurformules. Polymelkzuur wordt vaak gemaakt uit het zogenoemde dilactide: Het dilactidemolecuul is op te vatten als een koppelingsproduct (verestering), dat is ontstaan uit twee melkzuurmoleculen. 3. Het dilactide kan ontstaan omdat bij verestering van twee melkzuurmoleculen de vrije hydroxyl-groep en carboxyl-groep gemakkelijk met elkaar kunnen reageren. Laat m.b.v. een tekening met structuurformules zien dat dit inderdaad het geval is. 4. Leg uit dat van het dilactide 3 stereo-isomeren voorkomen. Maak bij je uitleg gebruik van het feit dat een dilactide molecuul uit twee moleculen L-melkzuur, D-melkzuur of uit een mengsel van D en L-melkzuur moleculen gevormd kan worden. 5. Als grondstof voor kristallijn PLA met een hoog smeltpunt, wordt D- melkzuur gebruikt. Welke ruwe grondstoffen kunnen hiervoor gebruikt worden? Combineer hiervoor de gegevens uit de tabellen 1 en 2 van Route -1 uit paragraaf Een nadeel van kristallijn PLA is dat het veel slechter biologisch afbreekbaar is dan amorf PLA. Amorf PLA wordt gemaakt uit een mengsel van D en L-melkzuur. Welke ruwe grondstoffen kunnen nu gebruikt worden? Uit een dilactide kunnen behalve polymeren van melkzuur ook zogenoemde oligomeren van melkzuur worden gevormd. Oligomeren van melkzuur zijn opgebouwd uit veel minder melkzuureenheden dan polymeren. Oligomeren van melkzuur kunnen worden gemaakt via reactie 1: reactie 1 Stof A en het dilactide worden, samen met een katalysator, verwarmd tot 130 C. In het vloeibare mengsel treedt dan de vorming van oligomeren op. Het aantal melkzuureenheden 51
52 per oligomeermolecuul wordt de polymerisatiegraad genoemd. Bij reactie 1 ontstaat een mengsel van oligomeren. De gemiddelde polymerisatiegraad van de oligomeren in dit mengsel wordt bepaald door de gekozen molverhouding tussen stof A en het dilactide. 7. Bereken hoeveel mmol stof A nodig is om 69 mmol (10 g) dilactide volledig om te zetten tot oligomeren met een gemiddeld aantal van 10 melkzuureenheden per oligomeermolecuul. Ga ervan uit dat ook stof A volledig reageert en dat geen andere reactie optreedt dan reactie 1. Na de synthese van oligomeren van melkzuur uit stof A en het dilactide is het mengsel van de ontstane oligomeren onderzocht met behulp van een bepaalde methode van massaspectrometrie. Hierbij vallen de moleculen niet uiteen in brokstukken. Ze blijven intact, maar worden voorzien van een positieve lading door ze te behandelen met een oplossing waarin H + ionen, NH 4 + ionen en Na + ionen voorkomen. Zo n positief geladen oligomeerion ontstaat doordat een ongeladen oligomeermolecuul een H + ion of een NH 4 + ion of een Na + ion bindt. In het massaspectrum dat zo wordt verkregen, is een regelmatig patroon te zien van steeds groepjes van drie pieken. Dit is duidelijk te zien in figuur 14 waarin een deel is weergegeven van het massaspectrum van een mengsel van oligomeren. De eerste piek in elk groepje van drie is toe te kennen aan een oligomeermolecuul dat een H + ion heeft gebonden. De andere twee pieken zijn toe te kennen aan oligomeermoleculen die een NH + 4 ion respectievelijk een Na + ion hebben gebonden. Figuur 20: massaspectrum oligomeren Uit het massaspectrum blijkt dat bij de synthese zowel oligomeren zijn ontstaan met een even als met een oneven aantal melkzuureenheden per oligomeermolecuul. 8. Bereken de polymerisatiegraad van de oligomeer waaraan de piek bij m/z = 575 moet worden toegekend. 9. Leg uit dat uit figuur 14 de conclusie over het even en oneven aantal melkzuureenheden per oligomeermolecuul kan worden getrokken. De onderzoeker die deze synthese uitvoerde, verbaasde zich over het feit dat ook oligomeren met oneven aantallen melkzuureenheden waren ontstaan. 10. Stel een hypothese op waarmee het ontstaan van oligomeren met oneven aantallen melkzuureenheden kan worden verklaard. 52
53 Uitwerkbijlage Wat je nu moet weten Toepassingen melkzuur o Levensmiddelen industrie o Cosmetische industrie o Farmaceutische/ medische industrie o Grondstof voor de productie van o.a. polymelkzuur o Chemische industrie Productie van melkzuur o Chemisch o Melkzuurbacteriën De groeicurve heeft 4 fasen Fed-batch proces Zuivering melkzuur o Filtratie o Extractie o Tegenstroom wassen o Reactieve extractie o Indampen o Destillatie o Elektrodialyse Productie polymelkzuur (PLA) o Twee productieprocessen o Azeotrope destillatie o Gefractioneerde destillatie 53
54 Hoofdstuk 5 Moderne biotechnologie: de productie van 1,3-propaandiol 1,3-Propaandiol Eigenschappen 1,3-Propaandiol is een halfproduct met molecuulformule C 3 H 8 O 2. Bij kamertemperatuur is de stof vloeibaar: dit betekent dus ook dat 1,3-propaandiol verkocht wordt als vloeistof. De stof behoort met twee hydroxylgroepen tot de alcoholen. Tabel 1. Eigenschappen van 1,3-propaandiol Molecuulformule C 3 H 8 O 2 Molaire massa 76,09 g/mol Dichtheid 1,0597 g/cm³ Smeltpunt -28 C Kookpunt 211 C Structuurformule HO OH Toepassingen 1,3-Propaandiol kent verschillende toepassingen. De monomeer 1,3-propaandiol wordt onder andere gebruikt als koelvloeistof en als antivriesmiddel in bijvoorbeeld ruitensproeiervloeistof, daarnaast wordt de stof verwerkt in make-up en deodorants. Figuur 1: Materialen waarin 1,3-propaandiol verwerkt is. Zuiver 1,3-propaandiol wordt met name gebruikt voor de productie van polymeren. Deze polymeren zijn copolymeren, dat wil zeggen dat ze door condensatiepolymerisatie ontstaan uit 1,3-propaandiol en nog een andere monomeer. 54
55 De andere monomeer kan bijvoorbeeld tereftaalzuur zijn. Deze polymeren worden onder andere gebruikt in tapijten, onderdelen voor auto s en vliegtuigen, coatings, lijm en verf. Figuur 2: Toepassingen van 1,3-propaandiol. 5.1 Synthese van 1,3-propaandiol 1,3-Propaandiol kan via een chemische synthese gemaakt worden uit aardolie, maar kan ook met behulp van micro-organismen via een biosynthetische route gemaakt worden. Vanwege economische redenen wordt 1,3-propaandiol tegenwoordig alleen nog maar biosynthetisch geproduceerd. Dit is echter niet altijd zo geweest. Shell was tot voor kort de grootste producent van 1,3- propaandiol uit aardolie en is pas in het begin van de 21 e eeuw gestopt met de productie. Tegenwoordig wordt de bulk van de 1,3-propaandiol via biosynthese geproduceerd door DuPont, een Amerikaans chemiebedrijf, dat onder andere verschillende textielsoorten produceert. DuPont heeft ook een vestiging in Nederland. In de loop van de tijd is het steeds voordeliger geworden 1,3-propaandiol op biosynthetische wijze te gaan produceren. Dit komt onder andere doordat de olieprijs enorm is gestegen: voor de chemische synthese zijn de grondstoffen voor het maken van 1,3-propaandiol dus relatief duur geworden. De prijzen voor het biosynthetisch produceren zijn ongeveer gelijk gebleven. Net als voor melkzuur (zie hoofdstuk 4, tabel 1), zijn er in de afgelopen jaren zelfs nieuwe grondstoffen beschikbaar gekomen. Met verschillende bewerkingen kan men van allerlei soorten bioafval een waardevolle grondstof voor de productie van 1,3-propaandiol maken. 55
56 Figuur 3: voorbeelden van bioafval: wei, papier en hout. Naast het feit dat chemisch gesynthetiseerd 1,3-propaandiol relatief duur geworden is om te produceren, is het zo dat er voor de biosynthese een stuk minder extreme reactiecondities nodig zijn. Waar men bij de chemische synthese werkt met hoge druk en temperatuur, gebruikt men bij de biosynthese micro-organismen die dezelfde reactie kunnen uitvoeren bij kamertemperatuur en standaarddruk. Vraag 1. Leg uit waarom werken bij hoge temperatuur en druk relatief kostbaar is. Een ander voordeel van het biosynthetisch produceren van 1,3-propaandiol is dat men niet afhankelijk is van olie. Met de oprakende olievoorraden is het aan te raden naar productieprocessen te zoeken, waarbij geen gebruik wordt gemaakt van olie. Bovendien is de koolstofkringloop op deze manier in balans. Vraag 2. Waarom is de koolstofkringloop in balans bij de productie van 1,3-propaandiol via biosynthese? Licht je antwoord duidelijk toe. Chemische synthese van 1,3-propaandiol 1,3-Propaandiol werd chemisch geproduceerd (door Shell) uit acroleïne en uit etheen, zie voor de reactieschema s figuur 4. Acroleïne is een halfproduct dat in de industrie grootschalig wordt gebruikt voor het produceren van allerlei bulkchemicaliën, zoals het aminozuur methionine. Daarnaast kennen we acroleïne als een schadelijke stof, die onder andere in sigarettenrook voorkomt. Etheen is een restproduct van het kraken van olie, het is uitgaande van aardolie de meest geproduceerde chemische stof ter wereld! De reactieomstandigheden waaronder 1,3-propaandiol uit etheen of acroleïne gevormd kan worden, zijn zeer extreem. Dit betekent dat je de mogelijkheid moet hebben zeer hoge temperatuur of druk te kunnen bereiken, zonder dat dit schadelijk is voor de omgeving. Een hoge druk betekend dat alle reactoren leidingen en afsluiters dikken wanden moeten hebben, de besturing vanuit een bunker moet plaatsvinden en dat de fabriek ver van de bebouwde kom moet staan. Hoge temperaturen kosten veel energie. Daarom werd 1,3-Propaandiol dan ook aanvankelijk geproduceerd in fabrieken waar al zware chemische industrie plaatsvond. 56
57 O H acroleine O2 etheen H2O O... O etheenoxide HO H 3-hydroxypropanal H2 O HO H 3-hydroxypropanal HO OH 1,3-propaandiol H2 HO OH 1,3-propaandiol A B Figuur 4: Reactieschema van (A) acroleïne naar 1,3-propaandiol en van (B) etheen naar 1,3- propaandiol. Vragen 3. Geef de systematische naam voor acroleïne. 4. Geef de reactievergelijking in molecuulformules voor de vorming van 3- hydroxypropanal uit acroleïne. 5. Geef de reactievergelijking in molecuulformules voor de vorming van 1,3-propaandiol uit 3-hydroxypropanal. 6. Geef de totaalreactie van de reacties uit vraag 4) en 5) in molecuulformules. 7. Geef in structuurformules de reactievergelijking voor de omzetting van etheen in etheenoxide. 8. Leg met behulp van een reactievergelijking in structuurformules uit met welke stof etheenoxide reageert bij de vorming van 3-hydroxypropanal. Opdracht 1 a) Bestudeer de onderstaande tekst over de biosynthese van 1,3-propaandiol en geef de juiste stofnamen voor de lege vakjes op de kaart met biosynthetische routes van figuur 7. b) Geef de structuurformules bij de stofnamen en geef de reactievergelijkingen in structuurformules van alle reacties voor de vorming van 1,3-propaandiol uit DHAP. 57
58 Biosynthese van 1,3-propaandiol De productie van 1,3-propaandiol door micro-organismen werd voor het eerst beschreven in Verschillende micro-organismen werden ontdekt, zoals Clostridium, Enterobacterium en andere soorten. Deze organismen maken 1,3-propaandiol uit glycerol (1,2,3-propaantriol). In de evolutie hebben deze organismen zich zo ontwikkeld, dat ze van nature kunnen leven op glycerol. Ze gebruiken glycerol als bouwsteen voor de opbouw van hun eigen cel, voor onderhoud en voor het produceren van andere stoffen. Omdat de grondstoffen voor de chemische synthese van 1,3-propaandiol, acroleïne en etheen, in de loop der tijd erg duur zijn geworden, is er daarom gezocht naar een organisme dat 1,3-propaandiol kan maken uit goedkope en gemakkelijk verkrijgbare stoffen. In eerste instantie beschikte men natuurlijk over de micro-organismen die van nature al 1,3- propaandiol produceren: Clostridium en Enterobacterium. Deze organismen hebben voor de productie van 1,3-propaandiol twee omzettingstappen nodig: van glycerol naar 3- hydroxypropanal (3HPA) en van 3-hydroxypropanal naar 1,3-propaandiol. In de cel is voor iedere omzetting minstens één enzym nodig. Voor de eerste omzetting maakt de cel gebruik van het enzym glycerol dehydratase, dat een watermolecuul aan glycerol onttrekt. Hierbij ontstaat 3-hydroxypropanal. De volgende omzetting wordt gekatalyseerd door het enzym 1,3-propaandiol oxidoreductase en zorgt ervoor dat 3-hydroxypropanal, in aanwezigheid van NADH, omgezet wordt in 1,3-propaandiol. Clostridium en Enterobacterium gebruiken echter glycerol als voedingsbron, ze kunnen dus niet groeien op goedkoop verkrijgbare stoffen als glucose. Men ging op zoek naar een organisme dat uit glucose 1,3-propaandiol kan produceren en dat glucose tevens kan gebruiken voor zijn cellulaire processen. Deze micro-organismen waren er echter niet. Daarom heeft men uiteindelijk de bacterie Escherichia coli (E.coli) genetisch zo gemodificeerd dat de nieuwe stam 1,3-propaandiol uit glucose kan maken. In het DNA van E.Coli moet dus een aantal veranderingen worden aangebracht, zodat de bacterie met behulp van de biosynthetische routes die het van oorsprong al gebruikt, nieuwe producten kan maken. In dit geval is dat nieuwe product 1,3- propaandiol. E. coli maakt gebruik van de glycolyse om glucose af te breken en zo zijn cel te voorzien van energie en van de benodigde stoffen voor de cellulaire processen. We willen de bacterie nu zo aanpassen, dat deze naast de voor de levenscyclus benodigde stoffen zoveel mogelijk 1,3-propaandiol uit glucose gaat maken. Uitgangspunt bij genetische modificaties is dat het niet te complex moet worden. Je zoekt dus naar een stof waarvan de structuur verwant is aan de te Figuur 5: Escherichia coli produceren stof. We weten al dat bacteriën 1,3- propaandiol uit glycerol maken. We moeten dus nu op zoek naar een stof uit een al bestaande biosynthetische route in E.coli, die veel op glycerol lijkt. Dit is dihydroxyacetonfosfaat (DHAP)uit de glycolyse zoals in de volgende pagina beschreven staat. 58
59 Figuur 9 uit hoofdstuk 3: De 10 stappen van de glycolyse. Bij de moleculen is alleen het aantal C-atomen (zwarte bolletjes) en de posities van de fosfaatgroepen (gele P) weergegeven. Figuur 6: DHAP Als de fosfaatgroep van dihydroxyacetonfosfaat wordt verwijderd en de dubbelgebonden O aan het tweede koolstofatoom wordt vervangen door een hydroxylgroep ontstaat er glycerol. In de praktijk gebeurt dit door een tweetal omzettingen: 1. In de eerste stap wordt dihydroxyacetonfosfaat omgezet in glyceraldehyde. 2. In de tweede stap wordt uit glyceraldehyde glycerol gevormd. Voor deze omzettingen moeten er ook weer een aantal enzymen aanwezig zijn, die de reactie kunnen katalyseren. Dit is dus de totale biosynthetische route om van glucose 1,3-propaandiol te maken. Om deze afbraakroute daadwerkelijk te laten verlopen, moet er voor gezorgd worden dat alle enzymen die daar voor nodig zijn ook in de cel aanwezig zijn. Hiertoe moet het DNA van de bacterie worden aangepast. In figuur 7 staat de overzichtskaart met biosynthetische routes met daarin getekend de route naar 1,3-propaandiol. 59
60 Figuur 7: Biosynthetische routes in de cel met de route van glucose naar 1,3-propandiol. 60
61 5.2 Opbrengst van de 1,3-propaandiol productie verhogen Het is natuurlijk de bedoeling dat de nieuwe E. coli-stam zoveel mogelijk 1,3-propaandiol uit zo weinig mogelijk glucose maakt, de aanschafkosten van de grondstof (suiker) moeten zo laag mogelijk blijven. Om de 1,3-propaandiol productie zo optimaal mogelijk te maken, moeten we weer inzoomen op de metabole routes van de E.coli (zie figuur 7). Zoals we in hoofdstuk 3 (figuur 9) al besproken hebben kan de cel glucose (een molecuul met 6 C-atomen) tijdens de glycolyse omzetten in dihydroxy-acetonfosfaat (DHAP, 3 C-atomen) en glyceraldehyde-3-fosfaat (GAD-3P, 3 C-atomen). Voor de cel is het mogelijk om GAD-3P om te zetten in DHAP en andersom. Dit zou betekenen dat ieder koolstofatoom uit glucose via DHAP in 1,3-propaandiol terecht zou kunnen komen. Er zit echter een addertje onder het gras. Figuur 8: GAD-3P kan omgezet worden in DHAP Om de glucose te kunnen verwerken, moet deze in de cel aanwezig zijn. E.coli gebruikt het Fosfo-Transferase Systeem (PTS) om glucose via actief transport in de cel te krijgen. Voor dit transport gebruikt de cel de ATP die gevormd wordt tijdens de glycolyse bij de omzetting van fosfo-enolpyruvaat (PEP) naar pyruvaat (zie figuur 9). De ATP wordt dan gebruikt om glucose naar glucose-6-fosfaat om te zetten en tegelijkertijd over het celmembraan heen te transporteren. GLYCOLYSE 1,3-propaandiol Glucose 2 Pyruvaat ATP 2 ATP ADP 2ADP Glucose-6-fosfaat P 2 P Fosfoenolpyruvaat 2H 2 O Fructose-6-fosfaat P 2 P 2-Fosfoglyceraat ATP ADP Fructose- 1,6-difosfaat P P 2 P 3-Fosfoglyceraat 2NAD + 2 NADH + 2H + 2 2ADP ATP P P 2 P P Dihydroxyacetonfosfaat Glyceraldehyde- 3-fosfaat 2 Pi 1,3-Difosfoglyceraat Figuur 9: de vorming van dihydroxyacetonfosfaat in de glycolyse Het is dus noodzakelijk dat de gewone glycolyse blijft doorgaan om nieuwe glucose in de cel te krijgen. Dat betekent dat niet alle GAD-3P omgezet kan worden in DHAP (en dus in 1,3- propaandiol), maar dat de GAD-3P gebruikt moet worden om fosfo-enolpyruvaat van te maken. Je 61
62 kunt dus per molecuul glucose niet 2 moleculen 1,3-propaandiol maken, maar slechts één! De opbrengst van deze reactie is dus hoogstens 50% (mol/mol). Om de opbrengst van 1,3-propaandiol te verhogen, is in de gemodificeerde E.coli stam het gehele PTS uit het organisme verwijderd. Men heeft alle genen die bij de productie van de verschillende eiwitten van het PTS horen, opgespoord. Daarna heeft men deze genen verwijderd en vervangen door een systeem dat glucose de cel in brengt, zonder dat dit energie kost. Dit systeem is van origine niet aanwezig, omdat de bacterie niet gewend is onder glucoserijke omstandigheden te leven. De normale leefomgeving van de bacterie is een veel gevarieerdere omgeving, waar veel meer voedselbronnen aanwezig zijn dan alleen glucose. In plaats van ATP te gebruiken uit de omzetting van fosfo-enolpyruvaat naar pyruvaat om nieuwe glucose in de cel te krijgen, kan glucose nu "kostenloos" de cel in worden getranspor-teerd. Dit leidt tot de volgende situatie: A Glucose B Glucose Fosfoenolpyruvaat 3 Pyruvaat Glucose 1 GAD-3P 2 Glucose-6-fosfaat Cytoplasma 4 Glucose-6-fosfaat Cytoplasma Figuur 10: (A) Fosfo-Transferase Systeem. (B) Nieuw (gemodificeerd) glucose transport systeem, waarbij glucose passief de cel in getransporteerd wordt. Vragen 9. Bestudeer figuur 10A en 10B. Welke stoffen horen bij de pijlen 1, 2, 3 en 4 te staan? (zie ook figuur 10) 10. Hoeveel mol GAD-3P wordt omgezet in 1,3-propaandiol per mol binnengebracht glucose? (zie figuur 9) Afsluiting We hebben er nu voor gezorgd dat glucose de cel in kan, onafhankelijk van de glycolyse. Om ervoor te zorgen dat de bacterie nog efficiënter 1,3-propaandiol produceert, moet er nog een laatste modificatie worden gedaan. We hebben een nieuw gen in de bacterie gezet, om ervoor te zorgen dat er glycerol wordt gemaakt, maar E.coli heeft in een normale situatie niet te maken met zoveel glycerol in zijn cel. De bacterie zou dit als ongewenst beschouwen en de glycerol dus gaan afbreken. Hiervoor heeft de bacterie een tweetal enzymen nodig, namelijk glycerol kinase en glycerol dehydrogenase. In de gemodificeerde stam zijn de genen voor deze twee enzymen verwijderd, zodat glycerol enkel met het nieuwe enzym glycerol dehydratase tot 1,3-propaandiol afgebroken kan worden. Er is nu met succes een E.coli-stam gemaakt die zoveel 1,3-propaandiol produceert, dat de bacterie voor een industrieel proces kan worden gebruikt. 62
63 5.3 De productie van 1,3-propaandiol voor Sorona Keuze- en verdiepingsopdracht Figuur 11: Schematisch overzicht van het productieproces van Sorona Figuur 12: Fabriek van DuPont in Loudon, USA, waar de Sorona wordt geproduceerd. Opdracht: De productie van 1,3-propaandiol voor Sorona De directie van DuPont is in gesprek met Nederlandse investeerders over een nieuw te bouwen fabriek voor Sorona Tijdens de gesprekken blijken er nog vragen te zijn. Ook heeft de directie onderstaand blokschema ontvangen en wil weten welke stoffen bij de pijlen vervoerd worden. De directie is nu aan het lunchen met de investeerders en wil de antwoorden na de lunch hebben. Als team van bedrijfschemici moeten jullie voor de antwoorden zorgen. 63
64 Maak teams van 8 personen en vraag je aan de docent het werkblad De productie van 1,3- propaandiol voor Sorona. Wijs een voorzitter aan die ervoor zorgt dat het werk goed verdeeld wordt. Zorg ervoor dat je als team voor het einde van de les heldere antwoorden op alle vragen hebt en dat het blokschema compleet is. De antwoorden kan je bijna allemaal in hoofdstuk 5 vinden. Bespreek daarna de antwoorden met elkaar zodat een ieder van jullie de antwoorden kan toelichten.(aan de directie). Vragen van Directie Vraag 1 Metabolic engineering E.coli. Hoe gaat het inbrengen van genen precies te werk? Kan kort maar duidelijk uitgelegd worden wat de functies van plasmiden en promotoren zijn? Zie bron 1. Vraag 2 Is glucose de werkelijke grondstof? Welke grondstoffen zijn in Nederland beschikbaar? Vraag 3 De reactor is een aërobe (bio)reactor. Er is dus zuurstof nodig. Hoe wordt die in de reactor gebracht? Geef een schematische afbeelding van een aërobe (bio)reactor die geschikt zou zijn voor de productie van 1,3-propaandiol. Zie bron 2. Vraag 4 Waarom is het nodig te verhitten? De micro-organismen verdwijnen door filtratie toch al uit het product? Zie bron Vraag 5 Hoeveel kj per kg geproduceerd 1,3-propaandiol kost het verhitten, als in een batch 1,3-propaandiol een concentratie heeft van 135 g/l? Zie bron 4. Vraag 6 Wat zijn eigenlijk de afmetingen van de poriën bij microfiltratie, bij utrafiltratie en bij nanofiltratie? Waarom na elkaar in drie stappen Micro-,Ultra- en Nanofiltratie? Waarom niet in 1 stap? Zijn Micro-,Ultra- en Nanofiltratie geschikt om te gebruiken op industriele schaal en hoe dan? Zie bron 5. Vraag 7 Hoe werkt een industriële ionenwisselaar. En wat wordt er gescheiden? Waarom moet er een stof toegevoegd worden. Zie bron 6. Vraag 8 Waarom een dubbele destillatie? Waarom moet de 1,3- propaandiol een zuiverheid van 99,992 % hebben? Zie bron Vraag 9 Welke grondstof(fen) is/zijn, naast 1,3-propaandiol, nog meer nodig voor de productie van Sorona.? Hoeveel ton van die grondstof is nodig per ton geproduceerde Sorona? Zie bron 8. Figuur 13: blokschema voor de productie van Sorona 64
65 * Informatiebronnen bij de opdracht: De productie van 1,3-propaandiol voor Sorona Bron 1: Metabolic engineering van E.coli Om te zorgen dat het organisme uiteindelijk de enzymen gaat maken, die als katalysator dienen voor de reacties waarbij dihydroxyacetonfosfaat wordt omgezet in 1,3-propaandiol, moeten er nieuwe genen op het plasmide geplaatst worden. Plasmiden zijn kleine ringvormige stukken DNA, die bacteriën onderling kunnen uitwisselen. De plasmiden worden door biotechnologen gebruikt om de genetische informatie van een ander organisme op te slaan. De plasmide bevat dan een stukje DNA van een ander organisme. Hoe dat precies werkt is in onderstaande tekening te zien. * G A AT T C CTTAAG DNA wat in het plasmide moet worden ingebouwd * * * GAATTC CTTAAG A T CT G G T A TAA C * Plasmide CTTAAG G A AT T C G A AT T C CTTAAG DNA wordt geknipt bij de oranje pijlen * Plasmide met nieuw DNA Figuur 14: inbouw van vreemd DNA in een plasmide 65
66 Het cirkelvormig plasmide wordt uit de cel gehaald en daarna opengeknipt met speciale enzymen, zogenaamde restrictie enzymen. Deze restrictie enzymen knippen slechts in één bepaalde volgorde van nucleotiden. In figuur 14 knipt het restrictie enzym, EcoR1, altijd tussen G en A in de sequentie G*AATTC (zie de oranje pijlen). Als het in te brengen stukje DNA ook met dit restrictie enzym geknipt wordt, zullen de knipplaatsen van het plasmide en het in te brengen DNA precies aan elkaar passen. Na het knippen worden de opengeknipte plasmide en het in te brengen stukje DNA bij elkaar gebracht. Door toevoeging van DNA ligase wordt het DNA weer aan elkaar geplakt. Je krijgt dan een plasmide met daarin nieuwe genen. Dit genetisch gemodificeerde plasmide, het recombinant plasmide, kan weer door bacteriën worden opgenomen. Het ingebrachte nieuwe DNA wordt tot expressie gebracht in de bacterie. Het plasmide in Escherichia coli is op hierboven beschreven manier gemodificeerd. In tabel 2 staan de namen van de nieuwe genen die in het plasmide van Escherichia coli zijn geplaatst om de productie van 1,3-propaandiol mogelijk te maken. De nieuwe genen zullen via transcriptie (DNA RNA) en translatie (RNA eiwit) zorg dragen voor de productie van de eiwitten, die als enzymen de reacties katalyseren voor de vorming van 1,3-propaandiol. Ieder enzym heeft een eigen gen, dus er zal een aantal verschillende genen in het plasmide gezet moeten worden. Tabel 2: Genen die nodig zijn voor de productie van eiwitten voor de omzettingen van dihydroxyacetonfosfaat (DHAP) naar 1,3-propaandiol. Omzetting Naam enzym Naam bijbehorende gen DHAP glyceraldehyde Fosfaat dehydrogenase DAR1 Glyceraldehyde glycerol Glycerol-3-fosfaat fosfatase GPP2 Glycerol 3- Glycerol dehydratase dhab1-3 hydroxypropanal 3-hydroxypropanal 1,3-propaandiol Propaandiol oxidoreductase dhat Opdracht 2 Bekijk onderstaande videofragmenten video over de werking van een restrictie enzym plaatsen van vreemd DNA in E.coli In de animatie heb je gezien hoe een restrictie enzym over een DNA-streng glijdt en daarbij zoekt naar een bepaalde sequentie (= een specifieke volgorde van baseparen). Wanneer het enzym de specifieke volgorde heeft gevonden, zal hij het DNA hier knippen. Neem bijvoorbeeld het enzym EcoR1, dat knipt bij de sequentie G*AATTC (het sterretje geeft de plaats aan waar de knip komt). Stel, je gaat de volgende DNA-sequentie knippen met behulp van EcoR1. 66
67 5 GCATTGGAATTCGTCGAT 3 3 CGTAACCTTAAGCAGCTA 5 EcoR1 gaat nu op zoek naar de sequentie G*AATTC en knipt daar het DNA. Er ontstaat dus 5 GCATTGG 3 5 AATTCGTCGAT 3 3 CGTAACCTTAA GCAGCTA 5 Merk op dat als je van de 5 -kant van het DNA naar de 3 -kant glijdt, je zowel in de bovenste als in de onderste streng AATT tegenkomt. EcoR1 knipt zowel onder als boven: het DNA komt dus ook van elkaar los! (let op: het plasmide DNA is circulair, dus de uiteinden van dit DNA zitten eigenlijk aan elkaar!): Wanneer je zowel het plasmide-dna als je gen, dat je in de plasmide wilt opnemen, met hetzelfde restrictie-enzym knipt, krijg je twee uiteinden die je aan elkaar kunt plakken. We bekijken weer het voorbeeld van EcoR1: Een deel van het onderstaande gen, het gen van interesse, willen we in de plasmide plaatsen: 5' AAGCCGAATTCATTAGGCGCGAATTCCTACCGGTGACCGG 3' 3' TTCGGCTTAAGTAATCCGCGCTTAAGGATGGCCACTGGCC 5' Als we het gen knippen met EcoR1 (let op: er zitten twee GAATTC-sequenties in het gen, dus EcoR1 zal twee keer knippen!) krijgen we de onderstaande fragmenten: 5' AAGCCG 3' 5' AATTCATTAGGCGCG 3' 5' AATTCCTACCGGTGACCGG 3' 3' TTCGGCTTAA 5' 3' GTAATCCGCGCTTAA 5' 3' GGATGGCCACTGGCC 5' Wanneer je nu de opengeknipte plasmide en het gen van interesse bekijkt, zie je dat deze in elkaar passen: 5 GCATTGG 3 5' AATTCATTAGGCGCG 3' 5 AATTCGTCGAT 3 3 CGTAACCTTAA 5 3' GTAATCCGCGCTTAA 5' 3 GCAGCTA 5 Voor het aan elkaar zetten van de stukken DNA, hebben we ook weer een enzym nodig: DNA ligase. Dit enzym ligeert (plakt aan elkaar) de stukken DNA, tot één geheel. Wanneer je bovenstaande drie stukken DNA aan elkaar gaat plakken krijg je dus de volgende situatie: 5 GCATTGG AATTCATTAGGCGCG AATTCGTCGAT 5 3 CGTAACCTTAA GTAATCCGCGCTTAA GCAGCTA 3 5 GCATTGGAATTCATTAGGCGCGAATTCGTCGAT 5 3 CGTAACCTTAAGTAATCCGCGCTTAAGCAGCTA 3 We weten nu dus hoe je een stuk DNA in een plasmide moet plakken. Het is van essentieel belang dat je gen een sequentie bevat, dat door het restrictie-enzym geknipt kan worden. Er bestaan een groot aantal verschillende restrictie-enzymen, die allemaal verschillende sequenties knippen. Sommige restrictie-enzymen zoeken sequenties van 4 baseparen, sommige van 6 of zelfs 8 baseparen. 67
68 Om er zeker van te zijn, dat je nieuw ingebrachte genen ook daadwerkelijk in de cel afgelezen worden, moet je ook dit proces regelen. In de cel worden genen pas verwerkt tot eiwitten op het moment dat ze afgelezen worden. Dit is afhankelijk van een zogenaamde promotor, een DNAsequentie die zegt dat het DNA vanaf een bepaalde plaats (het begin van het gen dus) afgelezen moet worden. Zonder deze promotor-sequentie wordt je gen niet afgelezen. Het is dus essentieel dat je deze ook in de plasmide plakt! Alle genen uit tabel 2 worden dus in de plasmide geplakt. De plasmide is nu klaar om in de natuurlijke cel gebracht te worden. Wanneer het plasmide-dna gemengd is met het natuurlijke DNA, is E.coli in staat glucose om te zetten in 1,3-propaandiol. We hebben dus nu een micro-organisme gemaakt, dat in staat is suikers om te zetten in 1,3- propaandiol. Bron 2: Aerobe fed-batch reactor De productie van 1,3-propaandiol vindt plaats in een fed-batch reactor onder aerobe condities. Het meeste 1,3-propaandiol wordt geproduceerd tijdens de groeifase van de bacterie. E.coli is een snel groeiende bacterie, dus de productie vindt plaats in kortdurende batches (zie paragraaf 4.2). In het fermentatiemengsel zitten de volgende stoffen: 1,3-propaandiol water (de bacteriën worden gekweekt in een vloeibaar mengsel) biomassa (de bacteriën zelf) en de daarbij behorende eiwitten glycerol (niet alle glycerol wordt omgezet in 1,3-propaandiol, dus er blijft nog iets over) andere bijproducten (van alle tussenproducten, zoals 3-hydroxypropanal, geldt dat niet alles reageert, er blijft dus altijd wat over) allerhande soorten voeding voor de bacteriën We willen uiteindelijk alleen 1,3-propaandiol overhouden, dus het fermentatiemengsel moet, net als bij de melkzuurproductie, een aantal zuiveringsstappen doorlopen om 1,3-propaandiol zuiver te verkrijgen. 68
69 Bron 3: Wet en regelgeving gemodificeerde organismen Allereerst gaan we uit het fermentatiemedium de biomassa halen. In Nederland is er een wetgeving die stelt, dat als er met genetisch gemodificeerde organismen (GGO) gewerkt wordt, dat de biomassa afgedood moet worden voordat deze in de natuur terecht komt. 69
70 Bron 4: Afdoden micro-organismen door verhitten met een warmtewisselaar Biomassa mag dus niet in het milieu komen; de bacteriën moeten eerst afgedood worden door verhitting (met behulp van een warmtewisselaar). Het fermentatiemengsel wordt zo hoog verhit dat alle bacteriën afsterven. Daarna wordt het hele mengsel weer afgekoeld, om in vervolgstappen te kunnen zuiveren. Het voordeel van een warmtewisselaar is dat er zeer weinig energie verloren gaat. De warmtewisselaar is een lange buis, waarin het fermentatiemengsel rondgepompt wordt. Allereerst wordt het nog koude mengsel opgewarmd. De temperatuur van het mengsel in de buis stijgt, zodat de bacteriën het steeds moeilijker krijgen. Op een gegeven moment is de temperatuur zo hoog dat de bacteriën zullen sterven. Niet alle bacteriën sterven tegelijk, maar geleidelijk gaan ze allemaal dood. Het geheel wordt nog steeds rondgepompt, het fermentatiemengsel komt nu in een lang, geïsoleerd traject terecht, waar de temperatuur constant blijft. Hier wordt het mengsel de tijd gegund alle bacteriën af te doden. Aan het einde van deze geïsoleerde buis zijn 1 2 Koud Heet 1 = fermentatiemengsel 2 = Fermentatiemengsel (afgedood) Warmtewisselaar Loop met isolatie Figuur 15: Schematische voorstelling van een warmtewisselaar om de bacteriën af te doden. alle bacteriën dood en wordt het mengsel weer afgekoeld. Het is dus erg belangrijk dat de buis lang genoeg is om alle bacteriën te kunnen doden. De warmte die vrijkomt bij het afkoelen van het fermentatiemengsel kan weer worden gebruikt om een nieuwe lading fermentatiemengsel op te warmen. Dit hergebruik van warmte is het grote voordeel van een warmtewisselaar. Hierdoor hoeft slechts weinig energie toe gevoegd te worden en kunnen de kosten voor het afdoden van de biomassa laag blijven. In de industrie gebruikte warmtewisselaars verwarmen het fermentatiemengsel tot 95 graden Celsius, waarbij het mengsel zo'n 5 minuten verblijft, voordat het weer afgekoeld wordt. Tot wel 85% van de warmte wordt op deze manier hergebruikt. Bij het berekenen (schatten) van voor het afdoden benodigde energie wordt vaak aangenomen dat de warmtecapaciteit (soortelijke warmte) van het 1,3-propaandiolmengsel gelijk is aan die van water en dat de temperatuur van het fermentatiemengsel 25 C is. 70
71 Bron 5: Microfiltratie, ultrafiltratie, nanofiltratie Na het afdoden van de bacteriën in de warmtewisselaar doorloopt het fermentatiemengsel een aantal filtratiestappen. Achtereenvolgens wordt er een microfiltratie, ultrafiltratie en een nanofiltratie uitgevoerd. In onderstaand schema staan een aantal gegevens over deze filtratiemethoden. Figuur 16: filtratieschema Een logische vraag zou zijn: waarom wordt niet meteen een nanofiltratie membraan gebruikt, dan worden alle stoffen in één keer uit de oplossing verwijderd? Dit zou inderdaad kunnen, ware het niet dat de membranen de eigenschap hebben heel snel dicht te slibben. Als de membranen dichtgeslibd zijn, kan er niets meer door het membraan. Daarom is ervoor gekozen de filtratie in drie stappen te doen: micro-, ultra- en nanofiltratie. Filtratie Ook met gescheiden filtratiestappen slibben de membranen dicht, er stromen immers nog steeds dezelfde stoffen langs. Dit is niet te voorkomen. Men moet daarom de membranen regelmatig schoonmaken. Om dit geautomatiseerd te kunnen doen, heeft men een systeem bedacht van 6 verschillende zuiveringsinstallaties met membranen die om de beurt gebruikt en vervolgens schoongemaakt worden. Wanneer het membraan is dichtgeslibd, draait de hele installatie door en wordt een vers schoongemaakt membraan gebruikt. Je verkrijgt een onderstaande situatie, die constant ronddraait. 71
72 Figuur 17: Schematische voorstelling van een roterend filtratiesysteem. In iedere stap worden twee filtratieopstellingen tegelijk gebruikt. Zodra deze zijn dichtgeslibd draait het geheel door, worden de volgende twee filtratieopstellingen gebruikt. In de tussentijd worden de filtratiesystemen die niet gebruikt worden schoongemaakt. Figuur 18: Voorbeeld van een filtratiecaroussel zoals boven beschreven. Elke zak is een filtratiesysteem 72
73 + + Bron 6: Ionenwisselaar Na de nanofiltratie wordt het overgebleven fermentatiemengsel in een ionenwisselaar gebracht om de kleine, geladen deeltjes uit de oplossing halen. Dit zijn met name de zuren en basen die nog in de oplossing zitten, aminozuren en voedingsstoffen. Deze zijn nog niet met behulp van nanofiltratie uit de oplossing gehaald. Een ionenwisselaar, het woord zegt het al, bestaat uit een vaste stof waarop ionen kunnen wisselen. De werking van de ionenwisselaar is gebaseerd op het feit dat concentraties in een oplossing altijd overal gelijk willen zijn. Opgeloste stoffen proberen zich zoveel mogelijk in een oplossing te verdelen. Begin Eind Begin Eind + H + + H + H+ + H + H + H + H + H+ H + H + H + H+ H+ OH - H+ H + OH - OH - OH - H+ OH - OH - + OH - H + H+ H + H+ OH - OH - OH - OH - H + H + H+ OH - OH - OH - OH - OH - OH - OH - H + H + H+ H + H+ H + H+ H + OH - H+ OH - OH- OH H + OH - OH - H + H + H+ H + H + OH - OH - H + H + Kolom 1 (positieve ionen wisselaar) Kolom 2 (negatieve ionen wisselaar) Figuur 19: ionenwisselaar Stel je een ionenwisselaar voor als een buis met allemaal kleine bolletjes, waarlangs de oplossing geleid wordt. Als je inzoomt op deze bolletjes, zie je dat ze allemaal geladen zijn met ionen. Een bolletje heeft als het ware een schil van ionen, die gebonden zijn aan de oppervlakte van het bolletje. Vaak wordt als positief ion bijvoorbeeld het H + -ion gebruikt aan de oppervlakte van deze bolletjes. Wanneer de oplossing langs de bolletjes stroomt, zal er sprake zijn van een verstoorde evenwichtssituatie: de H + -ionen worden uitgewisseld met de positieve ionen in de oplossing. Zo komt het dat de bolletjes in de ionenwisselaar na gebruik niet omringd zijn door H + -ionen, maar door de positief geladen ionen die eerst in de oplossing zaten. Wanneer je maar genoeg bolletjes met positieve ionen gebruikt, houd je uiteindelijk een oplossing over waarbij alle positieve ionen zijn vervangen door H + -ionen. 73
74 Er zijn in de oplossing echter ook negatieve ionen te vinden. Deze worden eruit gehaald met behulp van dezelfde techniek, alleen zitten er nu andere bolletjes in de buis. We hebben nu een type bolletjes nodig waarbij negatief geladen ionen (meestal OH - ) aan de oppervlakte zijn gebonden. Deze kunnen dan uitgewisseld worden met de negatieve ionen die door de oplossing zweven. De negatieve ionenwisselaar heeft nog een extra voordeel. Behalve dat er met deze zuiveringsmethode negatieve ionen uit de oplossing gehaald kunnen worden, bezitten organische zuren ook een negatieve carboxylgroep. Deze worden ook aangetrokken door de bolletjes met OH - -ionen. Ook zuren worden dus door middel van ionenwisseling uit de oplossing gehaald. Op een gegeven moment zijn alle bindingplaatsen bezet door de verwijderde ionen en zal niet meer in staat zijn de ionen uit de oplossing te verwijderen. De kolom moet nu geregenereerd worden. Bij regeneratie vindt het omgekeerde proces plaatst. OH - en H + worden nu op de bolletjes gebracht. De truc daarbij is dat OH - en H + ionen in grote overmaat en hoge concentratie door de kolom worden geleid zodat de geadsorbeerde ionen worden verdrongen worden. Bron 7: Dubbele Destillatie De oplossing die we nu overhouden, bevat nog glycerol, propaandiol en water. Dit zijn bij kamertemperatuur alle drie vloeistoffen: ze lenen zich dus uitstekend voor een scheidingsmethode als destillatie. De kookpunten van de stoffen zijn hieronder weergegeven. Tabel 3. Kookpunten van de verschillende te destilleren stoffen. Stof Kookpunt ( C) 1,3-propaandiol 211 Glycerol 290 Water 100 In plaats van een conventionele scheiding met twee verschillende stoffen, zoals bij een mengsel van alcohol en water, gaan we nu destilleren met drie verschillende stoffen. Dit betekent dat je niet één, maar twee destillaties moet uitvoeren. Een schematische voorstelling van de destillatie is getekend in figuur 20. Figuur 20: Schematische voorstelling van de destillatie. 74
75 Het mengsel van glycerol, water en 1,3-propaandiol wordt in de eerste destillatiekolom gebracht, waar het geheel verwarmd wordt. Het residu uit de tweede destillatiekolom is zuiver 1,3- propaandiol. Je kunt je deze destillatiekolommen voorstellen als reusachtige, rechtopstaande buizen. Er geldt namelijk hoe groter de kolom, hoe nauwkeuriger de scheiding. Bron 8: Productie Sorona Het 1,3-propaandiol dat met de beschreven zuiveringsstappen wordt verkregen is geschikt voor verdere verwerking tot eindproducten. Met deze zuiveringstechnieken kan men een zuiverheid verkrijgen van 99,992%. We noemen dit zuiver 1,3-propaandiol. Het zuivere 1,3-propaandiol wordt onder andere gebruikt voor de productie van een polymeer die wordt gebruikt voor het maken van textiel. Sorona is een voorbeeld van zo n polymeer. De polymeer Sorona, geproduceerd door de Amerikaanse firma DuPont, wordt als vezel geleverd aan met name de textielindustrie. Het dient als grondstof voor bijvoorbeeld vloerbedekking, de matjes die je in de auto onder je voeten vindt, maar ook kleding. Voor het maken van de polymeer Sorona laten we het verkregen zuivere 1,3-propaandiol reageren met tereftaalzuur (een aromatisch dicarbonzuur). 1,3-Propaandiol en tereftaalzuur reageren hierbij in de verhouding 1:1 onder vorming van poly(trimethyleentereftelaat). Dit is een verestering: de alcoholgroepen van 1,3-propaandiol reageren met de carboxylgroepen van het tereftaalzuur. Je kunt je voorstellen, dat als de 1,3-propaandiol niet goed zuiver aangeleverd wordt, de polymerisatiereactie niet goed zal verlopen. Meestal is het zo, dat als een grondstof niet helemaal zuiver is, er stoffen in het mengsel aanwezig zijn die veel op de grondstof lijken. Bij 1,3-propaandiol kunnen dat bijvoorbeeld glycerol of 1-propanol zijn. Bij de productie van Sorona moeten lange, lineaire ketens gevormd worden, dit zijn namelijk de vezels die nodig zijn voor de textielindustrie. Op het moment dat je met behulp van glycerol of 1-propanol gaat polymeriseren, krijg je structuren in je vezel die zeer ongewenst zijn. Zie daarvoor onderstaande figuren. 75
76 Figuur 22: Schematische voorstelling van de polymere eigenschappen van 1-propanol, 1,3-propaandiol en glycerol. Het rechthoekje stelt het C3-molecuul voor, de pijl een oorspronkelijke OH-groep. De gele lijn is een weergave van het polymeer. Je ziet dat 1-propanol en glycerol beiden een verschillende invloed hebben op het polymeer. 1-Propanol zorgt ervoor dat het wel bindt aan het polymeer, maar dat het aan de andere kant geen nieuw tereftaalzuur meer kan binden. 1-Propanol stopt dus de vorming van de keten. We noemen deze stof daarom een "chain terminator". Glycerol daarentegen zorgt er wél voor dat er nieuw tereftaalzuur kan binden, het polymeer kan dus wel langer worden bij binding van een molecuul glyercol. Glycerol heeft echter niet twee bindingsplaatsen, maar drie. Als op alle drie de bindingsplaatsen een nieuwe keten aangroeit, zie je dat het oorspronkelijke polymeer vertakt. We noemen deze stof daarom een "chain brancher", een stof die een lineaire keten vertakt. Vertakte ketens verzwakken de vezels. Om deze effecten te voorkomen moet dus zuiver 1,3-propaandiol aangeleverd worden. 76
77 5.4 Oefenopgave In deze oefenopgave gaan we rekenen aan de productie van 1,3-propaandiol. Kijk voordat je aan de opgaven begint welke rekenstappen je in oefenopgave 4.5 hebt gemaakt. Chemisch technologen rekenen vaak met geschatte waarden van de kosten en opbrengsten van het productieproces. Hieronder is een dergelijke tabel gegeven. Tabel 1: De opbrengst, verdunningsfactor en de extra kosten per kilogram eindproduct per zuiveringsstap onder industriële condities. Opbrengst (kg/kg) verdunningsfactor Extra kosten ( /kg product) afdoden 1,00 1,0 0,005 extractie 0,98 1,5 0,03 Ionen wisselaar (negatief) 0,99 1,0 0,01 Ionen wisselaar (positief) 0,99 1,0 0,01 Ultrafiltratie 0,98 1,2 0,05 Microfiltratie 0,99 1,0 0,02 Nanofiltratie 0,99 1,0 0,05 Destillatie 0,99 1,0 0,03 1. Laat zien met een berekening dat de totale opbrengst van 1,3-propaandiol 0,93 kg/kg is. 2. Ultra- en Nanofiltratie zijn relatief kostbaar t.o.v. extractie. Waarom is het toch aantrekkelijk Ultra- en Nanofiltratie te gebruiken i.p.v. extractie? In Ommen staat een bedrijf dat hightech exclusieve sportkleding wil gaan maken. Daarvoor is 1,3- propaandiol nodig. Daarom wordt, toevallig naast de calciumlactaat fabriek, ook een 1,3- propaandiol fabriek gebouwd. De grondstof is weer melasse wat door de aanwezigheid van een grote suikerfabriek in Groningen ruim beschikbaar is. Tabel 2: Maximale concentratie, opbrengst en productiviteit van 1,3-propaandiol door gemodificeerde E-coli onder industriële condities. 1,3-PDO concentratie 135 g L -1 1,3-PDO opbrengst uit glucose 0,51 g g -1 Maximale productiviteit 35 g L -1 h -1 Duur van één batch (exclusief onderhoud en 6 h schoonmaak) 3. Bereken hoeveel ton melasse er nodig is voor de productie van 1000 ton zuiver 1,3- propaandiol. Melasse bestaat ongeveer voor 50% uit sacharose dat in water gemakkelijk hydrolyseert tot twee moleculen glucose. Gebruik de totale opbrengst van opgave Bereken het minimale volume dat de fed-batch reactor moet hebben voor de productie van 1000 ton 1,3-PD per jaar. Neem aan dat 15% van de reactortijd gebruikt wordt voor het schoonmaken van de reactor tussen batches en voor onderhoud. 5. Bereken uit de totale opbrengst en met de gegevens uit tabel 1 de prijs per kg 1,3- propaandiol. Neem als de kostprijs van de melasse 20 eurocent per kg. 6. Vergelijk die prijs uit de vorige opgave met die van calciumlactaat uit hoofdstuk 4. Kijk daarbij naar de verschillen in kosten van de grondstoffen en kosten van de zuivering. Geef een verklaring voor het gevonden prijsverschil. Maak daarbij onderscheid tussen grondstofkosten en kosten voor de zuivering. 77
78 Vanwege de grote vraag naar 1,3-propaandiol besluit de fabriek in Ommen zijn productie op te schalen om uiteindelijk ton 1,3-propaandiol te produceren. Er komt een nieuwe fed-batch reactor met een volume van L. De totale duur van een batch blijft hetzelfde als bij de kleine fermentor (zie tabel 2). Ook het nanofiltratiesysteem wordt vernieuwd. Het nieuwe roterende systeem bestaat uit zes nanofiltratieinstallaties per carrousel, zoals in informatie 4 wordt beschreven. Eén nanofiltratieinstallatie heeft een volume van 2 m 3. Een volledige draai van de filtratiecarrousel duurt 3 uur. Het totale reactorvolume moet in de nanofiltratieopstelling passen. 7. Bereken hoeveel nanofiltratiecarrousels er nodig zijn, zodat de fabriek perfect continu kan draaien. Ga er vanuit dat het roteren van de opstellingen 5 % extra volumecapaciteit kost. Verwerk in je berekening ook de verdunning die optreedt bij de zuiveringsstappen (zie tabel 1). 8 Het reactiemengsel dat gefiltreerd wordt bestaat uit water, cellen, eiwitten, DNA, polysachariden, glycerol en 1,3-propaandiol. Geef in onderstaande tabel aan welke deeltjes in de verschillende filtratiestappen in micro-,ultra- en nanofiltratie verwijderd worden. Gebruik BI- NAS tabel 78A. microfiltratie ultrafiltratie nanofiltratie 9 Leg uit waarom in een ionenwisselaar gekozen wordt voor H + -ionen om de positieve ionen te verwijderen en voor OH -ionen om de negatieve ionen te verwijderen. Tereftaalzuur is de andere grondstof voor Sorona naast 1,3-propaandiol 10 Geef de structuurformule op van tereftaalzuur. 11 Geef in structuurformules de reactie van 1,3-propaandiol met tereftaalzuur. 12 Geef een gedeelte van het polymeer Sorona in structuurformule weer. Neem hiervoor 4 monomeer eenheden uit het midden van een polymeerketen. 78
79 Afsluiting In dit hoofdstuk hebben we de metabole routes van E.coli aangepast. Zoals we gezien hebben zijn metabole routes een ingewikkeld stelsel van evenwichtsreacties en stofstromen. Omzettingen binnen de metabole routes kunnen de bacterie energie kosten of juist energie opleveren. Om de invloed van energie op de ligging van evenwichtsreacties en stofstromen beter te kunnen begrijpen introduceren we in het volgende hoofdstuk een nieuwe grootheid; de Gibbs energie. Wat je nu moet weten Chemische synthese van 1,3-propaandiol Biosynthese van 1,3-propaandiol o Koppeling met de glycolyse Metabolic Engineering van E.coli o Werking van een restrictie enzym o Inbouw van vreemd DNA en een plasmide o Fosfo-Transferase Systeem Productie van 1,3-propaandiol o Afdoden van bacteriën met een warmtewisselaar Zuivering van 1,3-propaandiol o Microfiltratie o Ultrafiltratie o Nanofiltratie o Destillatie Productie Sorona o Productieschema o Polycondensatie polymerisatie 79
80 Hoofdstuk 6 Gibbs energie In de derde klas heb je de begrippen exotherm en endotherm leren kennen. Bij exotherme reacties wordt energie afgestaan aan de omgeving. Een voorbeeld is het verbranden van aardgas, hierbij komt veel energie vrij. Bij een endotherme reactie wordt juist energie aan de omgeving onttrokken. Een voorbeeld is de oplosreactie van kaliumnitraat. Bij het oplossen wordt het water koud. Er wordt energie aan het water onttrokken. De woorden endotherm en exotherm laten eigenlijk zien dat, wat je tot nu toe onder exotherm en endotherm verstaan hebt, alleen geldig is als het gaat om warmte. Of een reactie endotherm of exotherm is, zegt niet zoveel over het daadwerkelijke energieverschil van een reactie. De voor de hand liggende reden is dat energie in meer vormen voorkomt dan alleen als warmte (bijv. elektriciteit, licht). Bovendien is het zo dat het energieverschil van een reactie van de omstandigheden afhangt. De druk en temperatuur zijn altijd belangrijk, maar de concentraties van de reagerende stoffen en de samenstelling van een reactiemengsel kunnen ook het energieverschil beïnvloeden. Het energieverschil van een reactie hangt ook af van welke omstandigheden tijdens de reactie constant blijven en welke omstandigheden veranderen. Het energieverschil van een reactie die uitgevoerd wordt bij constant volume en bij een oplopende druk is niet gelijk aan het energieverschil van de reactie, als deze uitgevoerd wordt bij constante druk en oplopend volume. Dit effect is erg belangrijk en speelt een grote rol bij het ontwerpen van stoommachines en verbrandingsmotoren. Vraag 1. Moderne, hoog rendement, benzinemotoren werken met veel hogere drukken dan oude benzinemotoren met een lager rendement. Beredeneer hoe het energieverschil van verbranding van benzine van de druk afhangt. Voor biologen en chemici is het energieverschil van een reactie die verloopt bij constante temperatuur en constante druk een belangrijke grootheid. Het verschil van energie bij deze omstandigheden bepaalt namelijk of reacties spontaan kunnen verlopen en bij evenwichtsreacties bepaalt het de ligging van het evenwicht. Deze energie wordt de Gibbs energie (G) genoemd. Het verschil in Gibbs energie voor en na de reactie heeft als symbool G. Een reactie zal spontaan verlopen als de Gibbs energie afneemt G < 0. Er moet energie bij als de Gibbs energie van de reagerende stoffen toeneemt G > 0. Bij chemisch evenwicht veranderen de concentraties van de reagerende stoffen niet meer en blijft de Gibbs energie gelijk G = 0. Voorbeelden: Verbranding van aardgas is een spontaan verlopende reactie: CH 4(g)+2O 2(g) CO 2(g) + 2H2O(l) G < 0 Zilverchloride lost niet spontaan (slecht) op in water + - AgCl(s) Ag (aq)+cl (aq) G > 0 In een verzadigde oplossing van kaliumchloride is vast kaliumchloride in evenwicht met de opgeloste fase. KCl(s) K + (aq) + Cl - (aq) G = 0 Vraag 2. Biologen rekenen bij reacties in levende cellen bijna altijd met de Gibbs energie. Leg uit waarom juist de Gibbs energie het energieverschil bij reacties in een cel goed beschrijft 80
81 6.1 Berekening G 0 In het speciale geval dat reacties verlopen bij standaard omstandigheden wordt de standaard 0 0 Gibbs energie met symbool G gebruikt. De verandering in G is het verschil van de Gibbs energie van de uitgangsstoffen en de Gibbs energie van de reactie producten onder standaardomstandigheden G = G na G voor. 0 Onder standaardomstandigheden verstaan we een druk van p = p0, een temperatuur van T = 273 K en alle stoffen aanwezig in zuivere vorm en in een concentratie van 1 mol L -1. Deze voorwaarden ben je eerder tegengekomen bij de standaardelektrodepotentiaal (Binas tabel 48) Voorbeeld berekening 1 G 0 Onderstaande reactie geeft het uitharden van cement weer. ( ) Ca OH (s)+co (g) CaCO (s)+h O(l) 2 0 Om G te berekenen moet je de Gibbs energieën van Ca(OH) 2, CO 2, CaCO 3 en H 2 O kennen. Echter van geen enkele stof is de Gibbs energie bekend. In tabellen worden geen Gibbs energieën maar G waarden gegeven. De grootheid G wordt de vormingsenergie genoemd en geeft aan hoeveel de standaard Gibbs energie van een stof verschilt met die van de elementen waaruit deze gevormd is. Er is namelijk afgesproken dat bij de elementen onder standaard omstandigheden G = 0. Voor berekeningen maakt dit niet uit, je kunt met G rekenen alsof het standaard Gibbs energieën zijn. Een tabel met vormingsenergieën van een aantal stoffen staat achteraan dit hoofdstuk (tabel 1). Vormingsenergie (KJ mol -1 ) 0 Ca, C, H 2, O 2 (T = 298 K en p = p 0 ) G = 394,2 kj mol CO 2 (g) -1 Ca(OH) 2 (s) H 2 O (l) CaCO 3 (s) G -1 G = 897,5 kj mol -1 G = 1128,8 kj mol = 237,1 kj mol -1 Figuur 1: De vormingsenergieën ( elementen ) van CO 2, Ca(OH) 2, H 2 O en CaCO 3 uit de We gaan nu even terug naar de reactie ( ) De Gibbs energie voor de reactie is De Gibbs energie na de reactie is Ca OH (s)+co (g) CaCO (s)+h O(l) Ca( OH ) 2 CO2 2 G + G = -897,5+(-394,2)=-1291,7 kjmol -1 G + G = -1128,8+(-237,1)=-1365,9 kjmol -1 CaCO3 H2O ( ) ( ( ) CO ) = = + + = -1365,9-(-1291,7)=-74,2 kjmol -1 0 G Gna - Gvoor G CaCO G 3 H2O G Ca OH G 2 2 De berekening geeft aan dat het uitharden van cement een spontaan proces is, waarbij energie vrijkomt. Dit klopt, want bijvoorbeeld bij de aanleg van de betonnen Hooverdam in de VS werd tijdens de bouw het uithardende beton binnen in de dam gekoeld om te voorkomen dat er scheuren in het beton zouden ontstaan. 81
82 Figuur 2 geeft de berekening in een diagram weer. Gibbs energie (KJ mol -1 ) 0 Ca, C, H 2, O 2 (T = 298 K en p = p 0 ) G = 1291,7 kj mol Ca(OH) 2 (s)+ CO 2 (g) G -1 = 74,2 kj mol 0-1 G = 1365,9 kj mol CaCO 3 (s) + H 2 O (l) -1 Figuur 2: De verandering in standaard Gibbs energie van de reactie berekend uit de de reagerende stoffen. Uit de figuur volgt dat = -74,2 kjmol -1 waarden van Voorbeeld berekening 2 G 0 Is de verbranding van glucose een spontaan proces? De reactievergelijking is C H O (s)+6o (g) 6CO (g)+6h O(l) Let op! De reactie coëfficiënten zijn nu ongelijk aan 1: 0 G = G - G Vragen na voor ( ) ( ) 0 G = 6 394, ,1 ( 910,5 + (6 0)) = 2877,3 kjmol -1 0 G < 0 dus de verbranding is een spontaan proces. 3. Waarom is G zuurstof = 0 bij 278 K en p = p 0? 4. Bereken 0 G voor de vorming van CO 2 uit grafiet en zuurstof Bereken G voor de verbranding van propaan waarbij enige tijd na de reactie de producten weer op kamertemperatuur zijn. 6. Bij het oplossen van ammoniumnitraat is de oploswarmte kj mol -1. Wordt de oplossing warm of koud door het oplossen van ammoniumnitraat? Bereken m.b.v. tabel 1 of het oplossen van ammoniumnitraat een spontaan proces is. 82
83 6.2 G 0 en reactiesnelheid. De snelheid van een reactie hangt onder andere af van de activeringsenergie. De reactiesnelheid 0 0 wordt niet voorspeld door G. Dit komt omdat G alleen iets zegt over het verschil in energie 0 tussen de beginstoffen en de reactie producten. G is onafhankelijk van het reactiemechanisme en zegt daarom niets over de activeringsenergie. Voorbeeld berekening 3 G 0 0 Bereken G voor de omzetting van diamant in grafiet. diamant: G = 2,9 kjmol -1 en grafiet: G = 0 (zie tabel 1) 0-1 G G = G = 0 2,9 = -2,9 kjmol grafiet diamant Dus de omzetting van diamant in grafiet is een spontane reactie. Gelukkig is de activeringsenergie zo hoog dat onder normale omstandigheden deze omzetting niet plaatsvindt. Vraag 7. Waaruit kan je concluderen dat bijvoorbeeld de verbrandingsreacties van grafiet en propaan een hoge activeringsenergie moeten hebben? 6.3 G 0 bij evenwichten Bekijk de evenwichtsreactie A+B C+D De evenwichtsvoorwaarde voor een homogeen evenwicht wordt gegeven door K = [ C][ D] [ A][ B] Waarbij [A], [B, [C] en [D] de concentraties van beginstoffen en producten in het evenwichtmengsel zijn. Nu is het belangrijk te beseffen dat op twee manieren afgeweken wordt van standaardomstandigheden. 1 De stoffen zijn niet in zuivere vorm aanwezig 2 De concentraties zijn hoogstwaarschijnlijk anders dan 1 mol L -1. In de inleiding is gegeven dat bij evenwicht de Gibbs energie gelijk blijft dus G = 0. Maar omdat er geen standaardomstandigheden heersen zullen de Gibbs energie en de standaard Gibbs energie van elkaar verschillen dus G G. 0 Nu is er iets bijzonders aan de hand. Het is namelijk zo dat de waarde van K berekend kan worden 0 uit de G van de reactie via = 0 G 2,303RT log K waarin R de gasconstante is (8,31 J K -1 mol -1 ) en T de temperatuur (in K). Dus bij evenwicht blijft 0 de Gibbs energie gelijk daarom is G = 0, maar G 0. Bovendien bepaalt de waarde van G 0 de ligging van het evenwicht. Daarom is G een belangrijke grootheid in de scheikunde. 0 83
84 Vragen 8. Voor een evenwichtsreactie C(s)+CO 2(g) 2CO(g) is gegeven dat 1 bij 298 K. Bereken K. Ligt het evenwicht naar links of rechts? 0 G = 120 kj mol - 9. Voor een evenwichtsreactie 2NO ( g ) +O ( g) 2NO ( g) kj mol -1 bij 750 K. Bereken K. 2 2 is gegeven dat 0 G = -2, G in steady state Als bij een reactie de uitgangsstoffen voortdurend worden aangevoerd en de reactieproducten voortdurend worden afgevoerd kan een situatie ontstaan, waarbij de reactie doorgaat maar de concentraties van de reagerende stoffen niet meer veranderen. Dit wordt een steady state genoemd. Omdat we nu met een mengsel van stoffen in plaats van zuivere stoffen te maken hebben, mogen 0 we formeel niet meer rekenen met G. Om toch het verschil in Gibbs energie uit te kunnen rekenen, maken we gebruik van het feit dat in evenwicht, ongeacht de samenstelling van een mengsel, altijd geldt dat G = 0. Ook maken we gebruik van het feit dat zowel bij steady state als bij evenwichtsreacties de concentraties constant zijn. Afleiding We gaan weer terug naar evenwichtsreactie A+B C+D 0 In de vorige paragraaf is gegeven dat G = 2,303RT log K of anders geschreven; 0 G + 2,303RT log K = 0. Bovenstaande vergelijking invullen in G = 0 levert 0 G = G + 2,303RT logk. De evenwichtsvoorwaarde voor de reactie invullen in bovenstaande vergelijking levert [ ][ ] [ A][ B] C D 0 G = G + 2,303RT log Met bovenstaande vergelijking kan G in een mengsel van uitgangsstoffen en reactieproducten uitgerekend worden. De vergelijking laat verder zien dat hoe verder een steady state reactie uit evenwicht is, hoe groter het verschil in Gibbs energie wordt. Voorbeeld berekening 4 G in steady state In levende organismen vinden veel steady state omzettingen plaats. We nemen als voorbeeld de verbranding van glucose C H O (aq)+6o (aq) 6CO (aq)+6h O(l) Met steady state concentraties [glucose] = 1,0 mmol L -1, [O 2 ] = 0,23 mmol L -1 en [CO 2 ] = 0,16 mmol L -1, T= 298 K en p = p 0. (Voor de G 0 van deze reactie, zie voorbeeldberekening 2). 84
85 Onder deze voorwaarden wordt de Gibbs energie die vrijkomt per mol glucose gegeven door 6 [ CO2 ] [ ][ ] 0 G = G + 2,303RT log glucose O 3 G = 2870, ,303 8, log G = kj mol ( 1,6 10 ) 3 4 ( 1,0 10 ) ( 2,3 10 ) Vragen 10. Stel dat een organisme veel efficiënter is in het afvoeren van de CO 2 die gevormd wordt bij de reactie, waardoor de concentratie van CO keer lager wordt dan in bovenstaand voorbeeld Bereken nu hoeveel Gibbs energie vrijkomt per mol glucose. 11. Zoek in tabel 49 BINAS de K b voor NH 3 (aq) op en bereken met water: + - NH 3(aq)+ H2O(l) NH 4 (aq)+oh (aq) 6 0 G voor de reactie van NH Bereken G voor de reactie uit de vraag 11) als in steady state [NH 3 ] = 100 mmol L -1, [NH + 4 ] = 1,00 mmol L -1 en [OH - =1,50 mmol L -1. Welke reactie zal onder deze omstandigheden verlopen. De reactie naar links of de reactie naar rechts? Licht je antwoord toe. 85
86 6.5 Oefenopgave bij Gibbs energie Gibbs energie in melkzuurproductie Voor de productie van D-lactaat wordt wel Lactobacillus delbrueckii gebruikt. Deze bacteriesoort kan erg veel melkzuur produceren en daarom moet, om tijdens de productie de ph boven ph = 6,0 te houden, calciumcarbonaat aan de fed-batch reactor worden toegevoegd. Een neveneffect is dat daarbij vrijwel al het aanwezige melkzuur omgezet wordt in calciumlactaat. Calciumlactaat is veel minder goed oplosbaar in water dan melkzuur. De hoge melkzuur concentraties kunnen voor problemen zorgen, omdat na toevoeging van calciumcarbonaat het opgeloste melkzuur gedeeltelijk kan neerslaan als calciumlactaat. Dit leidt tot een lagere efficiëntie van het productieproces. (zie hoofdstuk 4-route 4) Marianne wordt als bedrijfschemicus gevraagd te onderzoeken of een neerslag van calciumlactaat te verwachten is. Zij begint met een literatuuronderzoek, maar in de literatuur kan zij het oplosbaarheidproduct van D-calciumlactaat niet vinden. Wel vindt zij G ø waarden voor D-melkzuur, D- lactaat (aq) en D-calciumlactaat (zie onderstaande tabel). Om de betrouwbaarheid van onderstaande data te controleren, berekent Marianne met behulp van deze data de pkz van melkzuur. Als deze correspondeert met de al bekende pkz voor melkzuur zullen de G ø waarden wel correct zijn. Tabel G ø waarden voor enkele lactaten Stof G ø (kjmol -1 ) D-melkzuur CH 3 CHOHCOOH (s) -522,9 D-melkzuur CH 3 CHOHCOOH (aq) -540,3 D-lactaat CH 3 CHOHCOO (aq) -517,8 D-calciumlactaat Ca(CH 3 CHOHCOO) 2 (s) -1584,0 1. Bereken G 0 voor de reactie CH + - 3CHOHCOOH(aq) H (aq)+ch3chohcoo (aq) Gebruik daarbij ook tabel 1 uit dit hoofdstuk. 2. Laat met een berekening zien dat de pk z berekend uit de G 0 overeenkomt met de bekende pk z = 3,95 van melkzuur. De G ø waarden lijken betrouwbaar dus gaat Marianne deze gebruiken voor het berekenen van de oplosbaarheid van calciumlactaat. 3. Geef de reactievergelijking voor het oplossen van calciumlactaat. 4. Bereken G 0 voor de oplosreactie van calciumlactaat 5. Geef de evenwichtvoorwaarde voor bovenstaande reactie. 6. Bereken K s voor bovenstaande reactie. 7. Laat met een berekening zien of alle lactaat in oplossing blijft als in een melkzuuroplossing van 90,0 g L -1 alle melkzuur wordt omgezet in calciumlactaat(aq) 86
87 Enigszins geschrokken van het resultaat van de berekening uit opgave 6 realiseert Marianne zich dat de temperatuur in de fed-batch reactor 42 C is, terwijl de gevonden waarde voor K s geldig is bij 298 K. Bij een hogere temperatuur zal de oplosbaarheid meestal groter zijn. Een nieuwe speurtocht in de literatuur levert de oplosbaarheid van L-calciumlactaat als functie van de temperatuur. Figuur 3: De oplosbaarheid van L-calciumlactaat als functie van de temperatuur. 8. Hoeveel procent van het oorspronkelijke melkzuur blijft als lactaat in oplossing als bij 42 C in een 90,0 g L -1 oplossing alle melkzuur wordt omgezet in calciumlactaat(aq)? Neem daarbij aan dat de relatieve toename van de oplosbaarheid met toenemende temperatuur voor D-calciumlactaat en L-calciumlactaat gelijk zijn. 9. Hoe hoog moet de temperatuur in de fed-batch reactor worden om alle calciumlactaat in oplossing te houden? 10. Bedenk een andere manier om de neerslagvorming te voorkomen. 87
88 Tabel 1 Vormingsenergieën bij T=298 K en p=p 0 Stof G (kj mol -1 ) Ag (s) 0 Ag + (aq) +77,1 AgBr (s) -96,9 AgCl (s) -109,8 AgNO 3 (s) -33,4 Ba (s) 0 Ba 2+ (aq) -560,8 BaCl 2 (s) -810,4 C(s) diamant +2,9 C(s) grafiet 0 Ca (s) 0 Ca(OH) 2 (s) -897,5 Ca 2+ (aq) -553,6 CaCl 2 (s) -748,1 CaCO 3 (s) -1128,8 CaO (s) -604,0 Cl - (aq) -131,2 Cl 2 (g) 0 CO (g) -137,2 CO 2 (aq) -386,0 CO 2 (g) -394,2 CO 2-3 (aq) -527,8 H + (aq) 0 H 2 (g) 0 H 2 CO 3 (aq) -623,1 H 2 O (g) -228,6 H 2 O (l) -237,1 H 2 O 2 (l) -120,4 H 2 S (g) -33,6 H 2 SO 4 (l) -690,0 HCl (g) -95,3 HCO - 3 (aq) -586,8 HNO 3 (l) -80,7 HS - (aq) -27,8 HSO - 4 (aq) -755,9 I - (aq) -51,6 I 2 (g) +19,3 I 2 (s) 0 K (s) 0 K + (aq) -283,27 KBr (s) -380,7 KCl (s) -409,1 KI (s) -324,9 KOH (s) -379,1 N 2 (g) 0 N 2 O (g) +104,2 N 2 O 4 (g) +97,9 Na (s) 0 Na ,9 NaBr (s) -349,0 NaCl (s) -384,1 NaI (s) -286,1 NaOH (s) -379,5 NH 3 (aq) -26,5 NH 3 (g) -16,5 NH + 4 (aq) -79,3 NH 4 NO 3 (s) -183,9 NO (g) +86,6 NO 2 (g) +51,3 NO - 3 (aq) -108,7 O 2 (g) 0 O 3 (g) +163,2 OH - (aq) -157,2 S(s) (S 8 ) 0 S 2- (aq) +85,8 SO 2 (g) -300,2 SO 3 (g) -371,1 SO 2-4 (aq) -744,5 Koolwaterstoffen CH 4 (g) (methaan) -50,7 C 2 H 2 (g) (ethyn) +209,2 C 2 H 4 (g) (etheen) +68,15 C 2 H 6 (g) (ethaan) -32,82 C 3 H 8 (g) (propaan) -23,5 C 4 H 10 (g) (butaan) -17,0 C 5 H 12 (g) (pentaan) -8,20 C 6 H 6 (l) (benzeen) -124,3 C 6 H 12 (l) (cyclohex.) +26,8 C 6 H 8 (l) (hexaan) -0,25 Alcoholen CH 3 OH (l) (methanol) -166,3 C 2 H 5 OH (l) (ethanol) -174,8 Carbonzuren HCOOH (l) -361,4 CH 3 COOH (l) -390,0 CH 3 COOH (aq) -396,5 CH 3 COO - (aq) -369,3 Suikers C 6 H 12 O 6 (s) (glucose) -910,5 C 6 H 12 O 6 (aq) -917,5 88
89 Hoofdstuk 7 Gibbs energie en de dissimilatie van glucose In dit hoofdstuk koppelen we onze kennis over Gibbs energie uit hoofdstuk 6 aan de dissimilatie van glucose uit hoofdstuk 3. Als we de processen bekijken die in een bacterie verlopen, kunnen we stellen dat over een periode van enkele minuten er in de cel sprake is van homeostase (Grieks voor constante toestand). Tijdens homeostase zijn veel reacties in steady state: de reacties vinden plaats maar de concentraties van de reagerende stoffen veranderen niet. Dit komt doordat de uitgangsstoffen doorlopend worden aangevoerd en de reactieproducten afgevoerd. Zo wordt in de glycolyse in steady state evenveel pyruvaat gemaakt als afgestaan en evenveel glucose omgezet als er door de bacterie netto wordt opgenomen uit zijn omgeving. Het handhaven van een balans voor ATP en NADH is gezien hun centrale rol extra belangrijk. ATP en NADH kunnen de cel niet in of uit getransporteerd worden. Dit houdt overigens niet in dat er geen ATP gemaakt of afgebroken kan worden in de steady state, maar wel dat de totale snelheid van de ATP vorming in steady state gelijk moet zijn aan de totale snelheid van de ATP afbraak (hydrolyse). Aangezien de glycolyse een centrale rol speelt in het metabolisme en daarom ook in het handhaven van homeostase moet deze route goed gereguleerd worden. Allereerst gaan we kijken naar de rol van de Gibbs energie in de energieopbrengst en de regulatie van de glycolyse. 7.1 Gibbs energie en de regulering van de glycolyse Gibbs energie is de bruikbare energie die uit moleculen gehaald kan worden en in de cel kan worden overgedragen naar ADP + P i. Zoals we in hoofdstuk 6 gezien hebben is de Gibbs energie die bij een reactie beschikbaar komt gelijk aan het verschil in Gibbs energie tussen de beginstoffen en de producten: De reacties in een cel zijn altijd evenwichtsreacties die in een bepaalde richting moeten verlopen om efficiënt een biosynthetische route te vormen. De verandering van Gibbs energie geeft informatie over 1. Of er energie beschikbaar komt ( G is negatief) of nodig is ( G is positief); 2. Hoe de ligging is van het evenwicht. Als de G 0 negatief is, ligt het evenwicht naar rechts, als de G 0 positief is, ligt het evenwicht naar links. Er zijn drie reacties in de glycolyse die onder normale omstandigheden niet omkeerbaar zijn. Hierdoor kan de glycolyse maar in één richting verlopen. Het gaat hierbij om de stappen 1, 3 en 10 en respectievelijk de enzymen hexokinase, fosfofructokinase en pyruvaatkinase (zie figuur 1 hieronder). Deze reacties zijn niet omkeerbaar doordat ze een sterk negatieve G hebben. 89
90 Figuur 1: de 10 stappen van de glycolyse Tabel 1: De Gibbs energie van de glycolyse onder standaardomstandigheden. De nummers in deze tabel corresponderen met de stappen in figuur 1. Nummer Enzym G 0 (kj/mol) G (kj/mol)* 1 Hexokinase -16,7-33,5 2 Fosfohexose-isomerase +1,7-2,5 3 Fosfofructokinase -14,2-22,2 4 Aldolase +23,9-1,3 5 Triosefosfaat-isomerase +7,6 +2,5 6 Glyceraldehyde-3-fosfaat-dehydrogenase +12,6-3,4 7 Fosfoglyceraatkinase -37,6 +2,6 8 Fosfoglyceraatmutase +8,8 +1,6 9 Enolase +3,4-6,6 10 Pyruvaatkinase -62,8-33,4 *gemeten in spierweefsel van konijnen 90
91 Een reactie met een hoge positieve G 0 waarde (bijv.aldolase) zal normaal gesproken alleen naar links verlopen. Hoe kan het dan dat deze reacties in de cel toch naar rechts verlopen? Dat kan bijvoorbeeld doordat onder steady state voortdurend het gevormde product van een reactie wordt verbruikt. Een tweede mogelijkheid is dat de reactie met een positieve G 0 gekoppeld is aan een reactie met een negatieve G 0. De eerste reactie in de glycolyse (figuur 1) is hiervan een goed voorbeeld. De reactie heeft een sterk negatieve G 0. Dit wordt veroorzaakt door de koppeling van de fosforylering van glucose (eerste deelreactie) aan de hydrolyse van ATP (tweede deelreactie). Door de koppeling van deze twee reacties wordt een energetisch gunstige totaalreactie verkregen: 1 e deelreactie: Glucose + HPO H + Glucose-6-phosphate + H 20 G 0 = +14 kj/mol 2 e deelreactie: ATP + H 2 O ADP + P i + H + G 0 = -30,5 kj/mol Totaalreactie: Glucose + ATP Glucose-6-phosphate + ADP G 0 = -16,5 kj/mol Opdracht 1. Maak met behulp van tabel 1 een grafiek waarbij je de stappen van de glycolyse uitzet tegen de G 0 en de G. a. Vergelijk de grafieken en geef aan welke verschillen je het meest opvallen. b. Verklaar de verschillen tussen de twee grafieken. Vragen 1. Bereken met behulp van tabel 1 en de vergelijking G 0 = - 2,303 RTlogK de waarden van de evenwichtsconstante voor de reacties die gekatalyseerd worden door fosfofructokinase en aldolase. 2 a. Bereken met behulp van G 0 uit tabel 1 de evenwichtsconstante voor stap 10. b. Bereken met behulp van de G 0 en G waarden uit tabel 1 met behulp van de vergelijking voor G in steady state de verhouding van de beginstoffen en de reactieproducten bij de in tabel 1 gegeven G. 7.2 G 0 en de standaardelektrode potentiaal Bacteriën gebruiken verschillende stoffen om energie uit te halen en ATP te vormen. Een aantal van deze stoffen, bijvoorbeeld nitriet en sulfide, leveren energie via een redoxreactie. Ook de vorming van NADH en de reacties van de ademhalingsketens zijn redoxreacties. Bij een redoxreactie is het vaak eenvoudiger om de standaardelektrode potentiaal V 0 in plaats van G 0 te gebruiken om te voorspellen of een reactie kan plaatsvinden. De energie die vrijkomt door overdracht van elektronen bij een redoxreactie zorgt voor het ontstaan van een potentiaalverschil: V = V V. elektronenacceptor elektronendonor De maximale hoeveelheid elektrische arbeid (W) die verricht kan worden door het gevormde potentiaalverschil wordt gegeven door de vergelijking W = q V (q is de lading in Coulomb (C), en V is het potentiaalverschil in Volt (V). De Gibbs energie komt overeen met de negatieve waarde van de maximale hoeveelheid elektrische arbeid: G = W. 91
92 Aangezien q = nf (n is het aantal elektronen die van de reductor overgaan naar de oxidator en F is de constante van Faraday (Binas tabel 7)) kunnen we bovenstaande vergelijking omzetten naar G = nf V of onder standaardomstandigheden G = nf V. Uit deze vergelijking kunnen we afleiden dat V 0 > 0 de reactie loopt naar rechts V 0 < 0 de reactie loopt naar links V 0 = 0 evenwicht Tabel 1 geeft de standaardelektrode potentialen van een aantal reacties die je bent tegengekomen in hoofdstuk 3. Een belangrijke toepassing van het gebruik van V 0 waarden is om te voorspellen of bepaalde bacteriën geschikt zijn om bijvoorbeeld nitriet, nitraat en sulfaten in afvalwater af te breken. Tabel 2: Standaard elektrodepotentialen voor enkele reacties (298 K en ph = 7) Halfreactie V 0 (V) O 2 + 4H + + 4e - 2H 2 O +0,816 NO H + + 2e - NO H 2 O +0,421 Fumarate H + + 2e - succinate 2- +0,031 FAD + 2H + + 2e - FADH 2-0,219 S + 2H + + 2e - H 2 S -0,243 NAD + + 2H + + 2e - NADH + H + -0,320 Vragen 3 Hoeveel moleculen ATP kunnen maximaal geproduceerd worden door de oxidatie van 1 molecuul succinaat met zuurstof? Gebruik tabel 2. 4 In hoofdstuk 3 heb je gezien dat er uit NADH en FADH 2 via een redoxreactie ATP gevormd kan worden. a. Hoeveel ATP kan er theoretisch uit 1 molecuul NADH of FADH 2 gevormd worden met zuurstof als elektronenacceptor? b. Waarom kan er meer ATP gevormd worden uit NADH dan uit FADH 2? 5 In levende cellen is via nauwkeurige metingen vastgesteld dat er uit 1 mol NADH gemiddeld 2,5 mol ATP gevormd wordt. Geef een verklaring voor het verschil tussen deze waarde en de theoretische waarde die je in de vorige vraag hebt berekend. 92
93 6 De Anammox reactie (anaerobe ammonia oxidatie) wordt uitgevoerd door verschillende bacteriën. Via het Anammox-proces wordt ammonium en nitriet in afvalwater direct omgezet in stikstofgas: NH (aq) + NO (aq) N (g) + 2H O(l) De halfreactie met NH 4 + als reductor is: NH N + 8H + 6e a. Stel de andere halfreactie op. b. De Anammox reactie zoals boven beschreven heeft een G van 357 kj/mol. Wat is de V van deze reactie? Figuur 2: Anammoxbacterie onder de microscoop. 7.3 Andere regulatie mechanismen Hoewel de Gibbs energie dus veel informatie geeft over de richting van de reactie of de ligging van een evenwicht, is de Gibbs energie onafhankelijk van het reactiemechanisme. De Gibbs energie zegt dus niet via welke tussenproducten of met welke snelheid een reactie verloopt. Daarom heeft bijvoorbeeld een katalysator zoals een enzym geen invloed op de Gibbs energie. De activiteiten van bijvoorbeeld hexokinase, fosfofructokinase en pyruvaatkinase worden nauwkeurig geregeld door de concentraties van deze enzymen en hun substraten op het juiste niveau te houden Een goed voorbeeld van de regulering van de activiteit van de enzymen zelf, is de wijze waarop de activiteit van fosfofructokinase wordt beïnvloed door de aanwezigheid van ATP en AMP. Fosfofructokinase katalyseert de snelheidsbepalende stap in de glycolyse. ATP remt dit enzym terwijl AMP deze remmende werking juist tegengaat. Als de ATP concentratie in de cel toeneemt, verloopt de glycolyse dus langzamer en als de ATP concentratie afneemt, verloopt de glycolyse sneller. Onder normale omstandigheden verandert de ATP concentratie echter niet zo veel, maar de AMP concentratie kan juist wel snel toenemen. Dit komt doordat het enzym adenylaatkinase de reactie 2 ADP ATP + AMP katalyseert. De verhoudingen tussen ATP, ADP en AMP concentraties zijn gewoonlijk 100:10:1. Hierdoor zal een kleine verandering in de concentratie van ATP een grote verandering in de concentratie van AMP tot gevolg hebben. AMP is daardoor de belangrijkste regulerende factor voor fosfofructokinase. Vraag 7 Bereken met behulp van de evenwichtsvoorwaarde de verandering in de AMP concentratie die plaatsvindt wanneer 8% van de ATP in een cel plotseling wordt gehydrolyseerd tot ADP. De K voor deze reactie is 0,44 (298 K). De beginconcentraties voor ATP, ADP en AMP zijn 1800 µm, 180 µm, 20 µm. Wat je nu moet weten Gibbs energie en de regulering van de glycolyse Het verband tussen G 0 en V 0 De rol van V 0 bij biosynthetische reacties in de cel. 93
Celademhaling & gisting
 Celademhaling & gisting Tekst voor de leerlingen V. Rasquin - 1 - DISSIMILATIE - TEKST VOOR DE LEERLINGEN celademhaling & GISTING Wij weten dat heel wat processen endergonisch zijn (ze vergen energie).
Celademhaling & gisting Tekst voor de leerlingen V. Rasquin - 1 - DISSIMILATIE - TEKST VOOR DE LEERLINGEN celademhaling & GISTING Wij weten dat heel wat processen endergonisch zijn (ze vergen energie).
Vragen bij deoefen- en zelftoets-module behorende bij hoofdstuk 9 van Biology, Campbell, 8 e druk Versie 2010-2011
 Celstofwisseling I Vragen bij deoefen- en zelftoets-module behorende bij hoofdstuk 9 van Biology, Campbell, 8 e druk Versie 2010-2011 Inleiding 1-12 Deze module gaat over de omzetting van voedsel in energie
Celstofwisseling I Vragen bij deoefen- en zelftoets-module behorende bij hoofdstuk 9 van Biology, Campbell, 8 e druk Versie 2010-2011 Inleiding 1-12 Deze module gaat over de omzetting van voedsel in energie
Studiehandleiding Biochemie I
 Studiehandleiding Biochemie I 2006-2007 1 Proeftentamen Biochemie I 1. Vul de juiste term uit de lijst op de open plaatsen in onderstaande tekst in. Elke term mag maar éénmaal worden gebruikt maar niet
Studiehandleiding Biochemie I 2006-2007 1 Proeftentamen Biochemie I 1. Vul de juiste term uit de lijst op de open plaatsen in onderstaande tekst in. Elke term mag maar éénmaal worden gebruikt maar niet
Nederlandse samenvatting voor geïnteresseerden buiten het vakgebied
 Nederlandse samenvatting voor geïnteresseerden buiten het vakgebied Met dit proefschrift ga ik promoveren in de biochemie. In dit vakgebied wordt de biologie bestudeerd vanuit chemisch perspectief. Het
Nederlandse samenvatting voor geïnteresseerden buiten het vakgebied Met dit proefschrift ga ik promoveren in de biochemie. In dit vakgebied wordt de biologie bestudeerd vanuit chemisch perspectief. Het
Moderne Biotechnologie van cel naar fabriek 6 vwo. DvD-bijeenkomst Moderne Biotechnologie & Bionanowetenschappen 24 maart 2011
 Moderne Biotechnologie van cel naar fabriek 6 vwo DvD-bijeenkomst Moderne Biotechnologie & Bionanowetenschappen 24 maart 2011 Ontwikkelteam 2008-2010 Coach Coach: Aonne Kerkstra Docenten Ingeborg de Kooter
Moderne Biotechnologie van cel naar fabriek 6 vwo DvD-bijeenkomst Moderne Biotechnologie & Bionanowetenschappen 24 maart 2011 Ontwikkelteam 2008-2010 Coach Coach: Aonne Kerkstra Docenten Ingeborg de Kooter
Examen Voorbereiding Cellen
 Examen Voorbereiding Cellen Teylingen College Leeuwenhorst 2015/2016 Thema 2 Cellen Begrippenlijst: Begrip Organellen Plastiden Stamcellen Embryonale stamcellen Adulte stamcellen Endoplasmatisch reticulum
Examen Voorbereiding Cellen Teylingen College Leeuwenhorst 2015/2016 Thema 2 Cellen Begrippenlijst: Begrip Organellen Plastiden Stamcellen Embryonale stamcellen Adulte stamcellen Endoplasmatisch reticulum
De cel metabolisme cel cel- membraan eiwitsynthese DNA aminozuren 1.1 De cel celcyclus celmembraan Afbeelding 1.1
 de cel Elk levend wezen is opgebouwd uit cellen. Het eerste deel van dit hoofdstuk gaat over de verschillende onderdelen van een cel. We bespreken het celmembraan, het cytoplasma en de belangrijkste organellen.
de cel Elk levend wezen is opgebouwd uit cellen. Het eerste deel van dit hoofdstuk gaat over de verschillende onderdelen van een cel. We bespreken het celmembraan, het cytoplasma en de belangrijkste organellen.
BIOLOGIE Energie & Stofwisseling HAVO Henry N. Hassankhan Scholengemeenschap Lelydorp [HHS-SGL]
![BIOLOGIE Energie & Stofwisseling HAVO Henry N. Hassankhan Scholengemeenschap Lelydorp [HHS-SGL] BIOLOGIE Energie & Stofwisseling HAVO Henry N. Hassankhan Scholengemeenschap Lelydorp [HHS-SGL]](/thumbs/23/1930424.jpg) BIOLOGIE Energie & Stofwisseling HAVO Henry N. Hassankhan Scholengemeenschap Lelydorp [HHS-SGL] Docent: A. Sewsahai De student moet de bouw en werking van enzymen kunnen beschrijven moet het proces van
BIOLOGIE Energie & Stofwisseling HAVO Henry N. Hassankhan Scholengemeenschap Lelydorp [HHS-SGL] Docent: A. Sewsahai De student moet de bouw en werking van enzymen kunnen beschrijven moet het proces van
Biotechnologie vmbo-b34. CC Naamsvermelding 3.0 Nederland licentie.
 Auteur VO-content Laatst gewijzigd Licentie Webadres 20 December 2016 CC Naamsvermelding 3.0 Nederland licentie http://maken.wikiwijs.nl/73574 Dit lesmateriaal is gemaakt met Wikiwijs Maken van Kennisnet.
Auteur VO-content Laatst gewijzigd Licentie Webadres 20 December 2016 CC Naamsvermelding 3.0 Nederland licentie http://maken.wikiwijs.nl/73574 Dit lesmateriaal is gemaakt met Wikiwijs Maken van Kennisnet.
Celmembraan (duh! dat maakt het een cel) Celwand Ribosomen (voor eiwitsynthese) Soms: uitsteeksels zoals flagel (zweepstaart)
 Bacterie cel: prokaryoot: geen kern, geen chromosomen zoals wij ze kennen maar cirkelvormig Chromosoom: dus wel DNA Sommige autotroof: als ze pigmenten hebben waarmee ze fotosynthese kunnen uitvoeren Meeste
Bacterie cel: prokaryoot: geen kern, geen chromosomen zoals wij ze kennen maar cirkelvormig Chromosoom: dus wel DNA Sommige autotroof: als ze pigmenten hebben waarmee ze fotosynthese kunnen uitvoeren Meeste
Samenvatting Biologie Samenvatting hoofdstuk 1 bvj
 Samenvatting Biologie Samenvatting hoofdstuk 1 bvj Samenvatting door Fabienne 1166 woorden 24 oktober 2017 5 2 keer beoordeeld Vak Methode Biologie Biologie voor jou Hoofdstuk 1: stofwisseling Paragraaf
Samenvatting Biologie Samenvatting hoofdstuk 1 bvj Samenvatting door Fabienne 1166 woorden 24 oktober 2017 5 2 keer beoordeeld Vak Methode Biologie Biologie voor jou Hoofdstuk 1: stofwisseling Paragraaf
VIII Samenvatting voor alle anderen
 VIII Samenvatting voor alle anderen Voor het bestuderen van biologische processen, zoals die plaatsvinden in alle levende cellen van zowel flora als fauna, wordt vaak gebruik gemaakt van bacteriën. Bacteriën
VIII Samenvatting voor alle anderen Voor het bestuderen van biologische processen, zoals die plaatsvinden in alle levende cellen van zowel flora als fauna, wordt vaak gebruik gemaakt van bacteriën. Bacteriën
Samenvatting. Samenvatting
 Samenvatting Samenvatting De gist Saccharomyces cerevisiae is bij de meeste mensen bekend onder de naam bakkersgist. De bekendste toepassing van deze gist is het gebruik voor het rijzen van brood, maar
Samenvatting Samenvatting De gist Saccharomyces cerevisiae is bij de meeste mensen bekend onder de naam bakkersgist. De bekendste toepassing van deze gist is het gebruik voor het rijzen van brood, maar
Scheikundige begrippen
 Scheikundige begrippen Door: Ruby Vreedenburgh, Jesse Bosman, Colana van Klink en Fleur Jansen Scheikunde begrippen 1 Chemische reactie Ruby Vreedenburgh Overal om ons heen vinden er chemische reacties
Scheikundige begrippen Door: Ruby Vreedenburgh, Jesse Bosman, Colana van Klink en Fleur Jansen Scheikunde begrippen 1 Chemische reactie Ruby Vreedenburgh Overal om ons heen vinden er chemische reacties
Organismen die organisch en anorganische moleculen kunnen maken of nodig hebben zijn heterotroof
 Boekverslag door A. 1802 woorden 20 juni 2007 5 71 keer beoordeeld Vak Methode Biologie Biologie voor jou Samenvatting stofwisseling Stofwisseling is het totaal van alle chemische processen in een organisme
Boekverslag door A. 1802 woorden 20 juni 2007 5 71 keer beoordeeld Vak Methode Biologie Biologie voor jou Samenvatting stofwisseling Stofwisseling is het totaal van alle chemische processen in een organisme
Nederlandse samenvatting
 Nederlandse samenvatting Archaea en hyperthermofielen De levende organismen op onze aarde kunnen verdeeld worden in twee groepen, de prokaryoten en de eukaryoten. Eukaryote cellen hebben een celkern, een
Nederlandse samenvatting Archaea en hyperthermofielen De levende organismen op onze aarde kunnen verdeeld worden in twee groepen, de prokaryoten en de eukaryoten. Eukaryote cellen hebben een celkern, een
Naar: D.O. Hall & K.K. Rao, Photosynthesis, Studies in Biology, Cambridge, 1994, blz. 106.
 Examentrainer Vragen Fotosynthese Vanuit tussenproducten van de fotosynthese worden niet alleen koolhydraten gevormd, maar ook vetten, vetzuren, aminozuren en andere organische zuren. Dag- en seizoensgebonden
Examentrainer Vragen Fotosynthese Vanuit tussenproducten van de fotosynthese worden niet alleen koolhydraten gevormd, maar ook vetten, vetzuren, aminozuren en andere organische zuren. Dag- en seizoensgebonden
Tentamen Biochemie, onderdeel Abrahams, 2e jaar MST,
 Tentamen Biochemie, onderdeel Abrahams, 2e jaar MST, 26-09-2014 1. Tijdens fotosynthese ontstaat O 2. Uit welke grondstof(fen) wordt dit O 2 gevormd? De reactie vereist energie. Hoeveel moleculen ATP worden
Tentamen Biochemie, onderdeel Abrahams, 2e jaar MST, 26-09-2014 1. Tijdens fotosynthese ontstaat O 2. Uit welke grondstof(fen) wordt dit O 2 gevormd? De reactie vereist energie. Hoeveel moleculen ATP worden
Celstofwisseling II (COO 5) Vragen bij deoefen- en zelftoets-module behorende bij hoofdstuk 9 en 10 van Biology, Campbell, 8 e druk Versie
 Celstofwisseling II (COO 5) Vragen bij deoefen- en zelftoets-module behorende bij hoofdstuk 9 en 10 van Biology, Campbell, 8 e druk Versie 2010-2011 Elektronen-transportketen 1. Van enkele processen in
Celstofwisseling II (COO 5) Vragen bij deoefen- en zelftoets-module behorende bij hoofdstuk 9 en 10 van Biology, Campbell, 8 e druk Versie 2010-2011 Elektronen-transportketen 1. Van enkele processen in
Basisscheikunde voor het hbo ISBN e druk Uitgeverij Syntax media
 Hoofdstuk 14 Chemische processen bladzijde 1 Opgave 1 Wat denk je, zijn de volgende processen continuprocessen of batch-processen? a productie van verschillende soorten medicijnen b productie van verschillende
Hoofdstuk 14 Chemische processen bladzijde 1 Opgave 1 Wat denk je, zijn de volgende processen continuprocessen of batch-processen? a productie van verschillende soorten medicijnen b productie van verschillende
Nederlandse samenvatting voor geïntereseerden buiten dit vakgebied
 Hoofdstuk 8 Nederlandse samenvatting voor geïntereseerden buiten dit vakgebied Alle levende wezens zijn opgebouwd uit cellen. Het menselijk lichaam heeft er 10 14 oftewel rond de 100 biljoen, terwijl bacteriën
Hoofdstuk 8 Nederlandse samenvatting voor geïntereseerden buiten dit vakgebied Alle levende wezens zijn opgebouwd uit cellen. Het menselijk lichaam heeft er 10 14 oftewel rond de 100 biljoen, terwijl bacteriën
DNA & eiwitsynthese Vragen bij COO-programma bij hoofdstuk 11 en 12 Life
 DNA & eiwitsynthese Vragen bij COO-programma bij hoofdstuk 11 en 12 Life De vragen die voorkomen in het COO-programma DNA & eiwitsynthese zijn op dit formulier weergegeven. Het is de bedoeling dat je,
DNA & eiwitsynthese Vragen bij COO-programma bij hoofdstuk 11 en 12 Life De vragen die voorkomen in het COO-programma DNA & eiwitsynthese zijn op dit formulier weergegeven. Het is de bedoeling dat je,
3 Factoren die het watergehalte van organismen 40 bepalen. 3.1 Bepalende factoren voor watergehalte 40 3.2 Belang van water voor levende wezens 41
 3 1 Functionele morfologie van de cel 1 De cel gezien door de lichtmicroscoop 06 2 De cel gezien door de elektronenmicroscoop 09 2.1 Bouw en functie van het eenheidsmembraan 10 2.2 Overzicht van de celorganellen
3 1 Functionele morfologie van de cel 1 De cel gezien door de lichtmicroscoop 06 2 De cel gezien door de elektronenmicroscoop 09 2.1 Bouw en functie van het eenheidsmembraan 10 2.2 Overzicht van de celorganellen
BIOLOGIE Thema: Stofwisseling Havo
 BIOLOGIE Thema: Stofwisseling Havo Henry N. Hassankhan Scholengemeenschap Lelydorp [HHS-SGL] Docent: A. Sewsahai De student moet de bouw en werking van enzymen kunnen beschrijven moet het proces van foto
BIOLOGIE Thema: Stofwisseling Havo Henry N. Hassankhan Scholengemeenschap Lelydorp [HHS-SGL] Docent: A. Sewsahai De student moet de bouw en werking van enzymen kunnen beschrijven moet het proces van foto
Cellulomonas knipt! Aantonen van cellulose afbraak door Cellulomonas sp.
 Aantonen van cellulose afbraak door Cellulomonas sp. Inleiding In de hout en papierindustrie ontstaat veel afval in de vorm van cellulose. Als men dit zou kunnen verwerken tot veevoer, wordt waardeloos
Aantonen van cellulose afbraak door Cellulomonas sp. Inleiding In de hout en papierindustrie ontstaat veel afval in de vorm van cellulose. Als men dit zou kunnen verwerken tot veevoer, wordt waardeloos
De cel, didactische schrijfopdracht 4 VMBO T Een reis door de subcellulaire structuur van de cel
 De cel, didactische schrijfopdracht 4 VMBO T Een reis door de subcellulaire structuur van de cel Auteurs: Sjoerd Schouten & Kelly Simons Studentnr: 0889861, 0879682 Datum: 8 Februari 2015 instituut: Hogeschool
De cel, didactische schrijfopdracht 4 VMBO T Een reis door de subcellulaire structuur van de cel Auteurs: Sjoerd Schouten & Kelly Simons Studentnr: 0889861, 0879682 Datum: 8 Februari 2015 instituut: Hogeschool
Moderne Biotechnologie van cel naar fabriek 6 vwo. Woudschoten chemie conferentie 4 november 2011
 Moderne Biotechnologie van cel naar fabriek 6 vwo Woudschoten chemie conferentie 4 november 2011 Ontwikkelteam 2008-2010 Coach Coach: Aonne Kerkstra Docenten Ingeborg de Kooter(Chr. Lyceum Delft) Dirk
Moderne Biotechnologie van cel naar fabriek 6 vwo Woudschoten chemie conferentie 4 november 2011 Ontwikkelteam 2008-2010 Coach Coach: Aonne Kerkstra Docenten Ingeborg de Kooter(Chr. Lyceum Delft) Dirk
Bacteriën maken zwavel Vragen en opdrachten bij de poster
 Vragen en opdrachten bij de poster Bacteriën maken zwavel Vragen en opdrachten bij de poster 3 vwo Probleem: Zuur gas T1 Waterstofsulfide ontstaat bij de afbraak van zwavelhoudende organische stoffen.
Vragen en opdrachten bij de poster Bacteriën maken zwavel Vragen en opdrachten bij de poster 3 vwo Probleem: Zuur gas T1 Waterstofsulfide ontstaat bij de afbraak van zwavelhoudende organische stoffen.
Samenvatting Biologie Hoofdstuk 1 Stofwisseling
 Samenvatting Biologie Hoofdstuk 1 Stofwisseling Samenvatting door M. 1566 woorden 14 januari 2017 4,2 5 keer beoordeeld Vak Methode Biologie Biologie voor jou Biologie Thema 1: stofwisseling Paragraaf
Samenvatting Biologie Hoofdstuk 1 Stofwisseling Samenvatting door M. 1566 woorden 14 januari 2017 4,2 5 keer beoordeeld Vak Methode Biologie Biologie voor jou Biologie Thema 1: stofwisseling Paragraaf
a. 38 b. 38 c. 0 d. 36/38
 Microbiologiedeel: Hieronder staan vier vragen die de stijl en diepgang hebben van de vragen van het microbiologiedeel zoals ze op het tentamen gevraagd kunnen worden. 1.a. Hoeveel ATP kan de gram negatieve
Microbiologiedeel: Hieronder staan vier vragen die de stijl en diepgang hebben van de vragen van het microbiologiedeel zoals ze op het tentamen gevraagd kunnen worden. 1.a. Hoeveel ATP kan de gram negatieve
1 Stoffen worden omgezet. Stofwisseling is het vormen van nieuwe stoffen en het vrijmaken van energie. Kortom alle processen in organismen.
 THEMA 1 1 Stoffen worden omgezet 2 Fotosynthese 3 Glucose als grondstof 4 Verbranding 5 Fotosynthese en verbranding 1 Stoffen worden omgezet. Stofwisseling is het vormen van nieuwe stoffen en het vrijmaken
THEMA 1 1 Stoffen worden omgezet 2 Fotosynthese 3 Glucose als grondstof 4 Verbranding 5 Fotosynthese en verbranding 1 Stoffen worden omgezet. Stofwisseling is het vormen van nieuwe stoffen en het vrijmaken
DNA & eiwitsynthese Oefen- en zelftoetsmodule behorende bij hoofdstuk 16 en 17 van Campbell, 7 e druk December 2008
 DNA & eiwitsynthese Oefen- en zelftoetsmodule behorende bij hoofdstuk 16 en 17 van Campbell, 7 e druk December 2008 DNA 1. Hieronder zie je de schematische weergave van een dubbelstrengs DNA-keten. Een
DNA & eiwitsynthese Oefen- en zelftoetsmodule behorende bij hoofdstuk 16 en 17 van Campbell, 7 e druk December 2008 DNA 1. Hieronder zie je de schematische weergave van een dubbelstrengs DNA-keten. Een
Leerlingenhandleiding
 Leerlingenhandleiding Afsluitende module Alternatieve Brandstoffen - Chemie verdieping - Ontwikkeld door dr. T. Klop en ir. J.F. Jacobs Op alle lesmaterialen is de Creative Commons Naamsvermelding-Niet-commercieel-Gelijk
Leerlingenhandleiding Afsluitende module Alternatieve Brandstoffen - Chemie verdieping - Ontwikkeld door dr. T. Klop en ir. J.F. Jacobs Op alle lesmaterialen is de Creative Commons Naamsvermelding-Niet-commercieel-Gelijk
Stoffen, structuur en bindingen
 Hoofdstuk 1: Stoffen, structuur en bindingen Scheikunde vwo 2011/2012 www.lyceo.nl Onderwerpen Scheikunde 2011 2012 Stoffen, structuur en binding Kenmerken van Reacties Zuren en base Redox Chemische technieken
Hoofdstuk 1: Stoffen, structuur en bindingen Scheikunde vwo 2011/2012 www.lyceo.nl Onderwerpen Scheikunde 2011 2012 Stoffen, structuur en binding Kenmerken van Reacties Zuren en base Redox Chemische technieken
BOUWSTENEN VAN HET LEVEN
 BOUWSTENEN VAN HET LEVEN Pearson Basisboek Biologie 10voorBiologie VWO Hoofdstuk 1 L. Grotenbreg (MSc.) Bouwstenen van het leven Organische moleculen, groot of klein, bevatten chemische energie en zijn
BOUWSTENEN VAN HET LEVEN Pearson Basisboek Biologie 10voorBiologie VWO Hoofdstuk 1 L. Grotenbreg (MSc.) Bouwstenen van het leven Organische moleculen, groot of klein, bevatten chemische energie en zijn
Oefenopgaven CHEMISCHE INDUSTRIE
 Oefenopgaven CEMISCE INDUSTRIE havo OPGAVE 1 Een bereidingswijze van fosfor, P 4, kan men als volgt weergeven: Ca 3 (PO 4 ) 2 + SiO 2 + C P 4 + CO + CaSiO 3 01 Neem bovenstaande reactievergelijking over
Oefenopgaven CEMISCE INDUSTRIE havo OPGAVE 1 Een bereidingswijze van fosfor, P 4, kan men als volgt weergeven: Ca 3 (PO 4 ) 2 + SiO 2 + C P 4 + CO + CaSiO 3 01 Neem bovenstaande reactievergelijking over
Paragraaf 1: Fossiele brandstoffen
 Scheikunde Hoofdstuk 2 Samenvatting Paragraaf 1: Fossiele brandstoffen Fossiele brandstof Koolwaterstof Onvolledige verbranding Broeikaseffect Brandstof ontstaan door het afsterven van levende organismen,
Scheikunde Hoofdstuk 2 Samenvatting Paragraaf 1: Fossiele brandstoffen Fossiele brandstof Koolwaterstof Onvolledige verbranding Broeikaseffect Brandstof ontstaan door het afsterven van levende organismen,
Samenvatting Scheikunde Hoofdstuk 1 + 2
 Samenvatting Scheikunde Hoofdstuk 1 + 2 Samenvatting door K. 1077 woorden 22 maart 2016 6,1 9 keer beoordeeld Vak Scheikunde Impact 3 vwo Scheikunde hoofdstuk 1 + 2 Paragraaf 1: Stoffen bijv. Glas en hout,
Samenvatting Scheikunde Hoofdstuk 1 + 2 Samenvatting door K. 1077 woorden 22 maart 2016 6,1 9 keer beoordeeld Vak Scheikunde Impact 3 vwo Scheikunde hoofdstuk 1 + 2 Paragraaf 1: Stoffen bijv. Glas en hout,
Eindexamen vwo scheikunde I
 Waterstof uit afvalwater 1 maximumscore 4 C 6 H 1 O 6 + 4 H O 4 H + CH COO + HCO + 4 H + molverhouding CH COO : HCO = 1 : 1 en C balans juist 1 coëfficiënt voor H + gelijk aan de som van de coëfficiënten
Waterstof uit afvalwater 1 maximumscore 4 C 6 H 1 O 6 + 4 H O 4 H + CH COO + HCO + 4 H + molverhouding CH COO : HCO = 1 : 1 en C balans juist 1 coëfficiënt voor H + gelijk aan de som van de coëfficiënten
4. deleted. 1. ATP kan een reactie aandrijven omdat
 1. ATP kan een reactie aandrijven omdat a. bij de hydrolyse van ATP warmte vrijkomt b. de hydrolyse van ATP de entropie doet toenemen c. ATP sterk bindt aan het substraat van enzymen d. ATP thermodynamisch
1. ATP kan een reactie aandrijven omdat a. bij de hydrolyse van ATP warmte vrijkomt b. de hydrolyse van ATP de entropie doet toenemen c. ATP sterk bindt aan het substraat van enzymen d. ATP thermodynamisch
Eindexamen scheikunde 1 vwo 2003-II
 4 Antwoordmodel Etheen 1 Het juiste antwoord kan als volgt zijn weergegeven: 2 H 2 H 2 H 2 H 2 H H H H H H H H + 2H 2 2 H + H H H H H H H 2 voor de pijl 1 formule van glucose en het overgebleven fragment
4 Antwoordmodel Etheen 1 Het juiste antwoord kan als volgt zijn weergegeven: 2 H 2 H 2 H 2 H 2 H H H H H H H H + 2H 2 2 H + H H H H H H H 2 voor de pijl 1 formule van glucose en het overgebleven fragment
Wereldoriëntatie - Natuur Wereldoriëntatie - Techniek Geschatte lesduur Hoofdstuk 1.2. Nuttige microben benadrukt dat niet alle
 Wereldoriëntatie - Natuur Algemene vaardigheden: 1.1 & 1.2 Levende en niet-levende natuur: 1.3 & 1.5 Wereldoriëntatie - Techniek 2.16* Geschatte lesduur 50 minuten Hoofdstuk 1.2. Nuttige microben benadrukt
Wereldoriëntatie - Natuur Algemene vaardigheden: 1.1 & 1.2 Levende en niet-levende natuur: 1.3 & 1.5 Wereldoriëntatie - Techniek 2.16* Geschatte lesduur 50 minuten Hoofdstuk 1.2. Nuttige microben benadrukt
Micro-organismen. organismen
 Micro-organismen organismen Agenda Wat zijn micro-organismen? Verschil tussen bacteriën en virussen Wat zijn micro-organismen? Een micro-organisme is niet zichtbaar met het blote oog: Bacteriën (gram positief/negatief)
Micro-organismen organismen Agenda Wat zijn micro-organismen? Verschil tussen bacteriën en virussen Wat zijn micro-organismen? Een micro-organisme is niet zichtbaar met het blote oog: Bacteriën (gram positief/negatief)
Intermezzo, De expressie van een eiwit.
 Samenvatting Bacteriën leven in een omgeving die voortdurend en snel verandert. Om adequaat te kunnen reageren op deze veranderingen beschikken bacteriën over tal van sensor systemen die de omgeving in
Samenvatting Bacteriën leven in een omgeving die voortdurend en snel verandert. Om adequaat te kunnen reageren op deze veranderingen beschikken bacteriën over tal van sensor systemen die de omgeving in
Mitochondriële ziekten
 Mitochondriële ziekten Stofwisseling NCMD Het Nijmeegs Centrum voor Mitochondriële Ziekten is een internationaal centrum voor patiëntenzorg, diagnostiek en onderzoek bij mensen met een stoornis in de mitochondriële
Mitochondriële ziekten Stofwisseling NCMD Het Nijmeegs Centrum voor Mitochondriële Ziekten is een internationaal centrum voor patiëntenzorg, diagnostiek en onderzoek bij mensen met een stoornis in de mitochondriële
NATIONALE SCHEIKUNDEOLYMPIADE
 NATIONALE SCHEIKUNDEOLYMPIADE CORRECTIEMODEL VOORRONDE 1 af te nemen in de periode van woensdag 5 januari 01 tot en met woensdag 1 februari 01 Deze voorronde bestaat uit 4 meerkeuzevragen verdeeld over
NATIONALE SCHEIKUNDEOLYMPIADE CORRECTIEMODEL VOORRONDE 1 af te nemen in de periode van woensdag 5 januari 01 tot en met woensdag 1 februari 01 Deze voorronde bestaat uit 4 meerkeuzevragen verdeeld over
Antwoorden Biologie Hoofdstuk 1: Stofwisseling
 Antwoorden Biologie Hoofdstuk 1: Stofwisseling Antwoorden door een scholier 1478 woorden 16 februari 2009 5,6 56 keer beoordeeld Vak Methode Biologie Biologie voor jou Biologie voor jouw Havo 5 Hoofdstuk
Antwoorden Biologie Hoofdstuk 1: Stofwisseling Antwoorden door een scholier 1478 woorden 16 februari 2009 5,6 56 keer beoordeeld Vak Methode Biologie Biologie voor jou Biologie voor jouw Havo 5 Hoofdstuk
Meerkeuzevragen. Fotosynthese, celademhaling en gisting. V. Rasquin
 Meerkeuzevragen Fotosynthese, celademhaling en gisting V. Rasquin MEERKEUZEVRAGEN FOTOSYNTHESE 1. Een brandende kaars dooft vlug onder een glazen stolp. Plaatst men naast de kaars ook een plant onder de
Meerkeuzevragen Fotosynthese, celademhaling en gisting V. Rasquin MEERKEUZEVRAGEN FOTOSYNTHESE 1. Een brandende kaars dooft vlug onder een glazen stolp. Plaatst men naast de kaars ook een plant onder de
Cellen aan de basis.
 Cellen aan de basis. Cellen aan de basis In het thema cellen aan de basis vinden we twee belangrijke thema s uit biologie voor jou terug. 1. Organen en cellen (thema 1 leerjaar 3) 2. Stofwisseling (thema
Cellen aan de basis. Cellen aan de basis In het thema cellen aan de basis vinden we twee belangrijke thema s uit biologie voor jou terug. 1. Organen en cellen (thema 1 leerjaar 3) 2. Stofwisseling (thema
Structuur, vorm en dynamica van biologische membranen
 SAMENVATTING Structuur, vorm en dynamica van biologische membranen Biofysica is de studie van de natuurkunde achter biologische processen. Haar werkterrein is voornamelijk de individuele cel. Cellen zijn
SAMENVATTING Structuur, vorm en dynamica van biologische membranen Biofysica is de studie van de natuurkunde achter biologische processen. Haar werkterrein is voornamelijk de individuele cel. Cellen zijn
Samenvatting. Samenvatting
 Samenvatting Samenvatting Gisten zijn ééncellige organismen. Er zijn veel verschillende soorten gisten, waarvan Saccharomyces cerevisiae, oftewel bakkersgist, de bekendste is. Gisten worden al sinds de
Samenvatting Samenvatting Gisten zijn ééncellige organismen. Er zijn veel verschillende soorten gisten, waarvan Saccharomyces cerevisiae, oftewel bakkersgist, de bekendste is. Gisten worden al sinds de
Verterende bodembacteriën? Aanwezigheid van amylase producerende bacteriën in de bodem
 Inleiding In de bodem leven bacteriën die het enzym amylase produceren. Amylase breekt zetmeelmoleculen (lange ketens van aan elkaar gekoppelde glucosemoleculen) af tot losse glucosemoleculen. In dit experiment
Inleiding In de bodem leven bacteriën die het enzym amylase produceren. Amylase breekt zetmeelmoleculen (lange ketens van aan elkaar gekoppelde glucosemoleculen) af tot losse glucosemoleculen. In dit experiment
Afsluitende les. Leerlingenhandleiding. Alternatieve brandstoffen
 Afsluitende les Leerlingenhandleiding Alternatieve brandstoffen Inleiding Deze chemie-verdiepingsmodule over alternatieve brandstoffen sluit aan op het Reizende DNA-lab Racen met wc-papier. Doel Het Reizende
Afsluitende les Leerlingenhandleiding Alternatieve brandstoffen Inleiding Deze chemie-verdiepingsmodule over alternatieve brandstoffen sluit aan op het Reizende DNA-lab Racen met wc-papier. Doel Het Reizende
CENTRALE COMMISSIE VOORTENTAMEN SCHEIKUNDE TENTAMEN SCHEIKUNDE. datum : donderdag 29 juli 2010
 CENTRALE COMMISSIE VOORTENTAMEN SCHEIKUNDE TENTAMEN SCHEIKUNDE datum : donderdag 29 juli 2010 tijd : 14.00 tot 17.00 uur aantal opgaven : 6 Iedere opgave dient op een afzonderlijk vel te worden gemaakt
CENTRALE COMMISSIE VOORTENTAMEN SCHEIKUNDE TENTAMEN SCHEIKUNDE datum : donderdag 29 juli 2010 tijd : 14.00 tot 17.00 uur aantal opgaven : 6 Iedere opgave dient op een afzonderlijk vel te worden gemaakt
1. Stofwisseling, assimilatie en dissimilatie
 Samenvatting door A. 1427 woorden 12 april 2013 6,5 5 keer beoordeeld Vak Methode Biologie Biologie voor jou Biologie H3 - Energie 1. Stofwisseling, assimilatie en dissimilatie Stofwisseling (metabolisme):
Samenvatting door A. 1427 woorden 12 april 2013 6,5 5 keer beoordeeld Vak Methode Biologie Biologie voor jou Biologie H3 - Energie 1. Stofwisseling, assimilatie en dissimilatie Stofwisseling (metabolisme):
Hoofdstuk 4. Chemische reacties. J.A.W. Faes (2019)
 Hoofdstuk 4 Chemische reacties J.A.W. Faes (2019) Hoofdstuk 4 Chemische reacties Paragrafen 4.1 Kenmerken van een reactie 4.2 Reactievergelijkingen 4.3 Rekenen aan reacties Practica Exp. 1 Waarnemen Exp.
Hoofdstuk 4 Chemische reacties J.A.W. Faes (2019) Hoofdstuk 4 Chemische reacties Paragrafen 4.1 Kenmerken van een reactie 4.2 Reactievergelijkingen 4.3 Rekenen aan reacties Practica Exp. 1 Waarnemen Exp.
Cellen in het lichaam.
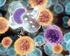 Hfdst. 1 Hfdst. 2 Hfdst. 3 Hfdst. 4 Hfdst. 5 Hfdst. 6 Hfdst. 7 Cellen in het lichaam. Besturing Energievoorziening Beweging en vorm Celbehoud Transport Celdeling Stevigheid van de cel Bron: bewerkt naar
Hfdst. 1 Hfdst. 2 Hfdst. 3 Hfdst. 4 Hfdst. 5 Hfdst. 6 Hfdst. 7 Cellen in het lichaam. Besturing Energievoorziening Beweging en vorm Celbehoud Transport Celdeling Stevigheid van de cel Bron: bewerkt naar
Onderdelen van de cel
 Auteur Laatst gewijzigd Licentie Webadres Kevin Koorda 31 january 2016 CC Naamsvermelding 3.0 Nederland licentie https://maken.wikiwijs.nl/71664 Dit lesmateriaal is gemaakt met Wikiwijs van Kennisnet.
Auteur Laatst gewijzigd Licentie Webadres Kevin Koorda 31 january 2016 CC Naamsvermelding 3.0 Nederland licentie https://maken.wikiwijs.nl/71664 Dit lesmateriaal is gemaakt met Wikiwijs van Kennisnet.
Oefenvragen Hoofdstuk 3 Bouwstenen van stoffen antwoorden
 Vraag 1 Geef het symbool van: Oefenvragen Hoofdstuk 3 Bouwstenen van stoffen antwoorden I. IJzer Fe Aluminium Al Koolstof C IV. Lood Pb V. Chloor Cl VI. Silicium Si Vraag 2 Geef de naam van de atoomsoort.
Vraag 1 Geef het symbool van: Oefenvragen Hoofdstuk 3 Bouwstenen van stoffen antwoorden I. IJzer Fe Aluminium Al Koolstof C IV. Lood Pb V. Chloor Cl VI. Silicium Si Vraag 2 Geef de naam van de atoomsoort.
Eindexamen scheikunde havo 2001-II
 Eindexamen scheikunde havo 00-II 4 Antwoordmodel Energievoorziening in de ruimte et (uiteenvallen van de Pu-38 atomen) levert energie dus het is een exotherm proces. er komt energie vrij aantal protonen:
Eindexamen scheikunde havo 00-II 4 Antwoordmodel Energievoorziening in de ruimte et (uiteenvallen van de Pu-38 atomen) levert energie dus het is een exotherm proces. er komt energie vrij aantal protonen:
Examen scheikunde HAVO tijdvak uitwerkingen
 Examen scheikunde HAV tijdvak 2 2018 uitwerkingen Bodem bedekken 1p 1 fotosynthese/koolzuurassimilatie 2 25,0 kg 3 Aantal m 3 polymelkzuur in 1,00 m 3 bolletjes = 3 3 1,24 10 kg/m 2,016 10 2 m 3 4 Volume
Examen scheikunde HAV tijdvak 2 2018 uitwerkingen Bodem bedekken 1p 1 fotosynthese/koolzuurassimilatie 2 25,0 kg 3 Aantal m 3 polymelkzuur in 1,00 m 3 bolletjes = 3 3 1,24 10 kg/m 2,016 10 2 m 3 4 Volume
Microbiology & Biochemistry (MIB-10306, microbiologie deel)
 Microbiology & Biochemistry (MIB-10306, microbiologie deel) 1. Morfologie (vorm, grootte, onderdelen) a. Teken schematisch de doorsnede van een bacterie en benoem 10 structuren. vacuole met reservestoffen,
Microbiology & Biochemistry (MIB-10306, microbiologie deel) 1. Morfologie (vorm, grootte, onderdelen) a. Teken schematisch de doorsnede van een bacterie en benoem 10 structuren. vacuole met reservestoffen,
 SAMENVATTING 141 Aminozuren zijn bouwstenen voor de synthese van eiwitten die nodig zijn voor de groei van een organisme. De synthese van aminozuren kost energie dat wordt gewonnen uit de voedingstoffen
SAMENVATTING 141 Aminozuren zijn bouwstenen voor de synthese van eiwitten die nodig zijn voor de groei van een organisme. De synthese van aminozuren kost energie dat wordt gewonnen uit de voedingstoffen
Anabolisme: anabole processen: opbouwstofwisseling Energie wordt toegevoegd: assimilatie
 Fysiologie les 2 BIO-ENERGETICA Celstofwisseling = cel metabolisme Basis metabolisme: stofwisseling in rust Anabolisme: anabole processen: opbouwstofwisseling Energie wordt toegevoegd: assimilatie Katabolisme:
Fysiologie les 2 BIO-ENERGETICA Celstofwisseling = cel metabolisme Basis metabolisme: stofwisseling in rust Anabolisme: anabole processen: opbouwstofwisseling Energie wordt toegevoegd: assimilatie Katabolisme:
Chemie (ph) bij het inkuilen Scheikunde klas V41a en V41b door Erik Held
 Chemie (ph) bij het inkuilen Scheikunde klas V41a en V41b door Erik Held Inkuilproces Proces bij het inkuilen: In de kuil ondergaat het gewas een biochemisch proces onder invloed van micro-organismen Een
Chemie (ph) bij het inkuilen Scheikunde klas V41a en V41b door Erik Held Inkuilproces Proces bij het inkuilen: In de kuil ondergaat het gewas een biochemisch proces onder invloed van micro-organismen Een
Samenvatting Biologie Stofwisseling
 Samenvatting Biologie Stofwisseling Samenvatting door een scholier 1466 woorden 13 juni 2006 5,6 46 keer beoordeeld Vak Methode Biologie Biologie voor jou Samenvatting Thema 1 Stofwisseling Doelstelling
Samenvatting Biologie Stofwisseling Samenvatting door een scholier 1466 woorden 13 juni 2006 5,6 46 keer beoordeeld Vak Methode Biologie Biologie voor jou Samenvatting Thema 1 Stofwisseling Doelstelling
4,5. Samenvatting door L woorden 17 december keer beoordeeld. Biologie voor jou. 1. Vrije en gebonden energie.
 Samenvatting door L. 1850 woorden 17 december 2012 4,5 7 keer beoordeeld Vak Methode Biologie Biologie voor jou 1. Vrije en gebonden energie. Vrije energie (kinetische energie) komt voor als warmte en
Samenvatting door L. 1850 woorden 17 december 2012 4,5 7 keer beoordeeld Vak Methode Biologie Biologie voor jou 1. Vrije en gebonden energie. Vrije energie (kinetische energie) komt voor als warmte en
Overzicht van reactievergelijkingen Scheikunde
 verzicht van reactievergelijkingen Scheikunde Algemeen Verbranding Een verbranding is een reactie met zuurstof. ierbij ontstaan de oxiden van de elementen. Volledige verbranding Bij volledige verbranding
verzicht van reactievergelijkingen Scheikunde Algemeen Verbranding Een verbranding is een reactie met zuurstof. ierbij ontstaan de oxiden van de elementen. Volledige verbranding Bij volledige verbranding
Nederlandse samenvatting
 Nederlandse samenvatting Nederlandse samenvatting Om te kunnen overleven moeten micro-organismen voedingsstoffen opnemen uit hun omgeving en afvalstoffen uitscheiden. Het inwendige van een cel is gescheiden
Nederlandse samenvatting Nederlandse samenvatting Om te kunnen overleven moeten micro-organismen voedingsstoffen opnemen uit hun omgeving en afvalstoffen uitscheiden. Het inwendige van een cel is gescheiden
7.1 Het deeltjesmodel
 Samenvatting door Mira 1711 woorden 24 juni 2017 10 3 keer beoordeeld Vak NaSk 7.1 Het deeltjesmodel Een model van een stof Elke stof heeft zijn eigen soort moleculen. Aangezien je niet kunt zien hoe een
Samenvatting door Mira 1711 woorden 24 juni 2017 10 3 keer beoordeeld Vak NaSk 7.1 Het deeltjesmodel Een model van een stof Elke stof heeft zijn eigen soort moleculen. Aangezien je niet kunt zien hoe een
5-1 Moleculen en atomen
 5-1 Moleculen en atomen Vraag 1. Uit hoeveel soorten moleculen bestaat een zuivere stof? Vraag 2. Wat is een molecuul? Vraag 3. Wat is een atoom? Vraag 4. Van welke heb je er het meeste: moleculen of atomen?
5-1 Moleculen en atomen Vraag 1. Uit hoeveel soorten moleculen bestaat een zuivere stof? Vraag 2. Wat is een molecuul? Vraag 3. Wat is een atoom? Vraag 4. Van welke heb je er het meeste: moleculen of atomen?
scheikunde vwo 2017-II
 Kerosine uit zonlicht maximumscore 3 Een voorbeeld van een juiste berekening is: E = ( 2,42 0 5 ) + 0,5 ( 3,935 0 5 ) + 0,5 (,05 0 5 ) = +3,84 0 5 (J mol ). juiste verwerking van de vormingswarmten van
Kerosine uit zonlicht maximumscore 3 Een voorbeeld van een juiste berekening is: E = ( 2,42 0 5 ) + 0,5 ( 3,935 0 5 ) + 0,5 (,05 0 5 ) = +3,84 0 5 (J mol ). juiste verwerking van de vormingswarmten van
Eindexamen vwo scheikunde pilot II
 Selectieve opname koolstofdioxide 1 maximumscore 2 Een juist antwoord kan als volgt zijn weergegeven: rechts van de pijl H + 1 juiste coëfficiënten 1 Indien in een overigens juiste vergelijking H 2 is
Selectieve opname koolstofdioxide 1 maximumscore 2 Een juist antwoord kan als volgt zijn weergegeven: rechts van de pijl H + 1 juiste coëfficiënten 1 Indien in een overigens juiste vergelijking H 2 is
Moleculaire Gastronomie: Gluten
 Moleculaire Gastronomie: Gluten Het maken en analyseren van deeg met gluten Inleiding Moleculaire gastronomie heeft alles te maken met het ontdekken van nieuwe smaakcombinaties, experimenteren met structuren
Moleculaire Gastronomie: Gluten Het maken en analyseren van deeg met gluten Inleiding Moleculaire gastronomie heeft alles te maken met het ontdekken van nieuwe smaakcombinaties, experimenteren met structuren
Archaebacteriën. Eubacteriën. Eukaryoot
 H5n 10-09-2001 16:41 Pagina 100 Samenvatting De gist Saccharomyces cerevisiae is bij de meeste mensen bekend als bakkersgist en wordt behalve voor het bereiden van brood onder andere ook gebruikt voor
H5n 10-09-2001 16:41 Pagina 100 Samenvatting De gist Saccharomyces cerevisiae is bij de meeste mensen bekend als bakkersgist en wordt behalve voor het bereiden van brood onder andere ook gebruikt voor
Samenvatting Scheikunde Hoofdstuk 4: voeding
 Samenvatting Scheikunde Hoofdstuk 4: voeding Samenvatting door Remco 1344 woorden 31 maart 2015 6,3 24 keer beoordeeld Vak Methode Scheikunde Chemie overal 4.1 Voedsel Voedsel is leven Voeding is noodzakelijk
Samenvatting Scheikunde Hoofdstuk 4: voeding Samenvatting door Remco 1344 woorden 31 maart 2015 6,3 24 keer beoordeeld Vak Methode Scheikunde Chemie overal 4.1 Voedsel Voedsel is leven Voeding is noodzakelijk
BIOLOGIE Energie & Stofwisseling VWO
 BIOLOGIE Energie & Stofwisseling VWO Henry N. Hassankhan Scholengemeenschap Lelydorp [HHS-SGL] ARTHUR A. HOOGENDOORN ATHENEUM - VRIJE ATHENEUM - AAHA Docent: A. Sewsahai De student moet de bouw en werking
BIOLOGIE Energie & Stofwisseling VWO Henry N. Hassankhan Scholengemeenschap Lelydorp [HHS-SGL] ARTHUR A. HOOGENDOORN ATHENEUM - VRIJE ATHENEUM - AAHA Docent: A. Sewsahai De student moet de bouw en werking
Biosynthese. Biosynthese. Metabolic engineering. 8 Oktober 2014
 Biosynthese Metabolic engineering 8 Oktober 2014 CV 1982 Studie Moleculaire Wetenschappen, WU 1989 Promotie productie monoklonale antilichamen Bioprocestechnologie&RIVM 1994-2001 Post-docs 2001 Universitair
Biosynthese Metabolic engineering 8 Oktober 2014 CV 1982 Studie Moleculaire Wetenschappen, WU 1989 Promotie productie monoklonale antilichamen Bioprocestechnologie&RIVM 1994-2001 Post-docs 2001 Universitair
Waar leven is, zijn ook Enzymen
 Waar leven is, zijn ook Enzymen De verschillende functies van de Enzymen zijn ontelbaar veelzijdig, net zo als bij Microorganismen, maar Enzymen zijn geen Micro organismen. Het betreft hier dus geen levende
Waar leven is, zijn ook Enzymen De verschillende functies van de Enzymen zijn ontelbaar veelzijdig, net zo als bij Microorganismen, maar Enzymen zijn geen Micro organismen. Het betreft hier dus geen levende
Studentnummer: Schrijf je naam en studentnummer op elk vel. Omcirkel het juiste antwoord.
 Naam: Studentnummer: FLP1 Tentamen 31 05 2013, 14:00 17:00h Dit tentamen bestaat uit 25 opgaven op 6 bladzijden. Schrijf je naam en studentnummer op elk vel. Omcirkel het juiste antwoord. Je mag boek,
Naam: Studentnummer: FLP1 Tentamen 31 05 2013, 14:00 17:00h Dit tentamen bestaat uit 25 opgaven op 6 bladzijden. Schrijf je naam en studentnummer op elk vel. Omcirkel het juiste antwoord. Je mag boek,
EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN Dit examen bestaat voor iedere kandidaat uit 5 OPGAVEN
 MAVO-4 II EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN 1974 MAVO-4 Dinsdag 11 juni, 9.00 11.00 NATUUR-EN SCHEIKUNDE II (Scheikunde) OPEN VRAGEN Dit examen bestaat voor iedere kandidaat uit 5 OPGAVEN
MAVO-4 II EXAMEN MIDDELBAAR ALGEMEEN VOORTGEZET ONDERWIJS IN 1974 MAVO-4 Dinsdag 11 juni, 9.00 11.00 NATUUR-EN SCHEIKUNDE II (Scheikunde) OPEN VRAGEN Dit examen bestaat voor iedere kandidaat uit 5 OPGAVEN
Voorbereiding toelatingsexamen arts/tandarts Biologie: Eukaryote cel 7/2/2015. dr. Brenda Casteleyn
 Voorbereiding toelatingsexamen arts/tandarts Biologie: Eukaryote cel 7/2/2015 dr. Brenda Casteleyn Met dank aan: Leen Goyens (http://users.telenet.be/toelating) en studenten van forum http://www.toelatingsexamen-geneeskunde.be
Voorbereiding toelatingsexamen arts/tandarts Biologie: Eukaryote cel 7/2/2015 dr. Brenda Casteleyn Met dank aan: Leen Goyens (http://users.telenet.be/toelating) en studenten van forum http://www.toelatingsexamen-geneeskunde.be
PHA productie uit Organische reststromen. BIONND THE FUTURE. 8 mei 2014 Henk Doddema
 PHA productie uit Organische reststromen. BIONND THE FUTURE 8 mei 2014 Henk Doddema Meer dan 300 soorten bacteriën kunnen PHA s maken en opslaan in hun cellen Rhodomonas sp. Halomonas sp. Alcaligenes (nu
PHA productie uit Organische reststromen. BIONND THE FUTURE 8 mei 2014 Henk Doddema Meer dan 300 soorten bacteriën kunnen PHA s maken en opslaan in hun cellen Rhodomonas sp. Halomonas sp. Alcaligenes (nu
Bio- organische chemie, Biochemie & Celbiologie Deeltentamen 2 26 oktober 2009
 Vraag 1. Fototrofen en chemotrofen zijn sterk van elkaar afhankelijk omdat: 1. Fototrofen energie leveren aan de chemotrofen en de chemotrofen leveren suikers aan de fototrofen. 2. Fototrofen de chemotrofen
Vraag 1. Fototrofen en chemotrofen zijn sterk van elkaar afhankelijk omdat: 1. Fototrofen energie leveren aan de chemotrofen en de chemotrofen leveren suikers aan de fototrofen. 2. Fototrofen de chemotrofen
Eindexamen scheikunde havo 2006-I
 4 Beoordelingsmodel Rood licht Maximumscore 1 1 edelgassen 2 Voorbeelden van een juist antwoord zijn: De (negatieve) elektronen bewegen zich richting elektrode A dus is elektrode A de positieve elektrode.
4 Beoordelingsmodel Rood licht Maximumscore 1 1 edelgassen 2 Voorbeelden van een juist antwoord zijn: De (negatieve) elektronen bewegen zich richting elektrode A dus is elektrode A de positieve elektrode.
- 1 - Microbiologie en Biochemie (MIB-10306) Biochemie deel Vrijdag 29 februari 2008, uur
 Microbiologie en Biochemie (MIB-10306) Biochemie deel Vrijdag 29 februari 2008, 9.00-12.00 uur - Begin met het invullen van je naam en registratienummer. - Alle antwoorden moeten op het vragenformulier
Microbiologie en Biochemie (MIB-10306) Biochemie deel Vrijdag 29 februari 2008, 9.00-12.00 uur - Begin met het invullen van je naam en registratienummer. - Alle antwoorden moeten op het vragenformulier
Antwoorden. 3 Leg uit dat er in het zout twee soorten ijzerionen aanwezig moeten zijn.
 Antwoorden 1 Hoeveel protonen, elektronen en neutronen heeft een ion Fe 3+? 26 protonen, 23 elektronen, 30 neutronen 2 Geef de scheikundige namen van Fe 2 S 3 en FeCO 3. ijzer(iii)sulfide en ijzer(ii)carbonaat
Antwoorden 1 Hoeveel protonen, elektronen en neutronen heeft een ion Fe 3+? 26 protonen, 23 elektronen, 30 neutronen 2 Geef de scheikundige namen van Fe 2 S 3 en FeCO 3. ijzer(iii)sulfide en ijzer(ii)carbonaat
Opstel door B woorden 6 maart keer beoordeeld. Inleiding. Wat is biotechnologie?
 Opstel door B. 1149 woorden 6 maart 2013 8 2 keer beoordeeld Vak Methode ANW ANW Actief Inleiding Wat is biotechnologie? Het begrip biotechnologie omvat alle methodes waarbij organismen gebruikt worden
Opstel door B. 1149 woorden 6 maart 2013 8 2 keer beoordeeld Vak Methode ANW ANW Actief Inleiding Wat is biotechnologie? Het begrip biotechnologie omvat alle methodes waarbij organismen gebruikt worden
Bouw van een cel vmbo-b34. CC Naamsvermelding 3.0 Nederland licentie. https://maken.wikiwijs.nl/73566
 Auteur VO-content Laatst gewijzigd Licentie Webadres 19 december 2016 CC Naamsvermelding 3.0 Nederland licentie https://maken.wikiwijs.nl/73566 Dit lesmateriaal is gemaakt met Wikiwijs Maken van Kennisnet.
Auteur VO-content Laatst gewijzigd Licentie Webadres 19 december 2016 CC Naamsvermelding 3.0 Nederland licentie https://maken.wikiwijs.nl/73566 Dit lesmateriaal is gemaakt met Wikiwijs Maken van Kennisnet.
Eindexamen scheikunde havo 2001-I
 Eindexamen scheikunde havo -I 4 Antwoordmodel Nieuw element (in de tekst staat:) deze atomen zijn eerst ontdaan van een aantal elektronen dus de nikkeldeeltjes zijn positief geladen Indien in een overigens
Eindexamen scheikunde havo -I 4 Antwoordmodel Nieuw element (in de tekst staat:) deze atomen zijn eerst ontdaan van een aantal elektronen dus de nikkeldeeltjes zijn positief geladen Indien in een overigens
Tentamen Biochemie,, onderdeel Abrahams, 2e jaar MST, Antwoorden
 Tentamen Biochemie,, onderdeel Abrahams, 2e jaar MST, 26-09-2014 Antwoorden 1. Hieronder is de structuur weergegeven van octadecyl rhodamine B chloride. Let op de alifatische (CH 2 ) 17 keten die is veresterd
Tentamen Biochemie,, onderdeel Abrahams, 2e jaar MST, 26-09-2014 Antwoorden 1. Hieronder is de structuur weergegeven van octadecyl rhodamine B chloride. Let op de alifatische (CH 2 ) 17 keten die is veresterd
het machtigste leven op aarde erfelijkheid & ordening
 antwoorden en uitleg bij Micropia-onderwijsmateriaal Havo/VWO 3-4 het machtigste leven op aarde erfelijkheid & ordening In dit document vindt u de vragen uit het Micropia-onderwijsmateriaal voor Havo/VWO
antwoorden en uitleg bij Micropia-onderwijsmateriaal Havo/VWO 3-4 het machtigste leven op aarde erfelijkheid & ordening In dit document vindt u de vragen uit het Micropia-onderwijsmateriaal voor Havo/VWO
Aan de slag met Fotosynthese
 Auteur Laatst gewijzigd Licentie Webadres E i Kiwijs 27 september 2011 CC Naamsvermelding 3.0 Nederland licentie https://maken.wikiwijs.nl/32977 Dit lesmateriaal is gemaakt met Wikiwijs van Kennisnet.
Auteur Laatst gewijzigd Licentie Webadres E i Kiwijs 27 september 2011 CC Naamsvermelding 3.0 Nederland licentie https://maken.wikiwijs.nl/32977 Dit lesmateriaal is gemaakt met Wikiwijs van Kennisnet.
Eindexamen scheikunde 1 vwo 2007-II
 Beoordelingsmodel EcoEthanol TM 1 maximumscore 2 Voorbeelden van juiste argumenten zijn: Er komt minder broeikasgas / de toename van het 2 gehalte in de atmosfeer wordt minder / het gaat de opwarming van
Beoordelingsmodel EcoEthanol TM 1 maximumscore 2 Voorbeelden van juiste argumenten zijn: Er komt minder broeikasgas / de toename van het 2 gehalte in de atmosfeer wordt minder / het gaat de opwarming van
Examentrainer. Vragen. Broeikasgassen meten in wijn. 1 Uitgeverij Malmberg. Lees de volgende tekst.
 Examentrainer Vragen Broeikasgassen meten in wijn Lees de volgende tekst. Sterk toegenomen verbranding van organische stoffen leidt tot een verhoging van de concentratie CO 2 in de atmosfeer. Er is op
Examentrainer Vragen Broeikasgassen meten in wijn Lees de volgende tekst. Sterk toegenomen verbranding van organische stoffen leidt tot een verhoging van de concentratie CO 2 in de atmosfeer. Er is op
Biochemische principes Hans V. Westerhoff
 Hans V. Westerhoff Leerstof: Voet, Voet & Pratt: Fundamentals of Biochemistry (1999 editie) Hoofdstukken 13-17, 21 (zie syllabus voor details) Syllabus: de principes van het metabolisme (III.A-E) Syllabus:
Hans V. Westerhoff Leerstof: Voet, Voet & Pratt: Fundamentals of Biochemistry (1999 editie) Hoofdstukken 13-17, 21 (zie syllabus voor details) Syllabus: de principes van het metabolisme (III.A-E) Syllabus:
Bijlage VMBO-GL en TL 2004
 Bijlage VMBO-GL en TL 2004 tijdvak 1 BIOLOGIE CSE GL EN TL BIOLOGIE VBO-MAVO-D Deze bijlage bevat informatie. 400009-1-586-543b BIOTECHNOLOGIE INFORMATIE 1 OUDE TECHNIEKEN Al eeuwen gebruiken mensen organismen
Bijlage VMBO-GL en TL 2004 tijdvak 1 BIOLOGIE CSE GL EN TL BIOLOGIE VBO-MAVO-D Deze bijlage bevat informatie. 400009-1-586-543b BIOTECHNOLOGIE INFORMATIE 1 OUDE TECHNIEKEN Al eeuwen gebruiken mensen organismen
Eindexamen scheikunde havo 2008-II
 Beoordelingsmodel Forams 1 maximumscore 2 aantal protonen: 14 aantal neutronen: 16 aantal protonen: 14 1 aantal neutronen: 30 verminderd met het aantal protonen 1 Indien het juiste aantal protonen (7)
Beoordelingsmodel Forams 1 maximumscore 2 aantal protonen: 14 aantal neutronen: 16 aantal protonen: 14 1 aantal neutronen: 30 verminderd met het aantal protonen 1 Indien het juiste aantal protonen (7)
4. In een bakje met natriumjodide-oplossing worden 2 loden elektroden gehangen. Deze twee elektroden worden aangesloten op een batterij.
 Test Scheikunde Havo 5 Periode 1 Geef voor de volgende redoxreacties de halfreacties: a Mg + S MgS b Na + Cl NaCl c Zn + O ZnO Geef de halfreacties en de reactievergelijking voor de volgende redoxreacties:
Test Scheikunde Havo 5 Periode 1 Geef voor de volgende redoxreacties de halfreacties: a Mg + S MgS b Na + Cl NaCl c Zn + O ZnO Geef de halfreacties en de reactievergelijking voor de volgende redoxreacties:
Onderdelen van de cel
 Auteur Laatst gewijzigd Licentie Webadres Kevin Koorda 31 January 2016 CC Naamsvermelding 3.0 Nederland licentie http://maken.wikiwijs.nl/71664 Dit lesmateriaal is gemaakt met Wikiwijs Maken van Kennisnet.
Auteur Laatst gewijzigd Licentie Webadres Kevin Koorda 31 January 2016 CC Naamsvermelding 3.0 Nederland licentie http://maken.wikiwijs.nl/71664 Dit lesmateriaal is gemaakt met Wikiwijs Maken van Kennisnet.
